תוכן העניינים:
- חזרה על השיעור הקודם - בעיית הקצוות
- טלומרים - מבנה ותפקיד
- טלומראז (Telomerase)
- טופואיזומראז (Topoisomerase)
- קשר לסרטן ולרפואה
- PCR ויישומים מעבדתיים-קליניים
חזרה על השיעור הקודם - בעיית הקצוות
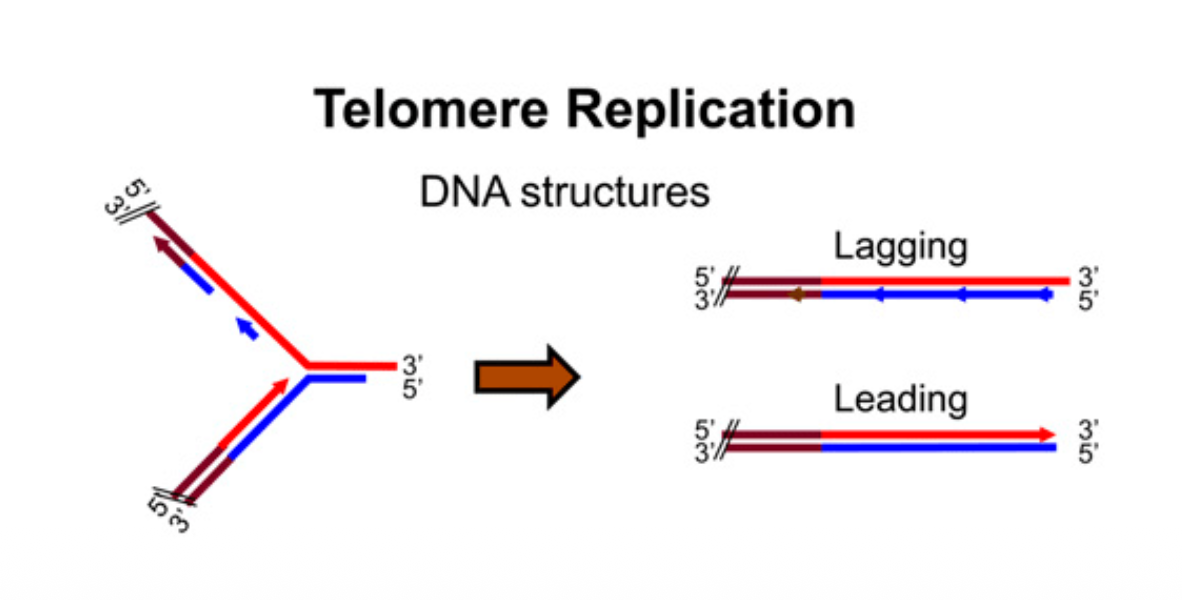
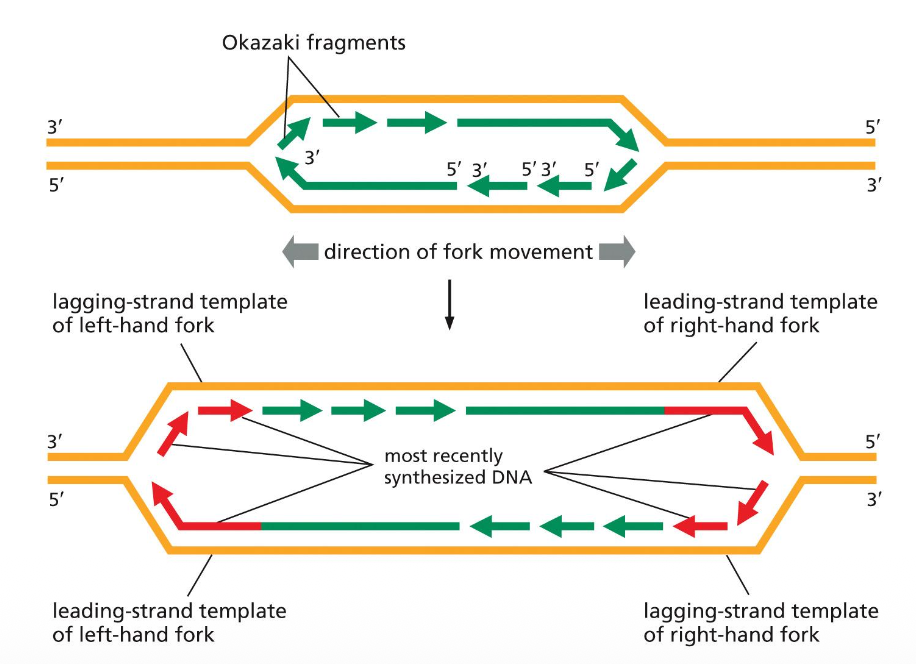
בשיעור הקודם דיברנו על מזלג ההכפלה, וראינו כי ה־leading strand מסונתז באופן רציף מן ה־origin ועד לקצה הכרומוזום. לעומתו, ה־lagging strand מסונתז באופן לא רציף, כמקטעי אוקזקי באורך של כ־200 נוקלאוטידים, אורך המשקף בקירוב את גודל היחידה הנוקלאוזומלית.
בעיית הקצוות: כאשר ה־lagging strand מגיע לקצה הכרומוזום, DNA פולימראז α מניח פריימר ומסנתז את מקטע האוקזקי האחרון. לאחר פירוק הפריימר, לא נשאר דבר שניתן להאריך ממנו. ה־DNA פולימראז אינו יכול להשלים את הרצף, משום שהוא לא מסוגל להתחיל סינתזה של שרשרת חדשה ללא קצה 3’-OH קיים. התוצאה היא שבכל מחזור רפליקציה מתרחשת התקצרות של קצה הכרומוזום.
טלומרים - מבנה ותפקיד
טלומר הוא הקצה של הכרומוזום. אורכו אינו קבוע לחלוטין, אלא נע סביב ערך ממוצע טיפוסי.
אורך הטלומרים נוטה להתייצב סביב אורך קבוע יחסית.
- כאשר הטלומר ארוך מדי, הוא נוטה להתקצר עד שהוא חוזר לאורך שיווי-המשקל.
- כאשר הטלומר קצר מדי, הוא נוטה להתארך עד שהוא חוזר לאותו אורך שיווי-המשקל.
לכן, בתאים מתחלקים אורך הטלומר אינו אקראי, אלא נשמר סביב מצב יציב (steady state), שמשקף שיווי-משקל בין שני תהליכים מנוגדים: התקצרות הטלומר במהלך הרפליקציה, והארכתו על־ידי טלומראז (ראו להלן).
גבול הייפליק (Hayflick Limit)
כאשר לוקחים תאים ראשוניים ממקור אנושי ומגדלים אותם במבחנה, הם מבצעים כ־20–50 חלוקות ואז נעצרים ומזדקנים. התופעה הזאת נקראת גבול הייפליק. הסיבה: קצה הכרומוזום מתקצר בכל חלוקה, וכאשר הטלומר מתקצר מספיק, מופעל צ’קפוינט שמונע המשך חלוקה. הטלומר משמש כשעון מולקולרי המודד את גיל התא.
יישום קליני: תאים אימורטליים (שורות תא מעבדתיות, תאים סרטניים) שומרים על יכולת חלוקה בלתי מוגבלת בין השאר בגלל הפעלה של טלומראז (ראו להלן).
אורך טלומרים בסוגי תאים שונים
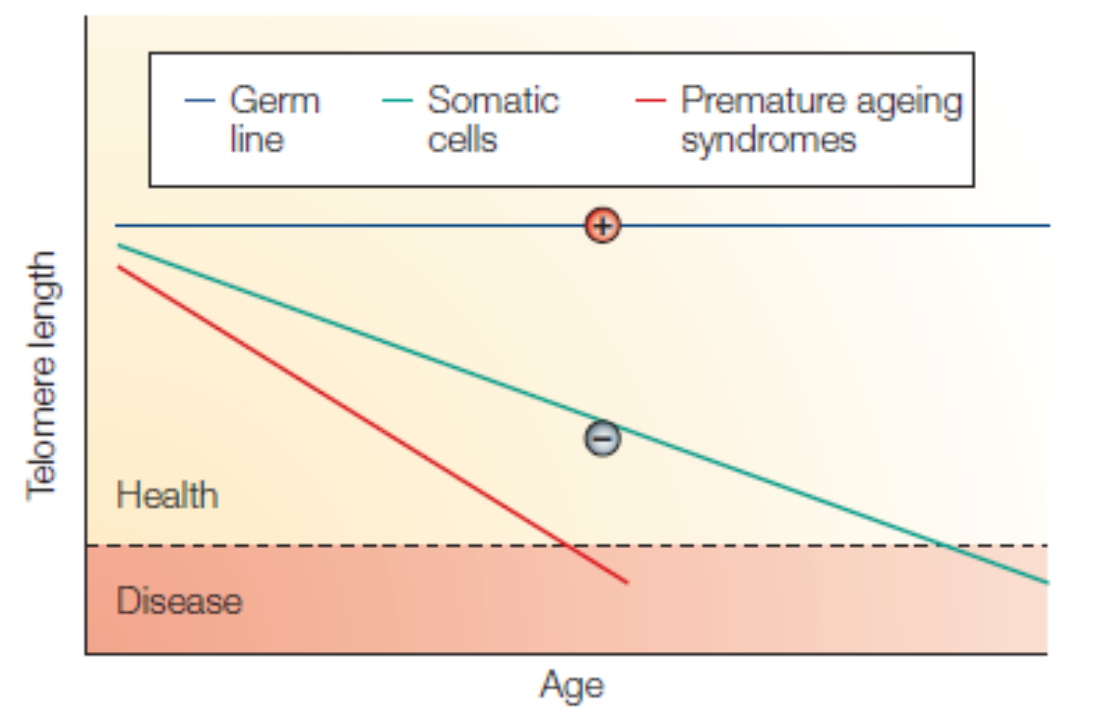
- תאים סומטיים נורמליים: אורך הטלומרים מתקצר באופן ליניארי עם כל חלוקה, עד שהם קצרים מדי בשביל לתמוך בפעילות ביולוגית ← מחלה / מוות של התא.
- מחלות הזדקנות מוקדמת: ההתקצרות מתרחשת הרבה יותר מהר מהצפוי - למשל הגעה לסף הקריטי בגיל 40 במקום 80.
- תאי גזע (Stem cells): אורך הטלומרים יציב - יש מנגנון פעיל (טלומראז) שמשמר אותו.
טלומראז (Telomerase)
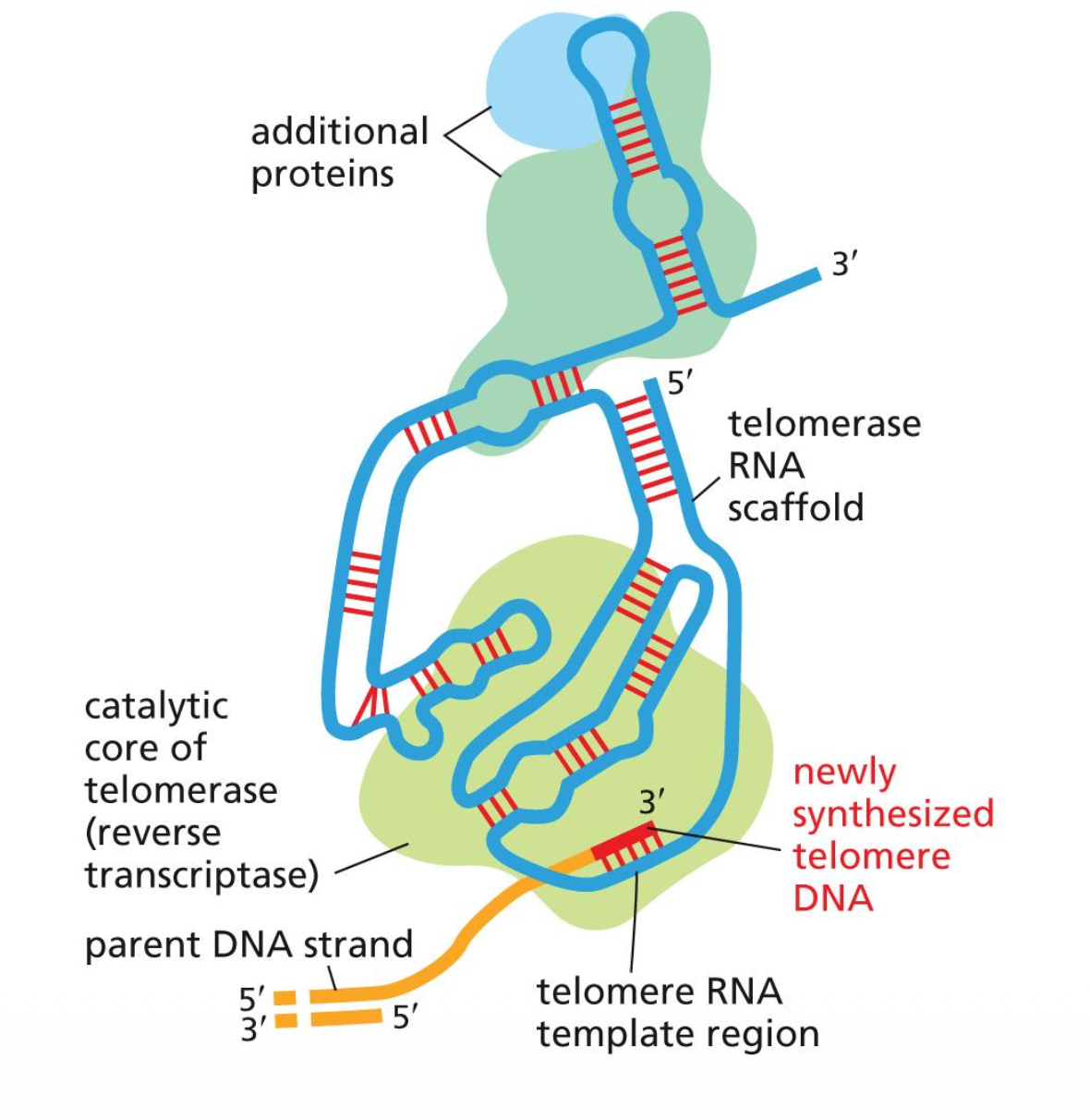
טלומראז הוא סוג מיוחד של DNA פולימראז, המכונה גם Reverse Transcriptase - אנזים שמסנתז DNA תוך שימוש ב־RNA כתבנית. (טרנספוזונים ורטרו־וירוסים הם דוגמאות נוספות למולקולות שמשתמשות ברוורס טרנסקריפטאז).
הגילוי: בשנות ה־80, Elizabeth Blackburn (שהחלה כפוסט-דוקטורנטית אצל Joe Gall ב־Yale) זיהתה את הפעילות. Carol Greider ו־Jack Szostak היו פוסט-דוקטורנטים שלה. שלושתם קיבלו פרס נובל בשנת 2009.
תכונות הטלומראז
| תכונה | טלומראז |
|---|---|
| כיוון סינתזה | 5’←3’ בלבד |
| יכולת התחלת שרשרת de novo | לא - יודע רק להאריך שרשרת קיימת |
| צורך בטמפלייט | כן - אך הטמפלייט פנימי לאנזים עצמו |
| סוג הטמפלייט | שרשרת RNA קצרה הקבועה בתוך מבנה החלבון |
מנגנון הפעולה
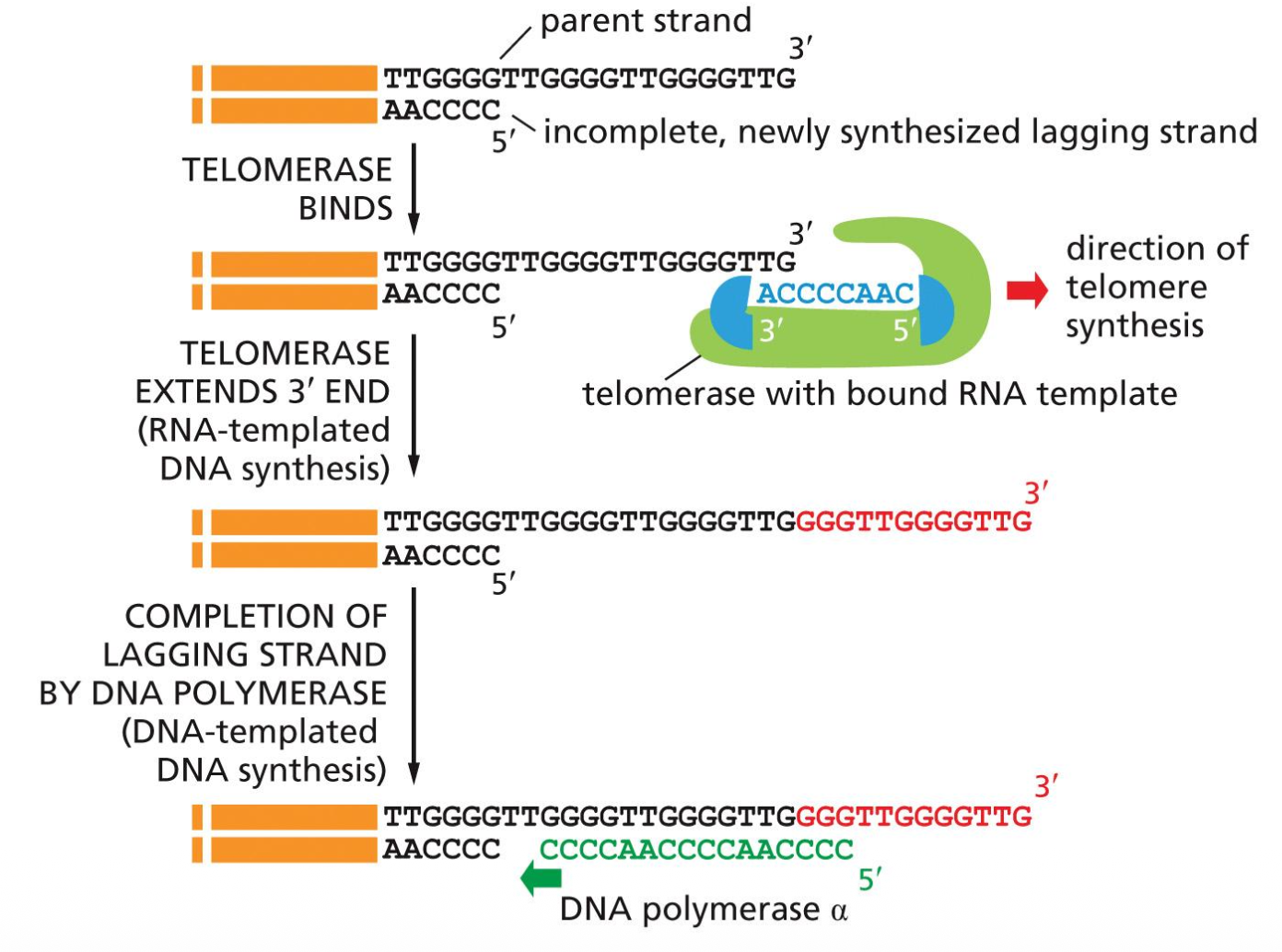
הטלומראז נקשר לקצה ה־DNA החד־גדילי שנותר פתוח לאחר הרפליקציה. הוא משתמש כתבנית ב־RNA פנימי, אשר מכיל רצף משלים לרצף הטלומרי, כדי להאריך את קצה ה־3’ של ה־DNA ולהוסיף חזרות של הרצף TTAGGG (באדם).
מנגנון הפעולה:
- הטלומראז נקשר לקצה ה־3’ של גדיל ה־DNA.
- תבנית ה־RNA הפנימית שלו מנחה את הסינתזה, ובכל מחזור נוספים כ־8 בסיסים.
- לאחר מכן הטלומראז זז קדימה על גבי הגדיל.
- הוא מבצע שוב סינתזה של אותה יחידה חוזרת.
- התהליך חוזר על עצמו שוב ושוב.
תוצאה: קצה הכרומוזום מורכב מרצפים חוזרניים שסונתזו לפי תבנית ה־RNA הפנימית של הטלומראז, ולכן אינו נושא מידע גנטי חיוני שעלול ללכת לאיבוד. ההתקצרות בכל מחזור רפליקציה מתרחשת בתוך הטלומר עצמו, ולא בתוך הרצף הגנטי החיוני.
לאחר שהטלומראז מאריך את הגדיל, נוצר single-strand overhang - קצה שבו אחד הגדילים ארוך יותר מהגדיל המשלים. הגדיל המוארך יכול לשמש כתבנית לסינתזה של ה־lagging strand, וכך מתאפשרת השלמה גם של הצד השני - לא באופן מלא, אך במידה מספקת.
מבנה הטלומר: לולאת T-Loop
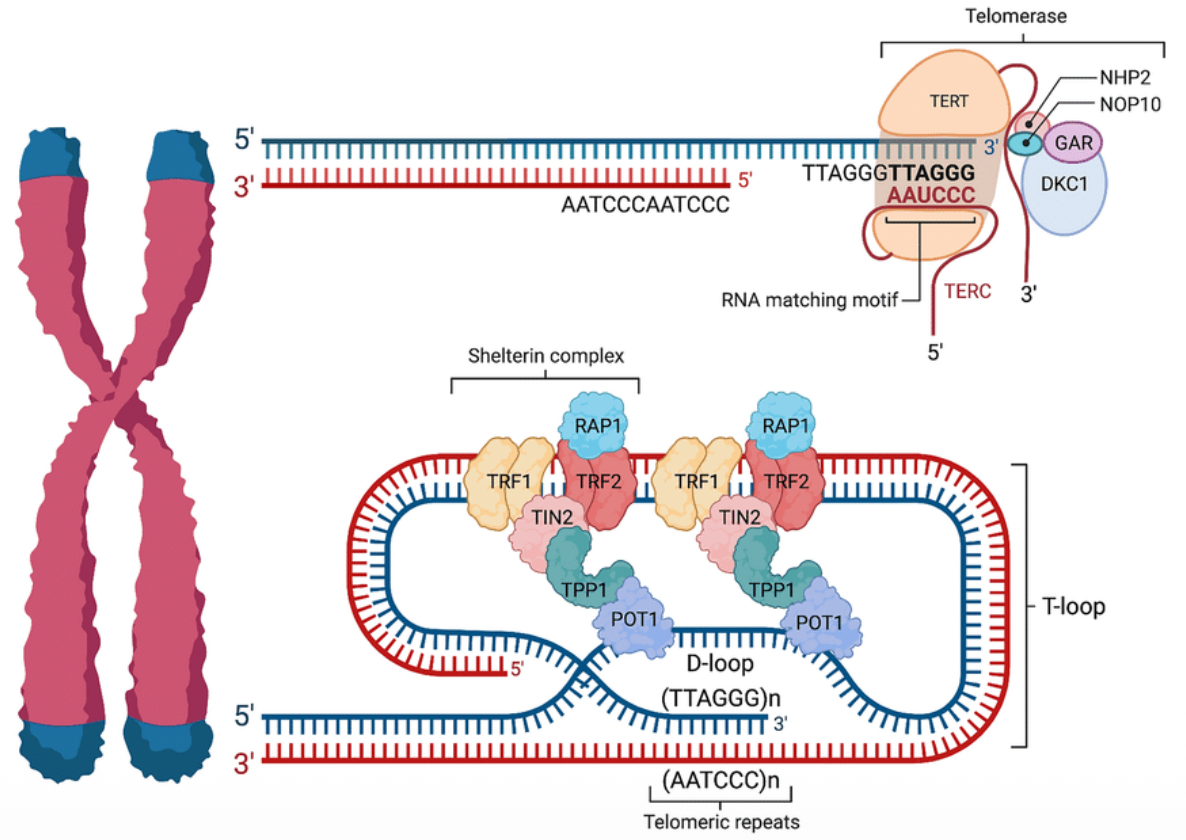
הקצה החד־גדילי החשוף של הטלומר עלול להיתפס בתא כאות אזהרה: התא עשוי לזהות אותו בטעות כשבר DNA דו־גדילי, או כ־DNA זר, ולהפעיל מנגנוני תיקון שאינם מתאימים. מצב כזה עלול לגרום לחיבור לא רצוי בין קצות כרומוזומים שונים.
כדי למנוע זאת, קצה הטלומר מאורגן במבנה הגנתי:
- ה־overhang החד־גדילי מתקפל חזרה אל תוך הטלומר.
- הוא פולש לאזור הדו־גדילי של הטלומר ויוצר מבנה לולאתי הנקרא T-loop.
- בנקודת הפלישה נוצר אזור תלת־גדילי מקומי, המכונה D-loop.
- כך הקצה הפתוח “מוסתר”, ולכן אינו מזוהה בקלות כנזק ל־DNA.
קומפלקס השלטרין (Shelterin)
מכיוון שקצה DNA חשוף אינו יציב ועלול להפעיל תגובת תיקון, הטלומר מוגן על ידי קומפלקס חלבוני הנקרא Shelterin. קומפלקס זה נקשר לאזור הטלומרי, מייצב את מבנה ה־T-loop ומסייע לדכא הפעלה לא רצויה של מנגנוני תיקון DNA.
הקומפלקס כולל בין היתר את החלבונים TRF1, TRF2, RAP1, וחלבונים נוספים. תפקידיו המרכזיים:
- ייצוב מבנה ה־T-loop.
- הגנה על קצה הכרומוזום מפני זיהוי כשבר DNA.
- סיוע בארגון אזור הטלומר במצב כרומטיני דחוס יותר, כלומר הטרוכרומטין.
- השפעה גם על האזור הסאב־טלומרי הסמוך, כך שגנים הקרובים לטלומר עשויים לעבור השתקה.
סמן להתקצרות טלומרים: כאשר הטלומר מתקצר, מבנה ה־T-loop ומצב ההטרוכרומטין נעשים פחות יציבים. כתוצאה מכך, גנים באזור הסאב־טלומרי עשויים להתחיל להתבטא. שינוי כזה נקשר לתהליכים הקשורים בהזדקנות תאית.
איחוי טלומרים (Telomere Fusion)
כאשר מבנה ה־Shelterin או ה־T-loop נפגע, קצות הכרומוזומים עלולים להישאר חשופים. במצב כזה התא עשוי לזהות אותם בטעות כשברי DNA דו־גדיליים, ולהפעיל מנגנוני תיקון שאינם מתאימים. במקום להגן על הקצה, מנגנונים אלו עלולים לחבר אותו לקצה כרומוזומלי אחר.
תופעה זו נקראת איחוי טלומרים (Telomere Fusion) והיא יכולה להתרחש בכמה מצבים:
- איחוי בין שתי כרומטידות אחיות של אותו כרומוזום - בצביעה עשויה להופיע נקודה אחת במקום שתי נקודות נפרדות.
- איחוי בין כרומוזומים שונים - נוצרים כרומוזומים המחוברים זה לזה בקצותיהם.
כאשר תא עם איחוי נכנס למיטוזה, הכרומוזומים המחוברים מתקשים להיפרד בצורה תקינה. בזמן האנאפאזה הם עלולים להימתח בין שני קטבי התא וליצור Anaphase Bridges. גשרים אלו עלולים להיקרע, לגרום לשברים כרומוזומליים, ולהוביל לאי־יציבות גנומית.
תפקיד נוסף: הגבלת תנועת הקצוות ושמירה על מבנה הטלומר
סגירת קצות הכרומוזום במבנה T-loop מגבילה את התנועה החופשית של הקצה הכרומוזומלי (מאפשרת מתח פיתולי) ומסתירה אותו ממנגנוני זיהוי נזקי DNA. כך נשמרת יציבות הטלומר, ונמנעת הפעלה לא רצויה של מנגנוני תיקון או איחוי בין כרומוזומים.
בנוסף, ארגון הקצה במבנה לולאתי תורם לסידור המרחבי של אזור הטלומר, ומשפיע על האופן שבו ה־DNA באזור זה נארז ומתפקד.
טלומרים, תאי גזע וסרטן
- תאי גזע: טלומראז פעיל - שומר על אורך הטלומרים. ברגע שתא יוצא ממצב תא גזע ומתחיל התמיינות, הביטוי של הטלומראז נסגר ולתא יש מספר חלוקות מוגבל. זה מנגנון בקרה שמונע חלוקה אינסופית.
- תאים ממוינים שאינם מתחלקים (כגון תאי עצב בוגרים): הבעיה פחות רלוונטית - לאחר שהגיעו למצבם הסופי, הם אינם מתחלקים.
- סרטן: תאים סרטניים צריכים לצבור כ־7 מוטציות. אחת התופעות השכיחות בתאים סרטניים היא הפעלה מחדש של טלומראז - מה שמקנה להם יכולת חלוקה בלתי מוגבלת / אימורטליות. לדוגמה: תאי HeLa. ולכן טלומראז הוא מטרה טיפולית אפשרית - פגיעה ספציפית בו תפגע בתאים סרטניים פחות מאשר בתאים נורמליים.
טופואיזומראז (Topoisomerase)
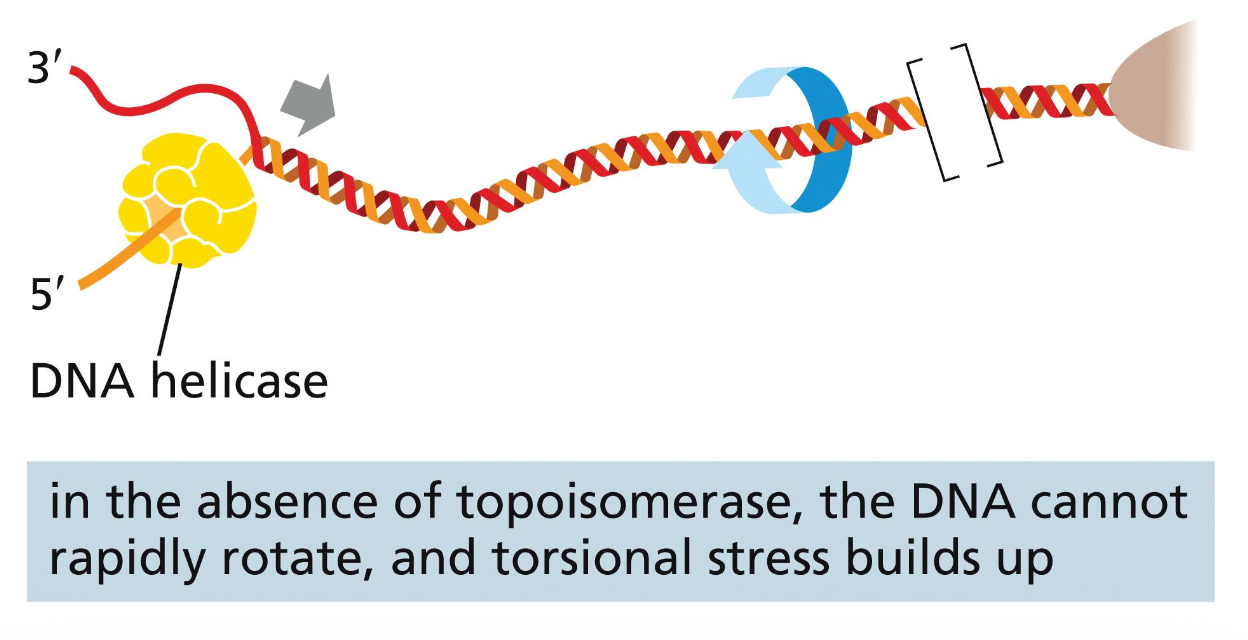
טופואיזומראזות הן אנזימים שיודעים לשנות את ה־Linking Number (Lk) של ה־DNA, ובכך לשנות את הטופולוגיה שלו. הן הוזכרו כבר בהקשר של הרפליקציה - כאשר ההליקאז פותח את הדו־גדיל, נוצר לפניו positive supercoiling שחייב להיפתר, אחרת הרפליקציה תיעצר.
מה מייחד טופואיזומראז מאנדונוקלאז? אנדונוקלאז חותך את ה־DNA ומשחרר את הקצוות - כל המתח הפיתולי משתחרר מיד ו־Wr מתאפס. טופואיזומראז לעומת זאת: חותך את ה־DNA אך ממשיך להחזיק את הקצוות - לא נותן לכל המתח להשתחרר בבת-אחת, אלא משחרר אותו בצורה מבוקרת, ואז סוגר מחדש את החיתוך.
סוגי טופואיזומראזות
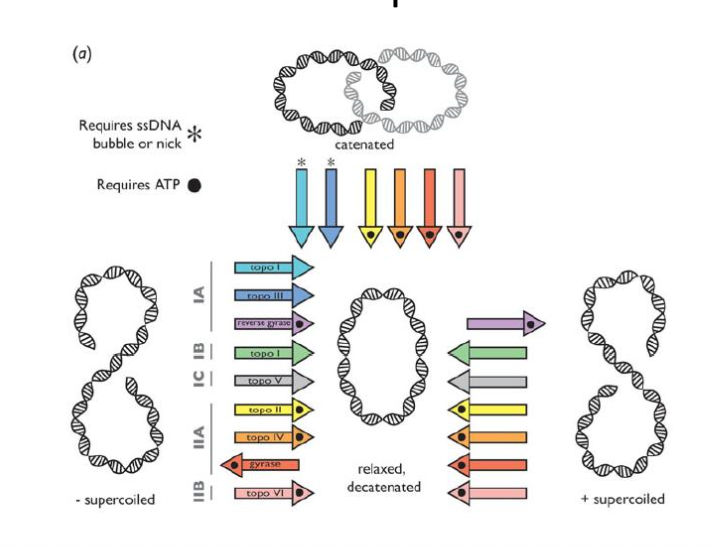
סוג I - חיתוך חד־גדילי:
- חותך גדיל אחד בלבד.
- מאפשר סיבוב של גדיל אחד ביחס לשני.
- משנה את Lk ב±1 בכל מחזור פעולה.
- אינו דורש ATP - עובר ממצב אנרגטי גבוה (supercoiled) למצב אנרגטי נמוך (relaxed).
סוג II - חיתוך דו־גדילי:
- חותך שני הגדילים (דו־גדיל שלם).
- מעביר דו־גדיל אחר דרך החיתוך.
- משנה את Lk ב±2 בכל מחזור פעולה.
- דורש ATP - לא לשחרור המתח (שגם הוא אנרגטי), אלא לשינויי קונפורמציה הנדרשים להעברת הדו־גדיל בתוך החלבון.
חריג: האנזים Gyrase (בחיידקים) - טופואיזומראז מסוג II שיודע לעשות את הכיוון ההפוך: ממצב relaxed למצב של negative supercoiling. דורש ATP (מצב אנרגטי גבוה). אין לו שקול ישיר באוקריוטים.
מנגנון פעולה - Type I
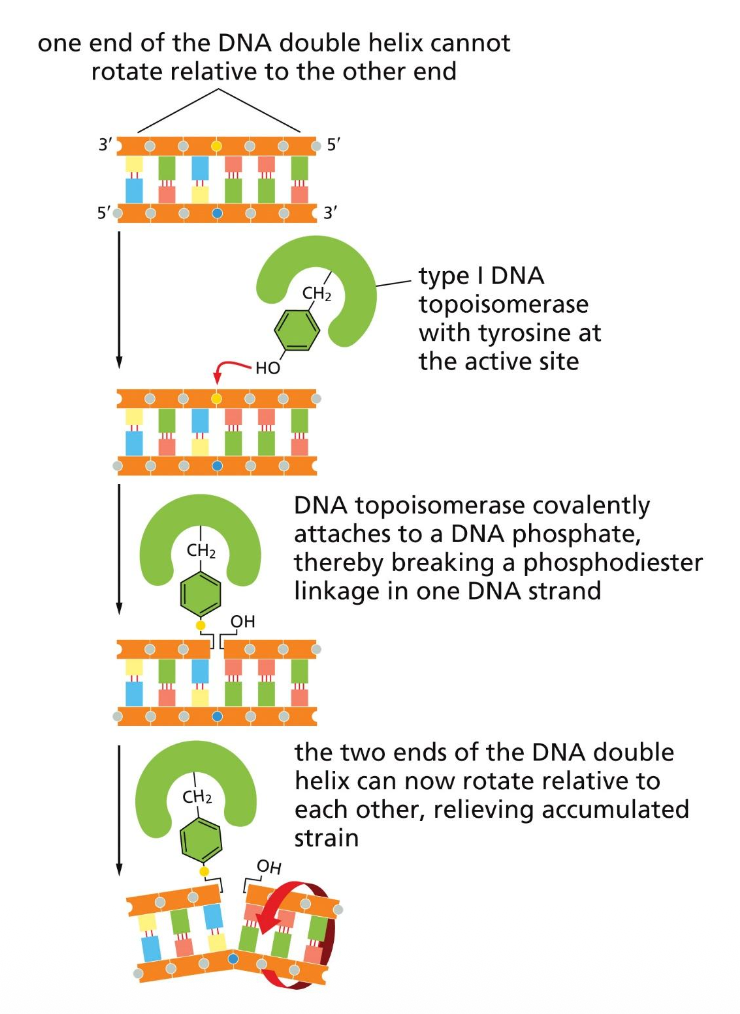
עקרון הפעולה של הטופואיזומראז טמון בשיירת טירוזין באתר הפעיל שלו. לטירוזין יש טבעת עם קבוצת הידרוקסיל בקצה - הדומה במידה מסוימת לנוקלאוטיד.
מחזור הפעולה:
- התקפה נוקלאופילית: קבוצת ה־OH של הטירוזין תוקפת את השלד הפוספוסוכרי ומבצעת הידרוליזה - שוברת את הקשר בין שני נוקלאוטידים סמוכים.
- יצירת קשר קוולנטי זמני: הטירוזין נקשר קוולנטית לקצה 3’ (או 5’, תלוי בסוג) של ה־DNA - הטופואיזומראז ממשיך להחזיק את הקצה.
- שחרור Tw: כעת ניתן לסובב גדיל אחד ביחס לשני - הקצה החופשי מבצע סיבוב, ומשחרר Tw אחד (שינוי Lk של 1). האנרגיה נשמרת בקשר הקוולנטי עם הטירוזין.
- סגירה מחדש: ה־OH החופשי תוקף בחזרה את הקשר בין הטירוזין לשלד, מחזיר את קשר הפוספודיאסטר ומשחרר את הטירוזין. ללא צורך בליגאז וללא צורך ב־ATP - האנרגיה נשמרה לאורך כל התהליך.
עיקרון חשוב: הטופואיזומראז עובד במחזורים - כל מחזור משחרר Tw אחד. אם משאירים אותו זמן רב עם DNA מסופרקוייל, הוא ימשיך לעבוד עד שהדו־גדיל יגיע למצב ה־Relaxed (Wr=0), שהוא המינימום האנרגטי.
מנגנון פעולה - Type II (Two-Gate Model)
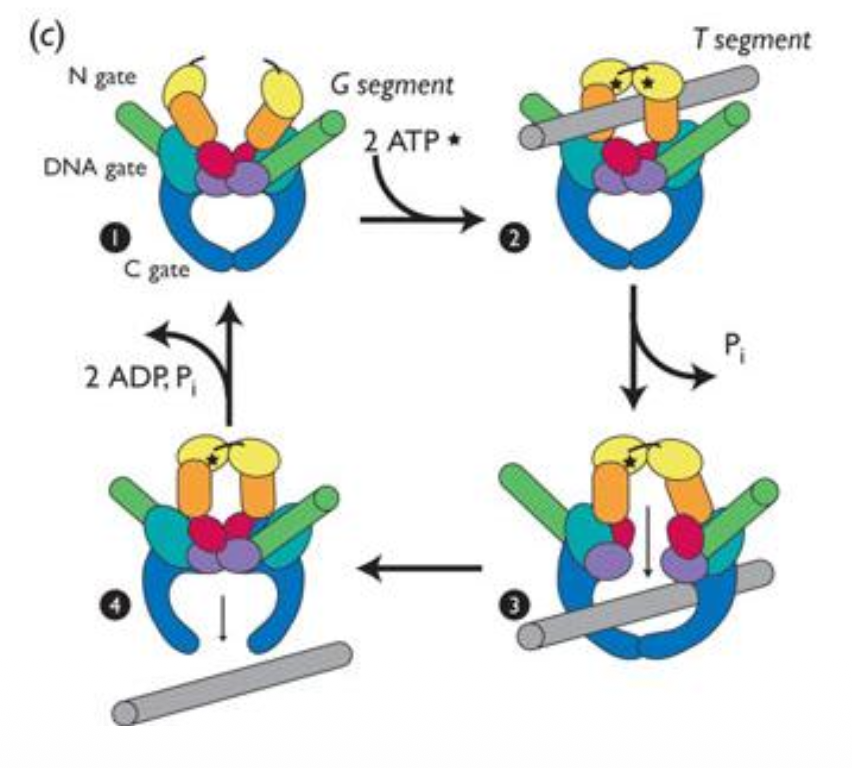
טופואיזומראז II עובד על שני דו־גדילים - חותך אחד ומעביר דרכו את השני:
- קישור: האנזים תופס שני דו־גדילים - ה”שייר” (G-segment) שייחתך, וה”מעביר” (T-segment) שיועבר דרכו.
- שינוי קונפורמציה (ATP): קישור של שתי מולקולות ATP סוגר את השער העליון ופותח את השער התחתון - האנזים שינה קונפורמציה.
- חיתוך: ה־G-segment נחתך בשני הגדילים, הקצוות מוחזקים על־ידי הטירוזינים.
- מעבר: ה־T-segment מועבר דרך החיתוך - דו־גדיל שלם עבר דרך דו־גדיל שלם אחר.
- סגירה: ה־G-segment נסגר מחדש; שני הדו־גדילים משתחררים.
- תוצאה: Lk השתנה ב־±2 (שני גדילים עברו).
הידרוליזה של ATP ל־ADP: נדרשת לשינויי הקונפורמציה (פתיחה/סגירה של השערים) ולא לשחרור המתח הפיתולי עצמו.
סיכום - השוואת סוגי טופואיזומראז
| Type I | Type II | |
|---|---|---|
| סוג החיתוך | חד־גדילי | דו־גדילי |
| מה משתנה | Tw | Wr |
| שינוי ב־Lk | ±1 | ±2 |
| צורך ב־ATP | לא | כן (לשינוי קונפורמציה בלבד) |
| ציר הפעולה | גדיל אחד מסתובב דרך שבר | דו־גדיל עובר דרך דו־גדיל |
קשר לסרטן ולרפואה
מחלות הקשורות לרפליקציה ולאנזימים
- מחלות של DNA פולימראז: מוטציות ב־Pol ε ו־Pol δ - פגיעה ב־Proofreading ← הצטברות מוטציות ← סרטן.
- Werner Syndrome: מוטציה בגן WRN1 (הליקאז). ההליקאז משמש גם בתיקון DNA וגם ברפליקציה - תקלה בו ← הזדקנות מוקדמת ונטייה לסרטן.
- Bloom Syndrome: מחלה גנטית תורשתית, שכיחה ביהודים אשכנזים - פגיעה בהליקאז, נטייה גבוהה לסרטן בגיל צעיר.
- Cornelia de Lange Syndrome: קשור לקוהיזין.
- מחלות
Trinucleotide Repeat: Fragile X, Huntington - נדונו בשיעור הקודם.
טרגטינג של מרכיבי הרפליקציה בטיפול בסרטן
- מעכבי טופואיזומראז: מטרה חשובה בכימותרפיה - עוצרים רפליקציה ב־DNA של התאים הסרטניים המתחלקים הרבה יותר מהר.
- פלטינום (Cisplatin ונגזרות): יוצר קרוסלינקינג קוולנטי בין גדילי ה־DNA - ה־DNA פולימראז אינו יכול לעבור את ה”חסם”.
- אנלוגים של נוקלאוטידים: חוסמים את ה־DNA פולימראז בכניסה.
- מעכבי טלומראז: מטרה אטרקטיבית כיוון שטלומראז פעיל בתאים סרטניים אך לא ברוב התאים הנורמליים.
האתגר: ספציפיות - רוב התרופות הנ”ל פוגעות גם בתאים נורמליים המתחלקים (מעי, שיער, מח עצם) ומייצרות תופעות לוואי. הפתרון: טרגטינג מקומי לגידול ספציפי, בייחוד לפני שהפך לגרורתי.
PCR ויישומים מעבדתיים-קליניים
PCR בסיסי
עקרון הריאקציה: טמפלייט + פריימרים + dNTPs + DNA פולימראז. בכל מחזור - דנטורציה (95°C), היברידיזציה (כ־55–65°C), סינתזה (72°C). הכפלה אקספוננציאלית: 2ⁿ מולקולות לאחר n מחזורים.
הטריק המרכזי: שימוש ב־Taq פולימראז מ־Thermus aquaticus - חיידקים ממעיינות חמים (Yellowstone) שעמידים ב־95°C. הרעיון של קארי מוליס (פרס נובל 1993): אנזים עמיד-חום שאינו עובר דנטורציה בכל מחזור.
גודל מקסימלי ב־PCR סטנדרטי: ~3,000–5,000 בסיסים; עם אנזים מיוחד עם Proofreading - עד כ־10,000 בסיסים.
יישום קליני - מחלות Trinucleotide Repeat: ניתן לקחת דגימת דם, להפיק DNA ופשוט למדוד את אורך המקטע כדי לדעת את מספר החזרות. למשל Fragile X - מספר חזרות CGG מעל 200 ← פתולוגי.
qPCR (Quantitative PCR)
מאפשר מידע כמותי - לא רק “כן/לא” אלא כמה עותקים (טיטר וירלי). מנגנון: שימוש ב־SYBR Green (קושר ספציפית ל־dsDNA) - מודד פלואורסנציה בכל מחזור. כיוון שפלואורסנציה פרופורציונלית למספר המולקולות, ניתן לחשב כמות.
יישום קליני: קורונה, שפעת וירוסי RNA אחרים - עם RT-PCR (Reverse Transcription + PCR): הרוורס טרנסקריפטאז הופך RNA → cDNA, ואז PCR סטנדרטי.
שיטת סנגר לריצוף DNA (Sanger Sequencing)
עיקרון: PCR עם תוספת ddNTPs (Dideoxynucleotides) - דומים ל־dNTPs אך חסרה קבוצת 3’-OH. אם ddNTP נכנס, הסינתזה נעצרת (אין 3’-OH להמשך שרשרת). בריכוז נמוך של ddNTPs, הריאקציה נעצרת באופן אקראי בכל מיקום ← מתקבלות מולקולות בכל האורכים. הפרדה קפילרית לפי גודל + צביעה פלואורסנטית לפי בסיס ← שחזור הרצף.
- אורך קריאה מקסימלי: כ־1,000 בסיסים (ה־100–200 הראשונים בדרך כלל באיכות נמוכה).
- זמן: בערך שעתיים, מכשיר קטן.
- יישום קליני: מוטציות נקודתיות, רצפים ויראליים ידועים, אימות מחלות גנטיות ספציפיות.
NGS - Next Generation Sequencing (Illumina)
מאפשר ריצוף גנום שלם:
- שבירה מכנית (סוניקציה) ל־כ־500 bp.
- חיבור אדפטורים (רצפים סינתטיים ידועים + אינדקסים להבדלת דוגמאות).
- היברידיזציה על צ’יפ עם פריימרים משלימים לאדפטורים.
- Bridge Amplification - יצירת קלאסטרים של ~200 מולקולות זהות.
- Reversible Terminator Sequencing - כימיה הפיכה: נוקלאוטיד פלואורסנטי נכנס ← צילום ← שחרור כימי ← כניסת הבסיס הבא.
- Bioinformatics: יישור כל המקטעים לגנום ייחוס ← שחזור הרצף המלא.
- כיסוי: 90%+ מהגנום; בעיה ברצפים חוזרים (לא ניתן למקם אותם בוודאות).
- מחיר: פחות מ־$1,000 לגנום שלם כיום.
יישום קליני: Whole Exome Sequencing (WES) לאבחון מחלות גנטיות; כאשר יש תינוק עם פיזיולוגיה לא מוסברת, WES הוא כלי האבחון העוצמתי ביותר.
Oxford Nanopore - הדור הבא
מבוסס על מדידה חשמלית של DNA שעובר דרך ממברנה - כל נוקלאוטיד יוצר התנגדות חשמלית שונה. יתרונות:
- קריאות ארוכות מאוד (כ־50,000–100,000 בסיסים) ← פתרון בעיית הרצפים החוזרים.
- מאפשר קריאת מודיפיקציות (מתילציה, אפיגנטיקה) ישירות מה־DNA - ללא שלבים נוספים.
עדיין אינו בשימוש קליני שגרתי; עיקר השימוש בו כיום הוא במחקר, אך בעתיד הוא עשוי להפוך לכלי זמין גם במרפאת רופא משפחה.
דור פסקל