מבוא למסלול ההפרשה (The Secretion Pathway)
ברוכים הבאים לסדרת שלושה שיעורים על הובלת וזיקולות בתוך התאים. הנושא נקרא The Secretion Pathway, או בעברית “מסלול ההפרשה” - למרות שכפי שציין המרצה, התרגום לעברית לא מעורר קונוטציות טובות ואולי צריך מיתוג מחדש.
חשוב להבין ש”מסלול ההפרשה” לא עוסק רק בהפרשה (secretion), אלא גם בהכנסת חומרים מבחוץ באמצעות אנדוציטוזה. זהו תהליך דו־כיווני החיוני לתפקוד התא.
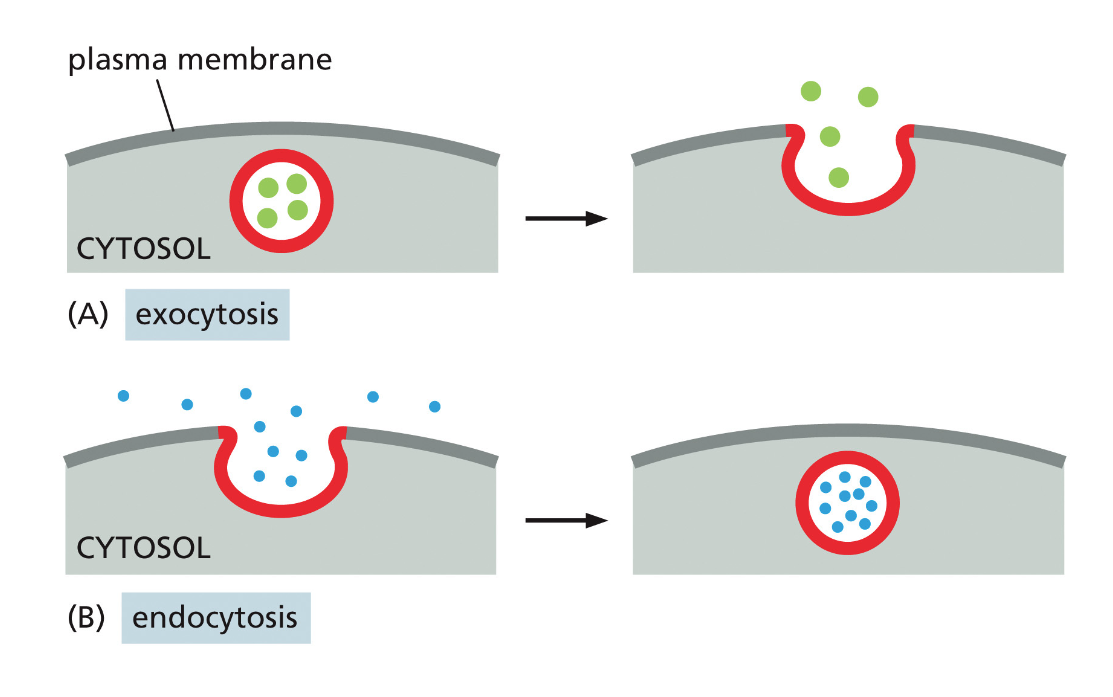
מנגנון כללי של הובלת וזיקולות
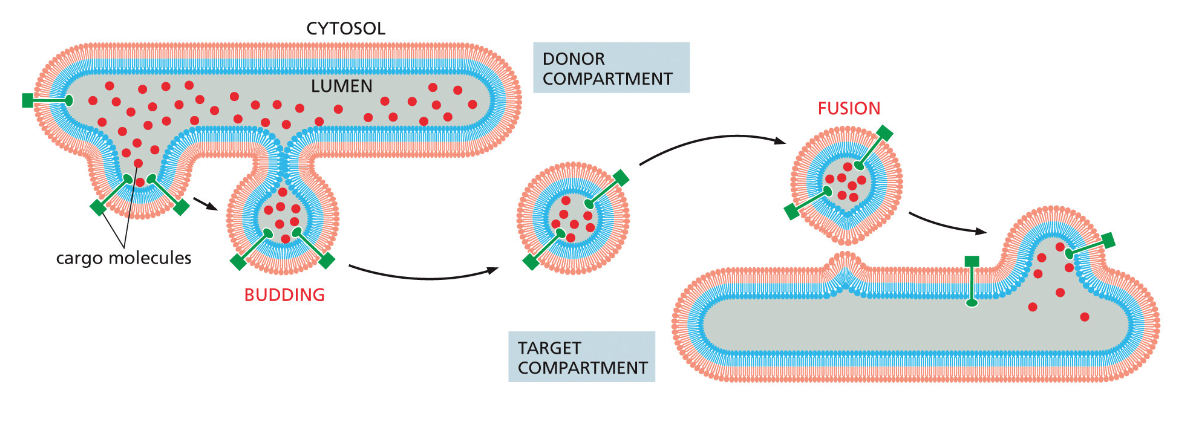
התהליך הבסיסי של הובלת וזיקולות בתא מתחלק לארבעה שלבים עיקריים:
- Budding (הנצה) - יצירת הוזיקולה מממברנה קיימת
- Tethering (קישור) - זיהוי ראשוני של המטרה
- Docking (עגינה) - התקרבות וחיבור מדויק
- Fusion (איחוי) - התמזגות הממברנות
בשלב ההנצה (Budding) נוצרת הוזיקולה מממברנה קיימת, ובמהלך התהליך הזה הווזיקולות מכוסות בחלבוני מעטפת המספקים מבנה מכני ומאפשרים זיהוי ראשוני של סוג הוזיקולה.
עם זאת, חלבוני המעטפת לבדם אינם מספיקים. אנחנו צריכים סימונים יותר מדויקים כדי שכל וזיקולה תגיע בדיוק לאן שהיא צריכה להגיע.
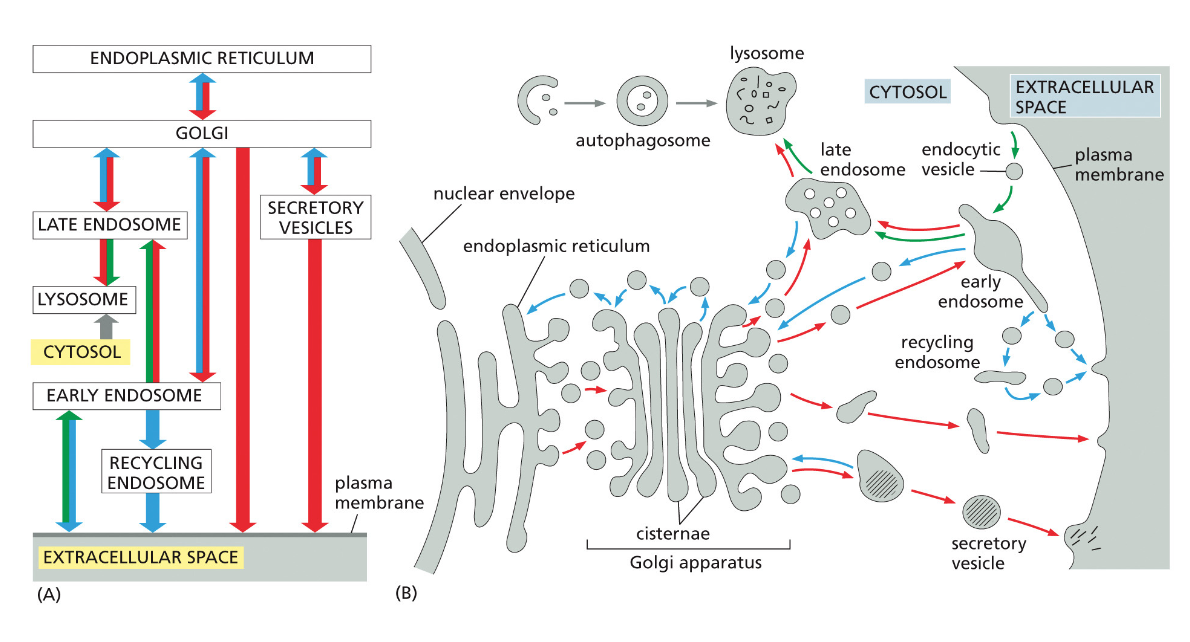
חלבוני Rab - מערכת הכתובות התאית
מי שמאפשר את הסימון המדויק של יעדי הווזיקולות הם משפחה של חלבונים שנקראים חלבוני Rab. יש Rab מ־1 עד 9 וגם 11 שמשתמשים בהם, וכנראה יש עוד חלבוני Rab שעדיין לא זיהינו.
כל חלבון Rab מסמן וזיקולה לכיוון מסוים - למשל, Rab1 יסמן וזיקולות השולחות מה־ER לגולג׳י, Rab2 יסמן וזיקולות שנמצאות באזור הציס-גולג׳י, ו־Rab3 יסמן וזיקולות בסינפסות שמשחררות נוירוטרנסמיטורים.
המנגנון עובד כך: חלבוני Rab יודעים לזהות חלבוני קישור (Rab effectors) שייחודיים עבורם. אם מדובר בחלבון Rab2 שנמצא בציס-גולג׳י, החלבון שאמור לקשור אותו נמצא רק בציס-גולג׳י. כך אנחנו מבטיחים שהוזיקולה תגיע רק למקום אחד שהיא צריכה להגיע.
זה לא מספיק כי שיש בעיה נוספת: ממברנות קרובות זו לזו אף פעם לא יעברו איחוי ספונטני בגלל שיש ביניהן מולקולות מים. צריך כוח מכני מספיק חזק בשביל לגרום לממברנות להתאחות.
| חלבון Rab | תפקיד |
|---|---|
| Rab1 | וזיקולות מ־ER לגולג׳י |
| Rab2 | וזיקולות באזור ציס-גולג׳י |
| Rab3 | וזיקולות בסינפסות (שחרור נוירוטרנסמיטורים) |
חלבוני SNARE - המנוע המכני
כאן נכנסים לתמונה חלבוני SNARE. יש לנו V-SNARE (Vesicle SNARE - על הוזיקולה) ו־T-SNARE (Target SNARE - על אברון המטרה). ברגע שחלבוני Rab מקרבים את הוזיקולה למטרה ויש את הקישור (Tethering), חלבוני SNARE נכנסים לפעולה בשלב ה־דוקינג.
התהליך יפה: חלבוני SNARE מתחברים זה לזה ועוברים תהליך כמו של שזירה - כמו כשלוקחים הרבה סיבים ומפתלים אותם יחד, האורך שלהם מתקצר. הכוח המכני הזה מקרב את הממברנות זו לזו, דוחק החוצה את מולקולות המים, עד שיש את השלב האחרון - Fusion, האיחוי. אחרי האיחוי, באמצעות ATP, החלבונים משתחררים ומוכנים למחזור הבא.
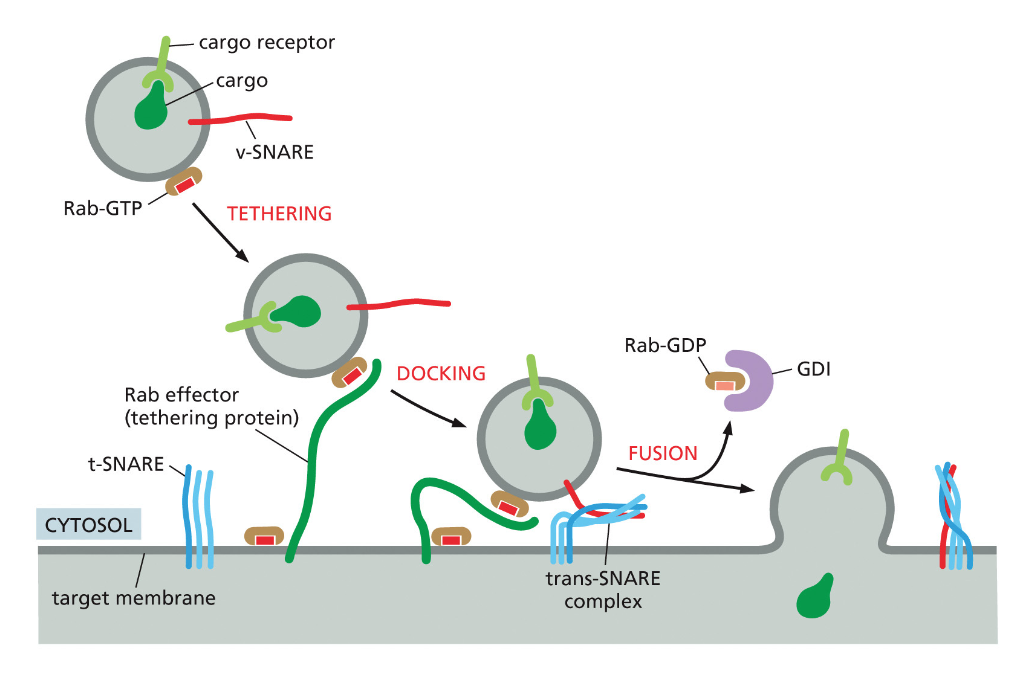
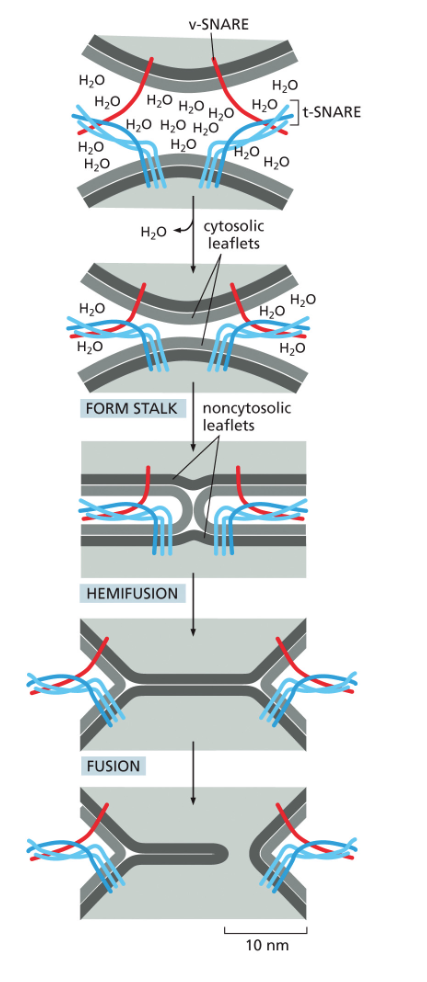
מה ההבדל המהותי בין SNARE ל־Rab? חלבוני Rab הם ספציפיים לכל וזיקולה ואברון מטרה אבל לא יכולים להפעיל כוח מכני. חלבוני SNARE הם כלליים (אותם SNARE על כל הווזיקולות) אבל יכולים להפעיל כוח מכני. צריך את שניהם - Rab לספציפיות, SNARE לביצוע.
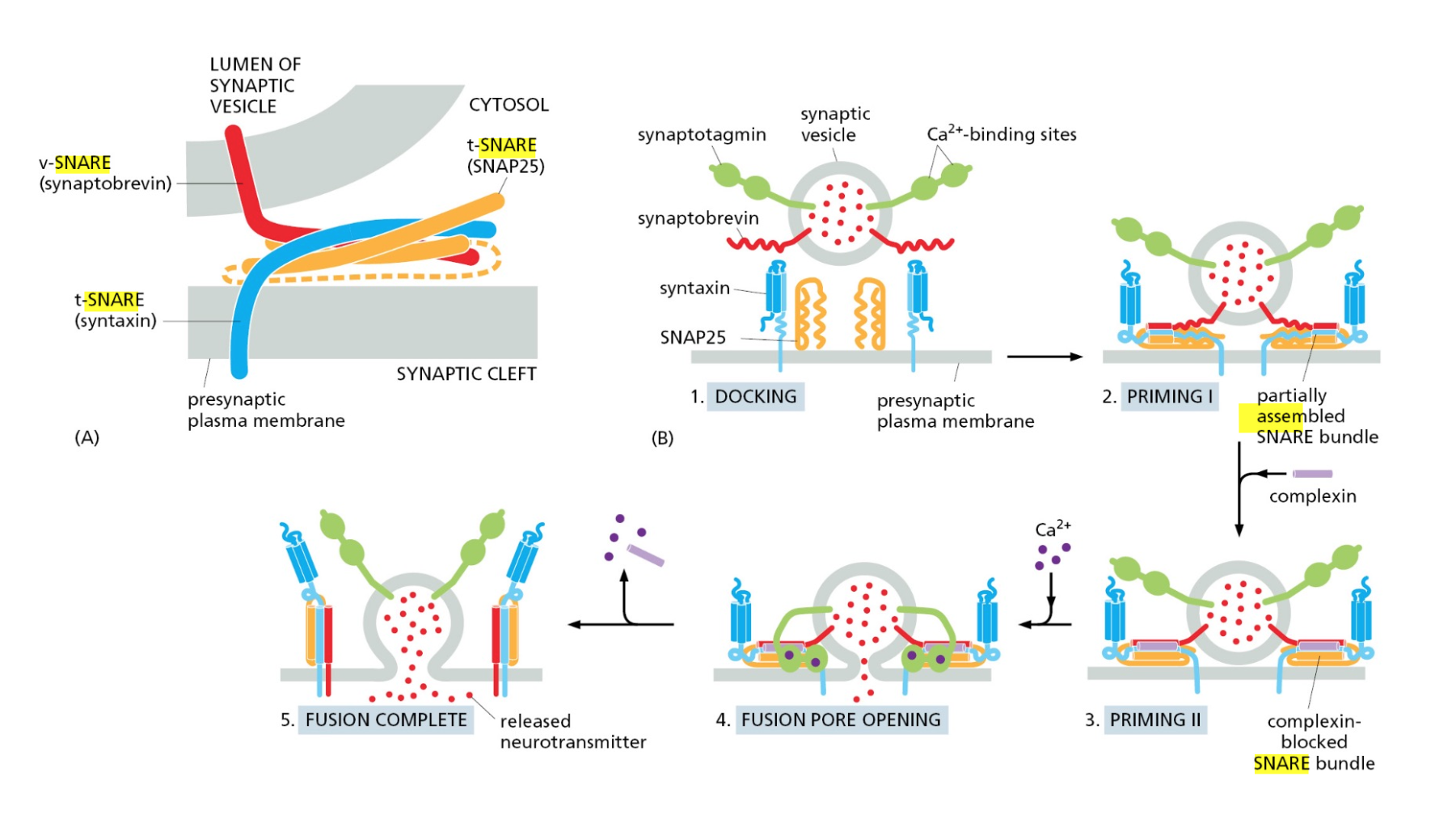
הבדלים תפקודיים: Rab מול SNARE
| היבט | חלבוני Rab | חלבוני SNARE |
|---|---|---|
| ספציפיות | ספציפיים לכל וזיקולה ויעד | כלליים לכל הווזיקולות |
| כוח מכני | אינם יכולים להפעיל | מפעילים כוח מכני |
| תפקיד | זיהוי ובחירת יעד | ביצוע האיחוי |
המסלול מה־ER לגולג׳י
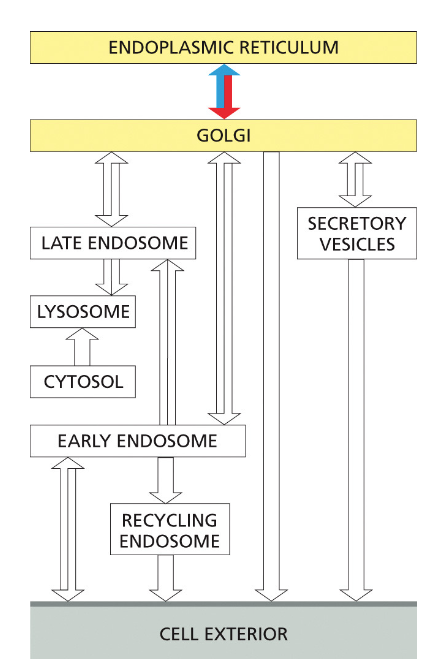
עכשיו נתחיל לדבר בצורה יותר ספציפית על המסלול מה־ER לגולג׳י. התהליך מתחיל באזורים ב־ER שנקראים Exit Sites (אתרי יציאה). למרות השם ביחיד, יש הרבה כאלה ב־ER והם נוצרים באופן רנדומלי.
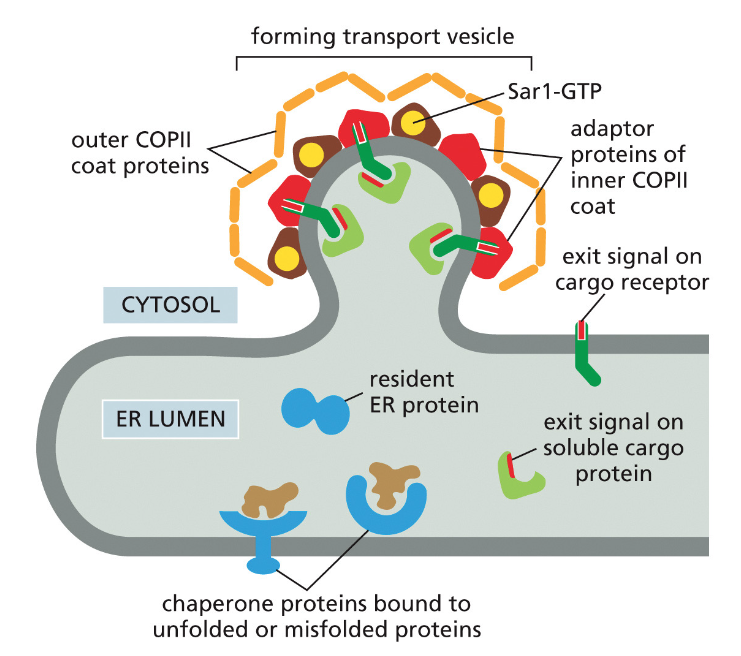
ברגע שחלבונים טרנס־ממברנליים מסונתזים, הם מיד “נתקעים” בממברנה. הם לא יכולים להסתובב חופשי בציטוזול או בלומן של ה־ER כי יש להם אזורים הידרופוביים שיגרמו להם להתקפל על עצמם. לחלבונים האלה יש סיגנל שנקרא Exit Signal - רצף ספציפי של חומצות אמינו שמזוהה על ידי חלבוני COPII.
מה קורה עם חלבונים שהם לא ממברנליים אבל צריכים להיכנס למסלול ההפרשה? הם “תופסים טרמפ” עם החלבונים הממברנליים. גם להם יש Exit Signal משלהם, והם נקשרים לחלבונים הטרנס־ממברנליים שנקשרים ל־COPII.
בקרת איכות - תפקיד השפרונים
המסלול הזה לא מושלם, ולפעמים נדחפים לתוך הוזיקולה גם חלבונים שצריכים להישאר ב־ER. אבל יותר חשוב - מאוד חשוב שלא יגיעו חלבונים שלא יוכלו לבצע את תפקידם כמו שצריך - וזה קורה כשחלבונים לא מתקפלים כראוי.
שפרונים הם חלבונים שעוזרים לחלבונים להתקפל כראוי. כשחלבון לא מתקפל כמו שצריך, השפרונים נקשרים אליו ומונעים ממנו להיכנס לווזיקולות.
הדוגמה של CFTR וציסטיק פיברוזיס
דוגמה קלאסית - חלבון CFTR שמוטציה בו גורמת לציסטיק פיברוזיס. זוהי תעלת יוני כלוריד שצריכה להעביר יונים כדי למשוך מים אל מחוץ לתאים. אם היא לא עובדת, מים לא יוצאים מהתאים והריר בריאות נהיה מאוד צמיגי.
מה שמעניין ופרדוקסלי: המוטציה לא מונעת מהחלבון לעבוד! אם ניקח את חלבון ה־CFTR ונצליח להביא אותו לממברנה, הוא יתפקד כתעלת כלוריד. אבל בגלל שהכיפול לא תקין, השפרונים לא משחררים אותו מה־ER. “הגוף מכשיל את עצמו”. אפילו אם החלבון יתפקד רק ב־30%, זה עדיף מאשר שלא יהיה בכלל.
תהליך ההובלה וההתקדמות
לאחר שהווזיקולות עוברות הנצה, חלבוני מנוע רצים על גבי המיקרוטובולים ולוקחים את הווזיקולות לכיוון חוץ התא. בשלב הזה הווזיקולות מורידות את חלבוני COPII, והן הופכות למה שנקרא VTC - Vesicular Tubular Clusters. השם מתאר את המראה שלהן במיקרוסקופ - הן נראות כמו צינורות (Tubular) שמורכבים מוזיקולות (Vesicular) שהתחברו יחד לצבר (Clusters).
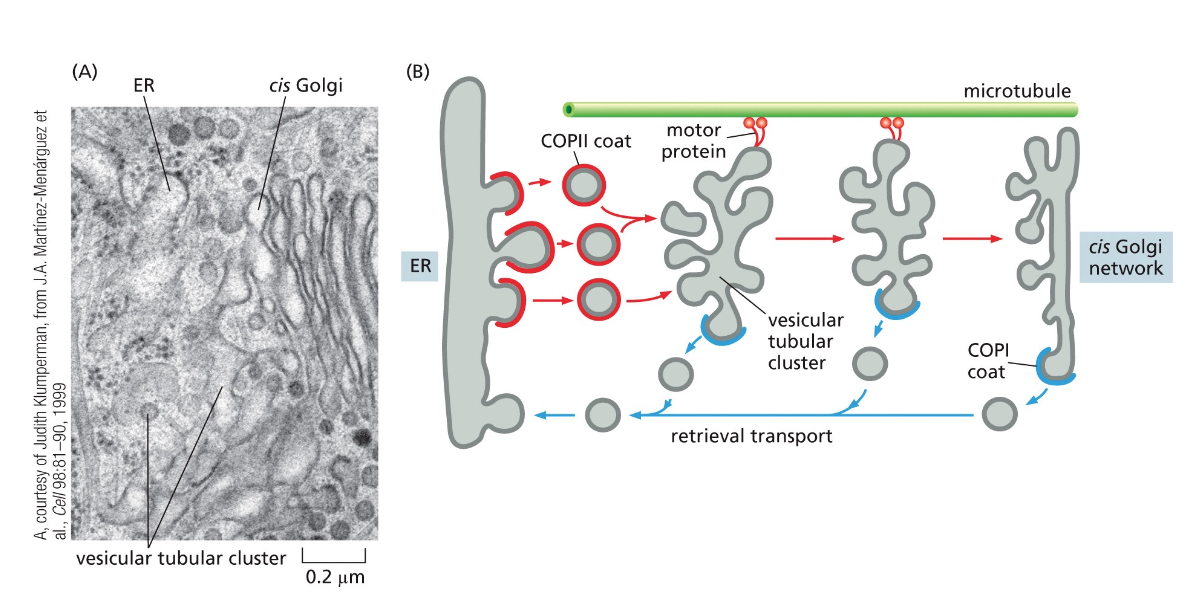
מסלול החזרה - מערכת KDEL
לאורך כל התהליך הזה יש מסלול של החזרה, שמסומן על ידי חלבוני COPI (לא COPII!). במסלול החזרה אנחנו מחזירים את הרצפטורים שתפסו את המטען, מחזירים ממברנות (אחרת ה־ER יתכווץ), ומחזירים חלבונים שבטעות יצאו מה־ER.
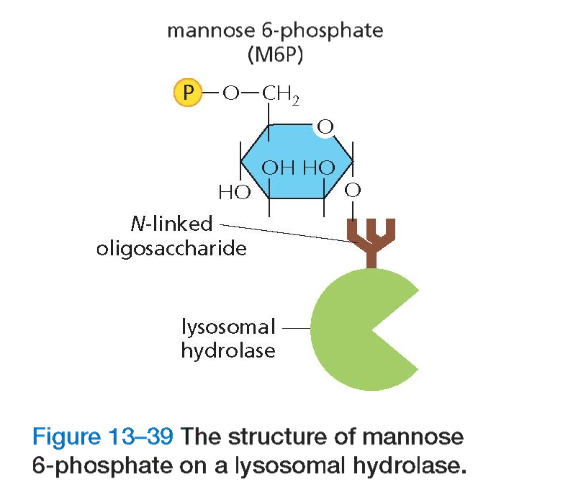
החוכמה של המערכת נמצאת ברצף KDEL - ארבע חומצות אמינו (K-D-E-L) שמסמנות חלבונים השייכים ל־ER. רצף KDEL נקשר לרצפטור ספציפי, והרצפטור נקשר ל־COPI.
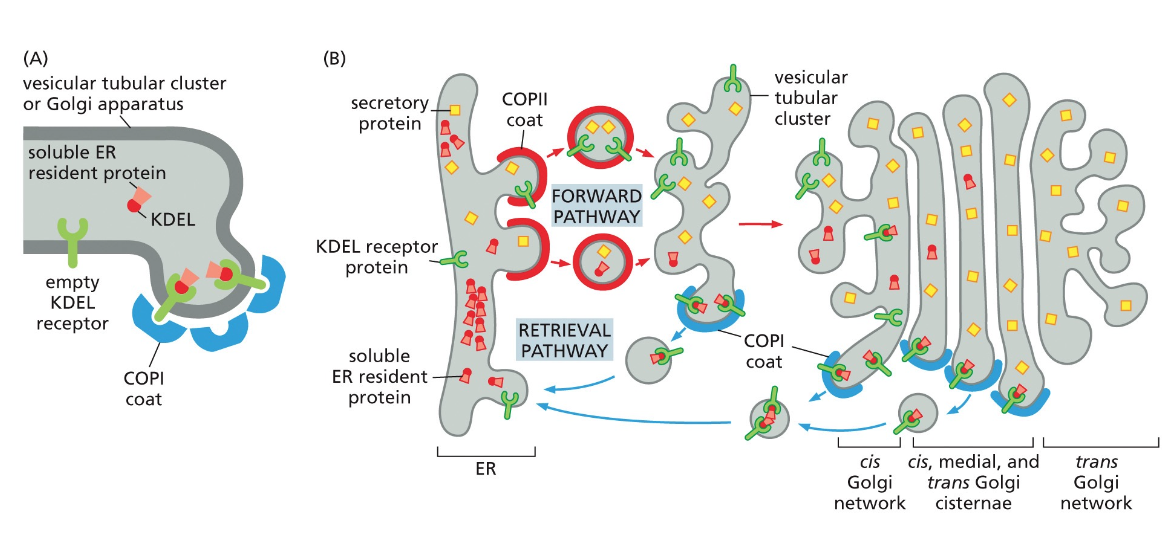
המנגנון החכם של pH
למה הקישור נעשה בגולג׳י ולא ב־ER? ה־pH ב־ER הוא קרוב ל־7 (ניטרלי), אבל ככל שמתקדמים בגולג׳י לכיוון וזיקולות שיוצאות מהתא, ה־pH יורד (נהיה חומצי). ב־pH חומצי, רצף KDEL נקשר לרצפטור. ב־pH ניטרלי, החלבון משוחרר.
זה תהליך מתמשך של “ניקוי” - כל פעם מושכים אחורה חלבונים שבטעות ברחו, עד שמגיעים לטרנס־גולג׳י שם אמור להיות מצב נקי. אם עושים מוטציה ב־KDEL, החלבון יצא מהתא במקום להישאר ב־ER - כך הוכיחו את החשיבות של הרצף.
מבנה הגולג׳י - מגדל הפיטות
הגולג׳י נראה כמו מגדל של פיטות - אם ניקח וזיקולה גדולה מאוד בצורת כדור ונלחץ אותה, נקבל משהו כמו פיטה עם חלל פנימי וממברנה מסביב. כשמערימים הרבה כאלה זו על זו, מקבלים את המבנה האופייני של הגולג׳י. המבנים האלה נקראים ציסטרנות.
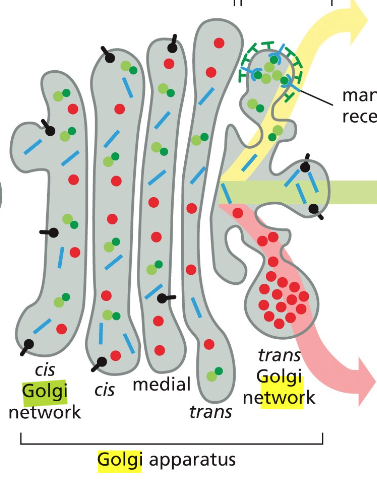
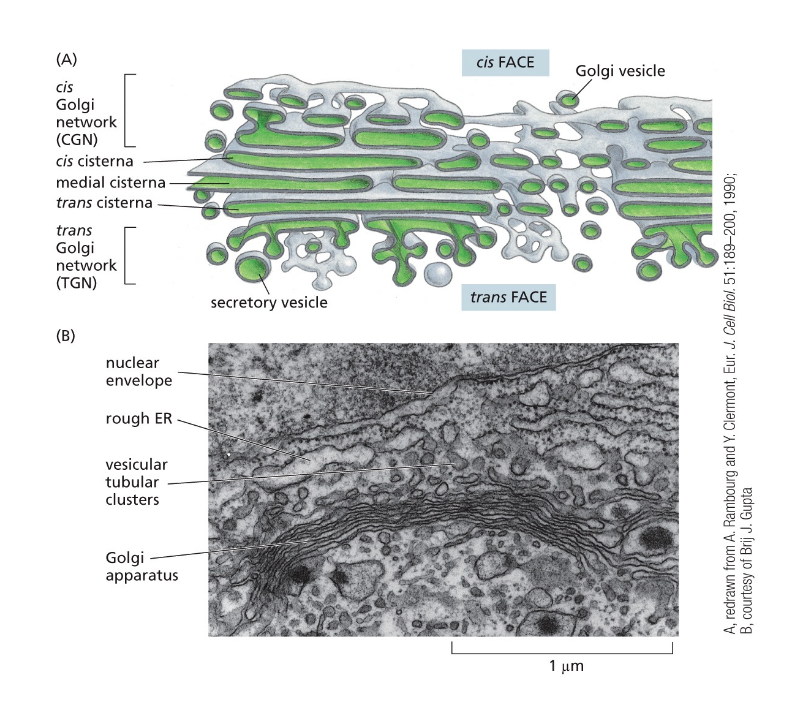
המיקרוטובולים מחזיקים את הציסטרנות במקום, כדי שכל ה”פיטות” האלה לא יתפזרו בחלל התא. יש לנו ציס-גולג׳י (הצד הפנימי הקרוב ל־ER) וטרנס־גולג׳י (הצד החיצוני הפונה לממברנת התא).
התעלומה: איך עוברים בין ציסטרנות?
ככל הנראה עדיין אין לנו מושג. יש שתי תיאוריות מתחרות:
תיאוריה ראשונה: בין ציסטרנה לציסטרנה יוצאות וזיקולות ומתחברות לציסטרנה הבאה.
תיאוריה שנייה: כל VTC שמגיע מה־ER הופך להיות הציס-גולג׳י החדש (כמו כשבאים לרופא ושואלים “מי האחרון?” ואומרים לך “אתה”). מי שהיה ציס מתחיל לנוע, וככל שמתחברות עוד וזיקולות, הציסטרנות מתקדמות. הציסטרנה נשארת אותו דבר, החלבונים לא עוזבים אותה - היא עצמה מתקדמת עד שהופכת לטרנס־גולג׳י ומתפרקת.
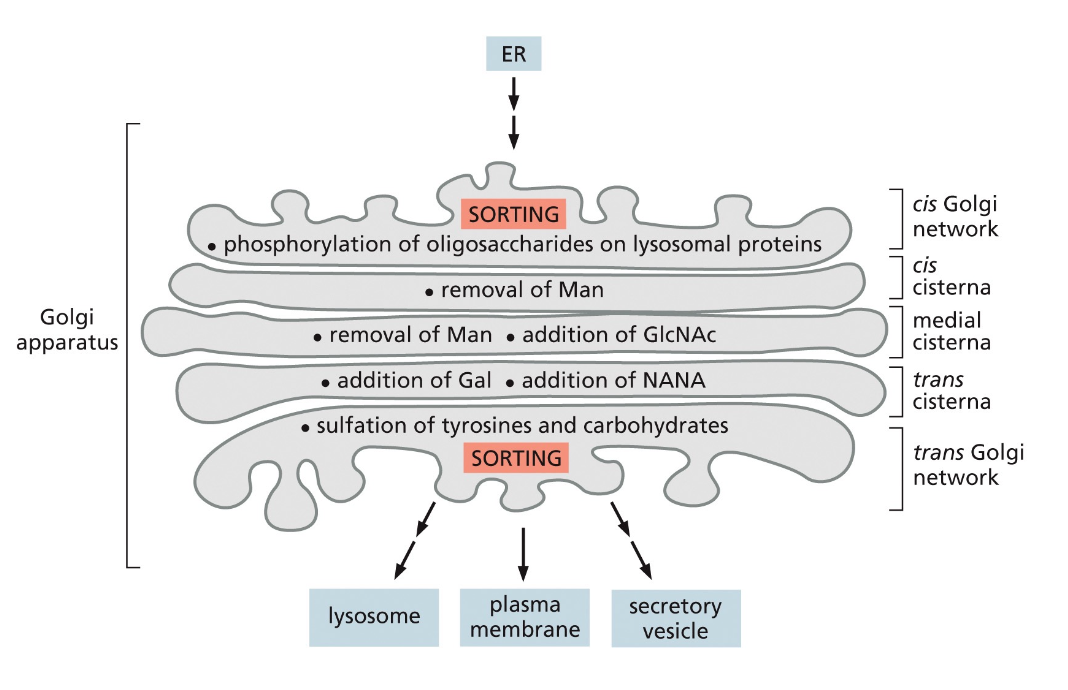
גליקוזילציה - אחד התפקידים המרכזיים של הגולג׳י
בגולג׳י מתרחש תהליך מאוד חשוב של גליקוזילציה - הוספה או הסרה של סוכרים מחלבונים. מה שמעניין הוא שבכל אזור בגולג׳י יש תהליך אחר של גליקוזילציה, וזה סופר חשוב כי יש המון סוגים שונים של סוכרים שצריכים להיבנות בסדר מסוים.
אפשר לחשוב על אותיות ומילים. אנחנו לא יכולים סתם לזרוק אותיות בסדר רנדומלי, אנחנו צריכים לשים אותן בסדר מסוים כדי שייצרו מילים שאנחנו יכולים להבין. הסוכרים זה בדיוק אותו דבר.
סוגי גליקוזילציה
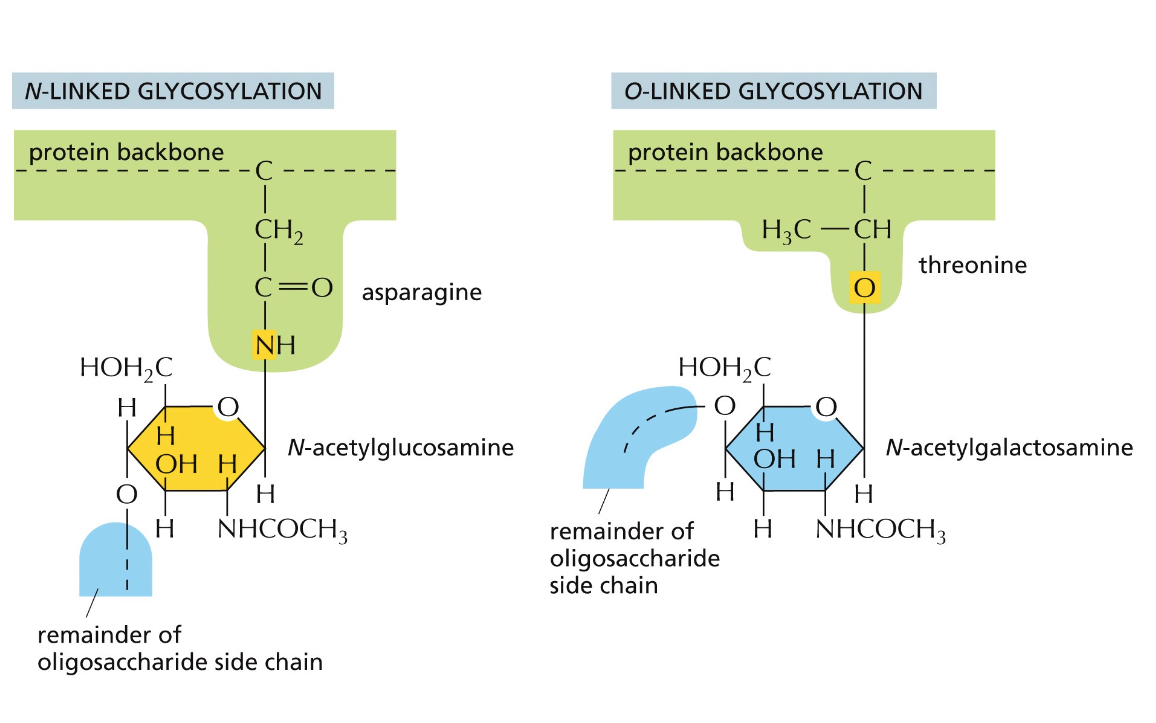
יש שני סוגים עיקריים:
- N-linked glycosylation: קישור דרך אטום חנקן
- O-linked glycosylation: קישור דרך אטום חמצן
תפקידי הסוכרים - דוגמת קבוצות הדם
הדוגמה הקלאסית היא קבוצות דם A, B ו־O. מה שאנחנו קוראים A ו־B זה פשוט עצי סוכרים ספציפיים על חלבונים ממברנליים. הגוף מזהה את הסוכרים האלה ויודע אם התא “שייך לי” או “הגיע מבחוץ ואני צריך להרוג אותו”. O הוא החוסר של A ו־B, לכן הוא תורם אוניברסלי - אין לו סוכרים שיגרמו לתגובה חיסונית. מצד שני, הוא לא יכול לקבל מאף אחד כי אם הגוף מזהה A או B, הוא תוקף.
תפקידים נוספים של הסוכרים: הם שומרים על החלבון מפני פרוטאזות (חלבונים שמפרקים חלבונים), משפיעים על המטען החשמלי, משפיעים על המבנה התלת־ממדי, ומגדילים משמעותית את נפח החלבון. נדיר מאוד למצוא חלבון במסלול ההפרשה שלא עובר גליקוזילציה.
ריר - דוגמה מרתקת לחשיבות הגליקוזילציה
יש הבדל בין עור למעי: העור שלנו “חסר תועלת” מבחינה פונקציונלית - לא נושמים או סופגים נוטריאנטים דרכו. השכבה החיצונית מורכבת מתאים מתים, מה שמספק הגנה. במעי זה לא אפשרי - התאים חייבים להיות חיים כדי לספוג מזון, מים וחמצן.
אז מה מונע מחיידקים להיכנס לתאים? מה מונע מהתאים להתייבש? התשובה היא ריר. איך אנחנו יודעים שריר זה פטנט מוצלח? כי כל אורגניזם בטבע שיש לו תאים חיים שפוגשים את העולם החיצוני מכוסה בריר - מקרפדות דרך אלמוגים ועד אלינו.
המרצה הראה תמונות מהמעבדה שלו - הריר יוצר הפרדה בין תאי האפיתל לחיידקים. המנגנון פשוט: החלבון עצמו כמעט חסר משמעות, הוא רק מאפשר לסוכרים להיבנות עליו. כשהחלבון מופרש מהתא, המים נספגים לסוכרים ונוצרת שכבת ג׳ל - “כמו ג׳לו או פודינג”.
הקשר למיקרוביום ומחלות
הגוף יכול לבחור את המיקרוביום שלו על ידי שינוי הסוכרים על הריר. חיידקים פתוגנים כמו סלמונלה, ליסטריה ושיגלה לא יודעים לאכול את הסוכרים שלנו, ולכן הם מתקשים להתחרות עם המיקרוביום הטבעי. קלוסטרידיום דיפיצילה, שגורם לזיהומים אגרסיביים בבתי חולים, גם לא יודע לאכול ריר - הטיפול היחיד שעובד נגדו הוא השתלת צואה.
בהקשר של כיבים ומחלות מעי דלקתיות, אפשר להסביר על הליקובקטר פילורי (וסיפר על החוקר ששתה את החיידק וקיבל פרס נובל), ועל הקשר החזק בין סטרס למחלות כמו קוליטיס כיבית. המערכת העצבית הגדולה ביותר מחוץ למוח נמצאת במעי, והיא אוטונומית - יכולה לתפקד גם ללא חיבור למוח.
במחקר מרשים של אסיה רולס מהטכניון, היא הראתה שאפשר לגרום לדלקת במעי על ידי גירוי אזור במוח.
סיכום
מסלול ההפרשה מהווה מערכת מורכבת ומתוחכמת המשלבת זיהוי ספציפי (חלבוני Rab), כוח מכני (חלבוני SNARE), בקרת איכות (שפרונים) ומערכת החזרה (KDEL). הגולג׳י ממלא תפקיד מרכזי כתחנת מיון וכמקום שבו מתרחשת גליקוזילציה - תהליך קריטי המשפיע על כל היבט בתפקוד החלבונים, מזיהוי עצמי/זר ועד יצירת ריר המגן עלינו.
דור פסקל