חזקים בשעתוק?
נסו 10 שאלות בנושא, עם עדיפות לשאלות שלא הצלחתם. בסיום תקבלו ציון וסקירה על הטעויות שלכם. הצלחתם? גלו בחנים בדפים נוספים
תוצאות המבחן
היסטוריית מבחנים
טוען את השאלות...
אנא המתן...
מבוא: הקשר בין מבנה לתפקוד
אנחנו ממשיכים להסתכל על התפקוד של התא דרך הבנה של המבנה. מבנה קובע תפקוד, ותפקוד יכול להשפיע על מבנה - זהו עיקרון מרכזי בביולוגיה של התא.
בשיעורים הקודמים התמקדנו בגרעין - אחד האברונים הגדולים והבולטים ביותר בתא. הגרעין הוא ה”בית” של הגנום, והתפקיד הראשוני והחשוב ביותר של מעטפת הגרעין וכל הקומפוננטים שבתוכו הוא לשמור על הגנום שלנו. שינויים בגנום יכולים לגרום למחלות, ולכן ההגנה עליו קריטית.
ארגון הגרעין והכרומטין
בגרעין באינטרפייז (מצב של אי־חלוקה) ניתן להבדיל מספר מרכיבים חשובים:
מעטפת הגרעין משמשת כ”כיפת ברזל” או “כיפת דוד” - שכבת הגנה נוספת מפני נזקים כמו ROS (Reactive Oxygen Species) שיכולים להיווצר במיטוכונדריה ולפגוע בגנום. אך למעטפת יש תפקיד נוסף: היא קובעת את המיקום של ההטרוכרומטין (כרומטין דחוס) וכך משפיעה על הנגישות לגנום. המיקום והפטרן של ההטרוכרומטין שונים בין תאים שונים, מה שקובע אילו גנים יהיו נגישים לביטוי.
הבחנה בין מצבי התא: באינטרפייז הכרומטין מפוזר, אך בחלוקה הכרומוזומים דחוסים מאוד ונקראים כרומטידים. במצב דחוס זה אפשר לראותם במיקרוסקופ ואפילו למיין אותם לפי צורתם. בשיטות ציטוגנטיות מתקדמות, כל כרומוזום נצבע בצבע ייחודי, מה שמאפשר לזהות טרנסלוקציות ושבירות כרומוזומליות.
הגנום האנושי: מספרים ופרדוקסים
הגנום האנושי מכיל כ־6 מיליארד זוגות בסיסים (בתא דיפלואידי), אך רק כ־1.5% מהגנום מקודד לחלבונים - כ־21,000 גנים בלבד. זהו פרדוקס מרתק: איך אנחנו מסתדרים עם מספר גנים הדומה לזה של תולעים קטנות או זבובי דרוזופילה? התשובה טמונה במנגנונים מתוחכמים של ויסות ועיבוד שנלמד עליהם.
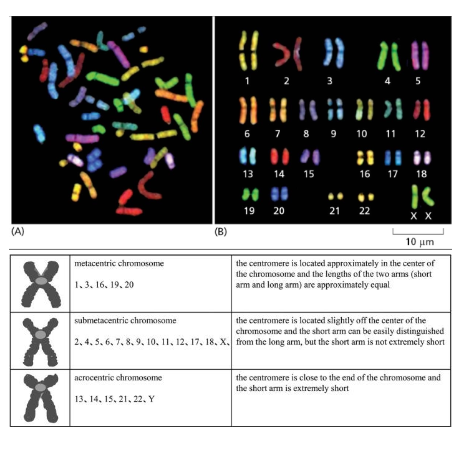
כרומוזומי המין והמחלות הקשורות
מתוך 46 הכרומוזומים האנושיים, 44 הם אוטוזומים (כרומוזומים רגילים) ו־2 הם כרומוזומי מין:
- בנות: XX
- בנים: XY
הגן SRY (Sex-determining Region Y) בכרומוזום Y קובע התפתחות של שכים במקום שחלות, ובכך קובע את מין העובר.
ההבדל במספר הגנים:
- כרומוזום X: כמעט 900 גנים מקודדי חלבון
- כרומוזום Y: רק 64 גנים
הגן דיסטרופין - חשיבות קלינית
דיסטרופין הוא אחד הגנים הגדולים ביותר בגנום האנושי, ממוקם על כרומוזום X. “תזכרו את הגן הזה, נחזור אליו בהמשך.” הגן מקודד לחלבון הנקשר לציטוסקלטון של תאי השריר ומגן עליהם מפני נזקי ROS שנוצרים במהלך פעילות גופנית אינטנסיבית.
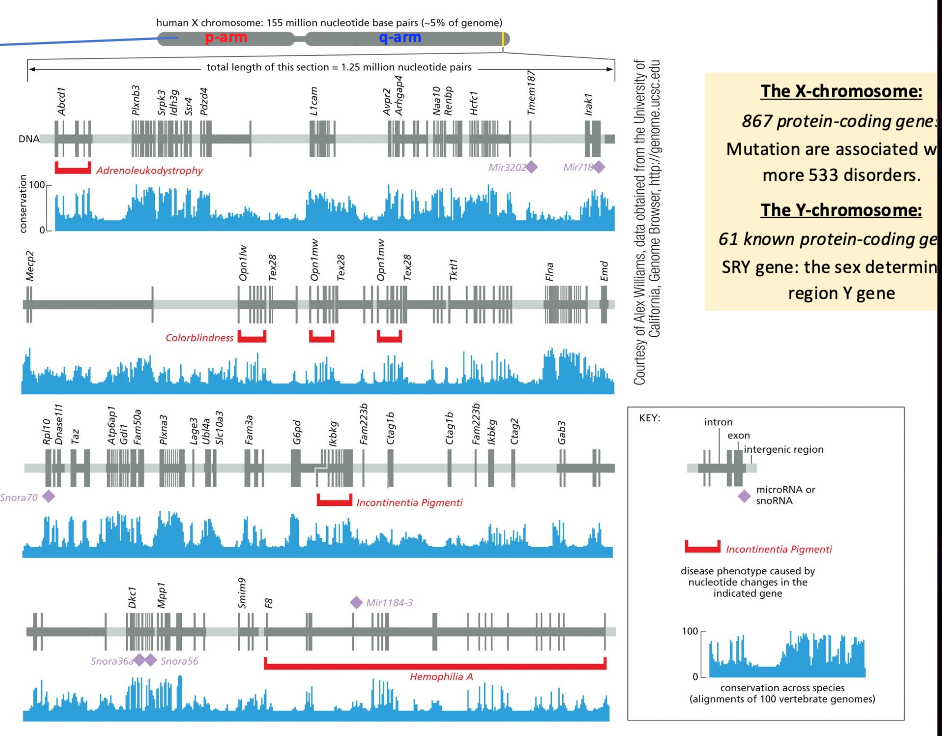
מוטציות בגן גורמות למחלות קשות (מסומנים בתמונה באדום):
- Duchenne Muscular Dystrophy
- Becker Muscular Dystrophy
בהיעדר החלבון התקין, סיבי השריר מתפרקים, והחולים סובלים מחולשת שרירים פרוגרסיבית - “לא יכולים לנשום, לא יכולים להתפתח”. המחלות שכיחות יותר בבנים מכיוון שיש להם עותק יחיד של כרומוזום X, בעוד שלבנות יש שני עותקים והסיכוי למוטציה בשני האללים קטן מאוד.
Dystrophin:
- around 3000 kB DNA
- 79 exons (0.6% DNA sequence)
- 14 kB mRNA
- 427 kDa protein
- Protects muscle fibers from breaking down when exposed to stress/enzymes.
- Localizes in skeletal muscle to the cytoplasmic surface of the sarcolemma (muscle fiber membrane) to provide a link between cytoskeletal actin and extracellular matrix.
- Mutations lead in boys to X-linked recessive (congenital) muscular dystrophy (e.g. Duchene muscular dystrophy or Becker muscular dystrophy).
נושא השיעור - יצירת חלבונים
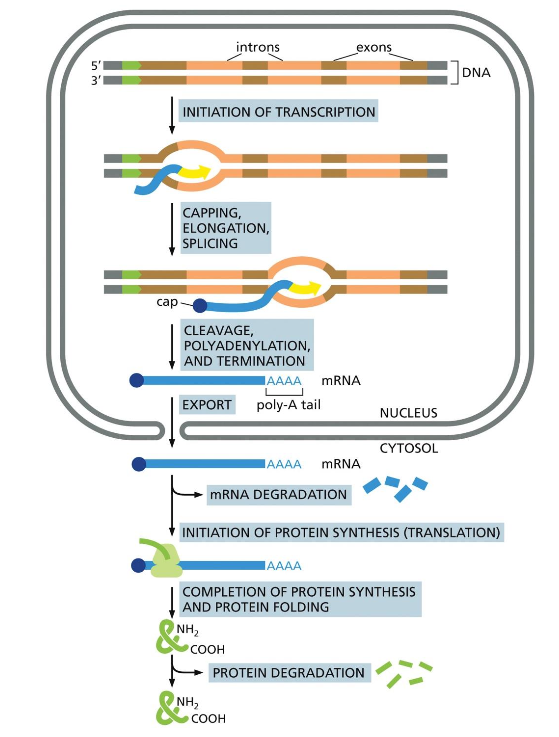
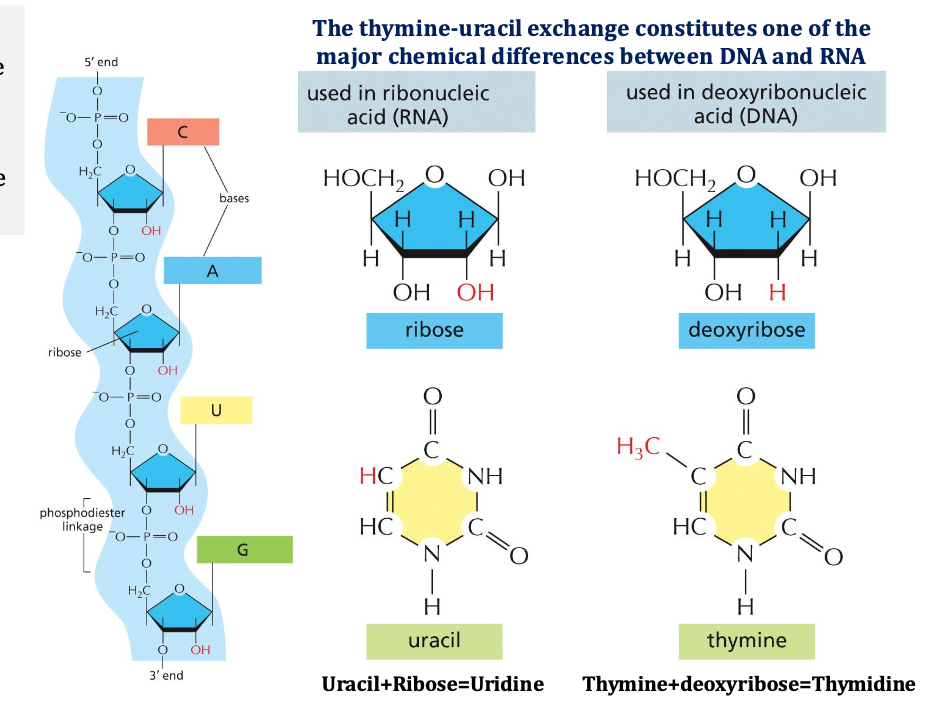
המולקולות הבסיסיות: DNA ו־RNA
מבנה ה־DNA
DNA הוא פולימר של נוקלאוטידים. כל נוקלאוטיד בנוי מ:
- בסיס חנקני: אדנין (A), גואנין (G), תימין (T), ציטוזין (C)
- סוכר: דאוקסיריבוז
- קבוצת פוספט
הבחנה חשובה במינוח:
- בסיס בלבד: אדנין, גואנין, תימין, ציטוזין
- נוקלאוזיד (בסיס + סוכר): אדנוזין, גואנוזין, תימידין, ציטידין
- נוקלאוטיד (בסיס + סוכר + פוספט): היחידה המלאה
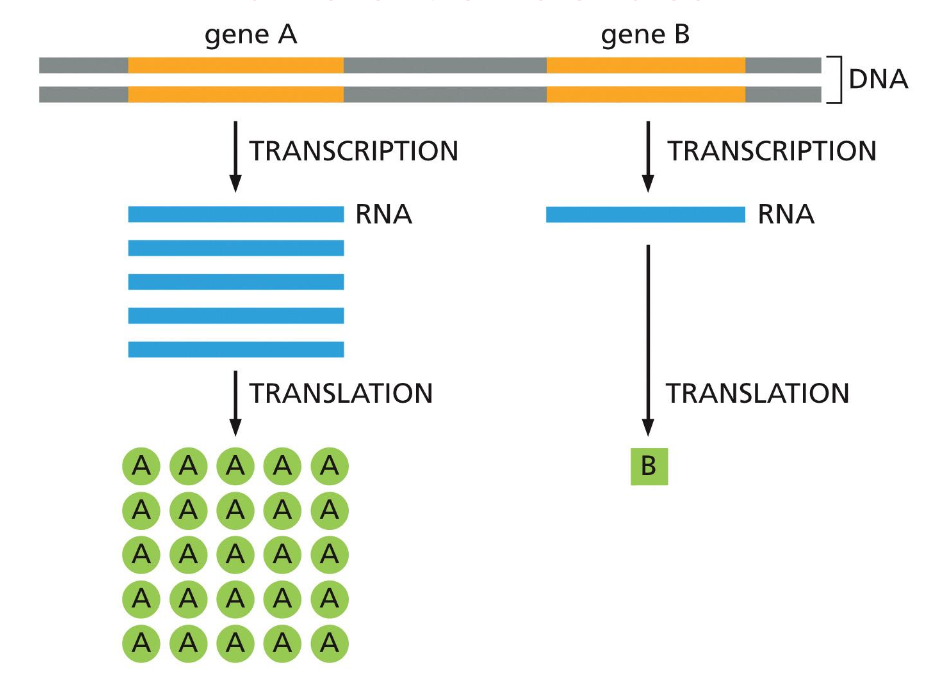
ביטוי של גנים
ההבדלים בין DNA ל־RNA
- מבנה: DNA דו־גדילי, RNA חד־גדילי (עם חריגים חשובים!)
- הבסיסים: במקום תימין ב־DNA, יש אורציל (U) ב־RNA
- הסוכר: ריבוז ב־RNA במקום דאוקסיריבוז ב־DNA - “יש כאן הידרוקסיל אחד נוסף”
ההבדלים הללו מאפשרים מגוון גנומי במהלך האבולוציה, אך גם יוצרים סכנות פוטנציאליות.
Uracil can also be found in DNA (!!)
- spontaneous (hydrolytic) deamination of cytosine; It is estimated that between 100 and 500 uracil residues per day, per cell, may be introduced into DNA as a result of this process.
- AID (activation-induced cytosine deaminase)- mediated DNA mutations.
- Uracil in DNA is also produced by the incorporation of dUMP during DNA replication.
נזקים ל־DNA - מוטציות
דאמינציה - המקור העיקרי למוטציות
דאמינציה היא איבוד קבוצת אמין מהבסיסים החנקניים. התהליך יכול להתרחש:
- ספונטנית - קורה באופן טבעי
- מוגברת על ידי חומרים טוקסיים - פורמלדהיד, בנזופירן, זיהום סביבתי
הסוגים העיקריים:
-
ציטוזין ← אורציל: השינוי הנפוץ ביותר. אורציל מזדווג עם אדנין במקום גואנין, וכך נוצרת מוטציה C:G ← T:A
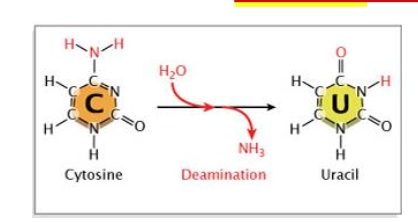
דה־אמינציה של ציטוזין בתא מובילה להיווצרות אורציל, שהוא בסיס דומה מאוד לתימין, אך מופיע ברנ”א ולא בדנ”א. אם שינוי זה לא מתוקן, בעת השכפול הבא האנזימים מתייחסים לאורציל כאל תימין, והוא מזדווג עם אדנין במקום גואנין. לכן, במקום זוג בסיסים תקין C:G, מתקבל זוג מוטנטי U:A, שמתורגם בסופו של דבר לזוג T:A — כלומר מוטציית החלפת בסיס מסוג טרנזישן (transition).
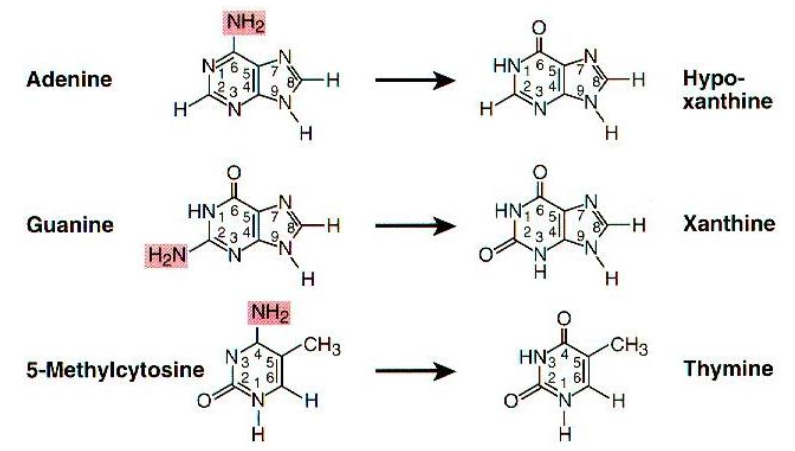
- אדנין ← היפוקסנטין: היפוקסנטין מזדווג עם ציטוזין, יוצר מוטציה A:T ← G:C
- גואנין ← קסנטין: משנה את דפוס הזיווג
- 5-מתילציטוזין ← תימין: מוטציה בעייתית במיוחד
התדירות מדהימה: בכל אחד מ־37 טריליון התאים בגופנו מתרחשים 500-100 אירועי דאמינציה מדי יום!
מנגנוני ההגנה - “איך אנחנו לא מוטנטים שנראים כמו איירון מן?”
התא מצויד במערכת תיקון מתוחכמת:
DNA גליקוזילאזות - אנזימים המזהים בסיסים פגומים ומחליפים אותם. “זה כמו החלפת חלקי חילוף במכונית… הוא מחליף לך את החלק החשוב מאוד.”
המנגנון העיקרי נקרא BER (Base Excision Repair) - חיתוך הבסיס הפגום והחלפתו בבסיס תקין.
DNA glycosylases play a key role in the elimination of such DNA lesions (BER): they recognize and excise damaged bases, thereby initiating a repair process that restores the regular DNA structure with high accuracy (e.g., uracil-DNA glycosylase). If not -> C:G in parental DNA can be changed into a T:A pair in the daughter DNA molecule.
Nonsense-mediated decay - מנגנון נוסף המזהה mRNA עם קודוני עצירה מוקדמים ומפרק אותם.
חשיפה לזיהום סביבתי מגבירה את קצב המוטציות, וזו הסיבה לקשר בין זיהום לסרטן - “מחלה שקשורה להצטברות מוטציות.”
“בביולוגיה הרבה מאוד BUT”
למרות ש־RNA מוגדר כחד־גדילי, במציאות נמצאות מולקולות RNA כפולות-גדיל במצבים רבים:
- זיהום ויראלי
- ביטוי של רטרו־אלמנטים (טרנספוזונים)
- שחרור DNA מיטוכונדריאלי לציטופלזמה בעקבות נזק
- מבנים משניים של RNA עצמו דרך זיווג תוך־מולקולרי
מולקולות אלה חשובות לזיהוי על ידי מערכת החיסון.
בסיסים לא קונבנציונליים
משפחת מולקולות ה־RNA
RNA מקודד לחלבון
mRNA (messenger RNA) - מהווה רק 1.5% מכלל ה־RNA המשועתק, אך חיוני לתרגום חלבונים.
RNA לא־מקודד (80% מה־RNA)
- rRNA (ribosomal RNA) - “בונים את התת־יחידות של ריבוזום… לא עוברים תרגום אבל משתתפים בתרגום”
- tRNA (transfer RNA) - “מביאים חומצות אמינו” - מולקולות קטנות הנושאות חומצות אמינו לריבוזום
- snRNA (small nuclear RNA) - עוזרים בשעתוק ועריכה של mRNA
- snoRNA (small nucleolar RNA) - מעורבים בעיבוד rRNA
- lncRNA (long non-coding RNA) - כולל כאלה המשועתקים מטרנספוזונים
- miRNA ו־siRNA - יכולים לגרום לחיתוך ודגרדציה של mRNA, משתתפים בוויסות ביטוי גנים
הנקודה החשובה: “רוב ה־RNAs לא עוברים תרגום, לא מקודדים לחלבון, אבל יש להם תפקיד חשוב!”
מנגנון השעתוק
RNA פולימראז - המכונה המולקולרית
RNA פולימראז הוא “קומפלקס מאוד גדול של לפחות 10 חלבונים ביחד”, לא אנזים בודד.
שלושה סוגים באיקריוטים:
- RNA Pol I - משעתק גנים של rRNA (למעט 5S rRNA)
- RNA Pol II - משעתק את כל הגנים של מסוג mRNA, רוב ה־snRNA, miRNA ו־lncRNA
- RNA Pol III - משעתק גנים של tRNA ו־5S rRNA
| סוג ה־RNA | תפקיד |
|---|---|
| mRNA | מעביר מידע גנטי מה־DNA לריבוזום |
| rRNA | מרכיב את הריבוזום |
| tRNA | מביא חומצות אמינו לריבוזום |
| snRNA | משתתף בשעתוק ועריכה של mRNA |
| snoRNA | מעורב בעיבוד rRNA |
| lncRNA | כולל RNA ארוך שאינו מקודד, מעורב בוויסות גנים |
| RNA Pol I | RNA Pol II | RNA Pol III |
|---|---|---|
| משעתק rRNA (למעט 5S) | משעתק mRNA, snRNA, miRNA, lncRNA | משעתק tRNA, 5S rRNA |
כיצד מתבצע השעתוק?
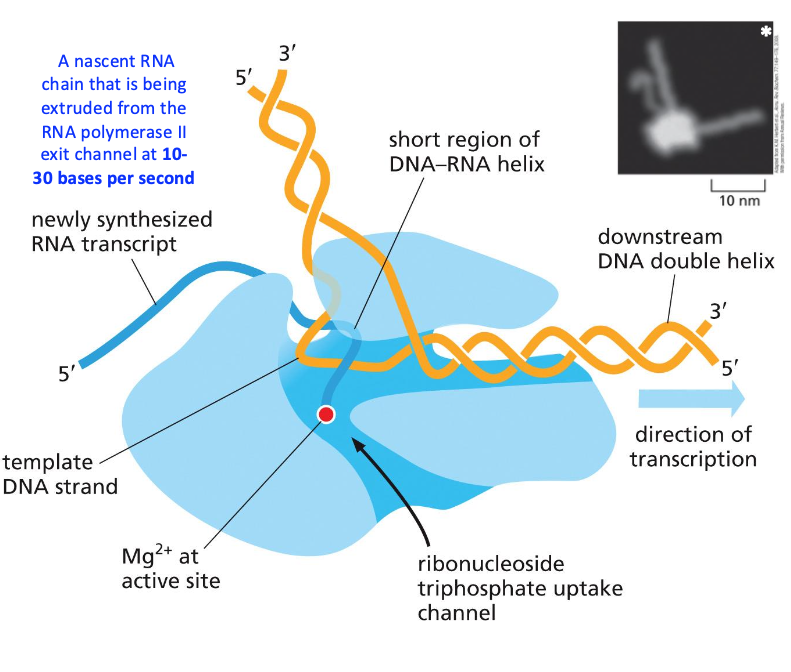
שאלת מפתח: “מאיזה צד בדיוק מגיעה הסינתזה?” התשובה: “אתה לא יכול לגשת לנוקלאוטידים מבחוץ, יש שם סוכר… כדי ש־RNA יסונתז, ה־DNA צריך להיפתח.”
שלבי השעתוק - מ־DNA ל־RNA
- אנזים הליקאז פותח את סליל הדנ”א הדו־גדילי באזור הפרומוטור (לא תמיד, לעיתים RNA פולימראז עושה זאת בעצמו בפרוקריוטים).
- RNA פולימראז נקשר לפרומוטור (באמצעות פקטורי תעתוק באיקריוטים), ופותח את הסליל במידה הדרושה.
- הוא מתחיל את סינתזת ה־RNA על־פי תבנית הדנ”א (הגדיל הלא־מקודד).
- קצב הסינתזה: כ־10–30 נוקלאוטידים בשנייה באיקריוטים, מהיר יותר בפרוקריוטים.
- כיוון הסינתזה: תמיד 5’ ל־3’, כי נוקלאוטידים חדשים מתחברים לקצה ה־3’ של השרשרת המתארכת. (הכיוון של השעתוק ביחס לגן משתנה, אך כיוון הסינתזה תמיד זהה).
- “RNA תמיד גדל מהקצה 5’ לקצה 3’“
- “תמיד יש אנטי-פרלליות בין התבנית לגדיל החדש”
לגן של 1000 נוקלאוטידים יידרשו כ־4-3 דקות לשעתוק מלא.
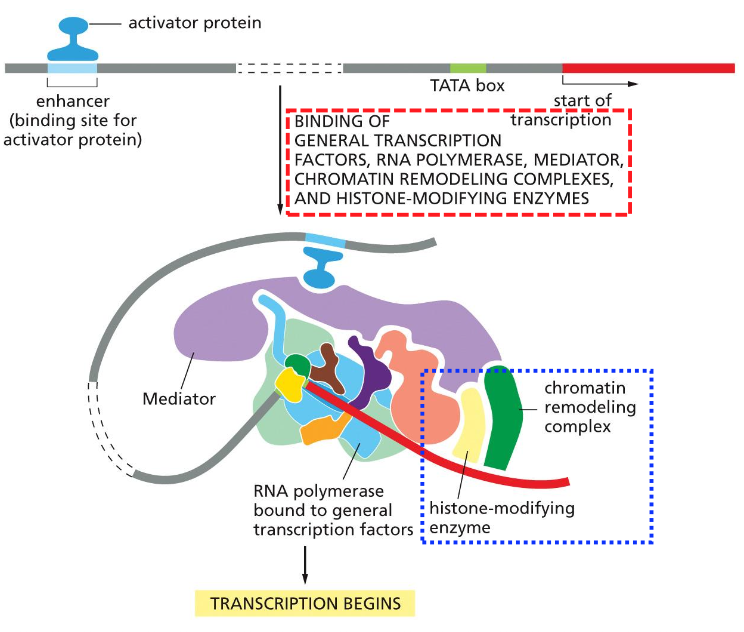
בקרת השעתוק - מערכת מורכבת
RNA פולימראז זקוק לTranscription Factors שמביאים אותו למקום הנכון ובזמן הנכון.
המערכת כוללת:
- Enhancers - אלמנטים רגולטוריים המגייסים mediators
- Mediators - מתווכים בין enhancers ל־RNA פולימראז
- Chromatin remodeling complexes - מסירים או מזיזים נוקלאוזומים כדי לחשוף את ה־DNA
- Promoter - “ממש בתחילת הגן, לפני הסטארט קודון של השעתוק” - המקום שבו RNA פולימראז מתיישב
הארגון התלת־ממדי של הכרומטין מאפשר לאנהנסרים רחוקים להשפיע על גנים דרך יצירת לולאות DNA.
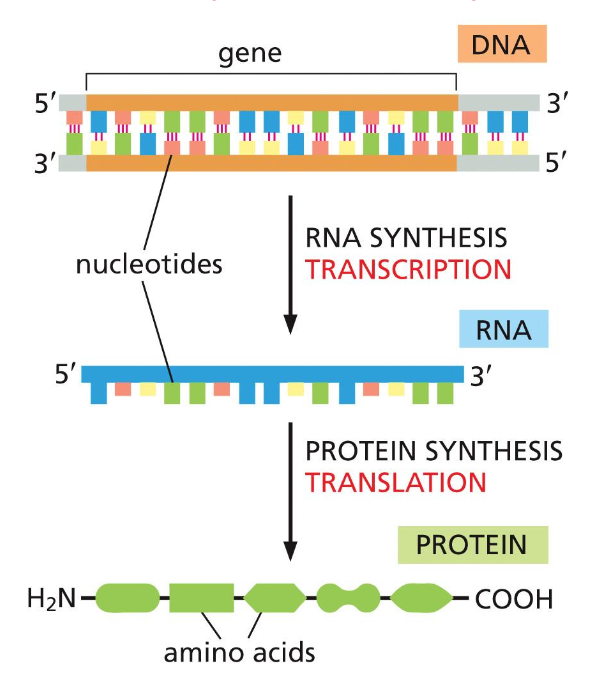
עיבוד RNA - תהליכים מקבילים לשעתוק
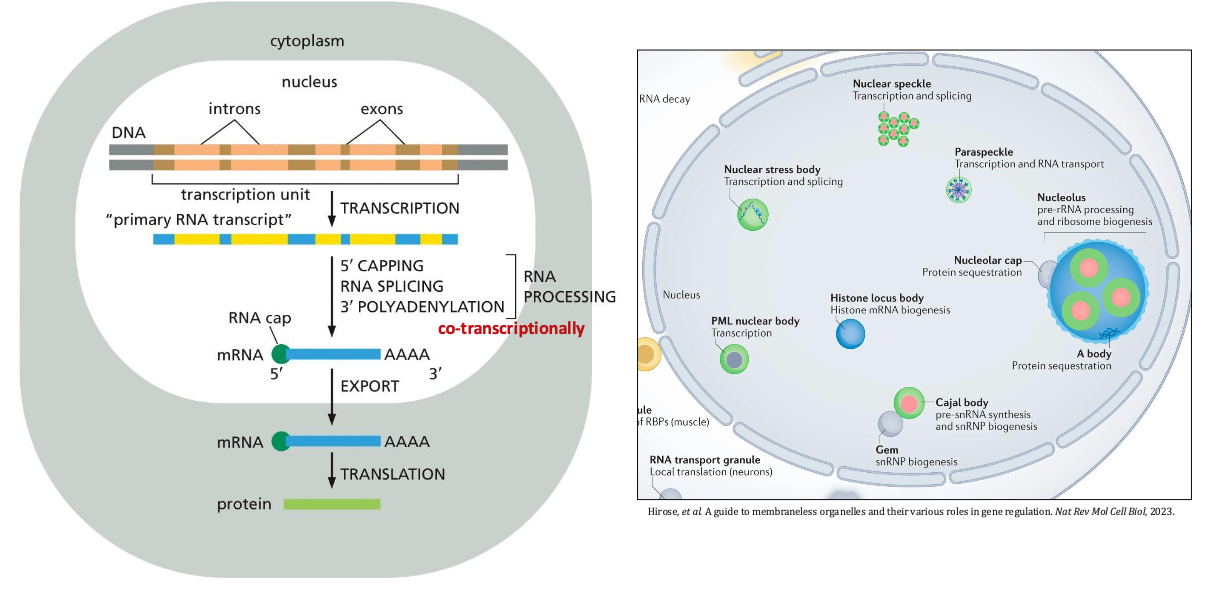
בתאים אוקריוטיים, כל mRNA חייב לעבור שלושה תהליכי עיבוד עיקריים. תהליכים אלה מתרחשים “co-transcriptionally” - במקביל לשעתוק.
מבנה הגן האיקריוטי
גנים אוקריוטיים מורכבים מ:
- אקזונים - אזורים המקודדים לחלבון
- אינטרונים - אזורים מפרידים שאינם מקודדים (Introns)
כל ה־DNA משועתק, כולל האינטרונים, אך רק האקזונים יופיעו ב־mRNA הבוגר.
Capping - הוספת “כובע” מגן
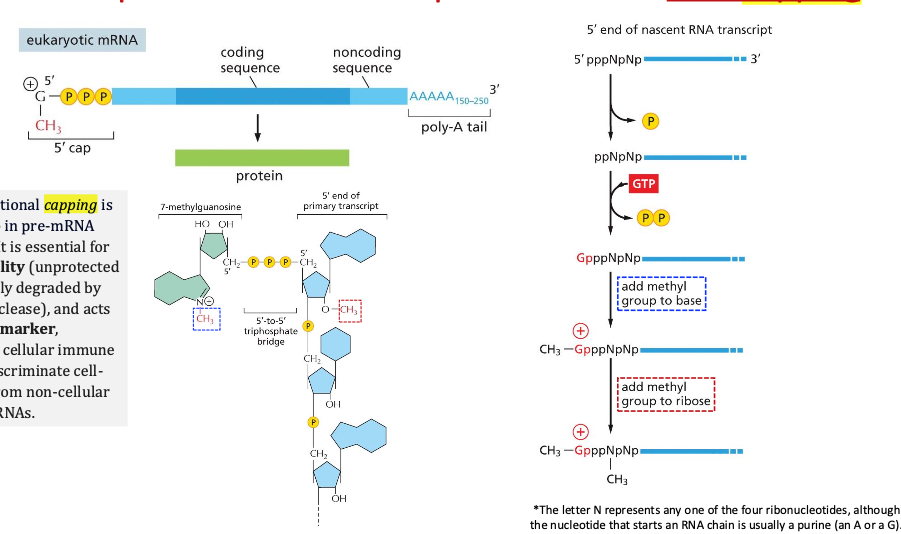
“קייפינג זה תהליך של הצמדה לנוקלאוטיד הראשון… מתיל גואנזין.”
מה כולל התהליך:
- הוספת 7-methylguanosine דרך קשר טריפוספטי ייחודי (5’-5’)
- מתילציה של הסוכר בנוקלאוטיד הראשון (ולעתים השני)
תפקידי ה־Cap:
- מאפשר לריבוזום לזהות את ה־mRNA
- הגנה מפני פירוק אנזימטי
- סימון למערכת החיסון - “self vs non-self”
- ייצוב המבנה התלת־ממדי
- חיוני ליצוא מהגרעין לציטופלזמה
- מאפשר לחלבונים לזהות “הנה mRNA שאני צריך לקחת החוצה”
Splicing - חיבור האקזונים
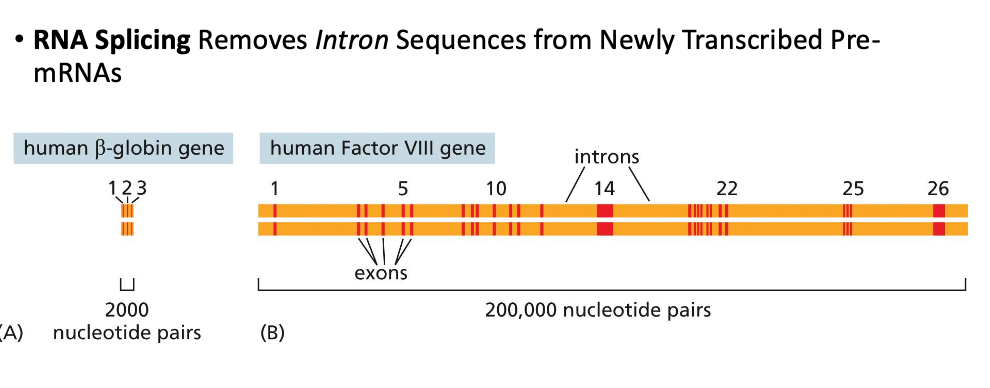
התהליך: “להוציא אינטרונים ולחבר בין אקזונים.”
דוגמאות למורכבות:
- גן β-globin: 3 אקזונים בלבד
- גן Factor VIII: 26 אקזונים
מה קורה לאינטרונים? “הם מפורקים לנוקלאוטידים… חוזרים למאגר.” זה חשוב כי לתהליכי שעתוק, תיקון ושכפול נדרש מאגר זמין של נוקלאוטידים.
טעויות בשחבור גורמות למחלות רבות, במיוחד נוירודגנרטיביות, כאשר אינטרונים נשארים בטעות או אקזונים מדולגים, ונוצר “חלבון מוטנטי”.
![מאת Courtesy: National Human Genome Research Institute - [1] (file), נחלת הכלל, https://commons.wikimedia.org/w/index.php?curid=212144](/biology/image-230.png)
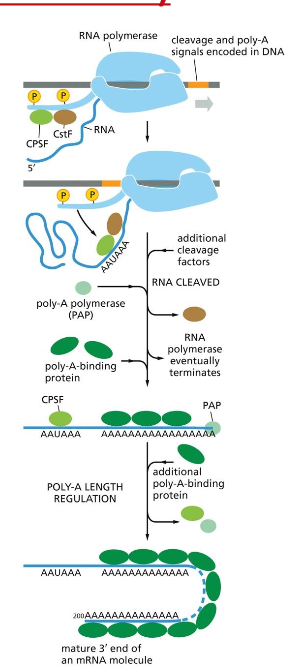
Polyadenylation - הוספת “זנב” מגן
הוספת כ־250-200 אדנינים בקצה 3’ של ה־mRNA.
תפקידים:
- הגנה מפני פירוק מהקצה
- סיגנל חיוני לאקספורט מהגרעין
- השפעה על יציבות ה־mRNA
- מאפשר תרגום יעיל
אזורי UTR
ב־mRNA הבוגר יש אזורים שאינם מתורגמים:
- 5’ UTR - האזור שלפני קודון ההתחלה (AUG)
- 3’ UTR - האזור שאחרי קודון העצירה
- רצף קוזאק - רצף מיוחד המסמן לריבוזום איפה להתחיל תרגום
הריבוזום מתרגם רק את האזור בין קודון ההתחלה לקודון העצירה, אך אזורי ה־UTR חיוניים לוויסות ויציבות.
הבדלים אבולוציוניים
פרוקריוטים (חיידקים)
- ללא capping
- ללא splicing (הגנים רציפים)
- ללא polyadenylation
- שעתוק ותרגום מתרחשים בו־זמנית
מיטוכונדריה
“כמעט אין שם capping, אין splicing, אבל יש polyadenylation.”
הדמיון לפרוקריוטים תומך בתיאוריה האנדוסימביוטית למקור המיטוכונדריה.
אברונים גרעיניים ותפקידם
Nuclear bodies הם “condensates של מולקולות שיכולות לזוז ממקום למקום, להתחבר או לעשות dissociation.” הם מכילים ריכוזים גבוהים של חלבונים ו־RNA המעורבים בתהליכי העיבוד, במיוחד small nuclear RNA שעוזרים בשחבור ועיבוד.
חשיבות קריטית של התהליכים
“זה הבסיס. אם תפספסו את זה, יהיה לכם נורא נורא קשה.”
כל mRNA שנוצר בתאים אוקריוטיים חייב לעבור RNA processing מלא. בלי התהליכים האלה - capping, splicing ו־polyadenylation - ה”mRNA ייצא פגום, mRNA פגום לא יתורגם לחלבון, בדרך כלל הוא עובר decay או פירוק.”
המורכבות של מערכת השעתוק והעיבוד היא שמאפשרת לגנום האנושי הקטן יחסית (21,000 גנים) ליצור את המגוון העצום של חלבונים ותפקודים הנדרשים לחיים מורכבים.