תוכן עניינים:
- חלק א’: גנטיקה התפתחותית
- חלק ב’: ריצוף הגנום האנושי
- חלק ג’: טרנספוזונים (Transposable Elements)
- חלק ד’: שיטות מחקר גנטי
- סיכום לבחינה
- לקסיקון מונחים
- שאלות תרגול מג׳ונרטות
- שאלות תרגול מג׳ונרטות: ריצוף DNA וגנומים
חלק א’: גנטיקה התפתחותית
מהי גנטיקה התפתחותית?
גנטיקה התפתחותית היא תחום העוסק באופן שבו גנים משפיעים על תהליכי ההתפתחות העוברית - מתא ביצית מופרה ועד לאורגניזם שלם. המוקד העיקרי הוא בשלבים העובריים המוקדמים, שבהם מתרחשים התהליכים הקריטיים ביותר.
נקודת המוצא: תא ביצית מופרה (זיגוטה) מכיל מידע גנטי משני מקורות - תא ביצית ותא זרע. שני אלה הם תאים הפלואידיים (עותק אחד של הגנום), הידועים גם בשמות:
- גמטות
- תאי מין
- תאי נבט (Germ cells)
כל שאר התאים בגופנו הם תאים סומטיים - תאים דיפלואידיים רגילים.
שלושת התהליכים המרכזיים בהתפתחות עוברית
במהלך ההתפתחות העוברית מתרחשים במקביל שלושה תהליכים קריטיים:
1. חלוקה מוגברת
החלוקה התאית המהירה ביותר בחיינו מתרחשת בשלבים העובריים. התאים מתחלקים בקצב גבוה מאוד כדי להגיע ממספר קטן של תאים למיליארדי תאים בזמן קצר.
דרישות לחלוקה מוגברת:
- אספקת אנרגיה מספקת
- פקטורי גדילה (פנימיים וחיצוניים)
- מעבר מהיר דרך נקודות הבקרה (Checkpoints)
הערה: לאחר ההפריה, כל החלוקות הן מיטוטיות - התא כבר דיפלואידי.
2. התמיינות (Differentiation)
תהליך שבו תאים מקבלים תפקידים ספציפיים - תא אחד הופך לתא לב, אחר לתא עצב, אחר לתא עצם.
מנגנונים המווסתים התמיינות:
- פקטורי שעתוק - רפרסורים שמשתיקים גנים שאינם נדרשים
- אפיגנטיקה - מתילציה על בסיסי C באזורי פרומוטור גורמת להשתקת גנים
- RNAi - מולקולות RNA קצרות שמעכבות mRNA של גנים ספציפיים
מושגי מפתח בפוטנציאל התמיינות:
| מצב | משמעות |
|---|---|
| Totipotent | יכול להתחלק לכל סוגי התאים (תא ביצית מופרה) |
| Pluripotent | יכול להתחלק לרוב סוגי התאים |
| Multipotent | יכול להתחלק למספר סוגי תאים מוגבל |
| Tissue-specific | יכול להתחלק רק לתאים מאותה רקמה |
ככל שתהליך ההתמיינות מתקדם, הפוטנציאל הולך וקטן - יותר גנים מושתקים, פחות אפשרויות נותרות.
3. מורפוגנזה (Morphogenesis)
תהליך יצירת צורת הגוף - לא רק שיהיו תאים מסוגים שונים, אלא שהם יתמקמו במקומות הנכונים ויצרו איברים מאורגנים.
למה צריך צירים? בדיוק כמו שצייר משתמש בקווי עזר, כך התאים צריכים “מערכת קואורדינטות” כדי לדעת:
- מה קדמי ומה אחורי
- מה עליון ומה תחתון
- ימין ושמאל
ללא מורפוגנזה תקינה: גם אם תהליך ההתמיינות מצליח, התאים עלולים להתפזר באופן אקראי - תא לב במקום הראש, תא מוח באזור הבטן.
מורפוגנים ויצירת צירי הגוף
מהם מורפוגנים?
מורפוגנים הם מולקולות סיגנל (בדרך כלל חלבונים) שמופרשות באזורים ספציפיים בעובר ויוצרות גרדיאנט ריכוזים - ריכוז גבוה באזור ההפרשה, וריכוז יורד ככל שמתרחקים.
עקרון הפעולה:
ריכוז גבוה ←――――――――――――――――→ ריכוז נמוך
↓ ↓
ביטוי גן A ביטוי גן C
↓
ביטוי גן B
- תאים שקולטים ריכוז גבוה של מורפוגן ← מבטאים קבוצת גנים מסוימת
- תאים שקולטים ריכוז בינוני ← מבטאים קבוצת גנים אחרת
- תאים שקולטים ריכוז נמוך או אפסי ← מבטאים קבוצת גנים שלישית
חשוב: לכל התאים יש רצפטורים לאותו מורפוגן, אבל רמת הסיגנל שנקלטת קובעת איזה גנים יתבטאו.
דוגמה: Bicoid ו־Caudal בזבוב הפירות
בזבוב הפירות (Drosophila), שני מורפוגנים מרכזיים קובעים את ציר ראש־זנב:
| מורפוגן | מקור ההפרשה | קובע |
|---|---|---|
| Bicoid | צד קדמי (ראש) | התפתחות מבני הראש |
| Caudal | צד אחורי (זנב) | התפתחות מבני הזנב |
סנכרון בין המורפוגנים: חלבון Bicoid מעכב את יצירת חלבון Caudal - כך שבאזור שיש הרבה Bicoid, לא יהיה Caudal, ולהיפך. מנגנון זה מבטיח הפרדה ברורה בין הצירים.
מקור האפקט המטרנלי: mRNA של Bicoid קיים כבר בתא הביצית עוד לפני ההפריה, ממוקם בצד ספציפי - זו נקודת ההתחלה של כל תהליך קביעת הצירים.
גנים הומיאוטיים (Hox Genes) בבני אדם
בבני אדם, גנים הנקראים Hox genes (או גני סגמנטציה) אחראים על קביעת דפוסי הגוף לאורך ציר קדמי-אחורי.
תפקיד: קביעת “גורל” של אזורים שונים בגוף - איזה איברים יתפתחו באיזה אזור.
פגמים בגנים הומיאוטיים: כשיש מוטציה במורפוגנזה, התוצאות הן לרוב לא־לטאליות רק במקרים חלקיים - רוב הפגמים הקשים מובילים להפלה ספונטנית בשליש הראשון של ההריון.
תאי גזע (Stem Cells)
מהם תאי גזע?
תאי גזע הם תאים שעדיין לא סיימו את תהליך ההתמיינות - יש להם פוטנציאל להתחלק ולהתמיין לסוגי תאים שונים.
סוגי תאי גזע
תאי גזע עובריים:
- פוטנציאל התמיינות גבוה (Pluripotent עד Totipotent)
- נמצאים בשלבים מוקדמים של ההתפתחות
תאי גזע בבוגר:
- פוטנציאל מוגבל יותר
- דוגמה מרכזית: תאי גזע במח העצם - יכולים להתחלק לכל סוגי תאי הדם
מה קובע לאן תא גזע יתמיין?
- סיגנלים מהסביבה - מה הרקמה צריכה, מה חסר
- פקטורי גדילה שונים - פקטורים שונים מעודדים התמיינות לכיוונים שונים
חשיבות קלינית של תאי גזע
| יישום | הסבר |
|---|---|
| מחקר | גידול תאים ספציפיים במעבדה לצורך ניסויים |
| טיפול ברקמות פגועות | השתלת תאים לתיקון נזקים |
| מניעת דחיית שתל | תאי גזע ממקור עצמי לא יידחו |
| הנדסה גנטית | תיקון גנטי בתאי גזע ישפיע על כל התאים שיתפתחו מהם |
דם טבורי: מכיל תאי גזע עובריים “צעירים” עם פוטנציאל התמיינות גבוה יותר מתאי גזע בבוגר. כיום נשמר בהקפאה לשימוש עתידי פוטנציאלי.
אפופטוזיס בהתפתחות
גם מוות תאי מתוכנת הוא חלק קריטי מההתפתחות התקינה.
דוגמה קלאסית: האצבעות שלנו נוצרות כ”גוש” אחד, והרווחים ביניהן נוצרים על ידי מוות מתוכנת של התאים באזורים שבין האצבעות.
כשאפופטוזיס לא מתרחש כראוי באזורים הללו, עלולה להיווצר סינדקטיליה (איחוי אצבעות).
חלק ב’: ריצוף הגנום האנושי
רקע - שיטת Sanger לריצוף
שיטת Sanger מבוססת על עקרונות ה־PCR עם תוספת קריטית אחת:
הרכיבים:
- DNA תבנית
- פריימרים ספציפיים
- נוקלאוטידים חופשיים (dNTPs)
- ddNTPs (Dideoxy-nucleotides) - מסומנים פלואורסצנטית
- אנזים Taq polymerase (עמיד בחום)
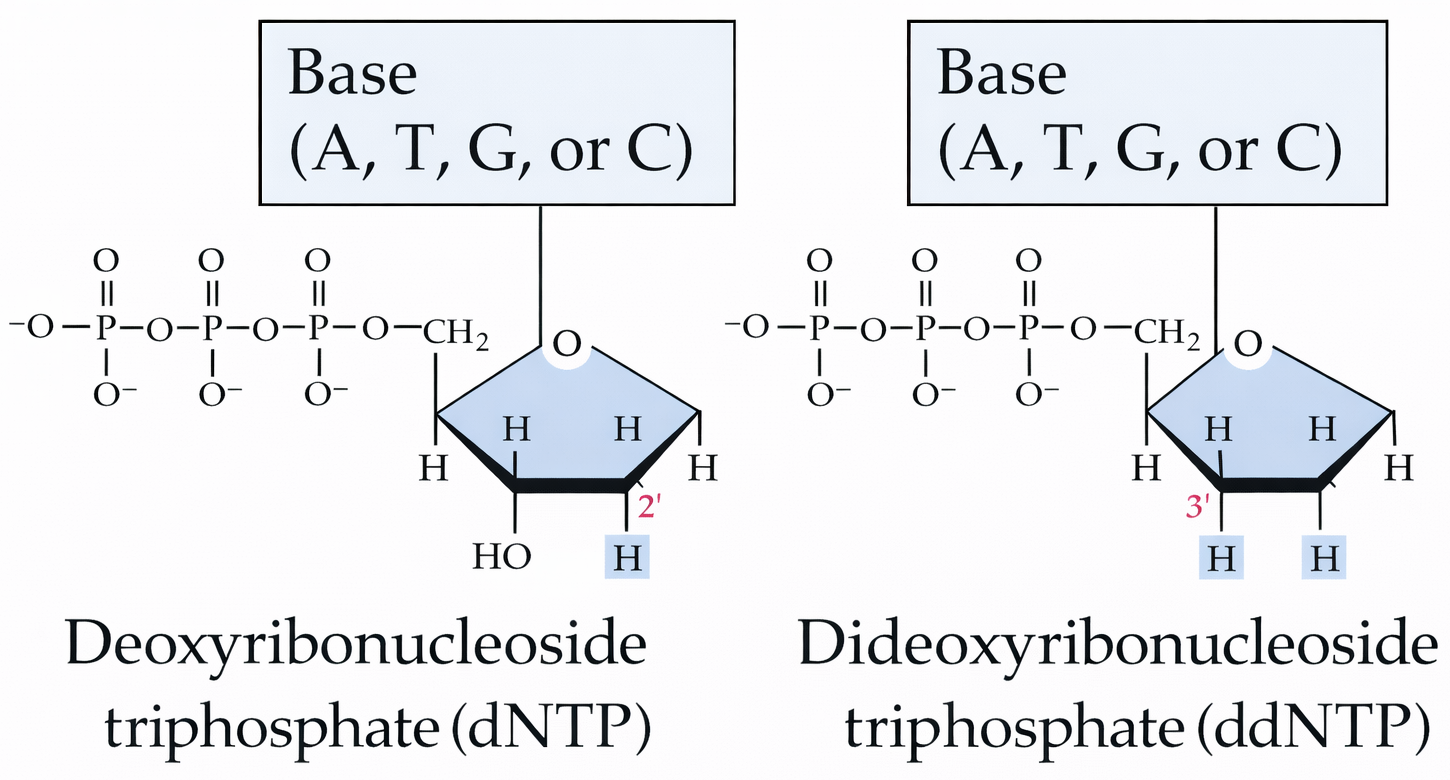
עקרון הפעולה: ה־ddNTPs דומים לנוקלאוטידים רגילים, אבל לא מסוגלים להתארך בקצה 3’ - כשהם מצטרפים לשרשרת, הסינתזה נעצרת.
התוצאה: בהרבה ריאקציות מקבילות, נוצרים מקטעים בכל האורכים האפשריים - מהקצר ביותר ועד הארוך ביותר. כל מקטע מסומן בצבע לפי הנוקלאוטיד האחרון שלו.
מגבלה קריטית: השיטה מדויקת עד כ־1,000 בסיסים בלבד. מעבר לכך, האיכות יורדת משמעותית.
הבעיה: כיצד לרצף 3 מיליארד בסיסים?
הגנום האנושי מכיל כ־3 מיליארד זוגות בסיסים. עם מגבלת Sanger של ~1,000 bp, נדרשים מיליוני מקטעים - בלתי אפשרי בשיטה ישירה.
שיטה 1: הליכה על גבי הכרומוזום (Chromosome Walking)
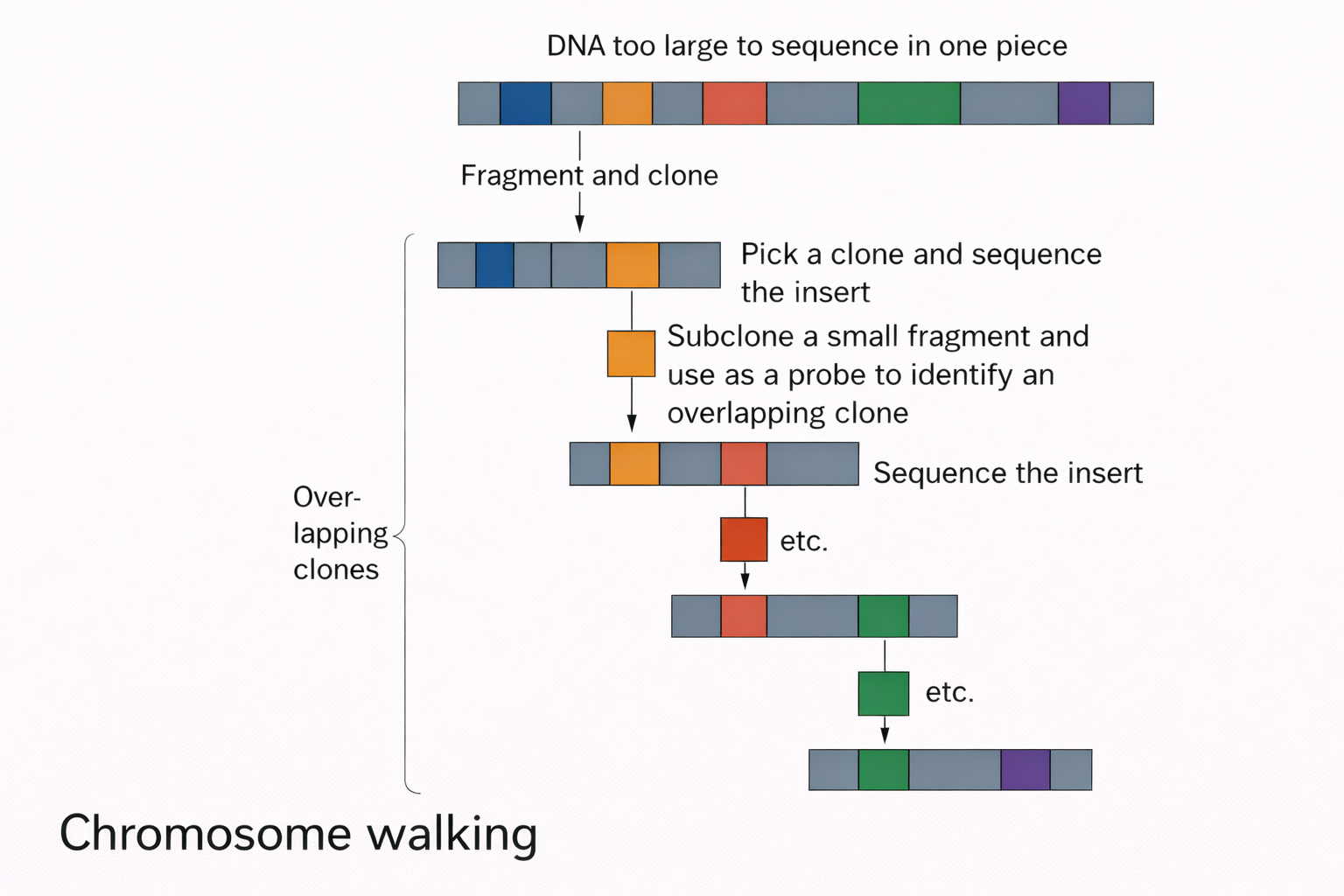
העיקרון
-
יצירת ספריות DNA: שבירת הגנום למקטעים באמצעות אנזימי רסטריקציה או גלי קול (סוניקציה), והכנסתם לווקטורים (פלסמידים או פאג’ים) בתוך חיידקים.
-
זיהוי סמנים: שימוש בסמנים גנטיים - רצפי DNA קצרים וייחודיים שמופיעים פעם אחת בגנום (Sequence-Tagged Sites (STS)).
- הליכה מסמן לסמן:
- מרצפים מקטע שמכיל סמן ידוע
- מזהים סמן נוסף במקטע
- מחפשים מקטע אחר שמכיל את הסמן הזה
- ממשיכים כך “צעד אחר צעד”
- בניית קונטיגים (Contigs): חיבור מקטעים שיש ביניהם חפיפה ליצירת רצפים ארוכים יותר.
מה מאפשר את החיבור? חיתוך עם אנזימי רסטריקציה שונים יוצר מקטעים שיש ביניהם אזורים חופפים - כך ניתן לזהות את הסדר הנכון.
חיסרון מרכזי: שיטה איטית מאוד, סיזיפית, דורשת עבודה ידנית רבה.
שיטה 2: Shotgun Sequencing
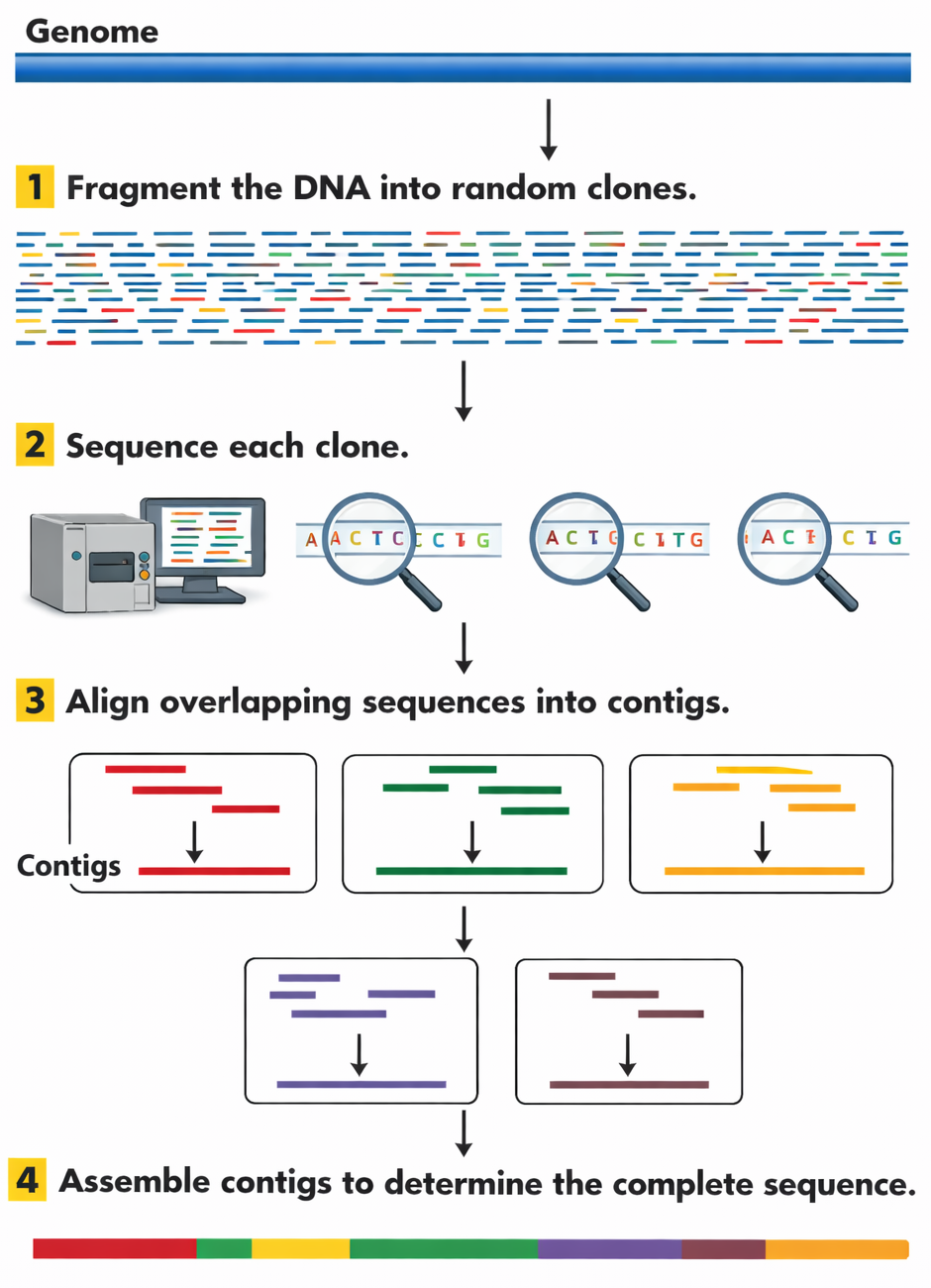
העיקרון (פותח על ידי חברת Celera)
-
שבירה אקראית: שבירת הגנום למקטעים קצרצרים (1,000-2,000 bp) באמצעות גלי קול - ללא אנזימי רסטריקציה.
-
ריצוף מסיבי: ריצוף של כל המקטעים במקביל.
-
הרכבה חישובית: שימוש במחשבי ענק לזיהוי חפיפות ולבניית הרצף המלא.
יתרונות:
- מהיר יותר משמעותית
- לא דורש זיהוי סמנים מראש
- ניתן לרצף מקטעים רבים במקביל
חיסרון: דורש כוח חישובי עצום
פרויקט הגנום האנושי - המירוץ
הפרויקט הציבורי (2005-1990)
- מימון: NIH וממשלות (18 מדינות, כולל ישראל)
- שיטה: Chromosome Walking
- מטרות:
- פענוח רצף 3 מיליארד בסיסים
- קביעת מיקום כל רצף
- זיהוי מספר הגנים
- יצירת מאגר מידע פתוח לציבור
- מקור ה־
DNA: 100 מתנדבים מקבוצות אתניות שונות (לא אדם בודד!)
חברת Celera (הפרויקט הפרטי)
- שיטה: Shotgun Sequencing
- יתרון: מהירות גבוהה יותר, עלות נמוכה יותר
- בעיה אתית: חברה פרטית עם אינטרסים מסחריים - סכנה שהמידע הגנטי יהיה בבעלות פרטית
התוצאה
שתי הקבוצות הגיעו לסיום כמעט בו־זמנית. המידע נותר פתוח לציבור.
התקדמות הטכנולוגיה:
- פרויקט מקורי: כ־15 שנים, מיליוני דולרים
- כיום (NGS): פחות מחודשיים, כ־1,000 דולר לאדם
מה גילינו מריצוף הגנום?
הרכב הגנום האנושי
| רכיב | אחוז | הסבר |
|---|---|---|
| רצפים מקודדים | 1.5%~ | אקסונים - מתורגמים לחלבונים |
| רצפים חזרתיים | 60%~ | מקטעים שחוזרים על עצמם |
| רצפי בקרה | משתנה | אינטרונים, פרומוטורים, אנהנסרים |
| רצפים לא מוכרים | משתנה | תפקיד לא ידוע (לא בהכרח “זבל”) |
תובנה מפתיעה: רק 1.5% מה־DNA שלנו מקודד לחלבונים! השאר - חלקו בעל תפקיד בקרתי, חלקו שריד אבולוציוני, וחלקו עדיין לא מובן.
מאגר UCSC Genome Browser
לאחר ריצוף הגנום נוצר מאגר מידע מקיף המאפשר:
- צפייה בכל כרומוזום ואזוריו
- זיהוי גנים, אקסונים ואינטרונים
- מיקום SNPs ווריאנטים
- השוואה לגנומים של אורגניזמים אחרים
- מידע על כל נוקלאוטיד בגנום
חלק ג’: טרנספוזונים (Transposable Elements)
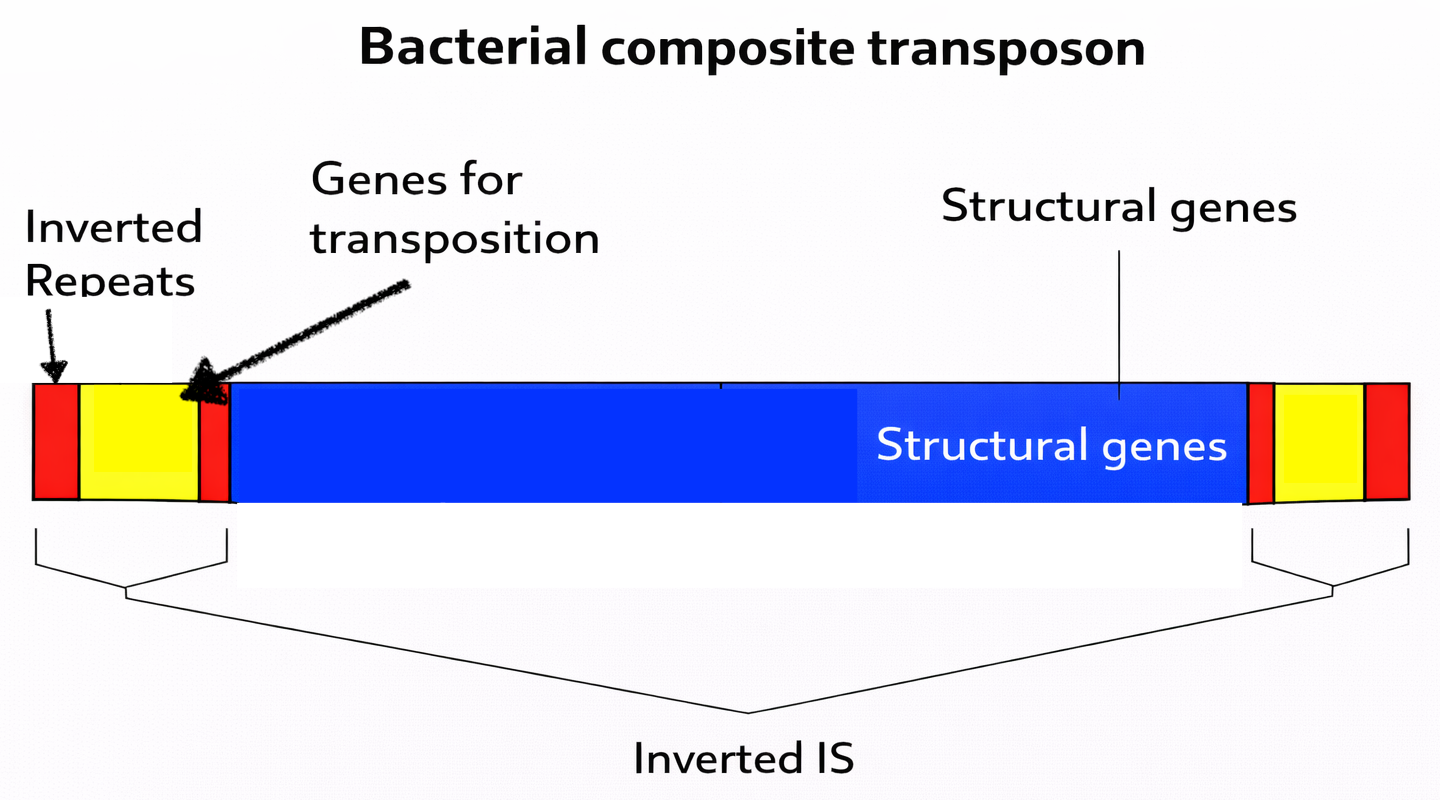
IS = Insertion Sequence
מהם טרנספוזונים?
טרנספוזונים הם מקטעי DNA שיכולים לעבור ממקום למקום בתוך הגנום. הם אחד ההסברים המרכזיים לקיום רצפים חזרתיים בגנום.
שני סוגי טרנספוזונים
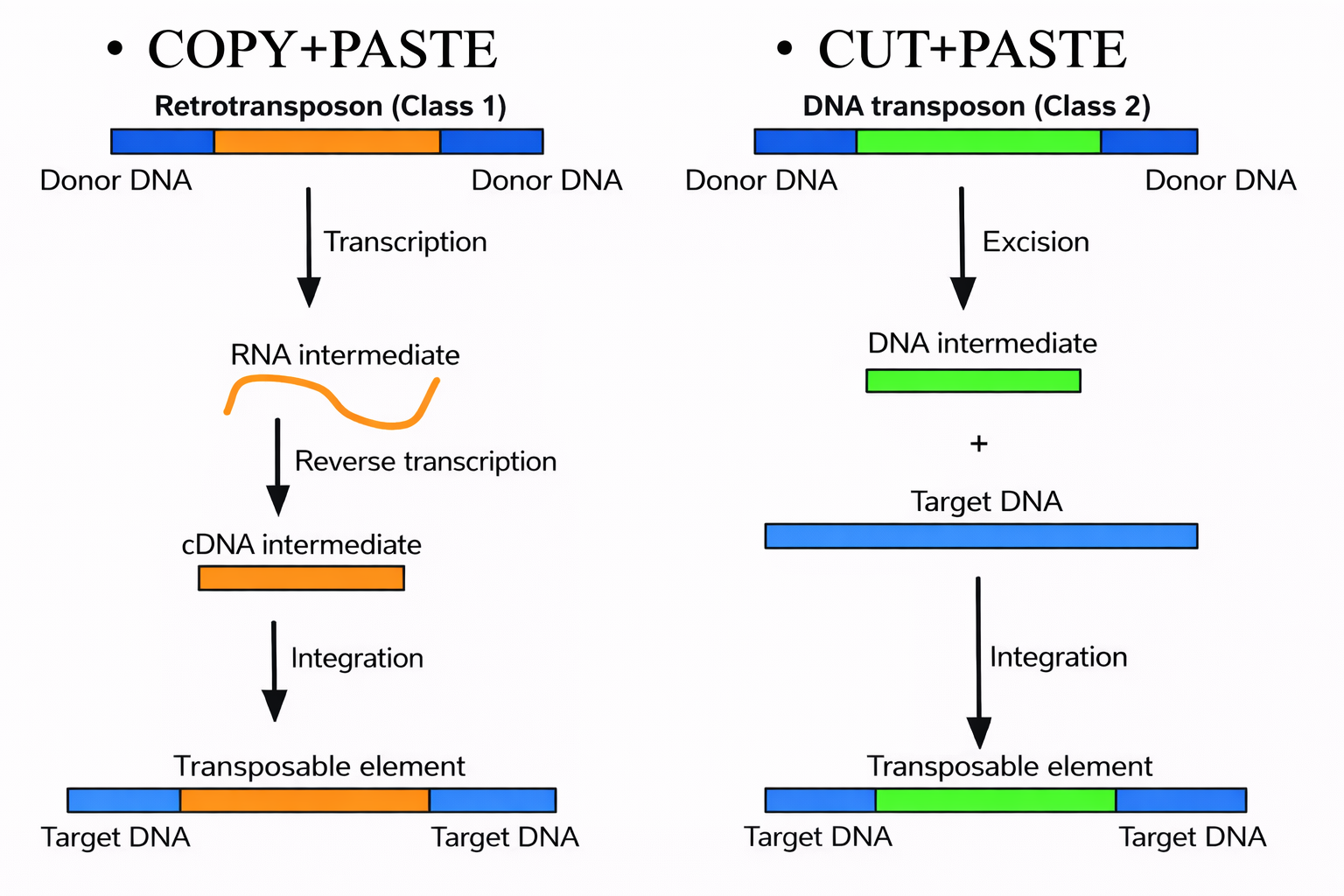
Class II - DNA Transposons (Cut and Paste)
מנגנון:
- אנזים טרנספוזאז מזהה את הטרנספוזון
- האנזים חותך את הטרנספוזון ממקומו המקורי
- הטרנספוזון משתלב במקום אחר בגנום
Class I - Retrotransposons (Copy and Paste)
מנגנון:
- הטרנספוזון משועתק ל־RNA
- אנזים Reverse Transcriptase יוצר cDNA מה־RNA
- ה־cDNA החדש משתלב במקום אחר בגנום
- העותק המקורי נשאר במקומו
הבדל קריטי: ב־Cut and Paste יש העברה. ב־Copy and Paste יש שכפול - נוצר עותק נוסף.
משמעות אבולוציונית
תרומות פוטנציאליות:
- יצירת עותקים של גנים חשובים - “גיבוי” גנטי
- שינוי בקרה - גן שעובר מקום עשוי להיות תחת בקרה שונה
- הגברת שונות גנטית - מנגנון לשינוי מהיר יחסית
סיכונים:
- השתלבות בתוך גן פעיל עלולה לשבש אותו
- עלול לגרום למוטציות מזיקות
קצב התנועה: טרנספוזונים לא נעים כל הזמן - התנועה יכולה להתרחש בתדירות נמוכה מאוד (פעם בדורות רבים).
שימוש במחקר
חוקרים משתמשים בטרנספוזונים ככלי מחקר:
- יצירת מוטציות מכוונות - הכנסת טרנספוזונים לגנים ספציפיים
- מעקב אחר ביטוי גנים - הוספת סמנים (כמו GFP) לטרנספוזון
- פוטנציאל לטיפול גנטי - הכנסת גנים תרפויטיים
חלק ד’: שיטות מחקר גנטי
Forward vs. Reverse Genetics
Forward Genetics
כיוון: מפנוטיפ ← לגנוטיפ
השאלה: יש לי תופעה/מחלה - איזה גן אחראי?
שיטות:
- השוואת רצפים בין קבוצות (חולים vs. בריאים)
- מחקרי GWAS (Genome-Wide Association Studies)
Reverse Genetics
כיוון: מגנוטיפ ← לפנוטיפ
השאלה: יש לי גן - מה הוא עושה?
שיטות:
- Knockout - השבתת גן ובדיקת ההשפעה
- מוטגנזה מכוונת - יצירת מוטציות בגנים ספציפיים
- שימוש בטרנספוזונים - הכנסה אקראית ומעקב אחר פנוטיפים
- ביטוי יתר - הגברת ביטוי של גן ובדיקת ההשפעה
מחקרי GWAS
מהו GWAS? Genome-Wide Association Study - מחקר שמשווה את כל הגנום בין קבוצות גדולות.
העיקרון:
- איסוף קבוצה גדולה של אנשים עם מאפיין/מחלה מסוימים
- איסוף קבוצת ביקורת (ללא המאפיין)
- ריצוף/סריקת הגנום של כל המשתתפים
- זיהוי אזורים גנטיים שונים באופן מובהק בין הקבוצות
למה צריך קבוצות גדולות? כי יש הרבה שונות “רגילה” בין אנשים - צריך מספיק נבדקים כדי להבחין בין שונות אקראית לבין שונות הקשורה למאפיין הנחקר.
פרויקט 1,000 Genomes
תקופה: 2015-2008
מטרות:
- בניית מפה מפורטת של שונות גנטית באוכלוסייה
- זיהוי מוטציות הגורמות למחלות
- הבנת שינויים אבולוציוניים בגנום האנושי
ממצאים:
- זוהו כ־2,000 לוקוסים הקשורים ל־300+ מחלות
- בממוצע, לכל אדם 300-250 וריאנטים הגורמים לאובדן פעילות של אלל אחד
- קצב המוטציות בדורות גבוה ממה שחשבו
סיכום לבחינה
גנטיקה התפתחותית
- שלושה תהליכים מקבילים: חלוקה מוגברת, התמיינות, מורפוגנזה
- מורפוגנים: חלבונים שמופרשים ויוצרים גרדיאנט ריכוזים; רמות שונות מפעילות גנים שונים
- Bicoid - מורפוגן ראש; Caudal - מורפוגן זנב (בזבוב)
- Hox genes - גנים הומיאוטיים בבני אדם לקביעת צירי הגוף
- פוטנציאל התמיינות: Totipotent > Pluripotent > Multipotent > Tissue-specific
- תאי גזע בבוגר: מח עצם - יכולים להתחלק לכל תאי הדם
ריצוף הגנום
- Sanger: מדויק עד ~1,000 bp בלבד
- Chromosome Walking: איטי, מבוסס סמנים וחפיפות
- Shotgun Sequencing: מהיר, מבוסס חישוב
- פרויקט הגנום: 2005-1990, 100 מתנדבים, מידע פתוח לציבור
- הרכב הגנום: רק 1.5% מקודד, ~60% רצפים חזרתיים
טרנספוזונים
- Class I (Retrotransposons): Copy and Paste דרך RNA
- Class II (DNA Transposons): Cut and Paste ישיר
- משמעות: הסבר לרצפים חזרתיים, מנגנון אבולוציוני
שיטות מחקר
- Forward Genetics: פנוטיפ ← גנוטיפ (GWAS)
- Reverse Genetics: גנוטיפ ← פנוטיפ (Knockout, מוטגנזה)
- GWAS: השוואת גנום בין קבוצות גדולות
לקסיקון מונחים
| מונח | הגדרה |
|---|---|
| מורפוגנזה | תהליך יצירת צורת הגוף וארגון האיברים |
| מורפוגן | מולקולת סיגנל שיוצרת גרדיאנט ריכוזים וקובעת גורל תאים |
| התמיינות | תהליך שבו תאים מקבלים תפקידים ספציפיים |
| Totipotent | יכולת להתחלק לכל סוגי התאים |
| Pluripotent | יכולת להתחלק לרוב סוגי התאים |
| Hox genes | גנים הומיאוטיים הקובעים דפוסי גוף |
| קונטיג (Contig) | רצף DNA מורכב ממספר מקטעים חופפים |
| Shotgun Sequencing | ריצוף מקביל של מקטעים קצרים והרכבה חישובית |
| טרנספוזון | מקטע DNA שיכול לעבור ממקום למקום בגנום |
| Retrotransposon | טרנספוזון שעובר דרך RNA (Copy and Paste) |
| Reverse Transcription | יצירת DNA מתבנית RNA |
| cDNA | DNA שנוצר מ־RNA (ללא אינטרונים) |
| GWAS | מחקר השוואת גנום בין קבוצות לזיהוי קשרים גנטיים |
| Forward Genetics | מחקר מפנוטיפ לגנוטיפ |
| Reverse Genetics | מחקר מגנוטיפ לפנוטיפ |
שאלות תרגול מג׳ונרטות
שאלה 1: שלבי ההתפתחות העוברית
מהם שלושת השלבים המרכזיים בהתפתחות עוברית?
- חלוקה תאית (Cleavage), גסטרולציה (Gastrulation), נוירולציה (Neurulation)
- חלוקה תאית (ריבוי תאים), דיפרנציאציה (התמיינות תאים), מורפוגנזה (עיצוב הגוף)
- מיוזה (יצירת גמטות), הפריה (יצירת זיגוטה), אורגנוגנזה (יצירת איברים)
- דיפרנציאציה (התמיינות), אורגנוגנזה (איברים), גדילה (Growth) עד שלב הלידה
פתרון
התשובה הנכונה היא (2).
מהשיעור (שקף 4):
| שלב | תיאור |
|---|---|
| חלוקה תאית | מיטוזה ומיוזה - ריבוי תאים מתא מופרה אחד |
| דיפרנציאציה | מתאי גזע עובריים לתאים ממוינים - תהליך רב־שלבי של בקרת ביטוי גנים הדורש סנכרון בין התאים |
| מורפוגנזה | עיצוב צורת הגוף - כולל יצירת ציר גוף (body axis) |
השאלה המרכזית של הגנטיקה ההתפתחותית: איך מתא יחיד עם גנום מלא מתפתח אורגניזם שלם?
מקור: שקפים 2-4
שאלה 2: מהזיגוטה לבלסטוציסט
מהו ה־Inner Cell Mass בבלסטוציסט, ומה משמעותו?
- שכבת תאים פנימית שמייצרת בעיקר את שק החלמון ורקמות תומכות עובר
- שכבת תאים חיצונית שממנה יתפתחו רוב תאי הגוף, בעוד התאים הפנימיים יוצרים שליה
- צבר התאים הפנימיים שממנו יתפתחו תאי גזע פלוריפוטנטיים ובהמשך מרבית תאי העובר
- חלל הבלסטוציסט (Blastocoel) שמכיל נוזל ותפקידו לאפשר דיפוזיה של מורפוגנים
פתרון
התשובה הנכונה היא (3).
מהשיעור (שקפים 5, 11):
תהליך ההתפתחות המוקדמת:
Sperm + Egg → Fertilized egg → Blastocyst
ה־Blastocyst מכיל:
- Inner Cell Mass - ממנו נוצרים תאים פלוריפוטנטיים → Embryonic Stem Cells ← כל תאי העובר
- שכבה חיצונית (Trophoblast) - תיצור את השליה ורקמות תומכות
בשלב הזיגוטה התא הוא Totipotent (יכול ליצור כל דבר, כולל שליה). Inner Cell Mass הוא Pluripotent - יכול ליצור כל סוג תא בגוף אך לא שליה.
מקור: שקפים 5, 11
שאלה 3: טוטיפוטנטיות מול פלוריפוטנטיות
מה ההבדל בין תא טוטיפוטנטי לתא פלוריפוטנטי?
- טוטיפוטנטי יוצר רק רקמות חוץ־עובריות (כמו שליה), ופלוריפוטנטי יוצר רק רקמות עובריות (תאי גוף)
- טוטיפוטנטי יכול ליצור אורגניזם שלם כולל רקמות חוץ־עובריות; פלוריפוטנטי יוצר את רוב תאי הגוף אך לא שליה
- טוטיפוטנטי הוא תא גזע בוגר (Adult stem cell), ופלוריפוטנטי נמצא רק בשלבי חלוקה מאוחרים של העובר
- טוטיפוטנטי ופלוריפוטנטי מתארים אותו דבר, ההבדל הוא רק במידת קצב החלוקה של התאים
פתרון
התשובה הנכונה היא (2).
מהשיעור (שקף 11 - Cell Determination):
| רמת פוטנטיות | יכולת | שלב |
|---|---|---|
| Totipotent | יכול ליצור אורגניזם שלם + שליה | זיגוטה ותאי ה־Cleavage הראשונים |
| Pluripotent | יכול ליצור כל סוגי תאי הגוף אך לא רקמות חוץ־עובריות | Inner Cell Mass / Embryonic Stem Cells |
| Multipotent | מוגבל למספר סוגי תאים ברקמה מסוימת | תאי גזע מבוגרים (למשל המטופויטיים) |
הסדר: ככל שההתפתחות מתקדמת, הפוטנטיות יורדת ← ההתמיינות היא בד”כ חד־כיוונית.
מקור: שקפים 11-10
שאלה 4: שלוש שכבות הנבט
רקמת מערכת העצבים (עצבים) ורקמת האפידרמיס (עור) מתפתחות משכבת נבט אחת. מהי?
- אקטודרם - שכבת נבט שתורמת בין היתר למערכת העצבים ולאפידרמיס
- מזודרם - שכבה שמייצרת שריר/שלד וגם חלקים של מערכת העצבים ההיקפית
- אנדודרם - שכבה פנימית שמייצרת אפיתל נשימתי ומערכת העיכול וגם עור
- טרופובלסט - שכבה עוברית שממנה מתפתחות שכבות הנבט והרקמות החוץ־עובריות יחד
פתרון
התשובה הנכונה היא (1).
מהשיעור (שקפים 11, 17):
שלוש שכבות הנבט (Germ Layers) נוצרות בתהליך הגסטרולציה:
| שכבה | איברים ומערכות |
|---|---|
| Ectoderm (אקטודרם) | עצבים (nerves), אפידרמיס (epidermis) |
| Mesoderm (מזודרם) | מערכת לב וכלי דם (cardiovascular), שלד ושרירים (musculoskeletal), מערכת השתן (urinary) |
| Endoderm (אנדודרם) | ריאות (lung), קיבה (stomach), לבלב (pancreas), כבד (liver), מעי (intestine) |
שימו לב: גם עצבים וגם עור - שנראים כמו רקמות שונות מאוד - מגיעים מאותה שכבה (Ectoderm).
מקור: שקפים 11, 17
שאלה 5: גסטרולציה
מהי גסטרולציה ומה נוצר בתהליך זה?
- שלב מעבר שבו הבלסטולה עוברת ארגון מחדש ונוצרות שכבות נבט עיקריות שמגדירות את תוכנית הגוף
- שלב חלוקות מוקדמות שבו הזיגוטה מתחלקת לתאי Blastomeres ונוצר כדור תאים ראשוני
- שלב שבו מתחילה נוירולציה ונוצרת התחלה של Neural Tube לאורך ציר הגוף
- שלב שבו מתחילה אורגנוגנזה מוקדמת ונוצרים ניצני איברים (כמו לב, כבד ומעי)
פתרון
התשובה הנכונה היא (1).
מהשיעור (שקפים 16-17):
סדר ההתפתחות המוקדמת:
Zygote → (Cleavage) → Eight-cell stage → Blastula → (Gastrulation) → Gastrula
Blastula = כדור חלול של תאים (Blastomeres) עם חלל פנימי מלא נוזל (Blastocoel).
בגסטרולציה: תאים נודדים פנימה דרך ה־Blastopore ← נוצרות שלוש שכבות נבט ← ומהן יתפתחו כל איברי הגוף.
מקור: שקפים 16-17
שאלה 6: קוטביות Anterior-Posterior
איזו קוטביות נקבעת עוד בשלב הביצית בדרוזופילה, וכיצד?
- קוטביות Anterior–Posterior נקבעת מוקדם ע”י לוקליזציה של mRNA אימהי בקוטב הקדמי ויצירת גרדיאנט חלבון לאחר ההפריה
- קוטביות Dorsal–Ventral נקבעת בביצית ע”י גרדיאנט Wnt שמופרש מהקוטב האחורי ומדכא גנים דורסליים
- קוטביות Right–Left נקבעת בביצית ע”י תנועת סיליות שמסיטות מורפוגנים לצד שמאל עוד לפני הפריה
- אין קוטביות בביצית; כל הצירים נקבעים רק לאחר חלוקת תאים והופעת שכבות הנבט
פתרון
התשובה הנכונה היא (1).
מהשיעור (שקפים 15, 21-23):
עוד לפני ההפריה, ה־mRNA של Bicoid מושקע בקוטב ה־Anterior של הביצית ע”י האם.
זוהי דוגמה ל־Maternal Effect Genes: האם מספקת ציטופלזמה (כולל mRNA) לביצית ← תוצרי הגנים האימהיים קובעים את הקוטביות המוקדמת של העובר.
ניסוי מרכזי (שקף 22): אם Bicoid mutant mother נראית תקינה בעצמה, אך ה־offspring שלה חסרים מבנים אנטריוריים (lack anterior structures) - כי האם לא יכלה לספק Bicoid mRNA לביצית.
מקור: שקפים 15, 21-23
שאלה 7: מורפוגנים - עקרון הפעולה
כיצד מורפוגן קובע גורלות תאיים שונים באותו רקמה?
- מורפוגן מופרש מנקודת מקור ויוצר גרדיאנט; תאים מפרשים ריכוזים שונים ומפעילים סטים שונים של גנים בהתאם לספים
- מורפוגן נקשר ל־DNA בכל תא באופן זהה, אך גורם לאותם גנים לפעול בזמן שונה בכל אזור ברקמה
- מורפוגן נכנס רק לתאי גזע; תאים ממוינים אינם מגיבים ולכן נוצר דפוס מרחבי עקיף
- מורפוגן גורם בעיקר למוות תאי של תאים רחוקים מהמקור וכך נוצר גבול רקמתי חד
פתרון
התשובה הנכונה היא (1).
מהשיעור (שקפים 19-20, 26):
מורפוגן = מולקולה המשפיעה על דפוסי התפתחות ע”י גרדיאנט ריכוזים.
דוגמאות: Bicoid, BMP, Shh (Sonic Hedgehog).
עקרון הפעולה (שקף 20):
Morphogen gradient → Signal interpretation → Tissue patterning
תאים קרובים למקור המורפוגן חשופים לריכוז גבוה ← מפעילים Gene A. תאים רחוקים יותר חשופים לריכוז נמוך ← מפעילים Gene B או Gene C. כך ממולקולה אחת נוצרים אזורים שונים ברקמה.
דוגמת Bicoid (שקף 26): Bicoid target genes דורשים רמות שונות של חלבון Bicoid - high, medium, low levels ← גנים שונים מופעלים במיקומים שונים לאורך הציר.
מקור: שקפים 19-20, 26
שאלה 8: Bicoid כמורפוגן ומווסת תרגום
חלבון Bicoid פועל בשני מנגנונים שונים. מהם?
- פועל כמפעיל שעתוק של גנים אנטריוריים וגם כמעכב תרגום של caudal mRNA באזור הקדמי
- פועל כמפעיל שעתוק של caudal באזור פוסטריור וגם כמעכב תרגום של hunchback באזור אנטריור
- פועל כ־Receptor ממברנלי שמפעיל מסלול איתות וגם כאנזים שמפרק mRNA בציטופלזמה
- פועל כמעכב שעתוק של גנים אנטריוריים וגם כמעכב תרגום של bicoid mRNA באמצעות משוב שלילי
פתרון
התשובה הנכונה היא (1).
מהשיעור (שקפים 25-27):
חלבון Bicoid - פועל בשני מנגנונים:
| מנגנון | פעולה | תוצאה |
|---|---|---|
| Transcriptional Activator | מפעיל גנים אנטריוריים (כמו hunchback, orthodenticle) | יצירת מבנים קדמיים |
| Translation Repressor | מעכב תרגום של caudal mRNA | מונע יצירת Caudal protein באנטריור |
caudal mRNA מפוזר באופן אחיד בביצית, אבל חלבון Caudal נוצר רק בפוסטריור - כי Bicoid מעכב את התרגום שלו באנטריור.
כך נוצרים שני גרדיאנטים הפוכים: Bicoid (גבוה באנטריור), Caudal (גבוה בפוסטריור).
מקור: שקפים 25-27
שאלה 9: Syncytial Blastoderm בדרוזופילה
מדוע ההתפתחות המוקדמת של דרוזופילה ייחודית בהשוואה ליונקים?
- חלוקות גרעיניות מהירות מתרחשות ללא ציטוקינזיס, ולכן נוצר syncytium עד שלב שבו נוצרת ממברנה סביב כל גרעין
- חלוקות תאים מוקדמות מתרחשות רק לאחר יצירת שכבות נבט, ולכן אין שלב של blastula אמיתי
- ההתפתחות מתבססת על מיוזה חוזרת של גרעינים ללא הפריה, ולכן נוצר עובר הפלואידי זמני
- אין מורפוגנים בדרוזופילה; דפוס הגוף נקבע רק ע”י אינטראקציות בין תאים לאחר cellularization
פתרון
התשובה הנכונה היא (1).
מהשיעור (שקף 24):
שלבי ההתפתחות המוקדמת של דרוזופילה:
Fertilized egg ← Division of nuclei (חלוקת גרעינים מהירה, כל 9 דקות!) ← More nuclear divisions, Movement to periphery ← Cellular blastoderm
| שלב | מאפיין |
|---|---|
| Syncytial stages | גרעינים רבים בציטופלזמה משותפת אחת, ללא ממברנות תא |
| Cellular blastoderm | רק אחרי 13 חלוקות גרעינים - נוצרות ממברנות ומתחילה חלוקה לתאים |
משמעות: המורפוגנים (כמו Bicoid) יכולים לדפוז באופן חופשי בציטופלזמה המשותפת ← מה שמאפשר יצירת גרדיאנטים יעילים.
מקור: שקף 24
שאלה 10: Maternal Effect Genes
אם לזבוב (דרוזופילה) נקבה יש מוטציה הומוזיגוטית בגן Bicoid - מה צפוי לקרות?
- הנקבה תיראה תקינה, אך העוברים שלה יפתחו חסר במבנים אנטריוריים עקב היעדר אספקת mRNA אימהי לביצית
- הנקבה עצמה תהיה חסרת מבנים אנטריוריים, כי Bicoid נדרש להתפתחות ראש אצל כל פרט
- העוברים יהיו תקינים כי הגנום של האב מספק Bicoid מוקדם ומאזן את החסר האימהי
- הנקבה תהיה עקרה תמיד, כי בלי Bicoid לא מתרחשת הפריה או התחלת חלוקות גרעין
פתרון
התשובה הנכונה היא (1).
מהשיעור (שקפים 23-22):
Bicoid הוא Maternal Effect Gene - תוצרו (mRNA) מסופק לביצית ע”י האם, לא ע”י הגנום של העובר.
| מצב | האם | העובר |
|---|---|---|
| Bicoid mutant mother | נראית תקינה (normal appearance) | חסר מבנים אנטריוריים (lack anterior structures) |
| אם תקינה | תקינה | עובר תקין |
למה האם תקינה? כי ה־Bicoid שלה עצמה סופק ע”י אמה. המוטציה ב־Bicoid משפיעה רק על הדור הבא - כי האם המוטנטית לא יכולה לספק Bicoid mRNA לביציות שלה.
זהו דפוס תורשה ייחודי: הפנוטיפ של העובר נקבע ע”י הגנוטיפ של האם (ולא של העובר עצמו).
מקור: שקפים 23-22
שאלה 11: גני סגמנטציה
מהו תפקידם של גני סגמנטציה (Segmentation genes)?
- כיוון יצירת סגמנטים ומיקומם לאחר שהוגדרו הצירים המרכזיים של העובר ע”י גנים אימהיים
- קביעת ציר Anterior–Posterior הראשוני באמצעות גרדיאנט של מורפוגנים אימהיים בביצית
- קביעת זהות סגמנטלית (ראש/חזה/בטן; אנטנה/רגל/כנף) לאחר שהסגמנטים כבר קיימים
- יצירת שלוש שכבות הנבט בתהליך הגסטרולציה וקביעת גורל רקמות מרכזיות
פתרון
התשובה הנכונה היא (1).
מהשיעור (שקף 30):
Segmentation genes: “the genes that direct the actual formation of segments after the embryo’s major axes are defined.”
הם פעילים בשלבים מוקדמים של ההתפתחות העוברית, לאחר שגנים אימהיים (כמו Bicoid) כבר קבעו את הקוטביות.
מה יקרה אם תהיה מוטציה בגן סגמנטציה? פגם בחלוקת הגוף לסגמנטים - ייתכנו סגמנטים חסרים, כפולים או חלקיים.
ההבדל מגנים הומיאוטיים: גני סגמנטציה קובעים את מספר ומיקום הסגמנטים. גנים הומיאוטיים קובעים את הזהות של כל סגמנט (ראש/חזה/בטן, רגל/אנטנה/כנף).
מקור: שקפים 30-31
שאלה 12: גנים הומיאוטיים - Homeotic Genes
מהו גן הומיאוטי ומה קורה כשיש בו מוטציה?
- גן שמגדיר את זהות הסגמנט ואת סוג המבנים שיתפתחו בו; מוטציה יכולה לגרום להחלפת איבר באיבר אחר במיקום שגוי
- גן שמגדיל את קצב חלוקת התאים בכל העובר; מוטציה גורמת לעיכוב כללי בהתפתחות ולגדילה איטית
- גן שמווסת יצירת שכבות נבט בגסטרולציה; מוטציה גורמת להיעדר מוחלט של מזודרם
- גן שמקודד לאנזים מטבולי בסיסי; מוטציה גורמת לכשל מטבולי כלל־גופי אך לא לשינוי מבני
פתרון
התשובה הנכונה היא (1).
מהשיעור (שקף 31):
Homeotic gene: “gene that specifies the types of appendages and other structures that each segment will form.”
הם פעילים אחרי שהוגדרו הסגמנטים - בכדי לפתח את האיברים המתאימים (רגל/אנטנה וכו’).
דוגמה קלאסית בדרוזופילה: מוטציה ב־Antennapedia ← רגליים גדלות מהראש במקום אנטנות. מוטציה ב־Bithorax ← זוג כנפיים נוסף במקום Halteres.
גנים אלו הם פקטורי שעתוק (Transcription Factors) המפעילים סדרות של גנים אחרים הקובעים זהות סגמנטלית.
מקור: שקפים 30-31
שאלה 13: גני Hox - שימור אבולוציוני
כמה אשכולות (clusters) של גני Hox קיימים באדם, והיכן הם ממוקמים?
- ארבעה אשכולות (HOX A–D) על כרומוזומים שונים; יש גם עקרון קולינאריות בין סדר הגנים לבין ציר הגוף
- אשכול יחיד גדול על כרומוזום אחד; הסדר הפנימי שלו אינו קשור לדפוס הביטוי העוברי
- שני אשכולות עיקריים על כרומוזומי המין; הם אחראים בעיקר לדימורפיזם מיני בעובר
- אשכולות רבים מפוזרים באופן אקראי בגנום; כל גן Hox פועל ללא קשר לשכניו בכרומוזום
פתרון
התשובה הנכונה היא (1).
מהשיעור (שקף 32):
| אשכול | כרומוזום (אדם) | כרומוזום (עכבר) |
|---|---|---|
| HOX A | 7p14-15 | 6C2 |
| HOX B | 17q21-22 | 11B4 |
| HOX C | 12q12-13 | 15F2 |
| HOX D | 2q31-37 | 2C3 |
עקרון Colinearity: הסדר של גני Hox על הכרומוזום (3’←5’) תואם את הסדר של ביטוי שלהם לאורך ציר הגוף (Anterior←Posterior).
שימור אבולוציוני: גני Hox שמורים מאוד מדרוזופילה (קומפלקס HOM-C אחד) דרך עכבר ועד אדם (4 קומפלקסים) - עדות לחשיבותם הקריטית בהתפתחות.
מקור: שקף 32
שאלה 14: מסלול Sonic Hedgehog - Shh
מהו תפקידו של מסלול Shh ואיזו מחלה נגרמת ממוטציה בו?
- התפתחות המוח והגפיים; פגיעה במסלול עלולה לגרום ל־Holoprosencephaly עקב כשל בדפוס מוקדם של המוח הקדמי
- ויסות חלוקת תאי דם; מוטציה גורמת ל־Anemia חרמשית עקב שינוי בהמוגלובין
- בניית סחוס וגדילת עצם ארוכה; מוטציה גורמת ל־Achondroplasia עקב FGFR3 פעיל־יתר
- התפתחות מערכת החיסון; מוטציה גורמת ל־SCID עקב כשל בהבשלה של לימפוציטים
פתרון
התשובה הנכונה היא (1).
מהשיעור (שקפים 28-29):
מסלול Shh (Sonic Hedgehog):
| מאפיין | פרט |
|---|---|
| תפקיד | התפתחות המוח והגפיים |
| מנגנון | Shh נקשר ל־Patched (Ptch) → מפעיל Smoothened (Smo) → GliA (activator) במקום GliR (repressor) → neural tube patterning |
| מחלה | Holoprosencephaly (HPE) - אין הפרדה תקינה בין אונות המוח |
| תזמון | שבועות עובריים ראשונים |
ה־Shh pathway פועל כגרדיאנט בצינור העצבי (Neural Tube) - ריכוז גבוה ב־Ventral, נמוך ב־Dorsal ← קובע סוגי נוירונים שונים לאורך הציר הדורסו־ונטרלי.
מקור: שקפים 28-29
שאלה 15: פקטורי שעתוק מרכזיים בהתמיינות
אילו פקטורי שעתוק חשובים לשמירה על פלוריפוטנטיות של תאי גזע?
- Sox2 ו־Oct4 - רשת רגולטורית שמייצבת פלוריפוטנטיות ומונעת התמיינות מוקדמת
- p53 ו־Rb - בקרה על מחזור התא ומניעת חלוקה לא מבוקרת ברקמות שונות
- MyoD ו־Myogenin - שפעול תוכנית התמיינות שרירית ויצירת סיבי שריר
- HoxA ו־HoxD - קביעת זהות סגמנטלית לאורך ציר הגוף בעובר
פתרון
התשובה הנכונה היא (1).
מהשיעור (שקף 34):
תהליכי בקרה של ההתמיינות כוללים:
| מנגנון בקרה | דוגמה |
|---|---|
| פקטורי שעתוק מרכזיים | Sox2, Oct4 - שומרים על פלוריפוטנטיות |
| אפיגנטיקה | מתילציה של DNA |
| RNAi | ויסות ע”י RNA קטנים |
| מורפוגנים ופקטורי גדילה | סיגנלים חיצוניים |
| אינטראקציות בין תאים | תקשורת ישירה בין תאים שכנים |
| אפופטוזיס | מוות תאי מתוכנת |
Sox2 ו־Oct4 הם בין הגנים המרכזיים ב־iPSC (Induced Pluripotent Stem Cells - Yamanaka factors) - ביטוי מחדש שלהם בתאים ממוינים יכול להחזיר אותם למצב פלוריפוטנטי.
מקור: שקף 34
שאלה 16: אפופטוזיס בהתפתחות
מדוע מוות תאי מתוכנת (אפופטוזיס) הכרחי להתפתחות עוברית תקינה?
- אפופטוזיס מאפשר “פיסול” של רקמות ע”י סילוק תאים במיקום וזמן מדויקים; כשל בו גורם למשל לסינדקטיליה
- אפופטוזיס נדרש רק כדי להשמיד תאים שעברו מוטציות, ולכן רלוונטי בעיקר למניעת סרטן בעובר
- אפופטוזיס הוא מנגנון שמאיץ חלוקת תאים ע”י שחרור גורמי גדילה מהתאים המתים לסביבה
- אפופטוזיס מחליף דיפרנציאציה: תאים שאינם מתים נשארים תאי גזע ולכן מבנים נוצרים נכון
פתרון
התשובה הנכונה היא (1).
מהשיעור (שקפים 35-36):
“מוות תאי הוא גם חלק הכרחי בהתפתחות עוברית” (שקף 35).
דוגמאות:
- הפרדת אצבעות: התאים בין האצבעות עוברים אפופטוזיס ← נוצרות אצבעות נפרדות
- ספיגת זנב הראשנים: אפופטוזיס מסלק את הזנב בשלב ההתפתחות
- עיצוב חלל הלב, מערכת העצבים ועוד
“וכשהוא לא מתרחש יש פגם התפתחותי” (שקף 36): כאשר האפופטוזיס בין האצבעות לא מתרחש ← סינדקטיליה (Syndactyly) - אצבעות מחוברות.
מקור: שקפים 35-36
שאלה 17: תסמונת מרפן (Marfan Syndrome)
מהו הפגם הגנטי בתסמונת מרפן ואילו מערכות מושפעות?
- מוטציה ב־FBN1 (פיברילין-1); פגיעה ברקמות חיבור עם ביטוי בשלד, עיניים, ריאות ולב וכלי דם
- מוטציה ב־CFTR; פגיעה בהפרשת כלוריד שגורמת למחלה רב־מערכתית עם דגש על ריאות ולבלב
- מוטציה ב־COL1A1; פגיעה בקולגן סוג I שמובילה לשברים חוזרים ועיוותי שלד
- מוטציה ב־FGFR3; אות יתר שמדכא גדילת עצם ארוכה וגורם לגמדות
פתרון
התשובה הנכונה היא (1).
מהשיעור (שקף 33):
תסמונת מרפן:
| מאפיין | פרט |
|---|---|
| גן | FBN1 (מקודד פיברילין-1) |
| חלבון | פיברילין - חלבון מפתח ברקמת חיבור, חלק מסיבי אלסטין |
| מנגנון | מוטציה ב־FBN1 ← פגם בסיבי אלסטין ← פגיעה ברקמות שתומכות באיברים |
| תסמינים | עיוותים ביציבה (שלד), התרחבות אבי העורקים (לב וכלי דם), בעיות ריאות (קריסת ריאות), בעיות עיניים |
זו דוגמה למחלה גנטית הקשורה לגנטיקה התפתחותית - כי פיברילין חשוב לתמיכה המבנית של רקמות במהלך הגדילה וההתפתחות.
מקור: שקף 33
שאלה 18: ההיררכיה הגנטית בדרוזופילה
מהו הסדר הנכון של ההיררכיה הגנטית בהתפתחות דרוזופילה?
- Maternal effect genes קובעים צירים, אחריהם Segmentation genes מחלקים לסגמנטים, ולבסוף Homeotic genes מגדירים זהות סגמנט
- Segmentation genes קובעים צירים ראשוניים, אחריהם Homeotic genes בונים סגמנטים, ולבסוף Maternal effect genes מייצבים זהות
- Homeotic genes פועלים ראשונים לקביעת זהות, אחריהם Maternal effect genes יוצרים גרדיאנטים, ולבסוף Segmentation genes מחלקים
- Maternal effect genes קובעים זהות סגמנטלית, Segmentation genes קובעים איברים, Homeotic genes קובעים קוטביות A–P
פתרון
התשובה הנכונה היא (1).
מהשיעור (שקפים 22-31):
| שלב | סוג גנים | תפקיד | דוגמה |
|---|---|---|---|
| ראשון | Maternal effect genes | קביעת קוטביות A-P ו־D-V | Bicoid (anterior), Nanos (posterior) |
| שני | Segmentation genes | חלוקת הגוף לסגמנטים (gap → pair-rule → segment polarity) | fushi tarazu, engrailed |
| שלישי | Homeotic genes | קביעת הזהות הספציפית של כל סגמנט | Hox genes (Antp, Ubx, Abd-B) |
כל שלב מבוסס על התוצרים של השלב הקודם - מדובר בקסקדה רגולטורית.
מקור: שקפים 22-31
שאלה 19: מחקר תאי גזע - חשיבות רפואית
מדוע יש עניין רב במחקר תאי גזע?
- כי הם מאפשרים רגנרציה/החלפה של תאים ורקמות ובכך פוטנציאל טיפולי במחלות ניווניות, פגיעות לב וסוכרת
- כי הם מתחלקים במהירות ולכן תמיד ניתן לייצר מהם כל רקמה בלי בעיות התאמה חיסונית
- כי שימוש בתאי גזע מתאים רק למחקר בסיסי ואינו רלוונטי לרפואה יישומית או תרפיה
- כי תאי גזע משמשים בעיקר לאבחון גנטי (screening) ואין להם שימושים קליניים עתידיים
פתרון
התשובה הנכונה היא (1).
מהשיעור (שקפים 10, 12-13):
תאי גזע יכולים להתמיין למגוון סוגי תאים:
| כיוון התמיינות | סוגי תאים |
|---|---|
| Erythroid | כדוריות דם |
| Hematopoiesis | B-cells, Macrophages, T-cells |
| Myogenesis | Cardiomyocyte, Smooth muscle |
| Neural | Astrocyte, Microglia, Oligodendrocyte, Photoreceptor |
| Structural | Chondrocyte, Osteoblast |
| Signaling | Beta cell |
שקף 13: “תאי גזע יכולים לשקם את רקמת הלב” - דוגמה לפוטנציאל הטיפולי.
יישומים אפשריים: השתלת תאי Beta לחולי סוכרת, שיקום רקמת לב לאחר אוטם, תיקון רקמת עצב פגועה.
מקור: שקפים 10, 12-13
שאלה 20: אינטגרציה - מוטציה בגן התפתחותי
חוקרת מזהה עובר דרוזופילה עם פנוטיפ שבו רגליים גדלות מאזור הראש במקום אנטנות. על מוטציה באיזה סוג גן מדובר, ומדוע?
- Homeotic gene - כי הסגמנט קיים אך הזהות השתנתה, ונוצרה “המרה הומיאוטית” (appendage swap)
- Maternal effect gene - כי פגיעה מוקדמת בצירים גורמת לכך שמבנים אנטריוריים מתפתחים כפוסטריוריים
- Pair-rule gene - כי חסר סגמנט חלופי מוביל לפיצוי שבו הראש “מפתח” איברים של החזה
- Gap gene - כי חסר רציף של סגמנטים משנה את מספר האיברים ולכן נוצרת רגל במקום אנטנה
פתרון
התשובה הנכונה היא (1).
מהשיעור (שקפים 30-31):
ניתוח הפנוטיפ: הראש קיים, הסגמנט קיים - אבל במקום אנטנות צומחות רגליים. זוהי Homeotic Transformation - שינוי בזהות הסגמנט, לא בקיומו.
מוטציה ב־Antennapedia (גן הומיאוטי) ← ביטוי לא־תקין באזור הראש ← הסגמנט “חושב” שהוא חזה ← מפתח רגליים במקום אנטנות.
| סוג מוטציה | פנוטיפ צפוי |
|---|---|
| Maternal effect | פגיעה בקוטביות כללית (למשל חסר anterior שלם) |
| Gap gene | סגמנטים שלמים חסרים (חורים בגוף) |
| Pair-rule gene | חסרים סגמנטים חלופיים (כל שני) |
| Segment polarity | כל סגמנט מאבד קוטביות פנימית |
| Homeotic gene | סגמנט קיים אך הזהות שלו שונתה (רגל במקום אנטנה, כנפיים נוספות) |
מקור: שקפים 30-31
שאלות תרגול מג׳ונרטות: ריצוף DNA וגנומים
נושאים:
- שיטת Sanger ו־ddNTPs
- אלקטרופורזה קפילרית
- וקטורים וספריות גנומיות
- Chromosome Walking מול Shotgun
- פרויקט הגנום האנושי
- הרכב הגנום (1.5% מקודד!)
- סוגי חזרות
- טרנספוזונים (Copy+Paste מול Cut+Paste)
- Reverse Transcriptase ו־cDNA
- עכברי Knockout
- P-element ו־Inverse PCR
- NGS עם Bridge Amplification
- GWAS
- 1000 Genomes
- וגנומיקה השוואתית
שאלה 1: עקרון ריצוף Sanger
מדוע ddNTPs (Dideoxynucleotide triphosphates) גורמים לעצירת סינתזת DNA?
- הם נקשרים לתבנית ה־DNA ומונעים מהפולימראז להמשיך את האלונגציה
- הם חסרים קבוצת 3’-OH (ובהם גם 2’ הוא H), ולכן לאחר שילובם אין אפשרות להוסיף נוקלאוטיד נוסף בקשר פוספודיאסטרי
- הם גורמים ל־DNA polymerase לשגיאות זיווג בסיסים שמפסיקות את הריאקציה באופן אקראי
- הם משנים את מבנה ה־DNA כך שהוא מפסיק לשמש כתבנית לקשירת פריימר
פתרון
התשובה הנכונה היא (2).
מהשיעור (שקף 4):
סאנגר פיתח נוקלאוטידים מיוחדים שאינם מסוגלים להתארך בקצה 3’-OH.
| נוקלאוטיד | עמדה 2’ | עמדה 3’ | תוצאה |
|---|---|---|---|
| dNTP (רגיל) | H | OH | סינתזה ממשיכה - ה־OH בעמדה 3’ מאפשר קשר פוספודיאסטרי |
| ddNTP (דידאוקסי) | H | H (מימן בעמדות 2+3) | סינתזה נעצרת - אין OH בעמדה 3’ ליצירת הקשר הבא |
שימו לב: אין לבלבל עם נוקלאוטידים של RNA שלהם יש הידרוקסיל גם בעמדה 2’ וגם בעמדה 3’.
מקור: שקף 4
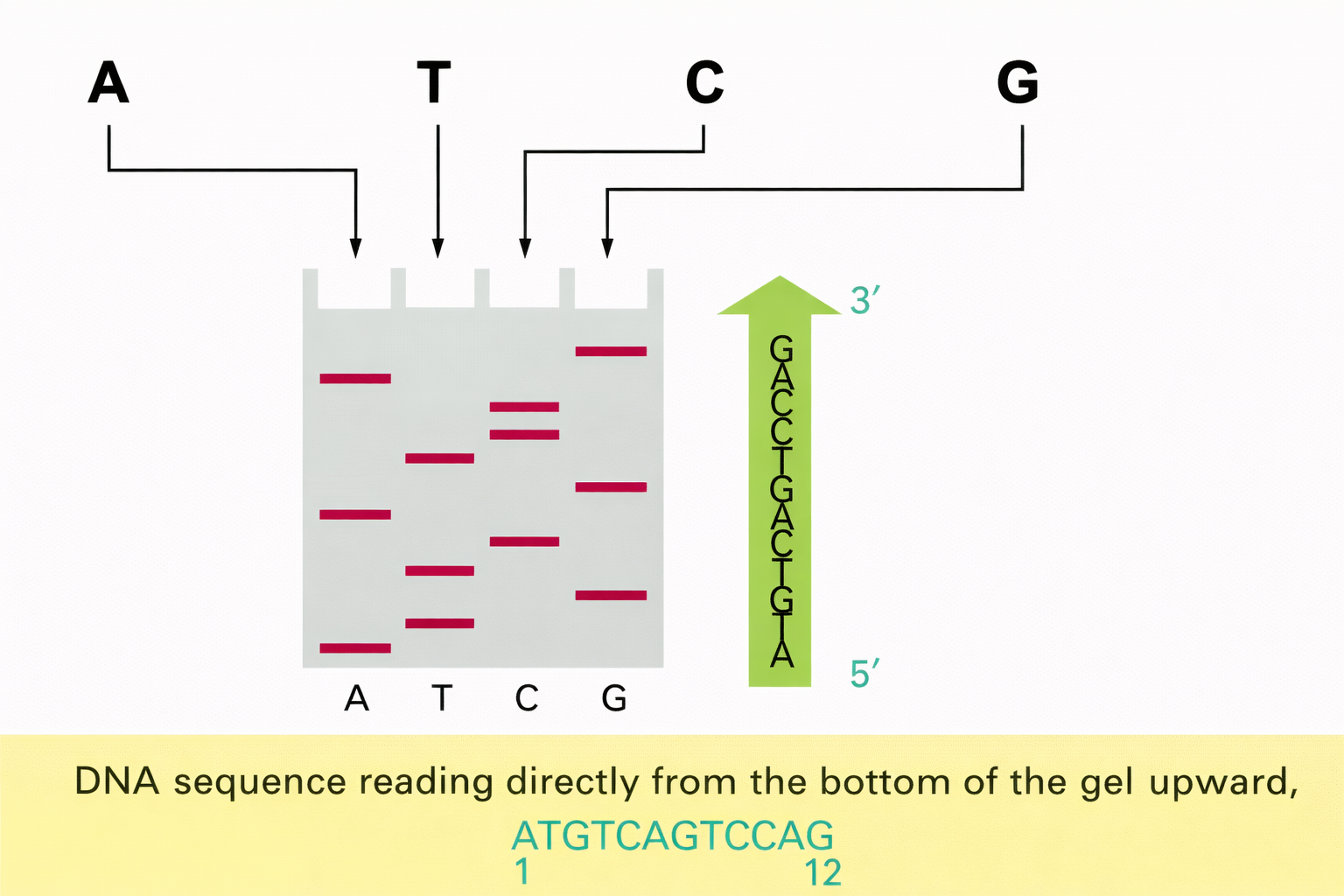
שאלה 2: ריאקציית Sanger - עקרון הריצוף
בריאקציית ריצוף Sanger מודרנית, כיצד מזהים באיזה נוקלאוטיד נעצרה כל שרשרת?
- ע”י פריימר מסומן פלואורסנטית, והצבע משתנה בהתאם לבסיס הבא בתבנית
- ע”י הרצה בארבע תעלות נפרדות (אחת לכל בסיס) ובניית הרצף לפי גובה הלהקות
- ע”י סימון פלואורסנטי שונה לכל ddNTP, כך שכל מקטע “מדווח” על הבסיס המסיים שלו בזמן המעבר בדטקטור
- ע”י מדידה ישירה של מסה מולקולרית לכל מקטע כדי להסיק איזה ddNTP שולב בסוף
פתרון
התשובה הנכונה היא (3).
מהשיעור (שקפים 7, 10):
השיטה שוכללה ע”י סמנים פלואורסנטיים בצבעים שונים לכל ddNTP:
- ddATP - צבע אחד
- ddTTP - צבע שני
- ddCTP - צבע שלישי
- ddGTP - צבע רביעי
לייזר + דטקטור סורקים את המקטעים בזמן שהם עוברים באלקטרופורזה ← כל מקטע שנעצר ב־ddNTP מסוים פולט צבע מתאים ← המחשב מתרגם את סדר הצבעים לרצף בסיסים.
בשיטה המקורית (לפני הצבעים) היו צריכים ארבע ריאקציות נפרדות וארבע שורות בג’ל.
מקור: שקפים 7, 10
שאלה 3: קריאת כרומטוגרמה
בריצוף Sanger אוטומטי, נקבל כרומטוגרמה עם פיקים בצבעים שונים. מה המשמעות כאשר סמוך לסוף הריאקציה מופיעים פיקים חופפים ולא ברורים?
- מדובר בהכרח בזיהום דגימה, ולכן יש למחוק את כל תוצאות הריצה
- איכות ההפרדה יורדת בסוף הקריאה, ולכן לעיתים הבסיס מסומן כ־N כאשר לא ניתן להכריע בין פיקים
- זה מעיד תמיד על הטרוזיגוטיות בבסיס האחרון שנקרא, גם אם אין פיקים כפולים לפני כן
- זו הוכחה שהפריימר נקשר באתר שגוי, ולכן אי אפשר לקבל שום קריאה אמינה מהריצה
פתרון
התשובה הנכונה היא (2).
מהשיעור (שקפים 13-14):
- בדרך כלל, ריאקציית Sanger מאפשרת קריאה ברורה של עד כ־600 בסיסים
- לקראת סוף הריאקציה, ההפרדה בין מקטעים שונים באורך דומה פוחתת ← הפיקים חופפים
- כאשר האנליזה לא ברורה (פיקים חופפים או עירבוב תוצרים) ← הנוקלאוטיד מסומן כ־N (נוקלאוטיד לא ברור)
זוהי מגבלה אינהרנטית של השיטה ולא בהכרח כשל טכני.
מקור: שקפים 13-14
שאלה 4: Capillary Electrophoresis מול ג’ל
מהם היתרונות של אלקטרופורזה קפילרית (CE) על פני ג’ל ריצוף מסורתי?
- CE מאפשרת הפרדה ברזולוציה גבוהה של מקטעים קצרים מאוד ולכן מפחיתה חפיפות פיקים, אך זמן הריצה דומה לג’ל ודורש כמויות DNA דומות
- CE מקצרת זמן ריצה ודורשת פחות DNA; הזיהוי נעשה בפלואורסנציה במקום צביעה בג’ל מסורתי
- CE זולה יותר מכל שיטה אחרת אך דורשת יותר DNA כדי לקבל אות יציב
- CE מאפשרת להריץ מספר גדול של דגימות באותו קפילר באותו זמן, כמו “מולטי־ליין” בג’ל
פתרון
התשובה הנכונה היא (2).
מהשיעור (שקף 12):
| מאפיין | CE (קפילרה) | ג’ל ריצוף |
|---|---|---|
| מספר דגימות | דגימה אחת בכל קפילרה | כמה דגימות יחד באותה הפרדה |
| משך זמן | דקות ספורות | מספר שעות |
| ריכוז DNA נדרש | ng בודדים | מיקרוגרמים |
| אופן הראיית DNA | פלואורסנציה | אתידיום ברומיד |
למרות שבכל קפילר בודד רצה דגימה אחת, מכשירים מודרניים מכילים עשרות קפילרות במקביל.
מקור: שקף 12
שאלה 5: וקטורים לספריות גנומיות
חוקרת רוצה לשבט מקטע DNA בגודל 200 Kb. איזה וקטור מתאים לה?
- BAC (טווח אופייני ~150–350 Kb), מתאים לשיבוט מקטעים גדולים בסדר גודל של מאות Kb
- קוסמיד (טווח אופייני ~35–45 Kb), מתאים למקטעים בינוניים אך לא למאות Kb
- פאג’ לאמדא (טווח אופייני ~20–25 Kb), שימושי לספריות קטנות יחסית
- פלסמיד רגיל (טווח אופייני ~5–20 Kb), נוח לעבודה אך מוגבל מאוד בגודל אינסרציה
פתרון
התשובה הנכונה היא (1).
מהשיעור (שקף 16):
| סוג הוקטור | גודל המקטע הממוצע (Kb) |
|---|---|
| פלסמיד | 20-5 |
| פאג’ לאמדא | 23 |
| קוסמיד | 45 |
| BAC | 350-150 |
| YAC | 1,000 |
מקטע בגודל 200 Kb גדול מדי לפלסמיד, פאג’ לאמדא או קוסמיד. BAC (כרומוזום חיידקי מלאכותי) יכול להכיל 350-150 Kb ולכן מתאים.
BACs שימשו תפקיד מרכזי בפרויקט הגנום האנושי - הגנום נחתך למקטעים של כ־150,000 בסיסים והוכנס ל־BACs.
מקור: שקפים 16, 33
שאלה 6: Chromosome Walking ו־Contigs
מהו Contig ומה תפקידו בריצוף גנומי?
- מקטע DNA קצר “מתויג” (STS) שמשמש נקודת עגינה ידועה להתקדמות לאורך כרומוזום
- קבוצת שכפולים (clones/reads) עם חפיפה שמורכבת לרצף רציף ארוך יותר ומשמשת לבניית רצף גנומי
- וקטור שיבוט גדול (כמו BAC/YAC) שנושא מקטעי גנום לשם ריצוף
- אנזים עזר שמאפשר ליגציה יעילה של מקטעים ליצירת ספריה גנומית
פתרון
התשובה הנכונה היא (2).
מהשיעור (שקפים 20-21):
Chromosome Walking: טכניקה שמייצרת סדרות של שכפולי DNA חופפים (overlapping clones) לחקר חלקים גדולים של DNA.
Contig = Group of clones representing overlapping regions of a genome.
השיטה מבוססת על Sequence-Tagged Sites (STS):
- רצפי DNA קצרים (200-500 bp) שמופיעים פעם אחת בגנום
- מיקומם ורצפם ידועים
- ניתן לתכנן מהם גלאים ולהתקדם בריצוף “צעד אחרי צעד” לאורך הכרומוזום
מדוע נחוצים שני אנזימי רסטריקציה? כדי לקבל חפיפה בין מקטעים - חיתוך בשני אנזימים שונים מייצר מקטעים שחופפים חלקית.
מקור: שקפים 22-20
שאלה 7: פרויקט הגנום האנושי - מטרות
איזו מהאפשרויות הבאות לא הייתה מטרה מוצהרת של פרויקט הגנום האנושי?
- בניית מאגרי מידע וכלים חישוביים לאחסון וניתוח רצפים בהיקף עצום
- זיהוי ומיפוי של גנים ורצפים בגנום האנושי לצד קבלת רצף ייחוס מלא
- פיתוח תרופות מותאמות אישית על בסיס מידע גנומי
- פענוח רצף הבסיסים של הגנום האנושי והנגשתו לקהילה המדעית
פתרון
התשובה הנכונה היא (3).
מהשיעור (שקפים 25-24):
פרויקט הגנום האנושי (2003-1990):
- מומן בעיקר ע”י NIH האמריקאי
- כ־18 מדינות סייעו (בישראל: מכון וייצמן ובי”ח הדסה)
- 15 שנה, 3 מיליארד דולר
המטרות המוצהרות:
- לפענח את רצף 3 מיליארד הבסיסים
- קבלת מיפוי (מיקום) של כל רצף
- לזהות את כלל הגנים בגנום (הערכה: 20,000)
- יצירת מאגר מידע מתאים
- שיפור כלים לאנליזת דאטא
פיתוח תרופות מותאמות אישית הוא יישום עתידי אפשרי (שקף 99), אך לא היה מטרה מוצהרת של הפרויקט עצמו.
מקור: שקפים 25-24, 99
שאלה 8: Whole Genome Shotgun Sequencing
מהו העיקרון של שיטת Shotgun Sequencing?
- התקדמות ליניארית לאורך כרומוזום באמצעות STS ו־“walking” בין שכפולים חופפים שנבחרו מראש
- פירוק אקראי של הגנום למקטעים רבים, ריצוף “reads” חופפים, והרכבת הרצף חישובית על בסיס חפיפות
- ריצוף של מקטעים ארוכים בלבד (≥150 Kb) כדי לצמצם בעיות חזרות ולבטל צורך באלגוריתמי הרכבה
- החדרה של כל הגנום לוקטור יחיד גדול, ריצופו ברצף, ואז חיתוך לתתי-רצפים לנוחות ניתוח
פתרון
התשובה הנכונה היא (2).
מהשיעור (שקפים 38-37):
Whole Genome Shotgun (WGS):
שלב 1: Make random clones - שבירת הגנום ליחידות של כ־200 בסיסים באופן אקראי וחופף (סוניקציה במקום אנזימי רסטריקציה).
שלב 2: Sequence each clone - ריצוף כל המקטעים.
שלב 3: Overlap sequence reads - חיבור לפי חפיפות ל־Contigs.
שלב 4: Overlap contigs for complete sequence - הרכבת הרצף המלא.
השיטה פותחה ע”י Craig Venter וחברת Celera (1998) - שטענו שיוכלו לרצף את הגנום מהר ובזול יותר. בפועל, Celera סיימה ב־3 שנים ו־300 מיליון דולר, לעומת 15 שנים ו־3 מיליארד דולר של הפרויקט הציבורי.
מקור: שקפים 38-37
שאלה 9: השוואת שיטות - Chromosome Walking מול Shotgun
מהו החיסרון המרכזי של שיטת ה־Shotgun ביחס לרצפי חזרות בגנום?
- רצפים חוזרים מונעים יצירת קצוות חופפים ולכן לא נוצרים contigs כלל
- רצפים חוזרים מקשים על Assembly כי “reads” מאזורים שונים נראים זהים ולכן קשה למקם אותם נכון
- אנזימי רסטריקציה אינם חותכים בתוך חזרות ולכן אי אפשר לפרק גנום עם חזרות למקטעים לריצוף
- רצפים חוזרים גורמים לעלייה בתוכן GC ולכן הפולימראז נתקע באלקטרופורזה הקפילרית
פתרון
התשובה הנכונה היא (2).
מהשיעור (שקף 42):
| מאפיין | Shotgun | Chromosome Walking |
|---|---|---|
| עבודת סידור מקדימה | אין כלל (סוניקציה של כל הגנום ללא סידור) | הרבה עבודת סידור וארגון לפני הריצוף |
| שימוש בידע קודם | כמעט ללא | נרחב - STS, גנים ידועים |
| מהירות | מהירה יחסית | איטית יחסית |
| כוח מחשוב | עצום | סביר |
| רצפי חזרות | מבלבלים מאוד - קשה למקם אותם נכון | קל יחסית למקם בגנום |
הבעיה: כשמקטעים רבים מאזורים שונים בגנום מכילים רצפים זהים (חזרות), האלגוריתם לא יכול להבחין מאיזה מיקום בגנום הם מגיעים ← Assembly שגוי.
מקור: שקפים 42-41
שאלה 10: הרכב הגנום האנושי
כמה אחוז מהגנום האנושי מקודד בפועל לחלבונים ו־RNA?
- כ־15% - רצפים לא־מקודדים ייחודיים שאינם חזרתיים
- כ־24% - אינטרונים שמצויים בתוך גנים אך אינם מתורגמים
- כ־1.5% - אקסונים שמקודדים לחלבון וגם גנים ל־rRNA/tRNA
- כ־59.5% - רצפים חזרתיים (כמו טרנספוזונים ואלמנטים חוזרים אחרים)
פתרון
התשובה הנכונה היא (3).
מהשיעור (שקפים 57, 59):
| רכיב | אחוז מהגנום |
|---|---|
| Exons (coding for protein, rRNA, tRNA) | 1.5% |
| Repetitive DNA | 59.5% |
| Introns | 24% |
| Unique noncoding DNA | 15% |
98.5% מהגנום הם רצפים לא־מקודדים! אלה מתחלקים לשני סוגים:
- רצפים שנמצאים בין גנים (intergenic)
- רצפים שמצויים בתוך גנים (כגון אינטרונים)
הגנום מכיל כ־20,000 גנים, מתוכם ידוע התפקיד של כ־80%.
מקור: שקפים 57, 59
שאלה 11: סוגי רצפי חזרות בגנום
מהם Microsatellites (STRs) וכיצד הם שונים מ־Minisatellites (VNTRs)?
- STRs הם חזרות של מאות בסיסים ($100–1,000\,\mathrm{bp}$); VNTRs הם חזרות של $13–100 \, \mathrm{bp}$ בלבד
- STRs הם חזרות קצרות מאוד (יחידת חזרה <13bp); VNTRs הם חזרות ארוכות יותר ($\approx 13–100 \, \mathrm{bp}$) במספר חזרות משתנה
- STRs ו־VNTRs זהים בגודל יחידת החזרה; ההבדל הוא רק אם הם נמצאים באקסונים או באינטרונים
- STRs נמצאים כמעט רק בכרומוזום X; VNTRs כמעט רק בכרומוזומים אוטוזומליים
פתרון
התשובה הנכונה היא (2).
מהשיעור (שקף 60):
| סוג חזרה | גודל יחידת חזרה | דוגמה |
|---|---|---|
| Microsatellites (STRs) | פחות מ־13 בסיסים | CA Repeats: CACACA… |
| Minisatellites (VNTRs) | 13-100 בסיסים | חזרות מסודרות “ראש לזנב”, 4-40 פעמים ברצף |
| Genome Wide Repeats | 100-1,000 בסיסים | LINEs, SINEs, טרנספוזונים |
- STR = Short Tandem Repeats
- VNTR = Variable Number of Tandem Repeats
מעל 50% מגנום האדם מורכב מרצפי חזרות שונים (יותר מששיערו). הסוגים כוללים טרנספוזונים, מיקרוסטליטים-STR, ומיניסטליטים.
מקור: שקף 60
שאלה 12: טרנספוזונים - סוגים ומנגנונים
מה ההבדל בין רטרוטרנספוזון (Class 1) לבין טרנספוזון DNA (Class 2)?
- רטרוטרנספוזון “Cut+Paste” ומשאיר אתר ריק; טרנספוזון DNA “Copy+Paste” ומגדיל עותקים
- רטרוטרנספוזון “Copy+Paste” דרך מתווך RNA ו־Reverse Transcription; טרנספוזון DNA “Cut+Paste” בעזרת טרנספוזאז
- שניהם “Copy+Paste”, אך רטרוטרנספוזון פועל רק באקסונים וטרנספוזון DNA רק באינטרונים
- שניהם “Cut+Paste”, אך ההבדל הוא רק בגודל הטרנספוזון ולא במנגנון
פתרון
התשובה הנכונה היא (2).
מהשיעור (שקפים 62, 67):
| מאפיין | Retrotransposon (Class 1) | DNA Transposon (Class 2) |
|---|---|---|
| מנגנון | Copy+Paste | Cut+Paste |
| תווך | RNA intermediate → Reverse Transcription → cDNA → Integration | DNA intermediate → Excision → Integration |
| אנזים מפתח | Reverse Transcriptase | Transposase |
| תוצאה | עותק חדש נוסף - מספר העותקים בגנום גדל | אותו עותק עובר מיקום - מספר העותקים לא משתנה |
טרנספוזונים:
- התגלו לראשונה בתירס (שם הם מהווים כ־90% מהגנום)
- כלי אבולוציוני חשוב
- ההשתלבות מחדש היא רנדומלית
- הטרנספוזאז חותך לפי רצפים חזרתיים הפוכים (Inverted Repeats) בקצוות הטרנספוזון
מקור: שקפים 62, 67, 69
שאלה 13: Reverse Transcriptase ושימושיו
מי משתמש באנזים Reverse Transcriptase באופן טבעי, ומדוע הוא חשוב במעבדה?
- חיידקים משתמשים בו ליצירת פלסמידים מ־RNA; במעבדה הוא משמש לריצוף Sanger
- רטרו־וירוסים ורטרוטרנספוזונים משתמשים בו ליצירת DNA מ־RNA; במעבדה משתמשים בו ליצירת cDNA ול־RT-PCR
- תאי גוף משתמשים בו בשכפול כרומוזומים; במעבדה הוא מחליף DNA פולימראז ב־PCR
- תאי גזע בלבד משתמשים בו לרגנרציה; במעבדה הוא משמש בעיקר לעריכת גנים בעוברים
פתרון
התשובה הנכונה היא (2).
מהשיעור (שקפים 63-64):
Reverse Transcriptase: אנזים שמשתמש בתבנית RNA כדי ליצור DNA.
שימוש טבעי: רטרו־וירוסים (כמו HIV) ורטרוטרנספוזונים.
שימושים במעבדה:
- יצירת cDNA מ־mRNA - הבסיס ללמוד על ביטוי גנים
- RT-PCR - למשל, בדיקות לזיהוי נגיף הקורונה (RNA virus → cDNA → PCR)
- בניית ספריות cDNA
מקור: שקפים 63-64
שאלה 14: cDNA מול DNA גנומי
מדוע cDNA שנוצר מ־mRNA שונה מה־DNA הגנומי המקורי?
- cDNA מכיל U במקום T ולכן רצפו שונה מה־DNA הגנומי
- cDNA משקף mRNA שעבר שחבור, ולכן הוא מורכב מאקסונים מחוברים ללא אינטרונים
- cDNA אינו יכול להפוך לדו־גדילי ולכן לא ניתן לבצע עליו PCR או שיבוט
- cDNA תמיד ארוך יותר כי הוא כולל את רצפי הפרומוטור ואת זנב ה־Poly-A
פתרון
התשובה הנכונה היא (2).
מהשיעור (שקף 65):
תהליך יצירת cDNA:
DNA (Intron 1 - Exon 1 - Intron 2 - Exon 2) → (RNA Polymerase) → mRNA (Exon 1 - Exon 2, ללא אינטרונים) → (Reverse Transcriptase + Primer 1) → cDNA (Exon 1 - Exon 2) → (DNA Polymerase + Primer A + Primer B) → שכפול
ה־cDNA שונה מה־DNA המקורי כי:
- ה־mRNA שימש כתבנית, וה־mRNA כבר עבר שחבור (splicing) → האינטרונים הוסרו
- לכן cDNA מכיל רק רצפי אקסונים מחוברים
- הוא קצר יותר מהרצף הגנומי המקורי
שאלה מהשיעור: האם אפשר לתכנן פריימר שיהפוך את כל רצפי ה־RNA ל־cDNA? כן - Oligo-dT primer נקשר לזנב ה־Poly-A של כל ה־mRNAs.
מקור: שקפים 65-66
שאלה 15: יצירת עכברי Knockout
מהו הסדר הנכון של השלבים ביצירת עכבר Knockout?
- הכלאה בין הורים מוטנטים ← סלקציה של צאצאים ← רקומבינציה בתאי מין ← החדרה לעובר
- החדרת DNA לתאי ES (לרוב באלקטרופורציה) ← רקומבינציה הומולוגית ← סלקציה באנטיביוטיקה ← החדרה לעובר ← יצירת עכבר כימרי
- עריכת הגן בעזרת אנזימי רסטריקציה ← ליגציה של גן עמידות ← הזרקה ישירה לעובר ← כימרה
- מיפוי הגן ← מחיקה כימית של האקסונים ← שכפול במבחנה ← השתלה בביצית ← לידה
פתרון
התשובה הנכונה היא (2).
מהשיעור (שקפים 75-77):
| שלב | תיאור |
|---|---|
| 1 | מחדירים בשוק חשמלי (Electroporation) לתא עוברי מקטע DNA מתאים לרקומבינציה המכיל גן עמידות לאנטיביוטיקה |
| 2 | במידה ומתרחשת רקומבינציה הומולוגית - מוחלף הגן התקין בעמידות לאנטיביוטיקה |
| 3 | מגדלים על מצע עם אנטיביוטיקה - סלקציה לתאים שעברו רקומבינציה |
| 4 | מחדירים בחזרה לעובר מתפתח ← נוצר עכבר כימרי (חלק מתאיו לא מבטאים את הגן) |
| 5 | אם תאי מין של הכימרי נושאים את החסר ← דור ראשון הטרוזיגוטי |
| 6 | הכלאה בין הטרוזיגוטים ← הומוזיגוט למוטציה (Knockout מלא) |
מקור: שקפים 76-77
שאלה 16: P-element בדרוזופילה
כיצד מופרד מערכת ה־P-element לשני חלקים כדי לאפשר שליטה בהכנסת גן זר?
- חותכים את ה־P-element לשני חצאים שווים כדי למנוע אינטגרציה לא מבוקרת
- מקודדים טרנספוזאז בנפרד ללא רצפי ההכרה, ומשאירים את רצפי ההכרה + גן מדווח על P-plasmid; טרנספוזיציה מתרחשת רק כששניהם יחד
- מפרידים את הפרומוטור מהגן הזר כדי לשלוט בביטוי לאחר אינטגרציה
- משתיקים את הטרנספוזאז ע”י RNAi ומפעילים אותו רק לאחר שהגן כבר השתלב בגנום
פתרון
התשובה הנכונה היא (2).
מהשיעור (שקפים 79-80):
ה־P-element מכיל במקור: טרנספוזאז + אזורי הכרה לחיתוך משני הצדדים.
ההפרדה המבוקרת:
| רכיב | תוכן | לבד |
|---|---|---|
| DNA המקודד לטרנספוזאז | אנזים טרנספוזאז בלי רצפי הכרה | לא פעיל - אין לו מה לחתוך |
| P-plasmid | גן מדווח (למשל עיניים אדומות) + אזורי קישור לטרנספוזאז | לא פעיל - אין אנזים שיחתוך |
רק כאשר שניהם יחד (כתוצאה מהכלאה) ← הטרנספוזאז מזהה את אזורי ההכרה ב־P-plasmid ← חותך ומשתלב בגנום ← הגן הזר (מדווח) נכנס לגנום.
לאן צריך להכניס? לתאי נבט (Germ line) - כדי שהשינוי יעבור לכל תאי הדור הבא.
מקור: שקפים 79-82
שאלה 17: Inverse PCR - זיהוי מיקום הטרנספוזון
כיצד מזהים היכן בגנום הוכנס ה־P-element?
- מזהים את מקום ההכנסה לפי רמת הביטוי של הגן המדווח ב־Western blot
- מבצעים Southern blot עם גלאים לכל כרומוזום כדי לראות באיזה כרומוזום יש להקה חזקה יותר
- חותכים DNA באנזים שחותך גם בתוך הטרנספוזון, מבצעים ליגציה עצמית למעגלים, עושים PCR עם פריימרים הפונים החוצה מתוך הטרנספוזון, ואז מרצפים את התוצר
- מרצפים את כל הגנום ב־NGS ומחפשים בדיעבד את רצף ה־P-element בכל ה־reads
פתרון
התשובה הנכונה היא (3).
מהשיעור (שקף 83):
שיטת Inverse PCR:
| שלב | פעולה |
|---|---|
| 1 | חיתוך כלל ה־DNA עם אנזים רסטריקציה שידוע כי הוא חותך גם בתוך הטרנספוזון |
| 2 | ליגציה עצמית - המקטעים החתוכים נסגרים למעגלים (פלסמידים) |
| 3 | PCR עם פריימרים בתוך הטרנספוזון בכיוונים מנוגדים ← מגבירים את הרצף הגנומי הסמוך לטרנספוזון |
| 4 | ריצוף התוצר ← פיענוח הרצף הסמוך לטרנספוזון ← זיהוי מיקום ההשתלבות בגנום |
העיקרון: אנחנו יודעים את הרצף של מה שהכנסנו (הטרנספוזון) ← ממנו “הולכים” החוצה כדי לגלות מה נמצא לידו בגנום.
מקור: שקף 83
שאלה 18: NGS - Bridge Amplification
מדוע נדרש שלב של Bridge Amplification לפני הריצוף בשיטת Illumina?
- כדי להוסיף אדפטורים דו־צדדיים למקטעים לפני הקשירה לפלטפורמה
- כדי להגדיל את מספר העותקים בכל אתר על ה־flow cell ולייצר אות פלואורסנטי חזק מספיק לקריאה במהלך הריצוף
- כדי למיין את מקטעי ה־DNA לפי אורך, כך שכל cluster יכיל מקטעים באותו גודל
- כדי לתקן שגיאות שנוצרו בסוניקציה באמצעות אנזימי proofreading לפני תחילת הריצוף
פתרון
התשובה הנכונה היא (2).
מהשיעור (שקפים 89-92):
שלושת שלבי ה־NGS:
| שלב | תיאור |
|---|---|
| 1. בניית ספריה | שבירת DNA למקטעים קצרים (סוניקציה) + הוספת אדפטורים |
| 2. קישור ושיכפול | קשירת מקטעים לפלטפורמה ← Bridge Amplification |
| 3. ריצוף | Illumina / SOLiD / 454 / Ion Torrent |
Bridge Amplification:
- מקטעי DNA נקשרים לפלטפורמה (Flow Cell) דרך האדפטורים
- סינתזת גדילים משלימים ע”י DNA פולימראז (בדומה ל־PCR)
- הנוקלאוטידים בשלב זה אינם פלואורוסנטיים
- מכל מקטע DNA התחלתי נוצר צבר של מאות-אלפי עותקים זהים
המטרה: מולקולה בודדת פולטת סיגנל חלש מדי לזיהוי ← צבר של עותקים זהים מייצר סיגנל חזק ומדיד.
מקור: שקפים 91-92
שאלה 19: GWAS ותוצאות 1000 Genomes
על פי תוצאות פרויקט 1000 Genomes, כמה וריאנטים הגורמים לאובדן תפקוד (loss-of-function) נושא כל אדם בממוצע?
- כ־50–100 וריאנטים
- כ־5–10 וריאנטים
- כ־250–300 וריאנטים
- כ־1,000–2,000 וריאנטים
פתרון
התשובה הנכונה היא (3).
מהשיעור (שקף 98):
ממצאי פרויקט 1000 Genomes (פורסם ב־Nature, 2012):
| ממצא | נתון |
|---|---|
| Loss-of-function variants | כל אדם נושא כ־250-300 וריאנטים באנוטציית גנים |
| וריאנטים הקשורים למחלות תורשתיות | כל אדם נושא כ־50-100 וריאנטים שזוהו בעבר כקשורים למחלות |
| קצב מוטציות de novo | ~10⁻⁸ לבסיס לדור |
בנוסף, מחקרי GWAS זיהו כ־2,000 לוקוסים באדם שיש להם השפעה על למעלה מ־300 מחלות.
דוגמה מהשיעור: גן FTO - SNP (שינוי בין C ל־T) באינטרון הראשון שמראה קשר מובהק לעלייה במשקל - הלוקוס עם ההשפעה המשמעותית ביותר על השמנה ו־BMI.
מקור: שקפים 85-86, 98
שאלה 20: גנומיקה השוואתית ואבולוציה
הזהות בגנום בין אדם לשימפנזה היא 99.4%, ובכל זאת הם שונים מאוד פנוטיפית. מהו ההסבר העיקרי?
- השימפנזה מכיל מספר גדול של גנים שאין לאדם ולכן ההבדל הוא בעיקר בכמות הגנים
- ההבדלים נובעים בעיקר מהבדלים במספר הכרומוזומים ולא מתכנים גנטיים אחרים
- מרבית ההבדלים המשמעותיים הם ברגולציה של ביטוי גנים (מתי/איפה/כמה), ולא רק בשינויי רצף באקסונים
- ההבדלים הם כמעט רק תוצאה של גורמים סביבתיים; ברמה המולקולרית אין פערי תפקוד
פתרון
התשובה הנכונה היא (3).
מהשיעור (שקף 111):
“גנים הם לא הכל…”
| השוואה | זהות בגנום |
|---|---|
| אדם לאדם | 99.8% |
| אדם לשימפנזה | 99.4% |
| אדם לעכבר | 80% |
המסקנה: “יש חשיבות עצומה לבקרת ביטוי הגנים” - ההבדלים הפנוטיפיים העצומים בין מינים קרובים נובעים בעיקר משינויים ברגולציה של ביטוי גנים: פרומוטורים, אינהנסרים, מתילציה, ומנגנוני בקרה אחרים.
תהליכים המשפיעים על שינויים אבולוציוניים בגנום (שקף 102): מוטציות, הרחבת רצפים חזרתיים, הכפלת גנים, איבוד תפקוד גנים.
שימושי גנומיקה השוואתית: גילוי מקור פתוגנים חדשים, הבנת תהליכי נדידה וסלקציה, למידה על העבר. דוגמה: ריצוף DNA מיטוכונדריאלי הראה שהפנדה האדומה דומה יותר לדביבון מאשר לדוב פנדה.
מקור: שקפים 102-103, 109-111