הערה: מומלץ להתמקד בחלק השני של הסיכום, שעורך בצורה טובה יותר ורלוונטי יותר למבחן ולתרגילים. החלק השני מתמקד בתמיסות, מסיסות, תכונות קוליגטיביות, לחץ אוסמוטי, לחץ אדים חלקי, שינויים בנקודת קיפאון וכיו”ב. החלק הנוכחי עוסק בכוחות באופן כללי, מצבי חומר, משוואת קלאוזיוס-קלפרון, נקודת רתיחה, דיאגרמת פאזות ומוצקים.
תוכן עניינים:
- כוחות בין־מולקולריים
- כוחות ואן דר ואלס וקשרי מימן
- חום אידוי ולחץ אדים
- נקודת רתיחה
- משוואת קלאוזיוס-קלפרון
- שאלה לדוגמה - קביעת מצב המים בכלי סגור
- דיאגרמת פאזות
- תמיסות ותכונות קוליגטיביות
- תכונות חומרים מוצקים
כוחות בין־מולקולריים
תופעות וכוחות בין־מולקולריים ממלאים תפקיד משמעותי בעולם הפיזיקלי והכימי. בעוד שקשרים בתוך מולקולה נלמדו קודם לכן, מולקולות אינן קיימות בבידוד - הן יוצרות אינטראקציה זו עם זו, דבר שמוביל לתופעות כמו מתח פנים, קוהזיה ואדהזיה.
מתח פנים
מתח פנים הוא הכוח שמפעילות מולקולות פני השטח של נוזל זו על זו, וכתוצאה ממנו מתקבל משטח נוזל “חזק” יחסית. תופעה זו מאפשרת:
- לחרקים כמו יתושים ופרפרים “ללכת” על פני המים.
- למחט לשקוע פחות מהצפוי על פני המים, אם משקלה קטן ממתח הפנים של הנוזל.
מתח הפנים נובע מכך שמולקולות פני השטח חוות כוחות לא מאוזנים, בעוד מולקולות בתוך הנוזל מאוזנות מכל הכיוונים.
כוחות קוהזיה ואדהזיה
- כוחות קוהזיה (cohesion): כוחות הפועלים בין מולקולות מאותו הסוג, לדוגמה בין מולקולות מים או אלכוהול.
- כוחות אדהזיה (adhesion): כוחות הפועלים בין מולקולות של נוזל למשטח, לדוגמה מים הנצמדים לזכוכית או לסיליקה, אך אינם מרטיבים משטחי טפלון.
כוחות אלו מסבירים תופעות כמו עלייה קפילרית של מים בצמחים: בשורשי העצים, המים נצמדים לסיליקה (adhesion) ומטפסים במעלה צינורות דקים (קפילרות) בעץ.
התאדות ומתח פנים
מולקולות שעל פני השטח של נוזל נוטות להתאדות, מכיוון שהן חוות כוחות לא מאוזנים. ההתאדות מתגברת כאשר:
- שטח הפנים של הנוזל גדול יותר (למשל, צלחת רחבה לעומת בקבוק צר).
- הטמפרטורה עולה, מה שמגביר את האנרגיה הקינטית של המולקולות.
שימושים ותופעות
הבנת כוחות בין־מולקולריים חשובה בהקשרים רבים:
- בתעשייה: שיפור תהליכי אידוי וייצור חומרים בעלי תכונות אדהזיה וקוהזיה מתאימות.
- בטבע: תנועת מים בצמחים וגיבוש מבנים יציבים כמו קורי עכביש.
- במדע: פיתוח טכנולוגיות חדשות המנצלות את תכונות מתח הפנים.
כוחות ואן דר ואלס וקשרי מימן
האינטראקציה בין מולקולות מכונה בכללותה “כוחות ואן דר ואלס”, על שם הכימאי ההולנדי שגילה אותם ואף כתב את משוואת הגזים הלא־אידיאליים.
כוחות ואן דר ואלס
- כוחות דיפול־דיפול: אינטראקציות בין מולקולות פולריות בעלות דיפול קבוע, כמו $\ce{HCl}$.
- כוחות לונדון (London Dispersion Forces): אינטראקציות בין מולקולות לא־פולריות הנוצרות מדיפול רגעי כתוצאה מתנודות בענן האלקטרונים, כמו בגזים אצילים.
לדוגמה, למולקולות $\ce{N2}$ ו־$\ce{O2}$ אין דיפול קבוע, אך ניתן להמיר אותן לנוזל בזכות כוחות לונדון. ככל שהמולקולה כבדה יותר, כוחות אלו חזקים יותר ונקודת הרתיחה גבוהה יותר - הליום ($\ce{He}$) רותח ב־$4 \, \mathrm{K}$, לעומת רדון ($\ce{Rn}$) שרותח ב־$211 \, \mathrm{K}$.
מולקולות לינאריות בעלות שטח פנים גדול יותר יוצרות אינטראקציות חזקות יותר לעומת מולקולות דחוסות/כדוריות.
קשרי מימן
קשרי מימן נוצרים כאשר אטום מימן קשור לאטום אלקטרושלילי מאוד: חמצן ($\ce{O}$), חנקן ($\ce{N}$) או פלואור ($\ce{F}$). הם חזקים יותר מכוחות ואן דר ואלס ואחראים לתכונות ייחודיות:
- מים ($\ce{H2O}$): נקודת רתיחה גבוהה, מתח פנים חזק, התאדות איטית.
- DNA: קשרי מימן מחזיקים את שני הגדילים ומאפשרים שכפול גמיש.
- אמוניה ($\ce{NH3}$) וחומצה פלואורית ($\ce{HF}$): צמיגות גבוהה ותכונות ייחודיות.
- חומצה אצטית ($\ce{CH3COOH}$): קשרי מימן בין קבוצות קרבוקסיליות קובעים צמיגות ויכולת המסה.
חום אידוי ולחץ אדים
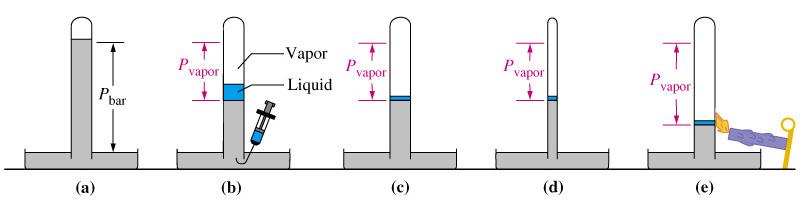
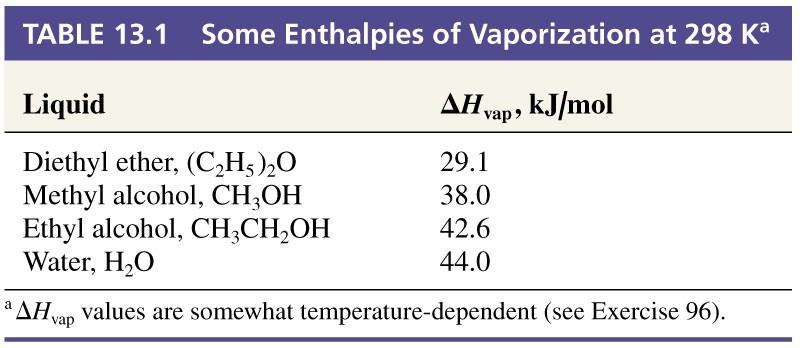
חום אידוי
חום האידוי ($\Delta H_{\text{vap}}$) הוא האנרגיה הדרושה להעברת חומר ממצב נוזלי למצב גזי. עבור מים, $\Delta H_{\text{vap}} \approx 44\ \text{kJ/mol}$.
כאשר נוזל נמצא בכלי פתוח, מולקולות מתאדות מהנוזל ונוצר שיווי משקל, שבו חלק מהמולקולות חוזרות לנוזל וחלק נשארות בגז. הלחץ שמפעילות המולקולות הגזיות על דפנות הכלי נקרא לחץ האדים.
לחץ אדים
לחץ האדים הוא הלחץ שמפעילות המולקולות הנפלטות מנוזל אל מרחב הגז שמעליו. כל נוזל בטמפרטורה נתונה מפעיל לחץ אדים ייחודי לו.
לדוגמה:
- אצטון, שמולקולותיו מחוברות בכוחות חלשים יותר, יפעיל לחץ אדים גבוה יותר ויתנדף מהר יותר.
- מים, בעלי קשרי מימן חזקים, יפעילו לחץ אדים נמוך יחסית.
- שמן, שבו הכוחות בין המולקולות חזקים מאוד, יפעיל לחץ אדים נמוך ביותר.
בכלי סגור, הנוזל מגיע לשיווי משקל דינמי: מולקולות עוברות בין נוזל לגז באותו קצב, עד שלחץ האדים מתייצב - הלחץ בשיווי משקל תלוי אך ורק בטמפרטורה.
לחץ אדים בחיי היומיום
לחץ אדים משחק תפקיד במוצרים יומיומיים, כמו בשמים. בשמים מתוכננים כך שיתנדפו לאט, ולכן כוללים חומרים בעלי לחץ אדים גבוה לצד חומרים שמאטים את ההתנדפות (כמו שמנים).
לחץ האדים רלוונטי גם לזיהוי חומרים באמצעות חוש הריח. לדוגמה:
- קוקאין והרואין מתאפיינים בלחץ אדים נמוך מאוד, ולכן אינם ניתנים לזיהוי על ידי בני אדם, אך כלבים עם רגישות ריח גבוהה יכולים לזהותם.
- מבריחים מנסים לטשטש את הלחץ על ידי ערבוב עם חומרים בעלי לחץ אדים גבוה, כמו קפה, אך כלבים מאומנים מתגברים על כך.
לחץ אדים ונקודת רתיחה
לחץ האדים של נוזל עולה עם הטמפרטורה, ומגיע ללחץ אטמוספרי ($760\ \text{mmHg}$) בנקודת הרתיחה שלו:
- דיאתיל אתר רותח ב־$34^\circ\text{C}$, כיוון שלחץ האדים שלו מגיע ל־1 atm בטמפרטורה נמוכה יחסית.
- אתנול רותח ב־$78^\circ\text{C}$.
- מים רותחים רק ב־$100^\circ\text{C}$.
נקודת רתיחה
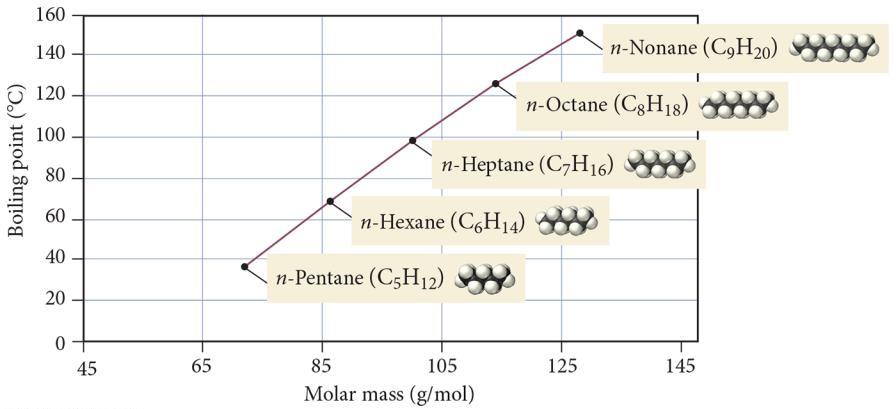
נקודת הרתיחה של חומר מוגדרת כנקודה שבה לחץ האדים של הנוזל שווה ללחץ האטמוספרי. עבור מים, נקודת הרתיחה היא $100^\circ\text{C}$ בלחץ של $760 \, \mathrm{mmHg}$.
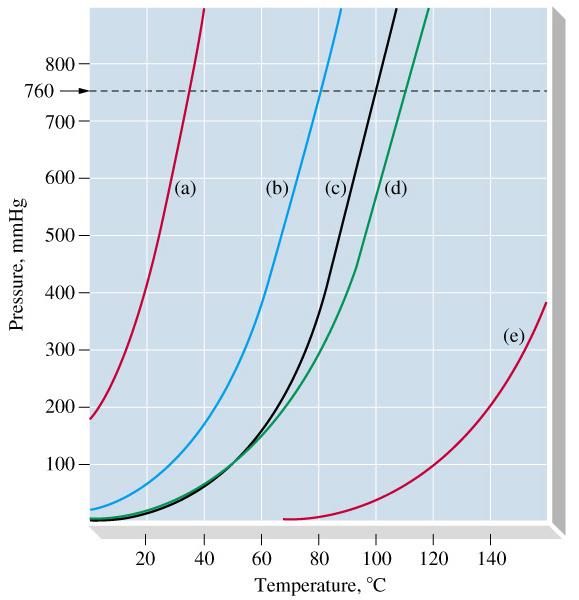
Vapor pressure curves of several liquids:
- (a) Diethyl ether, $\ce{(CH3CH2)2O}$;
- (b) benzene, $\ce{C6H6}$;
- (c) water, $\ce{H2O}$;
- (d) toluene, $\ce{C6H5CH3}$;
- (e) aniline, $\ce{C6H5NH2}$.
The normal boiling points are the temperatures at the intersection of the dashed line at P = 760 mmHg with the vapor pressure curves.
גורמים המשפיעים על נקודת הרתיחה
1. אורך השרשרת הפחמנית:
ככל שהשרשרת ארוכה יותר, יש יותר שטחי מגע בין מולקולות ואינטראקציות חזקות יותר:
| חומר | נקודת רתיחה |
|---|---|
| $n$-פנטאן | $36^\circ\text{C}$ |
| $n$-הפטאן | $98^\circ\text{C}$ |
| $n$-דקאן | $174^\circ\text{C}$ |
2. מבנה המולקולה:
מולקולות לינאריות יוצרות יותר אינטראקציות ממולקולות קומפקטיות/כדוריות. לדוגמה, $n$-פנטאן רותח בטמפרטורה גבוהה יותר מאיזו־פנטאן, ומבנים כדוריים מצמצמים את שטח המגע בין מולקולות ומובילים לנקודות רתיחה נמוכות יותר.
3. סוג הכוחות הבין־מולקולריים:
- כוחות ואן דר ואלס: חלשים יחסית, מתעצמים עם המסה המולקולרית.
- דיפול־דיפול: בין מולקולות קוטביות.
- קשרי מימן: חזקים ביותר, בנוכחות $\ce{O}$, $\ce{N}$, $\ce{F}$.
סובלימציה
סובלימציה היא מעבר ישיר ממוצק לגז ללא שלב נוזלי. דוגמה מפורסמת היא יוד, שמתאדה ישירות בחימום. לפי חוק הס:
\[\Delta H_{\text{sublimation}} = \Delta H_{\text{fusion}} + \Delta H_{\text{vap}}\]משוואת קלאוזיוס-קלפרון
כאשר אין טבלה, ניתן לחשב לחץ אדים באמצעות משוואת קלאוזיוס-קלפרון:
\[\ln\!\left(\frac{P_1}{P_2}\right) = \frac{\Delta H_{\text{vap}}}{R} \left(\frac{1}{T_2} - \frac{1}{T_1}\right)\]כאשר:
- $P_1,\ P_2$ - לחצי האדים בשתי טמפרטורות שונות.
- $\Delta H_{\text{vap}}$ - אנתלפיית האידוי.
- $R = 8.314\ \text{J·mol}^{-1}\text{·K}^{-1}$ - קבוע הגזים האידיאליים.
- $T_1,\ T_2$ - הטמפרטורות בקלווין.
צורה לינארית: ציור $\ln P$ כנגד $\frac{1}{T}$ נותן קו ישר, ששיפועו שווה $-\dfrac{\Delta H_{\text{vap}}}{R}$:
\[\ln P = -A\left(\frac{1}{T}\right) + B\] \[\ln \frac{P_2}{P_1} = -\frac{\Delta H_{\text{vap}}}{R} \left( \frac{1}{T_1} - \frac{1}{T_2} \right)\]שיטה נפוצה: משתמשים בנקודת הרתיחה הידועה ($P = 760\ \text{mmHg}$, $T = T_b$) כנקודת ייחוס ומוצאים לחץ אדים בכל טמפרטורה אחרת. ניתן למצוא בדרך זו גם את $\Delta H_{\text{vap}}$ מהשיפוע של הגרף.
דוגמה - חישוב לחץ אדים של מים ב־$35^\circ\text{C}$
נתונים:
- $P_1 = ?$, $T_1 = 35.0^\circ\text{C} = 308.3\ \text{K}$
- מטבלה: $T_2 = 40^\circ\text{C} = 313\ \text{K}$, $P_2 = 55.3\ \text{mmHg}$
- $\Delta H_{\text{vap}} = 44.0\ \text{kJ/mol}$
- $R = 8.3145\ \text{J·mol}^{-1}\text{·K}^{-1}$
התוצאה הגיונית: ב־$35^\circ\text{C}$ לחץ האדים נמוך יותר מב־$40^\circ\text{C}$ ($55.3\ \text{mmHg}$), בהתאם לכלל שלחץ האדים יורד עם ירידת הטמפרטורה.
שאלה לדוגמה - קביעת מצב המים בכלי סגור
נתונים: $0.132\ \text{g}$ מים, טמפרטורה $50^\circ\text{C}$, נפח כלי $5.2\ \text{L}$. שאלה: בשיווי משקל, האם המים יהיו: אדים בלבד, נוזל בלבד, או שיווי משקל בין נוזל וגז?
שלב 1 - נפח נוזלי:
צפיפות מים היא $1\ \text{g/mL}$, ולכן:
\[V_{\text{liquid}} = \frac{0.132\ \text{g}}{1\ \text{g/mL}} = 0.132\ \text{mL}\]שלב 2 - לחץ אם כל המים יהפכו לאדים:
\[n = \frac{0.132}{18} = 0.00733\ \text{mol}\]נציב $R = 0.0821\ \text{L·atm/(mol·K)}$ ו־$T = 50^\circ\text{C} = 323\ \text{K}$:
\[P = \frac{nRT}{V} = \frac{(0.00733)(0.0821)(323)}{5.2} = 0.037\ \text{atm}\]נמיר ללחץ כספית:
\[P = 0.037\ \text{atm} \times 760\ \frac{\text{mmHg}}{\text{atm}} = 281\ \text{mmHg}\]שלב 3 - השוואה ללחץ האדים של מים ב־$50^\circ\text{C}$:
לפי הטבלה, לחץ האדים של מים ב־$50^\circ\text{C}$ הוא $92.5\ \text{mmHg}$.
הלחץ המחושב ($281\ \text{mmHg}$) גדול בהרבה מלחץ האדים ($92.5\ \text{mmHg}$).
מסקנה: המערכת תגיע לשיווי משקל בין נוזל וגז - חלק מהמולקולות יישארו כנוזל, והאדים יפעילו לחץ של $92.5\ \text{mmHg}$.
בשיווי המשקל, מתקיים מעבר דינמי מתמיד: מולקולות עוברות מנוזל לגז ולהפך באותו קצב. הלחץ יהיה $92.5\ \text{mmHg}$ והיתרה תישאר בנוזל.
כלל:
- לחץ מחושב < לחץ אדים → כל המים באדים.
- לחץ מחושב > לחץ אדים → שיווי משקל בין נוזל וגז.
דיאגרמת פאזות
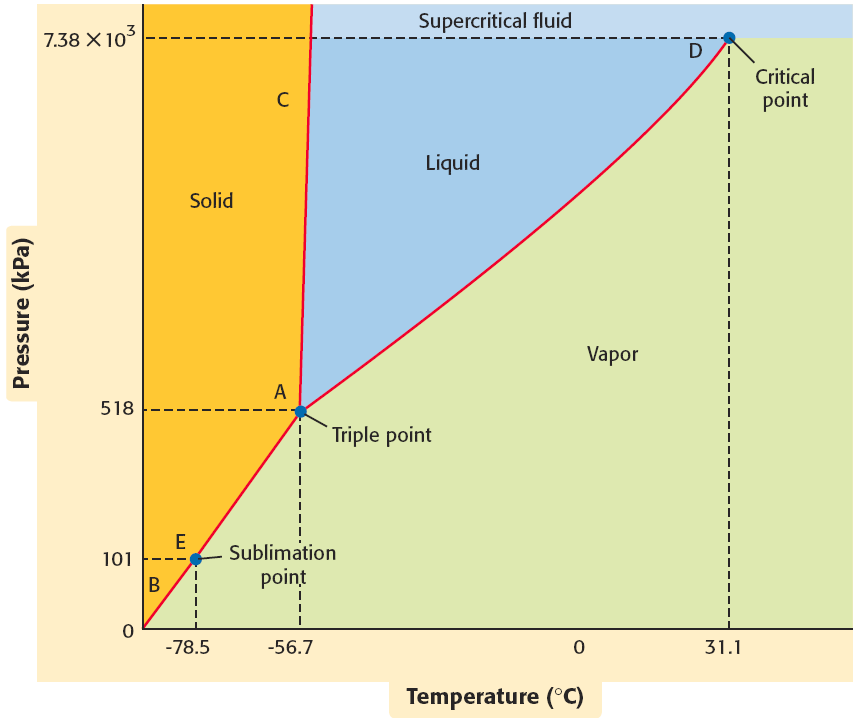
דיאגרמת פאזות היא ייצוג גרפי של מצבי הצבירה (מוצק, נוזל, גז) כפונקציה של טמפרטורה ולחץ.
רכיבים עיקריים
- נקודה משולשת: החומר נמצא בו־זמנית בשלושת הפאזות.
- נקודה קריטית: הנקודה שבה מתקיים מצב סופר־קריטי - החומר אינו נוזל ואינו גז אלא שילוב של שניהם.
- קווי שיווי משקל:
- קו מוצק-נוזל (קו ההתכה).
- קו נוזל־גז (קו האידוי - מתואר על־ידי משוואת קלאוזיוס-קלפרון).
- קו מוצק-גז (קו הסובלימציה).
מעברי פאזות
| מעבר | כיוון |
|---|---|
| Melting | מוצק ← נוזל |
| Vaporization | נוזל ← גז |
| Sublimation | מוצק ← גז |
| Freezing | נוזל ← מוצק |
| Condensation | גז ← נוזל |
| Deposition | גז ← מוצק |
מושגים נוספים
- איזותרמה: קו שבו הטמפרטורה קבועה והלחץ משתנה.
- איזוברה: קו שבו הלחץ קבוע והטמפרטורה משתנה.
דוגמאות
- $\ce{CO2}$: הנקודה המשולשת נמצאת ב־$-56.7^\circ\text{C}$ ו־$518 \, \mathrm{kPa}$. $\ce{CO2}$ במצב סופר־קריטי משמש למיצוי קפאין מקפה תוך שמירה על ארומה וטעם.
- מים: הדיאגרמה כוללת מצבי קרח שונים (Ice VI, Ice IX וכו’) בהתאם ללחץ ולטמפרטורה.
תמיסות ותכונות קוליגטיביות
תמיסה אידיאלית
בתמיסה אידיאלית, ערבוב $5 \, \mathrm{mL} + 5 \, \mathrm{mL}$ נותן בדיוק $10 \, \mathrm{mL}$. אם מתקבל פחות או יותר מ־$10 \, \mathrm{mL}$, התמיסה אינה אידיאלית. תמיסות אידיאליות נוצרות כאשר שני החומרים דומים במבנה, כך שהמשיכה הבין־מולקולרית דומה בין החומרים לבין עצמם ובין החומרים השונים.
לחץ אוסמוטי
\[\Pi = MRT\]כאשר:
- $\Pi$ - הלחץ האוסמוטי.
- $M$ - מולריות המומס.
- $R$ - קבוע הגזים.
- $T$ - טמפרטורה בקלווין.
במערכות ביולוגיות, הלחץ האוסמוטי משפיע על זרימת מים בין תאים לסביבה החיצונית.
תכונות קוליגטיביות
תכונות קוליגטיביות תלויות אך ורק בכמות המומס, לא באופיו. דוגמאות:
- הורדת נקודת קיפאון.
- העלאת נקודת רתיחה.
- שינוי לחץ אדים.
הורדת נקודת קיפאון (לדוגמה, מניעת קיפאון מים על ידי הוספת מלח):
\[\Delta T_f = -i \cdot K_f \cdot m\]כאשר:
- $\Delta T_f$ - שינוי נקודת הקיפאון.
- $i$ - פקטור ואן-הוף (מספר היונים שנוצרים).
- $K_f$ - קבוע קריוסקופי.
- $m$ - מולליות (mol/kg ממס).
חשוב לדעת לחשב
- לחץ אוסמוטי.
- הורדת נקודת קיפאון.
- העלאת נקודת רתיחה.
יישומים מעשיים
- זיקוק לשברים: הפרדת תערובות (כמו נפט) על בסיס הבדלי לחץ אדים.
- התפלת מים: אוסמוזה הפוכה - שימוש בלחץ להעברת מים דרך ממברנה המסננת מלחים ומומסים.
תכונות חומרים מוצקים
מבנה גבישי
מוצקים מסודרים במבנים מחזוריים ברורים. לדוגמה:
- יהלום: מבנה תלת־ממדי של $\ce{C}$ בקשרים קוולנטיים ($sp^3$), חוזק רב.
- גרפיט: שכבות $\ce{C}$ מישוריות ($sp^2$), קשרים חלשים בין שכבות - מתאים כחומר כתיבה.
גרפיט יציב יותר מיהלום תרמודינמית, אך מעבר מיהלום לגרפיט דורש תנאים מיוחדים.
כואזי-קריסטלים
תגליתו של דן שכטמן הציגה גבישים שאינם מחזוריים באופן מושלם אך מציגים סדר מרחבי ייחודי - כואזי-קריסטלים - שאתגרו את ההגדרות הקלאסיות של גבישים.
דור פסקל