תוכן העניינים:
- פתיחה: מהי שבירת סימטריה?
- התפתחות דטרמיניסטית לעומת התפתחות רגולטיבית
- התפתחות סטוכסטית לעומת התפתחות פרובביליסטית
- צירי העובר ומישורי החלוקה
- Cell lineage analysis: ניתוח שושלת תאים
- האם שני הבלסטומרים הראשונים זהים?
- יצירת תאומים מונוזיגוטיים בעכבר
- מבחן השרשה: למה קשה להסיק ממנו?
- Outgrowth assay: בדיקת הפוטנציאל של הבלסטומרים בתרבית
- Oct4-GFP ומספר תאי אפיבלסט
- תאומים מונוזיגוטיים באדם ו־ART
- איך נוצרים תאומים מונוזיגוטים באדם
- ארמדילו: תאומים מונוזיגוטיים כתהליך לא אקראי
- שלב ארבעת התאים: סוגי עוברים ומישורי חלוקה
- ניסוי כימרות מבלסטומרים בשלב ארבעת התאים
- אצטילציה, מתילציה וקוד אפיגנטי
- H3R26me ו־Carm1
- Long non-coding RNAs ו־LincGET
- המודל: LincGET, Carm1, Sox2/Nanog ו־Cdx2
- פולריזציה ו־Compaction: קשורים אך בלתי תלויים
- רצף האירועים המרכזי
- משפטי מפתח
פתיחה: מהי שבירת סימטריה?
בשיעור הקודם הוצג המודל שבו ההבחנה בין תאים חיצוניים לתאים פנימיים נוצרת דרך שילוב של Compaction, Polarization, מסלול Hippo, ורמות שונות של Cdx2. התאים החיצוניים מבטאים יותר Cdx2 ומתפתחים לכיוון Trophectoderm, ואילו בתאים הפנימיים Cdx2 יורד, והם נשארים במסלול של ICM.
השאלה המרכזית בשיעור הנוכחי היא איך בכלל מגיעים למצב כזה:
איך עובר שנראה בתחילה סימטרי, מגיע למצב שבו בשלב שמונת התאים יש תאים עם רמות שונות של Cdx2?
כלומר, אנחנו מחפשים את נקודות ההתחלה של שבירת הסימטריה. כדי לעשות זאת חוזרים אחורה: משלב שמונת התאים, אל שלב ארבעת התאים, אל שלב שני התאים, ולבסוף אל הזיגוטה.
התפתחות דטרמיניסטית לעומת התפתחות רגולטיבית
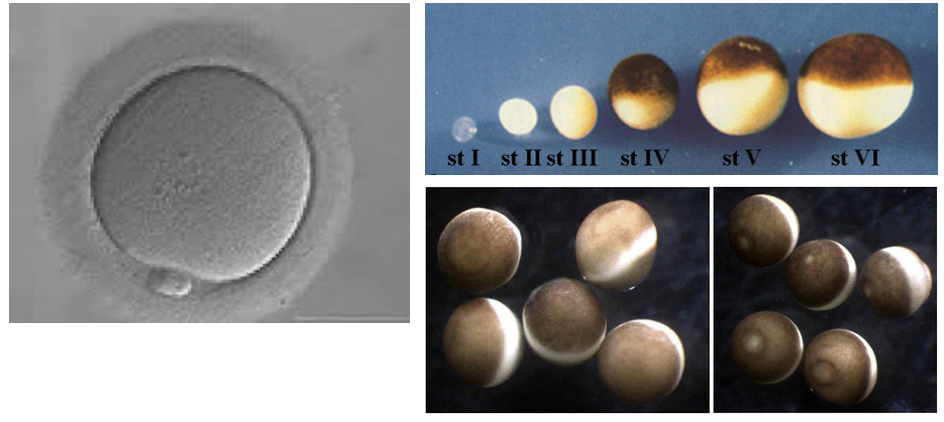
אפשר להבחין בין שני דפוסי התפתחות כלליים בבעלי חיים: התפתחות דטרמיניסטית והתפתחות רגולטיבית.
בביצית אנושית, לפחות לפי המראה החיצוני, אין הבדלים מרחביים בולטים. לעומת זאת, בביצים של צפרדעים ניתן לראות אזורים שונים, למשל אזור פיגמנטי כהה ואזור בהיר יותר. הביצית אינה הומוגנית: חומרים שונים ממוקמים באזורים שונים עוד לפני החלוקות הראשונות.
התפתחות דטרמיניסטית
במודל דטרמיניסטי, הביצית עצמה כבר מכילה חלוקה מרחבית של חומרים, מורפוגנים או דטרמיננטים, ולכן גורל התאים הראשונים נקבע מוקדם מאוד.
C. elegans - תולעת
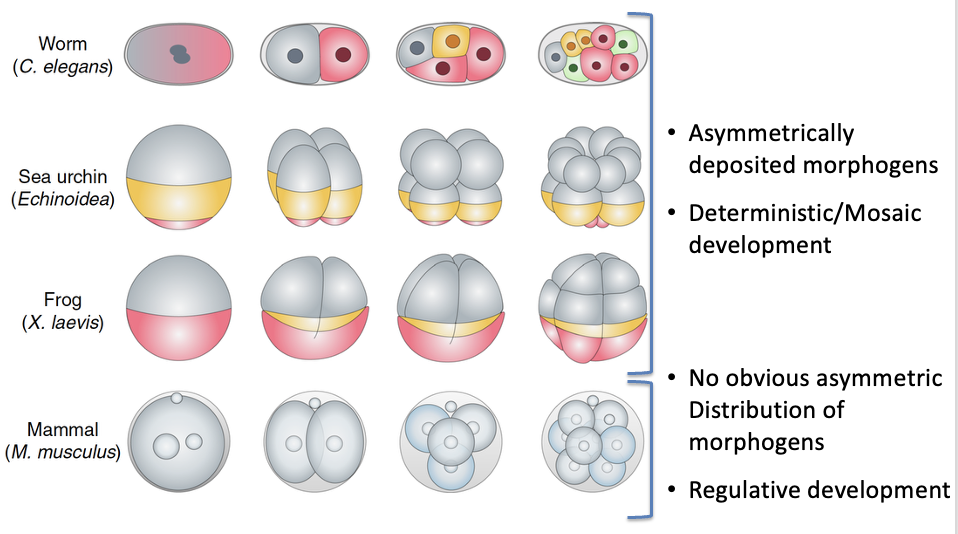
ב־C. elegans, תולעת שמורכבת מכאלף תאים, הביצית מכילה חומרים שמסודרים באופן לא שווה. אחרי ההפריה מתרחשת חלוקה א-סימטרית, וכבר בשלב שני התאים מתקבלים שני תאים בעלי זהות שונה. אם מוציאים אחד מהם, ההתפתחות לא יכולה להמשיך באופן תקין, כי אחד המרכיבים החיוניים להתפתחות כבר חסר.
זהו מודל דטרמיניסטי: ההתפתחות מוכתבת מאוד מוקדם על ידי מה שהיה מסודר בביצית.
התפתחות רגולטיבית
ביונקים, הדפוס שונה. ההתפתחות היא רגולטיבית: עד שלב הבלסטוציסט, המערכת עדיין גמישה ויכולה להתארגן מחדש. אם מוציאים תא, מפרידים תאים, או מבצעים מניפולציות מסוימות, העובר עדיין מסוגל לעיתים להתפתח, משום שהגורל עדיין לא נקבע באופן בלתי הפיך.
המשמעות היא שלא הביצית לבדה מכתיבה מראש את כל ההתפתחות. יש מערכת שמסוגלת לווסת, לפצות ולהתארגן מחדש.
| דפוס התפתחות | מאפיין מרכזי | משמעות של פגיעה מוקדמת |
|---|---|---|
| דטרמיניסטי | גורלות תאים נקבעים מוקדם לפי חלוקת חומרים בביצית | פגיעה בתא מוקדם יכולה לעצור את ההתפתחות |
| רגולטיבי | גורל התאים נקבע בהדרגה ותלוי באינטראקציות ובהקשר | המערכת יכולה לפצות על פגיעות מוקדמות מסוימות |
יש גם בעלי חיים שנמצאים במצב ביניים, למשל קיפודי ים או צפרדעים, שבהם הביצית אינה הומוגנית והחלוקות הראשונות כבר מייצרות הבדלים מסוימים, אך לא תמיד מדובר בדטרמיניזם מוחלט.
למה יש יתרון לשני הדפוסים?
היתרון תלוי בצורת הרבייה של האורגניזם. בבעלי חיים שמטילים מספר גדול מאוד של ביצים, פגיעה בחלק מהעוברים אינה בהכרח בעיה אבולוציונית גדולה, כי עדיין יישארו עוברים שימשיכו להתפתח. ביונקים, לעומת זאת, לרוב יש מספר קטן של עוברים, ולכן יש יתרון למערכת רגולטיבית שמסוגלת להתאושש מפגיעה או שינוי מוקדם.
התפתחות סטוכסטית לעומת התפתחות פרובביליסטית
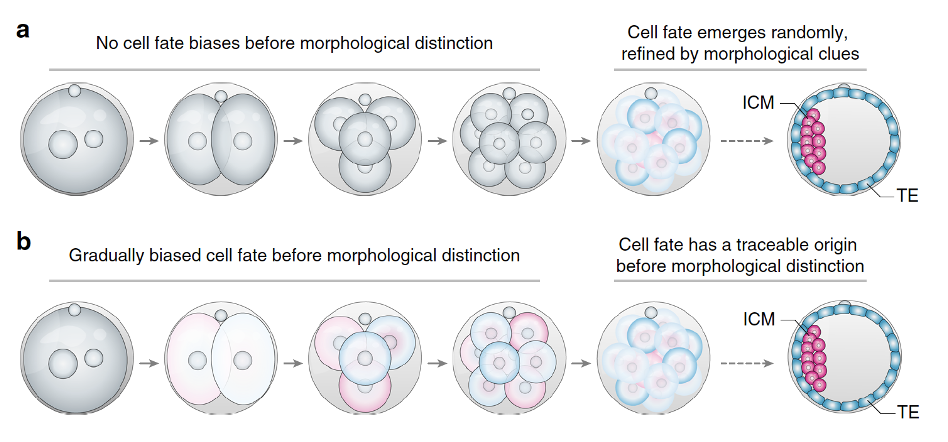
בתוך ההתפתחות הרגולטיבית עצמה צריך להבחין בין שני מושגים:
| מושג | משמעות | איך מזהים? |
|---|---|---|
| סטוכסטי Stochastic | תהליך אקראי באמת | אם יש שתי אפשרויות, נקבל בערך 50%-50%; אם יש ארבע אפשרויות, בערך 25% לכל אחת |
| פרובביליסטי Probabilistic | תהליך מוטה הסתברותית | יש סטייה משמעותית מהתפלגות שווה, כלומר למצב מסוים יש הסתברות גבוהה יותר |
כשאומרים שהתהליך פרובביליסטי, הכוונה שיש הטיה התחלתית: תא מסוים מקבל סיכוי גבוה יותר ללכת לכיוון אחד, ותא אחר מקבל סיכוי גבוה יותר ללכת לכיוון אחר.
ההבחנה הזאת מלווה את כל הדיון בשבירת סימטריה. השאלה היא האם ההבדלים ביניהם אקראיים לגמרי או שיש מנגנון שמטה את ההתפתחות בכיוון מסוים (ולא רק האם הם שונים).
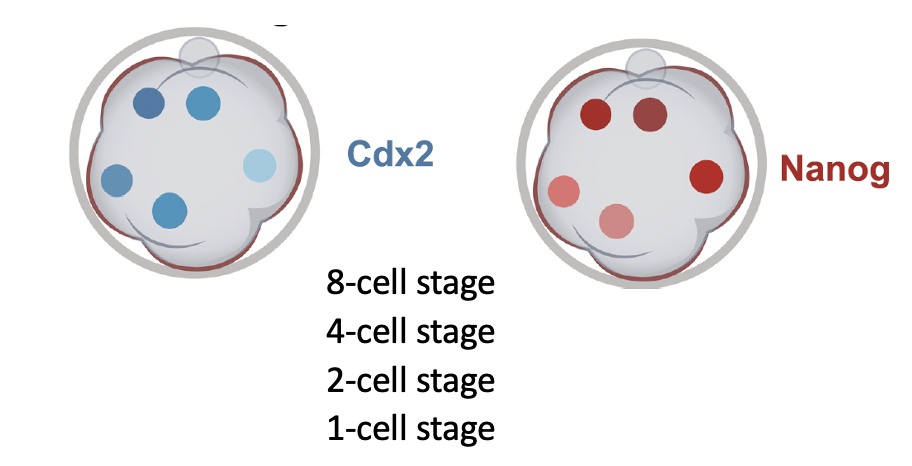
צירי העובר ומישורי החלוקה
כדי להבין מתי מתחילים ההבדלים בין התאים, צריך להסתכל על מישורי החלוקה (Division planes). מישור החלוקה קובע איך התא מתחלק, ואילו חלקים של התא יקבל כל תא בת.
זיגוטה ו־one cell embryo
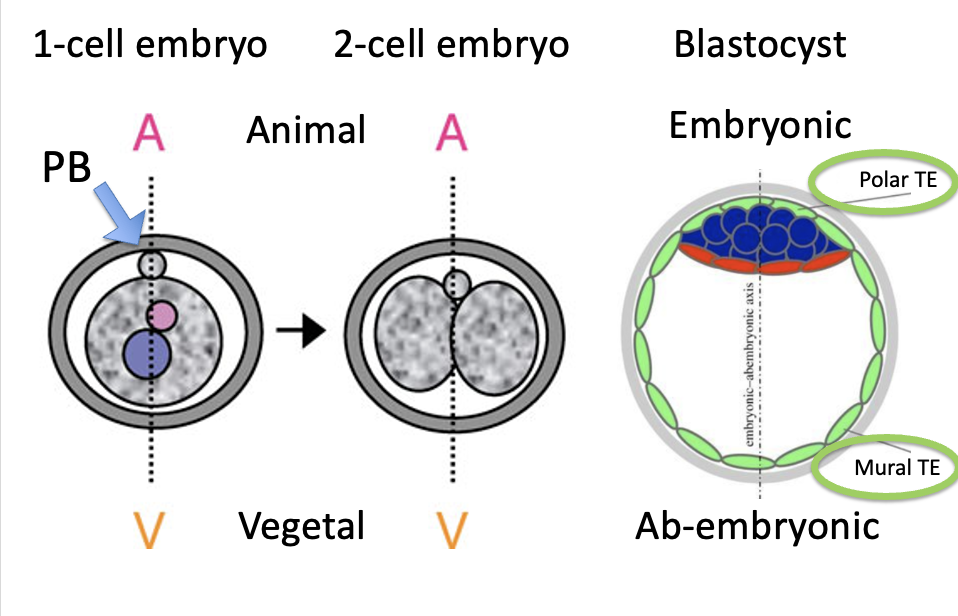
בזיגוטה ניתן לזהות שני גרעינים לפני האיחוי ואת ה־Polar body. הביצית עצמה נראית כדורית יחסית, ולכן קשה לראות בה ציר חיצוני ברור, אבל ה־Polar body מגדיר ציר חשוב:
| ציר | משמעות |
|---|---|
| Animal pole | הצד שבו נמצא ה־Polar body |
| Vegetal pole | הצד הרחוק מה־Polar body |
בחלוקה הראשונה של הזיגוטה, מישור החלוקה נוטה להסתדר בערך במקביל לציר animal-vegetal. לכן כבר בשלב הזה יש לעובר כיוון מועדף לחלוקה.
זה תהליך פרובביליסטי: החלוקה מושפעת מציר קיים בביצית, ולא נקבעת באקראיות מלאה.
הציר Embryonic-Abembryonic בבלסטוציסט
בבלסטוציסט מופיע ציר נוסף: Embryonic-Abembryonic axis.
- בצד ה־Embryonic נמצא ה־ICM, שממנו יתפתח העובר
- בצד ה־Abembryonic אין ICM
גם ב־Trophectoderm עצמו מבחינים בין שני אזורים:
| אזור | משמעות |
|---|---|
| Polar TE | ה־Trophectoderm שנמצא מעל/סביב ה־ICM, בצד העוברי |
| Mural TE | ה־Trophectoderm הרחוק מה־ICM, בצד האב־אמבריוני |
השאלה היא אם יש קשר בין הציר animal-vegetal שמוגדר כבר בזיגוטה לבין הציר embryonic-abembryonic שמופיע בבלסטוציסט.
Cell lineage analysis: ניתוח שושלת תאים
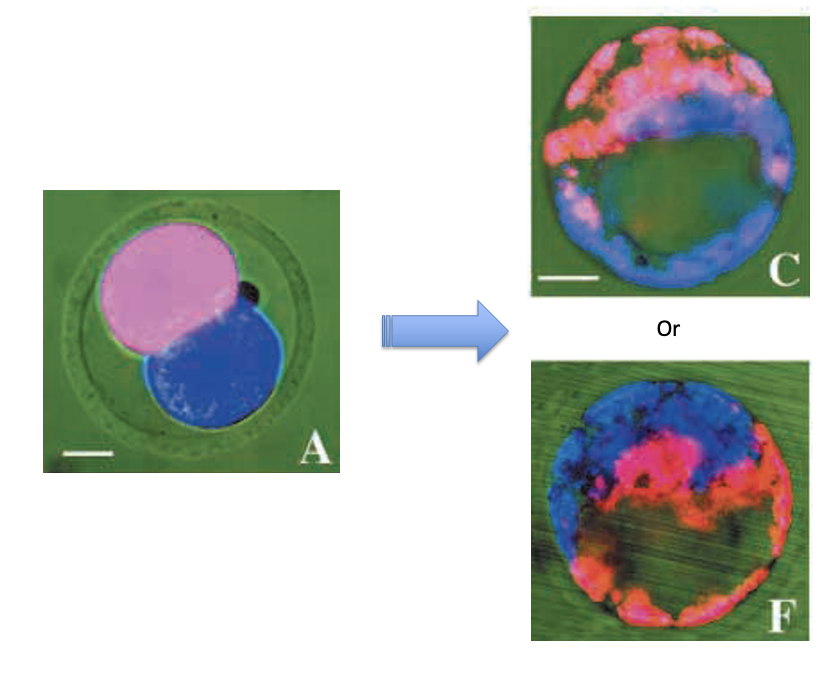
כדי לבדוק את הקשר בין הצירים מבצעים Cell lineage analysis: לוקחים עובר בשלב שני תאים, מסמנים תא אחד בצבע פלואורסצנטי אחד, ואת התא השני בצבע פלואורסצנטי אחר. לאחר מכן עוקבים אחרי העובר עד שלב הבלסטוציסט ושואלים לאן הגיעו הצאצאים של כל תא.
הניסוי מלמד שתי נקודות:
-
אין ערבוב גדול של התאים - אם תא אחד סומן באדום והשני בכחול, מתקבל לרוב בלסטוציסט שבו חצי אחד מקורו בתא אחד וחצי אחר מקורו בתא השני. כלומר, הצאצאים של כל בלסטומר נשארים יחסית יחד.
-
הציר embryonic-abembryonic מאונך בקירוב לציר animal-vegetal - בבלסטוציסט, הציר האמבריוני-אב־אמבריוני נוטה להסתדר כמעט בניצב לציר animal-vegetal. זה דפוס ביולוגי כללי, לא זווית מדויקת של 90 מעלות.
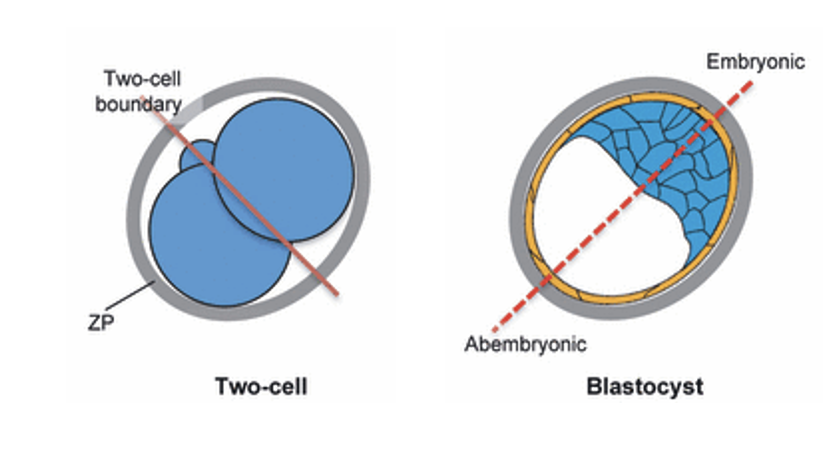
המסקנה החשובה היא שכבר בשלבים המוקדמים יש לעובר ארגון מרחבי: מישור החלוקה הראשון קשור לכיוון שבו יתארגן בהמשך הציר embryonic-abembryonic (במילים אחרות: הצירים לא מופיעים לגמרי באקראי).
האם שני הבלסטומרים הראשונים זהים?
לאחר החלוקה הראשונה מתקבלים שני בלסטומרים. השאלה המרכזית היא האם הם זהים מבחינה התפתחותית: האם לכל אחד מהם יש אותו פוטנציאל לתרום לעובר, באותה הסתברות ובאותו אופן?
כדי לבדוק זאת משתמשים במודל של תאומים מונוזיגוטיים.
תאומים מונוזיגוטיים לעומת דיזיגוטיים
| סוג תאומים | מקור |
|---|---|
| Monozygotic twins | תאומים שמקורם באותה ביצית מופרית |
| Dizygotic twins | שתי ביציות שונות שהופרו בנפרד; למעשה שני עוברים שונים באותו היריון |
בעכברים אין תאומים מונוזיגוטיים באופן טבעי כמו בבני אדם. עכברים בנויים לשֶׁגֶר של כמה עוברים, ולכן אינם מודל טבעי לחקר תאומים. אבל אפשר לבצע מניפולציה ניסויית כדי לשאול שאלה ממוקדת: מה הפוטנציאל של כל אחד משני הבלסטומרים הראשונים?
יצירת תאומים מונוזיגוטיים בעכבר
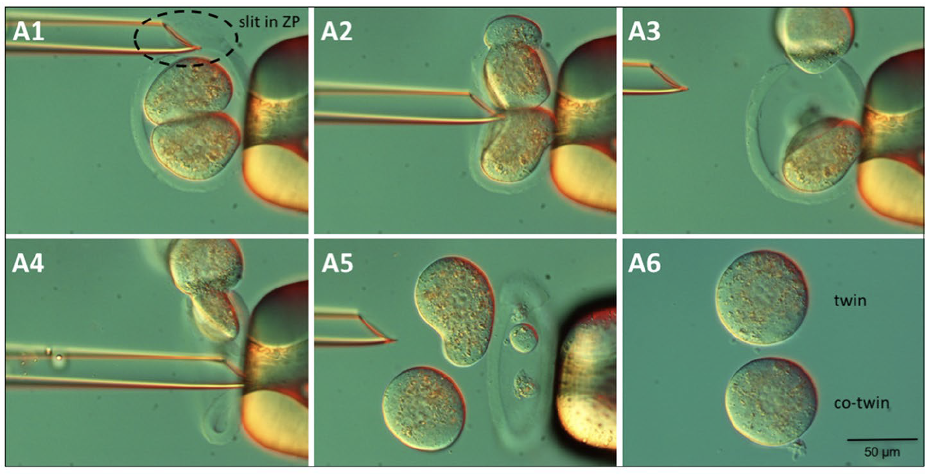
הניסוי מתחיל בעובר בשלב שני תאים:
- יוצרים חור קטן ב־Zona Pellucida
- מפעילים לחץ בעזרת פיפטה
- בלסטומר אחד יוצא החוצה
- מוציאים גם את הבלסטומר השני
- מקבלים שני בלסטומרים נפרדים, מחוץ ל־Zona Pellucida
לבלסטומר אחד קוראים twin, ולשני co-twin (השמות רק לצורך מעקב והתייחסות).
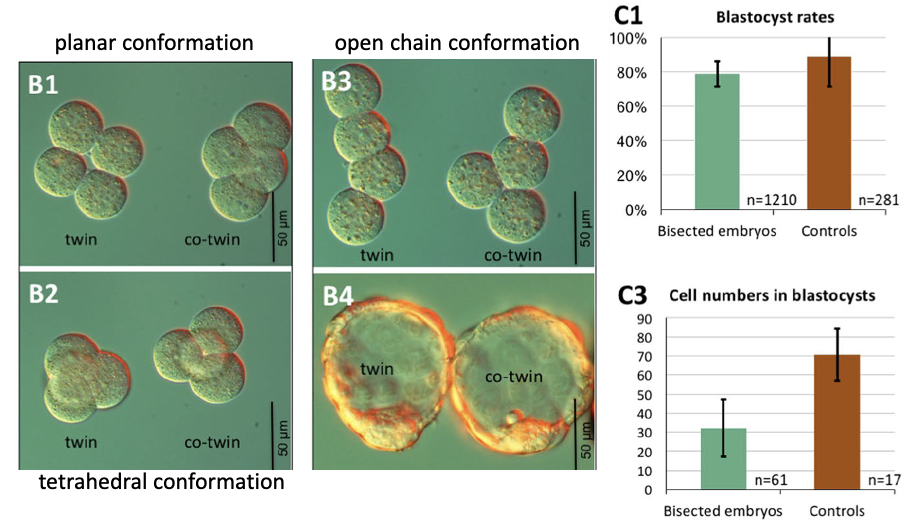
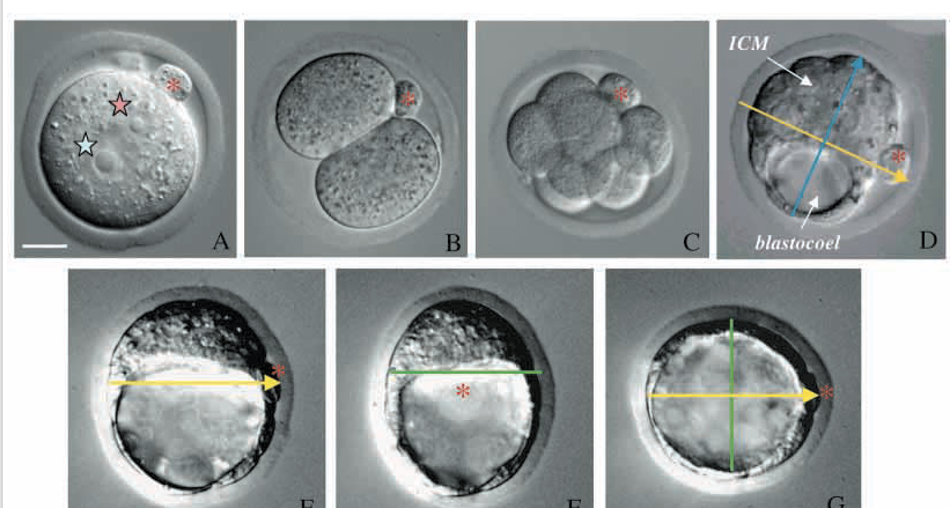
גם מחוץ ל־Zona Pellucida, שני הבלסטומרים יכולים להמשיך להתחלק ולהגיע לבלסטוציסט. לעיתים המבנים המרחביים נראים פחות “מסודרים” מהרגיל, למשל open-chain או tetrahedral conformation, אבל בסופו של דבר יכולים להיווצר בלסטוציסטים.
התפקיד הפיזיולוגי המרכזי של ה־Zona Pellucida הוא ההפריה - לאפשר לתא הזרע לזהות את הביצית. אחרי ההפריה העובר יכול להמשיך להתפתח גם מחוץ ל־Zona Pellucida בתנאי תרבית.
בניסוי הביקורת, עצם הפעולה הכירורגית לא פוגעת ביכולת להגיע לבלסטוציסט: עוברים שעברו הפרדה עדיין מגיעים לשלב בלסטוציסט בשיעור דומה לעוברים רגילים. עם זאת, הבלסטוציסטים שנוצרו מכל חצי עובר מכילים פחות תאים מבלסטוציסט רגיל, בערך חצי ממספר התאים.
בלסטוציסט מוגדר לפי המבנה שלו: Trophectoderm, Blastocoel ו־ICM - לא רק לפי מספר התאים.
מבחן השרשה: למה קשה להסיק ממנו?
השלב הבא הוא לשאול אם הבלסטוציסטים מסוגלים לעבור השרשה, להתפתח ולהיוולד.
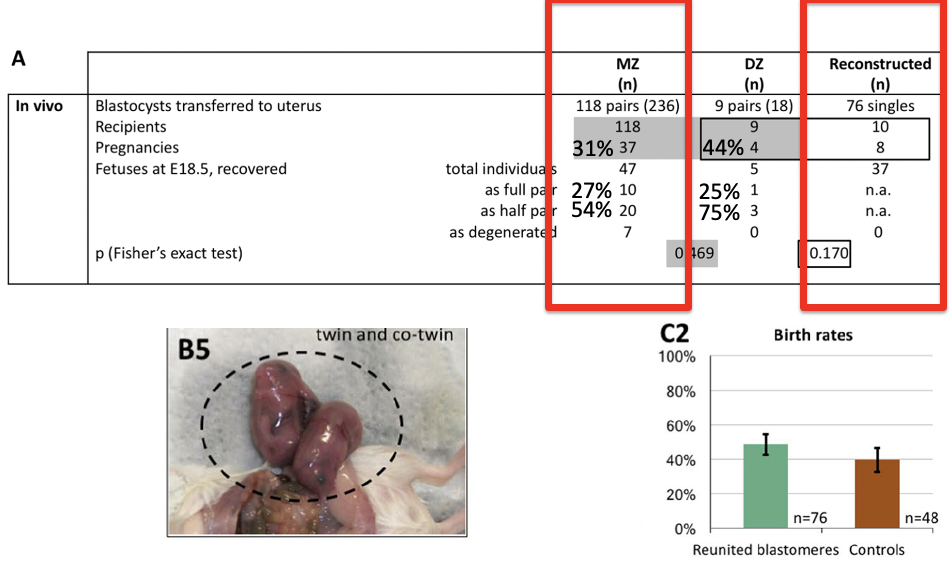
קודם צריך לבדוק שהפעולה עצמה אינה הבעיה. לכן מבצעים ביקורת: מפרידים את שני הבלסטומרים ואז מחברים אותם חזרה, נותנים להם להתפתח לבלסטוציסט, ומשתילים אותם בנקבות פונדקאיות. בניסוי התקבלו 37 עוברים מתוך 76 שהושתלו, כלומר מראש ההשתלה עצמה היא תהליך בעייתי ולא כל העוברים שורדים.
כשמשווים לעוברים שלא עברו את הפעולה, שיעור ההצלחה דומה יחסית. לכן הפעולה הכירורגית עצמה אינה ההסבר העיקרי לכישלון.
אבל כשמשתילים זוגות של “תאומים” מונוזיגוטיים בעכבר, קשה מאוד להסיק מסקנה חזקה. בעכבר צריך בדרך כלל שגר של כמה עוברים כדי שההיריון יצליח. אם משתילים רק זוג אחד, עצם תנאי ההשתלה כבר בעייתיים מאוד.
במבחן ההשרשה נולדו מקרים שבהם רק אחד משני התאומים שרד. זה רומז שאולי שני הבלסטומרים שונים בפוטנציאל שלהם.
אבל אותה בעיה הופיעה גם בזוגות דיזיגוטיים, כלומר בשני עוברים נפרדים שהושתלו יחד. לכן מבחן ההשרשה לבדו לא מספיק כדי לקבוע שהבלסטומרים שונים.
Outgrowth assay: בדיקת הפוטנציאל של הבלסטומרים בתרבית

כדי לעקוף חלק מהבעיות של השרשה בעכברים, משתמשים ב־Outgrowth assay. בניסוי כזה מניחים בלסטוציסט על צלחת תרבית, ותאי ה־Trophectoderm נפרסים על הצלחת. ה־ICM נשאר כגוש תאים מעליהם.
כשעושים זאת לזוגות שמקורם בשני הבלסטומרים הראשונים, בודקים האם שני הבלסטומרים מסוגלים ליצור outgrowth תקין.
התוצאות מראות הבדל בין זוגות דיזיגוטיים למונוזיגוטיים:
-
בזוגות דיזיגוטיים, ברוב גדול של המקרים שני העוברים יוצרים outgrowth.
-
בזוגות מונוזיגוטיים שנוצרו מהפרדת שני הבלסטומרים, יש שיעור משמעותי של מקרים שבהם רק אחד משני בני הזוג יוצר outgrowth תקין.
הניסוי הזה תומך במסקנה ברורה יותר:
הפוטנציאל ההתפתחותי של שני הבלסטומרים הראשונים לא זהה.
כלומר, ההתפתחות עדיין רגולטיבית ויש יכולת תיקון, אבל שני הבלסטומרים אינם שקולים לחלוטין.
Oct4-GFP ומספר תאי אפיבלסט
כדי להבין מה פירוש “פוטנציאל שונה”, מסתכלים על עכברים שבהם GFP נמצא תחת הבקרה של Oct4. בשלב הבלסטוציסט המאוחר, Oct4 משמש כאן כמרקר לתאי Epiblast.
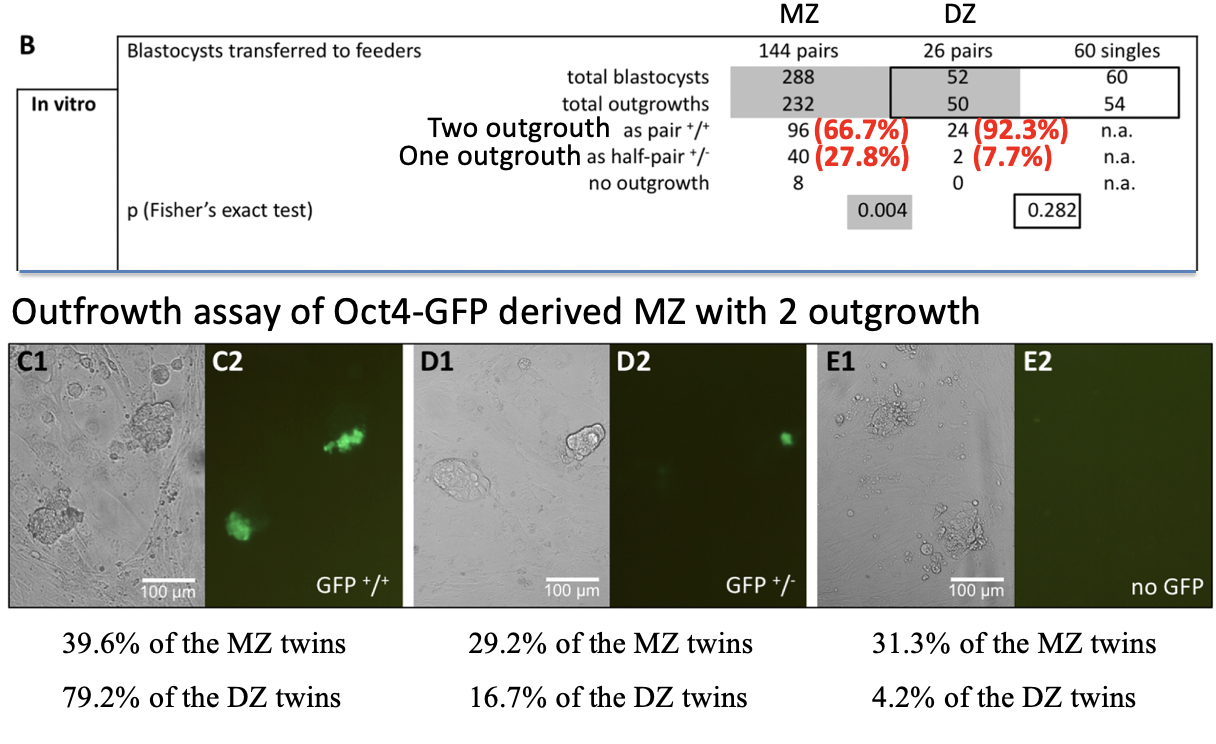
בוחנים רק מקרים שבהם נוצרו על הצלחת שני מוקדי outgrowth. לאחר מכן בודקים האם בכל מוקד יש תאי Epiblast מסומנים.
אפשר לקבל שלושה מצבים:
| מצב | משמעות |
|---|---|
| שני המוקדים GFP+ | בשניהם נוצר Epiblast |
| מוקד אחד GFP+ והשני לא | רק אחד יצר Epiblast |
| בשני המוקדים לא מזוהה GFP | בשניהם לא Epiblast זוהה |
בזוגות מונוזיגוטיים מתקבלת התפלגות שונה מזו של זוגות דיזיגוטיים. בזוגות מונוזיגוטיים יש הרבה יותר מקרים שבהם רק אחד מהשניים יוצר Epiblast, או ששניהם אינם יוצרים Epiblast ברור. בזוגות דיזיגוטיים, רוב הזוגות יוצרים Epiblast בשני הצדדים.
המסקנה היא שההבדל בין שני הבלסטומרים מתבטא בעיקר ביכולת לייצר ICM/Epiblast.
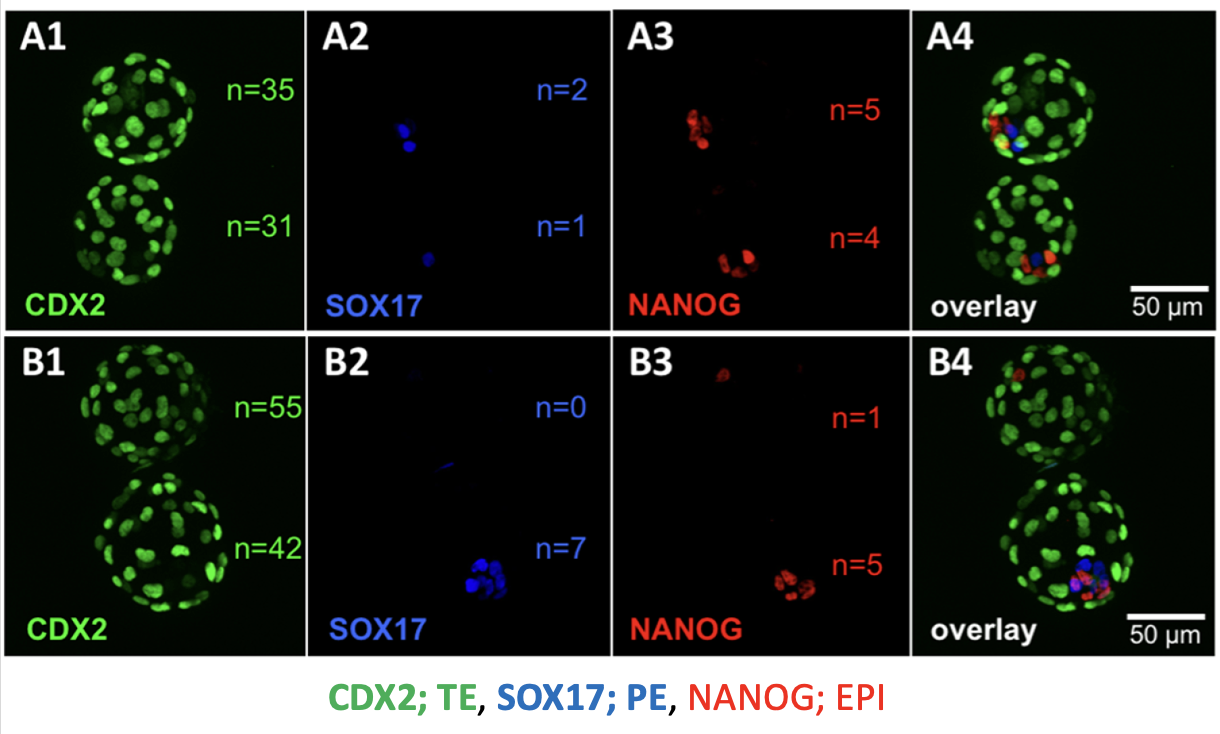
בצביעות נוספות בוחנים מרקרים שונים:
| Marker | אוכלוסייה |
|---|---|
| Cdx2 | Trophectoderm |
| Sox17 | Primitive endoderm |
| Nanog | Epiblast |
ההבדל המרכזי בין twin ל־co-twin הוא בעיקר ב־ICM: כמה תאים בו מבטאים Nanog.
יותר תאי ICM חיוביים ל־Nanog מצביעים על יכולת טובה יותר ליצור Epiblast.
השוואה בין עובר שלם לחצי עובר
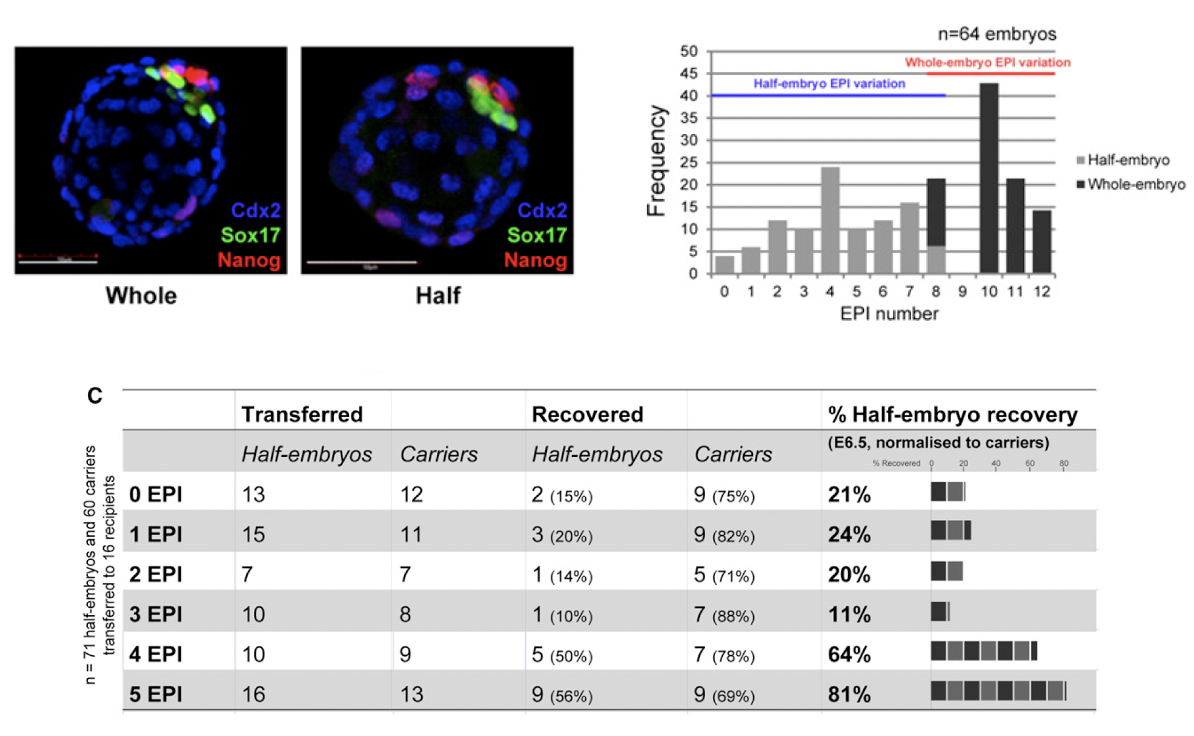
בניסוי נוסף משווים בין:
- Whole embryo - עובר שלם שהמשיך להתפתח משלב שני התאים.
- Half embryo - בלסטומר אחד מתוך שניים שניתן לו להתפתח לבד.
בבלסטוציסטים שנוצרו מחצי עובר יש שונות גדולה במספר תאי האפיבלסט: יש כאלה עם אפס תאי אפיבלסט, אחד, שניים, שלושה וכן הלאה. בעובר שלם, לעומת זאת, מספר תאי האפיבלסט גבוה יותר.
לאחר מכן משתילים בלסטוציסטים לפי מספר תאי האפיבלסט שלהם ושואלים האם הם נולדים. הנקודה המרכזית היא שמספר נמוך מאוד של תאי אפיבלסט קשור לסיכוי נמוך להתפתחות תקינה. סביב ארבעה תאי אפיבלסט ומעלה כבר יש פוטנציאל טוב יותר להתפתחות, השרשה ולידה.
המבחן כאן הוא פונקציונלי: האם בסוף נולד עובר או לא. הניסוי לא עונה על השאלה אם לעוברים שנולדו יהיו בעיות מאוחרות יותר.
תאומים מונוזיגוטיים באדם ו־ART
לפני שמדברים על תאומים מונוזיגוטיים באדם צריך להכיר שני קרומים עובריים:
| קרום | מקור עוברי |
|---|---|
| Chorion | Trophectoderm |
| Amnion | Epiblast |
המקור של הקרומים מאפשר להסיק, בזהירות, באיזה שלב ייתכן שהתרחש הפיצול.
איך נוצרים תאומים מונוזיגוטים באדם
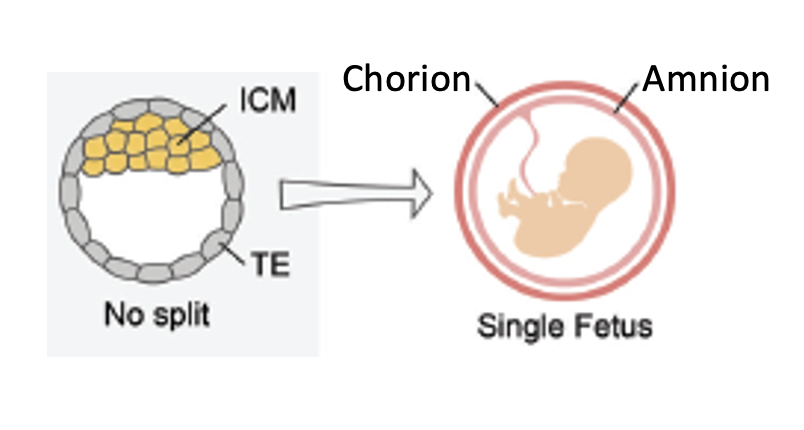
בבני אדם אין דרך ניסויית ישירה לבדוק את מנגנון היווצרות התאומים, ולכן מדובר במודלים ובהשערות שמבוססים על מבנים שנראים באולטרסאונד ועל הידע ההתפתחותי.
אפשר לחשוב על כמה אפשרויות:
-
פיצול בתוך ה־ICM - מתקבלים שני מוקדים בתוך אותו בלסטוציסט. אם הם קרובים מאוד, ייתכן שגם ה־Chorion וגם ה־Amnion משותפים.
-
שני מוקדי ICM נפרדים יותר - לכל עובר יכול להיווצר Amnion משלו, אבל ה־Chorion משותף, כי מקורו ב־Trophectoderm של אותו בלסטוציסט.
-
פיצול בשלב המורולה - שתי קבוצות תאים נפרדות יכולות ליצור שני בלסטוציסטים. במקרה כזה לכל עובר יהיה Chorion משלו ו־Amnion משלו. באולטרסאונד זה יכול להיראות כמו תאומים דיזיגוטיים, ולכן אין ודאות בלי בדיקת DNA.
הדרך הוודאית לדעת שתאומים הם מונוזיגוטיים היא בדיקת DNA. דמיון חיצוני אינו הוכחה.
מנגנון אפשרי: Blastocoel ו־Adherens junctions
אם ה־Adherens junctions של ה־ICM אינם חזקים מספיק, ייתכן שבזמן יצירת ה־Blastocoel נוצרים שני חללים או שני מוקדים שמפרידים את ה־ICM לשני אזורים. בהמשך, כשהחללים גדלים או מתאחים, המבנה הפיזיקלי יכול להשאיר שני מוקדי ICM.
מודל נוסף קשור ליציאה מה־Zona Pellucida. אם הפתח נוצר באזור לא רגיל, ייתכן שהלחץ של ה־Blastocoel גורם לכך שה־ICM יוצא ראשון, והיציאה עצמה יוצרת פיצול פיזיקלי ב־ICM.
אלה מודלים אפשריים, לא הוכחה ניסויית ישירה בבני אדם.
ART cases
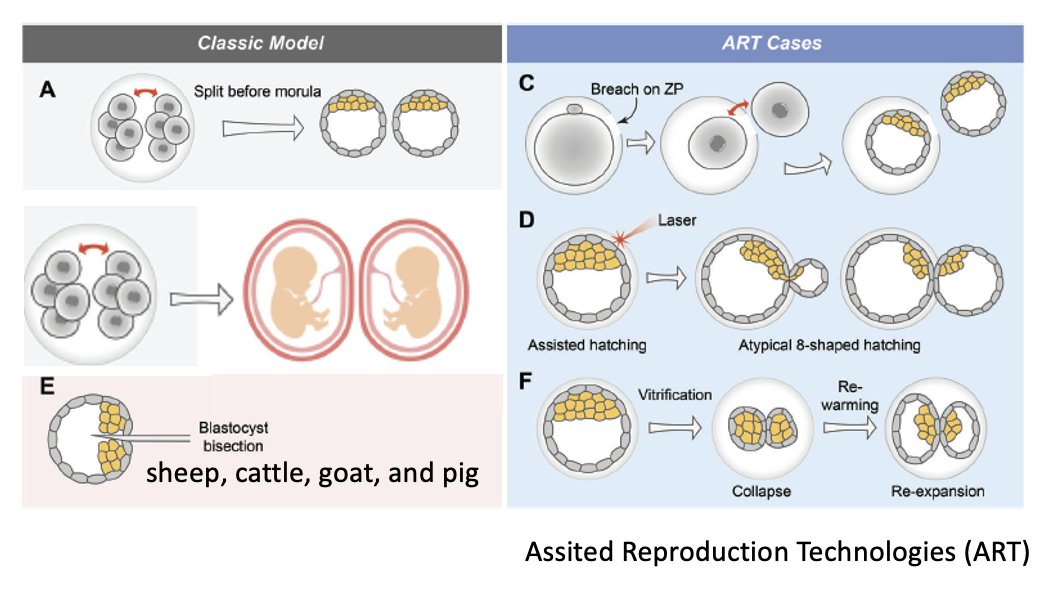
במסגרת Assisted Reproduction Technologies (ART), למשל IVF, נצפו מקרים שיכולים להסביר יצירת תאומים מונוזיגוטיים:
-
פגיעה או חור ב־Zona Pellucida בשלב שני התאים, כך שבלסטומר אחד יוצא החוצה וכל בלסטומר מתפתח לבלסטוציסט קטן.
-
Assisted hatching בלייזר, שבו פתח לא מדויק ב־Zona Pellucida יכול לגרום ליציאה לא רגילה ולפיצול פיזיקלי.
-
הקפאה והפשרה של עוברים (Vitrification) שמובילה לקריסה פיזיקלית של הבלסטוציסט, ולעיתים לאחר ההפשרה מתקבלים שני בלסטוציסטים.
גם אם פיצול כזה מתרחש, עדיין נשארת שאלה פתוחה: למה שני חלקים שנמצאים באותה Zona Pellucida אינם מתאחדים בחזרה? זו נקודה שלא נפתרה בשיעור, להבנתי.
ארמדילו: תאומים מונוזיגוטיים כתהליך לא אקראי
ארמדילו משמש דוגמה לכך שתאומים מונוזיגוטיים אינם חייבים להיות אירוע אקראי לחלוטין. בארמדילו יכולים להיווצר ארבעה עוברים זהים מאותה ביצית מופרית.
הדוגמה מדגישה עיקרון: כאשר תהליך מתרחש באופן עקבי במין מסוים, סביר שיש מאחוריו מנגנון מכוון או פרובביליסטי.
לכן תאומים מונוזיגוטיים יכולים להיווצר כתוצאה מתוכנית התפתחותית עם הטיה מסוימת, ולא רק כתוצאה ממקריות.
שלב ארבעת התאים: סוגי עוברים ומישורי חלוקה
אחרי שראינו ששני הבלסטומרים הראשונים אינם זהים לחלוטין, עוברים לשאלה הבאה: האם ארבעת הבלסטומרים בשלב ארבעת התאים זהים?
סוגי עובר - 4-cell stage
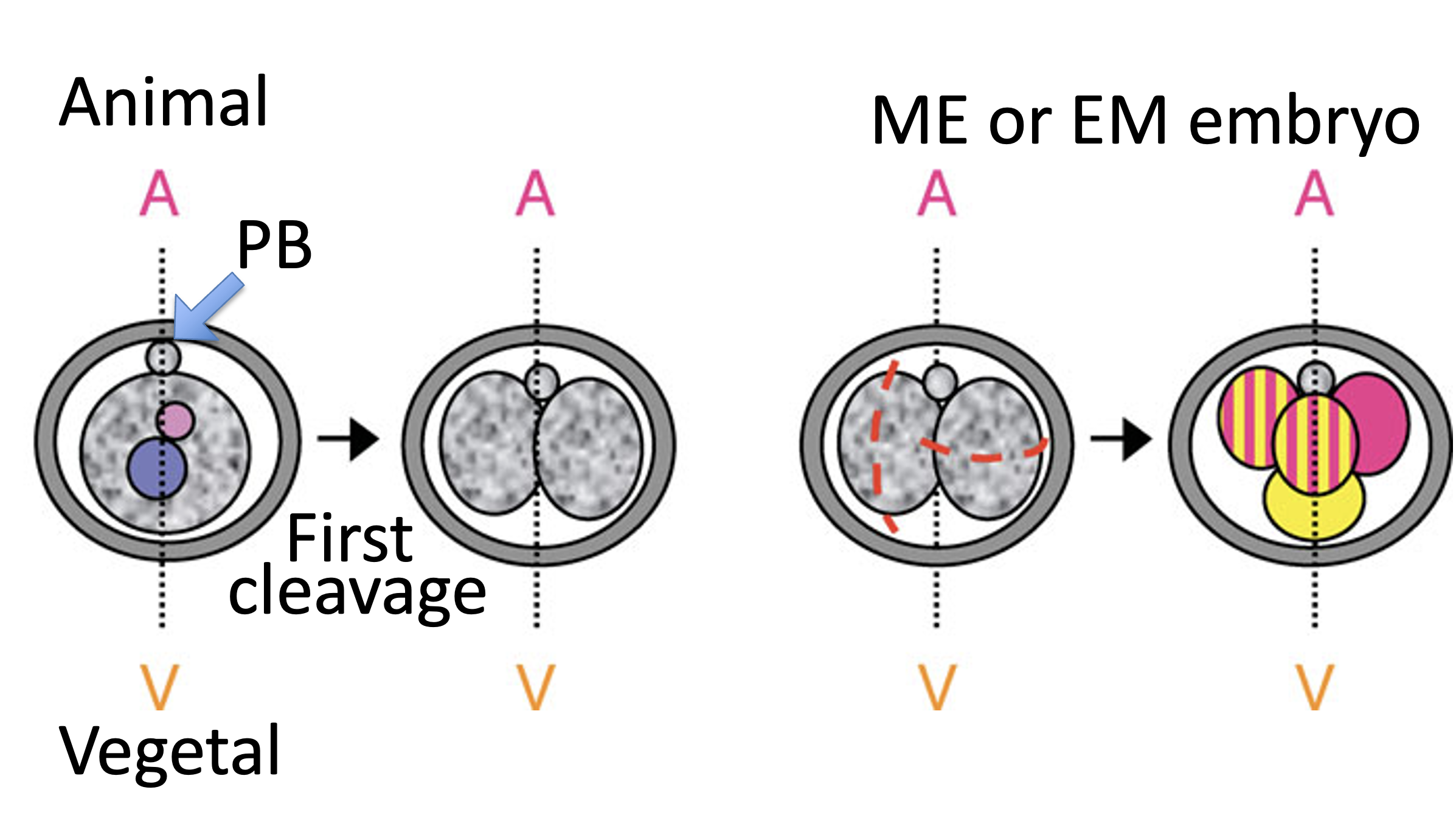
בשלב ארבעת התאים מבחינים בין כמה אפשרויות לפי מישורי החלוקה של שני הבלסטומרים משלב שני התאים.
| סוג חלוקה | הסבר | שם העובר |
|---|---|---|
| Meridional division (M) | חלוקה בכיוון מקביל לציר animal-vegetal | אם שני הבלסטומרים מתחלקים כך: MM embryo |
| Equatorial division (E) | חלוקה בכיוון אחר, סביב קו “משווה” ביחס לציר | אם שני הבלסטומרים מתחלקים כך: EE embryo |
| M ואז E / E ואז M | בלסטומר אחד מתחלק M והשני E | ME / EM embryo, לרוב מבנה tetrahedral |
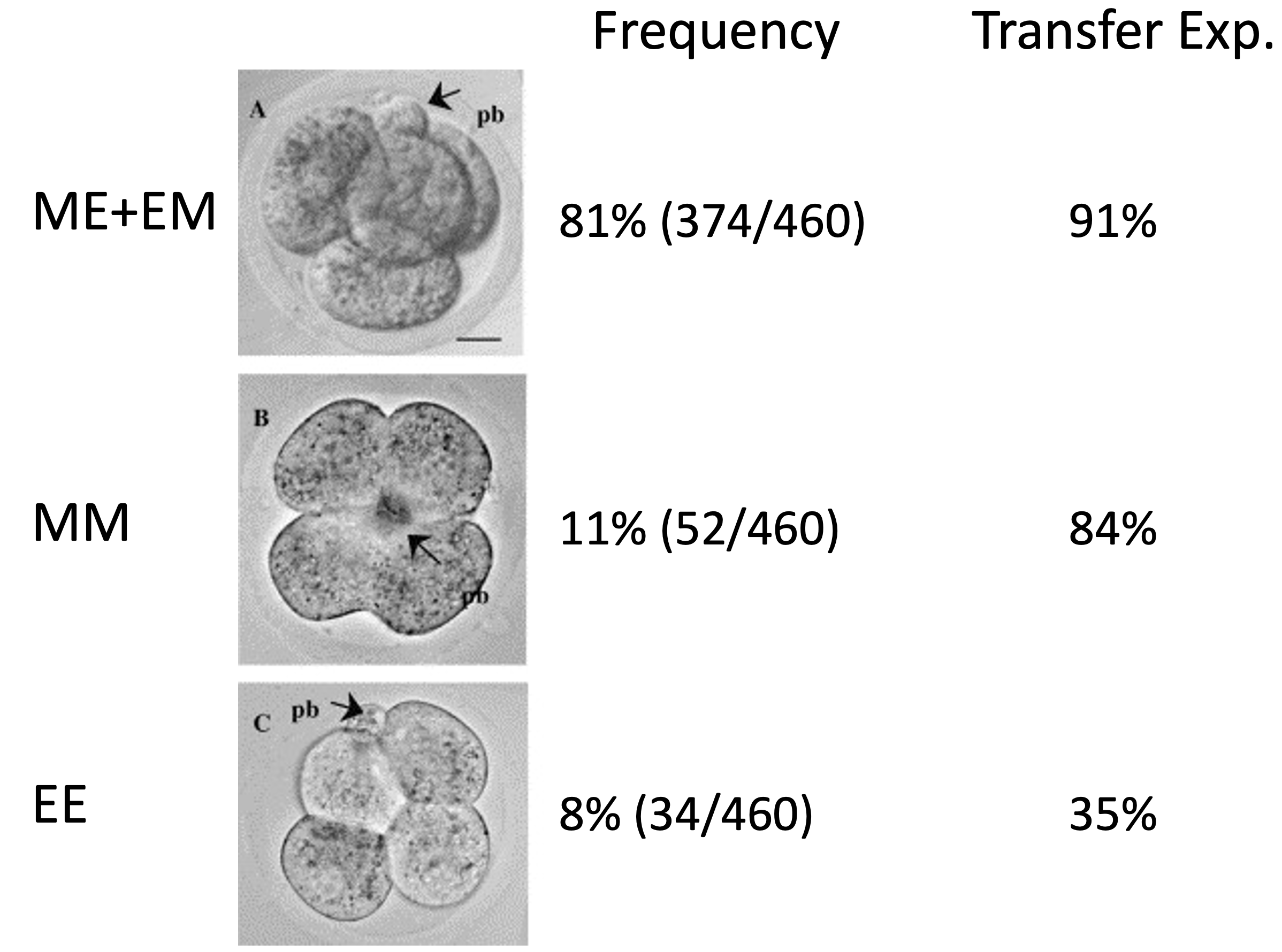
בעוברים שהוצאו מנקבות, רוב העוברים מופיעים במבנה ME/EM וטטרהדרלי; MM ו־EE מופיעים בשכיחות נמוכה יותר.
לכן גם כאן מדובר בתהליך פרובביליסטי ולא סטוכסטי. ההתפלגות מוטה לטובת מבנה ME/EM, ולכן מדובר בדפוס פרובביליסטי.
פוטנציאל ההתפתחות של הצורות השונות
כשמשתילים עוברים מהסוגים השונים, הפוטנציאל אינו זהה. עוברים מסוג EE מציגים פוטנציאל נמוך יותר לעומת צורות אחרות. מישורי החלוקה משפיעים גם על הסידור המרחבי של התאים וגם על הפוטנציאל ההתפתחותי שלהם.
מי שתורם לצד העוברי
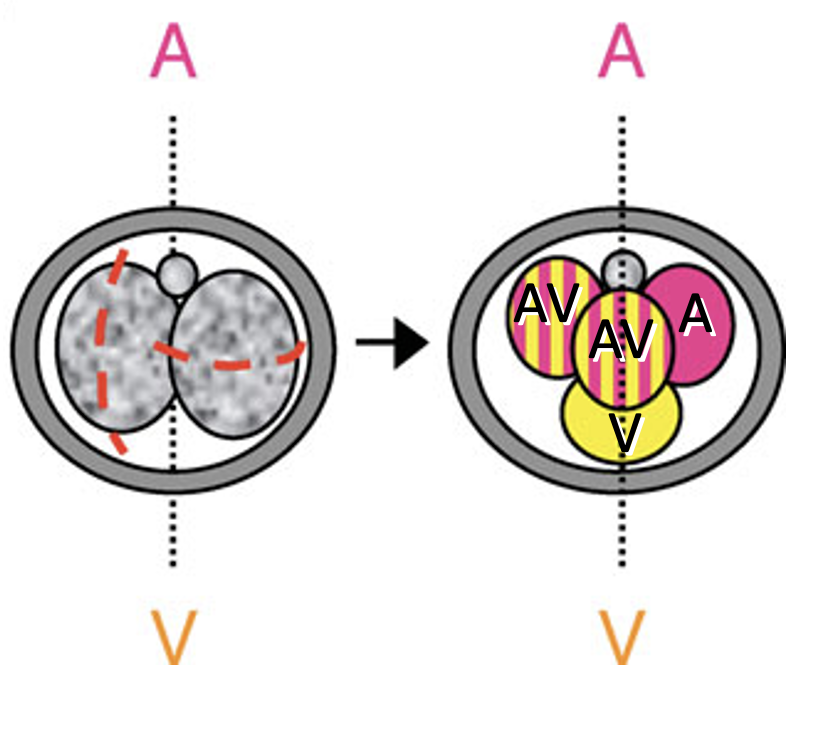
במבנה טטרהדרלי, אפשר לתת שמות לתאים לפי מיקומם ומקורם:
- שני התאים שמקורם בחלוקה מסוג M יכולים להיקרא AV או M cells
- התא שמקורו בחלוקה equatorial ונמצא קרוב ל־Polar body נקרא A
- התא שמקורו בחלוקה equatorial ונמצא רחוק מה־Polar body נקרא V
במעקב שושלת תאים רואים שתאים שונים תורמים לאזורים שונים בבלסטוציסט:
| תא בשלב ארבעת התאים | תרומה עיקרית בהמשך |
|---|---|
| M / AV cells | בעיקר לכיוון הצד העוברי / ICM |
| V cell | בעיקר לכיוון Trophectoderm |
| A cell | תרומה ביניים, גם ICM וגם Trophectoderm |
בשלב הזה הגורל עדיין גמיש, אבל התאים כבר שונים בפוטנציאל שלהם.
ניסוי כימרות מבלסטומרים בשלב ארבעת התאים
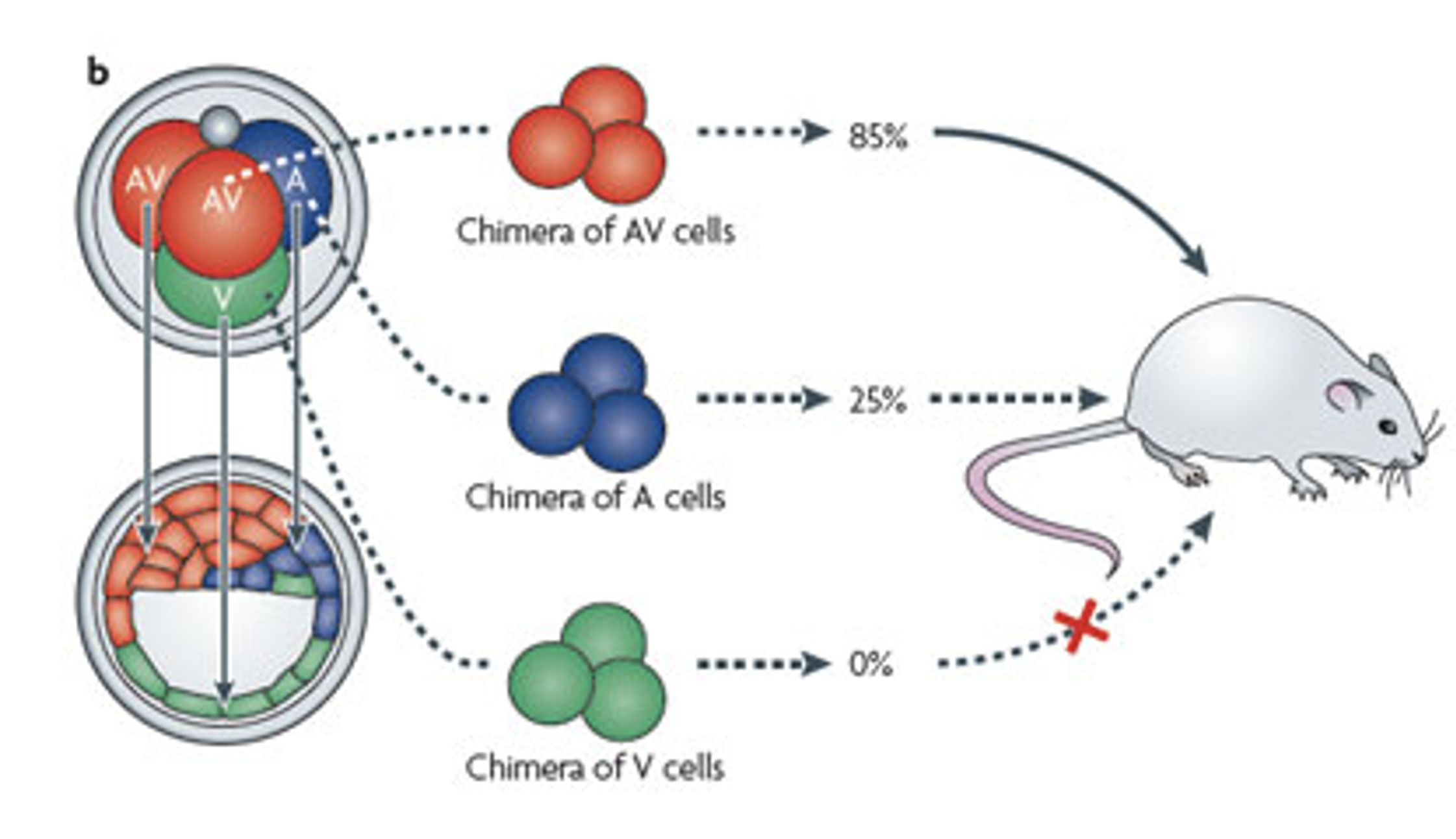
בניסוי נוסף מפרקים עוברים בשלב ארבעת התאים, מזהים את סוגי הבלסטומרים, ובונים כימרות:
- שלושה תאים מסוג AV/M
- שלושה תאים מסוג A
- שלושה תאים מסוג V
הסיבה שזה נקרא כימרה היא שכל עובר בשלב ארבעת התאים מכיל מספר מוגבל של תאים מכל סוג, ולכן כדי להרכיב שלושה תאים מאותו סוג צריך לקחת תאים מכמה עוברים.
אחרי שמרכיבים את הכימרות נותנים להן להתפתח לבלסטוציסטים ומשתילים אותן בנקבות.
התוצאות:
| סוג הכימרה | תוצאה כללית |
|---|---|
| AV/M cells | שיעור הצלחה גבוה יחסית |
| A cells | שיעור הצלחה נמוך יותר |
| V cells | לא התקבלו לידות בניסוי שתואר |
התוצאות מצביעות על הבדל בפוטנציאל ההתפתחותי בין סוגי התאים: כימרות שכללו תאי AV/M הצליחו יותר, כימרות מתאי A הצליחו פחות, ומתאי V לא התקבלו לידות בניסוי שתואר.
המשמעות היא שבשלב ארבעת התאים כבר קיימת הטיה בין הבלסטומרים. תאים שונים יכולים לתרום לעובר בסיכוי שונה, גם אם הגורל שלהם עדיין גמיש ותלוי בהקשר.
בשלב הזה נכון לדבר על הטיה פרובביליסטית: יש הבדל בפוטנציאל, אבל אין עדיין קביעה קשיחה וסופית של גורל התא.
אצטילציה, מתילציה וקוד אפיגנטי
כדי להבין מה יכול ליצור הבדלים מוקדמים בין בלסטומרים, עוברים לאפיגנטיקה.
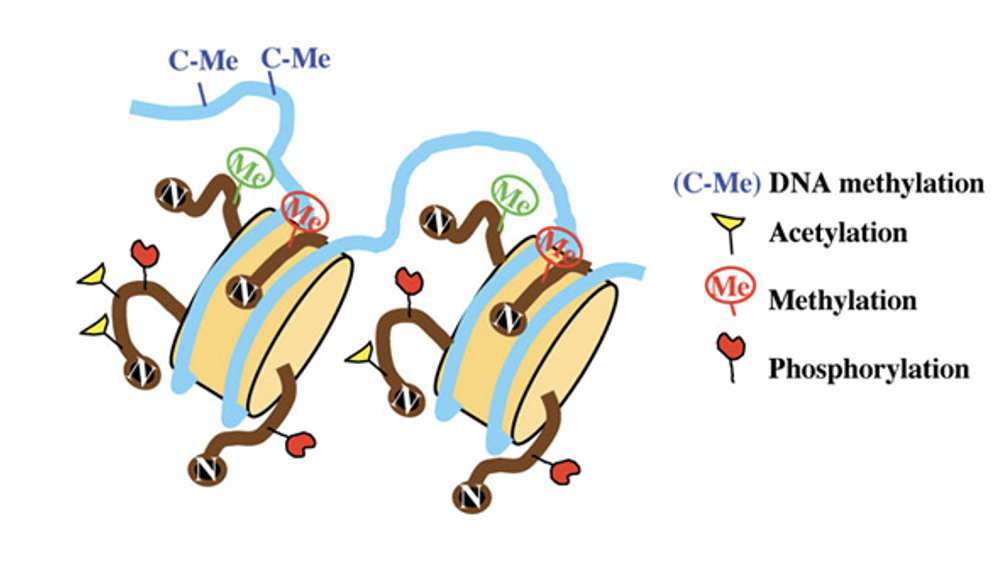
שתי רמות מרכזיות של רגולציה אפיגנטית:
- DNA methylation
- מודיפיקציות על היסטונים, למשל אצטילציה ומתילציה
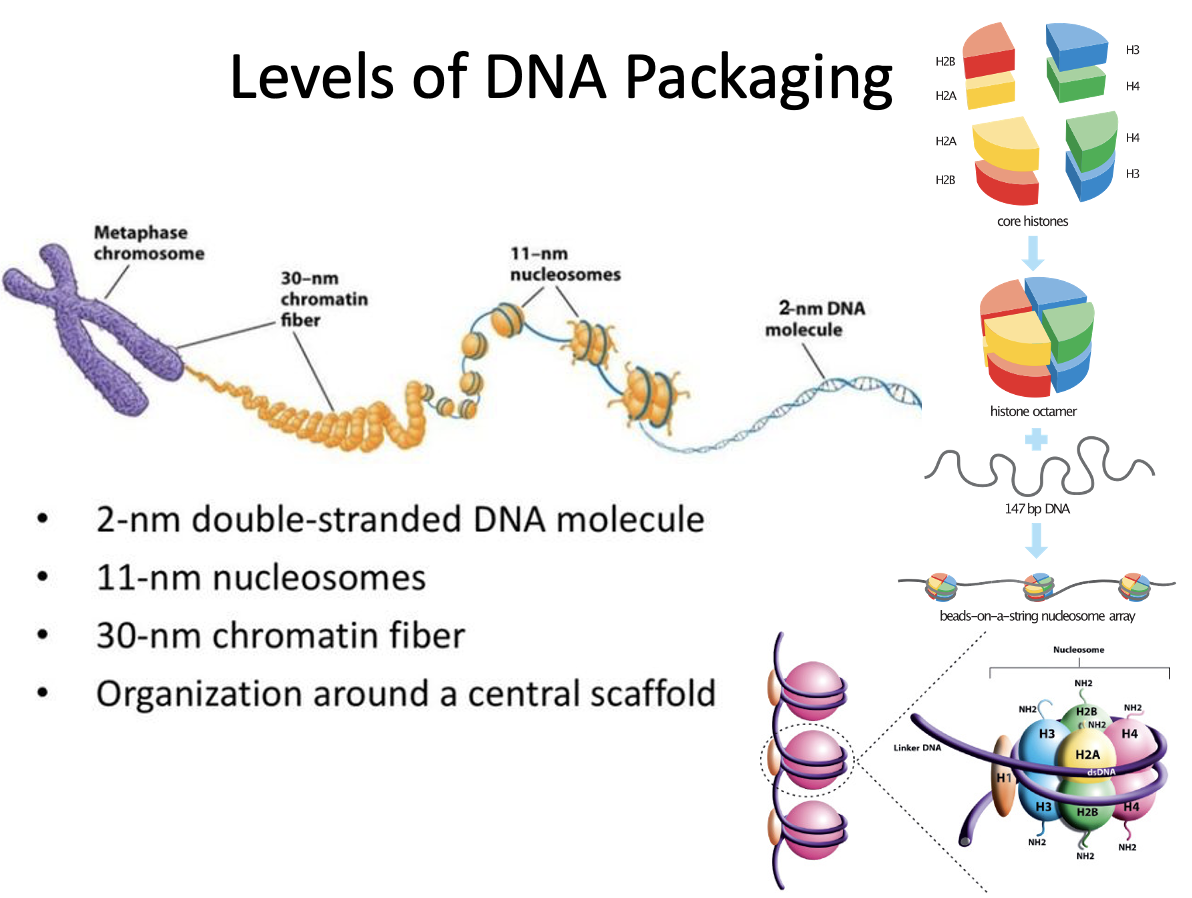
ה־DNA מלופף סביב נוקלאוזומים. כשהכרומטין פתוח יותר, למשל במבנה של “beads on a string”, קל יותר לבצע שעתוק. כשהכרומטין דחוס יותר, השעתוק קשה יותר.
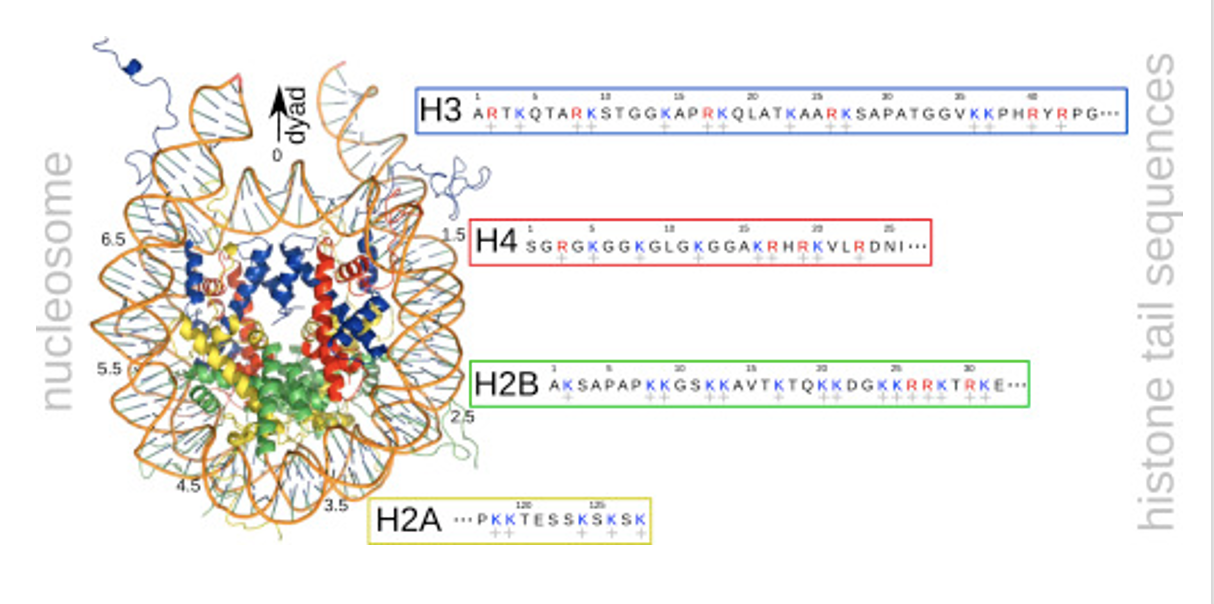
לכל היסטון יש Histone tail, אזור בקצה ה־N-טרמינלי. הזנבות עשירים בליזינים וארגינינים, שהם חומצות אמינו טעונות חיובית. מכיוון שה־DNA טעון שלילית, הזנבות עוזרים להחזיק אותו סביב ההיסטונים.
אצטילציה
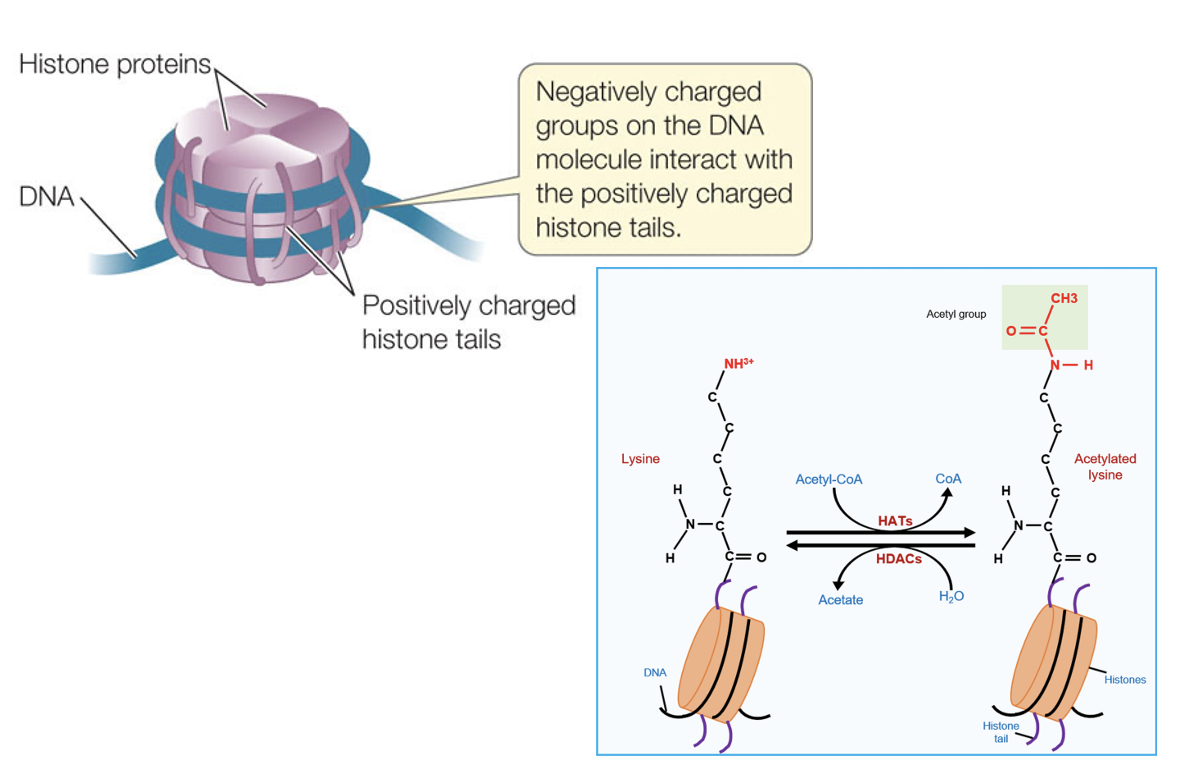
אצטילציה על ליזינים בהיסטונים מפחיתה את האינטראקציה החזקה בין הזנבות החיוביים לבין ה־DNA השלילי. לכן היא קשורה לפתיחת הכרומטין ולאפשרות לשעתוק.
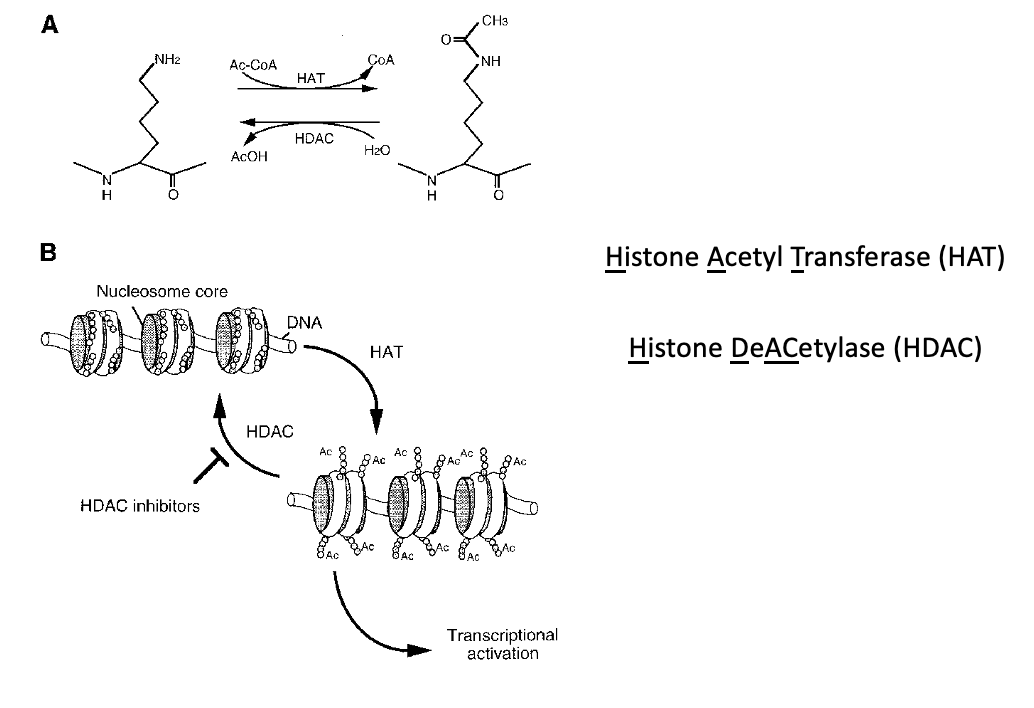
| אנזים | פעולה | משמעות כללית |
|---|---|---|
| HAT Histone acetyltransferase | מוסיף קבוצת אצטיל | קשור לפתיחת כרומטין ושעתוק |
| HDAC Histone deacetylase | מסיר קבוצת אצטיל | קשור לסגירת כרומטין/הורדת שעתוק |
מתילציה
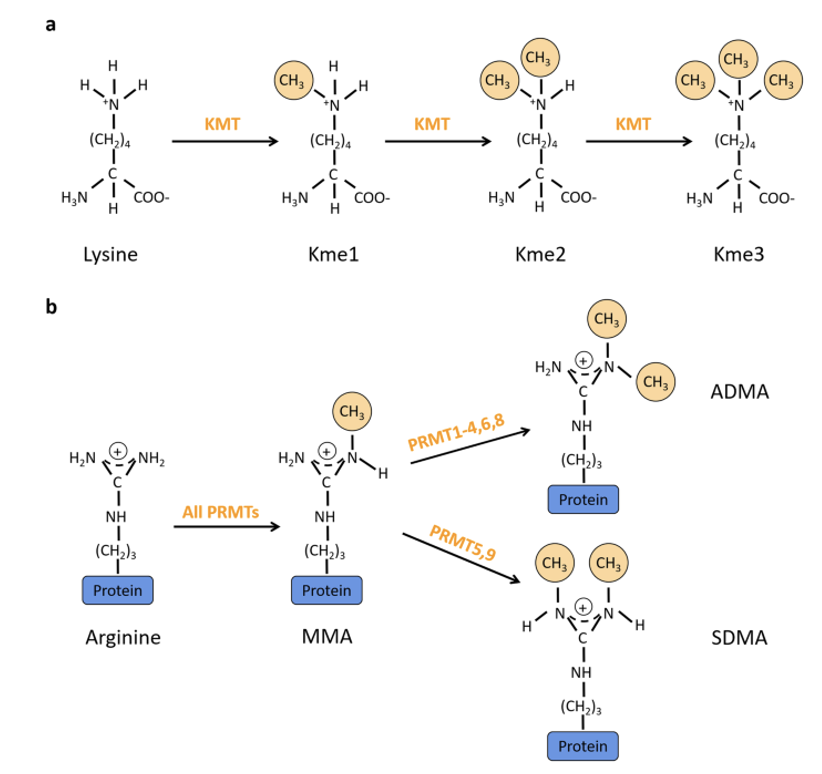
מתילציה יכולה להתרחש על ליזין או על ארגינין בזנבות ההיסטונים.
ההשפעה שלה נקבעת לפי ההקשר המדויק: סוג ההיסטון, החומצה האמינית שעברה מתילציה, המיקום שלה ברצף, וחלבוני ה־reader שיודעים לזהות את הסימון בתא.
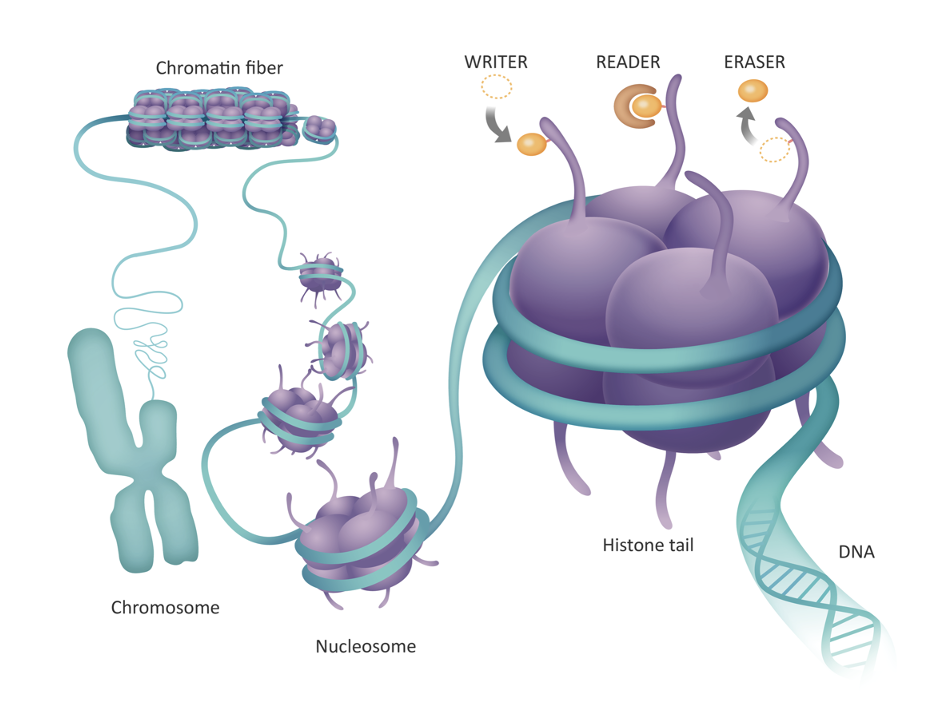
כאן נכנסים שלושה סוגי שחקנים:
| מושג | תפקיד |
|---|---|
| Writer | מוסיף מודיפיקציה, למשל קבוצת מתיל |
| Reader | מזהה את המודיפיקציה ומתרגם אותה לפעולה תאית |
| Eraser | מסיר את המודיפיקציה |
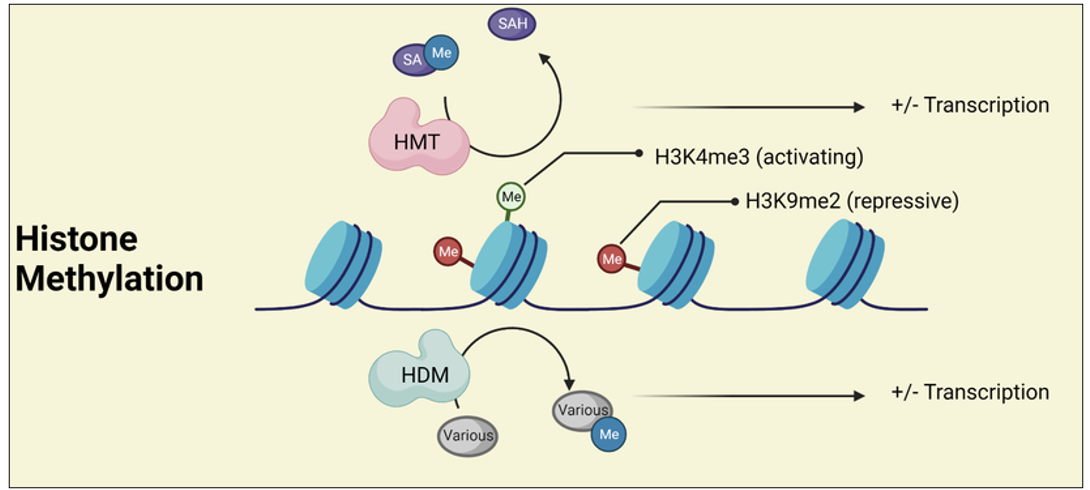
לדוגמה, מתילציה על H3K4 יכולה להיקרא על ידי readers שמובילים להפעלת שעתוק, ואילו מתילציה על H3K9 יכולה להיקרא בהקשרים אחרים כרפרסיה.
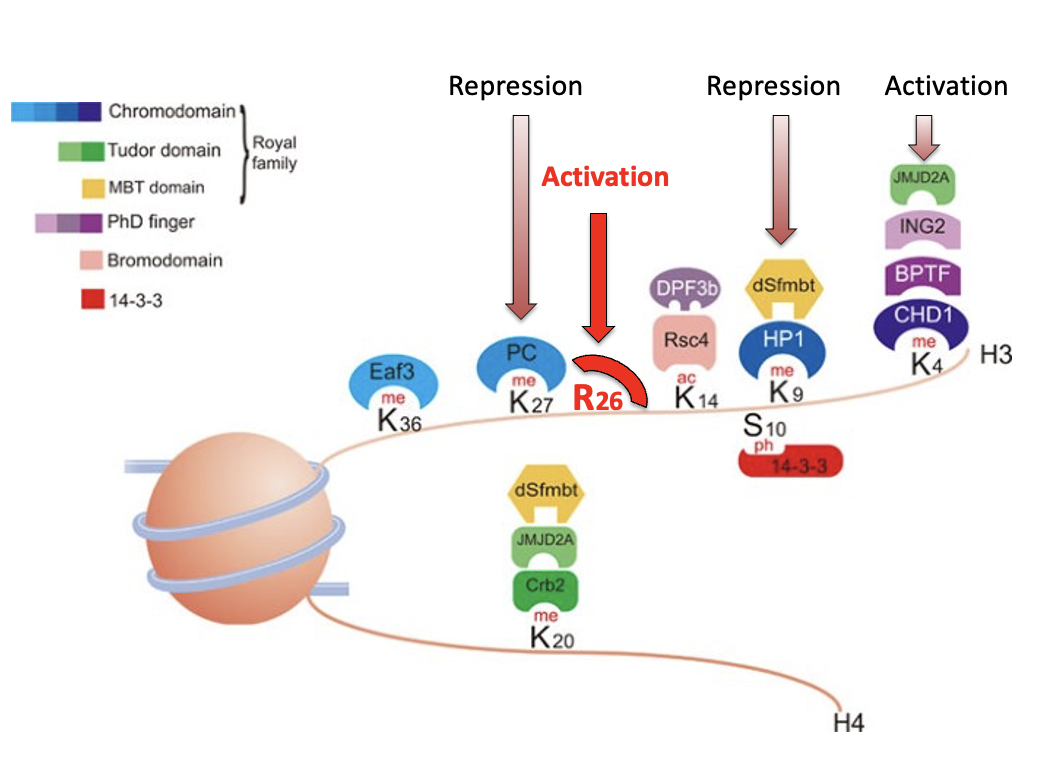
זו הסיבה שמדברים על קוד אפיגנטי: התא לא “רואה” רק שיש מתילציה, אלא קורא את המיקום המדויק שלה ומתרגם אותה למשמעות ביולוגית.
H3R26me ו־Carm1
המודיפיקציה המרכזית שהוצגה היא מתילציה של Histone H3 arginine 26, כלומר H3R26me.
כאשר ארגינין 26 בהיסטון H3 עובר מתילציה, יש reader שמסוגל לזהות את הסימון הזה, ובקונטקסט שהוצג הוא קשור לאקטיבציה של שעתוק.
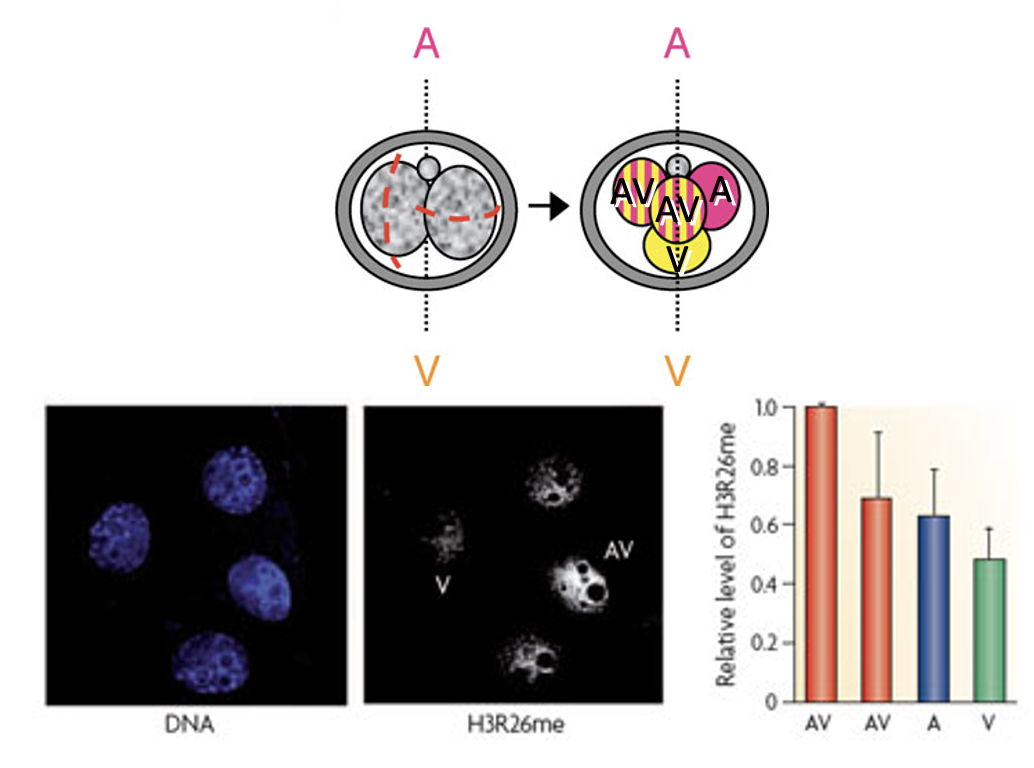
כשצובעים עובר בשלב ארבעת התאים ל־H3R26me, רואים שבמבנה טטרהדרלי מסוג ME/EM התאים נצבעים בעוצמה שונה; יש תא עם רמה גבוהה יותר של הסימון, ואחרים עם רמות נמוכות יותר.
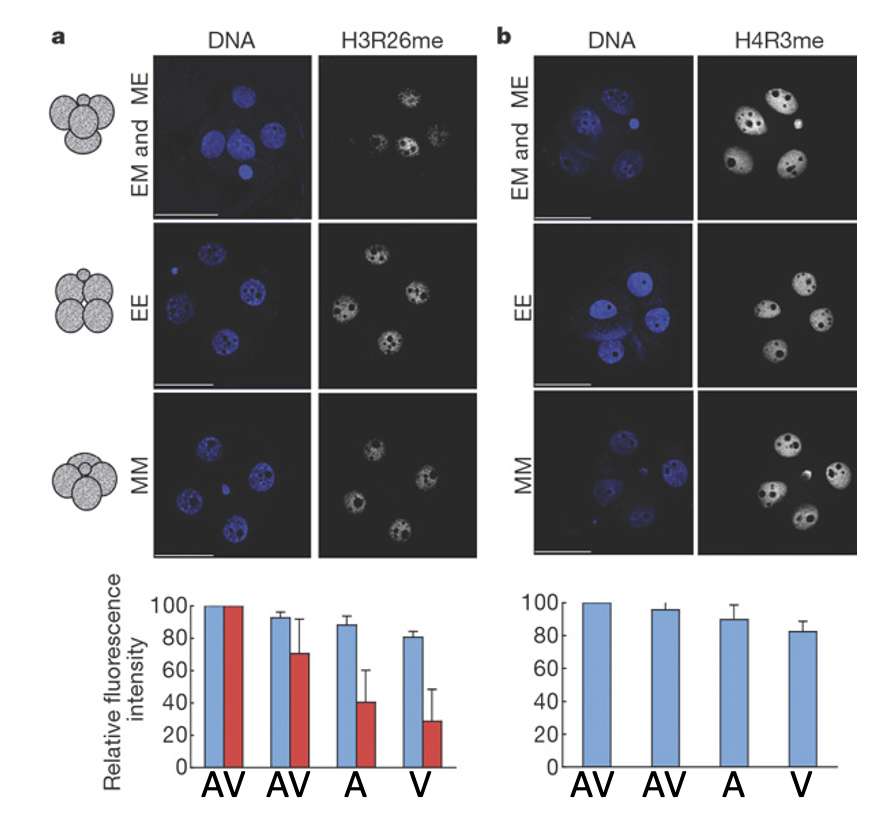
ההבדל מופיע בצורה ספציפית: הוא קשור למודיפיקציה מסוימת, בשלב ארבעת התאים, ובחלוקה לא שווה בין הבלסטומרים.
כלומר, לא מדובר בשינוי אפיגנטי כללי, אלא בסימון מסוים שיכול ליצור הטיה מוקדמת בין התאים.
האנזים שעושה את המתילציה - Carm1
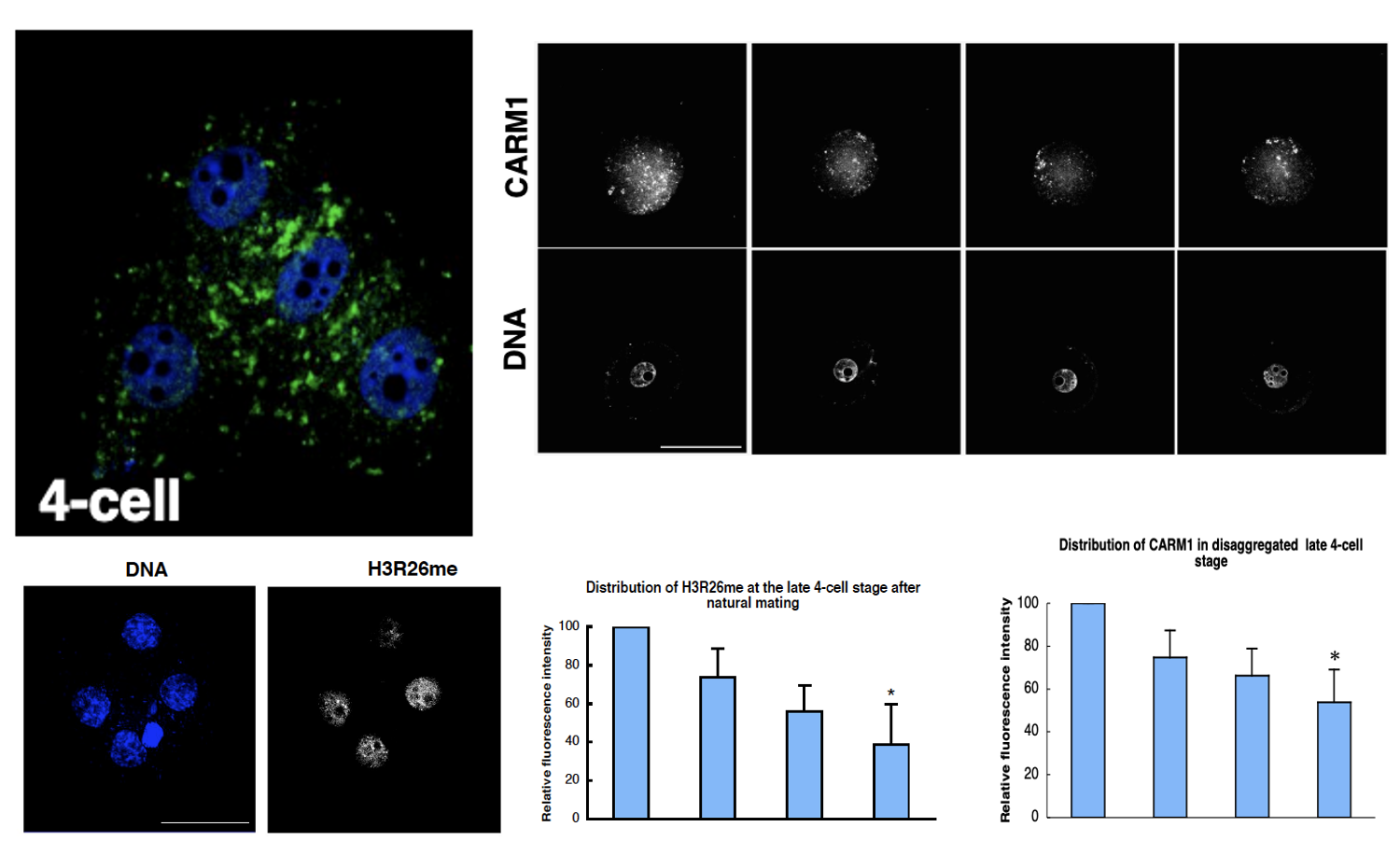
האנזים שמבצע את המתילציה הזאת הוא Carm1. בצביעה ל־Carm1 בעובר של ארבעה תאים רואים שיש תא אחד שמבטא יותר Carm1 מתאים אחרים. הדבר מתאים לרעיון שיש קשר בין רמות Carm1 לבין רמות H3R26me.
אבל קורלציה אינה מספיקה. השאלה הבאה היא האם ההבדל הזה משפיע על ההתפתחות.
העלאת Carm1 בתא אחד
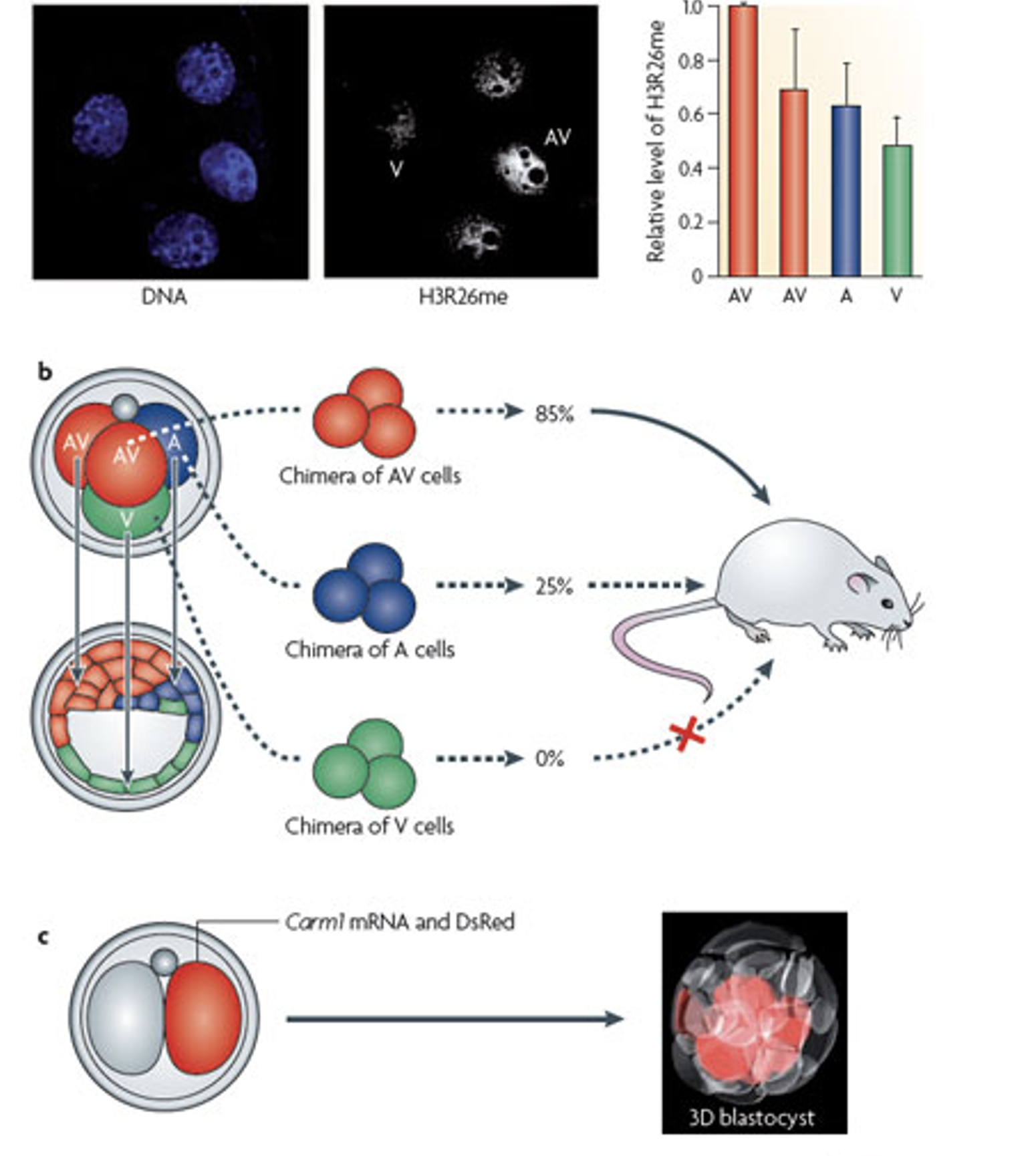
בניסוי מזריקים לתא אחד בעובר של שני תאים:
- mRNA שמקודד לסמן אדום, כדי לעקוב אחרי צאצאי התא.
- mRNA שמקודד ל־Carm1, כדי להעלות את רמות Carm1 באותו תא.
כאשר בודקים את הבלסטוציסט, התאים האדומים נמצאים בעיקר ב־ICM וכמעט לא ב־Trophectoderm.
המסקנה היא שהעלאת Carm1 בתא אחד מטה את הצאצאים שלו לכיוון פנימי/ICM. כדי שתא יהיה פנימי, הוא צריך להוריד את Cdx2. לכן Carm1 והמתילציה הקשורה אליו משתתפים בהטיית ה־First cell fate decision.
חשוב לדייק: הניסוי לא אומר שכל גורל התא נקבע רק על ידי Carm1. הוא מראה ש־Carm1 יכול להטות את הפוטנציאל ההתפתחותי של התא.
Long non-coding RNAs ו־LincGET
כדי להבין למה Carm1 פעיל בצורה שונה בין תאים, צריך להכיר את Long non-coding RNAs.
Long non-coding RNA הוא RNA שאינו מקודד לחלבון ואורכו מעל 200 נוקלאוטידים.
C-value paradox ו־G-value paradox
| פרדוקס | מה השאלה? | כיוון ההסבר שהוצג |
|---|---|---|
| C-value paradox | למה אין התאמה פשוטה בין כמות ה־DNA לבין מורכבות האורגניזם? | בעבר דיברו על “junk DNA”; היום ברור שיש יותר מורכבות רגולטורית |
| G-value paradox | למה מספר הגנים המקודדים לחלבונים דומה יחסית בין אורגניזמים שונים מאוד? | בין היתר Alternative splicing ו־non-coding RNAs |
LincGET
LincGET הוא long non-coding RNA. הוא אינו מקודד לחלבון, אבל יש לו תפקיד רגולטורי. הוא מופיע בשלב מוקדם מאוד של ההתפתחות.
כמה LincGET מתבטא בכל שלב
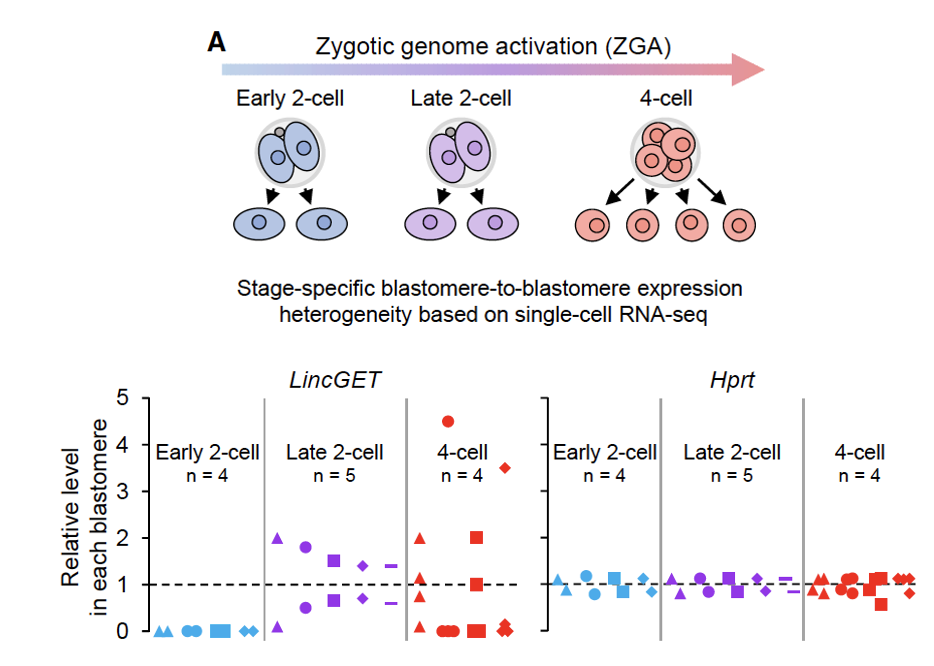
כאשר מודדים את LincGET לאורך ההתפתחות, רואים שהוא כמעט לא מתבטא באואוציט, עולה אחרי Zygotic genome activation, מגיע לפיק סביב שלב שניים-ארבעה תאים, ובהמשך יורד.
בבדיקה ברמת תא בודד, LincGET אינו מתבטא באותה רמה בכל הבלסטומרים. לעומת זאת, גן ביקורת מסוג housekeeping gene, כמו Hprt, מתבטא בצורה דומה בין התאים. לכן ההבדל אינו תוצאה של בעיה כללית במדידה, אלא תכונה של LincGET.
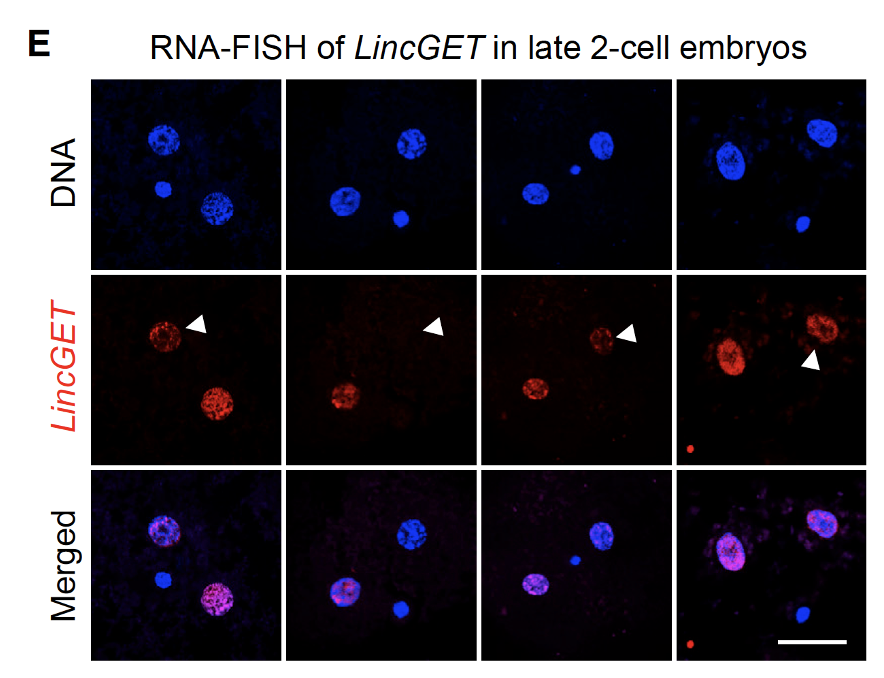
ב־RNA-FISH רואים ש־LincGET נמצא בעיקר בגרעין. זה מתאים לכך שהוא אינו mRNA רגיל שמיועד לצאת לציטופלזמה ולהיתרגם לחלבון, אלא RNA רגולטורי שפועל בגרעין.
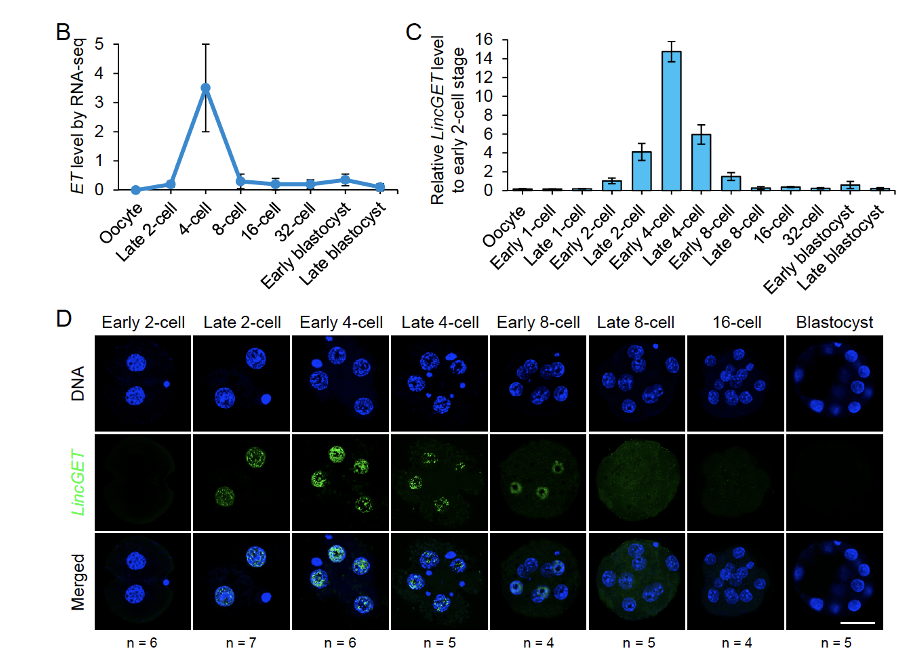
הנקודה המרכזית: כבר בשלב שני התאים, מיד אחרי ZGA, יש הבדל ברמות LincGET בין הבלסטומרים. זה מוקדם יותר מההבדלים הברורים ב־Carm1 וב־H3R26me שנראים במיוחד בשלב ארבעת התאים.
המודל: LincGET, Carm1, Sox2/Nanog ו־Cdx2
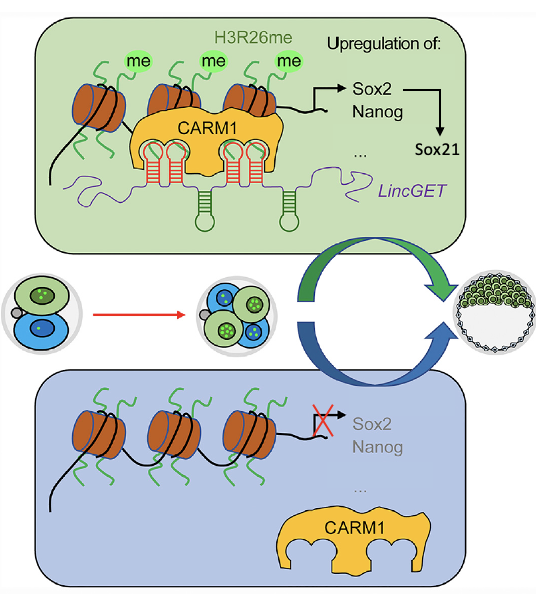
מתברר ש־Carm1 אינו מספיק בפני עצמו. כדי להיות פעיל, Carm1 צריך לקשור את LincGET. כלומר, LincGET ו־Carm1 יוצרים קומפלקס, והקומפלקס הזה מאפשר ל־Carm1 לבצע מתילציה על H3R26.
הקשר בין כל הרכיבים:
LincGET
↓ binds
Carm1 activation
↓
H3R26me
↓
activation of Sox2 / Nanog
↓
repression of Cdx2
↓
Bias toward ICM / inner-cell fate
אם LincGET מתבטא ברמה גבוהה יותר בתא מסוים, Carm1 יהיה פעיל יותר באותו תא. פעילות Carm1 מובילה ליותר H3R26me, והסימון הזה מאפשר ביטוי של גנים כמו Sox2 ו־Nanog.
כאשר Sox2 ו־Nanog עולים אפילו מעט, הם יכולים להשפיע על רשת פקטורי השעתוק:
- Sox2 ו־Nanog תומכים בכיוון ICM/פלוריפוטנטיות
- Sox2 יכול להעלות גם את Sox21
- Sox21 משתתף בדיכוי Cdx2
- ירידת Cdx2 מאפשרת לתא ללכת לכיוון פנימי יותר
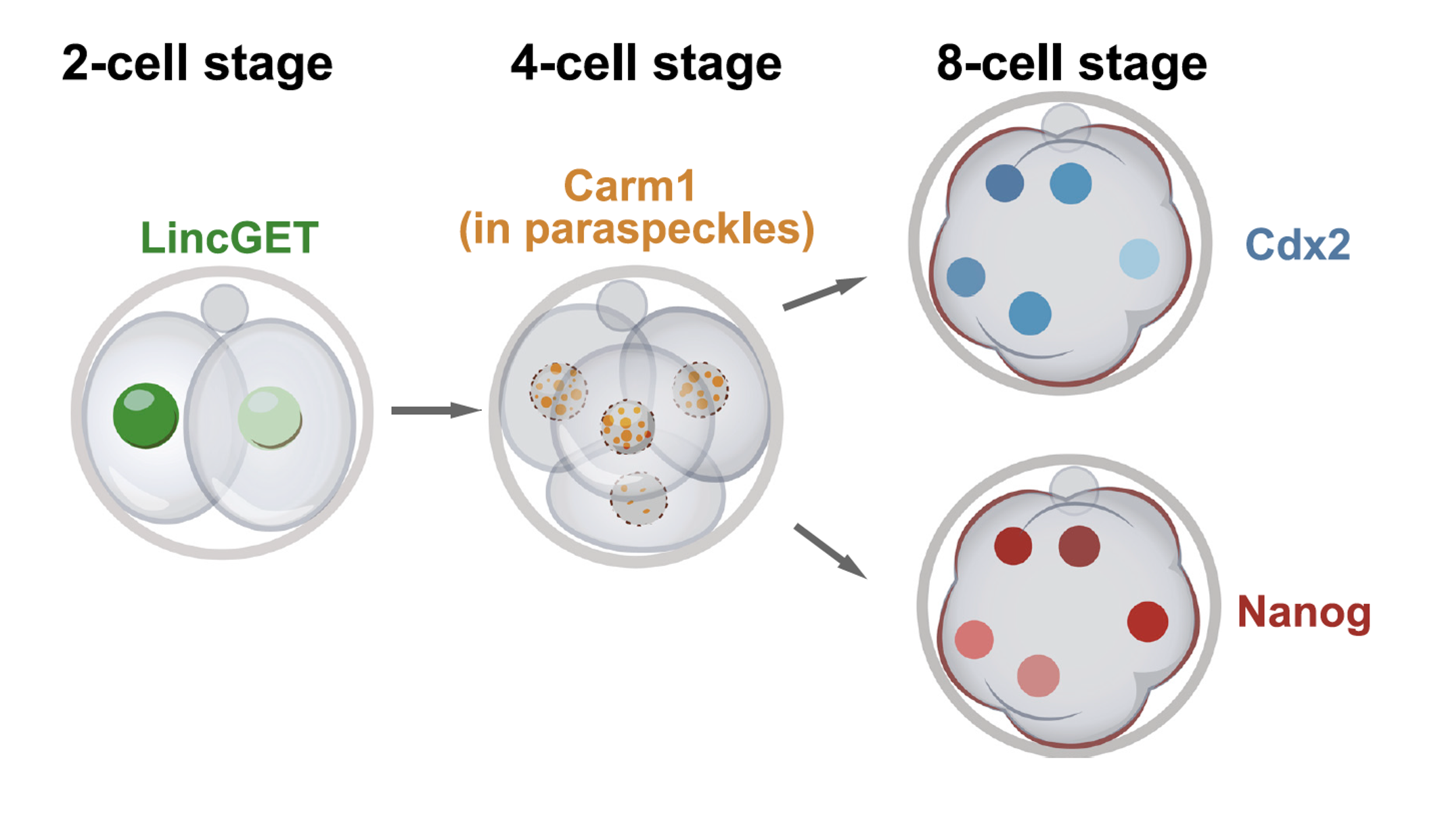
המודל המסכם:
- בשלב שני התאים יש כבר הבדל ברמות LincGET בין שני הבלסטומרים.
- Carm1 נמצא בשני התאים, אבל פעילותו תלויה ב־LincGET.
- תא עם יותר LincGET מפעיל יותר Carm1.
- Carm1 יוצר יותר H3R26me.
- H3R26me מאפשר ביטוי של Sox2/Nanog.
- Sox2/Nanog מורידים את Cdx2.
- ירידת Cdx2 מטה את התא לכיוון ICM.
זה מודל של הטיה התחלתית: LincGET ו־Carm1 מעלים את הסיכוי למסלול ICM, וכך מתחילה שבירת סימטריה בעובר שנראה בתחילה סימטרי.
פולריזציה ו־Compaction: קשורים אך בלתי תלויים
חזרנו לקשר בין Polarization לבין Compaction.
בשיעור הקודם הובהר שפולריזציה וקומפקשן מתרחשים סביב שלב שמונת התאים, ושניהם קשורים ל־First cell fate decision. כאן מתחדדת הנקודה שהם קשורים זה לזה, אבל אינם אותו תהליך ואינם תלויים לחלוטין זה בזה.
איך נוצרת פולריזציה?
בתהליך הפולריזציה, פילמנטים של אקטין מתחילים להתארגן באזור האפיקלי, ובהמשך מגויסים חלבוני apical polarity complex. הגיוס מתחיל באזור מרכזי של הממברנה האפיקלית, ולאחר מכן החלבונים נדחפים לצדדים ונוצרת טבעת actomyosin.
בתהליך משתתפים בין היתר:
| רכיב | תפקיד כללי שהוצג |
|---|---|
| Tfap2c | פקטור שעתוק הקשור לגיוס חלבוני פולריות |
| Tead4 | פקטור שעתוק נוסף; מוכר גם מהקשר למסלול Hippo |
| Rho | small G protein שמעורב בארגון מחדש של הציטוסקלטון |
לאחר Zygotic genome activation, Tfap2c ו־Tead4 מתחילים להתבטא. הרמות שלהם עולות עד סף מסוים, וסביב שלב שמונת התאים מתרחשת פולריזציה.
הטיית המקרה - לגרום לפולריזציה להתרחש בארבעה תאים
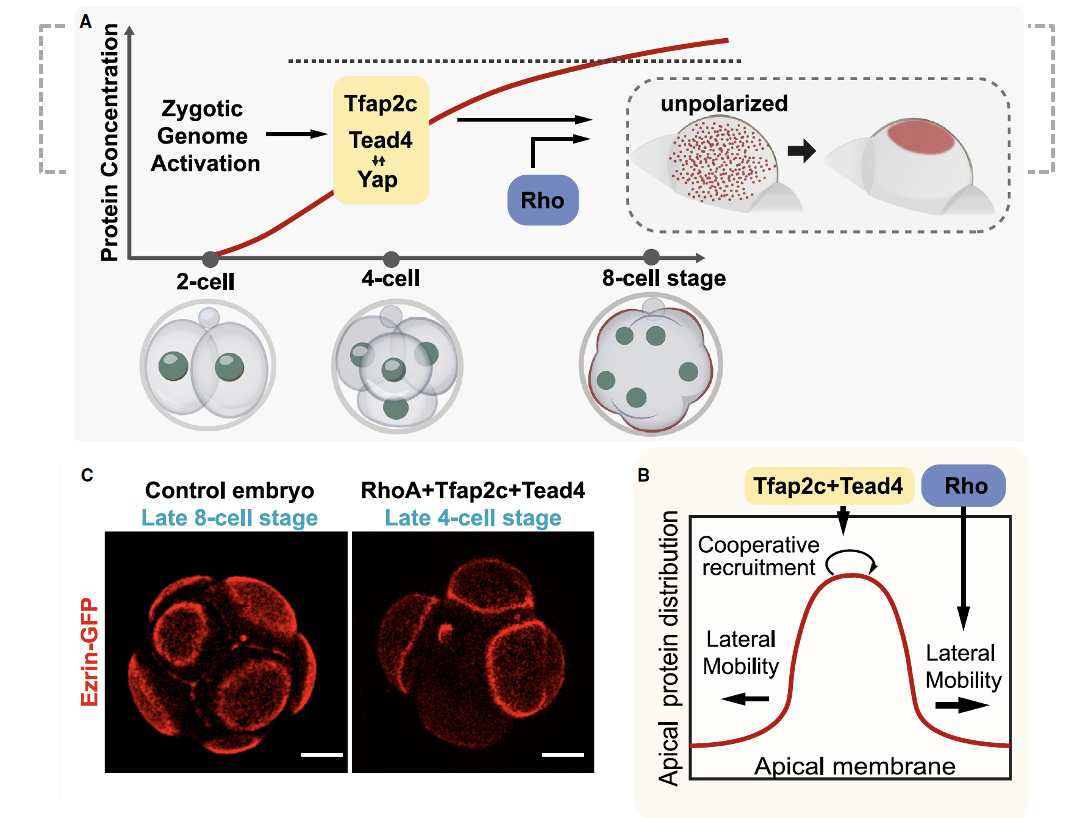
בניסוי, מזריקים לזיגוטה mRNA שמקודד ל־Rho, Tfap2c ו־Tead4. כך מעלים מוקדם את רמות החלבונים האלה, לפני הזמן שבו הם היו עולים באופן טבעי אחרי ZGA.
התוצאה: הפולריזציה יכולה להתרחש כבר בשלב ארבעת התאים.
המסקנה היא שפולריזציה אינה תלויה לחלוטין בקומפקשן. אפשר להקדים אותה בניסוי. מצד שני, בבלסטומר רגיל בתוך עובר, קומפקשן ו־Adherens junctions עוזרים לכוון את הפולריות לצד האפיקלי, כלומר לצד שפונה החוצה / לכיוון ה־Zona Pellucida.
אם מפרידים תאים ושמים אותם בצלחת, הם עדיין יכולים להפוך לפולריים, אבל כיוון הפולריות יהיה אקראי יותר. לכן:
פולריזציה יכולה להתרחש גם בלי קומפקשן, אבל קומפקשן עוזר למקם את הפולריות במקום הנכון בתוך העובר.
רצף האירועים המרכזי
Zygote / one-cell embryo
↓
Animal-vegetal axis defined by polar body
↓
First cleavage roughly parallel to animal-vegetal axis
↓
2-cell embryo
├─ LincGET appears asymmetrically after ZGA
└─ Carm1 protein may be present, but activity depends on LincGET
↓
4-cell embryo
├─ Different division patterns: ME/EM, MM, EE
├─ ME/EM is most frequent → probabilistic, not stochastic
├─ H3R26me appears asymmetrically in tetrahedral embryos
└─ Carm1/H3R26me biases cells toward Sox2/Nanog and lower Cdx2
↓
8-cell embryo
├─ Compaction
├─ Polarization
└─ Different Cdx2 levels between cells
↓
First cell fate decision
├─ Higher Cdx2 / polarity / outer position
│ ↓
│ Trophectoderm
│
└─ Lower Cdx2 / Sox2-Nanog bias / inner position
↓
ICM
משפטי מפתח
- שבירת סימטריה מתחילה לפני שרואים הבדל מורפולוגי ברור בין התאים.
- ביונקים ההתפתחות רגולטיבית, ועדיין בלסטומרים מוקדמים יכולים להיות שונים בפוטנציאל שלהם.
- ההבדלים בין בלסטומרים מוקדמים הם בעיקר הטיות פרובביליסטיות: הם משנים הסתברויות, בלי לנעול גורל סופי.
- מישור החלוקה הראשון מקביל בקירוב לציר animal-vegetal, ולכן כבר בזיגוטה יש כיוון מרחבי חשוב.
- Cell lineage analysis מראה שאין ערבוב גדול של צאצאי שני הבלסטומרים, ושהציר embryonic-abembryonic קשור לציר animal-vegetal.
- שני הבלסטומרים הראשונים אינם שקולים לחלוטין מבחינת פוטנציאל התפתחותי.
- ההבדל העיקרי בין twin ו־co-twin קשור ליכולת לייצר ICM/Epiblast, ובמיוחד למספר תאי Nanog+.
- בשלב ארבעת התאים, סוגי החלוקה ME/EM, MM ו־EE אינם מופיעים בשכיחות שווה; זהו דפוס פרובביליסטי.
- H3R26me הוא אירוע אפיגנטי ספציפי שמופיע ברמות שונות בין בלסטומרים.
- Carm1 מטה תאים לכיוון פנימי/ICM, כנראה דרך H3R26me והפעלת Sox2/Nanog.
- LincGET הוא long non-coding RNA שמתבטא מוקדם, ברמות שונות בין בלסטומרים, ומפעיל את Carm1.
- פולריזציה ו־Compaction קשורים, אבל אינם אותו תהליך: פולריזציה יכולה להתרחש בלי קומפקשן, וקומפקשן עוזר למקם אותה בכיוון הנכון.