תוכן העניינים:
- מבוא: למה צריך RNA כמתווך?
- תהליך השעתוק (Transcription)
- עיבוד ה־mRNA
- שחבור (Splicing)
- תרגום (Translation)
- בקרת ביטוי גנים
- בקרה ברמת השעתוק
- בקרה ברמת התרגום
- בקרה לאחר התרגום
- סיכום רמות הבקרה
- שאלות תרגול מג׳ונרטות
מבוא: למה צריך RNA כמתווך?
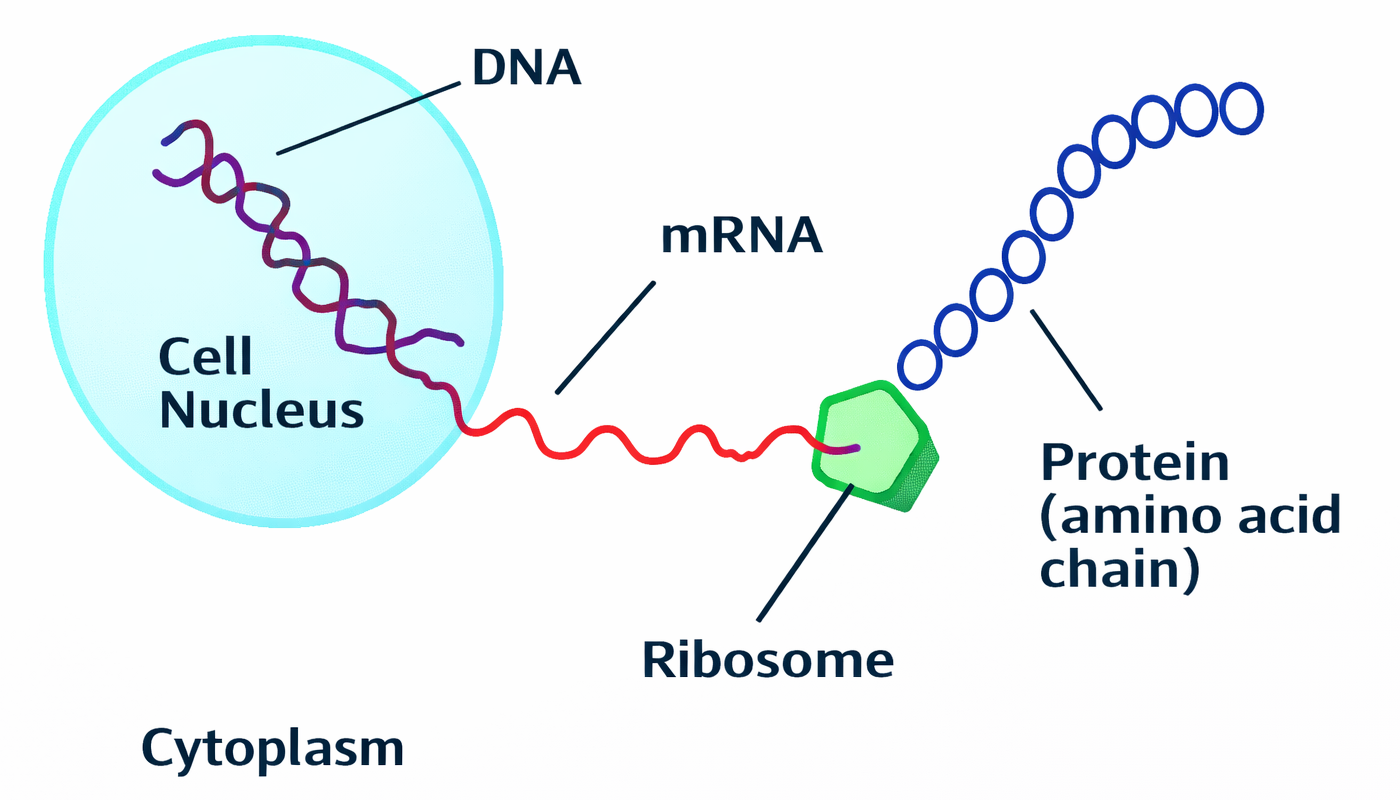
סיבות לקיום ה־mRNA
-
שמירה על ה־DNA: ה־DNA הוא המידע החשוב ביותר בתא. כל שינוי בו עשוי להשפיע על התכונות שלנו ולגרום למחלות כמו סרטן. לכן ה־DNA נשמר בגרעין (כמו בכספת), מוגן על ידי ממברנה, ולא בא במגע ישיר עם אנזימים בציטופלזמה
-
יעילות: ה־DNA הוא רצף ארוך מאוד. במקום לחבר את כל הכרומוזום לריבוזום, שולחים מקטעים קצרים וברורים של RNA.
-
הגברת ייצור: ניתן לייצר עותקים רבים של mRNA מאותו גן, ובכך לייצר כמויות גדולות של חלבון במהירות.
תהליך השעתוק (Transcription)
שעתוק מתבצע על ידי האנזים RNA פולימראז.
ה־RNA החדש תמיד נבנה מ־5’ ל־3’, ולכן ה־RNA פולימראז מתקדם על גבי גדיל התבנית של ה־DNA בכיוון 3’ ל־5’.
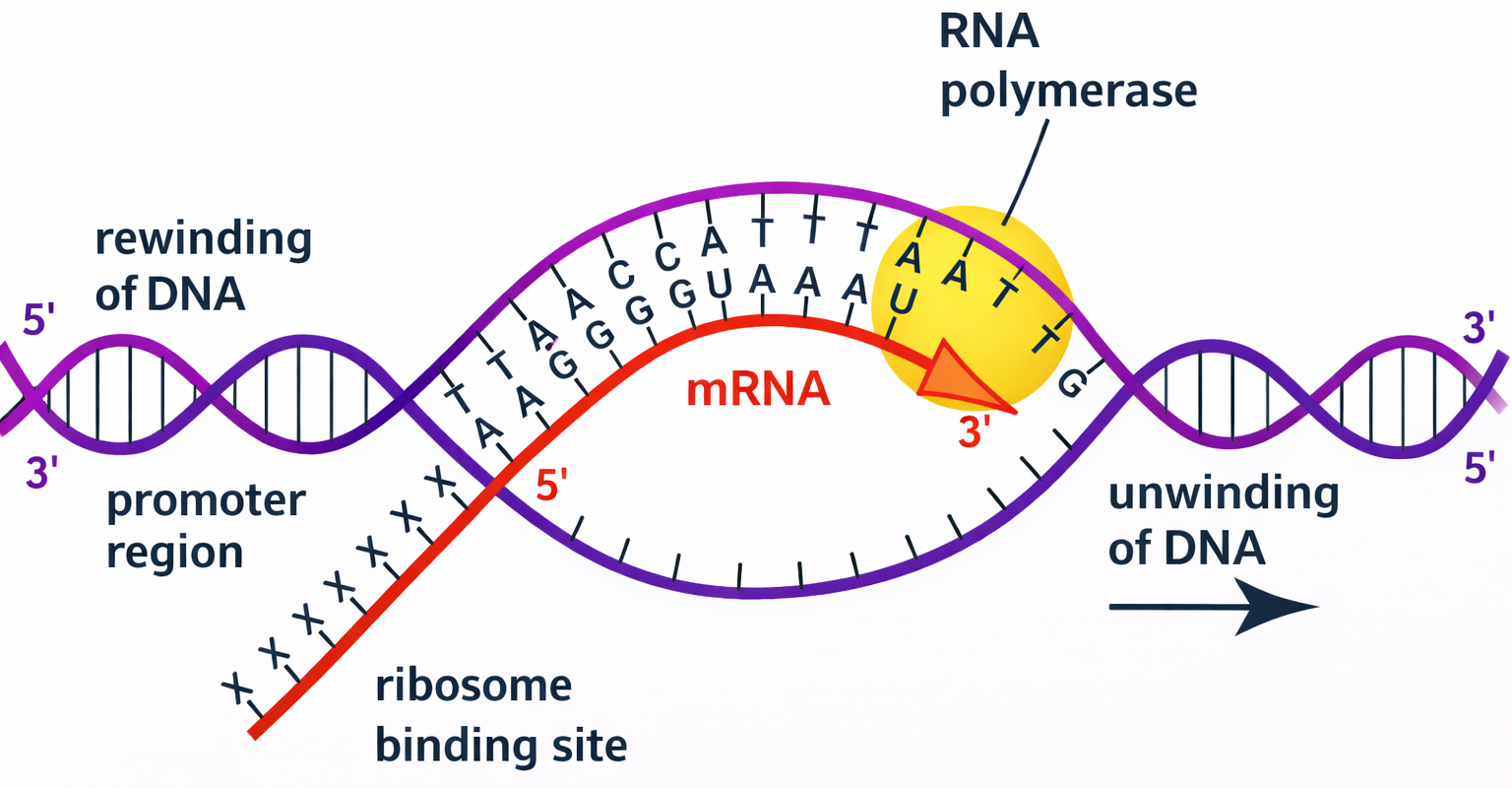
מושגי יסוד
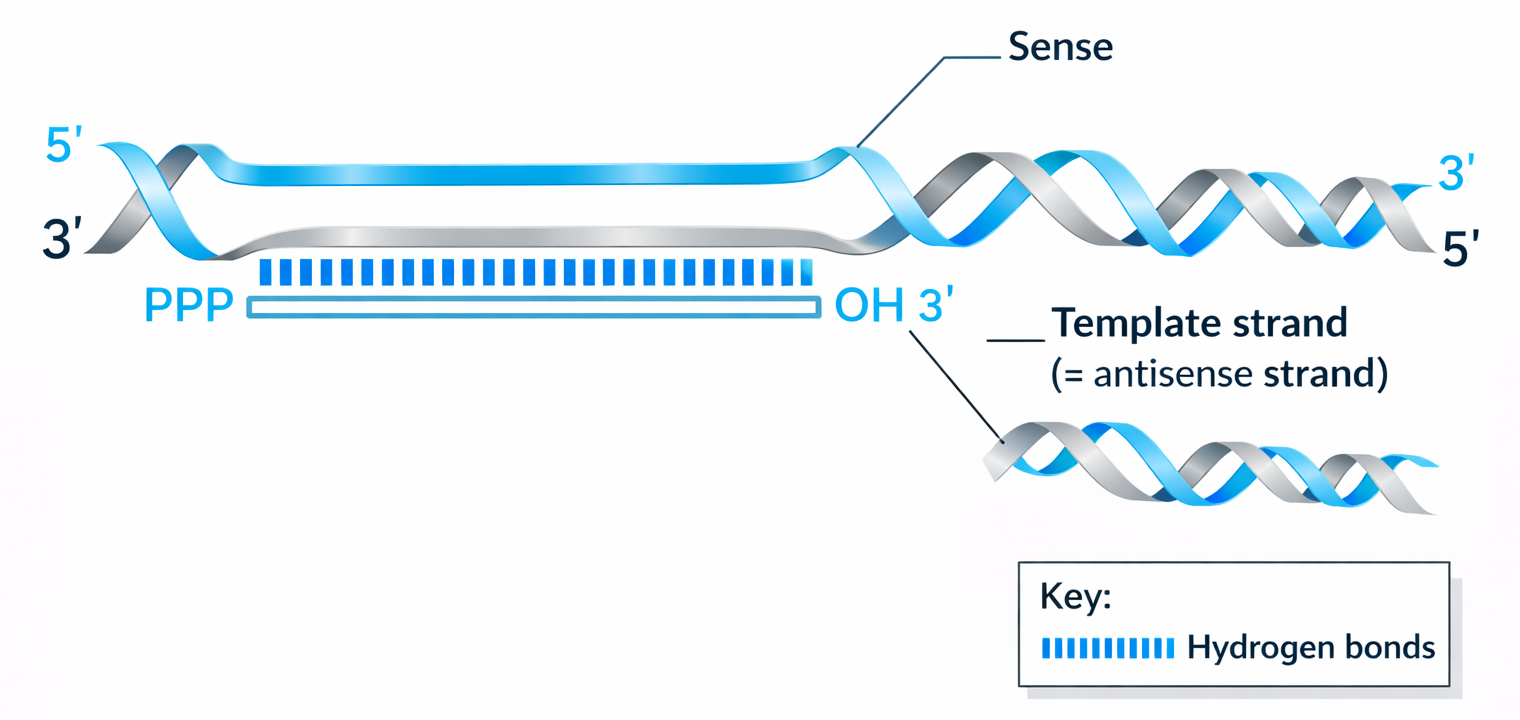
- גדיל Antisense - גדיל ה־DNA שמשמש כתבנית ליצירת ה־mRNA (בכיווניות הפוכה לגדיל שנוצר)
- גדיל Sense - הגדיל שלא משמש כתבנית, אך דומה מאוד לרצף ה־RNA עצמו
- הערה חשובה: הגדיל שמשמש כ־Antisense אינו קבוע - עבור כל גן יש Antisense ספציפי שונה.
RNA פולימראז - “סופר־אנזים”
RNA פולימראז מבצע מספר פעולות:
- פתיחה והפרדה בין גדילי ה־DNA (ללא צורך ב־Helicase)
- חיבור נוקלאוטידים משלימים
- אינו צריך פריימר להתחלת הסינתזה
מיקום השעתוק
| אורגניזם | מיקום |
|---|---|
| איקריוטים | בתוך הגרעין |
| פרוקריוטים | בציטופלזמה |
עיבוד ה־mRNA

יציבות ה־RNA
- RNA פחות יציב מ־DNA פי 100 בגלל:
- חד־גדילי (לא דו־גדילי)
- סוכר ריבוז (במקום דאוקסיריבוז)
- בסיס
UבמקוםT
- זמן מחצית חיים: דקות עד שעות (מקסימום יום-יומיים)
- יוצא דופן: mRNA בביציות - נשמר לאורך זמן רב
תוספות לקצוות ה־mRNA
Cap (קצה 5’)
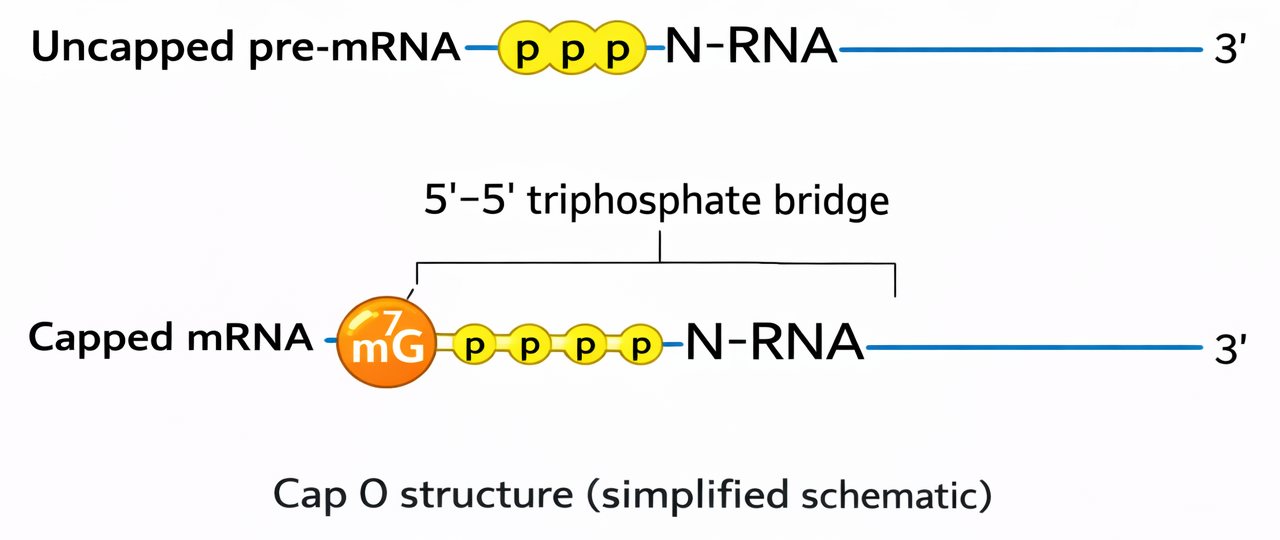
- מולקולת GTP הקשורה הפוך לרצף
- אנזים: Guanyl Transferase
- תפקידים:
- הגנה מפני אקסונוקלאזות
- סימון כיווניות
- זיהוי על ידי הריבוזום
זנב Poly-A (קצה 3’)
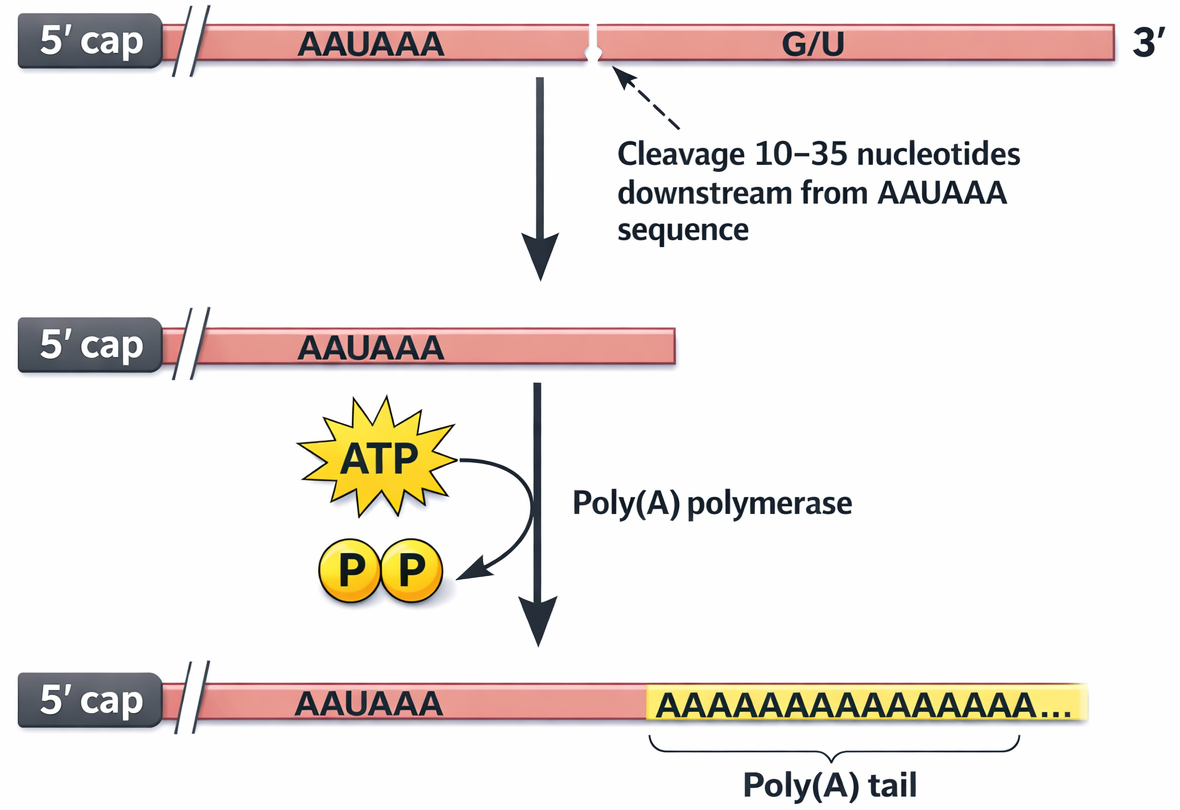
- רצף של כ־200 אדנינים (
A) - אנזים: Poly-A Polymerase. מזהה בסוף השעתוק את רצף ה־AAUAAA (terminator) ומוסיף את הזנב
- ככל שהזנב ארוך יותר, ה־mRNA יציב יותר
שחבור (Splicing)
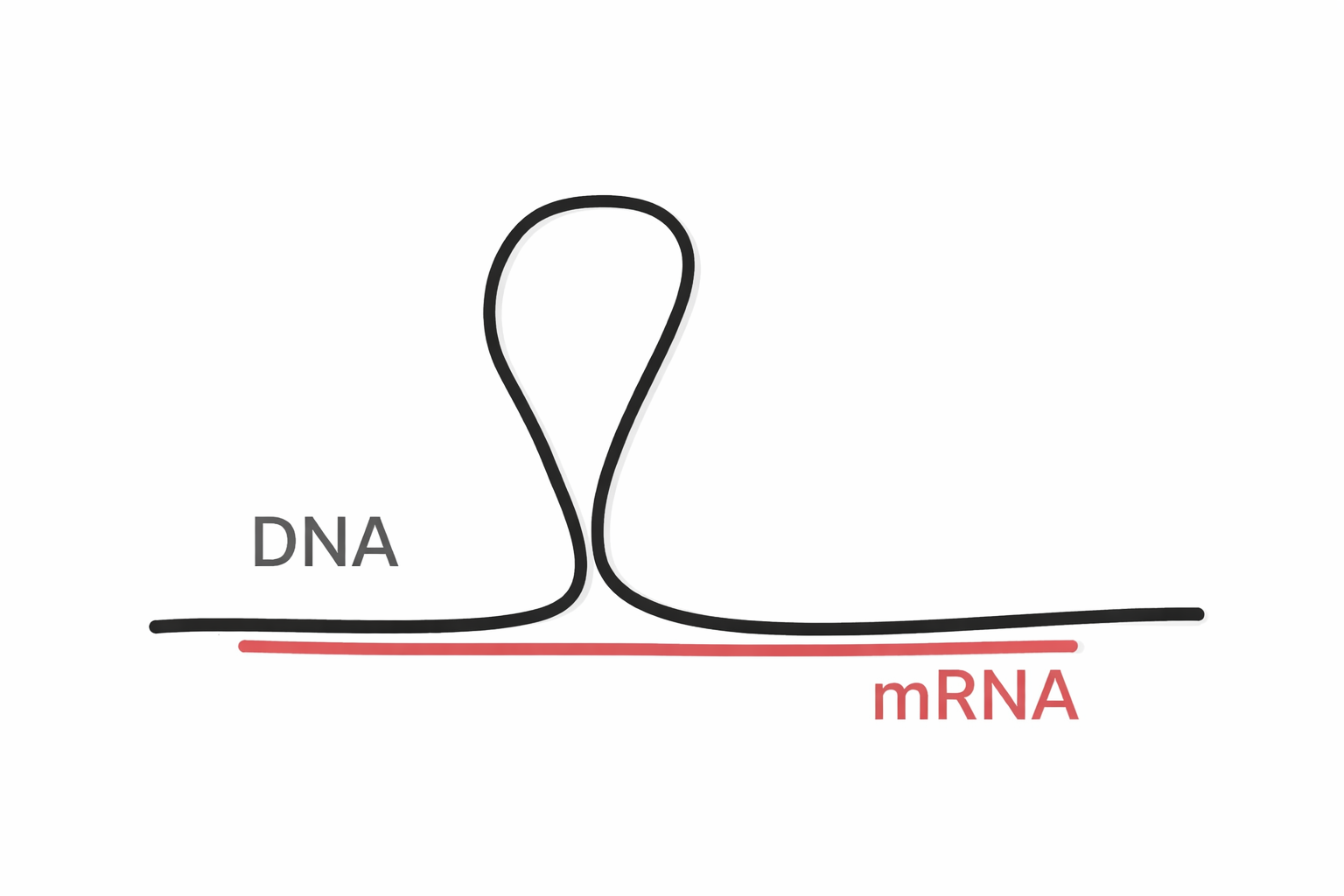
אקסונים ואינטרונים
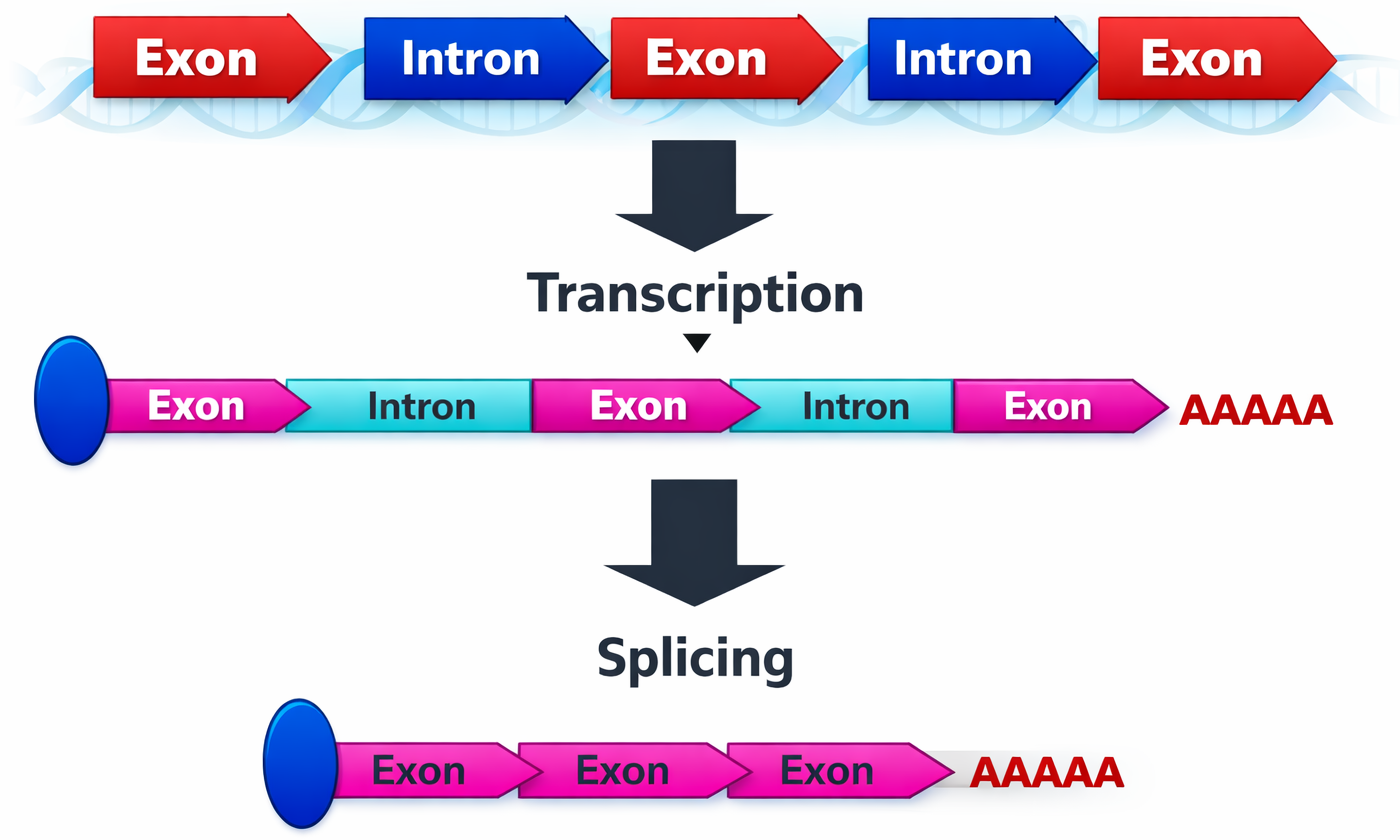
- אקסונים - אזורים מקודדים (יישארו ב־mRNA הבשל)
- אינטרונים - אזורים לא מקודדים (נחתכים החוצה)
מאפייני רצף האינטרון
| מיקום | רצף |
|---|---|
| תחילת אינטרון | GU |
| סוף אינטרון | AG |
| כ־30 בסיסים מהסוף | A בודד |
מנגנון השחבור - Spliceosome
- מורכב מ־snRNPs (Small Nuclear Ribonucleoproteins)
- יחידות: U1, U2, U4, U5, U6 (אין U3)
- התהליך דורש אנרגיה
הבדלים בין אורגניזמים
| אורגניזם | אחוז גנים עם אקסון יחיד |
|---|---|
| שמר | 95% |
| דרוזופילה | 17% |
| יונקים | מיעוט (עד 40-30 אקסונים לגן) |
בפרוקריוטים אין אינטרונים כלל!
שחבור חליפי (Alternative Splicing)
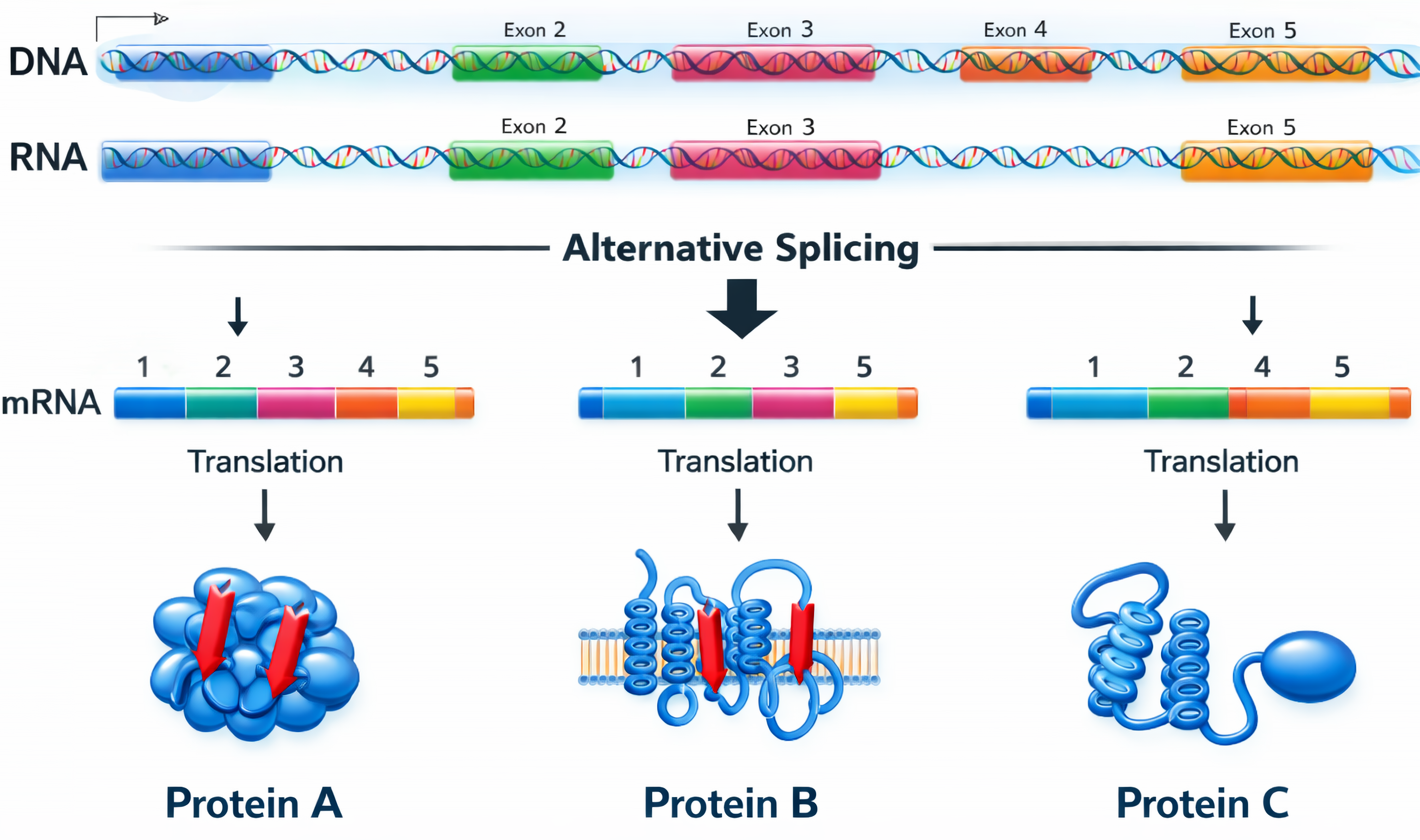
- מאפשר יצירת חלבונים שונים מאותו גן
- לפעמים נחתכים אקסונים יחד עם האינטרונים
- יכול להיות ספציפי לרקמה
תרגום (Translation)
הקוד הגנטי
- 64 קומבינציות של קודונים ($4\times4\times4=4^3$)
- 20 חומצות אמינו בלבד
- קודון התחלה:
AUG(מתיונין) - קודוני סיום:
UGA,UAA,UAG
מיקום התרגום
- ריבוזומים על ה־ER - חלבונים ממברנליים או מופרשים
- ריבוזומים חופשיים - חלבונים ציטופלזמיים
tRNA
- נושא אנטי-קודון מצד אחד
- חומצת אמינו מצד שני
- מתווך בין שפת הנוקלאוטידים לשפת חומצות האמינו
בקרת ביטוי גנים
עקרון כללי
לא כל הגנים מתבטאים בכל תא:
- הבדלים בין סוגי תאים (עור vs. שריר)
- הבדלים לאורך החיים (תינוק vs. קשיש)
- הבדלים פיזיולוגיים (הריון vs. לא בהריון)
בקרה ברמת השעתוק
1. פקטורי שעתוק (Transcription Factors)
אזור הפרומוטור
- נמצא לפני הגן
- כולל TATA Box - רצף עשיר ב־
Tו־A - אתר קישור ל־RNA פולימראז
אזור ה־Enhancer
- רחוק יותר מהגן (upstream)
- יכול להשפיע דרך יצירת לולאה ב־DNA
סוגי פקטורים
| סוג | תפקיד |
|---|---|
| אקטיבטורים | מגייסים את RNA פולימראז - מעודדים שעתוק |
| רפרסורים | חוסמים את אתר הקישור - מעכבים שעתוק |
- קיימים מעל 2,000 סוגים שונים של פקטורי שעתוק
- כולם בעלי DNA Binding Domain
הבדלים בין פרוקריוטים לאיקריוטים
| פרוקריוטים | איקריוטים | |
|---|---|---|
| מצב בסיסי | פתוח (ביטוי בזאלי) | סגור |
| פקטור שעתוק | Sigma Factor (אחד) | מאות פקטורים |
| מורכבות | פשוט | מורכב מאוד |
2. אפיגנטיקה
מתילציה של DNA
- תוספת קבוצת מתיל ($\ce{CH3}$) לבסיסי $\ce{C}$ באזורי CpG
- אנזים: DNA Methyl Transferase
- מתילציה = עיכוב שעתוק
מודיפיקציות של היסטונים
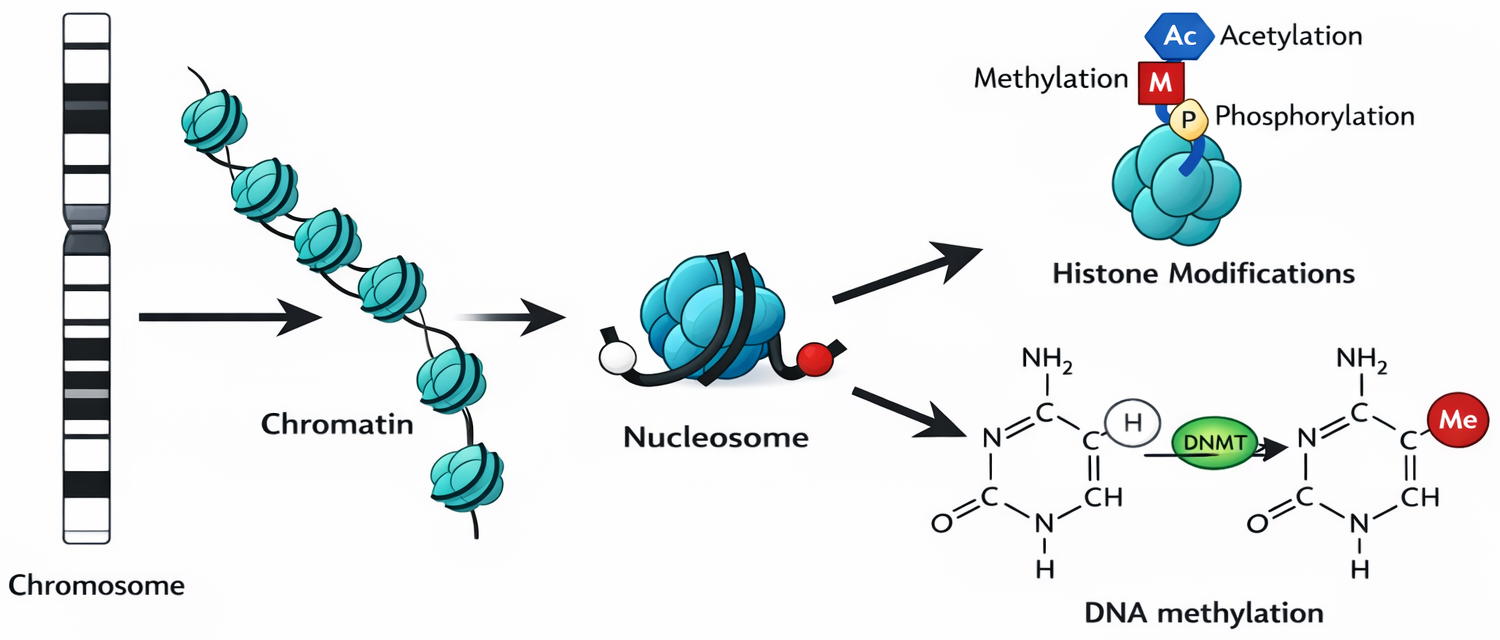
- מתילציה, אצטילציה, פוספורילציה
- משפיעות על צפיפות ה־DNA:
- DNA פרוס = שעתוק אפשרי
- DNA מקובץ = שעתוק מעוכב
תורשה אפיגנטית
- חלק מהמודיפיקציות עוברות לתאי בת
- חלק יכולות להשתנות מהשפעת הסביבה (תזונה, פעילות גופנית, מחלות)
3. מיקרו־רנ״א (miRNA)
- רצפים קצרים של RNA (23-21 בסיסים)
- לא מקודדים לחלבון - פעילים כ־RNA
- תפקיד: עיכוב ביטוי של גנים אחרים
תהליך היווצרות miRNA
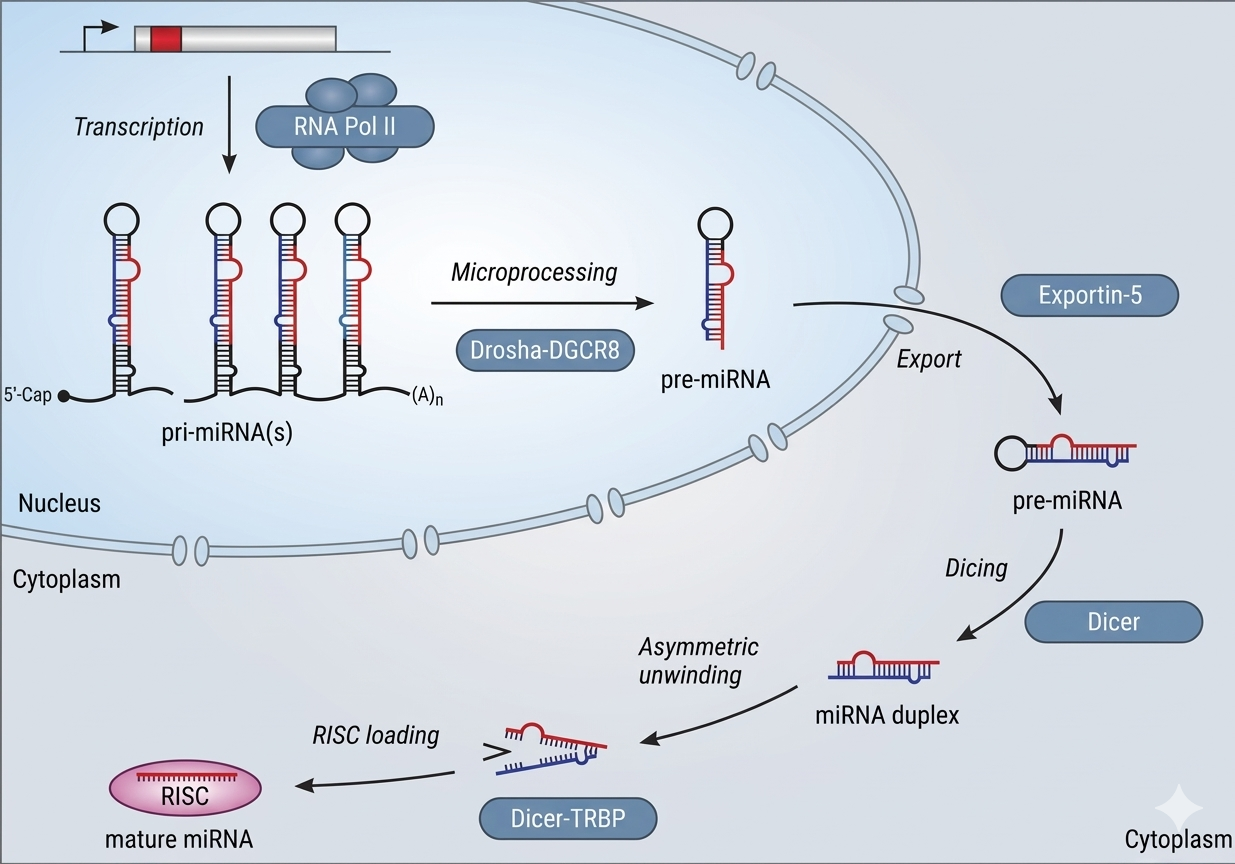
- שעתוק ← Pri-miRNA
- חיתוך על ידי Drosha (בגרעין)
- יציאה מהגרעין על ידי Exportin-5
- חיתוך על ידי Dicer (בציטופלזמה)
- התחברות לקומפלקס RISC עם חלבון Argonaute (AGO2)
- קישור ל־mRNA מטרה ← עיכוב תרגום/פירוק
שימושים רפואיים
- השתקת גנים בסרטן
- כשליש מהגנים תחת בקרת miRNA
בקרה ברמת התרגום
גורמים משפיעים
- כמות ריבוזומים
- זמינות קודון ההתחלה
- יציבות ה־mRNA
- קצב התרגום
סוגי בקרה
- Enhancers - מעודדי תרגום
- Inhibitors - מעכבי תרגום
בקרה לאחר התרגום
1. קיפול חלבונים
- חלק מתקפל באופן טבעי (מבנה שניוני ושלישוני)
- חלק בעזרת Chaperones (חלבוני Heat Shock)
- Chaperones רגישים לחום (בעיה בחום גבוה)
2. מודיפיקציות פוסט-תרגומיות
- פוספורילציה - הוספת זרחן (על ידי קינאזות)
- גליקוזילציה - הוספת סוכר
- הוספת שומנים
- חיתוך פרוטאוליטי
יתרון המודיפיקציות - הפעלה מהירה
- חלבונים יכולים להיות קיימים בתא אך לא פעילים
- רק לאחר מודיפיקציה (למשל פוספורילציה) הם הופכים לפעילים
- יתרון: כאשר נדרשת הפעלה/כיבוי מהירים של חלבון (בפרקי זמן קצרים), אין צורך לחכות לשעתוק ולתרגום מחדש
- מספיק לבצע מודיפיקציה אחת כדי להפעיל או לכבות את החלבון
- מתאים לחלבונים שצריך “לשחק” איתם במינונים משתנים
מפלי איתות (Signal Cascades)
- לעיתים קרובות קישור ליגנד לרצפטור מפעיל מפל של אקטיבציות
- קינאזות - אנזימים שמעבירים זרחן לחלבונים אחרים
- חלבון אחד עובר אקטיבציה ← מפעיל חלבון שני ← מפעיל חלבון שלישי וכן הלאה
דוגמה: אינסולין
- ייצור פרו־אינסולין בריבוזום
- קיפול ב־ER
- יצירת קשרי $\ce{S-S}$
- מעבר לגולג’י
- חיתוך על ידי פרוטאזות (אנזימים ספציפיים שחותכים חלבונים במקום מסוים)
- ← אינסולין פעיל
משמעות: אינסולין הוא דוגמה לחלבון שגם אחרי השלמת שעתוק ותרגום, הוא עדיין לא פעיל עד שעובר מודיפיקציות נוספות. זה מאפשר הזדמנויות נוספות לבקרה ולהפעלה רק כשבאמת יש צורך.
3. פירוק חלבונים - הפרוטאזום
- גילוי: פרופ’ אהרון צ’חנובר, אברהם הרשקו ופרופ’ אירווין רוז מקליפורניה (פרס נובל 2004)
מנגנון הפירוק
- סימון החלבון בשרשרת יוביקויטין (3 מולקולות)
- זיהוי על ידי הפרוטאזום
- פירוק לפפטידים קצרים ולחומצות אמינו בודדות
- מיחזור הרכיבים לבניית חלבונים חדשים
- התהליך דורש אנרגיה (ATP)
- משמש גם להגנה מפני פתוגנים (מפרק גם חלבונים שהגיעו ממקור חיצוני)
- הפרוטאזום הוא “תחנת מיחזור” לחלבונים בתא
חלבונים המיועדים לפירוק
- חלבונים זקנים
- חלבונים פגומים/שרופים
- חלבונים שאינם נחוצים יותר לתא
חשיבות קצב הפירוק
- גם אם נוצר הרבה חלבון מהר, אם הוא מתפרק מהר מאוד - הוא לא יישאר פעיל לאורך זמן
- קצב הפירוק משפיע על רמת החלבון הפעיל בתא
סיכום רמות הבקרה
| רמה | מנגנונים |
|---|---|
| שעתוק | פקטורי שעתוק, אפיגנטיקה, miRNA |
| עיבוד RNA | שחבור, יציבות |
| תרגום | זמינות ריבוזומים, קצב |
| פוסט-תרגום | קיפול, מודיפיקציות, פירוק |
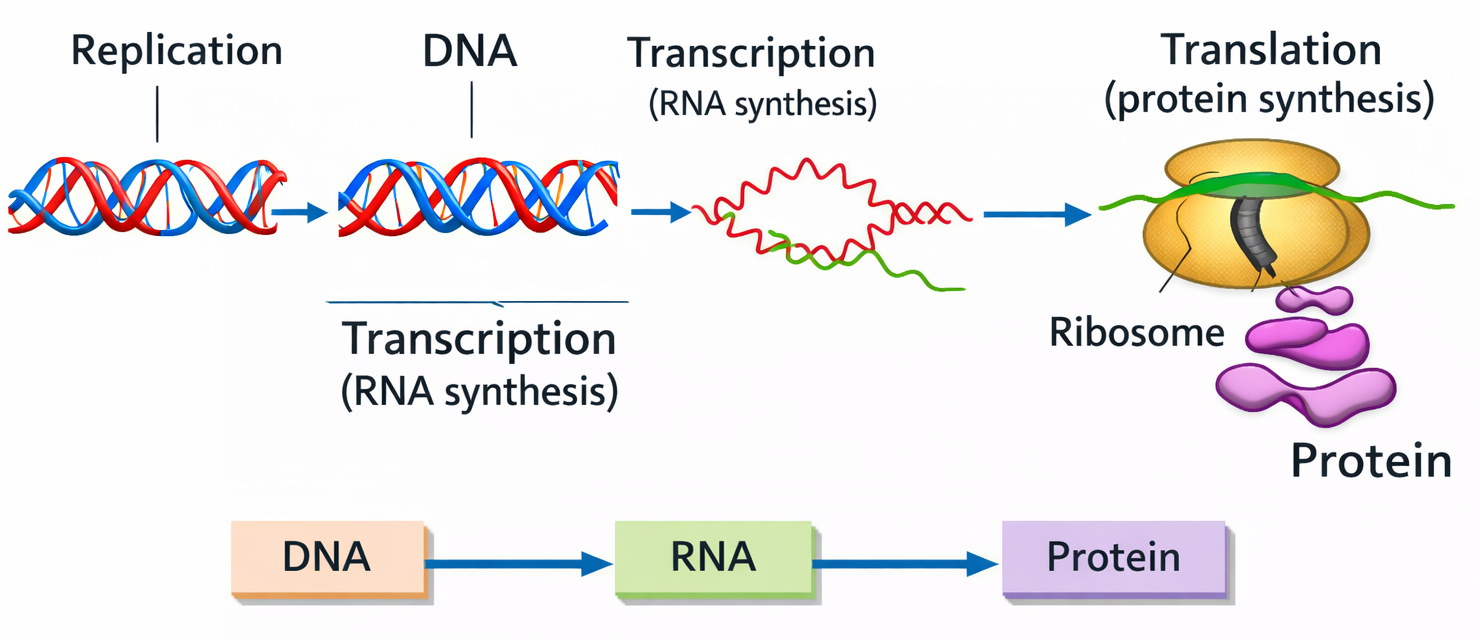
עיקרון מרכזי: הבקרה ברמת השעתוק היא הקריטית ביותר - אם לא צריך את החלבון, עדיף לא להתחיל את התהליך כלל. עם זאת, לאורך כל הדרך ואפילו אחרי שנוצר החלבון, עדיין אפשר ״לשחק״ עם הרמות שלו.
שאלות תרגול מג׳ונרטות
שאלות תרגול בגנטיקה על בסיס תרגול 5: הדוגמה המרכזית, שלבי בקרת ביטוי גנים, פרומוטור, פקטורי שעתוק, אפיגנטיקה, מתילציה, מודיפיקציות בהיסטונים, miRNA, Antisense RNA, בקרת תרגום, קיפול חלבונים, זירחון, יוביקוויטין-פרוטאוזום, SMA, טיפול גנטי.
שאלה 2: ביטוי גנים רקמה־ספציפי
האם כל החלבונים מתבטאים בכל תא בגוף?
- כן - כל תא מבטא את כל הגנים, אך רק חלק מהחלבונים פעילים לאחר תרגום
- לא - כל תא מבטא תת־קבוצה של גנים בהתאם לזהותו, בעוד שיתר הגנים מושתקים או מבוטאים ברמה זניחה
- כן - כל תא מבטא את אותם גנים, אך ההבדל הוא רק בקצב פירוק ה־mRNA והחלבון
- לא - תאים ממוינים כמעט לא מבטאים גנים, ורק תאי גזע מבצעים שעתוק פעיל
פתרון
התשובה הנכונה היא (2).
ברוב הרקמות: לכל התאים אותו DNA, אבל הם שונים באילו גנים פעילים ובאיזו רמה.
מהתרגול: כל תא מבטא רק את הגנים הרלוונטיים לתפקוד שלו:
- תא עצב ← גנים להעברת אותות
- תא דם אדום ← גנים לייצור המוגלובין
- תא כבד ← גנים לפירוק רעלים ומטבוליזם
אך: כל תא מכיל את אותו DNA (אותו גנום) — ההבדל הוא אילו גנים פעילים (מבוטאים).
מה קובע אילו גנים פעילים? מנגנוני בקרת ביטוי גנים — אפיגנטיקה, פקטורי שעתוק, miRNA ועוד.
שאלה 3: שלבי בקרת ביטוי גנים
מהם שלושת שלבי הבקרה העיקריים של ביטוי גנים?
- בקרה על שכפול DNA, בקרה על תיקון DNA, ובקרה על חלוקת התא
- בקרה על שעתוק, בקרה על עיבוד/תרגום RNA, ובקרה לאחר יצירת החלבון
- בקרה על ריצוף, בקרה על שחבור, ובקרה על טרנסלוקציה כרומוזומלית
- בקרה על מתילציה, בקרה על אצטילציה, ובקרה על זירחון כחלק משלושת שלבי הבקרה העיקריים
פתרון
התשובה הנכונה היא (2).
שלבי הבקרה הכלליים:
- Transcriptional - כמה mRNA מיוצר
- Translational - כמה mRNA מתורגם
- Post-translational - פעילות/יציבות/מיקום של החלבון לאחר שנוצר
(מתילציה/אצטילציה/זירחון הם מנגנונים בתוך שלבים שונים.)
| שלב בקרה | מנגנונים | דוגמאות |
|---|---|---|
| Transcriptional Control (בקרת שעתוק) | פקטורי שעתוק, אפיגנטיקה, רצפי RNA קצרים | שינוי תדירות התחלת שעתוק |
| Translational Control (בקרת תרגום) | יציבות RNA, קצב תרגום | שינוי אורך חיי mRNA, שינוי קצב תרגום |
| Post-translational Control (בקרה אחרי תרגום) | קיפול חלבונים, מודיפיקציות, פירוק | שינוי פעילות חלבון ע״י מודיפיקציות כימיות |
תשובה (4) שגויה כי מתילציה, אצטילציה וזירחון הם מנגנונים ספציפיים בתוך השלבים, לא השלבים עצמם.
שאלה 4: מבנה הפרומוטור
מהם רכיבים אופייניים שמעורבים בבקרת התחלת שעתוק של גן?
- TATA box, CAAT box, GC box ורצפי בקרה שאליהם נקשרים פקטורי שעתוק
- 5’ cap, Poly-A tail ואזורים ב־UTR שמווסתים יציבות ותירגום של mRNA
- Kozak sequence, אתרי התחלת תרגום ורצפי קישור של תת־יחידת הריבוזום
- רצפי אקסונים/אינטרונים ואתרי שחבור שקובעים איזה איזופורם חלבוני ייווצר
פתרון
התשובה הנכונה היא (1).
פרומוטור ורצפים רגולטוריים סמוכים (ולעתים גם רחוקים כמו enhancers) קובעים את הסיכוי להתחלת שעתוק ואת רמתו.
מבנה הפרומוטור (מהתרגול, שקף 6):
| רכיב | מיקום | תפקיד |
|---|---|---|
| TATA Box | $\sim -25$ | קובע נקודת ההתחלה של השעתוק (Startpoint) |
| CAAT Box | $\sim -75$ | בקרת קשירה ראשונית של RNA Polymerase |
| GC Box | $\sim -100$ | בקרת קשירה ראשונית של RNA Polymerase |
| Enhancer | מרחק משתנה | בקרת רמת ביטוי הגן (יכול להיות רחוק מאוד) |
נקודות חשובות מהתרגול:
- הפרומוטור הוא רצף של אלפי בסיסים על ה־DNA שאינו משועתק
- השעתוק מתחיל בנקודה +1 (קודון התחלה ATG)
- רצפי הפרומוטור שמורים אבולוציונית (כמעט ולא עברו מוטציות)
שאלה 5: פקטורי שעתוק - אקטיבטורים מול רפרסורים
מה ההבדל העקרוני בין Activator ל־Repressor בבקרת שעתוק?
- Activator מגייס קו־אקטיבטורים/מייצב קומפלקס שעתוק; Repressor מפריע לגיוס/מגייס קו־רפרסורים ומקטין התחלת שעתוק
- Activator נקשר רק ל־DNA דו־גדילי; Repressor נקשר רק ל־RNA חד־גדילי ולכן אינו פועל בשעתוק
- Activator מעלה תרגום ע”י קישור ל־5’UTR; Repressor מוריד תרגום ע”י קישור ל־3’UTR
- Activator קיים רק בפרוקריוטים; Repressor קיים רק באיקריוטים ולכן אינם מקבילים פונקציונלית
פתרון
התשובה הנכונה היא (1).
שניהם פקטורי שעתוק (או חלבונים רגולטוריים) שמשנים את ההסתברות להתחלת שעתוק - בכיוונים מנוגדים.
מהתרגול (שקפים 7-9):
פקטורי שעתוק = חלבונים המשמשים לבקרה על שעתוק. יש מעל 2,000 גנים כאלה בגנום. מתחלקים ל־2 סוגים:
| סוג | פעולה | נקשר ל… |
|---|---|---|
| Activator (מפעיל) | מושך RNA Polymerase ← מפעיל שעתוק | Enhancer |
| Repressor (מעכב) | חוסם גישת RNA Polymerase ← מעכב שעתוק | Silencer (איקריוטים) / Operator (פרוקריוטים) |
הבדל איקריוטים/פרוקריוטים:
- באיקריוטים: ה־Silencer יכול להיות קרוב או רחוק מהפרומוטור, ומשפיע בעקיפין
- בפרוקריוטים: ה־Operator לרוב חופף או צמוד לפרומוטור
המשותף לכל פקטורי שעתוק: יש להם DNA Binding Domain (DBD) - אזור שנקשר ל־DNA.
שאלה 6: מתילציה של DNA - מנגנון השתקה
כיצד מתילציה של DNA יכולה להפחית ביטוי של גן?
- מתילציה ב־CpG יכולה להפחית קישור של פקטורי שעתוק ולגייס חלבונים שמקדמים כרומטין דחוס ← ירידה בשעתוק
- מתילציה מחליפה את בסיס C בבסיס U וכך נוצרת “מוטציית RNA” שמפסיקה תרגום ← ירידה בשעתוק
- מתילציה מגדילה את פתיחת הכרומטין ומעלה גישה לפרומוטור ← עלייה בשעתוק
- מתילציה מתרחשת רק על היסטונים ולא על DNA ולכן אינה משפיעה ישירות על שעתוק
פתרון
התשובה הנכונה היא (1).
בפרומוטורים רבים, מתילציה קשורה לדיכוי שעתוק: פחות קישור פקטורים + יותר גיוס מדכאים/דחיסת כרומטין.
מתילציה של DNA (מהתרגול, שקפים 10-12):
מנגנון:
- הוספת קבוצת מתיל (CH₃) על בסיסי Cytosine (C) בצמדי CpG
- המתיל מפריע לקישור של פקטורי שעתוק ל־DNA
- רצף CpG ממותל מושך רפרסורים ספציפיים
- הכרומטין נעשה צפוף ← RNA Polymerase לא יכול לגשת ← השתקה
מושגים חשובים:
- CpG = צמד C ליד G על אותו גדיל (ה־p = קשר פוספודיאסטרי)
- איי CpG = אזורים בפרומוטורים עם ריכוז גבוה של CpG
- CpG הוא פלינדרומי - אם בגדיל אחד CG, בגדיל השני גם CG (בכיוון ההפוך)
מתילציה = השתקה. דה־מתילציה = הפעלה.
מחקר ישראלי: פרופ׳ חיים סידר ואהרון רזין מהאוניברסיטה העברית - חלוצי המחקר בתחום.
שאלה 7: מודיפיקציות בהיסטונים - אצטילציה מול מתילציה
מהי ההשפעה השכיחה של אצטילציה על היסטונים?
- אצטילציה מנטרלת מטען חיובי על ליזינים בזנבות היסטונים ← מפחיתה אינטראקציה עם DNA ← כרומטין פתוח יותר וביטוי עולה
- אצטילציה מוסיפה מטען חיובי לזנבות היסטונים ← מחזקת קשירה ל־DNA ← כרומטין סגור וביטוי יורד
- אצטילציה חותכת את זנבות ההיסטונים ← הנוקלאוזום מתפרק לחלוטין ← אין אריזת DNA בכלל
- אצטילציה מתרחשת רק ב־DNA (לא בהיסטונים) ולכן אין לה קשר ישיר לאריזת כרומטין
פתרון
התשובה הנכונה היא (1).
הרציונל החשמלי: DNA שלילי, היסטונים חיוביים; אצטילציה מפחיתה מטען חיובי ולכן “פותחת” כרומטין לרוב.
מודיפיקציות בהיסטונים (מהתרגול, שקף 13):
| מודיפיקציה | השפעה על כרומטין | ביטוי גן |
|---|---|---|
| אצטילציה | מפחיתה מטען חיובי ← כרומטין נפתח | גן פעיל ✓ |
| מתילציה (של היסטונים) | בד״כ כיווץ כרומטין | גן מושתק ✗ |
| פוספורילציה | משנה מבנה כרומטין | משתנה - תיקון DNA / ביטוי זמני |
הלוגיקה:
- היסטונים טעונים חיובית (הרבה Lysine ו־Arginine)
- DNA טעון שלילית (קבוצות פוספט)
- ← משיכה חשמלית חזקה = כרומטין צפוף וסגור
- אצטילציה מנטרלת מטען חיובי ← המשיכה נחלשת ← כרומטין נפתח ← שעתוק אפשרי
שאלה 8: miRNA - מנגנון פעולה
כיצד miRNA מפחית ביטוי של גן מטרה?
- miRNA נטען לקומפלקס חלבוני (כגון RISC) ונקשר ל־mRNA מטרה ← עיכוב תרגום ו/או פירוק mRNA
- miRNA נקשר לפרומוטור ב־DNA ומעכב קשירה של RNA polymerase II ← ירידה בשעתוק
- miRNA מתורגם לפפטיד קצר שנקשר לריבוזום ומפסיק elongation של התרגום
- miRNA נקשר ישירות ל־tRNA וגורם לטעינת חומצת אמינו שגויה ← חלבון פגום ולכן “ירידה בביטוי”
פתרון
התשובה הנכונה היא (1).
miRNA פועל בעיקר ברמת ה־mRNA: עיכוב תרגום/דגרדציה בהתאם להקשר ולמידת ההתאמה לרצף המטרה.
miRNA - Micro RNA (מהתרגול, שקף 14):
| מאפיין | פרט |
|---|---|
| אורך | 23-21 בסיסים |
| מקודד לחלבון? | לא - RNA לא־מקודד |
| מקור | ממולקולת אב בעלת מבנה stem-loop, מגן ספציפי או אינטרון |
| כמות גנים בגנום האנושי | ~700 גנים |
| תפקיד | עיכוב ביטוי של גנים אחרים |
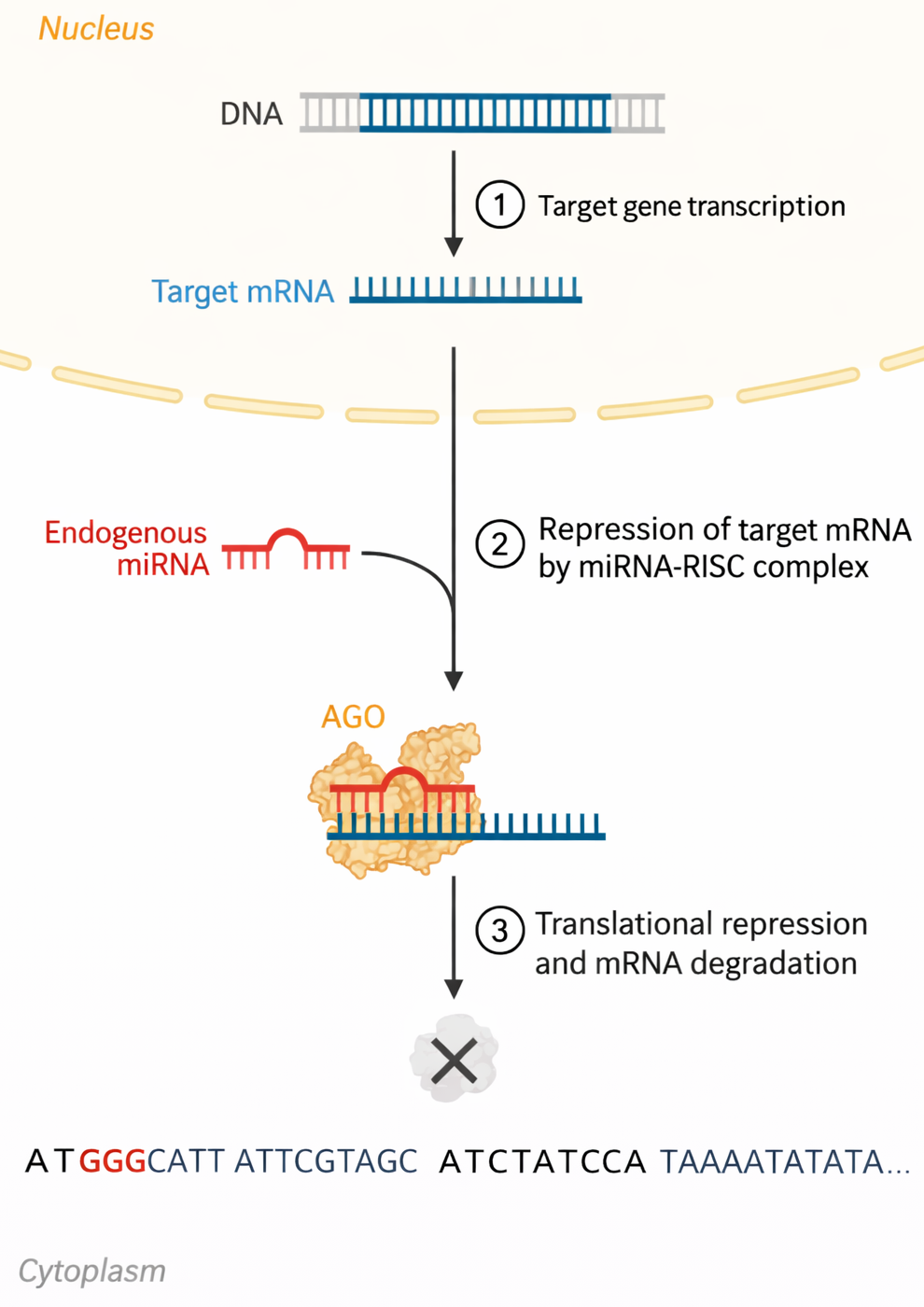
מנגנון (3 שלבים מהדיאגרמה):
- Target gene transcription ← נוצר Target mRNA
- Endogenous miRNA נקשר עם חלבון AGO ← יצירת miRNA-RISC complex ← נקשר ל־mRNA
- Translational repression (עיכוב תרגום) ו/או mRNA degradation (פירוק)
שאלה 9: Antisense RNA
כיצד Antisense RNA יכול להשתיק ביטוי גן?
- Antisense RNA מזווג בסיסים עם mRNA משלים ← מפריע לתרגום ויכול לקדם פירוק של ה־RNA
- Antisense RNA נקשר ל־DNA באזור הפרומוטור ויוצר קשרים קוולנטיים שמונעים שעתוק
- Antisense RNA נקשר לחלבון המטרה וגורם לו להתפרק בפרוטאוזום
- Antisense RNA מעכב שחבור ע”י פירוק snRNPs בגרעין ומפסיק עיבוד mRNA בכל התא
פתרון
התשובה הנכונה היא (1).
Antisense יוצר קומפלקס RNA-RNA שמפריע לריבוזום ו/או מערב מסלולים שמזהים RNA דו־גדילי.
Antisense RNA (מהתרגול, שקף 15):
- Sense mRNA = ה־mRNA ה״רגיל״ שמתורגם לחלבון (עם זנב Poly-A = AAAAAA)
- Antisense mRNA = רצף RNA קומפלמנטרי ל־Sense
- כאשר ה־Antisense נקשר ל־Sense mRNA ← נוצר RNA דו־גדילי ← ה־Ribosome לא יכול לתרגם ← ביטוי הגן מושתק
הבדל מ־miRNA:
- miRNA = קצר (23-21 בסיסים), פועל דרך RISC complex
- Antisense RNA = יכול להיות ארוך יותר, נקשר ישירות ל־mRNA
שאלה 10: בקרת תחילת תרגום - Translation Initiation
מה יכול לווסת את קצב התחלת התרגום של mRNA?
- קישור חלבונים/קומפלקסים ל־5’UTR ושינוי מבנים משניים או גיוס ריבוזום ← שינוי בקצב initiation
- קישור חלבונים לקודון הסיום (Stop codon) ושינוי קצב termination ← שינוי בקצב initiation
- שינוי ברצף ה־DNA בפרומוטור בזמן אמת לפי תנאי סביבה ← שינוי מיידי במהירות initiation
- פירוק שרשראות יוביקוויטין מהחלבון המתורגם ← שינוי ישיר בקצב initiation על אותו mRNA
פתרון
התשובה הנכונה היא (1).
התחלת תרגום מושפעת מאוד מגורמים שנקשרים ל־UTR (במיוחד 5’UTR) וממבנים משניים שמקלים/מקשים על גיוס וסריקה של הריבוזום.
בקרת תחילת תרגום (מהתרגול, שקף 17):
מבנה ה־mRNA: 5’ UTR ← AUG (התחלה) ← רצף מקודד ← UAA (סיום) ← 3’ UTR
| מצב | חלבון | השפעה |
|---|---|---|
| Enhancer bound to Leader | חלבון מפעיל | תרגום מואץ |
| Inhibitor bound to Leader | חלבון מעכב | תרגום מואט |
עקרון: רצפים ספציפיים ב־5’ UTR יוצרים מבנים משניים (Secondary Structures), וחלבונים ספציפיים נקשרים אליהם ומשפיעים על קצב גיוס הריבוזום.
שאלה 11: קיפול חלבונים - צ׳פרונים
מה תפקידם העיקרי של צ׳פרונים?
- סיוע לקיפול חלבונים ומניעת אגרגציה, במיוחד בתנאי עקה; חלקם גם מסייעים בקיפול מחדש
- חיתוך חלבונים לפפטידים כחלק קבוע מתהליך התרגום בריבוזום
- קישור ל־DNA באזור הפרומוטור ופתיחת כרומטין כדי להתחיל שעתוק של גנים
- הוספת קבוצות פוספט ל־Ser/Thr/Tyr כדי להפעיל מסלולי העברת אותות
פתרון
התשובה הנכונה היא (1).
צ׳פרונים (כולל HSPs רבים) תומכים בקיפול נכון ומפחיתים יצירת צברים של חלבונים לא תקינים.
צ׳פרונים (מהתרגול, שקף 19):
- אנזימים שמסייעים בקיפול או פתיחת מבנה של חלבונים
- הרבה מהם הם Heat Shock Proteins (HSPs) - מונעים יצירת אגרגטים (צברים) של חלבונים לא מתפקדים בתנאי חום או עקה
- רצף חומצות האמינו של חלבון קובע את המבנה התלת־מימדי שלו
למה זה חשוב?
- חלבון שלא מתקפל נכון ← לא מתפקד (או מתפקד בצורה שגויה)
- במחלות רבות (כמו אלצהיימר, פרקינסון) יש בעיה בקיפול חלבונים ← הצטברות אגרגטים
שאלה 12: זירחון חלבונים (Phosphorylation)
באילו חומצות אמינו נפוץ זירחון, ומה תפקידו?
- Serine/Threonine/Tyrosine - שינוי פעילות/קישור/לוקליזציה כחלק מבקרת מסלולי איתות
- Glycine/Alanine/Valine - יצירת קשרי דיסולפיד וייצוב מבנה שלישוני
- Methionine/Tryptophan/Phenylalanine - קביעת תחילת תרגום ועצירת elongation
- Lysine/Arginine/Histidine - סימון חלבון לפירוק בפרוטאוזום ע”י יוביקוויטין
פתרון
התשובה הנכונה היא (1).
זירחון הוא “מתג” נפוץ במסלולי איתות: קינאזות מוסיפות פוספט, פוספטאזות מסירות.
זירחון חלבונים (מהתרגול, שקף 21):
| מאפיין | פרט |
|---|---|
| חומצות אמינו | Serine, Threonine, Tyrosine |
| חשיבות | תהליכי העברת אותות (Signal Transduction) |
| כמות חלבונים | כמעט שליש מכלל החלבונים האנושיים יכול לעבור זירחון |
| אנזימים | קינאזות = מעבירות זרחן לחלבון; פוספטאזות = מסירות זרחן |
הלוגיקה: זירחון = ״מתג מולקולרי״ - הוספת קבוצת פוספט משנה את צורת/פעילות החלבון (מפעיל או מכבה אותו).
שאלה 13: מערכת יוביקוויטין-פרוטאוזום
מה מתאר נכון פירוק חלבונים תלוי יוביקוויטין?
- קישור יוביקוויטין לחלבון (לעיתים כשרשרת) מסמן אותו לזיהוי בפרוטאוזום ולפירוק לפפטידים/חומצות אמינו
- יוביקוויטין הוא פרוטאז שמפרק חלבונים ישירות בציטוזול ללא צורך בקומפלקס נוסף
- פרוטאוזום מוסיף יוביקוויטין לחלבון המטרה, ואז מעביר אותו לגרעין כדי להפסיק שעתוק
- יוביקוויטין נקשר ל־mRNA של הגן וכך מפחית את תרגומו ע”י ריבוזומים
פתרון
התשובה הנכונה היא (1).
התיוג ביוביקוויטין ← זיהוי ע”י פרוטאוזום ← פירוק; הרכיבים ממוחזרים.
מערכת יוביקוויטין-פרוטאוזום (מהתרגול, שקפים 22-24):
פרס נובל 2004: פרופ׳ אברהם הרשקו ופרופ׳ אהרון צ׳חנובר מהטכניון, יחד עם פרופ׳ אירווין רוז.
שלבי התהליך:
| שלב | אנזים | תפקיד |
|---|---|---|
| 1 | E1 | מפעיל יוביקוויטין (קושר לקצה C-terminal) |
| 2 | E2 | מחליף את E1 וקושר את היוביקוויטין |
| 3 | E3 (Ubiquitin Ligase) | מעביר את היוביקוויטין ל־Lysine על חלבון המטרה |
← התהליך חוזר ← שרשרת Poly-Ubiquitin
← חלבון מסומן נכנס ל־Proteasome ← מתפרק ל־פפטידים וחומצות אמינו
← יוביקוויטין ופרוטאוזום ממוחזרים
שאלה 14: יציבות חלבונים - N-Terminal Rule
ממה יכולה להיות מושפעת יציבות חלבון לפי עקרון ה־N-end rule?
- זהות חומצת האמינו בקצה ה־N-טרמינלי יכולה להשפיע על זיהוי החלבון במסלולי פירוק ועל זמן מחצית החיים שלו
- רק אורך החלבון קובע: חלבונים ארוכים תמיד מתפרקים מהר יותר מחלבונים קצרים
- רק מספר קשרי דיסולפיד קובע: יותר קשרים = תמיד יותר פירוק בפרוטאוזום
- רק סוג התאים קובע: באותו תא כל החלבונים יציבים באותה מידה, בלי תלות ברצף
פתרון
התשובה הנכונה היא (1).
חומצת האמינו ה־N-טרמינלית יכולה לשמש “סיגנל” לזיהוי ופירוק, בהתאם למערכת התא.
יציבות חלבון (מהתרגול, שקף 18):
N-End Rule - חומצת האמינו בקצה ה־N-terminal קובעת את זמן מחצית החיים של החלבון:
| חומצת אמינו ב־N-terminal | זמן מחצית חיים |
|---|---|
| Arginine | ~3 דקות |
| Methionine | 20+ שעות |
הלוגיקה: חומצות אמינו מסוימות ב־N-terminal ״מסמנות״ את החלבון כמועד לפירוק מהיר - מערכת היוביקוויטין מזהה אותן.
חשיבות: מאפשר לתא לשלוט בכמות חלבונים - חלבונים שצריכים להיות זמניים (למשל ציקלינים במחזור תא) מתפרקים מהר.
שאלה 15: SMA - הבדל בין SMN1 ל־SMN2
מה ההבדל המרכזי בין SMN1 ל־SMN2 ומדוע SMN2 לרוב לא מפצה לחלוטין?
- שינוי נקודתי ב־SMN2 משפיע על שחבור כך שאקסון 7 מדולג לעיתים קרובות ← פחות חלבון מלא תפקודי ביחס ל־SMN1
- SMN2 אינו מתועתק כלל ברקמות עצביות, בעוד SMN1 מתועתק רק בשריר
- SMN1 נמצא בכרומוזום אוטוזומלי ו־SMN2 בכרומוזום X ולכן אין אפשרות לפיצוי ביניהם
- SMN2 מייצר רק rRNA שקשור לריבוזום ולא חלבון, ולכן אין לו קשר ל־SMN
פתרון
התשובה הנכונה היא (1).
בגדול: SMN2 “מייצר” יותר איזופורמים חסרים בגלל דילוג אקסון 7, ולכן הפיצוי חלקי בלבד.
SMA - Spinal Muscular Atrophy (מהתרגול, שקפים 28-29):
| גן | חלבון שמייצר | הסבר |
|---|---|---|
| SMN1 | חלבון SMN תקין ופונקציונלי | אקסון 7 כלול |
| SMN2 | רוב החלבון לא־תפקודי | מוטציה נקודתית מפריעה לשחבור ← אקסון 7 נחתך |
מה קורה בכל מצב?
- SMA non-carrier: SMN1 (2 עותקים תקינים) ← הרבה חלבון תקין
- SMA carrier: SMN1 אחד חסר, אחד תקין ← מספיק חלבון
- SMA patient: שני עותקי SMN1 חסרים ← אין חלבון SMN תקין; SMN2 מייצר רק מעט חלבון תפקודי
חלבון SMN חיוני להרכבת snRNPs (חלק מהספלייסוזום) ← חסר בו גורם לפגיעה בשחבור RNA בנוירונים מוטוריים ← מוות נוירונים ← ניוון שרירים.
שאלה 16: SMA - טיפול ב־Zolgensma
על מה מבוסס הטיפול ב־Zolgensma ומדוע יעילותו מוגבלת כאשר מתחילים מאוחר?
- החדרת עותק תפקודי של SMN1 בעזרת וקטור (כגון AAV); התחלה מאוחרת פחות יעילה כי נזק נוירונלי מצטבר אינו הפיך במלואו
- הגברת תרגום של SMN2 ע”י קישור חלבון ל־3’UTR; התחלה מאוחרת לא יעילה כי mRNA כבר התפרק
- השתקת אונקוגן שמעכב נוירונים מוטוריים; התחלה מאוחרת לא יעילה כי הפרומוטור כבר ממותל
- פירוק מיוחד של חלבונים רעילים בעזרת פרוטאוזום; התחלה מאוחרת לא יעילה כי יוביקוויטין נגמר בתא
פתרון
התשובה הנכונה היא (1).
ככל שמתחילים מוקדם יותר, יש יותר תאי מטרה תקינים להצלה ולשמירה על תפקוד.
Zolgensma (מהתרגול, שקף 31):
| מאפיין | פרט |
|---|---|
| מנגנון | Gene Therapy - וקטור AAV מכניס עותק תקין של SMN1 לתאים |
| מתן | טיפול חד־פעמי |
| יעילות | עד גיל ~2 - לפני התקדמות נוירונלית משמעותית |
למה לא מתאים בגיל 7?
- בגיל 7, חלק גדול מהנוירונים המוטוריים כבר מתו - בגלל שנים ללא חלבון SMN
- תאי עצב אינם מתחדשים - אי אפשר להחזיר נוירונים שנעלמו
- גם אם מכניסים את הגן - אין תאי מטרה להכניס אליהם
עקרון: ככל שמתחילים טיפול מוקדם יותר, כך יותר נוירונים עדיין קיימים ואפשר להציל אותם.
שאלה 17: אפיגנטיקה - תאומים זהים
האם תאומים זהים שגדלו בסביבות שונות צפויים לשמור על דגם אפיגנטי זהה?
- לא בהכרח - DNA זהה, אך גורמי סביבה וגיל יכולים לשנות מתילציה/מודיפיקציות היסטונים ולהוביל להבדלים
- כן - אפיגנטיקה נקבעת רק בזמן ההפריה ולכן אינה משתנה במהלך החיים
- כן - תאומים זהים זהים גם אפיגנטית בכל הרקמות כי הכרומטין מועתק במדויק כמו DNA
- לא - תאומים זהים אינם חולקים את אותו DNA ולכן בהכרח גם האפיגנטיקה שונה
פתרון
התשובה הנכונה היא (1).
אפיגנטיקה דינמית יותר מ־DNA, ויכולה להשתנות לאורך החיים ובהשפעת סביבה.
מהתרגול (שקף 32):
שינויים אפיגנטיים כוללים: מתילציה של DNA, מודיפיקציות על היסטונים, שינויים במבנה הכרומטין, והשפעות של RNA לא־מקודד.
גורמי סביבה שמשפיעים על אפיגנטיקה:
- תזונה
- חומרים כימיים ותרופות
- מתחים ומצבים חברתיים
- גיל
דוגמה מהתרגול (שקף 33) - דגמים אפיגנטיים שונים:
| השוואה | דגם אפיגנטי | סיבה |
|---|---|---|
| תא עור מול תא כבד | שונה | מבטאים חלבונים שונים |
| שני תאי כבד מאותו תא אם | זהה | נשמר בחלוקה |
| תא גזע מול תא ממוין | שונה | תא גזע מבטא גנים רבים יותר |
| תא עור בגיל 12 מול גיל 70 | שונה | שינויים אפיגנטיים לאורך החיים |
שאלה 18: miRNA וסרטן
כיצד ירידה ב־miRNA מסוים יכולה לתרום להתפתחות סרטן?
- אם miRNA מדכא אונקוגן, ירידה בו מסירה דיכוי ← ביטוי יתר של אונקוגן וחלוקה לא מבוקרת
- אם miRNA מדכא מדכאי־גידול, ירידה בו תעצים מדכאי־גידול ולכן תגרום לסרטן
- miRNA פועל רק בעובר ולכן ירידה בו אינה משפיעה על גידולים בבוגר
- miRNA הוא אנזים שמפרק DNA; ירידה בו גורמת להצטברות DNA ולסרטן
פתרון
התשובה הנכונה היא (1).
עיקרון: miRNA יכול לשמש “בלם” על גנים מעודדי חלוקה; ירידה בבלם = יותר חלוקה/הישרדות.
miRNA וסרטן (מהתרגול, שקפים 36-37):
שני תרחישים:
| תרחיש | miRNA | תוצאה |
|---|---|---|
| ירידה ב־miRNA שמעכב אונקוגנים | פחות עיכוב | אונקוגנים פועלים ביתר ← סרטן |
| עודף ב־miRNA שמעכב גנים מדכאי גידול | יותר עיכוב | מדכאי גידול לא פועלים ← סרטן |
דוגמה מהתרגול - MRX34 (miR-34a):
- miR-34a = miRNA שמדכא אונקוגנים
- בסרטן, רמות miR-34a יורדות ← אונקוגנים לא מבוקרים
- MRX34 = תרופה סינתטית עם miR-34a בננו־חלקיקים ← מוזרקת לווריד ← חודרת לתאים סרטניים ← משחררת miR-34a ← מעכבת אונקוגנים
- הופסקה בניסוי קליני פאזה 1 עקב תגובה חיסונית חמורה (2016-2017)
שאלה 19: חישוב גודל חלבון מגודל גן
רצף מקודד (coding sequence) באורך 900 בסיסים. מהו הגודל המקסימלי של הפפטיד שניתן לקודד ממנו?
- כ־300 חומצות אמינו (בקירוב), משום שכל 3 בסיסים = קודון אחד שמקודד לחומצת אמינו אחת
- כ־450 חומצות אמינו (בקירוב), משום שכל 2 בסיסים = קודון אחד בתרגום
- כ־900 חומצות אמינו (בקירוב), משום שכל בסיס מקודד ישירות לחומצת אמינו אחת
- כ־150 חומצות אמינו (בקירוב), משום שכל 6 בסיסים נדרשים לקידוד חומצת אמינו אחת
פתרון
התשובה הנכונה היא (1).
900 / 3 = 300 (בקירוב). קודון סיום אינו מוסיף חומצה אמינית, אך זה עדיין סדר הגודל המקסימלי.
מהתרגול (שקף 25 - מקרה חלבונים מפרקי פלסטיק):
חישוב:
- כל 3 בסיסים (קודון) ← חומצת אמינו אחת
- 900 ÷ 3 = 300 חומצות אמינו מקסימום
למה “או פחות”?
- פרומוטור - לא משועתק ← מקטין את האזור המקודד
- אינטרונים - משועתקים אך נחתכים בשחבור ← לא מתורגמים
- 5’ UTR ו־3’ UTR - משועתקים אך לא מתורגמים
- קודון סיום - תופס 3 בסיסים שלא מקודדים לחומצת אמינו
הערה חשובה מהתרגול: אותו חלבון בחיפושית (איקריוט, 900 bp) ובחיידק (פרוקריוט, 500 bp) - ייתכן שהגן בחיפושית כולל אינטרונים שלא קיימים בחיידק, ולכן הגן ארוך יותר אך החלבון זהה.
שאלה 20: יתרון בקרה מוקדמת מול מאוחרת
מהו היתרון של בקרה ברמת השעתוק לעומת בקרה לאחר תרגום?
- בקרה ברמת השעתוק לרוב חסכונית יותר באנרגיה; בקרה לאחר תרגום מאפשרת תגובה מהירה יותר כי החלבון כבר קיים
- בקרה ברמת השעתוק תמיד מהירה יותר כי אין צורך בריבוזומים; בקרה לאחר תרגום תמיד איטית כי דורשת שעתוק מחדש
- בקרה לאחר תרגום תמיד חסכונית יותר כי לא נוצרים חלבונים כלל; בקרה ברמת השעתוק תמיד בזבזנית
- אין הבדל עקרוני: כל רמות הבקרה זהות בזמן תגובה ובעלות אנרגטית
פתרון
התשובה הנכונה היא (1).
יש trade-off: מוקדם = חסכוני אבל איטי יותר; מאוחר = מהיר יותר אבל עלול לבזבז משאבים.
מהתרגול (שקף 34):
| רמת בקרה | יתרון | חיסרון | דוגמה |
|---|---|---|---|
| בקרה מוקדמת (לפני/בזמן שעתוק) | חיסכון באנרגיה - לא נוצרים RNA וחלבונים מיותרים | תגובה איטית - צריך זמן לשעתוק ותרגום | גנים שצריכים רק בתאים ספציפיים |
| בקרה ברמת תרגום | תגובה מהירה - mRNA כבר קיים, רק צריך לתרגם | פחות חסכוני | אינסולין - mRNA מוכן מראש, מופעל במהירות כשסוכר עולה |
| בקרה אחרי תרגום | תגובה כמעט מיידית - חלבון כבר קיים | הכי פחות חסכוני | אנזימי קרישה, אדרנלין - מוכנים מראש, מופעלים ע״י זירחון/חיתוך |
עקרון: יש Trade-off בין חיסכון אנרגטי למהירות תגובה. הגוף משתמש בכל הרמות בהתאם לצורך.