יצירת אימינים ואנאמינים
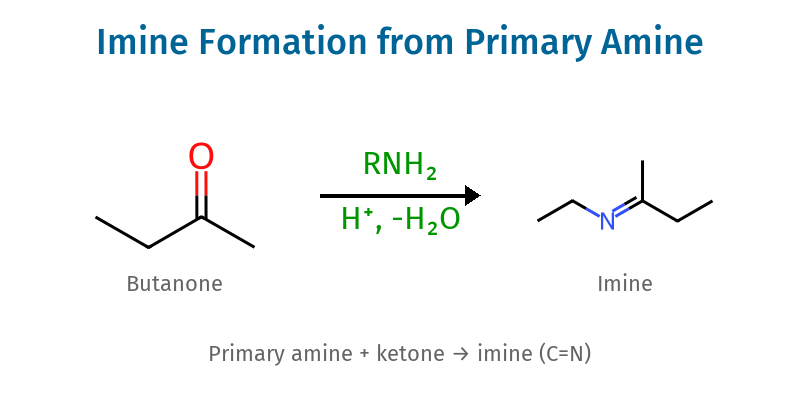
- אמין ראשוני + קטון/אלדהיד ← אימין ($\ce{C=N}$)
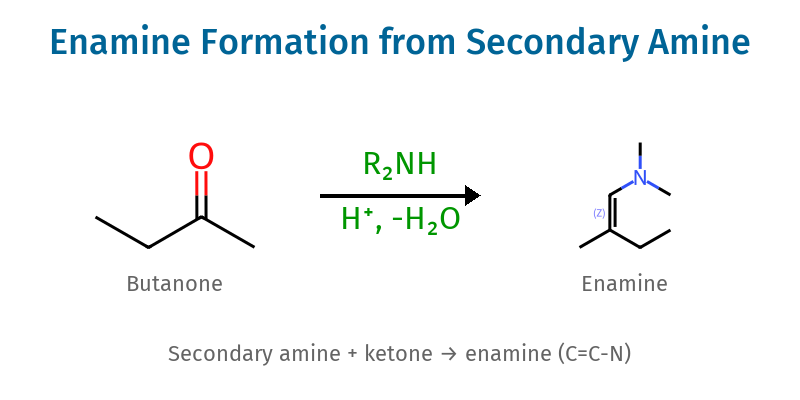
- אמין שניוני + קטון/אלדהיד ← אנאמין ($\ce{C=C-N}$)
- אמוניה ($\ce{NH3}$) ספציפית ← אימין עם $\ce{H}$ על החנקן
- כלל זיהוי: הפחמן בקשר כפול לחנקן = היה פעם קרבונילי
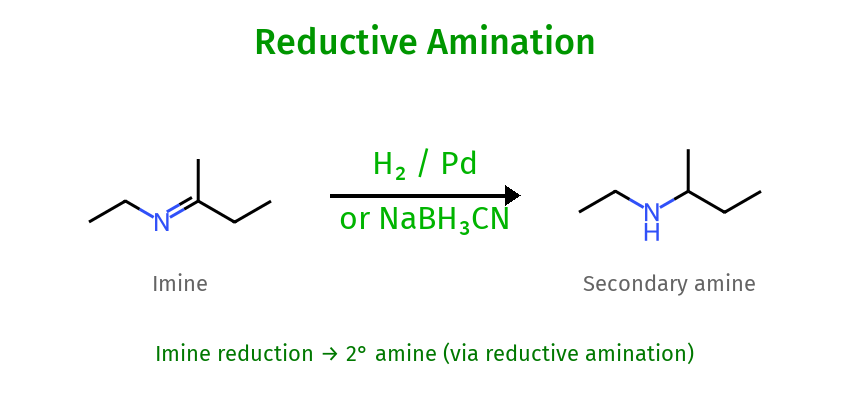
- חיזור עם $\ce{H2/Pd}$: אימין ← אמין שניוני, אנאמין ← אמין שלישוני
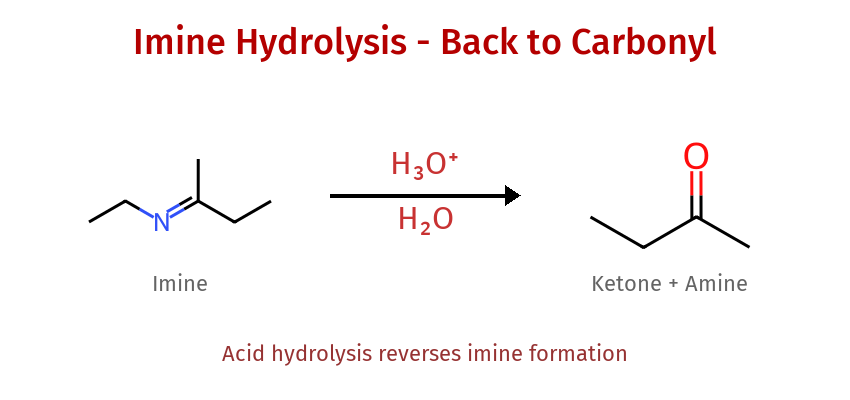
- פירוק חזרה: $\ce{H2O/H+}$ ← חזרה לקרבוניל + אמין
הלוגנציה בעמדה אלפא
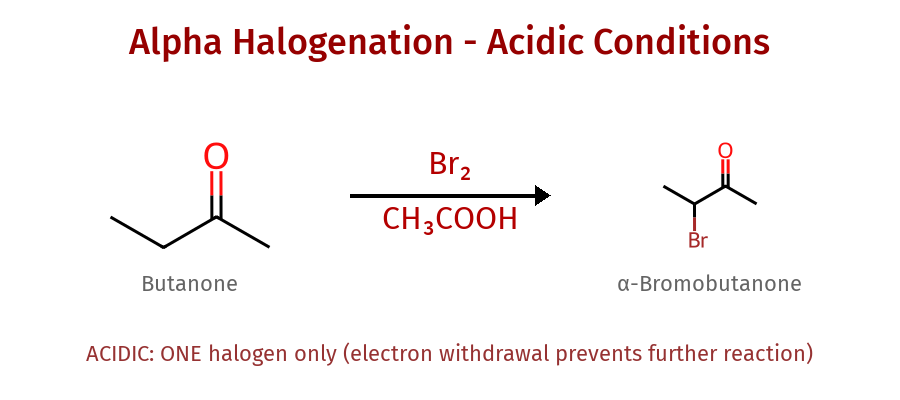
- תנאים חומציים ($\ce{Br2/CH3COOH}$): נכנס הלוגן אחד בלבד
- הברום עושה משיכה אינדוקטיבית ← קשה לעשות פרוטונציה נוספת
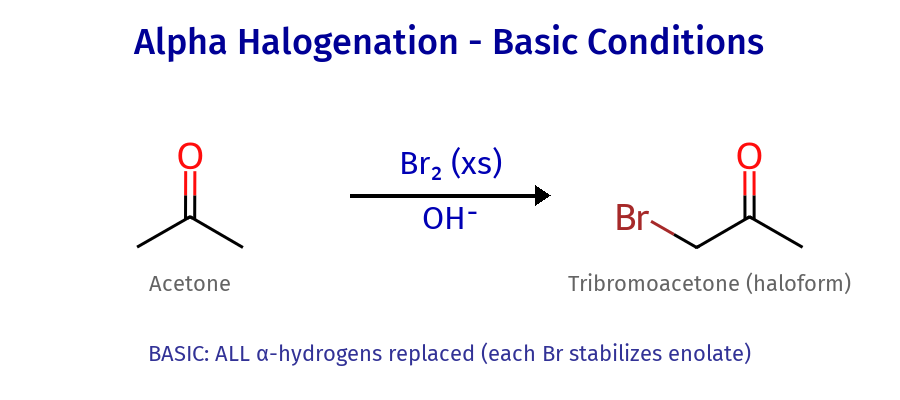
- תנאים בסיסיים ($\ce{Br2/OH-}$): נכנסים הלוגנים ככמות המימנים על פחמני אלפא
- כל הלוגן שנכנס מייצב את האנולאט ← קל יותר לקטוף פרוטון נוסף
- המימן האלדהידי אינו מימן חומצי - לא נחשב מימן אלפא
- מנגנון חומצי: דרך אינול / מנגנון בסיסי: דרך אנולאט
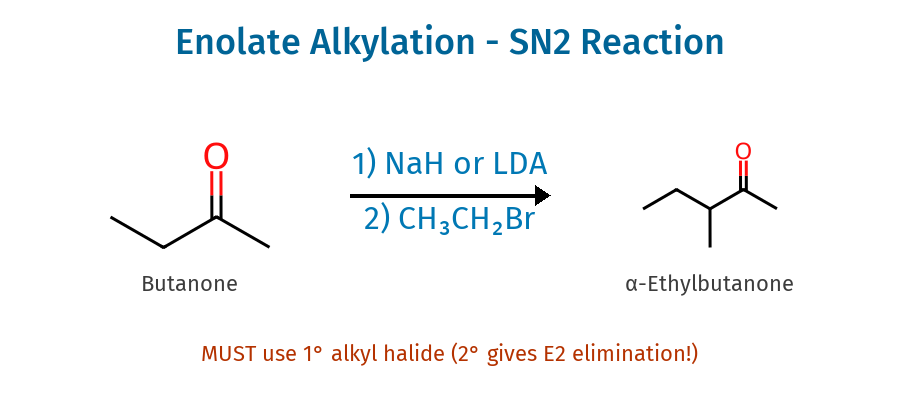
אלקילציה עם אנולאט
- בסיס חזק ($\ce{NaH}$, $\ce{NaOH}$) + קטון ← אנולאט (נוקלאופיל)
- אנולאט + אלקיל הליד ← תגובת $\ce{SN2}$
- חובה: אלקיל הליד ראשוני או $\ce{CH3X}$ (שניוני יעשה $\ce{E2}$)
- הפחמן האלקטרופילי: איפה שיושב ההלוגן
תגובת אלדול
עקרונות מנחים
- קטון/אלדהיד + $\ce{OH-}$ + חימום ← תגובת אלדול
- “אם אין עוד נוקלאופילים/אלקטרופילים” ← המולקולה תוקפת את עצמה
- תמיד למספר פחמנים - “אחרת עושים סלט עם התוצרים”
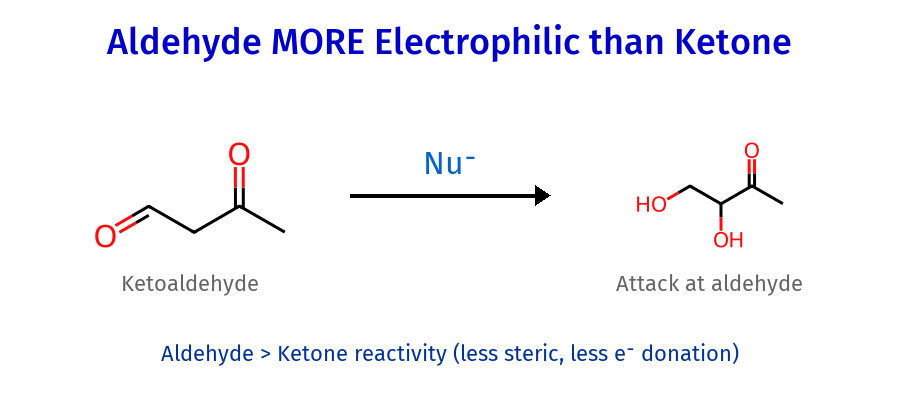
- אלדהיד יותר אלקטרופילי מקטון ← בתערובת הוא האלקטרופיל (הקרבוניל שתוקפים)
מנגנון ותוצרים
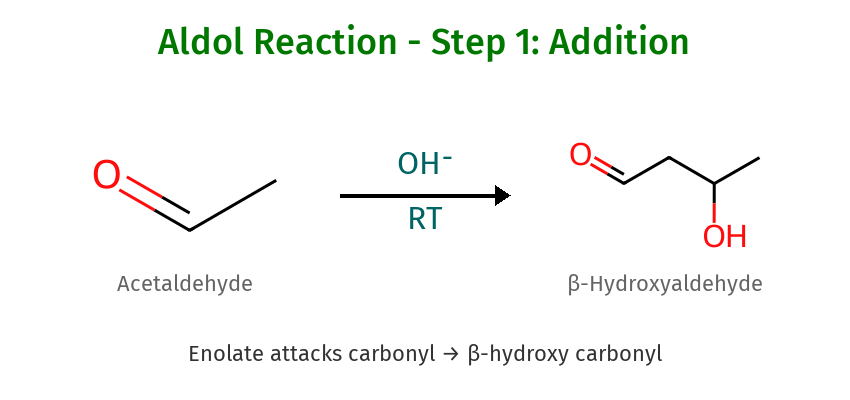
- שלב 1: אנולאט תוקף קרבוניל ← β-הידרוקסי קרבוניל
- פרוטונציה של $\ce{O-}$ ← $\ce{OH}$
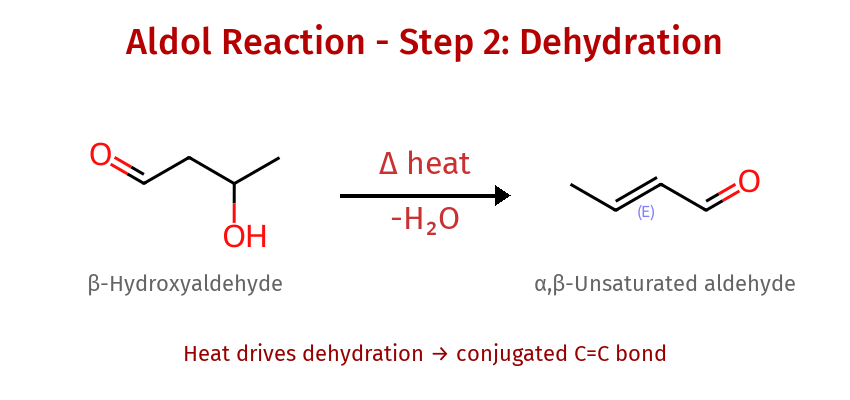
- שלב 2 (רק עם חימום): דהידרציה ← $\ce{C=C}$ בעמדה α,β
- “המימן ו־$\ce{OH}$ יוצאים החוצה”
- הקשר הכפול תמיד בין פחמן α (עם $\ce{H}$) לפחמן β (עם $\ce{OH}$)
- בלי חימום: נעצרים בתוצר אלדול (עם $\ce{OH}$)
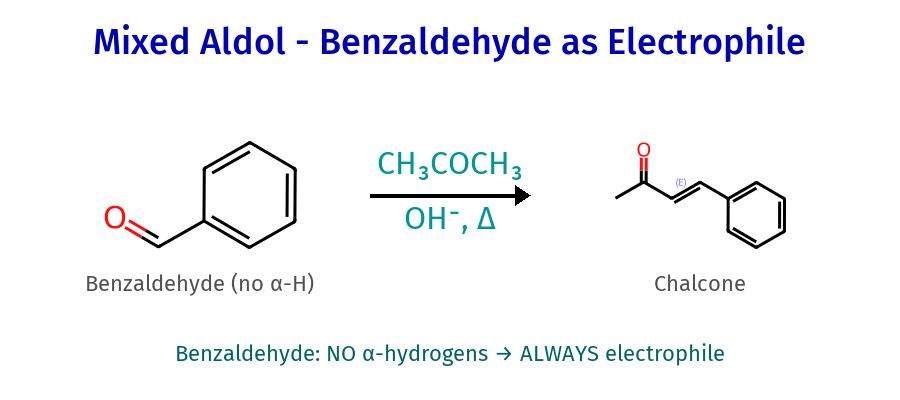
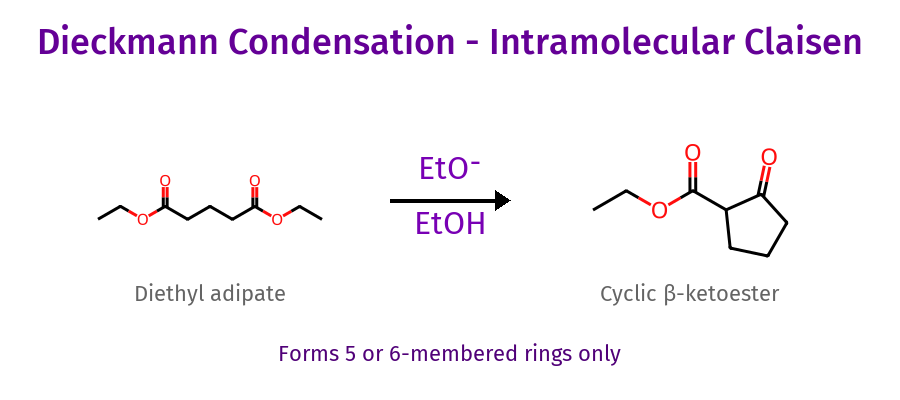
תגובה תוך־מולקולרית
- “רק טבעות של 5 או 6” - אחרות לא יציבות
- ספירת אטומים לבחירת צד: “1,2,3,4,5,6,7 - לא יציב”
- “התגובות האלה הרבה יותר מהירות” - המולקולה כבר באזור
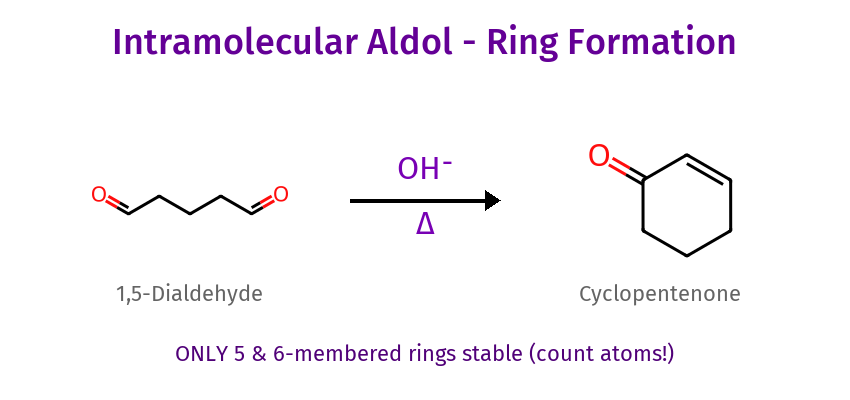
רטרו־אלדול (שאלות הפוכות)
- מחפשים קשר כפול α,β לקרבוניל - “זה השתתף באלדול”
- שוברים את הקשר $\ce{C-C}$ בעמדה β
- צד עם קרבוניל = היה אנולאט (נוקלאופיל)
- צד שני = הופך לקרבוניל (היה אלקטרופיל)
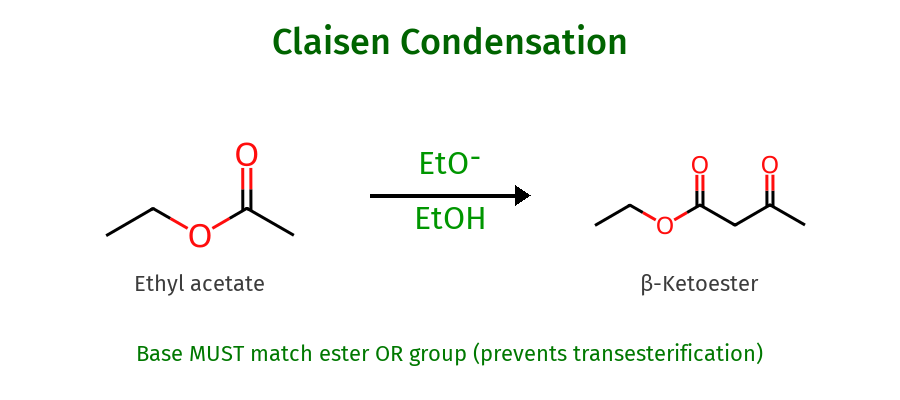
תגובת קלייזן
- אסטר + בסיס אתוקסיד ($\ce{EtO-}$) ← β-קטואסטר
- “הבסיס דומה לקבוצת $\ce{OR}$ של האסטר” - מונע ערבוב תוצרים
- ההבדל המרכזי מאלדול: קבוצת $\ce{OR}$ עוזבת ← נשאר קרבוניל (לא $\ce{OH}$)
- האלקטרונים: עולים למעלה ← חוזרים למטה ← מעיפים $\ce{OR-}$
- התוצר תמיד: קטון בעמדה β לאסטר
רטרו־קלייזן
- מחפשים: דיקטון עם אסטר בצד אחד
- “האסטר שתוקפים אותו הופך לקטון”
- הקשר שנשבר: בין פחמן α לפחמן הקרבונילי
דקרבוקסילציה
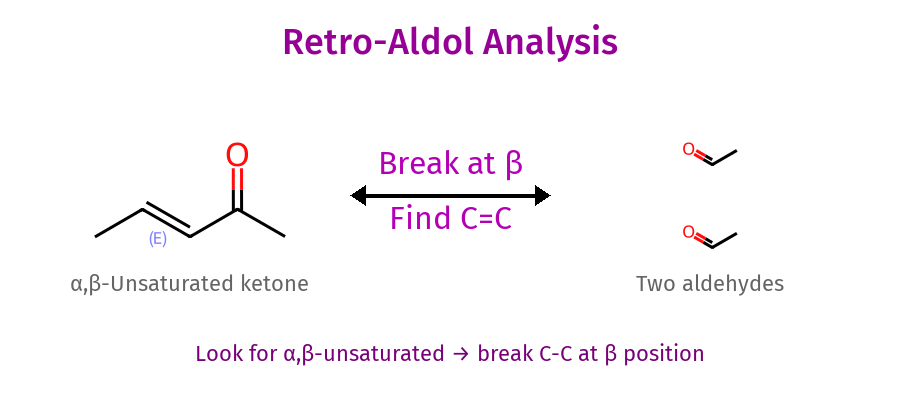
- תנאי הכרחי: $\ce{COOH}$ + קרבוניל בעמדה β + “הרבה חום”
- מה יוצא: $\ce{CO2}$ - רק פחמן החומצה הקרבוקסילית
- מנגנון: מצב מעבר טבעתי של 6 אטומים
- התוצר: מאבדים את $\ce{COOH}$, נשארים עם המולקולה
טיפים מהמרצה
סדר עבודה
- “תמיד למספר פחמנים” - במיוחד באלדול וקלייזן
- “מציירים קודם מי שתקף” ← יוצאים קשר ← מחברים מי שנתקף
- זיהוי קבוצות פונקציונליות ← קובע איזו תגובה
זיהוי מהיר
- “המתיל והקטון בהפרש של פחמן אחד” = סימן לאלדול
- קטון עם אסטר באותה מולקולה = קלייזן תוך־מולקולרי
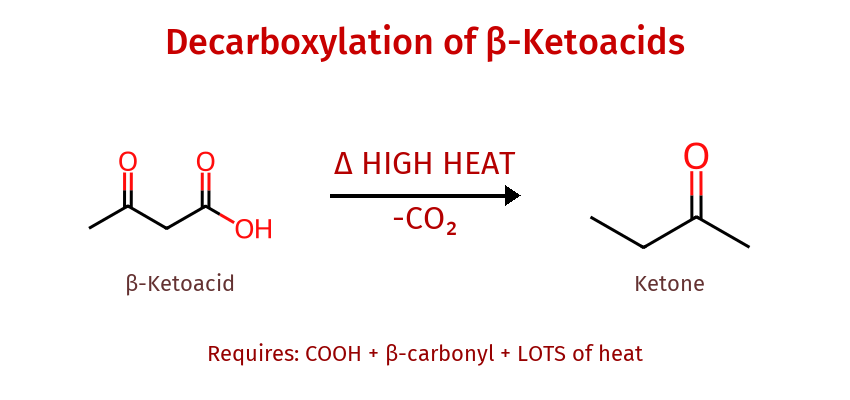
- בנזלדהיד ($\ce{PhCHO}$): “אין עליו מימני אלפא” - תמיד אלקטרופיל
מלכודות נפוצות
- “אלקיל הליד שניוני + בסיס חזק = בעיקר $\ce{E2}$” (לא $\ce{SN2}$)
- $\ce{PCC}$ על כוהל ראשוני: עוצר באלדהיד (לא ממשיך לחומצה)
- טבעת ארומטית: “קשה מאוד לשבור אותה - לא משתתפת”
רטרוסינתזה
- “תמיד להשוות תוצר לחומר התחלתי” - לזהות תוספת/הורדה של פחמנים
- סגירת טבעת? חשוב על אלדול/קלייזן תוך־מולקולרי
- פתיחת טבעת? אוזונוליזה על קשר כפול
האנולאט נוצר אצל מי שיש לו מימני אלפא.
האנולאט תוקף את הקרבוניל. האנולאט = הפחמן הטעון שלילית שמחתחבר לאלקטרופיל (הקרבוניל השני).
בדרך כלל, להבנתי, אלדהיד הוא האלקטרופיל, כי הוא יותר אלקטרופילי מקטון. אלקטרופיל = הקרבוניל שתוקפים.
דור פסקל