תוכן עניינים:
- פתיחה - מבט על ומנהלות
- תכניות התפתחותיות (Blueprints) בעובר
- עקרונות של התפתחות עוברית ויעדים
- ארבעת שלבי ההתפתחות העוברית (Embryogenesis)
- מסלולי העברת אותות (Signaling Pathways)
- מסלולי האותות (Pathways) הנלמדים בקורס
- אינטראקציות פיזיקליות בין תאים (Cell-Cell Physical Interactions)
- סכמה של מולקולת בטא-קטנין (CTNNB1)
- רגולציה על סיגנל ה־Wnt מחוץ לתא (Negative \& Positive Regulation)
פתיחה - מבט על ומנהלות
הקורס נכנס לעומק - ברמה המולקולרית - להבנת הנושא. אין לתת למילה ״מבוא״ בשם הקורס להטעות. הקורס דורש אינטגרציה של ידע קודם בביוכימיה, גנטיקה, ביולוגיה של התא וכימיה אורגנית.
למה זה חשוב - בעיקר חשיבה מדעית
הבסיס להשכלת רופא טוב הוא ידע רפואי. אנחנו נדרשים לחשיבה קלינית - והיא למעשה שם אחר לחשיבה מדעית. האנלוגיה בין עולם הרפואה למדע:
- השאלה: כפי שרופא שואל “מה לא תקין במטופל?”, המדען שואל שאלה מחקרית.
- הבדיקה: הרופא מבצע סדרת בדיקות (דם, שתן, CT, MRI) כפי שהמדען מבצע ניסויים.
- הדיאגנוזה: ניתוח תוצאות הבדיקות כדי להגיע למסקנה הוא לב־ליבה של החשיבה המדעית.
- הטיפול: הטיפול הרפואי הוא תמיד “Personalized” (אישי וספציפי) על סמך הממצאים המדעיים שנאספו.
מבט על - איך הקורס נראה ומה הפדגוגיה
חשוב להבחין בין תהליכים התפתחותיים לבין אמבריולוגיה.
- אמבריולוגיה (Embryogenesis): מתייחסת לשלבים שמהביצית המופרית ועד ללידה.
- תהליכים התפתחותיים: לא מסתיימים בלידה אלא נמשכים - גם עד גיל הבגרות ואף מעבר לכך (למשל במעי או בעור, שם התהליכים נמשכים גם לאחר גיל ההתבגרות להתחדשות הרקמות).
בקורס הנוכחי נלמד רק תהליכים שמתרחשים בעובר - אנחנו לא עוסקים בכל תחומי הביולוגיה ההתפתחותית.
כל התהליכים ההתפתחותיים מאוד שמורים ודומים באבולוציה (מתולעת, זבוב, דג זברה ועד אדם). הם דומים אך לא זהים - השוני נובע מאדפטציות אבולוציוניות שייצרו את המינים השונים על בסיס אותם מנגנונים.
לא נתמקד במושג אבולוציה מתוך הנחה (שלי לא ברורה) שאנחנו בקיאים בכך בלי קורס מקדים בנושא, או לחלופין שמדובר רק בהגדרה פשוטה שניתן לקרוא לבד.
שיטת ההוראה - השיטה ההשוואתית לעומת התמקדות במין
השיטה ההשוואתית (Comparative) כשמה כן היא - בוחנת תהליך ומשווה בין מינים. לעומת זאת, השיטה הלא־השוואתית מתמקדת במין אחד. בקורס שלנו נתמקד בשיטה לא השוואתית, כי השיטה ההשוואתית אומנם עמוקה יותר אך דורשת ידע קודם נרחב שאין לנו.
בקורס שלנו נלמד את העכבר. למה דווקא עכבר? לכאורה, למידה על בני אדם תהיה משעממת ולא תיתן לנו חשיבה מדעית (כך לפי המרצה), שכן היא בעיקרה תיאורית (דסקריפטיבית) ולא ניתן לערוך ניסויים ומניפולציות בבני אדם. (לעניות דעתי זה דווקא יוצר אתגר שדורש חשיבה, שוין).
המרצה הזכיר זבובים אך הסביר שהמורכבות הגנטית שלהם פשוטה מדי לעומת בני אדם. צוין שעכברים קרובים יחסית לבני אדם (יונקים), מאפשרים מחקר פעיל, ושהדברים שנלמד עליהם רלוונטיים ומבוססים על ניסויים.
תכניות התפתחותיות (Blueprints) בעובר
לעכבר יש תמיד 37 חוליות בעמוד השדרה - עובדה לכאורה טריוויאלית אך למעשה מהממת (לפי המרצה) שמעידה על תכנית התפתחותית מדויקת. בשקף אחר הוצג שלד עם צביעה מיוחדת - ניתן לראות שלחלק מהחוליות יש צלעות ולחלק אין.
לנחשים, לעומת עכברים, יש לפחות 400 חוליות (תלוי במין הנחש). בדומה לעכברים, גם כאן מספר החוליות יהיה זהה בכל הפרטים של אותו המין - מה שמלמד על כך שקיימת מערכת ספירה גנטית ברורה.

בירבוע (חיה עם שתי רגליים אחוריות ארוכות לריצה וקפיצה על חול, שתי רגליים קדמיות קצרות וזנב ארוך) ניתן לראות תכנית מדויקת לייצור גפיים שונות בכל הפרטים.
התפתחות כף היד בעכברים ובעטלפים
בתהליך של אפופטוזיס (מוות תאי מתוכנת) של הרקמה בין האצבעות נוצרת ההפרדה.
- Syndactyly (סינדקטילי): בעל חיים נולד בלי שנוצרת הפרדה, הפתולוגיה מתרחשת כשהאפופטוזיס נכשל. יכולה להיות גם חלקית (חיבור בין שתי אצבעות בלבד).
- השוואה לעטלף: בעטלף הוארכו האצבעות בצורה דרמטית, והאדפטציה האבולוציונית פשוט לא אפשרה לאפופטוזיס להפריד בין האצבעות כדי לייצר כנף. התהליך ההתפתחותי של יצירת הכנף והרגל דומים לחלוטין ברמה המולקולרית.
מבט כללי - אסימטריה (Symmetry vs Asymmetry)
מבחוץ האדם סימטרי, אך בציר ימין-שמאל יש מבפנים חוסר סימטריה (הלב משמאל, הכבד מימין). המוטיב החוזר: יש תכנית מאוד ברורה לקבוע את כל צירי הגוף (ימין-שמאל, ראש־זנב, גב־בטן).
באחוז קטן של בני האדם יש מה שנקרא Situs Inversus - היפוך מלא של ציר ימין-שמאל. התכנית יכולה להשתבש - לפעמים זה פתולוגי, ולפעמים (כמו בסיטוס אינברסוס) זה לא נחשב לפתולוגיה כי האדם בריא לחלוטין.
עקרונות של התפתחות עוברית ויעדים
דור - Generation
מבחינה ביולוגית, דור מוגדר כזמן שבין הפריית הביצית (יצירת האורגניזם) עד לשלב שאותו אורגניזם מגיע לבגרות מינית ויכול להתרבות.
שני יעדים לכל תהליך התפתחותי
- בתוך הדור: לייצר מגוון תאי (Cellular diversity) וארגונו של מגוון התאים במרחב.
- מדור לדור: המשכיות מדור לדור (Continuity of life). ליצירת אורגניזם נדרשת היכולת להתרבות, ובפרט יצירת תאי מין. עובר סטרילי כל התהליך שלו אינו רלוונטי ברמה האבולוציונית-ביולוגית.
מושגי יסוד
- התמיינות (Differentiation): התהליך שבו התאים רוכשים פונקציות שונות ונוצר המגוון התאי (Cellular diversity).
- מורפוגנזה (Morphogenesis): תהליך הסידור ויצירת צורה ומבנה. מבחינת התפתחות עוברית, איבר הוא בדיוק כמו מערכת.
ארבעת שלבי ההתפתחות העוברית (Embryogenesis)
לכל בעלי החיים יש ארבעה שלבים מרכזיים בהתפתחות העוברית לאחר ההפריה:
-
Cleavage (קליבג’): הביצית מתחלקת מהר עוד ועוד עד ליצירת קבוצה כדורית של תאים בשם בלסטולה (ביונקים קוראים לזה בלסטוציסט).
- Gastrulation (גסטרולציה): תנועה מסיבית של תאים, סידור מחדש של הבלסטולה. התוצר הסופי הוא יצירת שלוש שכבות הנבט (Germ layers) שהכרחיות להמשך:
- Ectoderm (אקטודרם)
- Mesoderm (מזודרם)
- Endoderm (אנדודרם)
-
Organogenesis (אורגנוגנזה): יצירת המערכות והאיברים מהשכבות שנוצרו.
- Germ cell formation: יצירת תאי המין. השלב הזה קורה מוקדם מאוד מבחינה כרונולוגית (בין הקליבג’ לתחילת הגסטרולציה) כדי להבטיח מוקדם ככל האפשר את הפרדת תאי המין מתאי הגוף הסומטיים, וכן את המשכיות הדורות.
מסלולי העברת אותות (Signaling Pathways)
שפת התקשורת של התאים בעובר היא Signaling pathways. יש ליגנד ורצפטור, המסלולים בדרך כלל נקראים על שם הליגנד (או לפעמים על שם הרצפטור).
כשליגנד נקשר לרצפטור יכולים להתרחש שני תהליכים (לעיתים במקביל):
-
Transcriptional dependent: השפעה על שעתוק גנים בגרעין. כולל לא רק אקטיבציה, אלא גם דיכוי או השתקה (סופרסיה) של גנים פעילים.
-
Transcriptional independent: תהליכים ציטופלזמטיים מהירים שלא דורשים הגעה לגרעין.
התא שמייצר את הסיגנל (Ligand production)
בהתפתחות עוברית יש חשיבות רבה לשאלה איזה תא מייצר את הליגנד, מתי הוא מייצר אותו ומה המרחק שלו מהתא המקבל.
אפקט אוטוקריני לעומת פאראקריני
- Autocrine (אוטוקריני): התא מפעיל את עצמו. אותו סוג של תא מייצר גם את הרצפטור וגם את הליגנד (יכול להשפיע גם על תא שכן מאותו סוג בדיוק).
- Paracrine (פאראקריני): תא אחד מייצר את הליגנד ותא שני (השכן) מייצר את הרצפטור ומגיב לו.
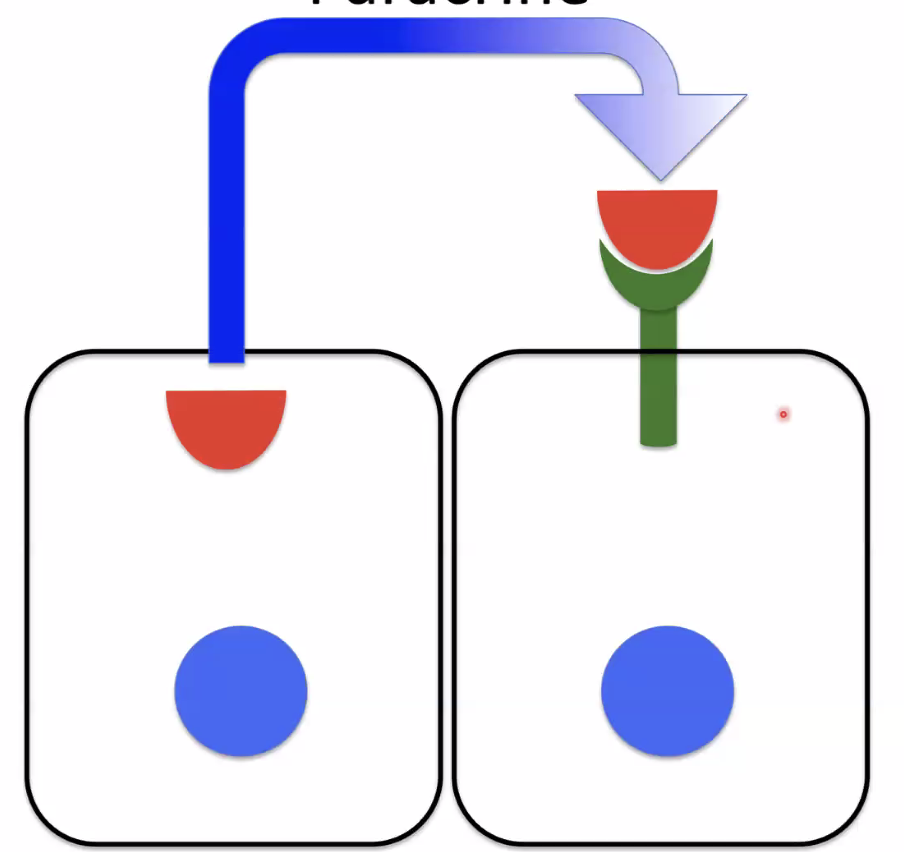
בסיגנל פאראקריני (כמו בתמונה למעלה) שני התאים אינם מאותו סוג אלא עברו התמיינות, שכן תא אחד מייצר רק ליגנד והשני רק רצפטור.
גרדיאנט מורפוגני (Morphogen Gradient)
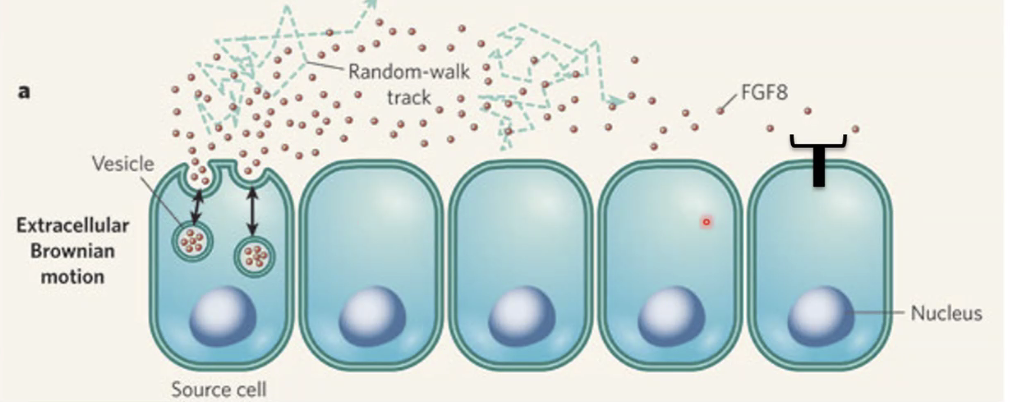
באיור למעלה רואים שלוש קבוצות של תאים בהקשר של מרחק מהליגנד:
- תא שיודע לייצר את הליגנד ומפריש אותו (השמאלי).
- תא שמבטא רצפטור, קרוב מספיק ולכן מגיב לליגנד.
- שלושה תאים מרוחקים שלמרות שיש להם רצפטור, הם “עיוורים” לליגנד כיוון שהוא לא מגיע אליהם (אולי עקב חלוקות תאים שהרחיקו אותם).
הליגנד מתפשט רנדומלית באמצעות דיפוזיה ולכן נוצר מפל ריכוזים (Gradient).
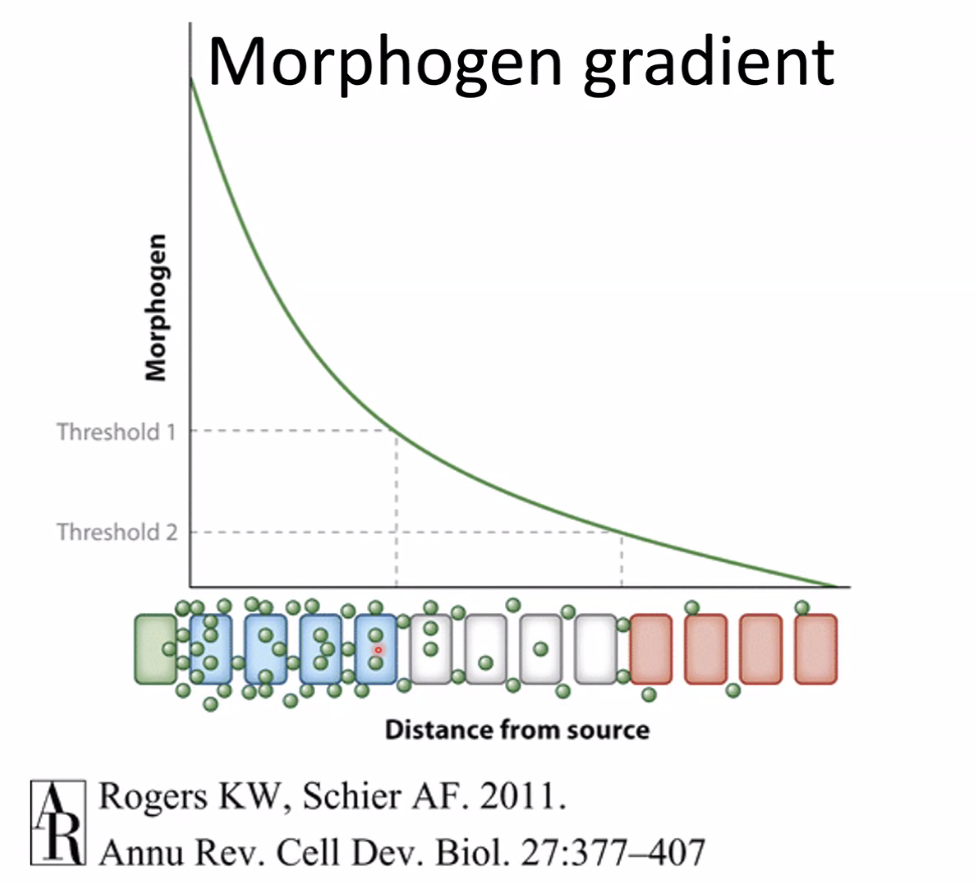
כאשר יש מפל ריכוזים וכל תא “רואה” ריכוז אחר של הליגנד, הריכוז עצמו יכול להשפיע על התגובה התאית (כל תא יתמיין למשהו אחר בהתאם לריכוז). במקרה כזה קוראים לליגנד מורפוגן (Morphogen). זה תלוי קונטקסט - אותו ליגנד במקום אחר יכול לפעול רק בצורת On/Off ללא קשר לריכוז.
רגולציה על הגרדיאנט: שרשראות סוכרים (HSPG)
מלבד הדיפוזיה וקצב ייצור הליגנד, ישנם גורמים נוספים השולטים במפל הריכוזים. על פני התאים ישנן שרשראות סוכרים ארוכות (קרבוהידרטים) שיש להן אפיניות נמוכה לליגנדים.
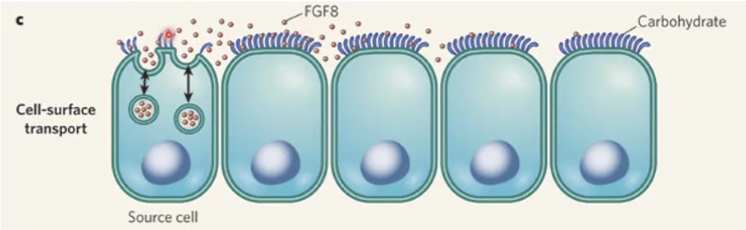
השרשראות הללו לוכדות את הליגנדים, מעכבות את תנועתם במרחב החוץ־תאי, וכך משפיעות משמעותית על הצורה והשיפוע של הגרדיאנט המורפוגני.
Heparan Sulfate Proteoglycans (HSPG): זה השם למבנה השלם של חלבון ושרשראות הסוכר. החלבון מכיל חומצת אמינו סרין (Serine), אליה נקשרים הסוכרים הראשונים.
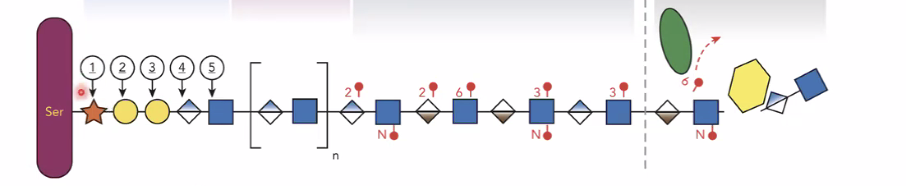
הסוכר הרביעי בשרשרת ההכנה (המעוין בתמונה) נקרא Glucuronic acid. אליו מוסיפים סוכר שנקרא GlcNAc (הכחול בתמונה). האנזימים מבצעים פולימריזציה ומוסיפים את הדימר (Glucuronic acid + GlcNAc) שוב ושוב עד שנוצרת שרשרת ארוכה של בין 100 ל־150 חזרות.
מודיפיקציות על השרשרת: לאחר שנוצרה, קבוצות של אנזימים עושות מודיפיקציות שונות על השרשראות:
- Sulfation (סולפטציה): הוספת קבוצות סולפט טעונות שלילית (הנקודות האדומות בתמונה) המשנות את האפיניות לליגנדים. השרשראות בדרך כלל טעונות שלילית (ולא חיובית).
- Epimerization (אפימריזציה): אנזים נוסף ממיר את ה־Glucuronic acid ל־
L-iduronic acidעל ידי שינוי המבנה המרחבי שלו.
הקומבינטוריקה של המודיפיקציות תלויה לחלוטין בהימצאות האנזימים ובריכוזם בכל תא ספציפי.
חלבוני הליבה (Core Proteins): למי מחברים את השרשראות הללו? 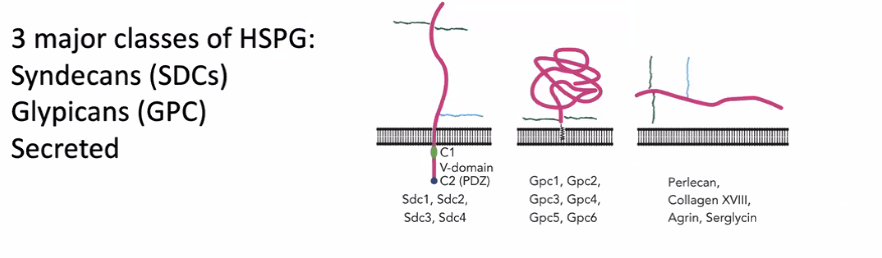
יש שלוש משפחות עיקריות של חלבונים נושאי שרשראות:
- Syndecans (SDCs): חלבונים חוצי-ממברנה.
- Glypicans (GPC): חלבונים שקשורים לממברנה באמצעות עוגן שומני.
- Secreted (מופרשים): חלבונים מופרשים למטריקס החוץ־תאי כמו Perlecan.
על פני קבוצה מסוימת של תאים יהיה רפרטואר מסוים של חלבונים ושרשראות בעלות מודיפיקציות שונות. על פני תאים אחרים הרפרטואר יהיה שונה לחלוטין. כתוצאה מכך, הגרדיאנט והפצת הליגנד תלויים לחלוטין בקונטקסט הרקמתי ובסוג החלבונים והסוכרים שיש באותו אזור. זה מסביר מה הכוונה ב”תלוי קונטקסט” (Context-dependent).
מסלולי האותות (Pathways) הנלמדים בקורס
השפה שבה התאים מדברים. המסלולים המרכזיים שניגע בהם:
- Wnt
- BMP (תת־משפחה בתוך סופר־משפחה גדולה שנקראת TGF-beta)
- FGF (תת־משפחה בתוך הסופר־משפחה RTK - רצפטורים בעלי פעילות טירוזין קינאז)
- Shh (Sonic Hedgehog)
- Notch
ארבעת הראשונים נקראים על שם הליגנד, והמסלול האחרון (Notch) נקרא על שם הרצפטור.
1. Wnt Pathway
משפחת הליגנדים כוללת 19 חברים (Wnts שונים), ומשפחת הרצפטורים (Frizzled) כוללת 10 חברים.
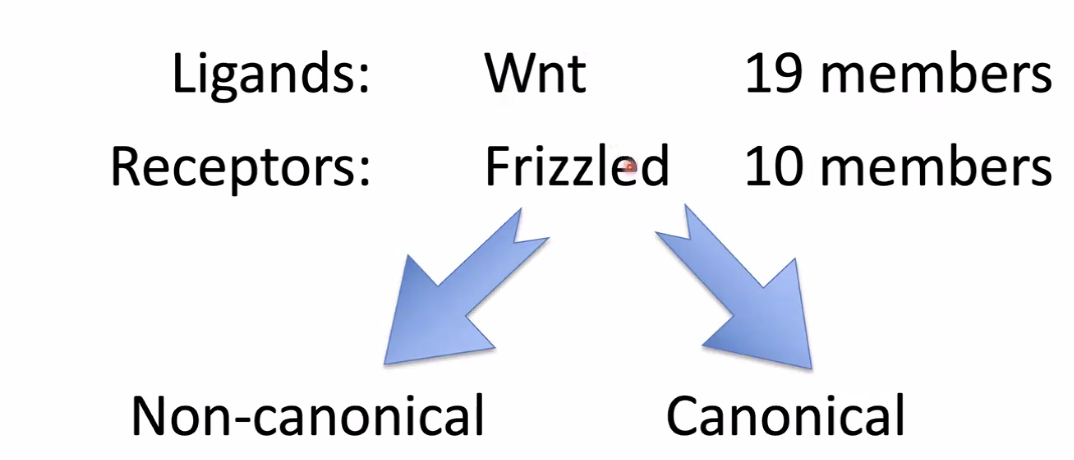
כשליגנד מסוג Wnt נקשר לרצפטור Frizzled, יכולים להתרחש שני מסלולים מרכזיים:
-
המסלול הקנוני (Canonical): מפעיל קו־פקטור לשעתוק בשם β-catenin. יש רק סוג אחד של β-catenin בתא, בניגוד לריבוי הליגנדים והרצפטורים. אופן הפעולה המדויק תלוי באינטרפרטציה של התא (רדונדנטיות וקונטקסט).
-
המסלול הלא־קנוני (Non-canonical): מסלולים שמופעלים ללא מעורבות של β-catenin.
מקור השם ״קנוני״/״לא־קנוני״ הוא היסטורי. בקורס נתמקד במסלול הקנוני.
מצב כבוי (Wnt OFF) - כשאין Wnt בסביבה
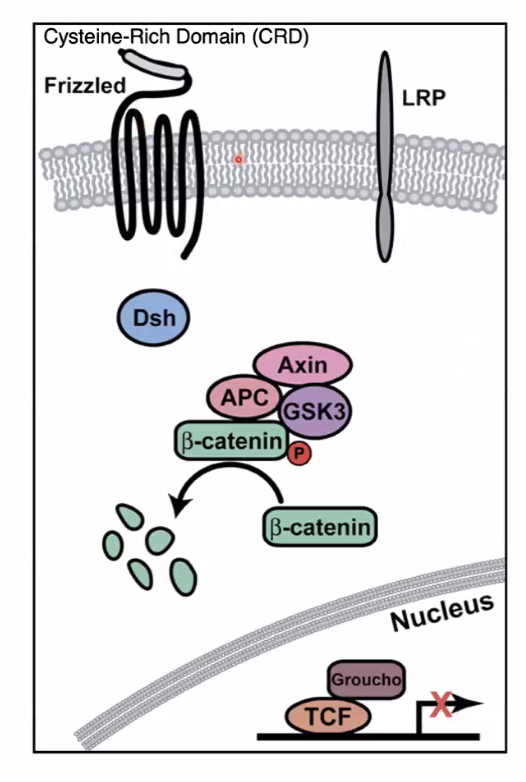
זהו המצב שבו אין ליגנד Wnt מחוץ לתא. על ממברנת התא נמצאים הרצפטור Frizzled, שהוא חלבון החוצה את הממברנה 7 פעמים, והקו־רצפטור LRP.
בציטוזול נמצא קומפלקס בשם Destruction Complex (“קומפלקס הפירוק”), שמורכב בעיקר מן החלבונים Axin ו־APC, יחד עם הקינאז GSK-3 beta.
תפקיד הקומפלקס הוא ללכוד את beta-catenin ולסמן אותו לפירוק. לשם כך, GSK-3 beta מבצע עליו פוספורילציה, ולאחר מכן החלבון עובר יוביקוויטינציה ומפורק בפרוטאוזום. להרחבה על מסלול הפירוק אפשר לראות שיעור 20 בקורס ביולוגיה של התא.
במקביל, בתוך הגרעין, פקטור השעתוק TCF קשור לחלבון המדכא Groucho. במצב הזה גני המטרה של מסלול Wnt נשארים כבויים, כלומר אין הפעלה של השעתוק שלהם.
מצב מופעל (Wnt ON) - כשיש ליגנד Wnt בסביבה
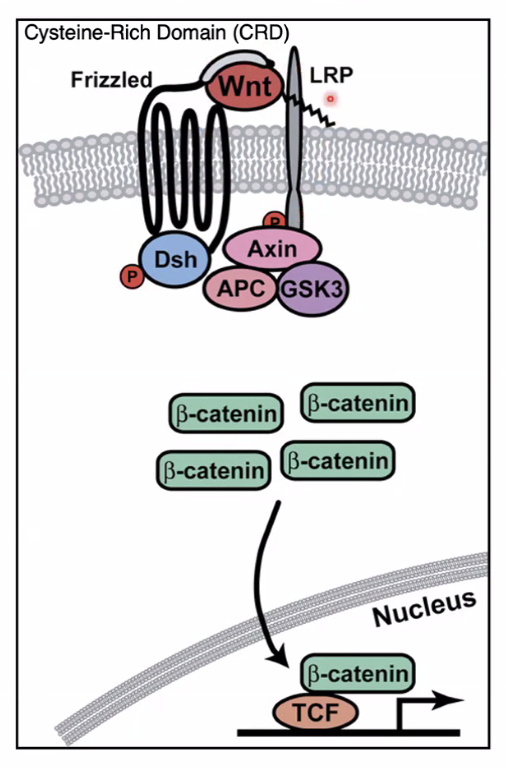
כאשר ליגנד Wnt נמצא בסביבה, הוא נקשר לדומיין החוץ־תאי של Frizzled וגם לקו־רצפטור LRP.
הקישור הזה גורם לגיוס של Destruction Complex אל ממברנת התא. ברגע שהקומפלקס מגויס לממברנה, הוא כבר לא מפרק ביעילות את beta-catenin.
כתוצאה מכך beta-catenin מצטבר בציטוזול. לאחר מכן הוא נכנס לגרעין, ושם הוא מסלק את Groucho, נקשר ל־TCF, והופך אותו מפקטור מדכא לפקטור מפעיל.
התוצאה הסופית היא הפעלה של שעתוק גני המטרה של מסלול Wnt.
התחלה והגברה של המסלול (Initiation & Amplification)
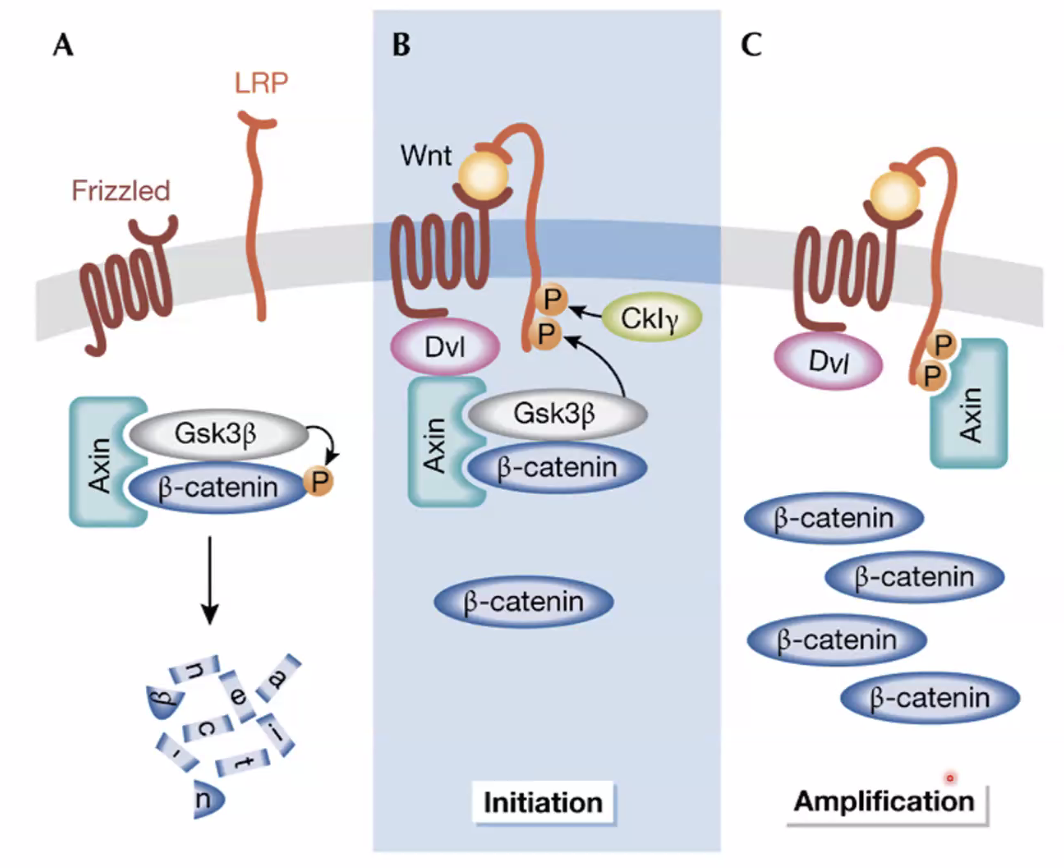
התגובה המיידית לקישור הליגנד היא ה־Initiation: ה־Destruction complex הקיים מגויס לממברנה. כשהקומפלקס נמצא על הממברנה, ה־GSK-3 beta מבצע פעולת פוספורילציה (זרחון) על הזנב של הקו־רצפטור LRP, שיוצרת אתר קישור חדש (Docking site) לחלבון הפיגום אקסין (Axin).
בשלב ה־Amplification (הגברה) אקסין שנוצר בתא מגויס ישירות לממברנה בזכות ה־Docking site שהזרחון יצר. בעקבות זאת, ה־Destruction complex לא יכול כלל להיווצר מחדש בציטוזול (כי חסר אקסין) והסיגנל מוגבר באופן משמעותי.
אינטראקציות פיזיקליות בין תאים (Cell-Cell Physical Interactions)
קיימים שלושה מנגנונים מרכזיים לאינטראקציות פיזיקליות בתאי אפיתל:
- Tight junctions: ממוקמים בצד האפיקלי. יוצרים מחסום הרמטי לחלוטין שלא מאפשר מעבר חומרים ומים בין התאים.
- Adherens junctions (AJ): צמתי הצמדה. ממוקמים לרוב מתחת ל־Tight junctions.
- Desmosomes (דסמוזומים): צמתים דמויי “כפתורים” מפוזרים באופן ספורדי שמחוברים לקורי ביניים (Intermediate filaments).
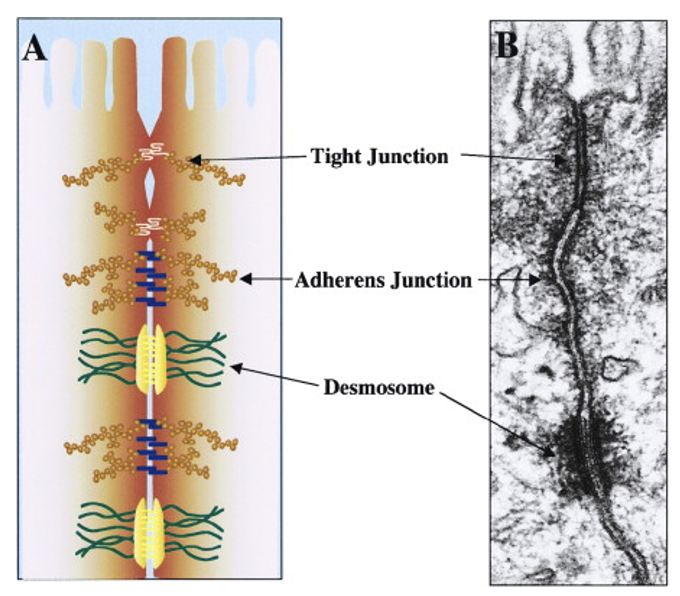
נסתכל על סכמה תלת מימדית של שלושה תאים:
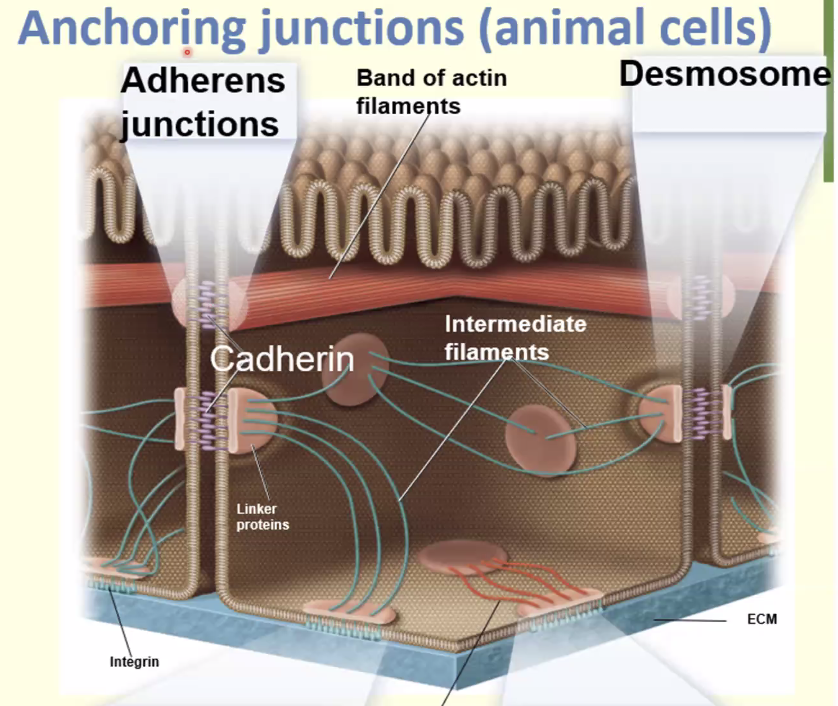
באמצעות המבנה ניתן לראות שה־Adherens junctions יוצרים חגורה (Zonula Adherens) שמקיפה ותופרת את התאים זה לזה לכל אורכם.
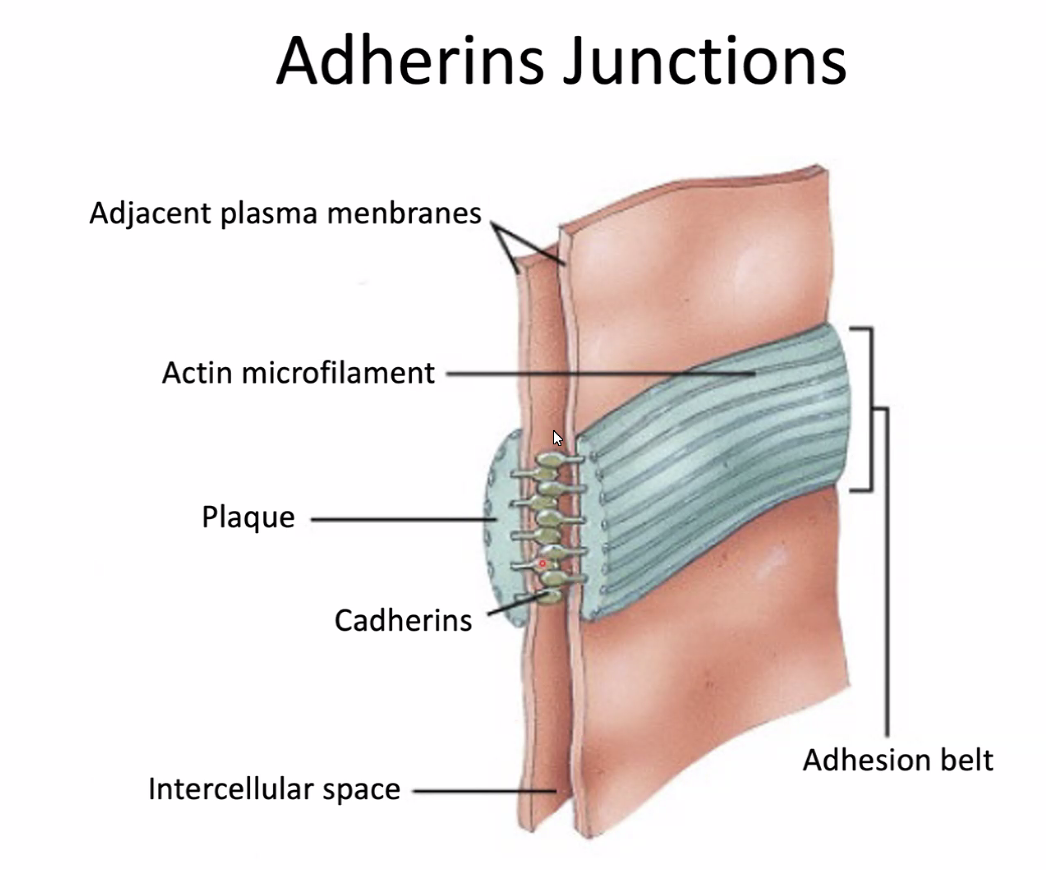
Cadherins (קדהירינים)
החלבונים שמתווכים את החיבור ב־Adherens junctions הם הקדהירינים. אלה חלבונים טראנס־ממברנליים שפועלים כמו “ריצ’רץ’” בין תאים.
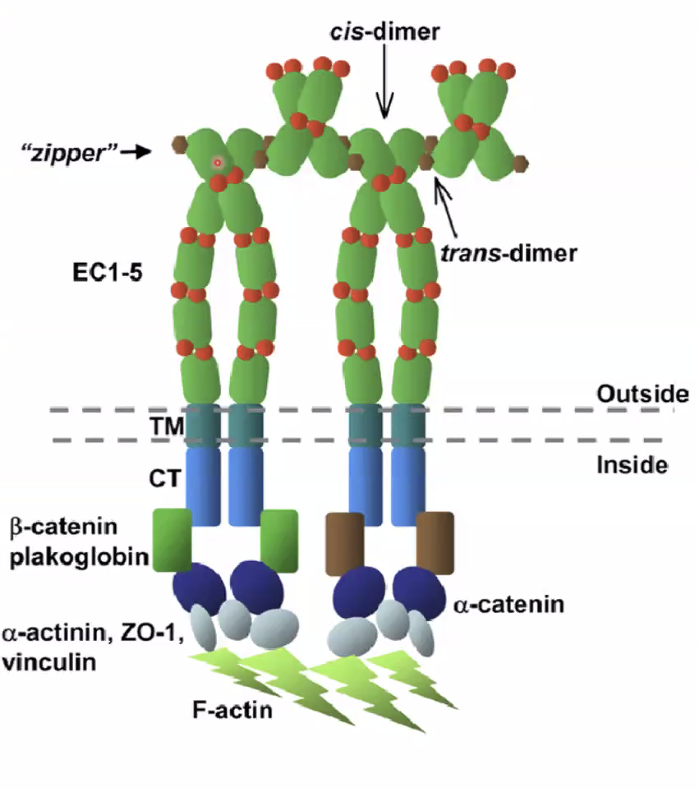
לכל קדהירין יש חמישה דומיינים חוץ תאיים (Extracellular domains), כשהאינטראקציה מתרחשת אך ורק בדומיין החיצוני והקיצוני ביותר.
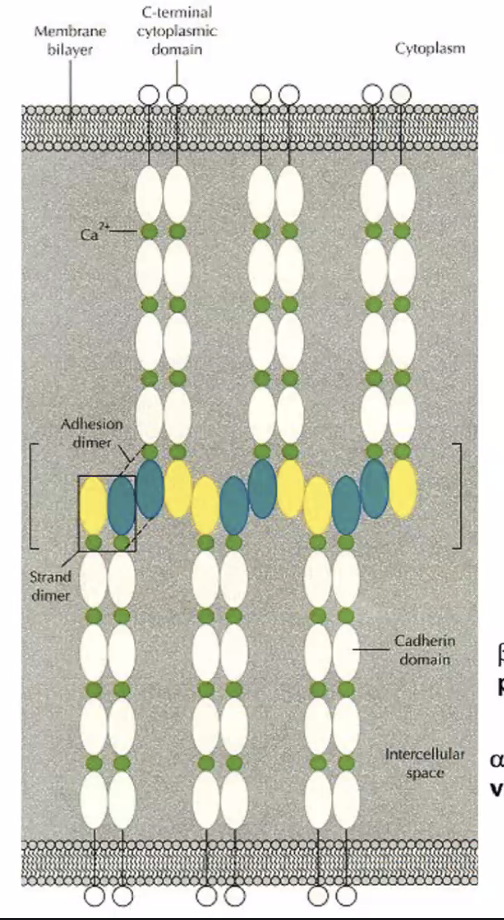
- Cis-dimer: כשהאינטראקציה מתבצעת בין מולקולות קדהירין על פני אותו התא (ליצירת דימר יציב).
- Trans-dimer: כשהאינטראקציה מתבצעת בין קדהירין של תא אחד לקדהירין של התא השכן (לצורך הצמדת התאים).
מבט על שני תאים - הצד הציטוזולי והקשר לβ-catenin
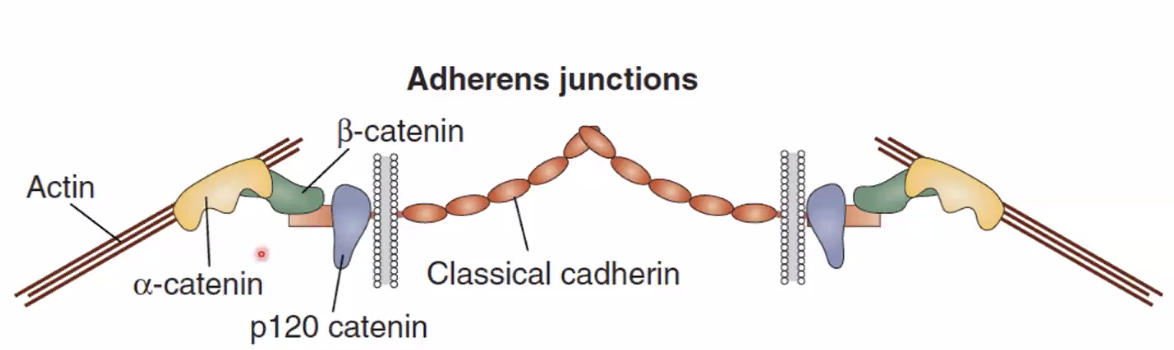
בצד התוך־תאי (ציטוזולי), מולקולת ה־β-catenin נקשרת לזנב של הקדהירין. אל הβ-catenin נקשר חלבון אחר בשם α-catenin (alpha-catenin), שמקשר את כל הקומפלקס הזה לפילמנטים של אקטין.
ל־β-catenin יש אפוא תפקיד כפול: גם במסלול השעתוק Wnt Signaling, וגם בייצוב צמתי ה־Adherens Junctions בשלד התא. הקדהירינים מסונתזים ב־ER, וה־β-catenin חייב להיקשר אליהם כבר שם כדי להגן עליהם מפירוק.
מורפולוגיה של צמתי ה־AJ
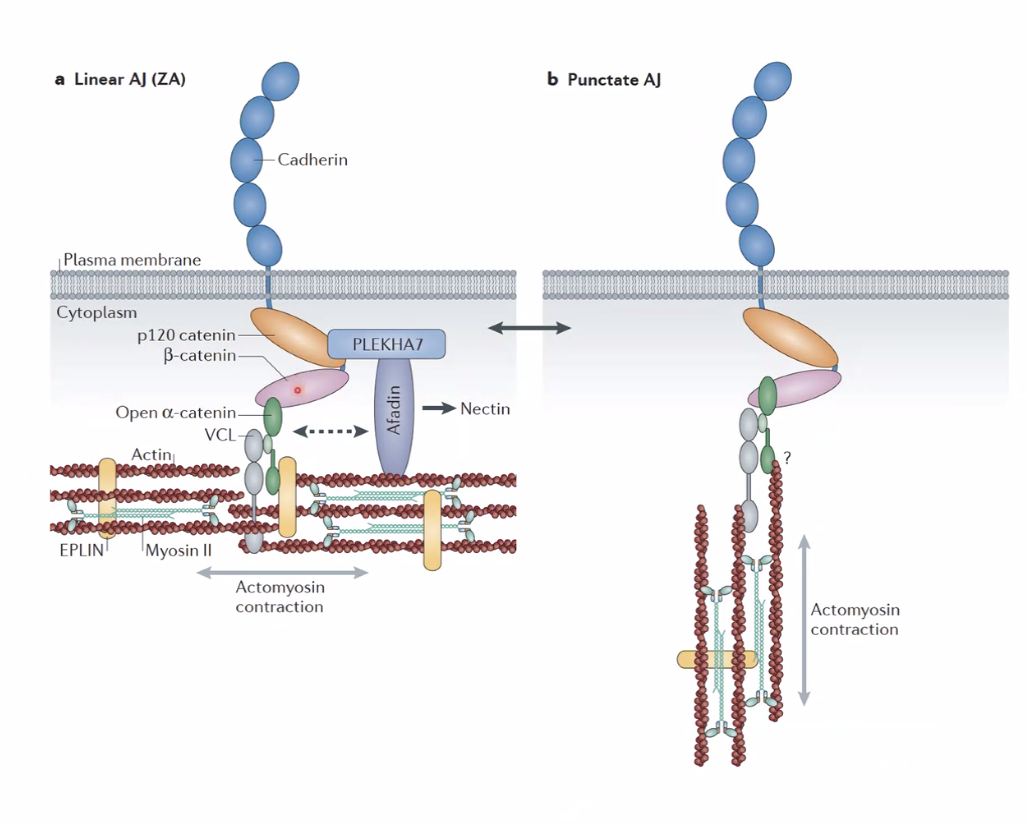
נסתכל איך החגורה בנויה, היא יכולה להופיע בשתי מורפולוגיות שונות:
- Linear AJ (בצד שמאל): חגורה קווית, ישרה ורציפה. הפילמנטים של אקטין שזורים בפילמנטים של חלבון הכיווץ מיוזין. הכיווץ שלהם מאפשר לשמור על יציבות ועל צורה של רקמת אפיתל חזקה.
- Punctate AJ (בצד ימין): חגורה משוננת, מנוקדת ומופרדת. כשהעובר צריך להתקפל או כשתאים צריכים לנוע ולנדוד (Migration), המערכת משנה את זווית סיבי האקטין, הצומת “נפתח” מליניארי לנקודתי, ומאפשר גמישות וניתוק של התאים.
אמונוסטיינינג (Immunostaining)
שיטה מדעית לצביעת תאים:
- DAPI (צבע כחול): מולקולה שחודרת לגרעין, נקשרת ל־DNA וזוהרת באור UV. צובעת גרעינים בלבד.
- נוגדנים ספציפיים (צבע אדום): מאפשרים צביעת חלבון ממוקד. בתמונה שהוצגה, נצבע β-catenin, והוא הופיע מרוכז בממברנה, דבר המוכיח את מיקומו הקבוע ב־Adherens junctions ללא קשר לסיגנל Wnt.
סכמה של מולקולת בטא-קטנין (CTNNB1)
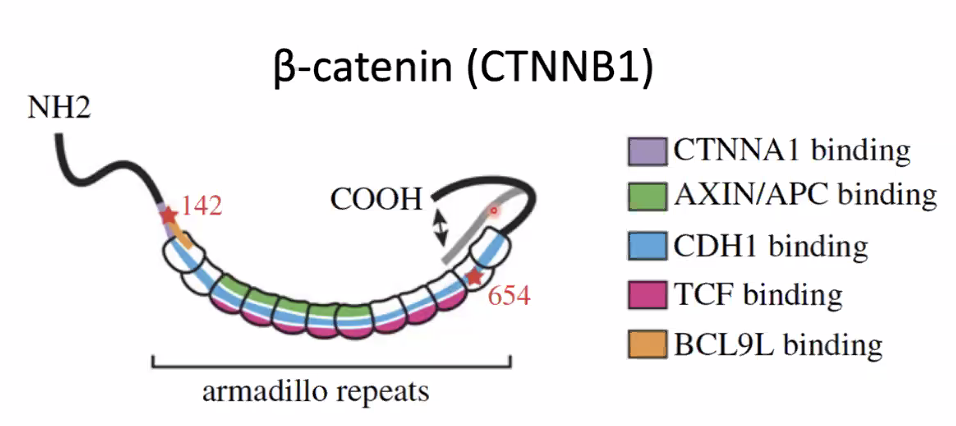
החלבון בטא-קטנין בנוי מכמה אזורים חשובים:
-
הקצה ה־N-טרמינלי באזור זה יש שיירי סרין ותריאונין. אלה הם אתרי פוספורילציה שמשמשים לסימון החלבון לפירוק.
-
האזור המרכזי - Armadillo repeats במרכז החלבון יש 12 חזרות מסוג Armadillo. זהו הדומיין שאליו נקשרים כמה שותפים שונים, ובהם:
- קדהירין
- ה־Destruction complex
- פקטור השעתוק TCF
חשוב להבין שאתרי הקישור האלה חופפים חלקית, ולכן בטא-קטנין לא יכול להיקשר לכולם בו־זמנית. בדרך כלל, בכל רגע נתון הוא יהיה קשור רק לאחד מהם.
-
טירוזין 654 בעמדה 654 נמצאת חומצת האמינו טירוזין. כאשר היא עוברת פוספורילציה, בטא-קטנין מתנתק מהקדהירין. כתוצאה מכך יציבות הקדהירין נפגעת, הצומת נפתח, וזה יכול לקרות גם בלי הפעלה של Wnt.
התמונה הגדולה
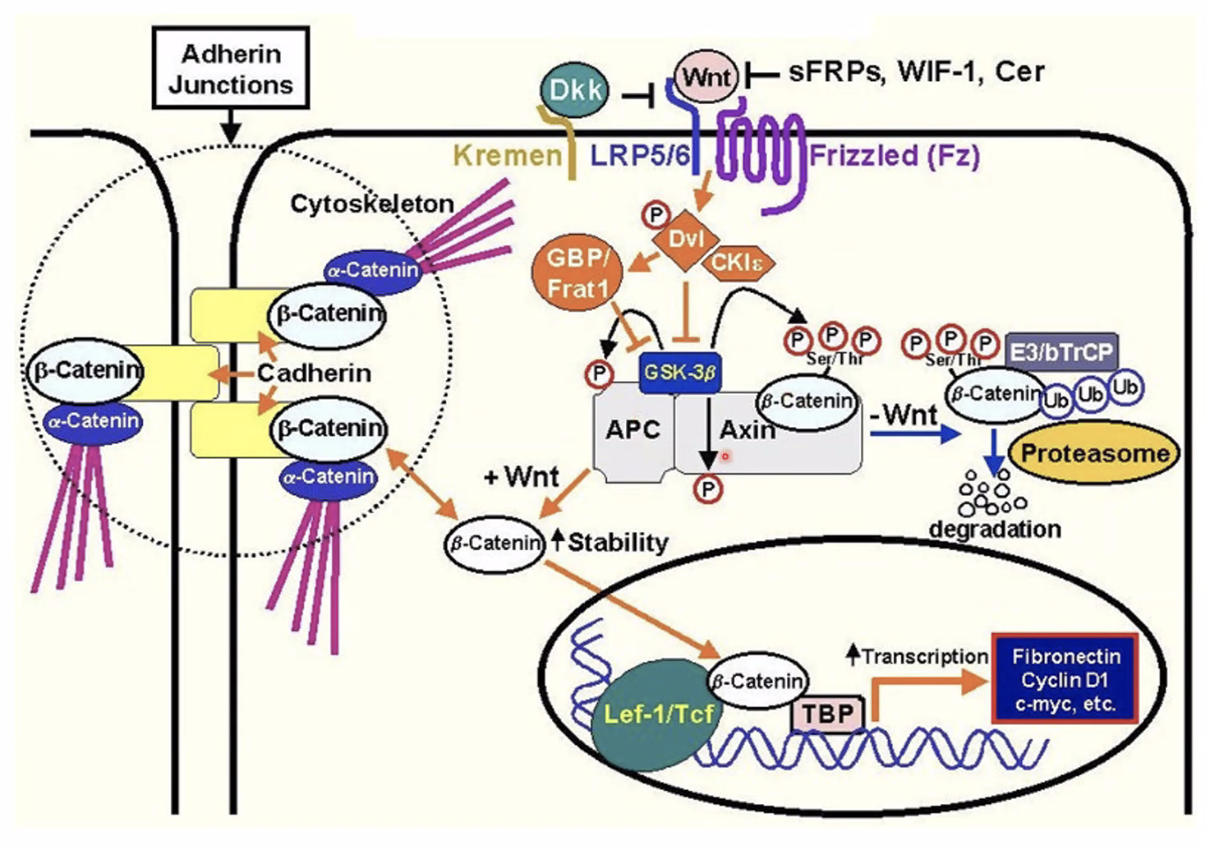
תרשים המסכם את הקשר בין שתי הפונקציות של הβ-catenin: כמתווך בהעברת סיגנל שעתוק בגרעין (כשיש Wnt), וכמייצב מבני בצמתי ה־Adherens בממברנה (כל עוד טירוזין 654 אינו מזורחן).
רגולציה על סיגנל ה־Wnt מחוץ לתא (Negative & Positive Regulation)
קיימים מנגנונים תאיים לשלוט ברגישות התא ל־Wnt.
מעכבים תחרותיים (Negative Regulation)
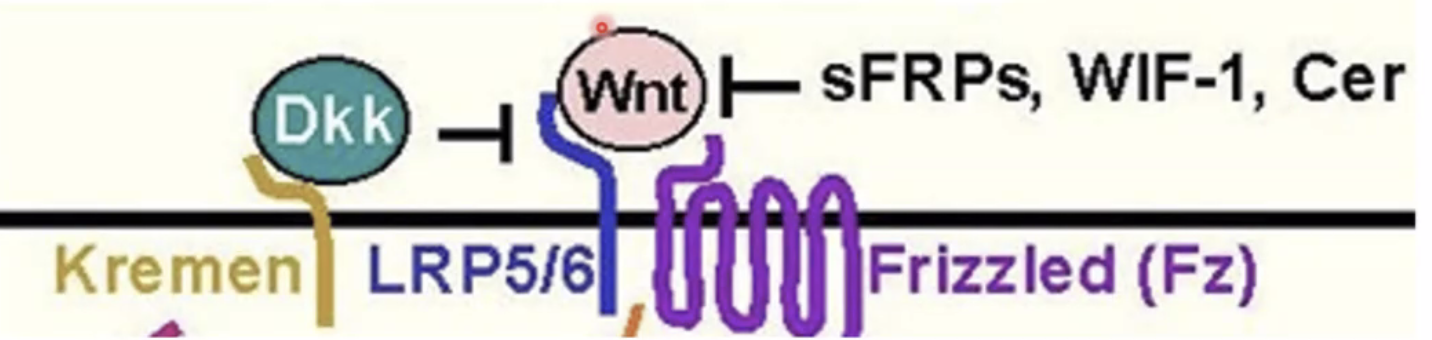
חלבונים כמו sFRP, WIF-1, ו־Cerberus הם חלבונים מסיסים שמופרשים מחוץ לתא. הם משמשים כמעכבים תחרותיים שנקשרים ישירות לליגנד Wnt בתמיסה, ומונעים ממנו לגשת לרצפטור. לדוגמה, sFRP דומה במבנה שלו לדומיין הקושר של הרצפטור Frizzled, מה שמאפשר לו לקשור את Wnt ביעילות ולעכב את המסלול.
סילוק הקו־רצפטור LRP (Kremen & DKK)
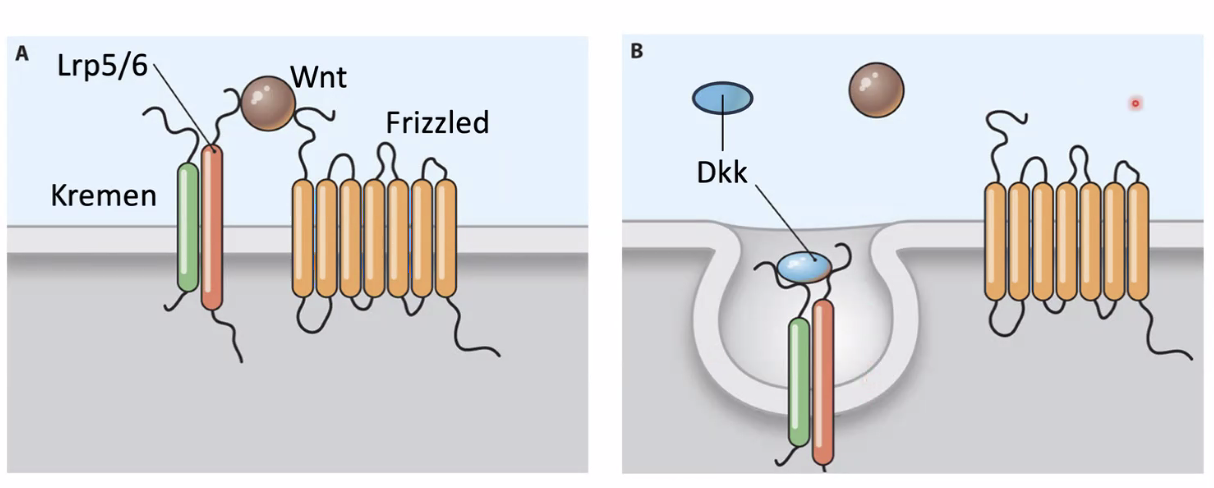
עוד סוג של רגולציה שלילית: החלבון DKK1 (שמופרש החוצה) יכול להיקשר ל־LRP ולחלבון טראנס־ממברנלי נוסף בשם Kremen. הקישור המשולש גורם לאינטרנליזציה (הכנסה באנדוציטוזה) של ה־LRP לתוך התא, כך שעל הממברנה נשאר רק הפריזלד ללא הקו־רצפטור שלו, והמסלול לא יכול להיות מופעל גם אם Wnt קיים.
פירוק פריזלד (Znrf3 / Rnf43)
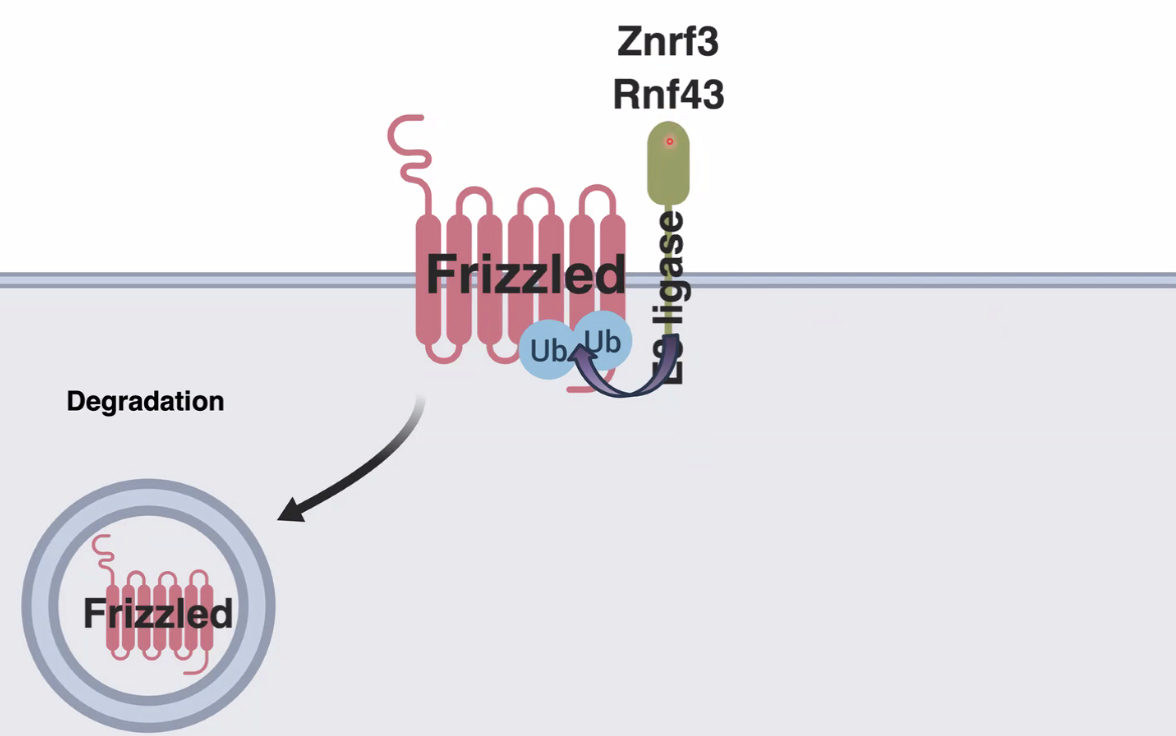
סוג שלישי של רגולציה שלילית מבוצע על ידי אנזימי E3 Ubiquitin ligases בשמות ZNRF3 ו־RNF43 הנמצאים בממברנה. הם מבצעים יוביקוויטינציה לרצפטור Frizzled עצמו, מסמנים אותו לפירוק ומסירים אותו מהממברנה באופן רציף. ללא רצפטור, התא עיוור לליגנד.
רגולציה חיובית: R-Spondins
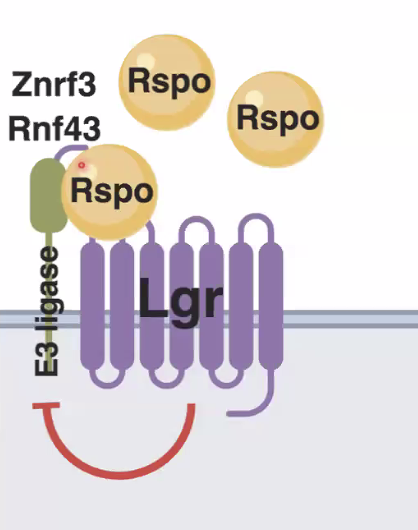
כדי להסיר את העיכוב השלילי של ZNRF3/RNF43 ולהפוך את התא לרגיש מאוד ל־Wnt, חלבונים מופרשים בשם R-spondins (Rspo) יודעים להיקשר לקו־רצפטור בשם LGR ולאנזימי הליגאז ZNRF3/RNF43 המעכבים. הקישור הזה מעכב את הפעילות הקטליטית של אנזימי הפירוק. התוצאה: רצפטורי הפריזלד מפסיקים לעבור פירוק, מצטברים על הממברנה, והתא יכול להגיב בעוצמה לליגנד Wnt.
סיכום רגולציה חיובית ושלילית
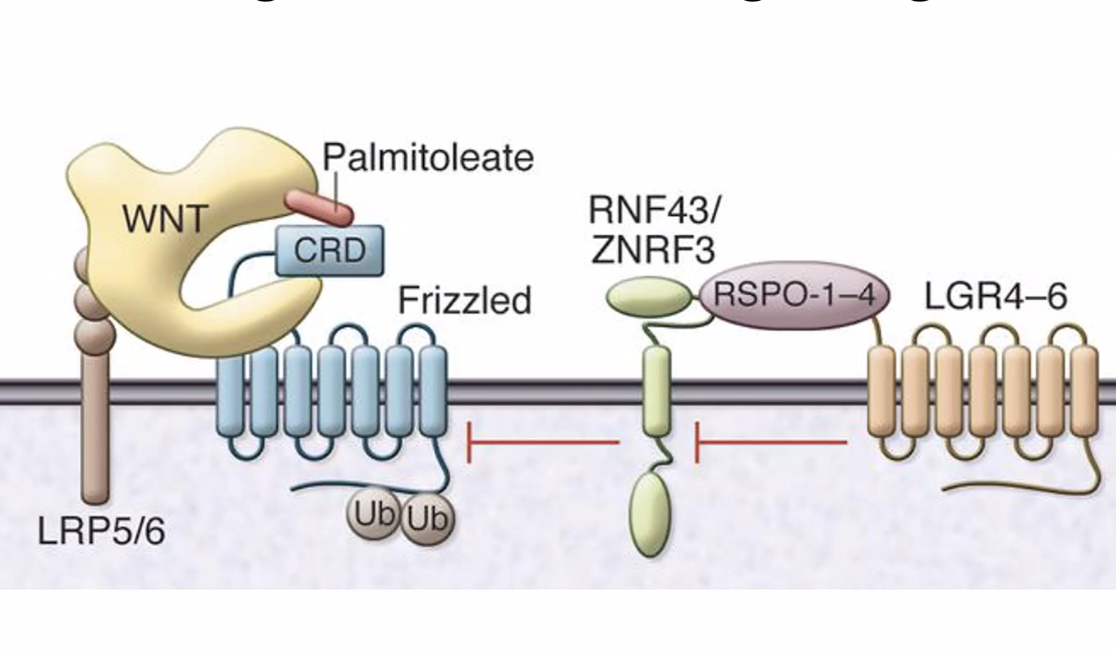
תרשים המסכם את כלל מנגנוני ה־Negative וה־Positive Regulation שפורטו לעיל ושולטים בעוצמת המסלול.
דור פסקל