מתודולוגיות לחקר התפתחות עוברים
עד עכשיו הקורס עסק ב״שפה״ שבה תאים עובריים מתקשרים זה עם זה כדי ליצור בסופו של דבר אורגניזם שלם. מכאן נכנסים לשלבי ההתפתחות העוברית עצמם: Cleavage, לאחר מכן גסטרולציה (Gastrulation), ובהמשך גם Organogenesis, לפי ההתקדמות.
לפני שניכנס ל־Cleavage נגדיר את המתודולוגיות האמפיריות המרכזיות שבהן משתמשים כדי להבין תהליכים התפתחותיים.
Loss of Function
Loss of function הוא ניסוי שבו פוגעים בגן מסוים שחושדים שמעורב בתהליך התפתחותי. הפגיעה יכולה להיות מחיקה של הגן או יצירה של חלבון לא פונקציונלי. המטרה היא לשאול מה קורה כאשר אותו גן או חלבון אינו פעיל.
יש שתי רמות מרכזיות שבהן משתמשים בגישה הזאת:
-
פגיעה במסלול איתות - כאשר רוצים להבין מסלול תקשורת בין תאים, לא תמיד מספיק לפגוע ברצפטור אחד. במסלולים רבים יש יתירות (Redundancy): מספר ליגנדים, רצפטורים או מרכיבים שמסוגלים לפצות אחד על השני. לכן מחפשים את צוואר הבקבוק של המסלול - נקודה מרכזית שאם פוגעים בה המסלול נחסם. לדוגמה, במסלול Wnt הקנוני יש הרבה ליגנדים ורצפטורים, אבל
β-cateninהוא אפקטור מרכזי אחד בלבד. -
פגיעה בפקטור שעתוק - פקטורי שעתוק (transcription factors) יכולים לשמש כ־master regulators: הם מכתיבים לתא תוכנית התפתחותית שלמה. לכן פגיעה בגן שמקודד לפקטור שעתוק יכולה לחשוף את תפקידו בתהליך ההתפתחותי.
Gain of Function
Gain of function הוא ניסוי שבו לא מורידים פעילות של גן, אלא מוסיפים או מגבירים אותה. יש שתי צורות עיקריות:
| סוג הניסוי | מה עושים? | משמעות |
|---|---|---|
| ביטוי יתר (Overexpression) | מעלים את רמת הביטוי של גן בתא שכבר מבטא אותו | בודקים מה קורה כאשר הפעילות קיימת בעוצמה גבוהה מהרגיל |
| ביטוי אקטופי (Ectopic expression) | מבטאים גן בתא שבדרך כלל אינו מבטא אותו | בודקים מה קורה כאשר תא מקבל חלבון שאינו חלק מהתוכנית הרגילה שלו |
לדוגמה, Pax6 בזבובי דרוזופילה: בניסוי loss of function, מוטציה ב־Pax6 גורמת לכך שלא נוצרת עין, בעוד ששאר הזבוב מתפתח יחסית כרגיל. מכאן אפשר להסיק ש־Pax6 חיוני ליצירת עין, אבל לא מעבר לכך.
בניסוי gain of function, כאשר מבטאים Pax6 באזורים בהם הוא לא אמור להתבטא, למשל ברגל או בגב, נוצרים שם מבנים דמויי עין. העיניים האלה אינן פונקציונליות כי הן לא מחוברות למערכת העצבים, אבל עצם הופעתן מראה ש־Pax6 מסוגל להפעיל תוכנית התפתחותית מורכבת של יצירת עין.
המסקנה המתודולוגית היא ש־gain of function ו־loss of function משלימים זה את זה: Gain of function בלבד לא מספיק כדי להבין משמעות פיזיולוגית, כי צריך לדעת גם מה קורה כאשר הגן חסר.
Cleavage: מושגים בסיסיים
לפני שנתאר את שלב ה־Cleavage (״קרע תא״ לפי ויקיפדיה) נסדר את המושגים הקשורים לתאי המין ולזיגוטה.
- זיגוטה - תא אחד שנוצר מאיחוד של ביצית ותא זרע; התא הראשון של העובר.
- Primordial germ cells (PGCs) - תאים שנוצרים בתחילת הגסטרולציה. בשלב הזה עדיין אין איברי מין, ולכן התאים האלה נודדים במהלך ההתפתחות העוברית עד שהם מגיעים לאיברי המין המתפתחים.
Germ cells (GCs)- PGCs שכבר התמקמו באיברי המין. בשלב הזה אין עדיין משמעות לזכר או נקבה; בהמשך, בהתאם לקונטקסט, הם מתמיינים לכיוון יצירת תאי זרע או לביציות.- גמטות (Gametes) - תאי המין הסופיים: תא זרע או ביצית. הם נוצרים מה־germ cells לאחר תהליך התמיינות וחלוקת הפחתה.
- תאים סומטיים (Somatic cells) - תאי הגוף.
ההבדל המרכזי בין תאים סומטיים ל־germ cells הוא שתאים סומטיים מבצעים מיטוזה בלבד, בעוד ש־germ cells יכולים לבצע גם מיטוזה וגם מיוזה.
מיוזה ומיטוזה
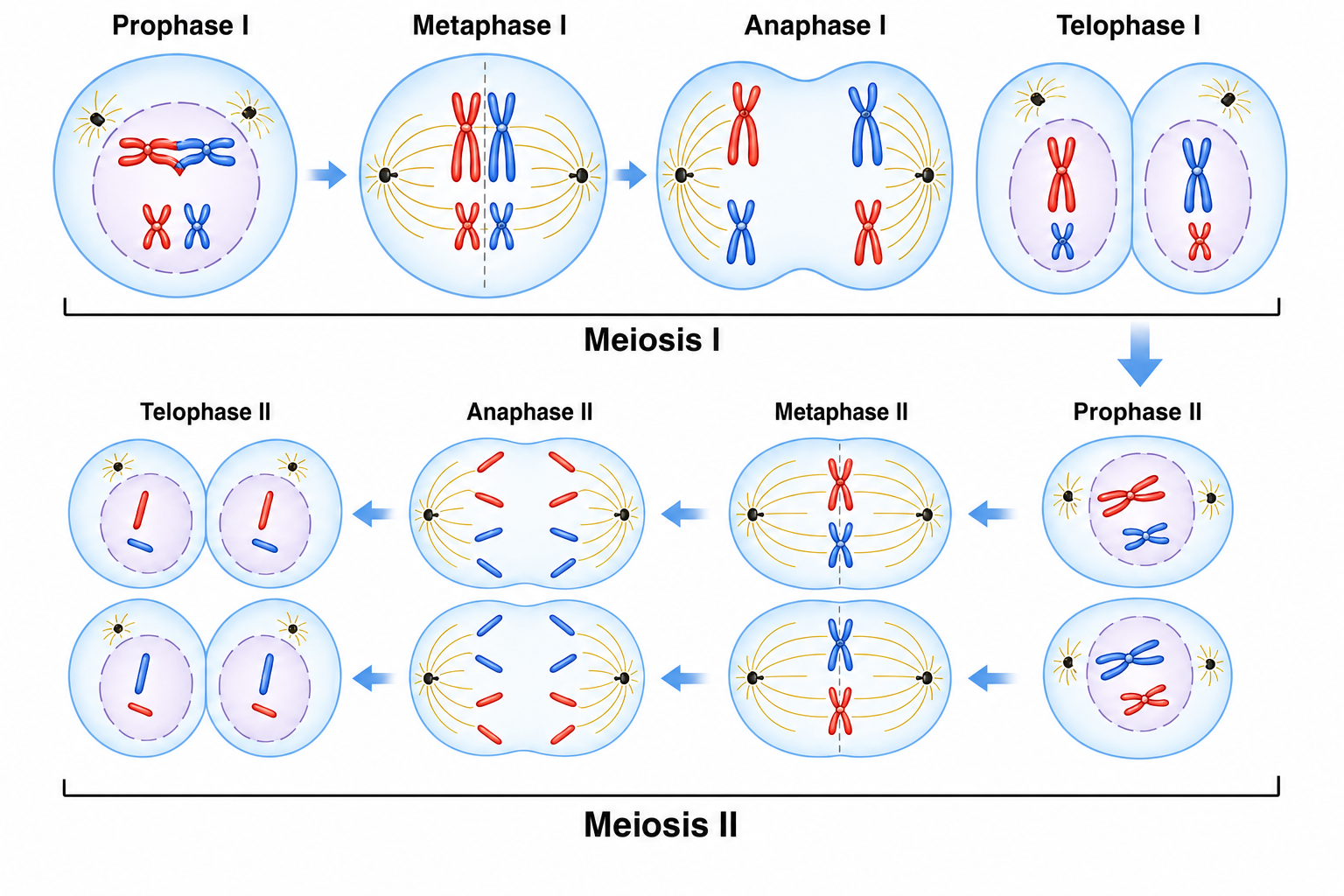
מיוזה כוללת שתי חלוקות: החלוקה המיוטית הראשונה והחלוקה המיוטית השנייה.
מיוזה I
בחלוקה המיוטית הראשונה, השלב הראשון הוא פרופאזה I. לפני הדיחסה מתרחשת הכפלה (רפליקציה) של ה־DNA, כך שנוצרות כרומטידות אחיות, ולאחר מכן הכרומוזומים ההומולוגיים מזדווגים זה עם זה (Pairing).
במעבר למטאפזה I, הכרומוזומים ההומולוגיים מסתדרים במרכז התא. כל כרומוזום הומולוגי כבר מורכב משתי כרומטידות אחיות, ולכן בשלב הזה יש מצב של 4n מבחינת כמות DNA. לאחר מכן, באנאפזה I, מתבצעת הפרדה של הכרומוזומים ההומולוגיים - זו חלוקת ההפחתה.
בסוף מיוזה I מתקבלים שני תאים. בכל אחד מהם נמצא כרומוזום אחד מכל זוג כרומוזומים הומולוגיים - כלומר, הזוגות ההומולוגיים כבר הופרדו. עם זאת, כל כרומוזום עדיין מורכב משתי כרומטידות אחיות מחוברות (ההפרדה של הכרומטידות מתרשת רק במיוזה II, להלן).
מיוזה II
במיוזה II מתרחש תהליך דומה מבחינה מבנית: הכרומוזומים נדחסים, מסתדרים במרכז התא, ואז מתבצעת הפרדה של הכרומטידות האחיות. בסוף התהליך מתקבלים ארבעה תאים שעברו חלוקת הפחתה ויכולים להתמיין לגמטות.
בזכרים, מכל Germ cell מתקבלים ארבעה תאי זרע; התהליך מתרחש בבגרות המינית.
מיוזה בנקבות
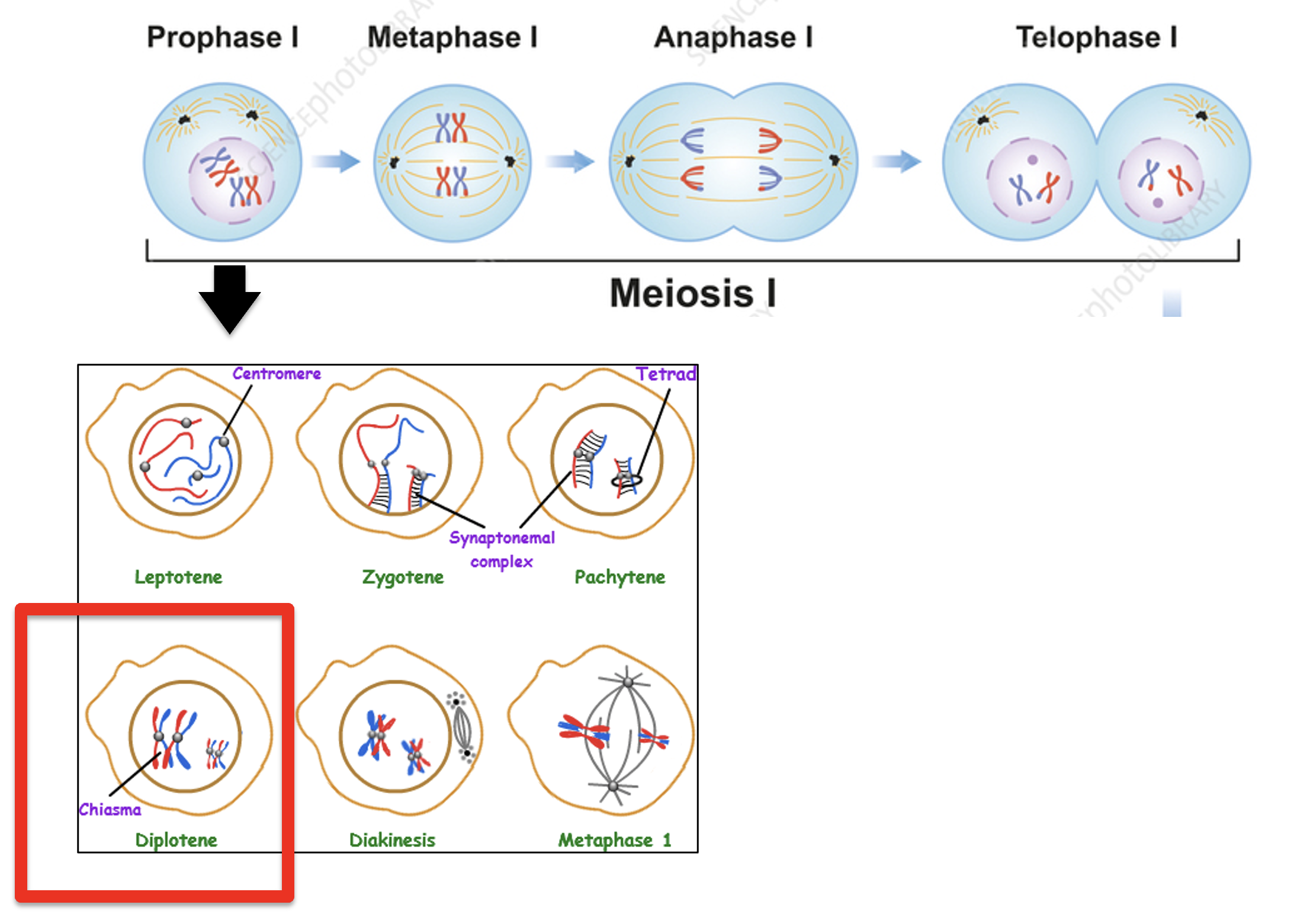
בנקבות התהליך מורכב יותר. ה־PGCs נודדים עד שנוצרות השחלות, נכנסים אליהן, ולפני הלידה עוברים פרוליפרציה מיטוטית משמעותית. חלק גדול מהתאים עובר מוות תאי, ונשארת אוכלוסייה של תאי מין.
לאחר מכן התאים נכנסים לחלוקה המיוטית הראשונה, כלומר מתחילים התמיינות לכיוון ביציות. כאשר אומרים שנקבות נולדות עם כל הביציות שלהן, הכוונה היא שהתאים האלה נכנסו לפרופאזה I ונעצרו שם.
במהלך פרופאזה I מתרחש כאמור זיווג של כרומוזומים הומולוגיים, נוצר Synaptonemal complex, מתרחש Crossing over ונוצרות Chiasmata. העצירה בנקבות מתרחשת בשלב ה־Diplotene, ממש לפני לידת העוברית (עוברית - מלשון עובר נקבה).
Primary Oocyte, Zona Pellucida ו־GVBD
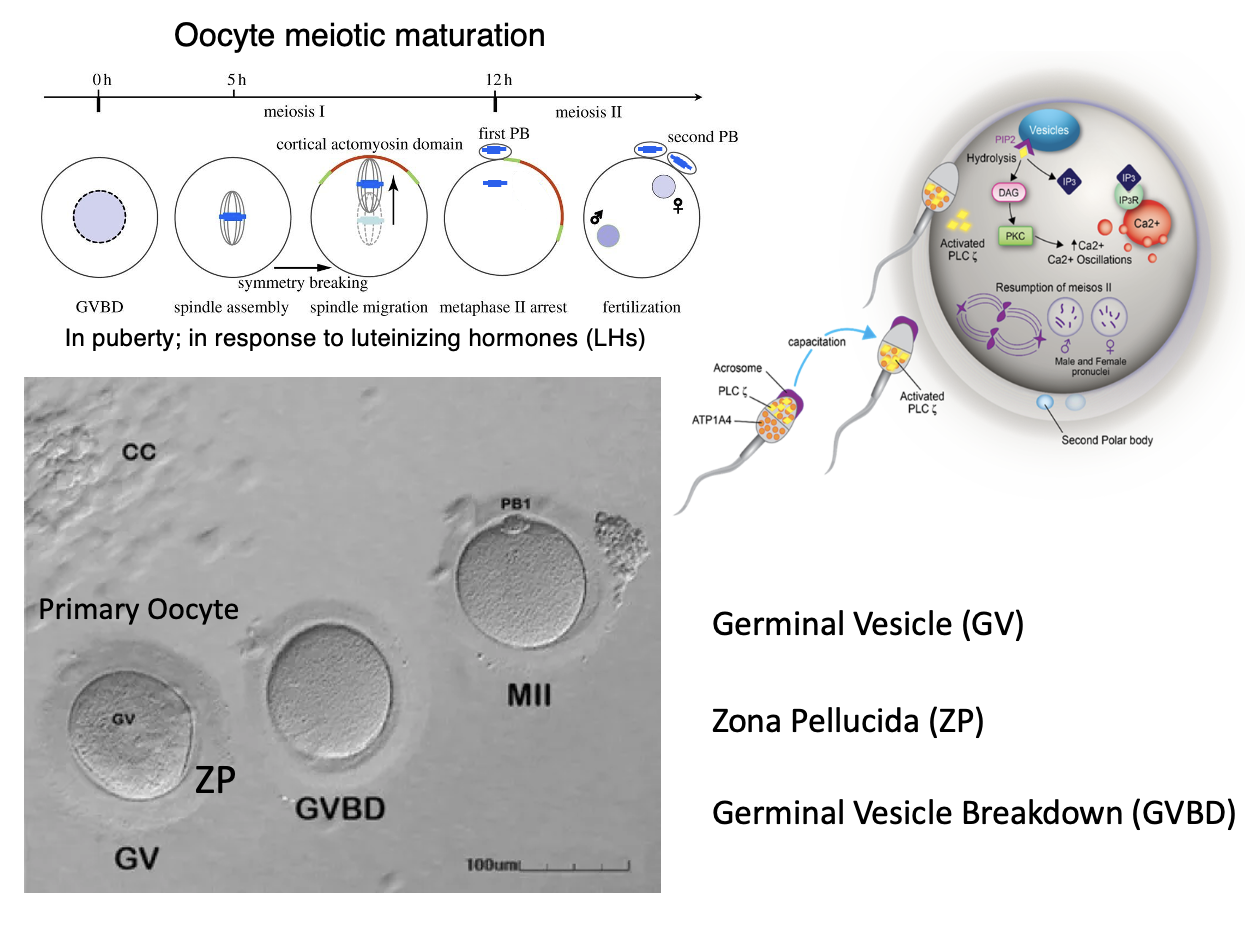
Oocyte היא ביצית. בביצית ראשונית (Primary Oocyte) רואים תא גדול ובמרכזו גרעין, שנקרא בהקשר הזה Germinal Vesicle (GV).
מסביב ל־Oocyte נמצאת Zona Pellucida (ZP), היא מורכבת משלושה חלבונים: ZP1, ZP2 ו־ZP3, ויוצרת מעטפת קשיחה סביב הביצית. ה־Zona Pellucida חיונית להפריה, בין היתר משום שתא הזרע מזהה אותה.
השלב הבא הוא GVBD - Germinal Vesicle Breakdown (פירוק הגרעין), שמאפשר לביצית להמשיך בתהליך המיוזה, לייצר כישור ולהתקדם לכיוון מטאפזה.
Oocyte Meiotic Maturation
בבגרות המינית, בהשפעת Luteinizing Hormone (LH), הביצית הראשונית יוצאת מהעצירה וממשיכה במיוזה. בתהליך הזה מתרחש אירוע ייחודי לביציות: שבירת סימטריה תאית (Symmetry Breaking); הכישור נע אל פריפריית התא, קרוב לממברנה, ולכן החלוקה אינה סימטרית.
לאחר החלוקה המיוטית הראשונה מתקבלים שני תאים לא שווים:
- תא גדול שנשאר הביצית
- First Polar Body, שמכיל סט כרומוזומים קטן ונעלם בהמשך
הסט שנשאר בביצית נותר צמוד לממברנה, נוצר שוב כישור, והביצית נעצרת במטאפזה II. מי שמוציא אותה מהעצירה השנייה הוא תא הזרע; לאחר כניסתו מתרחשת השלמת החלוקה, נוצר Second Polar Body, והכרומוזומים של הביצית ושל תא הזרע מתארגנים בגרעינים. לאחר איחוי (fusion) של שני הגרעינים מתקבלת הזיגוטה.
בסך הכול יש שתי עצירות במיוזה הנקבית (ביציות):
- עצירה לפני הלידה, בפרופאזה I.
- עצירה בזמן הביוץ, במטאפזה II.
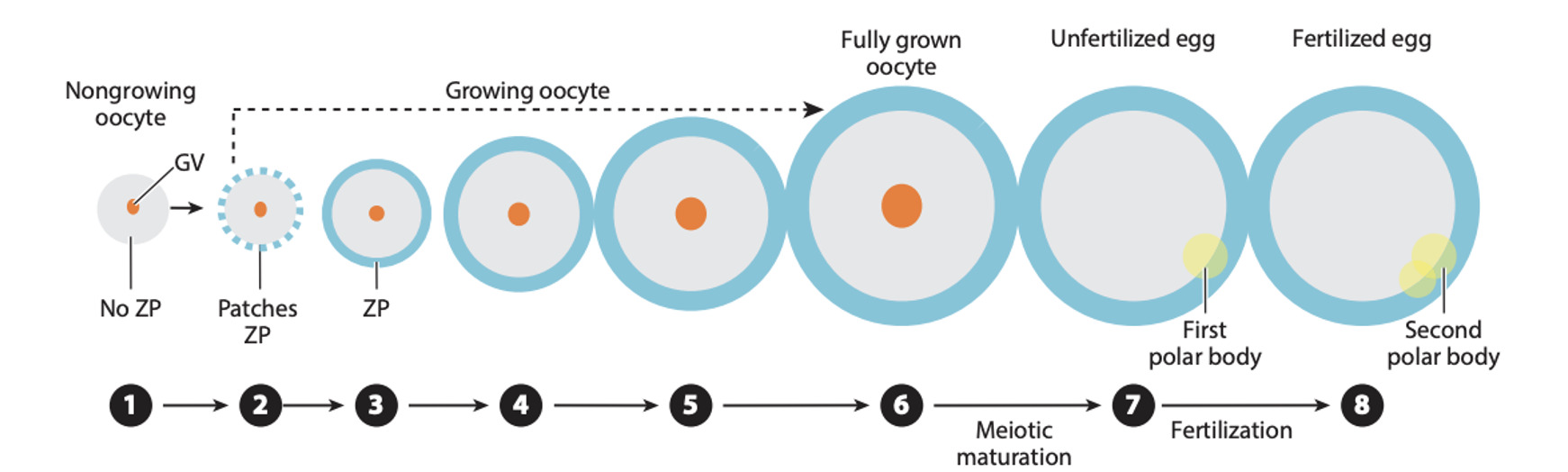
במהלך התפתחות ה־Oocyte, הביצית גדלה וצוברת כמויות גדולות של RNA. ה־RNA חשוב להמשך, משום שבתחילת ההתפתחות העוברית הגנום של העובר עדיין לא פעיל.
מההפריה ועד אחרי שלב שני התאים, העובר תלוי ב־RNA אימהי שהביצית הביאה; רק אחרי שלב שני התאים מתחילה אקטיבציה של הגנום העוברי ומתחיל שעתוק עוברי.
Cleavage והיווצרות הבלסטוציסט
ה־Zona Pellucida היא מעטפת קשיחה ולא מתיחה. לכן כל החלוקות הראשונות מתרחשות בתוך אותו נפח מוגבל, והתאים נעשים קטנים יותר ויותר.
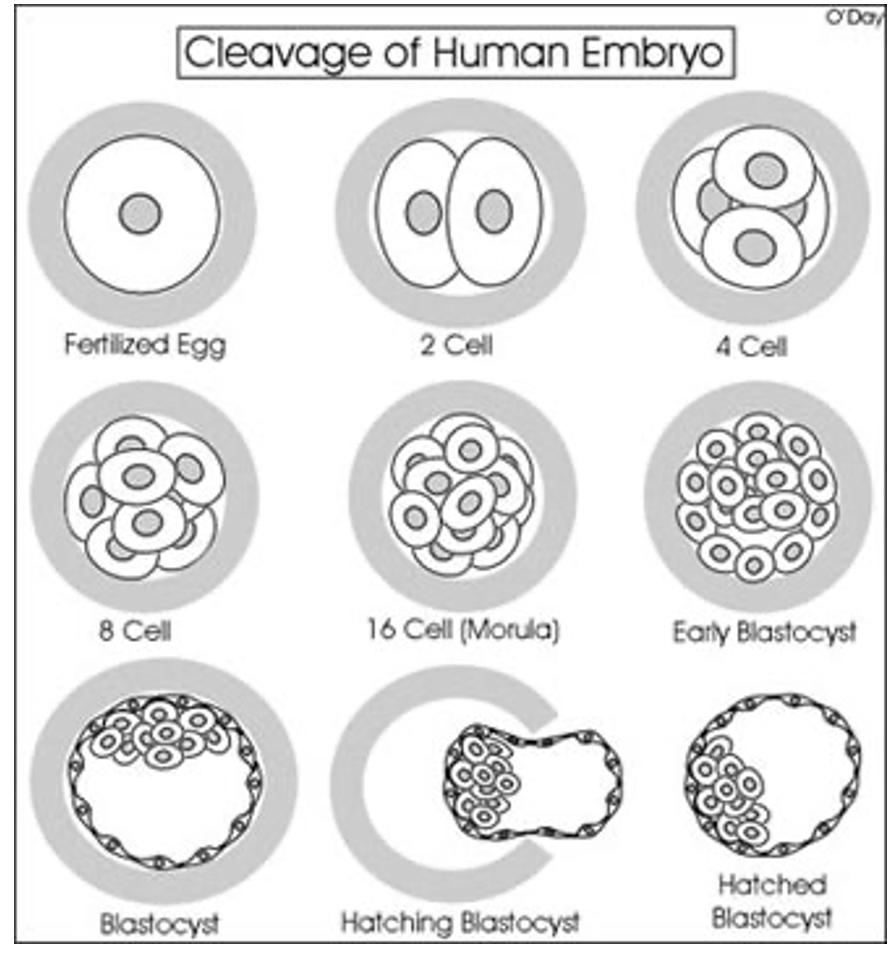
הסדר הכללי:
- זיגוטה - תא אחד
- חלוקה ראשונה לשני תאים
- חלוקה לארבעה תאים
- חלוקה לשמונה תאים
- מעבר ל־16 תאים - שלב המורולה (Morula)
- התחלת Cavitation - מעבר לבלסטוציסט מוקדם (Early Blastocyst)
- בלסטוציסט מתקדם יותר, שבו מבחינים ב־ICM וב־Trophectoderm
כל תא בשלבים הראשונים נקרא בלסטומר (Blastomere).
First Cell Fate Decision
שלב המורולה קשור ל־First cell fate decision. עד לשלב שמונת התאים, כל בלסטומר רואה סביבה דומה: מצד אחד Zona Pellucida ומשאר הצדדים בלסטומרים נוספים.
במורולה נוצרת הבחנה בין:
| אוכלוסייה | מה הם רואים? | כיוון התפתחותי בהמשך |
|---|---|---|
| תאים חיצוניים Outer cells | Zona Pellucida ובלסטומרים | Trophoblast / Trophectoderm |
| תאים פנימיים Inner cells | בלסטומרים בלבד | Inner cell mass (ICM) |
זו נקודה מרכזית משום שממנה מתחילה לראשונה הבחנה בין תאים שנמצאים בחוץ לבין תאים שנמצאים בפנים.
Cavitation ובלסטוציסט
בשלב מסוים מתחיל להיווצר בתוך העובר חלל. התהליך נקרא Cavitation, והחלל נקרא Blastocoel. ברגע שמופיע חלל ראשוני, העובר נקרא בלסטוציסט מוקדם.
בהמשך, ה־Blastocoel גדל ונוצר בלסטוציסט שבו ניתן להבחין בשתי אוכלוסיות:
- Trophoblast cells / Trophectoderm - תאי המעטפת; יוצרים רקמות חוץ־עובריות כמו שליה ועוד.
- Inner cell mass (ICM) - קבוצת תאים פנימית בצד אחד של הבלסטוציסט. ממנה מתפתח העובר עצמו.
יצירת הבלסטוציסט היא נקודה בלתי הפיכה מבחינה התפתחותית. בהמשך, הבלסטוציסט צריך לצאת מה־Zona Pellucida; הדבר נעשה באמצעות הפרשת פרוטאזות באזור מסוים, פירוק של ה־Zona Pellucida ויציאה החוצה. לאחר מכן הבלסטוציסט יכול לעבור השרשה ברחם.
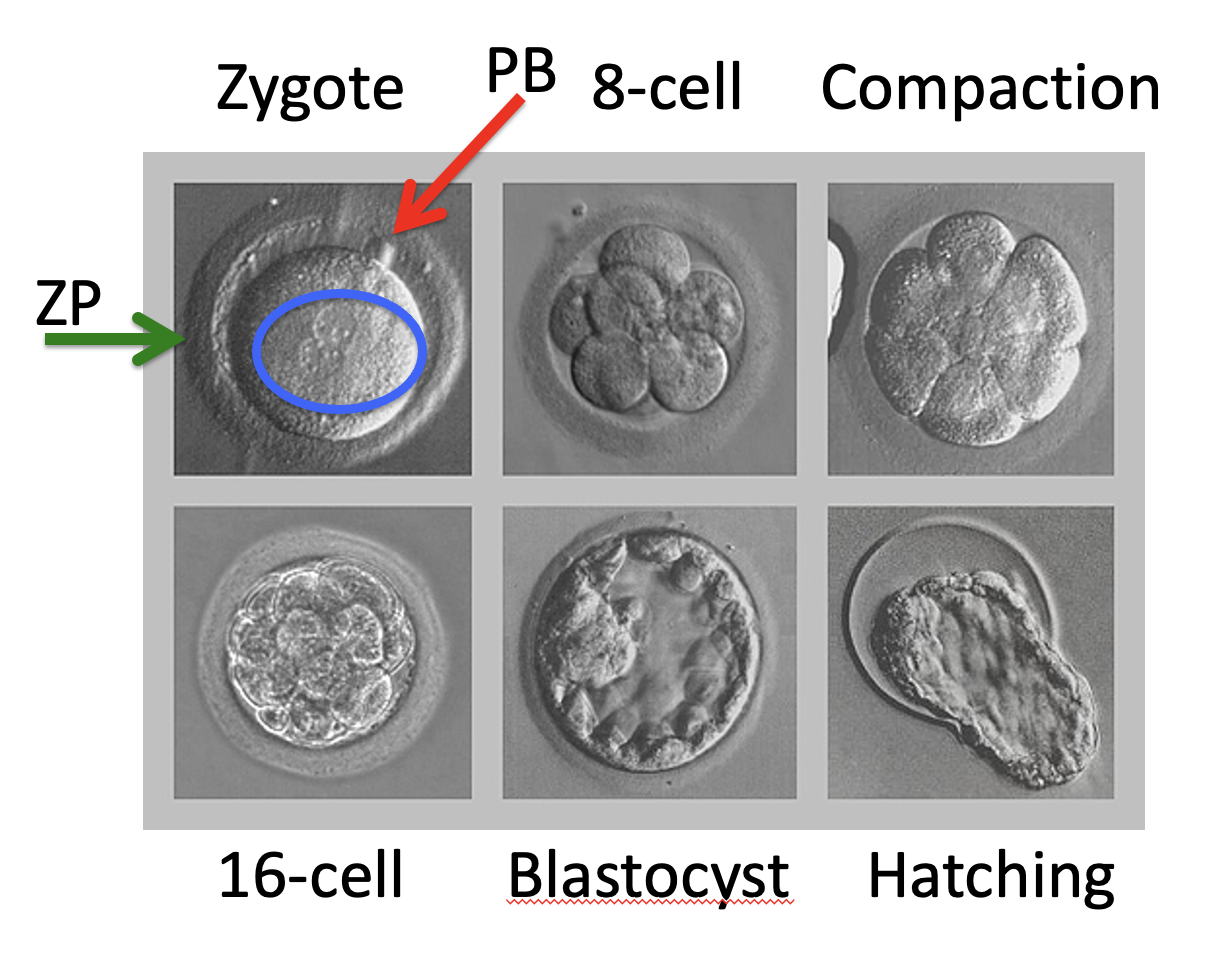
Compaction
Compaction הוא שלב שבו התאים עוברים דחיסה. מספר התאים לא בהכרח משתנה, אבל המורפולוגיה שלהם כן. זה חלק מהמעבר למבנה שבו מתחילים להבחין בין תאים חיצוניים לתאים פנימיים.
Totipotency, פלוריפוטנטיות והתמיינות
בשלבים המוקדמים, הזיגוטה והבלסטומרים הם Totipotent: יש להם יכולת לתת את כל העובר וגם רקמות חוץ־עובריות.
מתחתם ברמת הירכיית פוטנציאל ההתפתחות נמצאת פלוריפוטנטיות (Pluripotency): יכולת לתת הרבה סוגי רקמות עובריות, אך לא את כל הרקמות החוץ־עובריות (למשל תאי ה־ICM).
הסדר היררכי של פוטנציאל ההתפתחות (מהרחב לצר):
- Totipotent
- Pluripotent
- Oligopotent
- Unipotent
- Terminal differentiation
ההבחנה שהודגשה בהמשך היא שייתכן ש־Totipotency אינה עולם נפרד לגמרי מפלוריפוטנטיים, אלא פלוריפוטנטיים בתוספת רכיבים נוספים. לפי המודל שהוצג, מעבר מ־Totipotency לפלוריפוטנטיים יכול להיתפס כאיבוד של אותם רכיבים.
תאי גזע: שימור, הרחבה ואובדן
תאי גזע (Stem Cells) חייבים להיות מסוגלים לבצע התחדשות עצמית (self-renewal - תא גזע מייצר עוד תא גזע), ולתת לפחות שושלת אחת של תאים ממוינים.
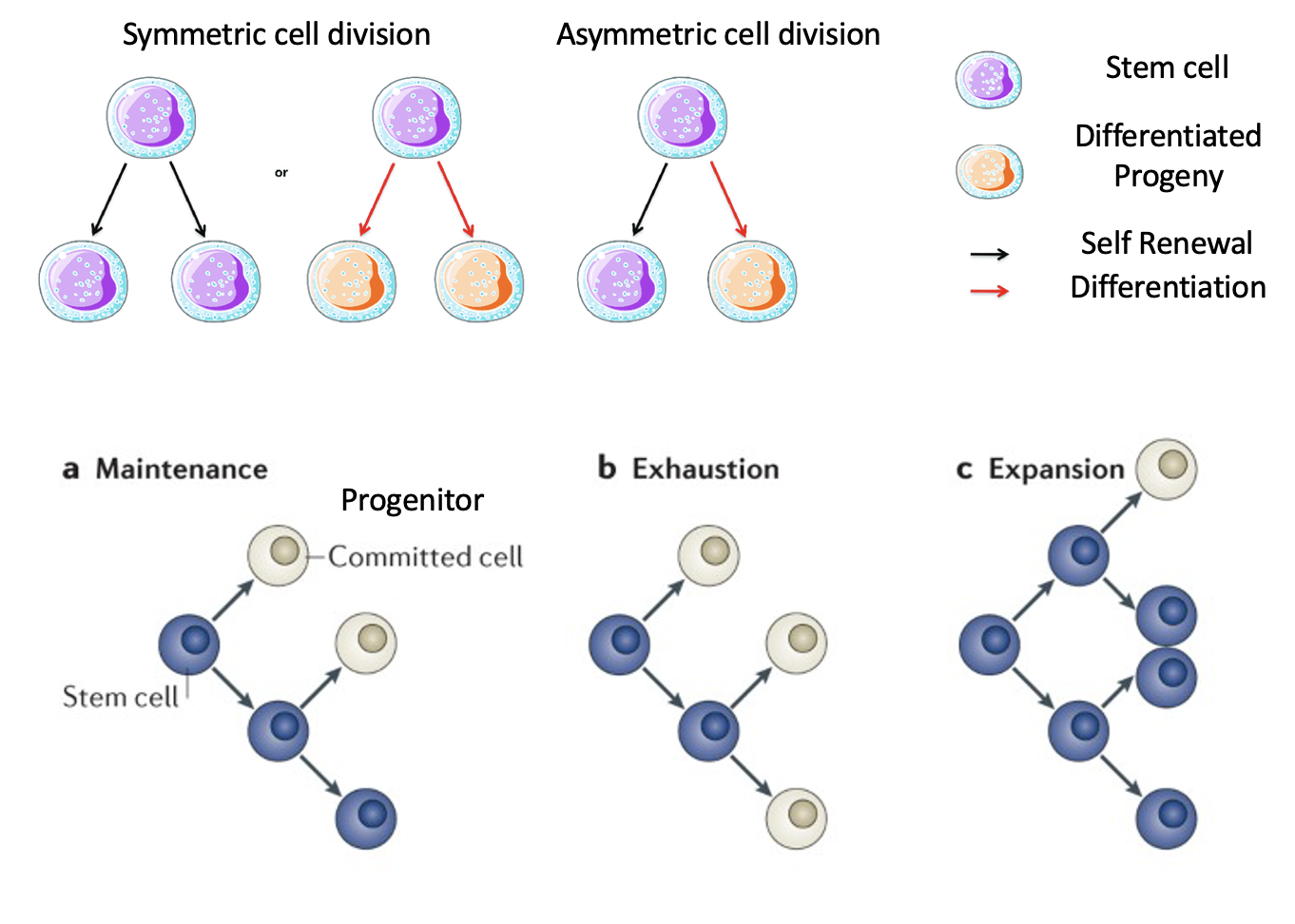
סוגי חלוקה של תאי גזע
תא גזע יכול להתחלק בכמה דרכים, והגורל של תאי הבת קובע אם אוכלוסיית תאי הגזע תישמר, תתרחב או תישחק.
חלוקה סימטרית
בחלוקה סימטרית, שני תאי הבת מקבלים גורל דומה:
- אם שני תאי הבת נשארים תאי גזע - מתרחשת התחדשות עצמית והאוכלוסייה יכולה לגדול.
- אם שני תאי הבת יוצאים ממאגר תאי הגזע ומתחילים התמיינות - יש ירידה במספר תאי הגזע.
כלומר, חלוקה סימטרית יכולה לתרום גם ל־Expansion וגם ל־Exhaustion, תלוי בזהות תאי הבת.
חלוקה א-סימטרית
בחלוקה א-סימטרית, תא הגזע מתחלק לשני תאים בעלי גורל שונה:
- תא בת אחד נשאר תא גזע.
- תא בת אחד מתחיל תהליך התמיינות או commitment לשושלת מסוימת.
בדרך זו נשמר מאגר תאי הגזע, ובמקביל נוצרים תאים שממשיכים להתמיין.
Maintenance
ב־Maintenance, אוכלוסיית תאי הגזע נשמרת; מתחילים עם מספר מסוים של תאי גזע ומסיימים עם מספר דומה, אף שבמהלך הדרך תאים התחלקו וחלק נתנו תאים committed שימשיכו להתמיינות.
מצב כזה יכול להתרחש למשל דרך חלוקות א-סימטריות, שבהן בכל חלוקה נשמר תא גזע אחד ונוצר תא נוסף שממשיך להתמיין.
Expansion
ב־Expansion, המטרה היא להגדיל את אוכלוסיית תאי הגזע. תא גזע עובר התחדשות עצמית ונותן שני תאי גזע, וכך האוכלוסייה גדלה. בהמשך חלק מהתאים יכולים להתחיל התמיינות.
מצב כזה מתאים בעיקר לחלוקות סימטריות שבהן שני תאי הבת נשארים תאי גזע.
אובדן תאי גזע (Exhaustion)
תאי גזע לא בהכרח ״חיים לנצח״; בהקשרים מסוימים אוכלוסיית תאי הגזע יכולה להיעלם, למשל אם חלוקות מובילות לכך שהתאים מפסיקים להיות תאי גזע והופכים לתאים ממוינים (committed).
מצב כזה יכול להתרחש כאשר יותר מדי חלוקות מובילות ליציאה ממאגר תאי הגזע, למשל בחלוקה סימטרית שבה שני תאי הבת מתחילים התמיינות במקום להישאר תאי גזע.
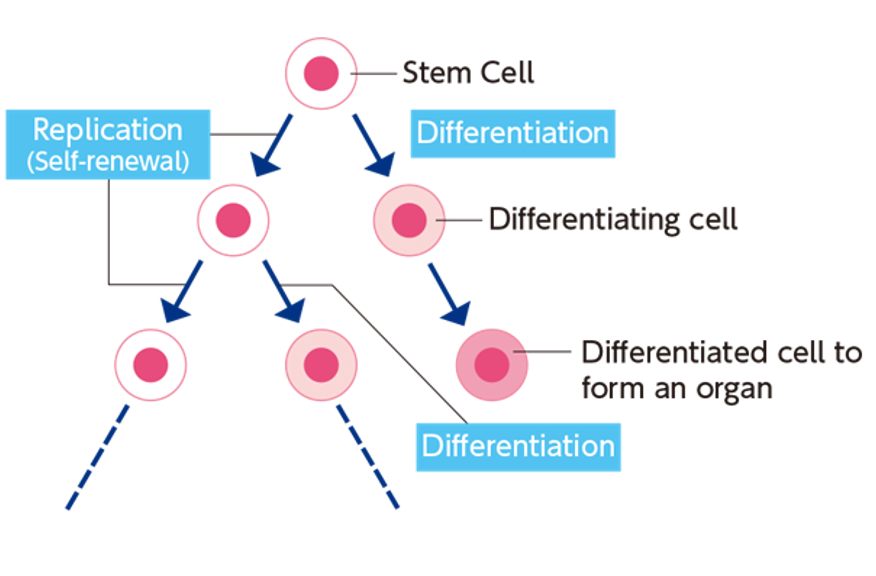
תאי גזע עובריים
Embryonic stem (ES) cells הם תאים שמקורם ב־ICM של הבלסטוציסט. באופן מלאכותי, אפשר לקחת בלסטוציסט, לפתוח אותו, להוציא את ה־ICM ולגדל את התאים בתרבית, בתנאים שמאפשרים להם להישמר וליצור מושבות.
לתאים האלה יש תכונות של פלוריפוטנטיות, משום שמקורם ב־ICM, שנותן את תאי העובר.
איך מוכיחים פלוריפוטנטיות?
השיטה האמפירית עושה שימוש בחלבון פלואורסצנטי ירוק (Green Fluorescent Protein - GFP): מכניסים לתאי גזע עובריים יכולת לבטא GFP, כך שיזהרו בירוק. לאחר מכן מזריקים אותם לתוך ה־Blastocoel של בלסטוציסט אחר.
חלק מהתאים ימותו וחלק יעברו Incorporation אל תוך ה־ICM. אם הם אכן משתלבים ב־ICM, הם יכולים לתרום לרקמות שונות בעובר. לאחר החזרת הבלסטוציסט לנקבה והתפתחות העובר, מתקבל עובר כימרי.
כימרה בהקשר הזה היא עובר שמורכב משתי אוכלוסיות תאים בעלות מקור גנטי שונה. אם רואים תאים זוהרים ברקמות שונות של העובר, זו הוכחה לכך שתאי הגזע העובריים (ES cells) התפתחו לסוגי תאים שונים בעובר ולכן הם פלוריפוטנטיים.
עם זאת, תאי גזע עובריים לבדם אינם יוצרים בלסטוציסט. צריך להזריק אותם לתוך בלסטוציסט קיים כדי שיוכלו להשתלב ב־ICM.
First and Second Cell Fate Decision
First Cell Fate Decision - תאים פנימיים וחיצוניים
כאמור, ה־First cell fate decision הוא המעבר שבו מבחינים בין תאים פנימיים לחיצוניים; הפנימיים יובילו ל־ICM, והחיצוניים ל־Trophectoderm.
Second Cell Fate Decision - אפיבלסט ופרימיטיב אנדודרם
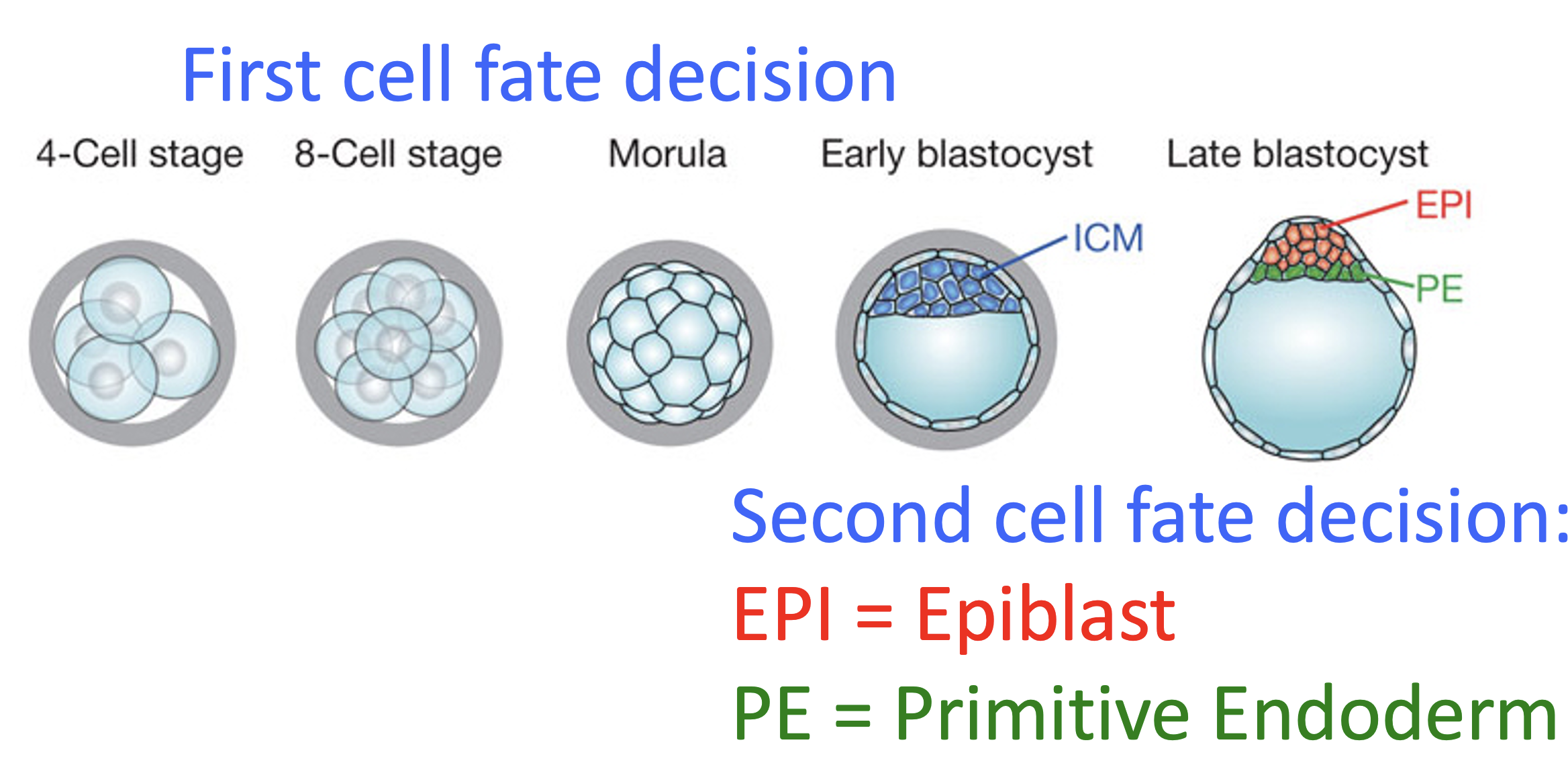
לאחר יצירת ה־ICM מתרחש אירוע נוסף: Second cell fate decision. ה־ICM עצמו עובר התמיינות לשני סוגי תאים:
| אוכלוסייה | מיקום/מאפיין | גורל |
|---|---|---|
| אפיבלסט Epiblast (EPI) | תאים שלא צמודים ל־Blastocoel | נותנים את העובר |
| אנדודרם פרימיטיבי Primitive Endoderm (PE) | תאים צמודים ל־Blastocoel | נותנים רקמות חוץ־עובריות נוספות (מעבר לאלו שמקורן ב־Trophectoderm) |
תשומת הלב שעדיין אין כאן Germ Layers; זה לא שלב הגסטרולציה.
התפתחות בלסטוציסט יכולה להתרחש בתנאי מעבדה (In vitro); בתוך צלחת, ללא רחם וללא השרשה. יש לכך חשיבות ניסויית כי הדבר מאפשר לעקוב אחר ההתפתחות תחת מיקרוסקופ.
הציר Embryonic / Abembryonic
בבלסטוציסט מופיע לראשונה ציר מרחבי: בצד אחד נמצא ה־ICM, שיתפתח לעובר, ובצד השני אזור ללא ICM. זהו ציר Embryonic-Abembryonic.
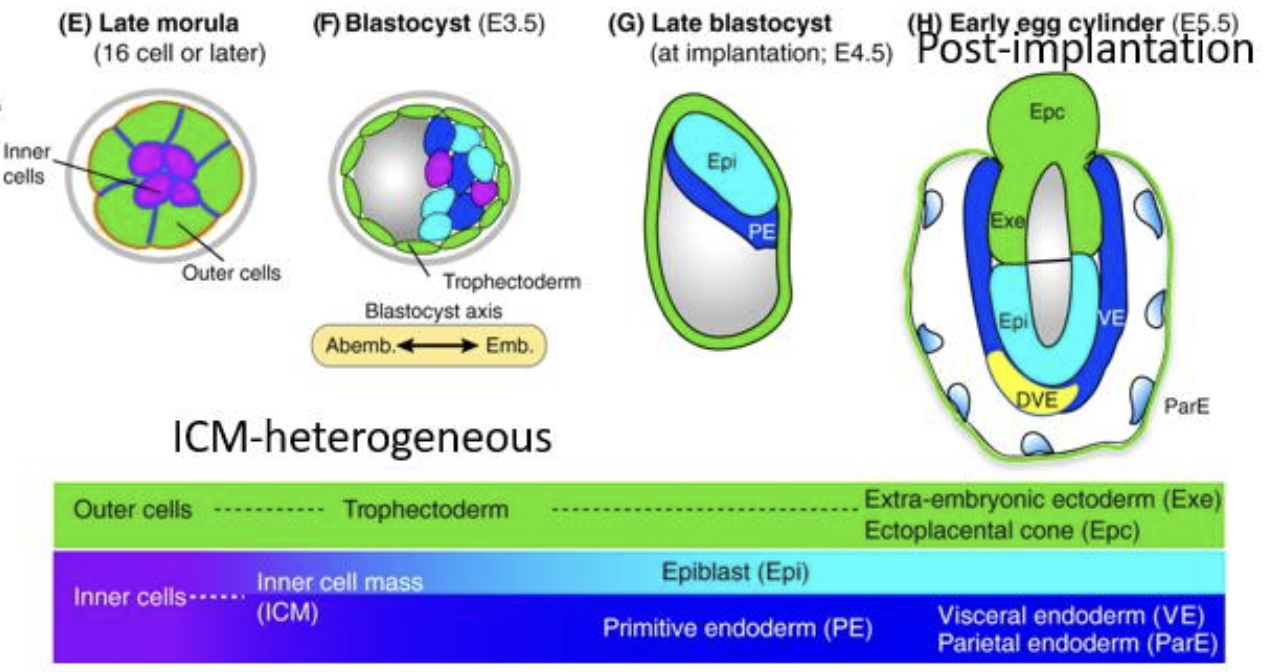
שינויים לאחר השרשה
סביב ההשרשה, המבנה המרחבי משתנה. הרקמות שתוארו קודם לכן ממשיכות להתקיים, אבל הן מסודרות אחרת:
- האפיבלסט, שהיה כדור תאים, מקבל צורה דמויית גביע.
- תאי Trophectoderm (בתמונה בצבע ירוק) מתחלקים מאוד ויוצרים Extraembryonic ectoderm (Exe).
- למעלה נמצא Ectoplacental cone (Epc), שיתפתח לשליה.
- האנדודרם הפרימיטיבי (בתמונה בצבע כחול) מקיף את האפיבלסט ואת ה־Extraembryonic Ectoderm.
האנדודרם הפרימיטיבי נותן שתי אוכלוסיות:
| אוכלוסייה | מאפיין |
|---|---|
| אנדודרם ויסרלי Visceral Endoderm (VE) | נשאר ומקיף את האפיבלסט ואת ה־Extraembryonic Ectoderm |
| אנדודרם פריאטלי Parietal Endoderm (ParE) | תאים שעזבו, נדדו והתמקמו בצד הפנימי של ה־Trophectoderm (הגושים הכחולים באיור למעלה) |
המאפיין שהודגש לגבי אנדודרם פריאטלי הוא יכולת הנדידה שלו.
ניסוי: מורולה לעומת בלסטוציסט מוקדם
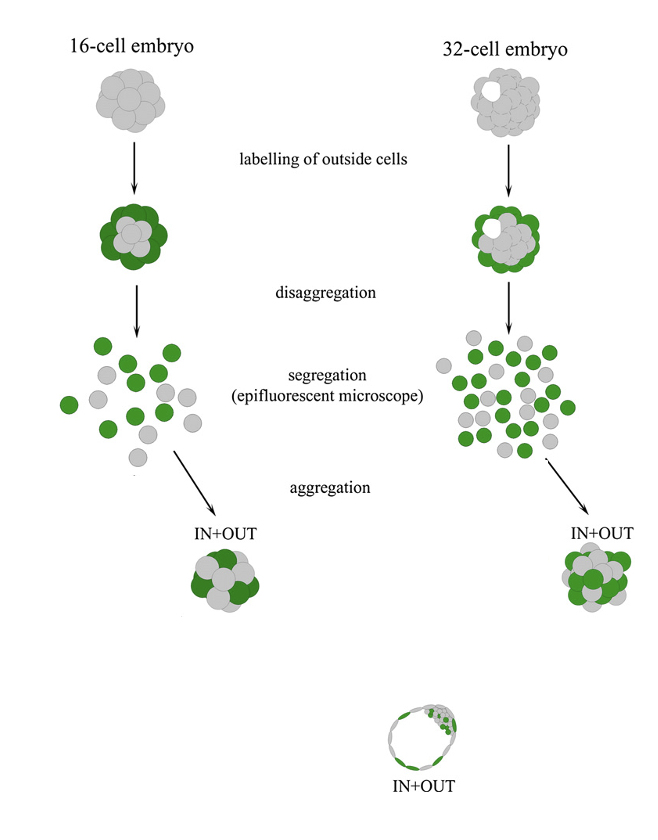
בניסוי נלקחו שני עוברים:
- עובר של 16 תאים - מורולה.
- עובר של 32 תאים - בלסטוציסט מוקדם (Early Blastocyst), משום שכבר יש התחלה של Cavitation ושל Blastocoel.
שני העוברים הוכנסו לצבען פלואורסצנטי ירוק שנקשר לממברנות. רק התאים החיצוניים נצבעו, כי רק הם חשופים לצבען. לאחר מכן פירקו את העוברים לתאים בודדים:
- תאים ירוקים = תאים חיצוניים
- תאים לא צבועים = תאים פנימיים
ניסוי ביקורת
כאשר לוקחים את כל התאים יחד, ירוקים ולא ירוקים, ומרכיבים אותם מחדש כאגרגט, מתקבל בלסטוציסט תקין. מכאן שהמניפולציה עצמה לא הרסה את העובר, ושבשלבים האלה התאים עדיין יכולים לתרום להתפתחות.
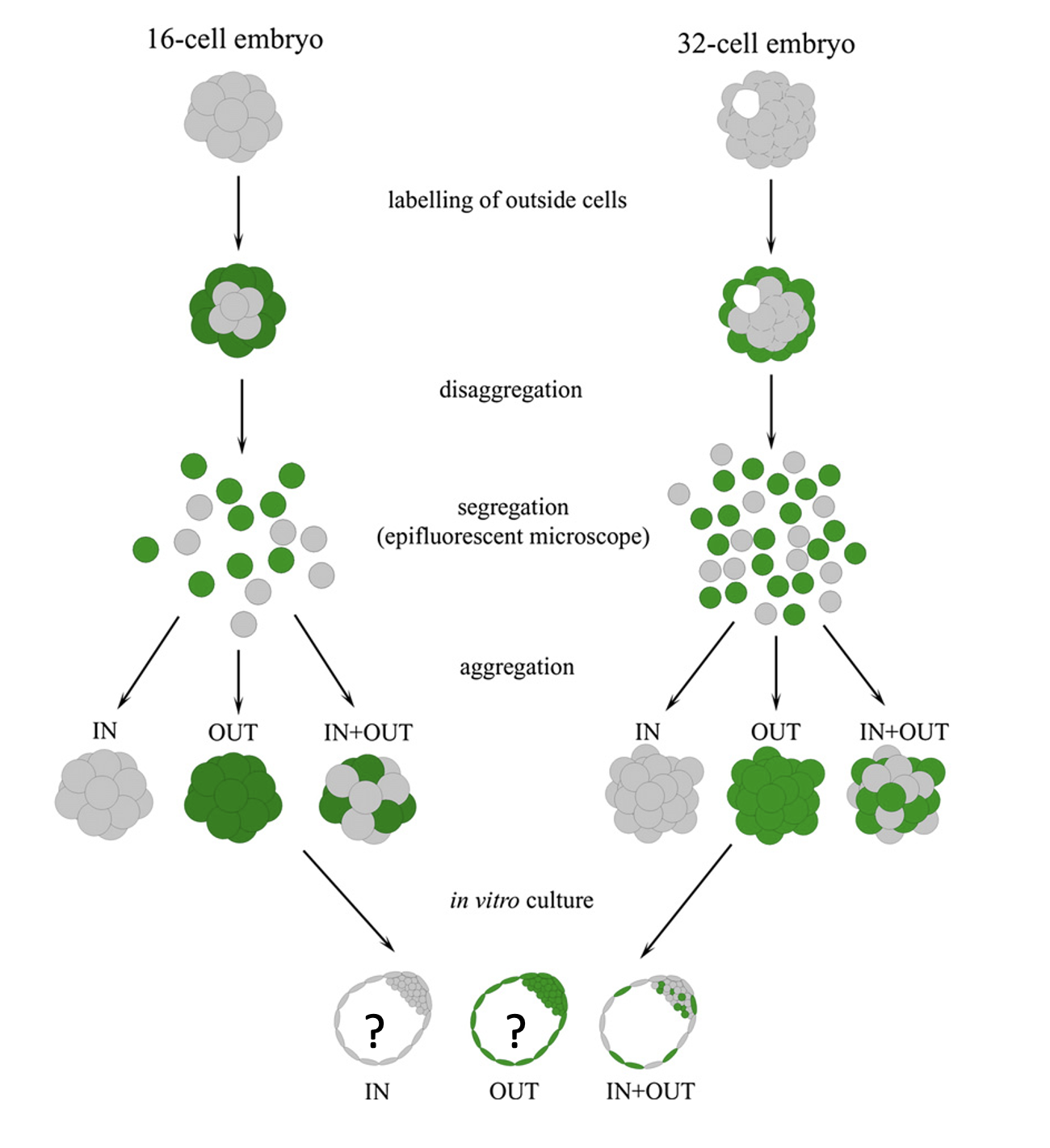
16-cell embryo
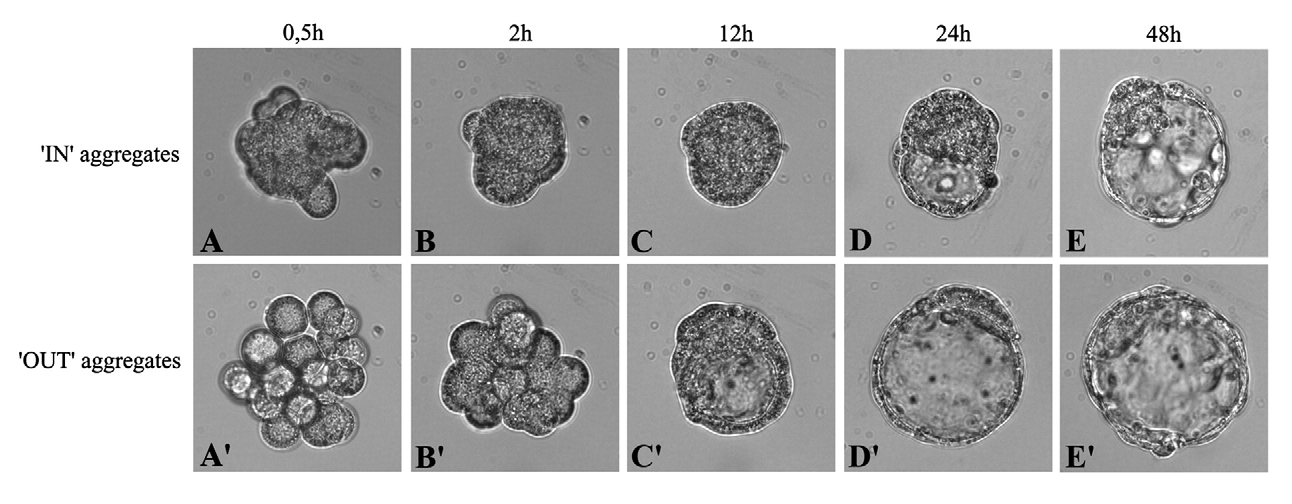
בעובר של 16 תאים, כאשר מרכיבים אגרגט רק מתאים פנימיים או רק מתאים חיצוניים, בשני המקרים מתקבל בלסטוציסט. כלומר, בשלב המורולה, גם הפנימיים וגם החיצוניים טרם התחייבו לכיוון מסוים; הם עדיין יכולים לתת ICM או Trophectoderm.
עם זאת, יש הבדל בתזמון: האגרגט של התאים החיצוניים מתקדם מהר יותר ליצירת בלסטוציסט לעומת האגרגט של הפנימיים. לפי השיעור, אין הסבר ברור להבדל בתזמון, אבל הוא מראה שהתאים אינם זהים לגמרי למרות שטרם התחייבו.
32-cell embryo
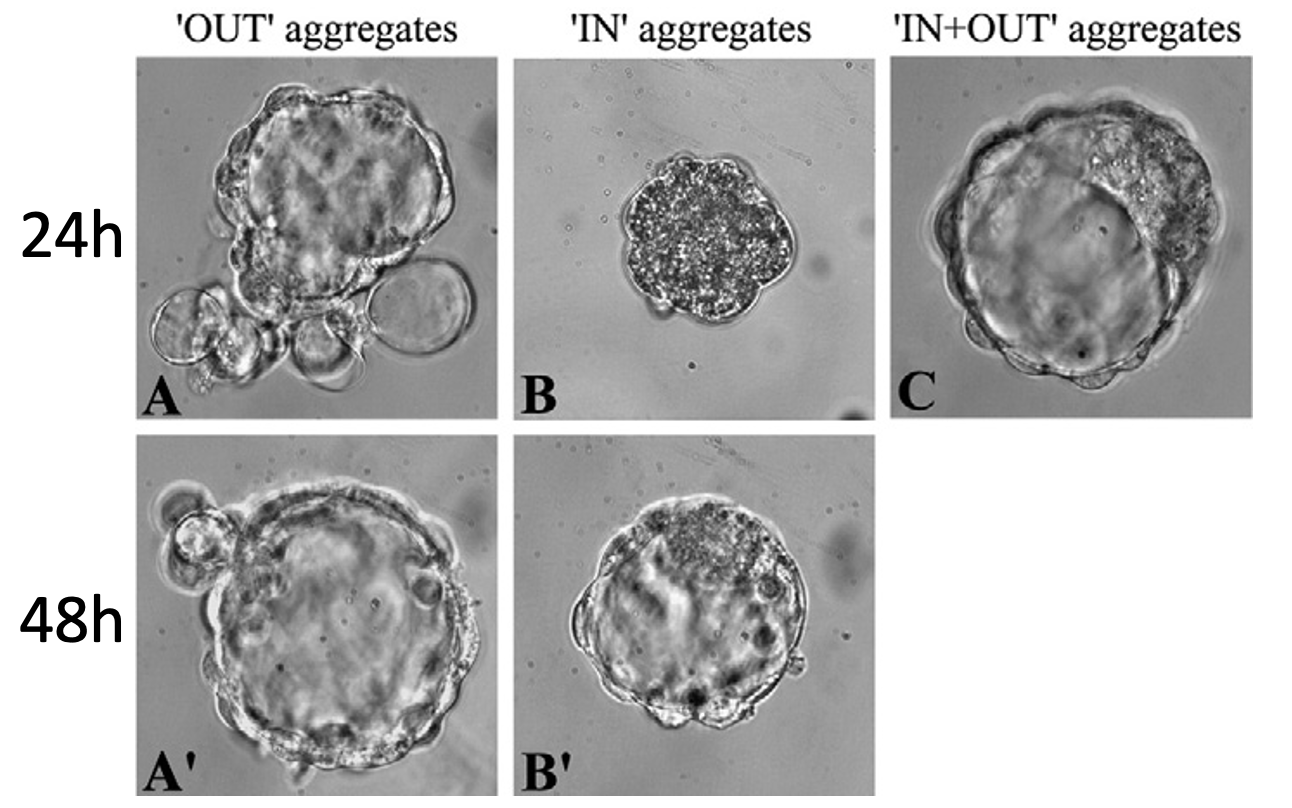
בשלב של 32 תאים, מתקבלת תמונה שונה:
- אגרגט של תאים פנימיים יכול ליצור מורולה ובהמשך בלסטוציסט עם Blastocoel, ICM ו־Trophectoderm.
- אגרגט של תאים חיצוניים יוצר מבנה עם Blastocoel ו־Trophectoderm, אבל ללא ICM.
המסקנה היא שבשלב הזה גורלם של התאים החיצוניים כבר נקבע לכיוון Trophectoderm, ולכן הם כבר לא יכולים ליצור את ה־ICM. זאת הכוונה בנקודת אל חזור - נקודת מעבר שבה הבחירה ההתפתחותית כבר בלתי הפיכה.
Cell Fate Decision ברמה המולקולרית
כדי להבין את ה־First cell fate decision ואת ה־Second cell fate decision ברמה מולקולרית, הוצגו כמה פקטורי שעתוק:
- Oct4
- Nanog
- Cdx2
- Gata4
- Gata6
פקטורי שעתוק צריכים לפעול בגרעין. לכן בצביעות אימונולוגיות שלהם מצפים לראות צביעה גרעינית.
בנוסף הוזכרה DAPI, מולקולה שנכנסת ל־DNA ומשמשת לסימון גרעינים, זורחת בכחול (ראו בתמונה למטה).
Cdx2 ו־Oct4
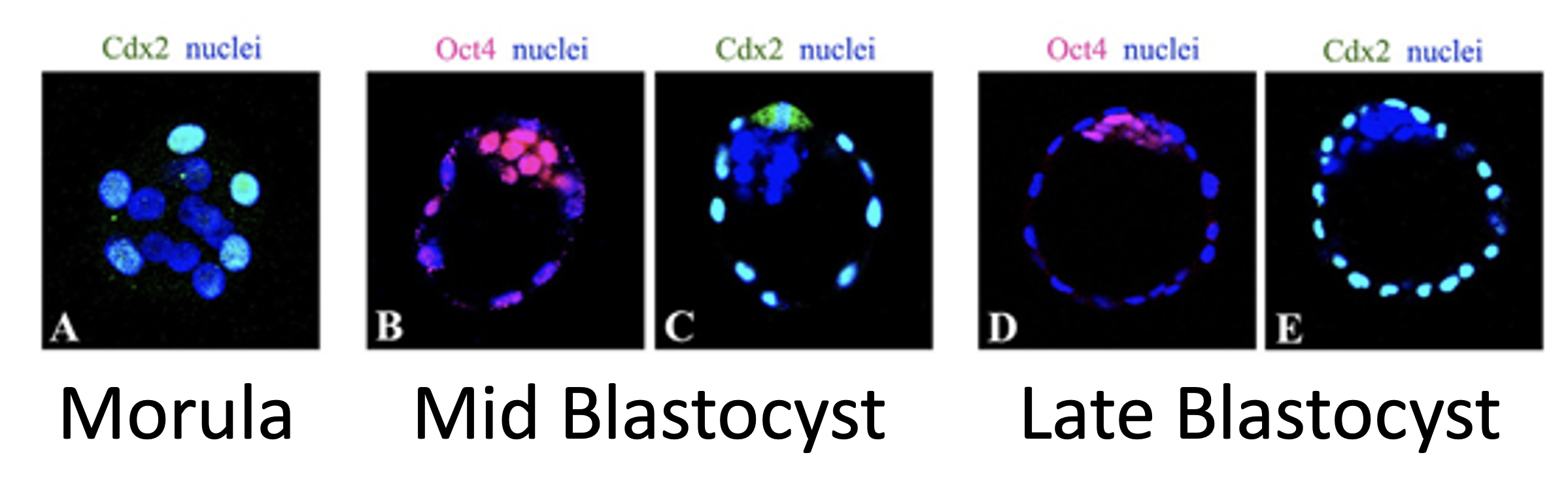
Cdx2
- בשלב המורולה
Cdx2מתבטא בתאים החיצוניים בלבד. - בבלסטוציסט ביניים (mid blastocyst) ובבלסטוציסט מאוחר (late blastocyst),
Cdx2מתבטא ב־trophectoderm בלבד (ה־ICM נקי מצביעת Cdx2).
כלומר, Cdx2 מסמן את הכיוון של outer cells / trophectoderm.
Oct4
לפי השיעור, בשלב המורולה כל התאים היו אמורים להיצבע ל־Oct4.
-
בבלסטוציסט ביניים, ה־ICM מבטא Oct4 ברמות גבוהות, וגם ה־trophectoderm מבטא Oct4 ברמות נמוכות.
-
בבלסטוציסט מאוחר, Oct4 כבר לא מתבטא ב־trophectoderm, אלא רק ב־ICM.
כלומר, Oct4 קשור לשמירה על הזהות של ה־ICM.
Nanog, Gata4 ו־Salt and Pepper Expression
Nanog
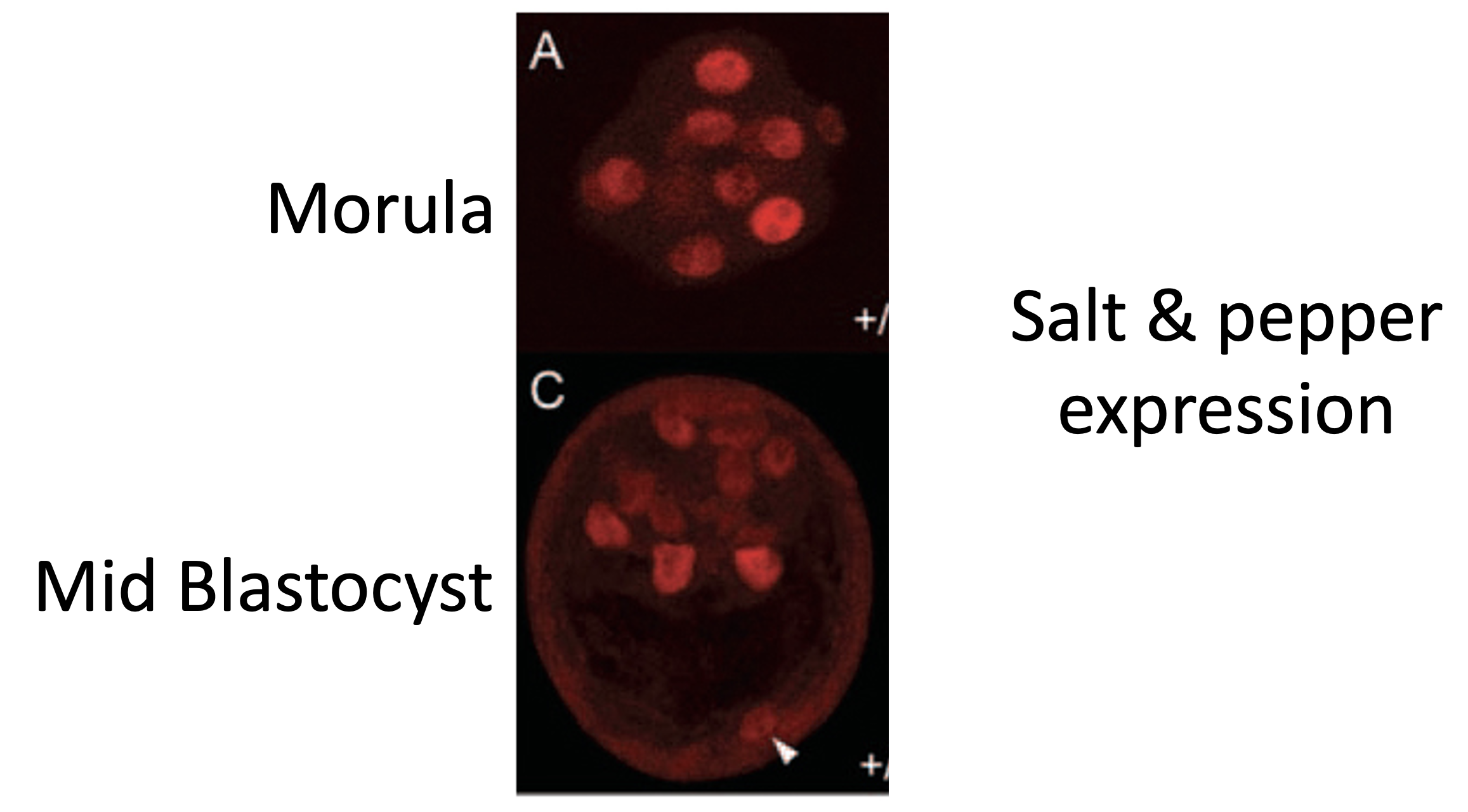
במורולה, הצביעה ל־Nanog אינה מאפשרת הבחנה ברורה בין תאים פנימיים לחיצוניים. בבלסטוציסט, רוב התאים שנצבעים נמצאים ב־ICM, אך לא כולם נצבעים באותה עוצמה: חלק חזק יותר, חלק חלש יותר וחלק לא נצבעים כלל.
לצורת הביטוי הזאת קוראים Salt and Pepper: בתוך אוכלוסיית תאים אחת יש תאים שמבטאים את הפקטור ויש כאלה שלא.
Nanog ו־Gata4
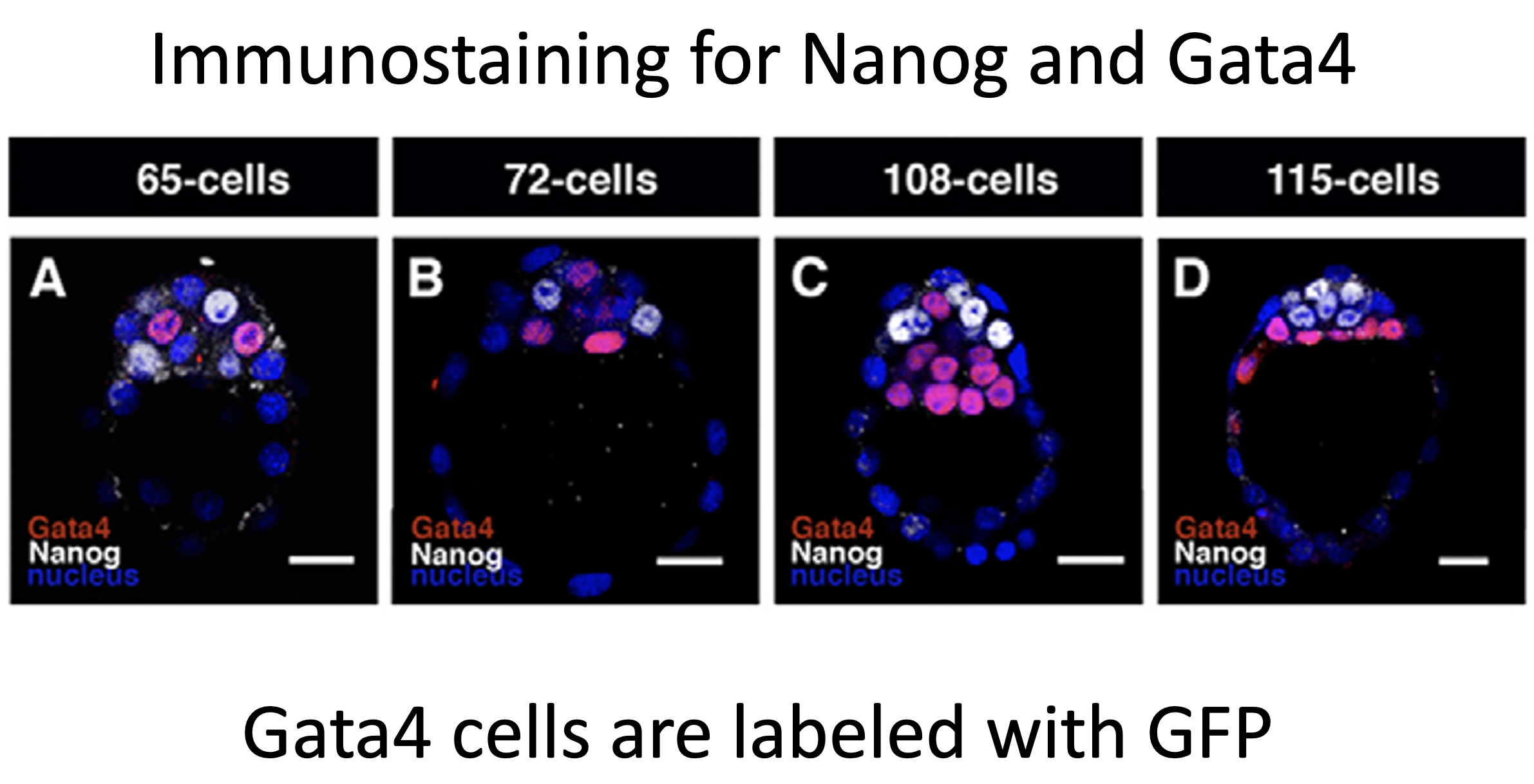
בצביעה כפולה ל־Nanog ול־Gata4 רואים ששני הפקטורים מתבטאים בעיקר ב־ICM, אבל באופן אקסקלוסיבי:
- תא שמבטא Nanog לא מבטא Gata4
- תא שמבטא Gata4 לא מבטא Nanog
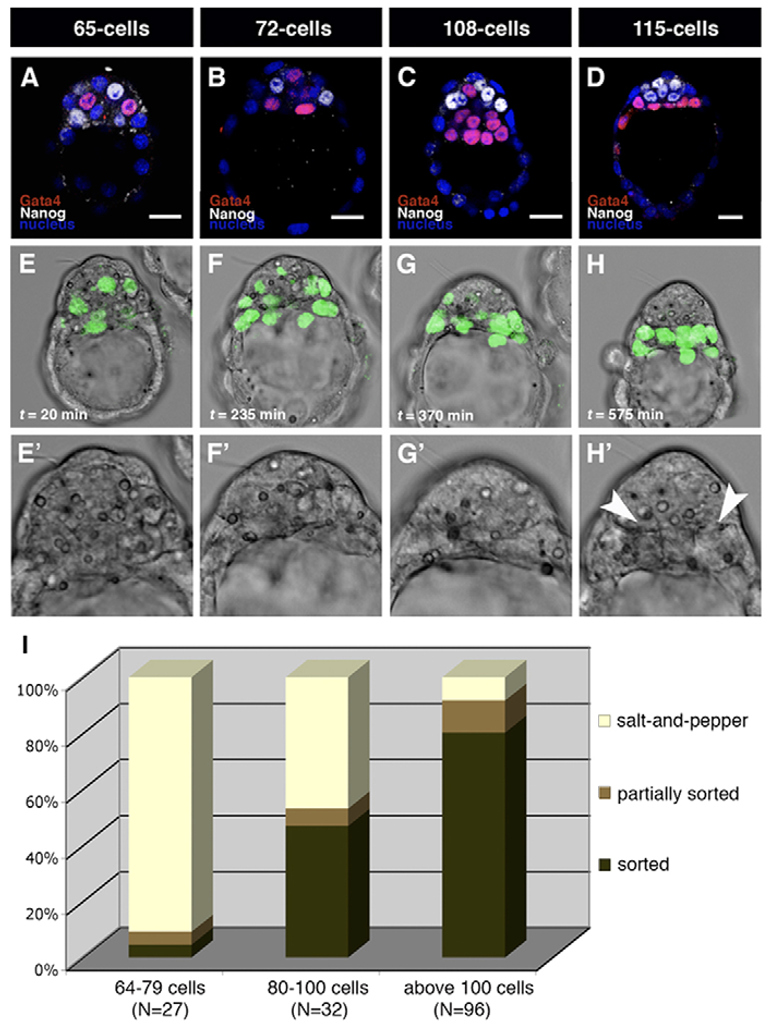
בשלבים מוקדמים יותר, למשל סביב 65 ו־72 תאים, הביטוי עדיין נראה כמו Salt and pepper. בשלב מאוחר יותר, סביב 108 תאים, תאי Gata4 נוטים להיות קרובים יותר ל־Blastocoel, ותאי Nanog פנימיים יותר. סביב 115 תאים, הסידור נעשה ברור יותר: תאי Gata4 נמצאים באזור שמתאים ל־PE, ותאי Nanog נמצאים באזור הפנימי שמתאים לאפיבלסט.
נשאלת השאלה איך עוברים מסידור salt and pepper לסידור שכבות. הוצעו שתי חלופות:
- Sorting - התאים זזים ומסתדרים במקומות המתאימים.
- Turn off - תאים שנמצאים במקום מסוים מכבים פקטור אחד ומפעילים/משמרים אחר.
כדי לבדוק איזו אפשרות נכונה משתמשים ב־Time-lapse microscopy. במקום להרוג את העובר בצביעה קבועה, מכניסים GFP ללוקוס של Gata4, כך שכל תא שמבטא Gata4 גם זוהר בירוק. במעקב חי רואים שהתאים נעים ומסתדרים, ולכן המודל הדומיננטי שהוצג הוא Sorting.
Markers
שני המרקרים שהודגשו בהקשר של PE (primitive endoderm) ותוצריו:
| Marker / אוכלוסייה | מקור | תיאור לפי השיעור |
|---|---|---|
| אנדודרם ויסרלי Visceral Endoderm (VE) | PE | אוכלוסייה שמקיפה את האפיבלסט ואת ה־extraembryonic ectoderm |
| אנדודרם פריאטלי Parietal Endoderm | PE | תאים שנודדים ומתמקמים בצד הפנימי של ה־trophectoderm |
בנוסף, K8 הוזכר כמרקר של תאי trophoblast / trophectoderm.
Loss of Function - Knockout
כדי לבדוק את תפקידם של פקטורי שעתוק משתמשים ב־knockout. בדוגמה הכללית, אם מוחקים אקסון חיוני בגן, מתקבל אלל לא פונקציונלי. בדרך כלל מתחילים מהטרוזיגוטים ומכליאים זכר ונקבה הטרוזיגוטים.
לפי גנטיקה מנדלית מצפים בערך ל:
- 25% wild type
- 50% heterozygotes
- 25% mutants
אם לא מתקבלים מוטנטים חיים, ייתכן שהגן הוא embryonic lethal. עם זאת, embryonic lethal לא בהכרח אומר שהגן ספציפי להתפתחות עוברית; ייתכן שמדובר בגן בסיסי שכל תא צריך, למשל גן חיוני למטבוליזם.
Oct4 Knockout - Loss of Function
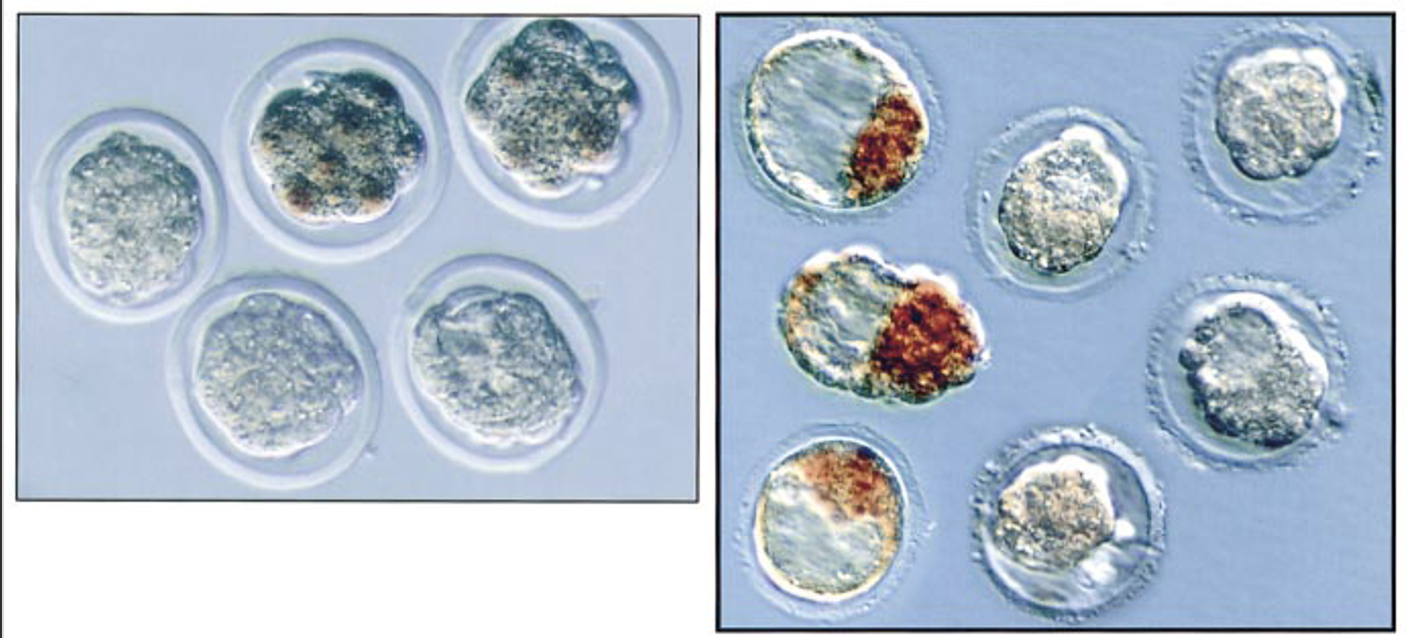
בשלב המורולה, בעוברים שחסר להם Oct4 עדיין מתקבלת מורולה. כלומר, לא צריך Oct4 כדי להגיע עד שלב המורולה.
בשלב מאוחר יותר נוצרים מבנים שנראים כמו בלסטוציסטים, אך העוברים קטנים יותר. כאשר סופרים את התאים, אין הבדל ברור במספר התאים בין wild type, הטרוזיגוט ומוטנטים, לא בתאים הפנימיים ולא בתאים החיצוניים. לכן הבעיה לא נראית כמו מוות תאי או פגם בפרוליפרציה.
Outgrowth Culture
בשלב Peri-implantation לוקחים עובר ומניחים אותו על צלחת בתנאים שמאפשרים לתאים לחיות. ב־wild type, תאי ה־Trophoblast נפרסים על הצלחת, וה־ICM נשארים מעליהם כמו גוש.
במוטנט של Oct4, לאחר פריסה רואים בעיקר Trophoblasts ולא רואים ICM תקין.
לאחר ארבעה ימים:
- ב־wild type רואים Trophoblasts, ICM ותאים של אנדודרם פריאטלי שנדדו.
- במוטנט רואים Trophoblasts בלבד.
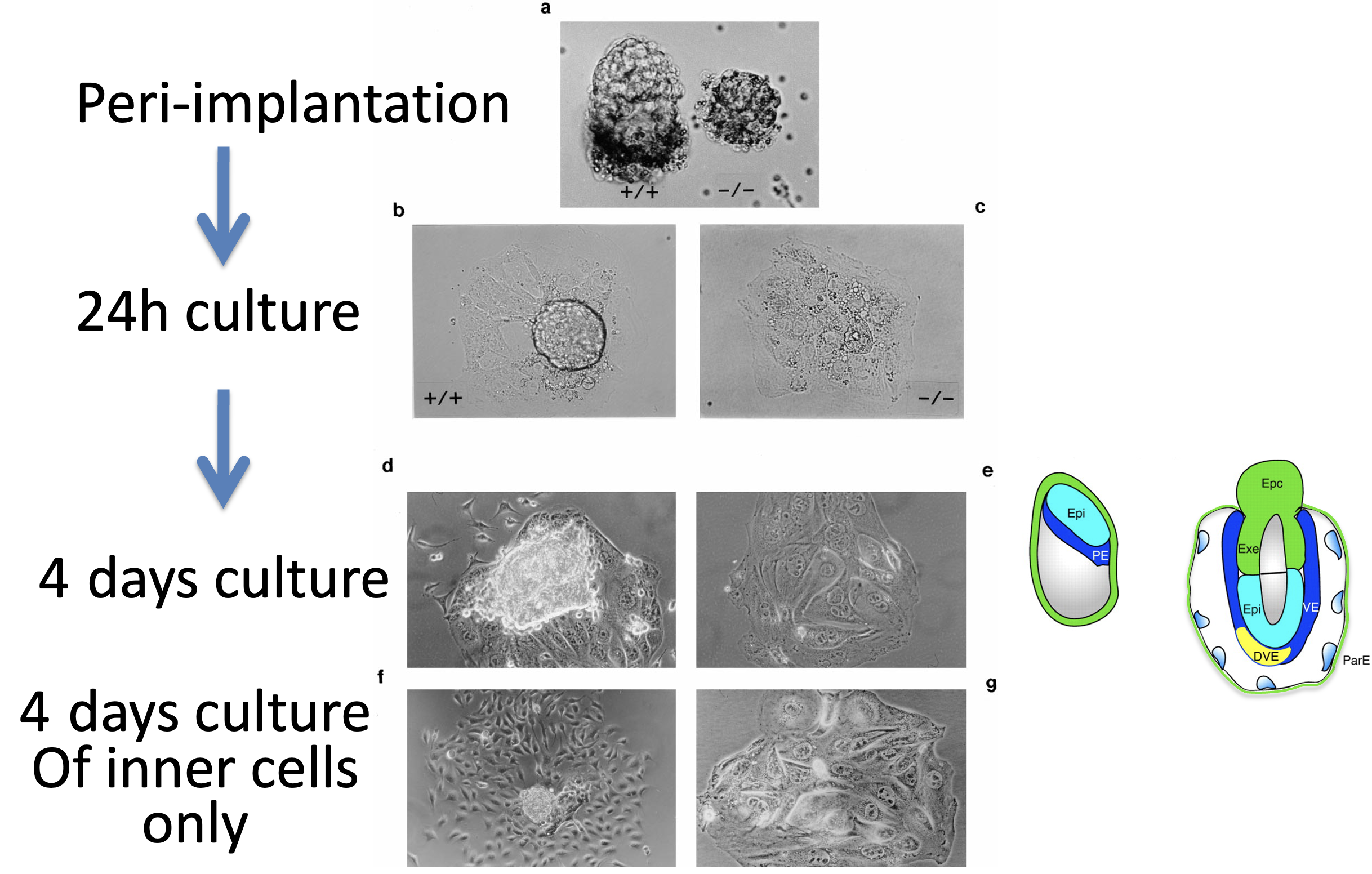
כאשר מקלפים את התאים החיצוניים ומשאירים רק את הפנימיים, ב־Wild type ה־ICM נותן אפיבלסט ו־Parietal endoderm. לעומת זאת, ב־Oct4 mutant, התאים הפנימיים מתנהגים כמו Trophoblasts.
K8 Immunostaining
K8 הוא מרקר של Trophectoderm / Trophoblast. כאשר מסירים את התאים החיצוניים וצובעים ל־K8, רואים שבמוטנט, התאים הפנימיים עצמם מבטאים מרקר של Trophoblast.
המסקנה: Oct4 דרוש כדי שתאים פנימיים יהפכו ל־ICM ולא ל־Trophoblast.
Nanog Loss of Function
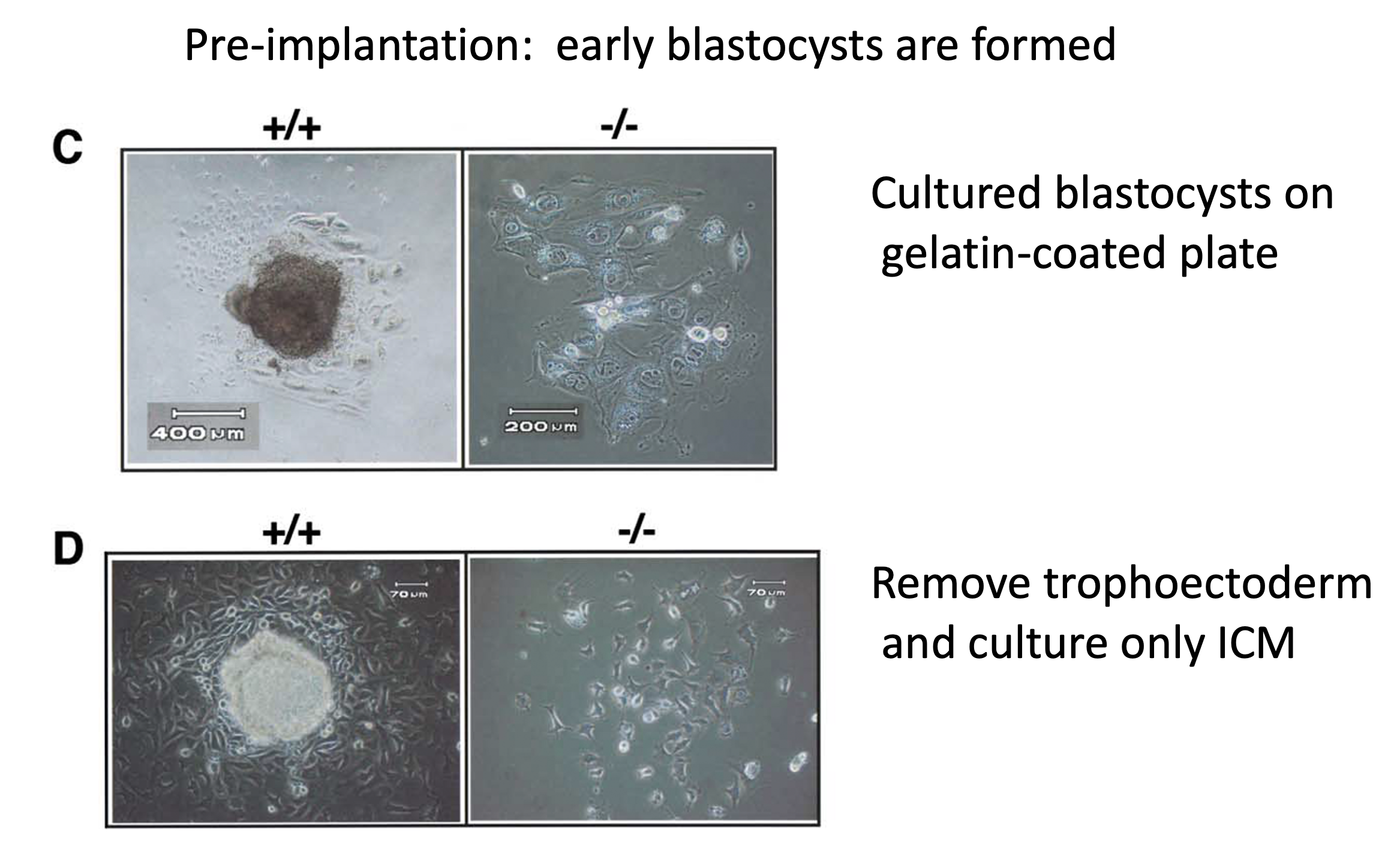
בעוברים חסרי Nanog, עד לשלב הבלסטוציסט המוקדם המראה יחסית תקין. כשמניחים אותם על צלחת, תאי trophoblast נפרסים, אך אין ICM תקין כמו ב־wild type.
למרות שהפנוטיפ של חסר ב־Nanog דומה לזה של חסר Oct4, אין להסיק ש־Oct4 ו־Nanog בעלי פונקציה זהה; אם שני גנים היו redundant לגמרי והיו עושים בדיוק את אותה פונקציה, פגיעה באחד מהם לא הייתה אמורה לתת פנוטיפ (פנוטיפ - בעיה, במקרה הזה), כי השני היה מפצה. העובדה שפגיעה בכל אחד מהם (בנפרד) עדיין נותנת פנוטיפ מלמדת שיש להם פונקציה שונה.
כאשר מקלפים את התאים החיצוניים ומשאירים את התאים הפנימיים:
- ב־wild type מתקבלים אפיבלסט ותאי אנדודרם פריאטלי שנודדים.
- ב־Nanog mutant מתקבלים בעיקר תאים עם מאפיינים של אנדודרם פריאטלי.
בהמשך הוצג גם RT-PCR למרקרים של PE, parietal endoderm ו־visceral endoderm, שמראה עלייה במרקרים האלה במוטנטים של Nanog.
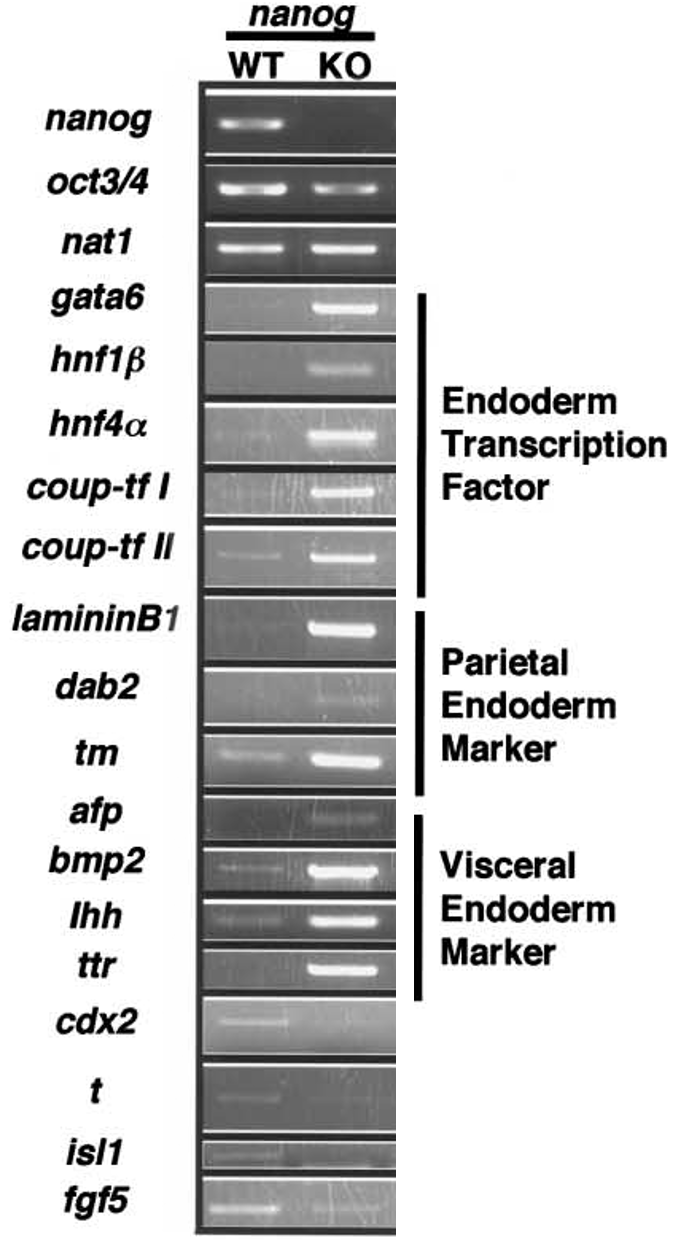
המסקנה: במקום שה־ICM ייתן גם אפיבלסט וגם PE, בהיעדר Nanog הוא נותן בעיקר PE / parietal endoderm-like cells.
המודל: Oct4, Nanog ו־Gata4/6
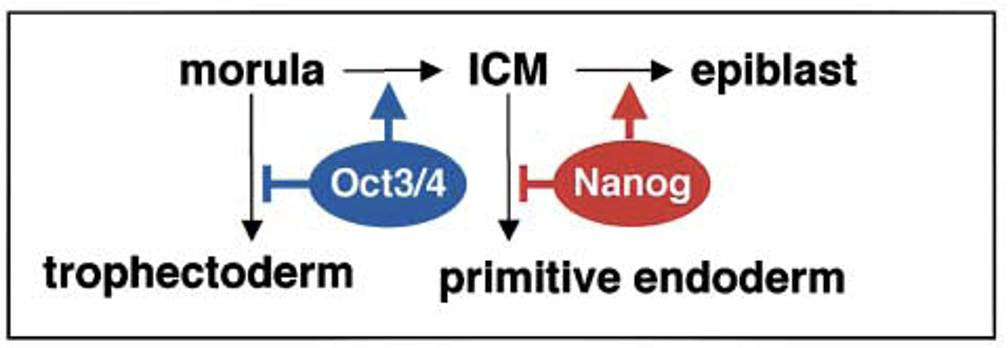
המודל שנבנה מהניסויים:
- בשלב המורולה יש תאים פנימיים ותאים חיצוניים.
- Oct4 דרוש לכך שתאים פנימיים יהפכו ל־ICM, ולא ל־trophoblast (לכן Oct4 פועל ב־first cell fate decision?)
- אם פוגעים ב־Oct4, לא נוצר ICM תקין, ותאים פנימיים מקבלים מאפיינים של Trophoblast.
- Nanog נמצא במורד הזרם ביחס ל־Oct4.
- Nanog מאפשר ל־ICM להפוך לאפיבלסט ומונע ממנו להפוך ל־PE.
- אם פוגעים ב־Nanog, לא מתקבל אפיבלסט תקין, ובמקום זאת מתקבלות אוכלוסיות בכיוון PE / Parietal endoderm.
במובן הזה, Oct4 ו־Nanog הם Pluripotency maintaining genes, אבל כל אחד פועל בנקודת זמן אחרת:
| פקטור | נקודת פעולה מרכזית | תפקיד במודל |
|---|---|---|
| Oct4 | First cell fate decision | שומר שהתאים הפנימיים יהפכו ל־ICM ולא ל־trophectoderm |
| Nanog | Second cell fate decision | שומר על כיוון אפיבלסט ומונע מעבר של אותם תאים ל־PE |
Gata4 ו־Gata6
Gata4 ו־Gata6 הם פקטורי שעתוק נוספים. לפי השיעור, הם עושים תפקיד דומה, והדיון התמקד ב־Gata4.
ב־Gata4 loss of function מתקבל עובר שאין בו PE. לכן Gata4 משתתף ב־Second cell fate decision ומאפשר ל־ICM להפוך ל־PE.
במודל:
- Nanog מקדם אפיבלסט בתאים שבהם הוא מתבטא.
- Gata4 מקדם PE.
Nanog, Gata4 ו־Cell Autonomy
לכאורה יש סתירה:
- מצד אחד, Nanog מעכב יצירת PE בתאים שבהם הוא מתבטא.
- מצד שני, ב־Nanog loss of function כמעט לא רואים ביטוי של Gata4, ולכן Nanog נדרש כדי ש־Gata4 יתבטא (ויקדם PE).
בנוסף לכך, Nanog נקשר לפרומוטר של Gata4, ובתאים שמבטאים Nanog אין Gata4. מכאן שבתא שבו Nanog מתבטא, הוא פועל כרפרסור של Gata4.
בדיקה עצמית - מה הסתירה?
הסתירה:
- Nanog מדכא Gata4
- אבל בלי Nanog אין כמעט Gata4
כדי לפתור את הסתירה הוצגו שני מושגים:
| מושג | משמעות |
|---|---|
| Cell autonomous | חלבון שמתבטא בתא ומשפיע על אותו תא עצמו |
| Cell non-autonomous | חלבון שמתבטא בתא אחד ומשפיע על תא אחר שאינו מבטא אותו |
לפי המודל:
- Cell autonomous - תא שמבטא Nanog נשמר בכיוון אפיבלסט, ו־Nanog מדכא בו את Gata4.
- Cell non-autonomous - תא שמבטא Nanog גורם לתא שכן (שאינו מבטא Nanog) להתחיל לבטא Gata4, דרך חלבון אחר שמופרש החוצה.
- תא שמבטא Gata4 ילך לכיוון PE.
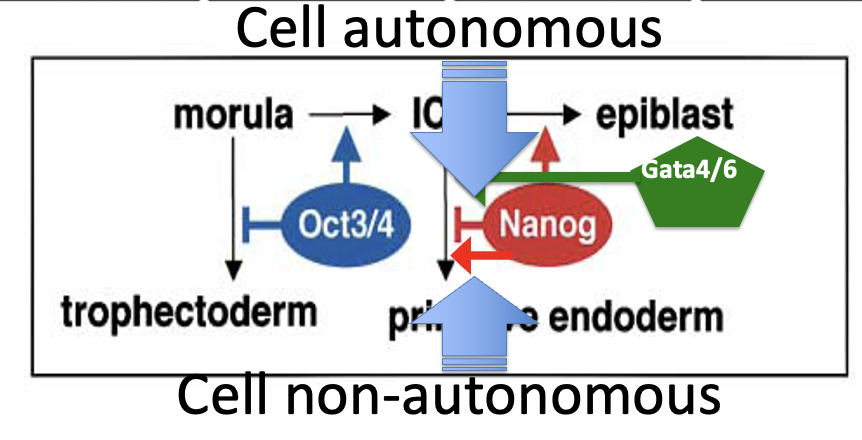
כך Nanog יכול מצד אחד למנוע מתא מסוים להפוך ל־PE, ומצד שני להיות נחוץ כדי שתאים אחרים בסביבה יבטאו Gata4 ודווקא כן יהפכו ל־PE.
בדיקה עצמית - מה הפתרון לסתירה?
בתא שמבטא Nanog:
Nanog ⊣ Gata4
→ epiblast
בתא סמוך שלא מבטא Nanog:
Nanog from other cell → signal secreted → Gata4/6
→ primitive endoderm
רצף האירועים המרכזי
Zygote
↓
2-cell embryo
↓
4-cell embryo
↓
8-cell embryo
↓
Morula
↓
Compaction
↓
First cell fate decision
├─ Outer cells
│ ↓
│ Trophectoderm / Trophoblast
│ ↓
│ Extraembryonic tissues
│ ├─ Extraembryonic ectoderm
│ └─ Ectoplacental cone → placenta
│
└─ Inner cells
↓
Inner cell mass (ICM)
↓
Second cell fate decision
├─ Epiblast (EPI)
│ ↓
│ Embryo proper
│
└─ Primitive endoderm (PE)
↓
Extraembryonic endoderm derivatives
├─ Visceral endoderm (VE)
│ ↓
│ Surrounds epiblast + extraembryonic ectoderm
│
└─ Parietal endoderm (ParE)
↓
Migrates along inner side of trophoblast