מומלץ לעיין תחילה בסיכומים של שיעור 1 - חומצות אמינו ומים ו־שיעור 2 - חומצות אמינו: מבנה, תכונות וחישובי pI לפני התרגול הבא.
שאלה 1: מטען נטו לאורך טווח $\text{pH}$
ציין את המטען נטו של גליצין בערכי ה־$\text{pH}$ הבאים: $1, 2.34, 7, 9.6, 11$.
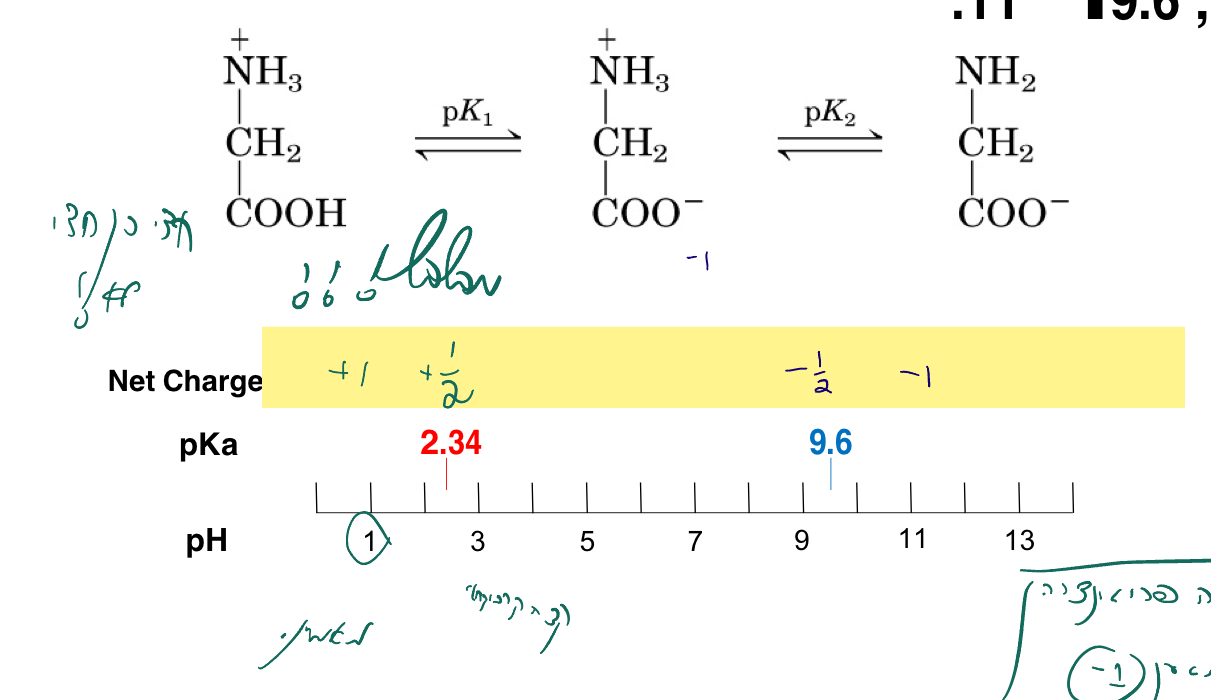
מעיון בטבלה של גליצין בשיעור 2, ניתן לראות ש־$\text{p}K_a$ של קצה הקרבוקסיל הוא $2.34$ ושל קצה האמינו הוא $9.6$. בנקודות האלה חצי מהמולקולות עוברות פרוטונציה/דה־פרוטונציה.
- $\text{pH} = 1$: מטען נטו = $+1$ (גם הקצה האמיני וגם קצה הקרבוקסיל פרוטונטים)
- $\text{pH} = 2.34$: מטען נטו = $+0.5$ (קצה הקרבוקסיל עובר דה־פרוטונציה)
- $\text{pH} = 7$: מטען נטו = $0$ (קצה הקרבוקסיל דה־פרוטונטי, קצה האמיני פרוטונטי)
- $\text{pH} = 9.6$: מטען נטו = $-0.5$ (קצה האמיני עובר דה־פרוטונציה)
- $\text{pH} = 11$: מטען נטו = $-1$ (גם קצה האמיני וגם קצה הקרבוקסיל דה־פרוטונטים)
שאלה 2: חישוב ערכי pI
חשבו את ערכי ה־$\text{p}I$ של החומצות אלנין, ליזין וחומצה גליטמית מתוך ערכי ה־$\text{p}K_a$ שלהן.
…
שאלה 3: מה ה־pI של הפפטיד הנתון
\[\text{Lys-Gly-Ala-Gly}\]נתוני pKa:
| קבוצת פרוטונציה | pKa |
|---|---|
| קצה אמיני (Lys) | $8.95$ |
| שייר צד בליזין (Lys) | $10.53$ |
| קצה קרבוקסילי (Gly) | $2.33$ |
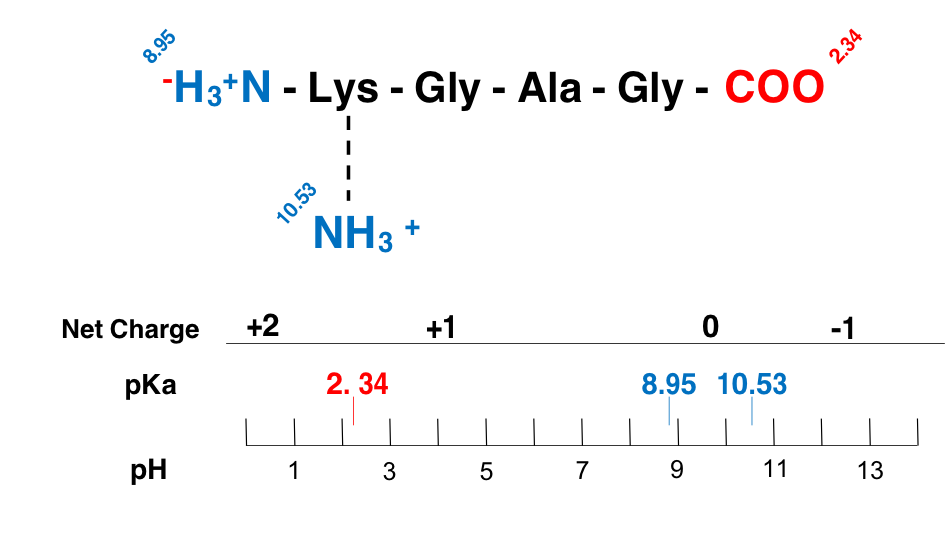
ברישום פפטידים הקצה האמיני מצד שמאל והקרבוקסילי מצד ימין.
נציב בנוסחה:
\[\text{pI} = \frac{pK_a1 + pK_a2}{2}\]כאשר $pK_a1$ ו־$pK_a2$ הם הערכים של הקבוצות הפרוטונציה שמקיפות את הנקודה שבה המטען נטו הוא אפס.
במקרה של הפפטיד הנתון, הקבוצות הפרוטונציה הן:
- קצה אמיני של ליזין ($pK_a = 8.95$)
- שייר צד בליזין ($pK_a = 10.53$)
לכן:
\[\text{pI} = \frac{8.95 + 10.53}{2} = \frac{19.48}{2} = 9.74\]שאלה 4: מסיסות במים
חומצה בינוזואית ופירידין בעלי $\text{p}K_a = 5$. איזו תרכובת תהיה יותר מסיסה במים לאחר הוספה של $\ce{NaOH}$ או $\ce{HCl}$?
מולקולה עם מטען יותר מסיסה במים.
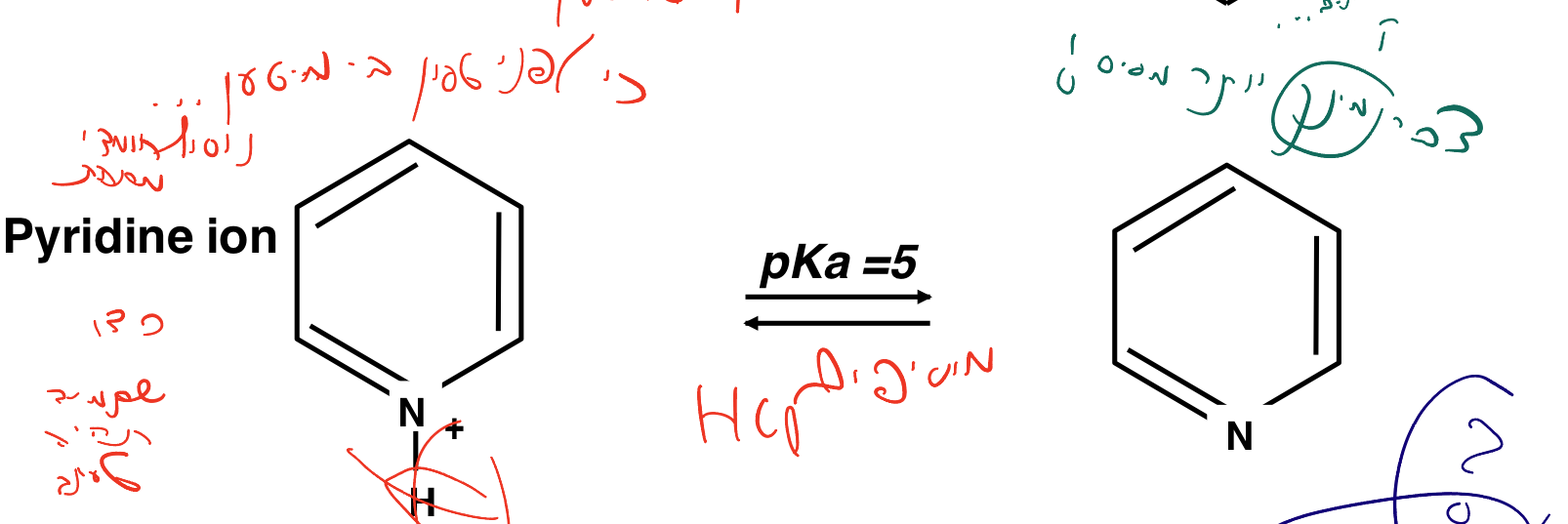
במקרה של פירידין, נרצה להוסיף $\ce{HCl}$ כדי להוריד את ה־$\text{pH}$ ואז לשמור על המטען החיובי בסביבה חומצית. במילים אחרות, כדי שתמיד תהיה טעונה. אם לעומת זאת נוסיף $\ce{NaOH}$, ה־$\text{pH}$ יעלה מעל ה־pKa ואז המולקולה תאבד את הפרוטון ותהפוך לחסרת מטען ולא מסיסה במים, כי לא תוכל להיקשר למים באופן יעיל. המימן מאפשר לה להיקשר טוב יותר.
מולקולה טעונה במטען פלוס אחד מתחת לpKa שלה. אם נעבור את ה־pKa, המולקולה תתנתק מפרוטון ותהפוך לחסרת מטען, כלומר, תאבד את המוטיבציה ליצור קשרים עם מולקולות מים ולהתמסס.
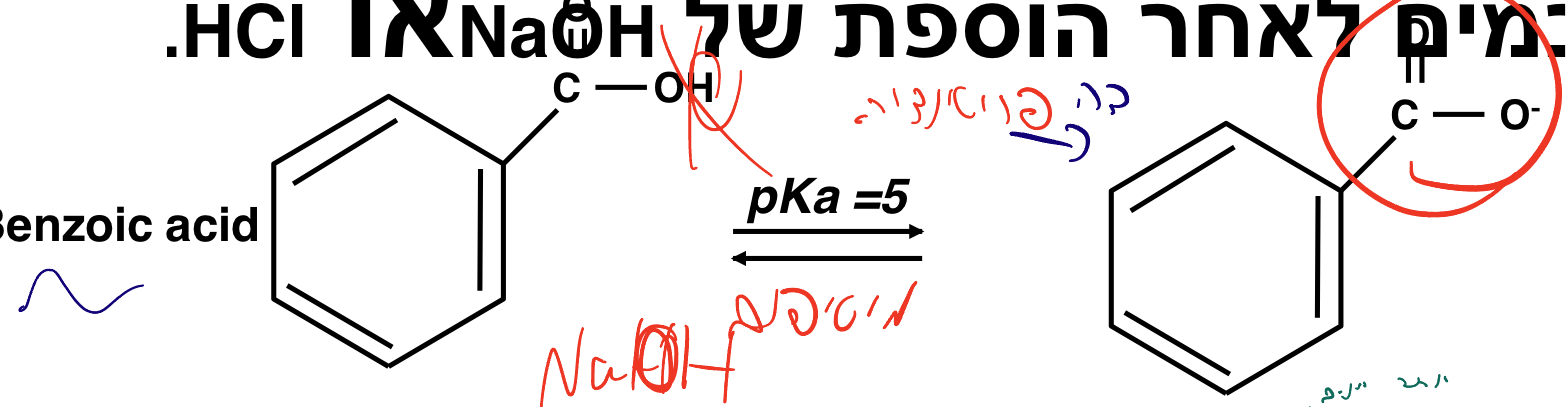
במקרה של חומצה בינוזואית בדיוק להפך: נרצה להוסיף $\ce{NaOH}$ כדי להעלות את ה־$\text{pH}$ מעל ה־pKa ואז כל המולקולה תהיה מיוננת (שלילית) ותהיה מסיסה במים.
אנחנו רוצים שיהיה יון - דבר מיונן (מטען חשמלי) יותר מסיס!
שאלה 5: מציאת אחוז של צורה מסוימת
צייר את צורת היינון של אלנין ב־$\text{pH}$ שווה ל־pI שלה. האם קיימת בתמיסה ב־$\text{pH}$ שווה ל־pI הצורה המצוירת? אם כן, מה האחוז שלה?
\[\begin{array}{ccc}& \text{Alanine (not in zwitterionic form)} & \\[6pt]& \quad\quad\textcolor{red}{\ce{COOH}} & \\[-2pt]& \vert \\[-2pt]& \quad\textcolor{blue}{\ce{H2N}}\ce{-C-H} \quad\quad & \\[-2pt]& \vert \\[-2pt]& \quad{\ce{CH3}} & \\[-2pt]\end{array}\]ה־pI של אלנין הוא בערך $6$. מהטבלה בשיעור 2, ניתן לראות שלאלנין יש שתי קבוצות פרוטונציה עם pKa של $2.34$ (קצה קרבוקסילי) ו־$9.69$ (קצה אמיני). מכאן ניתן להסיק שב־$\text{pH}$ של $6$ הקצה הקרבוקסילי יהיה דה־פרוטונטי (מטען שלילי) והקצה האמיני יהיה פרוטונטי (מטען חיובי). כלומר, הצורה המצוירת קיימת בתמיסה ב־$\text{pH}$ שווה ל־pI שלה.
אם נצייר קלאסי:
\[\begin{array}{ccc}& \text{Alanine} & \\[6pt]& \quad\quad\ce{COO-} & \\[-2pt]& \vert \\[-2pt]& \ce{H3N+-C-H} \quad\quad & \\[-2pt]& \vert \\[-2pt]& \quad\textcolor{red}{\ce{CH3}} & \\[-2pt]\end{array}\]כדי למצוא את האחוז של הצורה המצוירת ב־$\text{pH}$ שווה ל־pI, נשתמש במשוואת הנדרסון-האסלבלך:
\[\text{$\text{pH}$} = \text{p}K_a + \log_{10}\frac{[\ce{A-}]}{[\ce{HA}]}\]נחשב את האחוז עבור כל קבוצת פרוטונציה בנפרד:
-
עבור קצה הקרבוקסילי ($\text{p}K_a = 2.34$):
\[6.01 = 2.34 + \log_{10}\frac{[\ce{COO-}]}{[\ce{COOH}]}\] \[\log_{10}\frac{[\ce{COO-}]}{[\ce{COOH}]} = 6.01 - 2.34 = 3.67\] \[\frac{[\ce{COO-}]}{[\ce{COOH}]} = 10^{3.67} \approx \frac{4680}{1}\]כלומר, כמעט כל הקצה הקרבוקסילי יהיה דה־פרוטונטי (שלילי).
-
עבור קצה האמיני ($\text{p}K_a = 9.69$):
\[6.01 = 9.69 + \log_{10}\frac{[\ce{NH2}]}{[\ce{NH3+}]}\] \[\log_{10}\frac{[\ce{NH2}]}{[\ce{NH3+}]}\ = 6.01 - 9.69 = -3.68\] \[\frac{[\ce{NH2}]}{[\ce{NH3+}]} = 10^{-3.68} \approx 0.0002=\frac{1}{4680}\]כלומר, כמעט כל הקצה האמיני יהיה פרוטונטי.
כלומר, הסיכוי ששתי הקבוצות יהיו $\ce{COOH}$ ו־$\ce{NH2}$ הוא $1$ ל־$4680 \times 4680 = 21,902,400$.
שאלה 6: סימון פחמנים אסימטריים
…
שאלה 7: איפה תרופה נספגת לדם יותר
שאלה 7: אספירין הוא חומצה חלשה עם pKa=3.5 . התרופה עוברת לדם בדיפוזיה דרך הקיבה וגם במעי. איפה התרופה נספגת לדם יותר? (ה־$\text{pH}$ במעי 6 ובקיבה 1.5).
במעי ה־$\text{pH}$ יותר בסיסי ולכן זה יגרום לו לעבור דה־פרוטונציה.
מה שמפריד בין הסביבה החיצונית לפנימית הוא ממברה.
דווקא כשהאספירין לא טעון הוא יהיה הידרופובי ולכן יוכל לחדור דרך הממברנה.
מכאן שייספג יותר טוב דרך הקיבה.
דור פסקלדברים הידרופובים יכולים להיכנס דרך הממברנה יותר בקלות. מולקולות גדולות בעייתיות.
אין סיכוי שיונים ייכנסו לתוך הממברנה, ולכן הספיגה של אפסירין תהיה יותר טובה בקיבה שבה הוא לא מיונן, כי ה־$\text{pH}$ נמוך מה־pKa שלו.