הקדמה
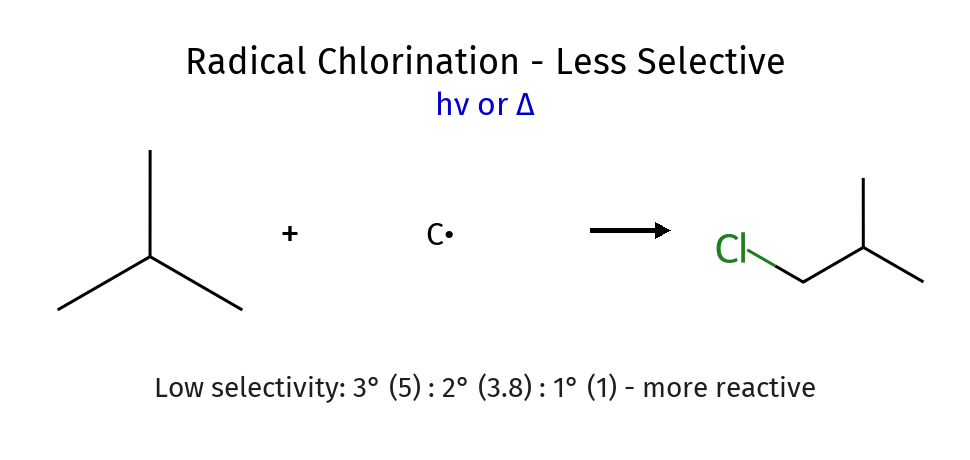
יותר ריאקטיבי ($\ce{Cl}$) פחות סלקטיבי
סלקטיבי ($\ce{Br}$) - יעדיף שלישוני או שניוני על פני ראשוני
הנושא החדש שלנו הוא יצירת אלקיל הלידים. אנחנו בתגובות התמרה ואלימינציה בעצם מגיבים על אלקיל הלידים ומקבלים תוצר של תגובת התמרה או תוצר של תגובת אלימינציה. כעת אנחנו הולכים לדבר על איך אנחנו מייצרים את אלקיל הלידים.
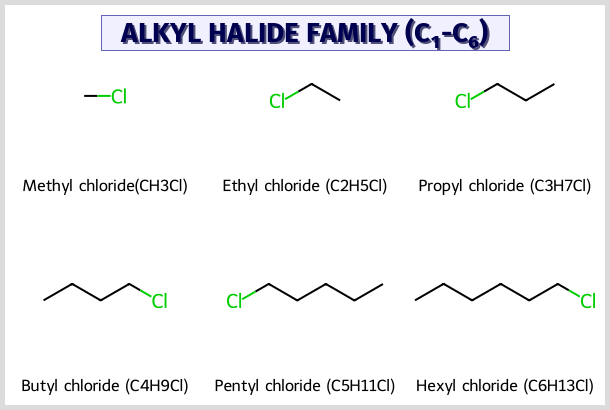
מאפייני אלקיל הלידים
אלקיל הלידים מורכבים מהלוגן (שמסומן בדרך כלל ב־$\ce{X}$) שמחובר לאלקאן - שרשרת פחמנים עם קשרים קוולנטיים (יחידים), כלומר מהצורה:
\[\ce{C}_{n} \ce{H}_{2n+1}\]ליתר דיוק - מולקולה אורגנית, שבה הלוגן ($\ce{F, Cl, Br, I}$) מחובר לפחמן בהיברידיזציית ${sp}^3$ (כלומר, פחמן עם ארבעה קשרים קוולנטיים).
אלקיל הלידים יכולים להיות:
| סוג אלקיל הליד | מבנה כללי | דוגמה |
|---|---|---|
| מתיל הליד | \(\begin{array}{ccc} & \ce{H} & \\ & \vert & \\ & \ce{H-C-X} & \\ & \vert & \\ & \ce{H} & \end{array}\) | |
| ראשוניים (1°) | \(\begin{array}{ccc} & \ce{H} & \\ & \vert & \\ & \ce{R-C-X} & \\ & \vert & \\ & \ce{H} & \end{array}\) | $\ce{CH3CH2CH2CH2-Br}$ (1-bromobutane) |
| שניוניים (2°) | \(\begin{array}{ccc} & \ce{R} & \\ & \vert & \\ & \ce{R-C-X} & \\ & \vert & \\ & \ce{H} & \end{array}\) | \(\begin{array}{ccc} & \ce{Cl} & \\ & \vert & \\ & \ce{CH3-C-H} & \\ & \vert & \\ & \ce{CH3} & \end{array}\) (2-chloropropane) |
| שלישוניים (3°) | \(\begin{array}{ccc} & \ce{R} & \\ & \vert & \\ & \ce{R-C-X} & \\ & \vert & \\ & \ce{R} & \end{array}\) |
מבנה מולקולרי
המבנה של אלקיל הלידים כולל:
- $\delta^+$ על הפחמן
- $\delta^-$ על ההלוגן
כלומר, אלקיל הליד היא מולקולה פולרית.
תגובת הלוגנציה רדיקלית
Methyl chloride:
\[\ce{CH4 + Cl2 ->[\Delta][or h\nu] CH3Cl + HCl}\]Ethyl bromide:
\[\ce{CH3CH3 + Br2 ->[\Delta][or h\nu] CH3CH2Br + HBr}\]Bonus:
\[\ce{CH4 + F2 ->[\Delta] explosive reaction}\]
התגובה הכללית
התגובה שאנחנו הולכים לעשות נקראת תגובה הלוגנציה רדיקלית - היא עובדת במנגנון רדיקלי.
התגובה באופן כללי:
\[\ce{Alkane + X2 ->[\Delta or h\nu] Alkyl~halide + HX}\]ניתן לרשום ״אור״ או חום גם בצורה סכמטית:
\[h\nu \text{ or } \Delta\]מאפיינים של הלוגנציה רדיקלית
התגובה הולכת טוב עם כלור וברום, אבל:
- עם פלואור (F) - התגובה מאוד נפיצה ואקסותרמית
- עם יוד (I) - התגובה איטית מאוד
לכן הריאגנטים הרלוונטיים לתגובה הם בדרך כלל:
- $\ce{Cl2}$
- $\ce{Br2}$
רקע - ריאקטיביות של אלקאנים
אלקאנים הם חומרים מאוד לא ריאקטיביים. כלומר, כמעט לא קורות עליהם תגובות. התגובות על אלקאנים, חוץ מתגובת ההלוגנציה הרדיקלית, הן מעטות וכוללות תגובת שריפה (צריבת אלקאנים בחימום בנוכחות חמצן - תגובה מאוד אקסותרמית שנותנת לנו דלקים: $\ce{CO2}$ ומים).
אלקאנים לא ריאקטיביים כי הם לא פולריים - אין $\delta^+$ ו$\delta^-$, אין כמעט שום דבר לעשות שם. יש להם קשרי סיגמה $\sigma$ חזקים ואטומים בלי מטען חלקי.
מנגנון התגובה הרדיקלית (Monochlorination of Methane)
הבנת פירוק הומוליטי לעומת הטרוליטי
עד עכשיו דיברנו על תגובות של מנגנון הטרוליטי:
פירוק הטרוליטי - פירוק לא שווה:
- מישהו אחד לוקח את האלקטרונים ונוצר $\delta^-$
- עוד מישהו אחד שעכשיו יהיה לו $\delta^+$ (חסר אלקטרונים)
פירוק הומוליטי - זה בעצם פירוק שווה:
- יש לנו קשר קוולנטי כלשהו שמכיל שני אלקטרונים
- ה־A לוקח אלקטרון אחד
- ה־B לוקח אלקטרון אחד
- כל אחד לוקח את האלקטרון שלו
דוגמאות לפירוק הומוליטי
פירוקסידים:
\[\ce{R-O-O-R ->[\Delta] 2 R-O^•}\]הלוגנים:
\[\ce{X-X ->[h\nu][\Delta] 2 X^•}\]המנגנון בשלושה שלבים
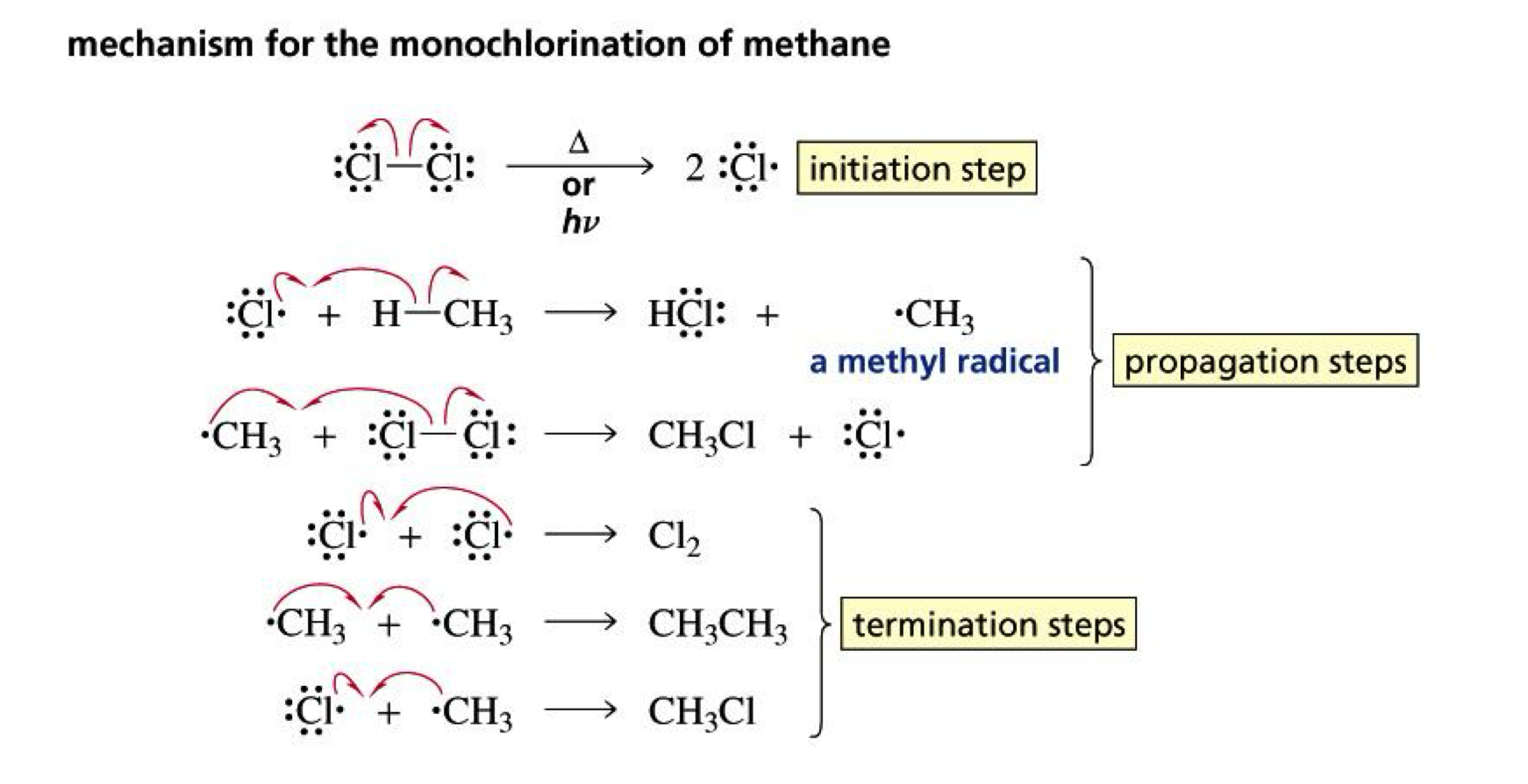
המנגנון מתחלק לשלושה חלקים:
1. Initiation (התחלה)
השלב ההתחלתי לתגובה - איך התגובה תתחיל.
כשניקח $\ce{Cl2}$ ונספק לו חום גבוה מאוד או אור, יקרה פירוק הומוליטי - נקבל כתוצאה מהתנאים האלה שתי מולקולות כלור רדיקל.
\[\ce{Cl2 ->[\Delta][or h\nu] 2 Cl^•}\]רדיקל - אטום שמופיע כמות שהוא בטבלה המחזורית. כמה אלקטרונים יש סביב הכלור? שבעה. הוא לא באוקטט, חסר לו אחד.
2. Propagation (התפשטות - פרופוגציה)
התגובה עצמה - לב התגובה. מתחלקת לשני שלבי הפרופגציה:
שלב הפרופגציה הראשון:
\[\ce{Cl^• + H-CH3 -> HCl + \underbrace{CH3^•}_{\text{a methyl radical}}}\]מגיע כלור רדיקל ופוגש את האלקן (במקרה הזה מתאן). כתוצאה מזה שהכלור רדיקל מתקרב למתאן, הוא גורם ל־C-H עצמו גם כן לעבור פירוק הומוליטי.
אם עכשיו $\ce{CH4}$ מתפרק כפירוק הומוליטי, נקבל: $\ce{CH3^•}$ רדיקל ועוד $\ce{H^•}$ רדיקל. ואז ה־$\ce{H^•}$ רדיקל מתחבר לכלור רדיקל - מה מקבלים? $\ce{HCl}$ ועוד מתיל רדיקל.
שלב הפרופגציה השני:
\[\ce{CH3^• + Cl2 -> \boxed{CH3Cl} + Cl^•}\]זה השלב שבו נקבל את התוצר: המתיל רדיקל מגיב עם עוד מולקולה של $\ce{Cl2}$. הוא גורם גם כן ל$\ce{Cl2}$ לעבור פירוק הומוליטי - יש לנו שתי כלור רדיקל. כלור רדיקל אחד מתחבר עם הפחמן רדיקל, מקבלת מתיל כלוריד, וקיבלנו גם עוד כלור רדיקל.
3. Termination (סיום)
התגובה מסתיימת באופן הבא - כל הרדיקלים נפגשים אחד עם השני ולמעשה נגמרים. כלומר,התגובה הסתיימה כשאין יותר רדיקלים. האפשרויות לכך (זה לא ״או או או״, אלא זה ״או וגם או וגם או וגם״):
\[\ce{Cl^• + Cl^• -> Cl2}\] \[\ce{CH3^• + CH3^• -> C2H6}\] \[\ce{Cl^• + CH3^• -> CH3Cl}\]אלה כל האפשרויות של רדיקלים שנוצרו איפשהו במהלך התגובה וצריכים להתחבר. ברגע שלא נוצרו יותר רדיקלים וחיברנו את כולם, התגובה הגיעה לסיומה.
דוגמה עם ברום (Monobromination of Ethane)
אותה תגובה במקום כלור ברום:
Initiation
\[\ce{Br2 ->[h\nu \text{ or } \Delta] 2 Br^•}\]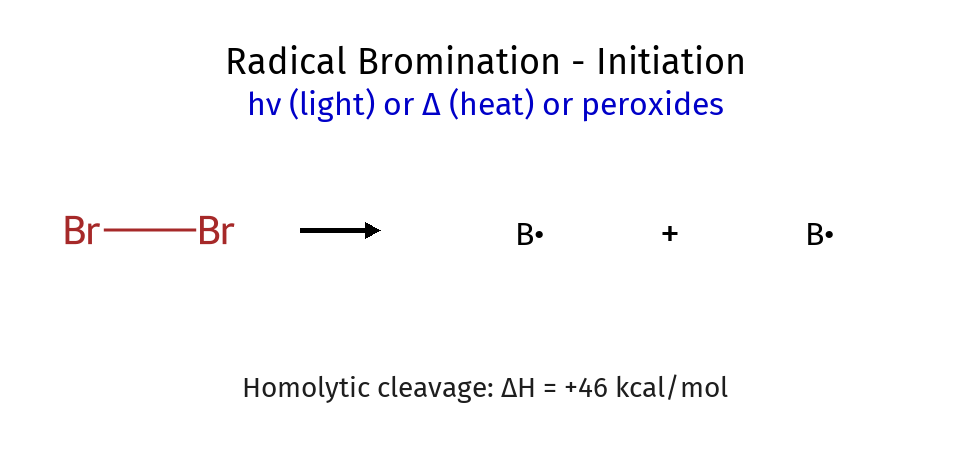
Propagation
שלב ראשון:
\[\ce{Br^• + C2H6 -> C2H5^• + HBr}\]שלב שני:
\[\ce{C2H5^• + Br2 -> C2H5Br + Br^•}\]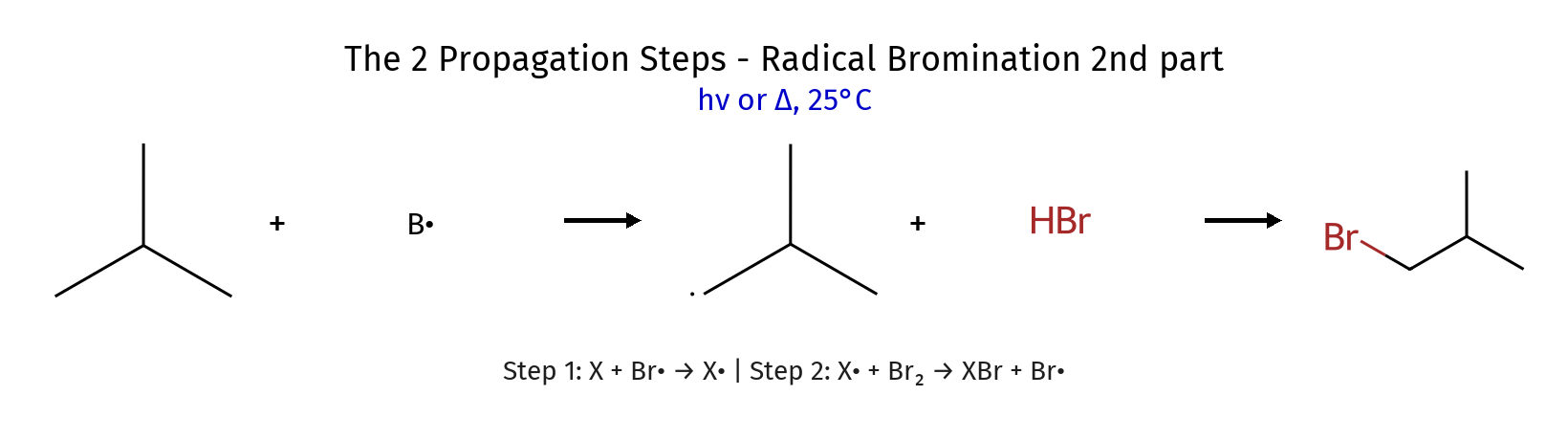
Termination
כל האפשרויות של החיבור:
- $\ce{Br^• + Br^•}$
- $\ce{C2H5^• + C2H5^•}$
- $\ce{Br^• + C2H5^•}$
בעיית הסלקטיביות באלקאנים מורכבים
הבעיה בבוטאן
כשעוברים לדבר על אלקאנים בסדר גבוה יותר, מתחילות הבעיות. למה? כי במתאן ($\ce{CH4}$) ובאתאן ($\ce{C2H6}$) יש רק סוג אחד של מימנים - כל המימנים אותו דבר.
אבל בבוטאן ($\ce{C4H10}$) יש סוגים שונים של מימנים:
- מימנים ראשוניים (6 מימנים)
- מימנים שניוניים (4 מימנים) - המימנים שמחוברים לפחמן שניוני, כלומר פחמן שמחובר לשני פחמנים אחרים. במקרה של בוטאן, אלה שני הפחמנים הפנימיים.

בשלב הראשון של הפרופגציה, ה־X רדיקל לוקח מימן רדיקל. אם כל המימנים אותו הדבר, אין בעיה - אבל אם יש לנו סוגים שונים של מימנים, אז יש פה בעיה - איזה מימן ייקטף?
התוצאות הצפויות לעומת הניסויות
מימנים ראשוניים:
\[\ce{X^• + CH3CH2CH2CH3 -> Primary~alkyl~radical + HX}\] \[\ce{Primary~alkyl~radical + X2 -> Primary~alkyl~halide + X^•}\]מימנים שניוניים:
\[\ce{X^• + CH3CH2CH2CH3 -> Secondary~alkyl~radical + HX}\] \[\ce{Secondary~alkyl~radical + X2 -> Secondary~alkyl~halide + X^•}\]ניתוח סטטיסטי וניסויי
צפוי (Expected):
- 6 מימנים ראשוניים ← 60% תוצר ראשוני
- 4 מימנים שניוניים ← 40% תוצר שניוני
ניסויי (Experimental):
- תוצר שניוני מועדף על פני הצפוי מהסטטיסטיקה
מסקנה
חוץ מהעניין ההסתברותי (Probability), יש עוד פקטור שמשפיע - פקטור הריאקטיביות.
מבנה ויציבות של רדיקלים
מבנה הרדיקל
המבנה של הרדיקל:
- הפחמן הרדיקלי קשור בעצם לשלושה קשרים
- יש לו אלקטרון נוסף באורביטל $\text{p}$
- הוא $\text{sp}^2$ עם אורביטל $\text{p}$ שהוא לא ריק, עם אלקטרון אחד
הדמיון לקרבוקטיון
לרדיקל יש מבנה שדומה לקרבוקטיון ($\ce{C^+}$) יותר מאשר מבנה שדומה לקרבואניון ($\ce{C^-}$).
למה?
- המבנה היציב של האטום הוא כאשר יש לו אוקטט
- האם יש לו פה אוקטט? לא
- הוא בעצם בחוסר - הוא מרגיש חסר
- המבנה של הרדיקל דומה יותר למבנה של מטען חיובי, שבעצם האטום מרגיש שחסר לו אלקטרון
יציבות רדיקלים
כמו בקרבוקטיונים - ככל שהרדיקל יותר מותמר (substituted), כך הוא יותר יציב:
סדר יציבות:
\[\text{Tertiary} > \text{Secondary} > \text{Primary}\]השפעה על הריאקטיביות
בשלב הראשון של הפרופגציה, כש־X רדיקל תולש מימן רדיקל מהאלקן, התגובה מועדפת לכיוון יצירת הרדיקל היציב יותר.
לכן, למרות שיש יותר מימנים ראשוניים (6) מאשר שניוניים (4), התגובה מועדפת לכיוון המימנים השניוניים כי הם יוצרים רדיקל שניוני שהוא יציב יותר מרדיקל ראשוני.
הערה: תגובות רדיקליות הן סופר חשובות בהיבט של מנגנונים ביולוגיים. רדיקלים זה דברים שיכולים לגרום כל מיני בעיות בגוף - לסרטן, תהליך הזדקנות של האדם וכל מיני דברים שנובעים מרדיקלים. יש לנו בגוף כל מיני חומרים שעוזרים לנו - הם מנטרלים את הרדיקלים האלה, אבל המנגנונים של רדיקלים הם מאוד חשובים בהיבט ביולוגי.
השפעת הריאקטיביות על התפלגות התוצרים
כשברום רדיקל מגיע לשלב הפרופגציה השני, הוא מתחבר עם מולקולת $\ce{Br2}$. הברום רדיקל מתחבר לפחמן רדיקל שנוצר בשלב הראשון, ונוצר עוד ברום רדיקל.
עיקרון יציבות הרדיקלים
אנחנו יודעים שככל שהקרבוקטיון יותר מותמר (substituted), הוא יהיה יותר יציב. אם אמרנו שרדיקל דומה מאוד בתכונותיו לקרבוקטיון - הוא מרגיש את החוסר - גם רדיקל, ככל שהוא יותר מותמר, יהיה יותר יציב.
גורמים המשפיעים על התפלגות התוצרים
כדי לקבוע את התפלגות התוצרים בתגובה, צריך להתחשב בשני גורמים:
- הגורם ההסתברותי - כמה מימנים ראשוניים לעומת כמה מימנים שניוניים
- הגורם הריאקטיביות - שנותן את הפחמן רדיקל היציב יותר (הפחמן רדיקל היותר מותמר)
חישוב התפלגות התוצרים
נתוני ריאקטיביות יחסית (עם כלור)
יחסי ריאקטיביות עם כלור:
\[1 : 3.8 : 5\](ראשוני : שניוני : שלישוני)
זאת אומרת, מימן שלישוני הוא פי 5 יותר ריאקטיבי לתולש אותו מאשר מימן ראשוני.
נוסחה לחישוב התפלגות תוצרים
\[\text{Total reactivity} = \text{Number of hydrogens} \times \text{Relative reactivity}\]לדוגמה בבוטאן:
- מימנים ראשוניים: $6 \times 1 = 6$
- מימנים שניוניים: $4 \times 3.8 = 15.2$
חישוב אחוזים:
- ראשוני: $\frac{6}{6 + 15.2} \times 100 = 29\%$
- שניוני: $\frac{15.2}{6 + 15.2} \times 100 = 71\%$
עקרון הריאקטיביות-סלקטיביות
העיקרון הבסיסי
חומר שהוא יותר ריאקטיבי יהיה פחות סלקטיבי
הסבר האנלוגיה
חומר מאוד ריאקטיבי הוא כמו אדם שמחפש חברה - לא אכפת לו עם מי להגיב. הוא כל כך רוצה להגיב שלא אכפת לו אם זה ראשוני או שניוני - “מה שבא ברוך הבא”.
חומר פחות ריאקטיבי הוא יותר סלקטיבי - יש לו זמן לבחור את המימן שייתן לו את הרדיקל היציב ביותר.
השוואה בין כלור לברום
יחסי ריאקטיביות עם ברום
יחסי ריאקטיביות עם ברום:
\[1 : 82 : 1600\]משמעות: רדיקל שלישוני כמעט תמיד יתקבל כתוצר עיקרי.
התפלגות תוצרים משווה
עם כלור: 29% ראשוני, 71% שניוני
עם ברום: 2% ראשוני, 98% שניוני
הסבר ההבדל
מדוע ברום יותר סלקטיבי?
-
גודל האטום: ברום הוא אטום יותר גדול (שורה רביעית בטבלה המחזורית) לעומת כלור (שורה שלישית)
-
יציבות הרדיקל: ברום רדיקל יותר יציב מכלור רדיקל
-
ריאקטיביות נמוכה יותר: ברום פחות ריאקטיבי ← יותר סלקטיבי
נתוני אנרגיה תומכים
אנרגיה הדרושה לפירוק הומוליטי:
- כלור: $\ce{Cl2 -> 2Cl^•}$ - 58 קילוקלוריות/מול
- ברום: $\ce{Br2 -> 2Br^•}$ - 46 קילוקלוריות/מול
ברום דורש פחות אנרגיה לפירוק ← ברום רדיקל יותר יציב ← פחות ריאקטיבי ← יותר סלקטיבי.
סטריאוכימיה של התגובה
מבנה רדיקל הביניים
כאשר נוצר רדיקל בשלב הפרופגציה הראשון:
- הפחמן הרדיקלי הוא $\text{sp}^2$
- יש לו אורביטל p עם אלקטרון אחד
- המבנה הוא planar (שטוח)
תוצאות סטריאוכימיות
אם הפחמן ההתחלתי היה כיראלי, בשלב השני של הפרופגציה:
\[\ce{radical + Br2 -> produced~product}\]הברום יכול להיכנס משני צדדי המישור:
- מלמעלה
- מלמטה
תוצאה: נקבל תערובת של שני אננטיומרים (רצמט) - בדיוק כמו ב־$\text{S}_\text{N}1$.
התגובה עם הלוגנים שונים
סקירת כל ההלוגנים
| הלוגן | התנהגות בתגובה | סיבה |
|---|---|---|
| פלואור (F) | לא מתאימה - נפיצה | אקסותרמית מדי |
| כלור (Cl) | מתאימה | איזון טוב בין ריאקטיביות וסלקטיביות |
| ברום (Br) | מתאימה | סלקטיבי מאוד |
| יוד (I) | לא מתאימה - איטית מדי | אנדותרמית |
ניתוח תרמודינמי
עם פלואור - מדוע נפיצה?
שלב ראשון של הפרופגציה:
\[\ce{F^• + CH4 -> CH3^• + HF}\]חישוב אנרגיה:
- אנרגיה נדרשת לשבירת C-H: +105 קק”ל/מול
- אנרגיה משוחררת ביצירת H-F: -136 קק”ל/מול
- סה”כ שלב ראשון: -31 קק”ל/מול
שלב שני של הפרופגציה:
\[\ce{CH3^• + F2 -> CH3F + F^•}\]חישוב אנרגיה:
- אנרגיה נדרשת לשבירת F-F: +38 קק”ל/מול
- אנרגיה משוחררת ביצירת C-F: -108 קק”ל/מול
- סה”כ שלב שני: -70 קק”ל/מול
סה”כ התגובה עם פלואור: -101 קק”ל/מול
זאת תגובה אקסותרמית ביותר שיכולה להיות נפיצה!
השוואת כל ההלוגנים
| הלוגן | $\Delta H$ כולל (קק”ל/מול) | אופי התגובה |
|---|---|---|
| F | -101 | אקסותרמית מדי - נפיצה |
| Cl | -24 | אקסותרמית סבירה |
| Br | -6 | אקסותרמית קלה |
| I | +13 | אנדותרמית - לא משתלמת |
שאלות תרגול
שאלה 1: זיהוי תוצר עיקרי
עבור התגובה:
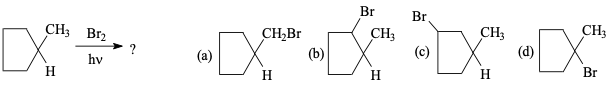
מבינים מנגנון רדיקלי מזה שיש שם ברום 2 ואור.
כלל: ברום מעדיף את המימן שייצור את הרדיקל הכי מותמר (יציב).
הכי מותמר זה המימן הימני התחתון, אז הוא יוצא ומתחבר במקומו ברום.
התשובה היא D.
שאלה 2: זיהוי כל התוצרים האפשריים
מה התוצר / תוצרים ?
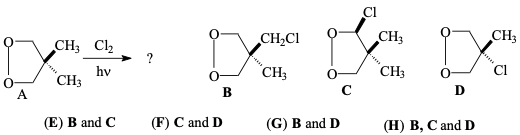
כלור תולש מימן משני מקומות אפשריים.
חשוב: מימנים זהים מבחינה סטריאוכימית יתנו אותו תוצר.
התשובה היא E.
שאלה 3: סדר יציבות רדיקלים
מהם כל תוצרי ההתמרה החד כלוריים האפשריים של החומר 2-מתילבוטאן? סדר את הרדיקלים לפי סדר יציבות עולה.
נתחיל בציור החומר:
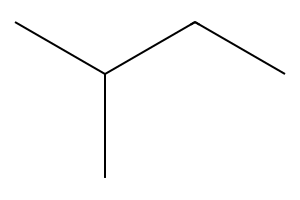
האפשרויות לקבל כלור הן:

סדר יציבות: שלישוני > שניוני > ראשוני > מתילי
שאלה מתקדמת: מבנה אלקן עם תוצר יחיד
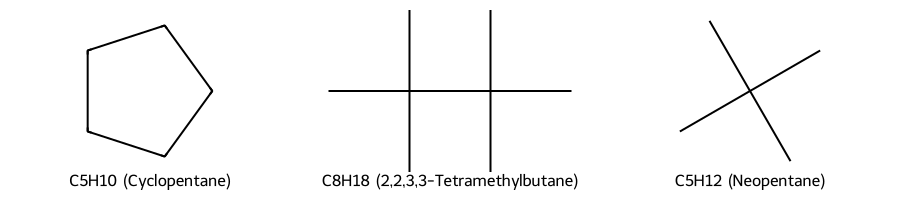
כל אחד מהאלקאנים הבאים מגיב עם Cl2 לתת תוצר מונו־כלורואלקאן יחיד. על סמך מידע זה קבע את המבנה של האלקאנים: $\ce{C5H10}$, $\ce{C8H18}$, $\ce{C5H12}$
אם אלקן $\ce{C5H10}$ (דרגת אי־רוויון = 1) נותן תוצר מונו־כלורו יחיד, מה המבנה שלו?
תשובה: מבנה טבעתי שבו כל המימנים שקולים סטריאוכימית.
 דור פסקל
דור פסקל