תוכן העניינים:
- פיזור הכרומטין בתא
הטרוכרומטיןואאוכרומטין (יוכרומטין)- ניתוח ארגון הכרומטין בשיטת Hi-C
- סיב הכרומטין - TADs
- קומפרטמנטים A ו־B
- טריטוריות כרומוזומליות (Chromosome Territories)
- מחזור התא והכרומטין - מעבר אינטרפאזה ↔ מיטוזה
- סיכום היררכיית ארגון הכרומטין
פיזור הכרומטין בתא
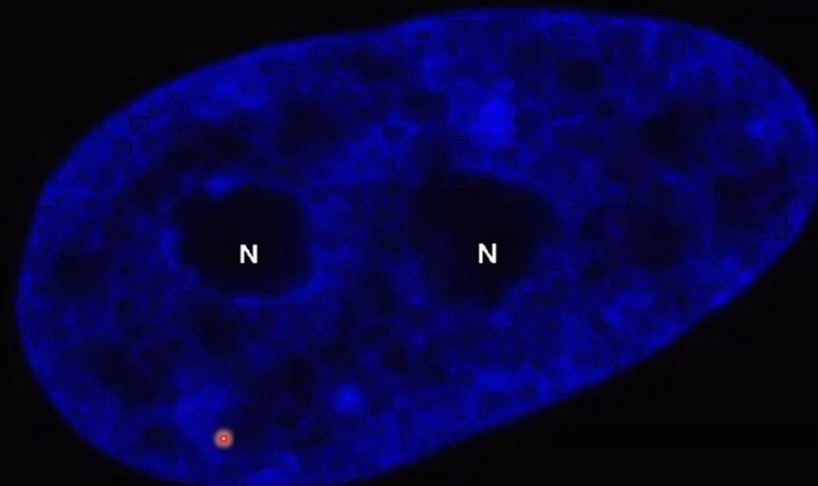 | 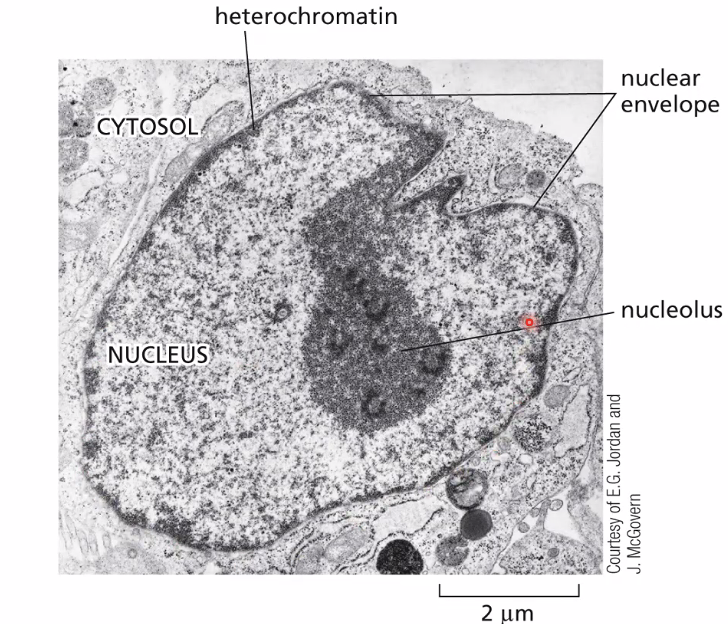 |
בתמונה הימנית (הכחולה) - גרעין של תא איקריוטי בצביעת DAPI (צבע פלואורסצנטי שנקשר ל־DNA). ניתן לצפות בפיזור הכרומטין בגרעין: הוא לא אחיד (אזורים שונים נצבעים בצפיפות שונה). בתמונות ממיקרוסקופ אלקטרוני (צביעת כסף), נראים אזורים צפופים ואזורים פחות צפופים של כרומטין:
- אזורים צפופים - נמצאים בעיקר צמוד לממברנה הגרעינית
- אזור צפוף במיוחד - הגרעינון (Nucleolus), אתר ייצור של RNA ריבוזומלי וטרנסקריפציה (״שעתוק״ או ״תעתוק״) מאסיבית (הצפיפות כאן לא מעידה על השתקה, אלא על פעילות גבוהה)
פעילות טרנסקריפציה לא בהכרח גוררת מראה “פתוח”, כמו של אאוכרומטין; הגרעינון הוא דוגמה לכך: למרות שהוא פעיל, הוא לא נראה כמו אאוכרומטין, אלא כמו אזור צפוף.
הטרוכרומטין ואאוכרומטין (יוכרומטין)
| אאוכרומטין (Euchromatin) | הטרוכרומטין (Heterochromatin) | |
|---|---|---|
| צפיפות | נמוכה יחסית | גבוהה |
| מצב | פתוח | סגור / דחוס |
| פעילות | גנים פעילים בטרנסקריפציה | גנים מושתקים |
| סמן היסטון אופייני | H3K4me3 (ואחרים של פעילות) | H3K9me3 |
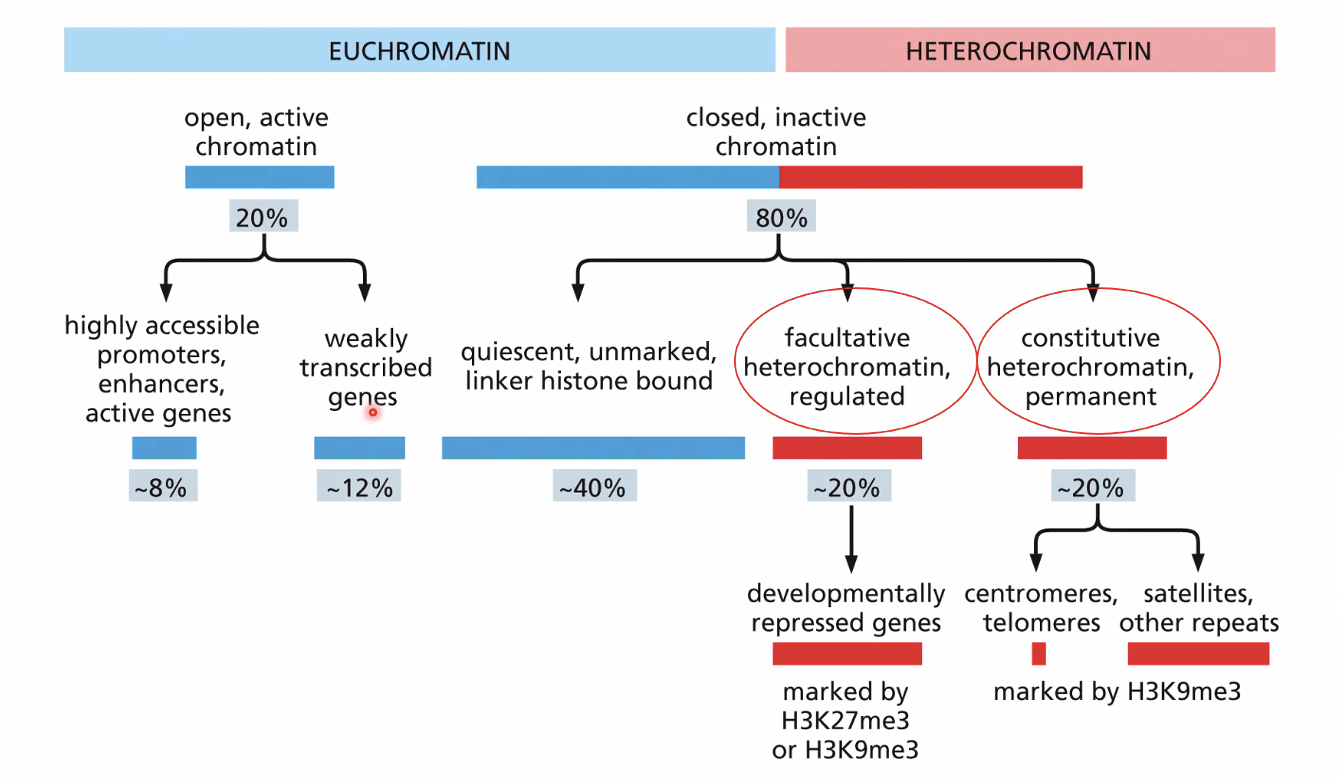
הטרוכרומטין קונסטיטוטיבי לעומת פקולטטיבי
- קונסטיטוטיבי (Constitutive Heterochromatin) - נשאר סגור לאורך כל חיי התא, ללא תלות בסיגנלים. מאפיין צנטרומרים, סטליטים, וחזרות גנומיות (repeats) שרידי אבולוציה שרוצים להשתיק לצמיתות. סמן: H3K9me3.
- פקולטטיבי (Facultative Heterochromatin) - נסגר מסיבות פונקציונליות ויכול להיפתח בתגובה לסיגנלים ביולוגיים. לדוגמה: גן התפתחותי שפעיל בשלב מסוים ונסגר עם השלמת הדיפרנציאציה. סמן: H3K9me3 + H3K27me3.
דינמיות: המעבר בין אאוכרומטין ל
הטרוכרומטיןהוא מאוד דינמי ומבוקר - תלוי בשלב ההתפתחותי, בהורמונים, בציטוקינים, ובסיגנלים סביבתיים אחרים. המודיפיקציות על ההיסטונים נקראות כל הזמן על ידי חלבוני Remodelers שמחליטים אם לשמר אותן או לסלק אותן.
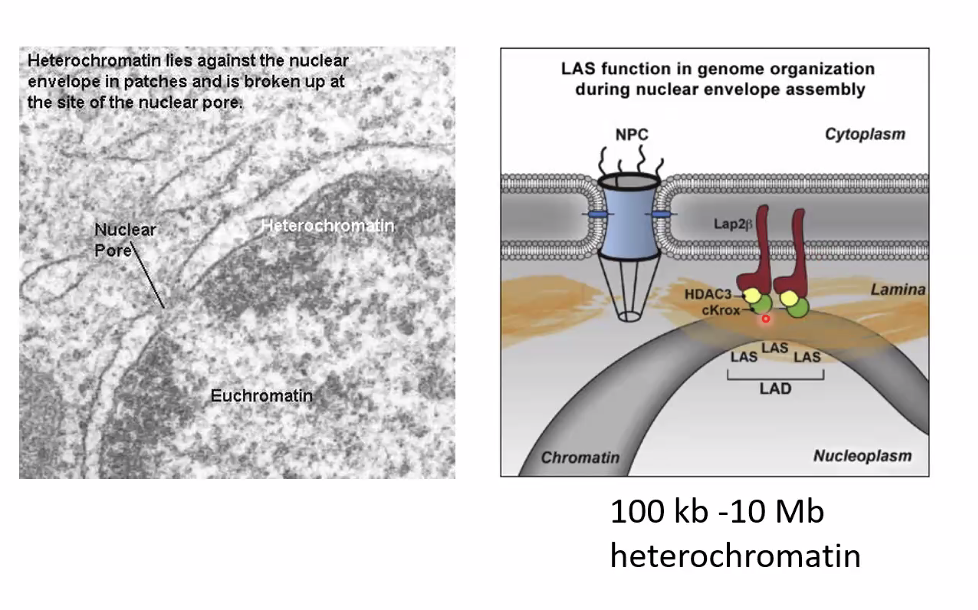
צימוד הכרומטין לממברנה הגרעינית - LADs
אזורי ההטרוכרומטין שצמודים לממברנה הגרעינית מחוברים אליה באמצעות חלבוני Lamin - תהליך מבוקר ובעל משמעות ביולוגית. לדוגמה, פרוגריה (Progeria): מחלה גנטית שנגרמת ממוטציה בחלבון Lamin A, גורמת לשיבוש הצימוד של הכרומטין לממברנה. התוצאה היא הזדקנות מואצת קשה בילדים - עדות לחשיבות הביולוגית של הסידור הפיזי של הכרומטין בתוך הגרעין.
ניתוח ארגון הכרומטין בשיטת Hi-C
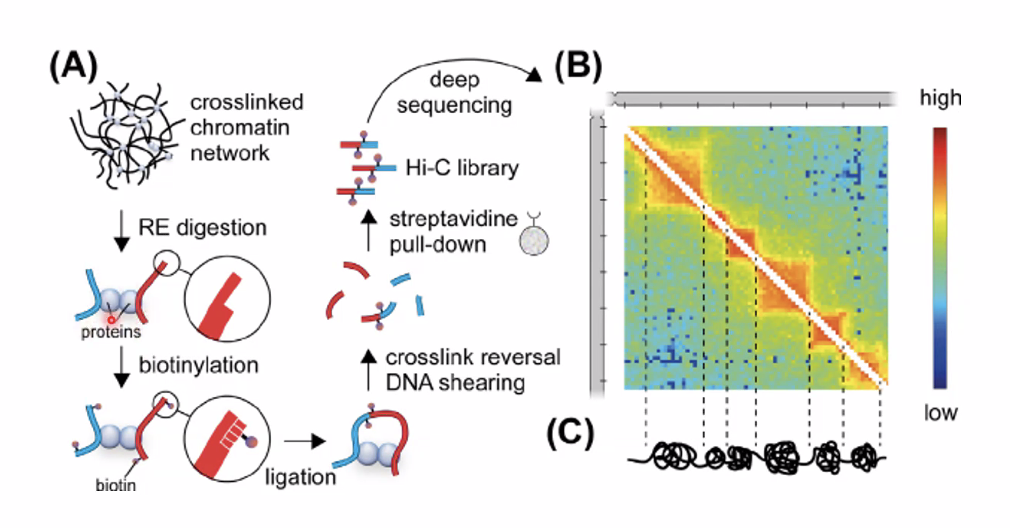
שיטות קלאסיות (מיקרוסקופיה אלקטרונית) מוגבלות ברזולוציה שלהן ואינן מאפשרות ניתוח ברמת הגן הבודד. לפני כ־15 שנה התפתחו שיטות מולקולריות מבוססות Chromosome Capture: 3C → 4C → Hi-C (רזולוציית כרומוזום/גנום שלם).
עקרון שיטת Hi-C
- Cross-linking - קיבוע הכרומטין (חלבון-חלבון, חלבון-DNA, DNA-DNA) כדי לשמר את הארכיטקטורה המרחבית.
- חיתוך - פירוק ה־DNA לחתיכות של $\sim 500 \, \mathrm{bp}$ בסוניקציה או באנדונוקלאז.
- ליגציה וסימון - חיבור בין קצוות של מקטעים שהיו קרובים במרחב (לא על הרצף הליניארי) וסימונם בביוטין.
- ריצוף - כל מקטע מכיל קצה מאזור אחד וקצה מאזור אחר ← בריצוף ניתן לזהות אילו אזורים היו קרובים.
- מפת חום (Heatmap) - בניית מטריצת אינטראקציות: ציר מרכזי = אינטראקציה עצמית (לא מעניין), אזורים מחוץ לאלכסון = אינטראקציות מרוחקות (מעניין).
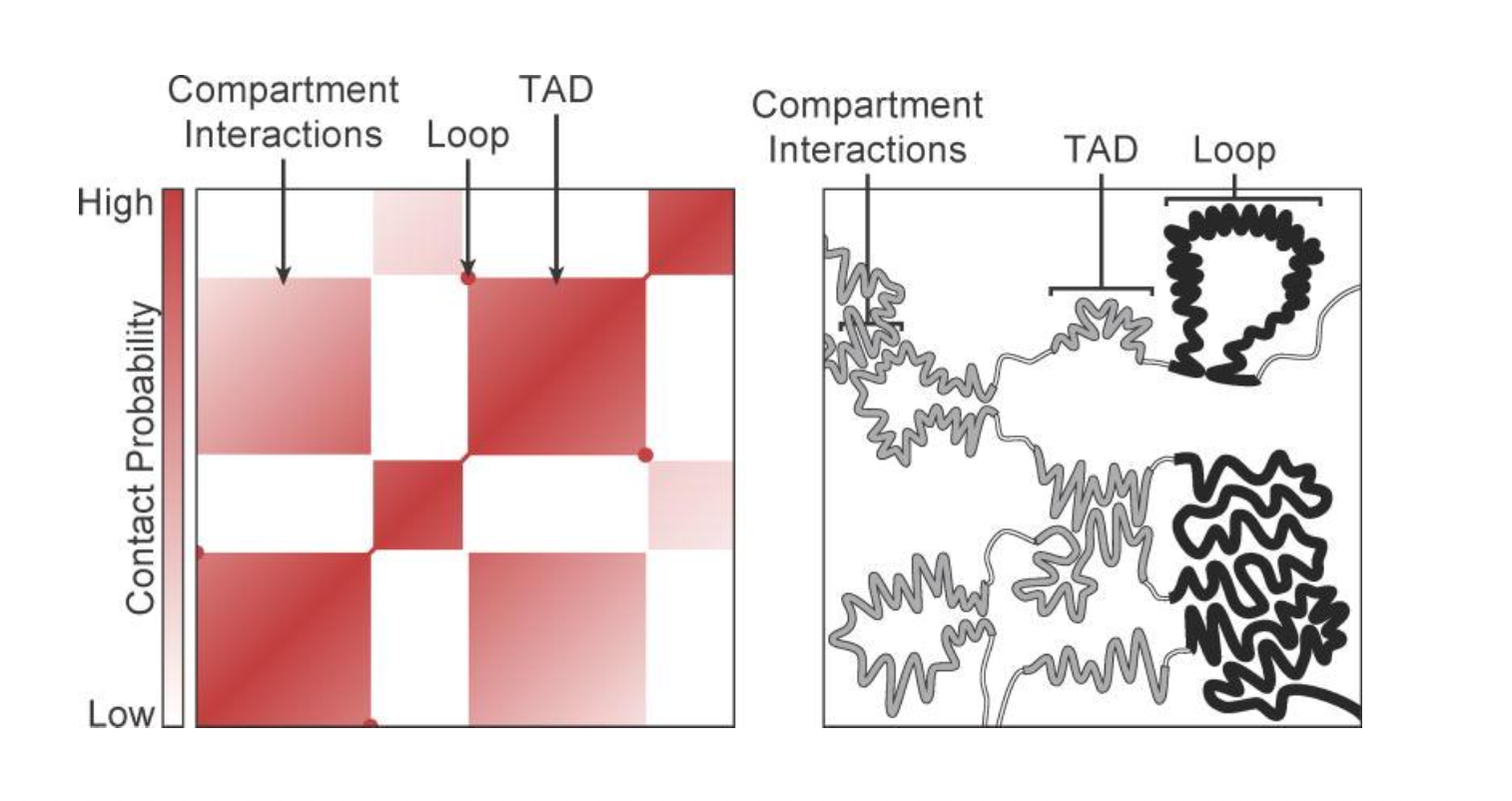
סיב הכרומטין - TADs
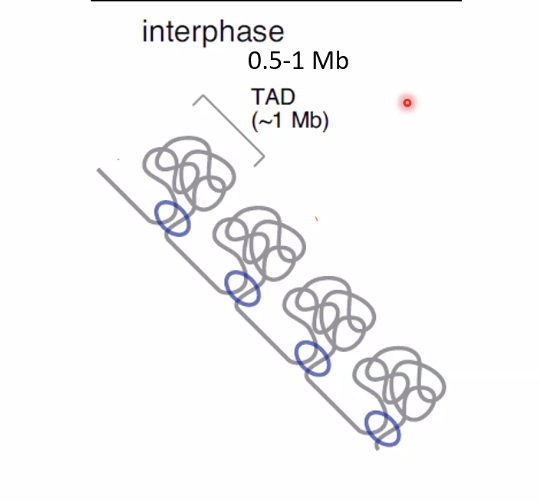
TAD - Topologically Associating Domain
TAD הוא לולאה בסיסית של כרומטין - אזור שבו ה־DNA “מקופל” כך ששני הקצוות של הלולאה קרובים זה לזה במרחב, למרות מרחקם הליניארי.
מאפייני TAD
- גודל: כ־1 מגה־בסיס (Mb)
- הכרומוזום בנוי מסדרה של TADs עוקבים, אחד אחרי השני
- הרבה אינטראקציות בתוך ה־TAD, מעט אינטראקציות בין TADs - מה שיוצר את תבנית “לוח השחמט” במפת ה־Hi-C
חשיבות פונקציונלית
- יחידה טופולוגית עצמאית - הנעילה בקצוות מאפשרת יצירת מתח טופולוגי (supercoiling) פנים-TAD
- הגברת סיכוי לאינטראקציות פנים-TAD ובידוד מאינטראקציות חוץ־TAD
- קו־רגולציה - גנים שפועלים יחד במסלול ביולוגי כלואים באותו TAD
- בקרת גנים על ידי Enhancer-Promoter:
- Enhancer ו־Promoter חייבים להיות באותו TAD כתנאי בסיסי לפגישה
- קיפול התוך־TAD מאפשר את המגע הפיזי ביניהם ← אקטיבציה
- הפרדה מרחבית (Enhancer בתוך הלולאה, Promoter מחוצה לה) ← סופרסיה
TADs הם דינמיים! בתהליכי דיפרנציאציה ניתן לראות שינויים בתבנית ה־TADs - פתיחה ובנייה מחדש בהתאם לתוכנית הטרנסקריפציה.
מנגנון יצירת TAD - קוהסין ו־CTCF
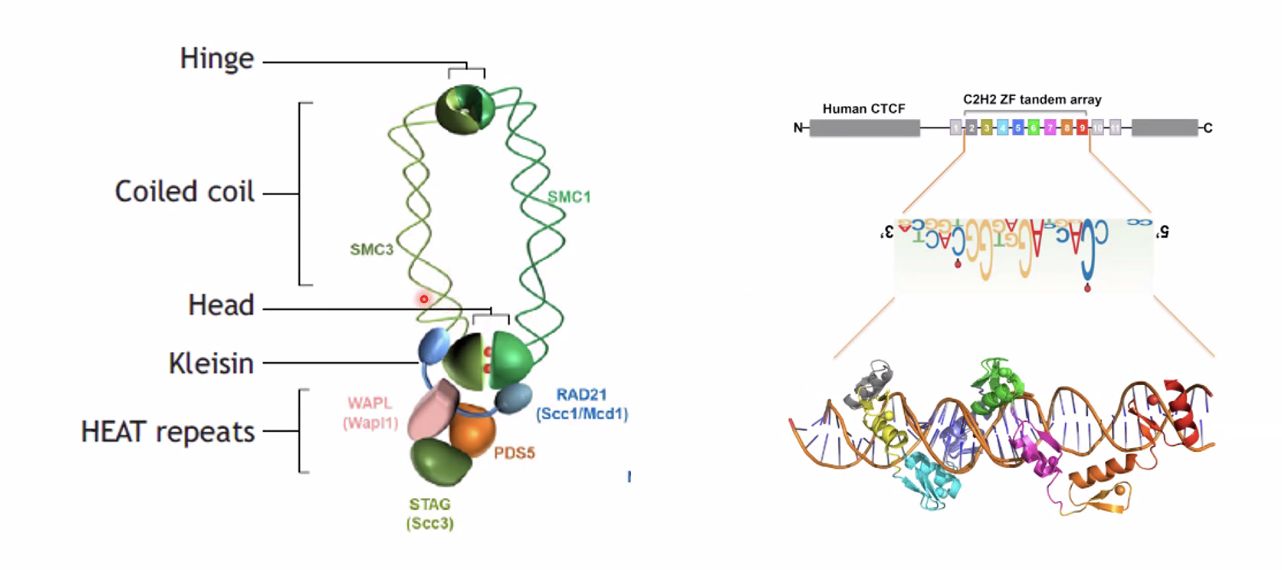
Cohesin ו־CTCF הם שני גורמים מרכזיים בארגון המרחבי של הכרומטין, ובעיקר ביצירת לולאות כרומטין וגבולות של TADs. Cohesin יוצר ומגדיל את הלולאה, ו־CTCF עוצר אותו במקום הנכון ומגדיר את הגבול.
קוהסין (Cohesin) - SMC Complex
- קומפלקס חלבוני בעל מבנה של טבעת - אוחז פיזית בשני גדילי DNA
- פעיל Loop Extrusion: נקשר לDNA באקראי ומושך את הגדילים פנימה ← יוצר לולאה שהולכת וגדלה (בצריכת ATP)
- בלם: עוצר כשפוגש CTCF
CTCF - Sequence-Specific Binding Protein
- נקשר לרצף DNA ספציפי דרך ה־Major Groove
- אלפי אתרי קישור בגנום
- פועל כבלם לקוהסין - אך רק כשהאוריינטציה של שני אתרי CTCF היא הפוכה (convergent orientation ← → )
- אם האוריינטציה זהה, הקוהסין ממשיך לעבור ← TAD גדול יותר
תהליך יצירת TAD
- קוהסין יושב אקראית על ה־DNA
- מתחיל משיכת לולאה (Loop Extrusion)
- פוגש שני אתרי CTCF בכיוון מנוגד ← עצירה
- קוהסין נועל את בסיס הלולאה ← TAD מוגדר
מחלה קלינית - Cornelia de Lange Syndrome (CdLS): פגיעה בתת־יחידות שונות של קוהסין גורמת לשיבוש תוכנית הטרנסקריפציה ההתפתחותית, עם ביטויים של פיגור שכלי, בעיות התפתחות פיזיות ועוד - דוגמה לחשיבות הקלינית של ארגון כרומטין תקין.
קומפרטמנטים A ו־B
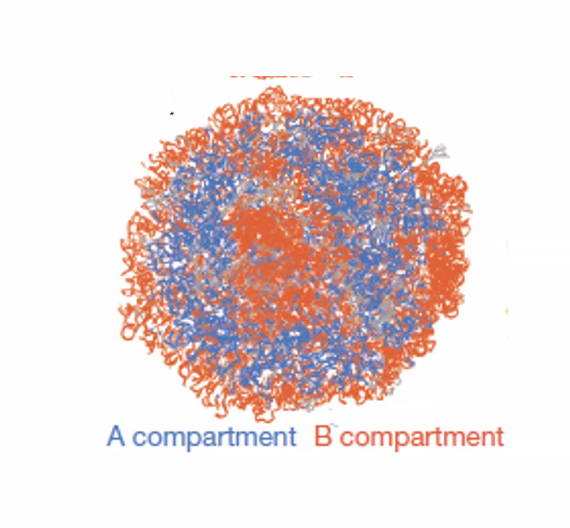
מתוך מפות Hi-C, מעבר לרמת ה־TAD, זוהו שתי קבוצות של TADs שמתקשרות ביניהן אך לא זו עם זו. הגדרה ברמת compartments היא לפי דפוסי אינטראקציה בין קבוצות של TADs ב־Hi-C, לא לפי מה שקורה בתוך TAD יחיד.
A compartment | B compartment | |
|---|---|---|
| מנמוניקה | Active | Blocked |
| פעילות | טרנסקריפציה פעילה | גנים מושתקים |
| מיקום בגרעין | מרכז הגרעין | צמוד לממברנה הגרעינית |
| מקביל ל… | אאוכרומטין | הטרוכרומטין |
כל כרומוזום נמצא גם ב
A compartmentוגם בB compartment- החלק הפעיל שלו במרכז, והחלק הלא־פעיל בפריפריה.
דינמיות קומפרטמנטים
- שינויים בין תאים, בהתאם לסוג התא, גיל, מצב במחזור התא וסיגנלים חיצוניים
- לדוגמה: תא B המופעל על ידי אנטיגן מעביר חלקים ממנו מ
B compartmentל־A ← פתיחת גנים של תגובה חיסונית
טריטוריות כרומוזומליות (Chromosome Territories)
כל כרומוזום תופס טריטוריה ייחודית בגרעין - הכרומוזומים לא שזורים זה בזה. אפילו שני הומולוגים (דיפלואיד) תופסים טריטוריות נפרדות ואינם מתקשרים ביניהם. הארגון הוא תהליך אקראי (לא קבוע בין תאים שונים) ומשתנה בהתאם לסוג התא, מצב ההתפתחות והסיגנלים החיצוניים.
מחזור התא והכרומטין - מעבר אינטרפאזה ↔ מיטוזה
למה צריך לארוז מחדש לכרומוזום מיטוטי?
בדומה לספגטי מבושל - כרומוזומים אינטרפאזיים פרוסים ושזורים זה בזה. ניסיון להפריד אותם בכוח יגרום לשברים פיזיים ולאובדן חומר גנטי. הפתרון: “ייבוש” הספגטי ← מקלות קשיחים (כרומוזום מיטוטי) ← הפרדה קלה וסדורה.
מבנה הכרומוזום המיטוטי - רוזטות ושלד
- פירוק כל מבנה האינטרפאזה (TADs, קומפרטמנטים, CTCF יורד)
- יצירת שלד מרכזי (Scaffold/Axial Core) - בנוי מקונדנסין ומטופואיזומראז II
- סביב השלד - קיפול הכרומטין לרוזטות (לולאות שטוחות, דו־ממדיות)
- הרוזטות מסודרות בשכבות (stacking) לאורך ציר השלד
תוצאה במפת Hi-C
באינטרפאזה - אינטראקציות מרוחקות רבות (TADs, קומפרטמנטים). במיטוזה - כמעט אפס אינטראקציות מרוחקות, רק אינטראקציות קצרות לאורך הציר.
לפי ChatGPAT, באינטרפאזה יש TADs; במיטוזה המבנה הזה בעיקר קורס ומוחלף בארגון דחוס אחר.
קונדנסין - SMC קלאסי של מיטוזה
בן-דוד של הקוהסין, שייך גם הוא למשפחת SMC (Structural Maintenance of Chromosomes). פועל באותו מנגנון של Loop Extrusion, אך יוצר את ארכיטקטורת הרוזטות של הכרומוזום המיטוטי.
שלושת חברי משפחת SMC:
- קוהסין - TADs באינטרפאזה + חיבור כרומטידות אחיות במיטוזה
- קונדנסין - קונדנסציה מיטוטית
- SMC5/6 - רפליקציה ותיקון DNA
קוהסין ובדיקת ה־Checkpoint המיטוטי
תפקיד קוהסין בסגרגציה
- מחבר פיזית כרומטידות אחיות (מ־S phase ועד מיטוזה)
- יוצר כוח נגדי למיקרוטובולי הספינדל - מה שמאפשר קישור ביפולרי (כל כרומטידה נמשכת לכיוון אחר)
- מתח מכני ← פעילות פוספורילציה/דה־פוספורילציה ← זיהוי קישור תקין
- השחרור של קוהסין מהזרועות (בפרומטפאזה) ולאחר מכן מהצנטרומר (בתחילת אנפאזה) ← סגרגציה
Ki-67 - חלבון מעטפת כרומוזומי
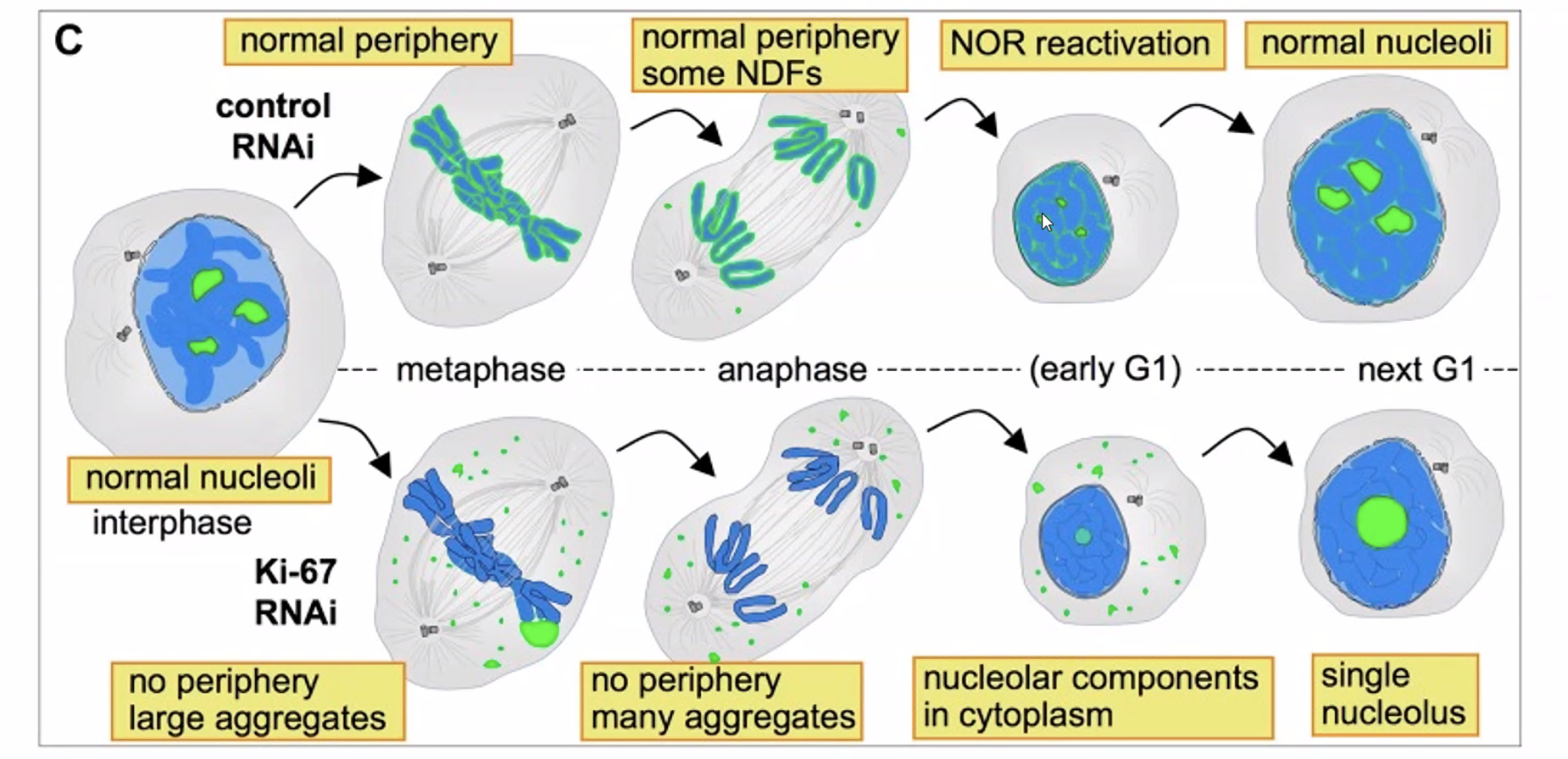
Ki-67 הוא חלבון הנקשר לאורך כל הכרומוזום המיטוטי ומצפה אותו.
מנגנון: מטען חשמלי חיובי על פני הכרומוזום ← דחייה אלקטרוסטטית בין כרומוזומים ← שמירה על הפרדה פיזית בין הכרומוזומים (שמירת טריטוריות, מונע אגרגציה של הכרומוזומים).
מה קורה ללא Ki-67?
- הסגרגציה המיטוטית תקינה!
- אך: לאחר המיטוזה, בכניסה ל־G1, במקום מוקדי התחלת טרנסקריפציה מרובים - מוקד אחד בלבד ← הפעלה לא תקינה של תוכנית הטרנסקריפציה.
- ← Ki-67 חיוני לשחזור תקין של תוכנית הטרנסקריפציה לאחר חלוקה.
חשיבות קלינית: מרקר לקביעת גידול של תאים
Ki-67 הוא סמן פרוליפרציה - בביופסיות סרטניות, צביעה ל־Ki-67 מאפשרת לכמת כמה תאים ברקמה נמצאים במיטוזה ← מדד לקצב חלוקת התאים הסרטניים.
אם כל החלבון ki67 בתא יפורק, מה יקרה לכרומוזומים בשלב המיטוזה?
- הם יפרדו אחד מהשני
- הם ייצמדו אחד לשני
- הם ינדדו לכיוון ממברנת התא ויצמדו אליה
תשובה
2. הם ייצמדו אחד לשני - ללא Ki-67, הכרומוזומים המיטוטיים יאבדו את ההפרדה הפיזית ביניהם וייצמדו זה לזה. הסגרגציה המיטוטית עצמה תתבצע (סגרגציה תקינה!), אך לאחר המיטוזה, בכניסה ל־G1, יופעל מוקד טרנסקריפציה אחד בלבד במקום רבים, מה שיגרום להפעלה לא תקינה של תוכנית הטרנסקריפציה בתא הבת.
סיכום היררכיית ארגון הכרומטין
DNA + נוקלאוזומים ("חרוזים על חוט")
↓
לולאות TAD
[Cohesin + CTCF] (~1 Mb)
↓
קומפרטמנטים A/B
[אקטיבי/מושתק; מרכז/פריפריה]
↓
טריטוריות כרומוזומליות
↓
(במיטוזה בלבד)
כרומוזום מיטוטי
[Condensin + Topo II + Scaffold + Rosettes]