נושאים:
- למה ביולוגיה מולקולרית?
- הדוגמה המרכזית - Central Dogma
- היסטוריה קצרה של גילוי ה־DNA
- מבנה ה־DNA
- הכוחות שמחזיקים את ה־DNA ביחד
- RNA לעומת DNA
- צורות ה־DNA - B, A, Z
- מבנים מיוחדים של DNA
- ביוטכנולוגיה - חיתוך וחיבור DNA
למה ביולוגיה מולקולרית?
ברפואה מקובל להסתכל על הדברים בצורה הוליסטית - על הדם, על הגוף, על המערכות. הביולוגיה המולקולרית דוגלת בגישה הפוכה: היא נוברת בגדול כדי להבין את החלקים הקטנים שמניעים אותו. ובכל זאת, בדיוק בגלל זה היא חיונית לרפואה - כי המולקולות הן מה שמכתיב את הכל. כשהן משתבשות, כמו במחלה גנטית שיש בה שינוי זעיר ב־DNA, ההשפעה על הפיזיולוגיה רחבה.
ביולוגיה מולקולרית מוגדרת כענף של הביולוגיה שמנסה להבין את הבסיס המולקולרי של הפעילות הביולוגית - בתוך התא ובין תאים. זה כולל סינתזה של ביומולקולות, מודיפיקציות שלהן, מכניזמים ואינטראקציות בין מולקולות.
הקורונה כדוגמה: ריצוף גנטי איפשר לזהות את מקור הנגיף ולעקוב אחר המוטציות שצבר. בדיקות ה־PCR הן אחת ההמצאות הגדולות של הביולוגיה המולקולרית במאה ה־20. חיסון ה־mRNA מבוסס על הבנה מעמיקה של זרימת מידע בתוך התא.
הדוגמה המרכזית - Central Dogma
פרנסיס קריק תיאר ב־1957 ופרסם ב־1958 את הדוגמה המרכזית של הביולוגיה המולקולרית: זרימת המידע בתוך התא היא מ־DNA ל־RNA לחלבון.
האם היא תמיד נכונה? לא לגמרי. כיום, הדוגמה המרכזית מורכבת יותר:
- מ־RNA לחלבון ל־DNA - רטרווירוסים (כמו HIV) יודעים לעשות רוורס טרנסקריפציה ולהעביר RNA חזרה ל־DNA.
- חלבונים יכולים להשפיע על ה־DNA - למשל מתילציה של DNA, שהיא חותמת אפיגנטית שמשנה את התפקוד שלו ללא שינוי הרצף.
- RNA יכול לפעול כמו חלבון - ריבוזימים הם RNA קטליטי, שיודע לעשות קטליזה ביוכימית כמו אנזים, ממש כמו חלבון.
- RNA יכול להשפיע על DNA - למשל XIST, שאחראי להשתקת אחד מכרומוזומי ה־X אצל נשים, הוא מולקולת RNA שנקשרת ל־DNA ומשתיקה אותו.
היסטוריה קצרה של גילוי ה־DNA
כבר ב־1869 זוהה חומר בגרעין התא, שנקרא אז “נוקלאין”. ב־1919 זוהו מרכיביו (פוספט, סוכר, בסיסים חנקניים). ב־1950 גילה צ’רגף את חוקיות הבסיסים: |A|=|T| ו־|G|=|C|. וב־1953 ווטסון וקריק פרסמו את המבנה הדו־גדילי.
סיפור רוזלינד פרנקלין: הנרטיב הפופולרי - שפרנקלין גילתה את המבנה ו”גנבו לה” את התוצאות - כנראה לא מדויק מבחינה היסטורית. פרנקלין עבדה בקינגס קולג’ ולקחה מאות תמונות קריסטלוגרפיה, ביניהן תמונה 51 - תמונת פיזור האלקטרונים של DNA. היא שמה אותה בצד כי ככל הנראה לא עניינה אותה. לאחר שעזבה את המעבדה, הנחה וילקינס סטודנט לחלוק את התמונה עם ווטסון וקריק. ווטסון זיהה מיד את החשיבות שלה, כיוון שהיא התאימה למודל התיאורטי שקריק פרסם. פרנקלין תרמה תרומה משמעותית - אך הסיפור מורכב יותר ממה שנהוג לספר.
מבנה ה־DNA
אבני הבניין
ה־DNA הוא פולימר ליניארי - מולקולה שמורכבת מיחידות חוזרות. היחידה הבסיסית היא דאוקסיריבונוקלאוטיד טריפוספט (dNTP), שמכיל שלושה אלמנטים:
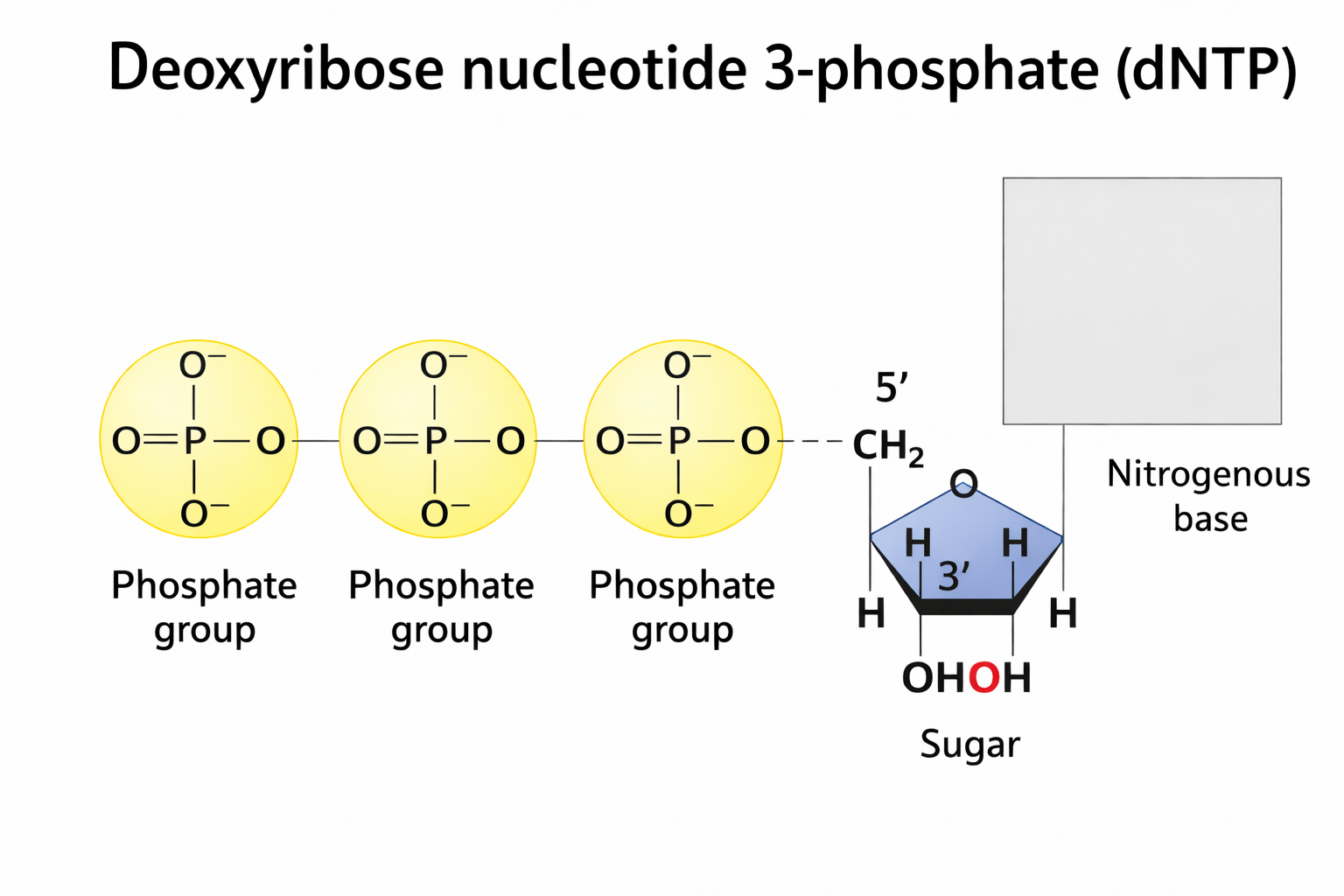
-
הסוכר - דאוקסיריבוז: טבעת מחומשת עם חמישה פחמנים (1’–5’). ההבדל בין ריבוז (ב־RNA) לדאוקסיריבוז (ב־DNA): בריבוז יש קבוצת הידרוקסיל (OH) על פחמן 2’, ב־דאוקסיריבוז יש שם רק H.
גם ל־DNA וגם ו־RNA יש קבוצת הידרוקסיל על פחמן 3’ - זה הכרחי כדי ליצור את הקשר הפוספודיאסטרי. ל־RNA יש בנוסף לכך גם OH על פחמן 2’ (סך הכל יש ל לו הידרוקסיל על פחמנים 2 ו־3).
-
קבוצות הפוספט: שלוש קבוצות פוספט הקשורות לפחמן 5’. הקשרים בין קבוצות הפוספט הם קשרים עתירי אנרגיה - האנרגיה הדרושה לסינתזת ה־DNA טמונה בתוך אבן הבניין עצמה, ולא מגיעה ממקור חיצוני.
-
הבסיס החנקני: יושב על פחמן 1’. יש ארבעה בסיסים, שמחולקים לשתי משפחות:
- פירימידינים (טבעת משושה אחת): ציטוזין (C) ותימין (T)
- פורינים (טבעת משושה + טבעת מחומשת): אדנין (A) וגואנין (G)
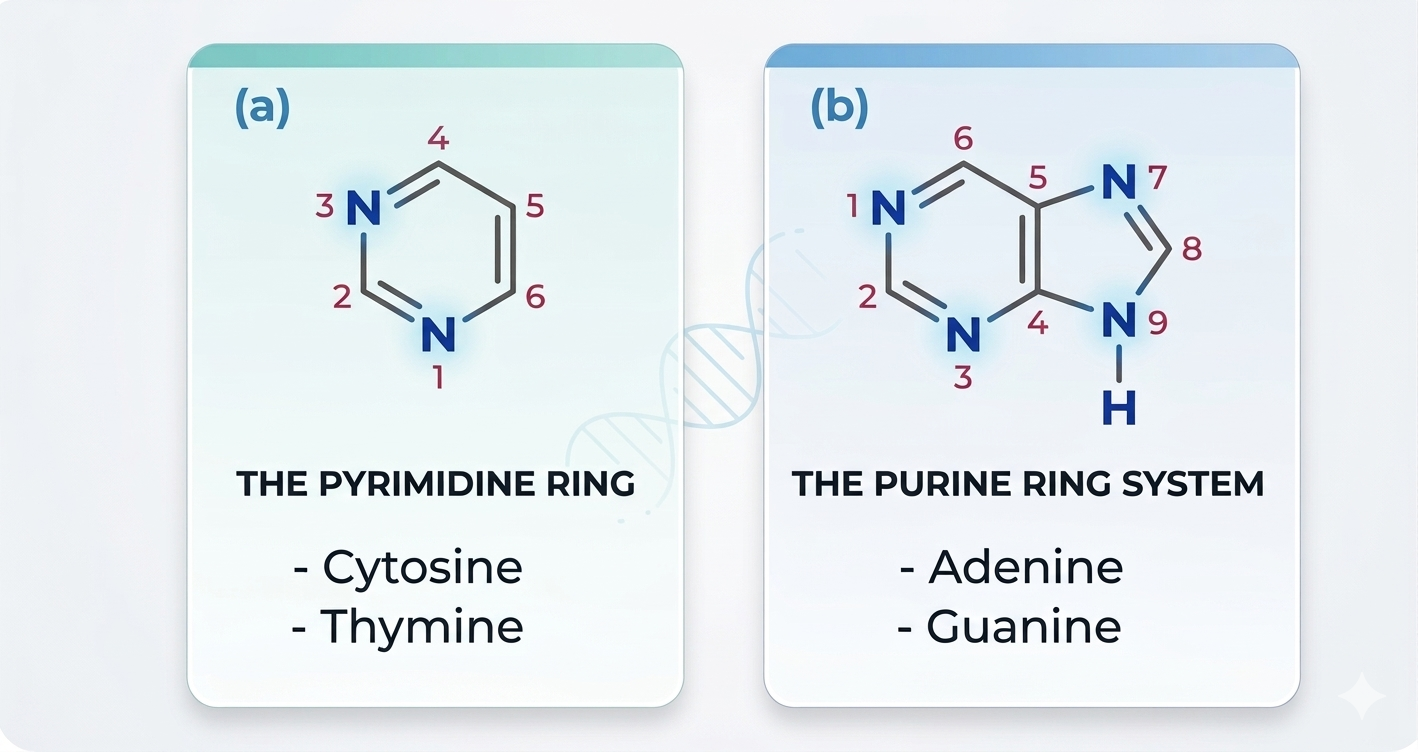
טיפ שראיתי באוסמוזיס לזכירת החלוקה:
CUT PY (pyrimidines) - Cytosine, Uracil, Thymine are the pyrimidines.
זיווג הבסיסים וקשרי מימן
כששני בסיסים מתקרבים מספיק - סדר גודל של כ־2.5 אנגסטרום - נוצרים ביניהם קשרי מימן. הזיווג הוא ספציפי: A עם T (שני קשרי מימן), G עם C (שלושה קשרי מימן).
זיווג G-C חזק יותר לא מפני שכל קשר בפני עצמו חזק יותר - כל קשר מימן הוא אותו קשר - אלא פשוט מפני שיש שלושה קשרים לעומת שניים.
דבר נוסף: זיווג בסיסים יוצר מישור פלנרי - הטבעות של שני הבסיסים נמצאות במישור אחד, אחד מול השני. ועוד: למרות שבין A-T יש שני קשרים ובין G-C יש שלושה, שניהם יוצרים בערך אותו מבנה מרחבי - עובדה קריטית לבניית הפולימר.
בניית הפולימר - כיווניות 5’←3’
הפולימר בנוי בכיוון 5’ ל־3’: הבסיס החדש מצטרף על ידי התקפה נוקלאופילית של ה־OH שנמצא על פחמן 3’ של הנוקלאוטיד האחרון, על קבוצת הפוספט של הנוקלאוטיד הנכנס, תוך שחרור דיפוספט ויצירת קשר פוספודיאסטרי חדש. הקשר הזה - בין החמצן לפוספט לחמצן - הוא מה שמחבר את כל הנוקלאוטידים בשרשרת.
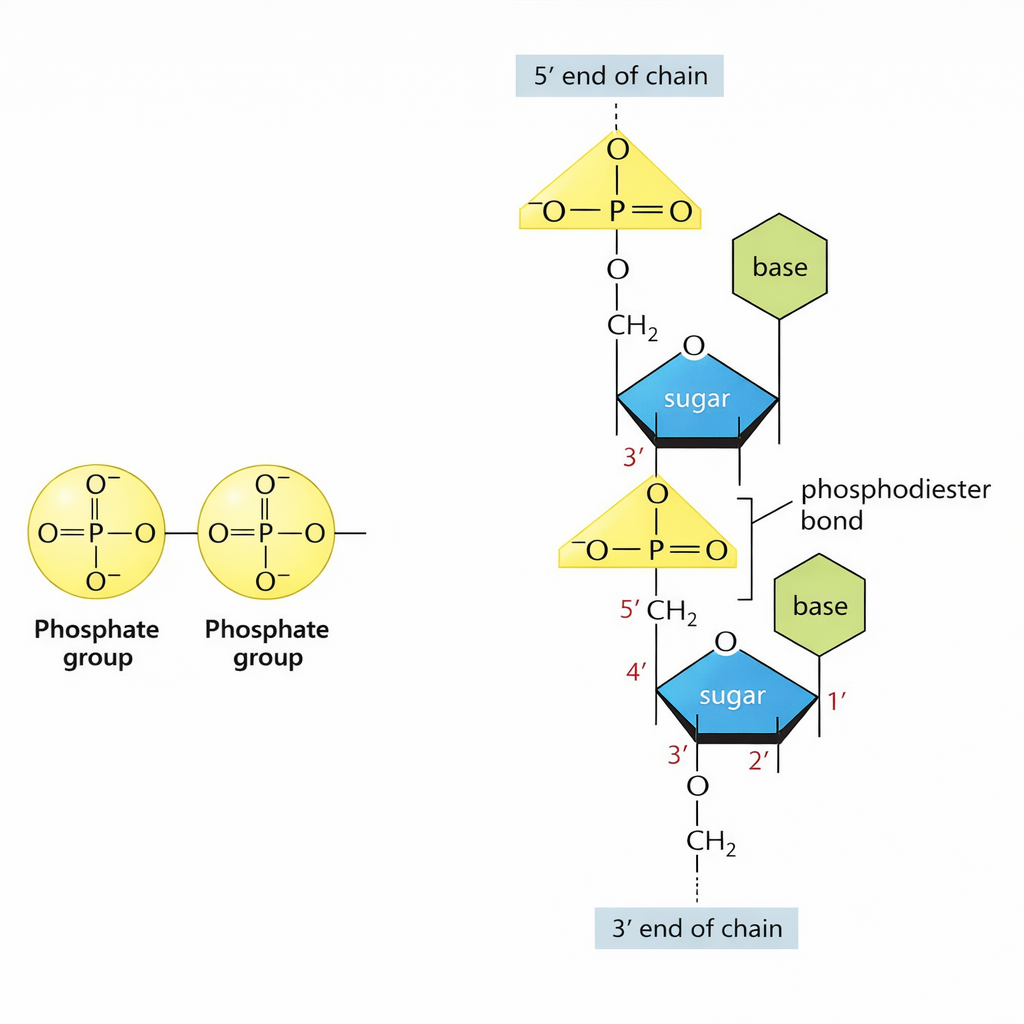
מה שנוצר הוא שלד פוספוסוכרי שמהווה את “עמוד השדרה” של המולקולה.
הדו־גדיל - Anti-parallel Double Helix
ה־DNA הדו־גדילי בנוי משני פולימרים ליניאריים נפרדים, מסודרים אנטי-פרללית: אחד הולך 5’←3’ בכיוון אחד, והשני 5’←3’ בכיוון ההופכי.
השלד הפוספוסוכרי נמצא מבחוץ, הבסיסים החנקניים מבפנים. ההיגיון הביולוגי ברור: אם פגיעה מגיעה מבחוץ, היא תיתקל קודם בשלד. השלד קל לתיקון כי הוא נראה אותו הדבר לאורך כל המולקולה - אין צורך ב”מידע” מיוחד לתיקון. מה שקשה לתקן הוא הבסיסים בפנים, כי שם האינפורמציה הגנטית.
למה נוצר הסליל? הפולימר הוא ליניארי, אך מבחינה אנרגטית לא ״נוח לו״ להישאר ישר - הקשר הפוספודיאסטרי נוטה באופן טבעי לזווית מסוימת. כל בסיס מוסיף סיבוב של בערך 36 מעלות, ולכן בערך כל 10.5 בסיסים יש לנו סיבוב שלם. הסיבוב הוא ימני (עם כיוון השעון) - זהו ה־B-DNA הקלאסי.
Major Groove ו־Minor Groove
כתוצאה מהסליל הזה נוצרים שני חריצים: ה־Major Groove (רחב ועמוק) וה־Minor Groove (צר ושטוח). למה הם חשובים?
הדרך שבה חלבונים “קוראים” את המידע הגנטי שנמצא פנימה בתוך הגליל היא דרך הגרוב. מבחוץ, מהשלד הפוספוסוכרי, הכל נראה אותו דבר מתחילת המולקולה ועד סופה. כדי להציץ פנימה ולזהות איזה בסיסים יושבים מול מי - כדי “לקרוא” את הרצף - חלבונים כמו גורמי שעתוק משתמשים בגרוב כחלון. רוב החלבונים משתמשים ב־Major Groove כי הוא רחב ועמוק יותר ואפשר לראות דרכו הרבה יותר טוב. אבל יש חלבונים שנכנסים גם ל־Minor Groove.
תיקון DNA: חלבונים שסורקים נזקי DNA עוברים לאורך השלד הפוספוסוכרי ומחפשים אנומליות במבנה - כמו קטר שרץ על מסילה ומחפש עיוות. ברגע שמזהים עיוות, מערכת התיקון מציצה פנימה דרך הגרוב כדי להבין מה השתבש ואיך לתקן.
הכוחות שמחזיקים את ה־DNA ביחד
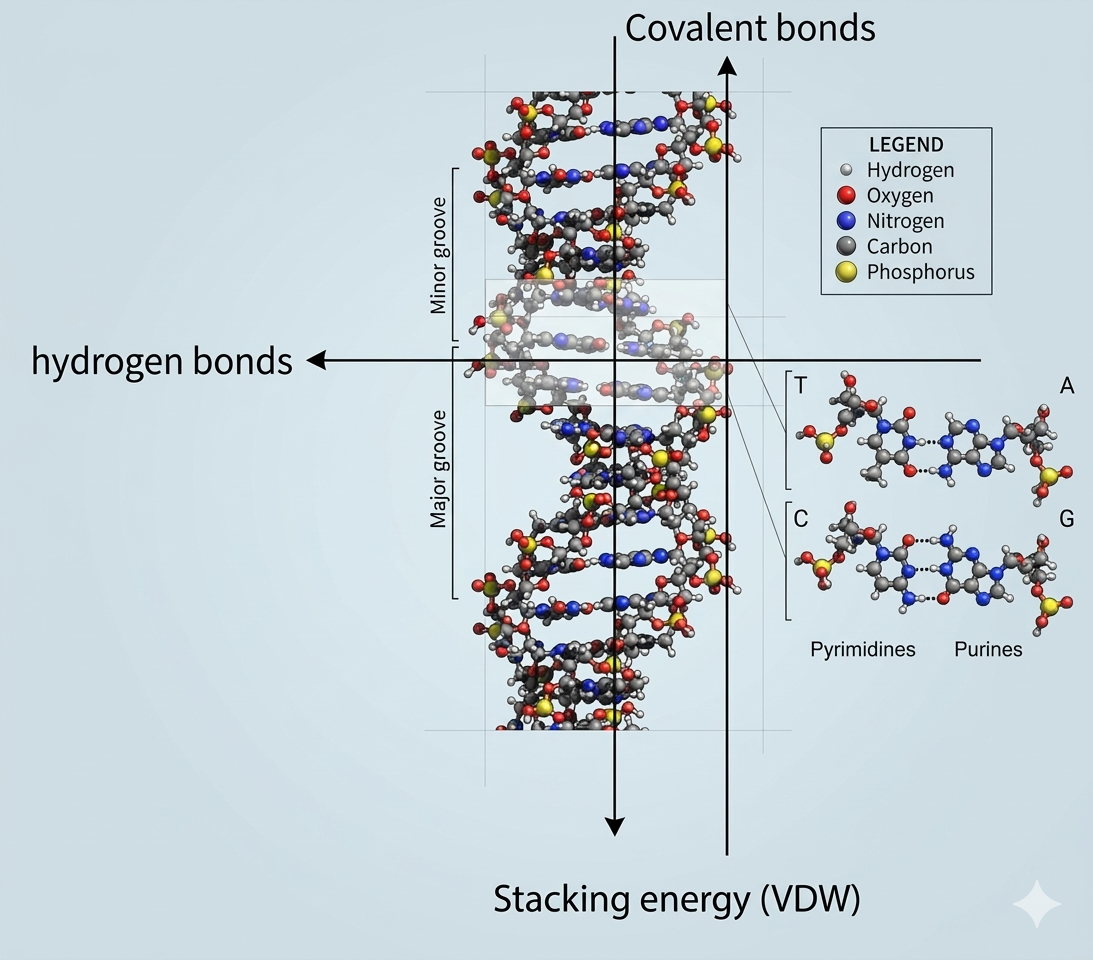
שלושה סוגי כוחות מחזיקים את מולקולת ה־DNA:
-
קשרים קוולנטים - הקשרים הפוספודיאסטריים בשלד הפוספוסוכרי. הקשר החזק ביותר שאנחנו מכירים בטבע.
-
קשרי מימן - בין הבסיסים המזווגים (A-T, G-C). אלה הכוחות שמחזיקים את שני הגדילים ביחד.
-
Stacking energy - כוח ואן-דר-ואלס שנוצר בין הטבעות הארומטיות של הנוקלאוטידים שנמצאים אחד מעל השני, כמו מדרגות בסולם. ככל שהמולקולה ארוכה יותר - כוח הסטאקינג גדול יותר. זה הכוח שנוצר בין הבסיסים שבאותו גדיל, ולא בין הגדילים.
הנקודה הכי פחות יציבה: הקצוות של המולקולה - שם לנוקלאוטידים הקיצוניים אין שכנים מצד אחד, ולכן אין סטאקינג מצד אחד. לכן הקצוות הם הנקודות שבהן ה־DNA “נושם” - נפתח ונסגר באופן ספונטני. התהליך הזה רלוונטי לתיקון DNA: שבר בגדיל אחד גורם לאזור ה־DNA הסמוך להפוך לפחות יציב ולהתחיל להיפרד.
Melting Temperature - Tm
אם מחממים DNA מספיק, קשרי המימן וה־stacking energy נשברים (לא הקשרים הקוולנטים!) והמולקולה עוברת ממצב דו־גדילי למצב חד־גדילי - זהו denaturation (היתוך). ה־Tm (Melting Temperature) היא הטמפרטורה שבה 50% מהמולקולות עברו היתוך.
DNA עשיר ב־G/C יעבור היתוך בטמפרטורה גבוהה יותר מ־DNA עשיר ב־A/T - פשוט כי שלושה קשרי מימן חזקים יותר משניים.
היברידיזציה - Hybridization
אחרי שהפרדנו דו־גדיל לשני חד־גדילים, מה קורה כשמקררים? שני החד־גדילים מוצאים אחד את השני באופן ספונטני, יוצרים גרעין של זיווג בסיסים, והגרעין גדל עד שהמולקולה חוזרת למצב הדו־גדילי. התהליך הזה נקרא היברידיזציה, והוא ספונטני - לא צריך אנרגיה, להפך, אנרגיה משתחררת בתהליך.
ה־DNA בתוך התא הוא מולקולה דינמית: כל הזמן נפתחת ונסגרת - לשם רפליקציה, טרנסקריפציה ותיקון. אחרי שתהליך כלשהו מסתיים, המולקולה שואפת תמיד לחזור למצב האנרגטי היציב ביותר - המצב הדו־גדילי.
יישומים קליניים: היברידיזציה משמשת בבדיקות FISH (Fluorescence In Situ Hybridization) לזיהוי כרומוזומים ספציפיים, ב־Microarray לזיהוי מוטציות, ובטכנולוגיות ריצוף (Sequencing) מודרניות.
RNA לעומת DNA
שתי המולקולות נמנות עם חומצות גרעין (Nucleic Acids), ומה שמשותף להן - שלד פוספוסוכרי, כיווניות 5’←3’, פולימר ליניארי. ההבדלים:
-
ריבוז במקום דאוקסיריבוז: לריבוז יש קבוצת OH על פחמן 2’, מה שהופך אותו לריאקטיבי יותר ופחות יציב - בדיוק מה שאנחנו רוצים מ־RNA, שהוא מולקולה זמנית. ה־DNA שאנחנו נושאים לכל החיים ומורישים לדור הבא צריך מקסימום יציבות - לכן דאוקסיריבוז.
-
אורציל (U) במקום תימין (T): לאורציל חסרה קבוצת מתיל שיש לתימין (תימין הוא בעצם אורציל עם קבוצת מתיל נוספת בעמדה 5 של הטבעת). מדוע?
-
ראשית, ציטוזין (C) יכול לעבור דמינציה - לאבד את הקבוצה האמינית ולהפוך לאורציל (U). אם אורציל נמצא ב־DNA, מערכת התיקון תדע שמשהו השתבש - כי ב־DNA לא אמור להיות U. מערכות תיקון מסוגלות לזהות זאת ולהחליף ל־C. אבל אם ה־DNA היה משתמש ב־U במקום ב־T, לא הייתה דרך לדעת אם ה־U שנמצא שם תקין (T מקורי) או מוטציה (C שעבר דמינציה). ה־T עם קבוצת המתיל מאפשר לנו להבדיל.
-
מולקולת U קלה יותר לסינתזה (לפי שאלות החזרה)
-
T תורם לקשיחות המבנית של ה־DNA
-
-
חד־גדילי לעומת דו־גדילי: ה־RNA הוא בדרך כלל חד־גדילי (אם כי יכול להתקפל ולצור אזורים דו־גדיליים עם עצמו).
צורות ה־DNA - B, A, Z
-
B-DNA: הצורה הקלאסית, הנפוצה ביותר בתנאים פיזיולוגיים. סיבוב ימני, כ־10.5 בסיסים לסיבוב.
-
A-DNA: נוצר כשמוציאים מים מה־B-DNA. הוא “מעוך” - רחב ונמוך יותר. גם לו סיבוב ימני.
-
Z-DNA: מבנה שונה לחלוטין - סיבוב שמאלי. יוצר תצורת זיגזג (ולכן “Z”). פעם חשבו שהוא רק מעבדתי - כיום יודעים שהוא קיים בתוך התאים באופן טבעי ויש לו תפקידים ביולוגיים, אם כי לא מובנים לגמרי.
מבנים מיוחדים של DNA
R-Loop
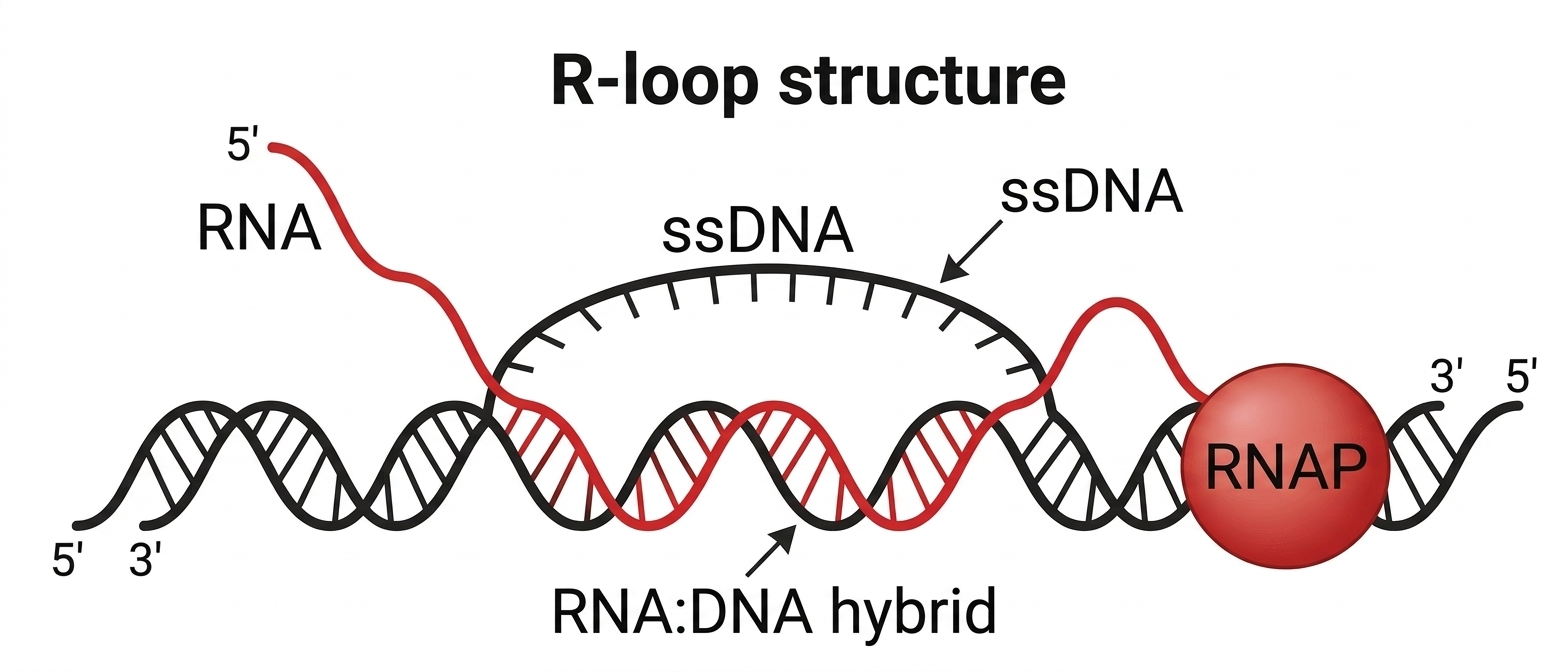
R-Loop נוצר באופן טבעי במהלך טרנסקריפציה. בתהליך הטרנסקריפציה, הדו־גדיל נפתח, וה־RNA פולימראז יוצר גדיל RNA על גבי אחד מגדילי ה־DNA. נוצר מבנה היברידי של גדיל DNA + גדיל RNA, בזמן שהגדיל השני של ה־DNA נמצא חשוף כחד־גדיל - זהו ה־R-Loop. החשיפה של גדיל ה־DNA מסוכנת: בסיסים חשופים חשופים לנזקים כימיים שונים כמו דמינציה. R-Loops רלוונטיים גם לתיקון DNA.
Stem-Loop / Hairpin
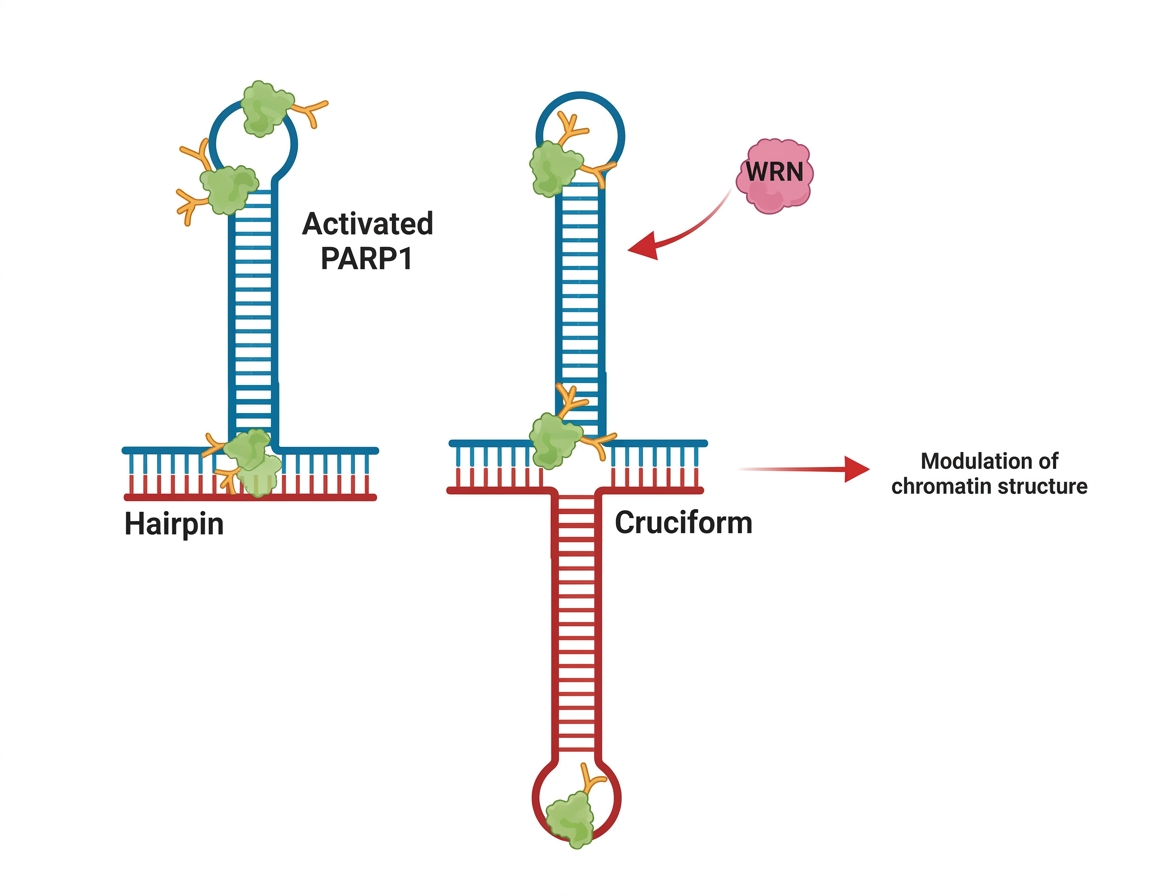
כשיש רצפים חוזרים (חזרות) בגנום, גדיל חד־גדילי יכול ליצור זיווג בסיסים עם עצמו במקום עם הגדיל המשלים - וליצור מבנה של ״לולאה״-ו״גבעול״. כאשר ה־DNA פולימראז פוגש מבנה כזה, הוא עלול לדלג עליו - ולגרום להתארכות או להתקצרות של רצף החזרות.
מחלות גנטיות של חזרות: הפרג’ל איקס (Fragile X) והנטינגטון הן מחלות שבהן רצפים חוזרים מתארכים לאורך הדורות, בגלל מבנים כאלה שנוצרים במהלך רפליקציה.
Triplex DNA
גדיל חד־גדילי (כמו זה שנחשף ב־R-Loop) יכול לחדור לתוך דו־גדיל DNA אחר וליצור מבנה תלת־גדילי. יש לזה חשיבות בתהליך תיקון שברים דו־גדיליים: הגדיל החד־גדילי משמש לחיפוש רצף הומולוגי ברחבי הגנום - כחלק ממנגנון תיקון שנקרא Homologous Recombination.
G-Quadruplex (G4)
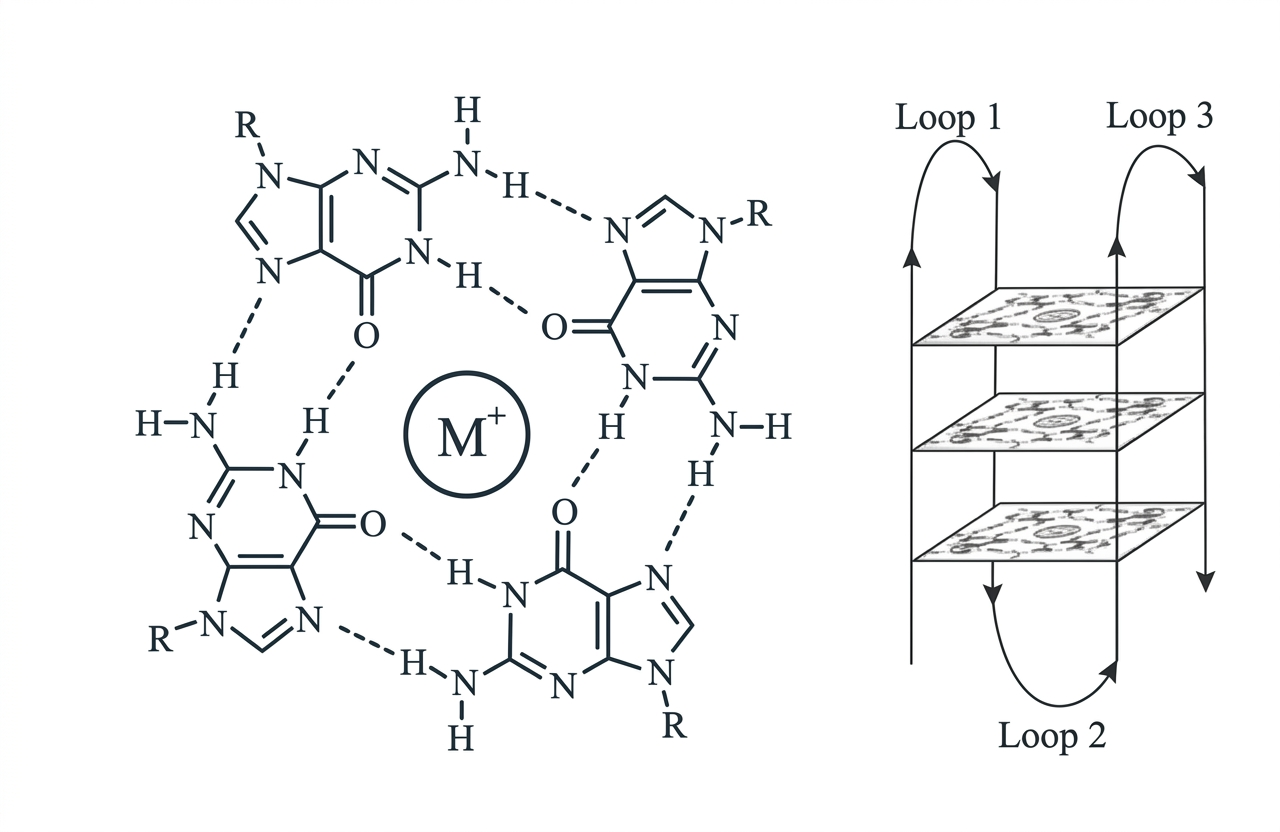
מבנה ארבעה־גדילי הנוצר כאשר ארבעה גואנינים (G), שנמצאים באותו מישור, יוצרים ביניהם קשרי הוקסטיין (Hoogsteen base pair) - קשרי מימן מיוחדים בין ארבעה גואנינים. המבנה הזה יציב ביולוגית. לאורך שנים חשבו שהוא תיאורטי, אחר כך שהוא מעבדתי בלבד. כיום, יודעים שהוא קיים בתוך התאים, בייחוד בטלומרים (קצות הכרומוזומים) ובאזורים נוספים, ושיש לו תפקידים ביולוגיים.
ביוטכנולוגיה - חיתוך וחיבור DNA
נוקלאזות
נוקלאז הוא שם כללי לחלבון שיודע לחתוך את השלד הפוספוסוכרי. יש שני סוגים:
-
אקסונוקלאז - חותך מהקצה (מקצה 3’ או מקצה 5’, תלוי בסוג).
-
אנדונוקלאז - חותך באמצע הרצף.
אנזימי רסטריקציה - Restriction Enzymes
סוג מיוחד של אנדונוקלאזות שהם סיקוונס-ספציפיים - חותכים רק ברצף מוגדר. לדוגמה, EcoRI מזהה את הרצף GAATTC ויחתוך בו בכל מקום שהוא מופיע לאורך המולקולה. האנזים נכנס דרך ה־Major Groove כדי לזהות את הרצף, ואז מבצע חיתוך בשני הגדילים.
שני סוגי חיתוך:
- Blunt end — חיתוך ישר של שני גדילי ה־DNA באותו מקום, ולכן מתקבלים קצוות קהים.
- Sticky end — חיתוך מדורג (staggered cut), שבו שני הגדילים נחתכים במיקומים שונים, ולכן מתקבלים קצוות חד־גדיליים בולטים.
הקצוות הדביקים יכולים לעבור היברידיזציה ספונטנית עם מקטע DNA אחר שנחתך באותו אנזים, ועיקרון זה עומד בבסיס ה־cloning הגנטי.
ליגאז - Ligase
לאחר שחיברנו שני מקטעי DNA, יש צורך לסגור את השלד הפוספוסוכרי. לשם כך משתמשים בליגאז - אנזים שסוגר קשרים פוספודיאסטריים. לא כמו בסינתזת ה־DNA שאנרגיה טמונה בנוקלאוטיד, כאן הנוקלאוטידים כבר “הוצאו” - לכן הליגאז מפרק ATP ומשתמש באנרגיה שלו לסגירת הקשר.
שיבוט גנטי (Genetic Cloning)
תהליך השיבוט: חותכים מקטע DNA עם אנזים רסטריקציה, חותכים פלסמיד (מולקולת DNA מעגלית ממיקרואורגניזם) עם אותו אנזים - ואז מערבבים. הקצוות הדביקים ייצרו היברידיזציה ספונטנית, ולאחר מכן ליגאז יסגור את הקשר. כך מכניסים “בצורה מכוונת” מקטע DNA ספציפי לתוך פלסמיד.
דור פסקלמוטציה בליגאז: אם הליגאז לא עובד כמו שצריך, לא ניתן לתקן שברים ב־DNA. כשה־DNA לא מתוקן, מצטברות מוטציות. צבירת מוטציות - בייחוד במנגנוני הבקרה על חלוקת תאים - היא מה שמוביל לסרטן. סרטן הוא מחלה של אי־יציבות גנטית.