חזקים בהובלות?
נסו 10 שאלות בנושא, עם עדיפות לשאלות שלא הצלחתם. בסיום תקבלו ציון וסקירה על הטעויות שלכם. הצלחתם? גלו בחנים בדפים נוספים
תוצאות המבחן
היסטוריית מבחנים
טוען את השאלות...
אנא המתן...
הרצאה 11: טרנספורט לגרעין (המשך)
מבוא והכוונה כללית
הדיון חוזר לנושאים שנדונו בסוף ההרצאה הקודמת, לשם הבהרה וחזרה. לאחר המעבר מכימיה אורגנית לביולוגיה של התא, הנושא הנוכחי הוא כניסה לגרעין.
רקע כללי - הכוונת חלבונים במדורים
חלק זה מסכם את הרצאה 11 ועובר להרצאה 12.
באופן כללי, הנושא המרכזי הוא הכוונה של חלבונים למדורים השונים בתא האיקריוטי. סדרת ההרצאות נועדה לספק תמונה כללית של האופן שבו תאים אוקריוטיים מבצעים את עיקרון “הפרד ומשול” — הכוונת חלבונים למדורים השונים וגם אל מחוץ לתא.
במקרה זה, הדיון מתמקד בכניסה לגרעין.
נקבוביות הגרעין (Nuclear Pore Complexes)
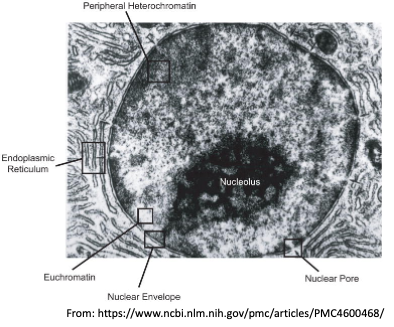
העקרונות המרכזיים, שכבר הוצגו, כוללים את הנוקלאר פור קומפלקסים (NPC), שהם שערים ענקיים במעטפת הממברנה הכפולה של הגרעין.
מאפיינים של השערים הגרעיניים
- לא מדובר בתעלות יונים, שהן קטנות משמעותית ביחס לשערים הענקיים האלה.
- אף על פי שתמונות ממיקרוסקופ אלקטרונים עשויות להראות תעלה פתוחה, היא אינה פתוחה.
- ההצגה הסכמטית מראה מחסום בררני תלת־ממדי.
המחסום הבררני המולקולרי
בעשורים האחרונים, פוענח במידה רבה מנגנון הפעולה של מבנה זה. מבלי להיכנס לפרטים ביוכימיים מתקדמים, המנגנון מבוסס על חזרות של שתי חומצות אמינו:
- פנילאלנין: חומצת אמינו עם שרשרת צדדית הידרופובית וטבעת ארומטית.
- אלפי עותקים של חומצות אמינו אלה, שהטבעות הארומטיות שלהן יוצרות את המחסום התלת־ממדי הסלקטיבי של הכניסה והיציאה מהגרעין.
מסלולי כניסה לגרעין - קטגוריות שונות
רצפטורים מסיסים ושאטלים מולקולריים
אלפי מולקולות שונות, המכונות “קארגו”, צריכות להיכנס לגרעין ולצאת ממנו, וחלקן אף נעות בשני הכיוונים. נדרש גורם שיתווך את המעבר הסלקטיבי.
מדובר באימפורט רצפטורים, שהם חלק ממשפחה כללית של רצפטורים מסיסים. בניגוד לרצפטורים ממברנליים, import receptors אינם מעוגנים לממברנה ונכנסים ויוצאים בין שני המדורים — הציטופלזמה והגרעין.
קטגוריות של אותות הכוונה לגרעין
הסכמה בתמונה 12.58 בספר מראה כי קיימות קטגוריות שונות של אותות הכוונה לגרעין, ולא רק רצף אחד.
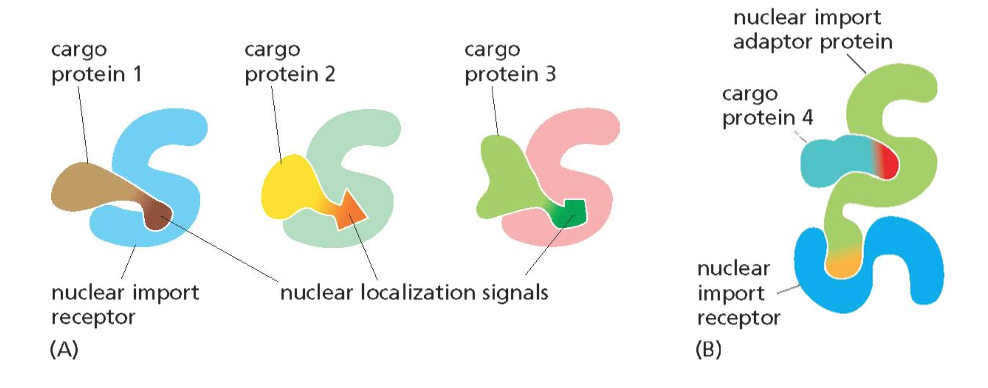
הדוגמה הקלאסית היא NLS (Nuclear Localization Signal):
- רצף של חמש חומצות אמינו טעונות חיובית.
- זהו רק סוג אחד של NLS.
- מאות חלבונים שונים נושאים את רצף ה־NLS לצורך הכוונה לגרעין.
לדוגמה, חלבון הנושא NLS מזוהה על ידי רצפטור מסיס. עם זאת, זוהי רק דוגמה אחת מני רבות. קיימות תת־קטגוריות שונות ומסלולים שונים של כניסה לגרעין, כאשר כל מסלול מתווך על ידי רצפטורים ייחודיים (אימפורטין מסוים).
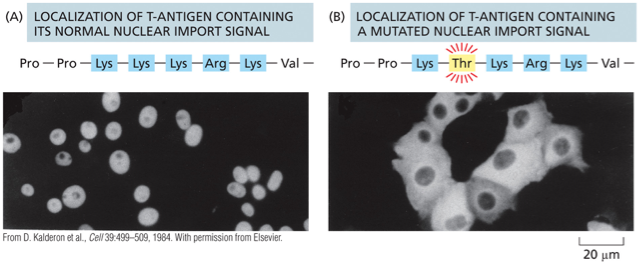
ה־NLS הוא פנימי, בתוך החלבון (ואינו נחתך)
מורכבות המערכת - רספטורים ואדפטורים
המערכת מורכבת אף יותר. הרצפטורים נכנסים ויוצאים, ומכניסים את מטעניהם — במקרה זה, חלבונים שצריכים להיכנס לגרעין.
כל סיגנל מזוהה על ידי רצפטור ייחודי, אך קיימות וריאציות. לעיתים, הרצפטור אינו מזהה ישירות את החלבון, אלא נעזר במתווך (אדפטור). קיימים מסלולים ותת־מסלולים רבים.
דוגמה מפורסמת: אימפורטין α ו־β
הדוגמה המוכרת ביותר (אין צורך לזכור את שמות החלבונים):
- הרצפטור המפורסם ביותר הוא אימפורטין β.
- האדפטור שלו, המתווך, נקרא אימפורטין α.
- בגנום האנושי קיימים שבעה סוגים שונים של אימפורטין α.
כאן נראה שוב עיקרון שכבר הוזכר — חלוקה למסלולים ולתתי-מסלולים.
Importins & exportints - Shuttling transport receptors

היתרונות של חלוקה למסלולים
מה היתרון בחלוקה זו?
החלוקה מאפשרת בקרה. חלוקה למסלולים, תתי-מסלולים וקומבינציות שונות של אימפורט רצפטורים ואדפטורים מאפשרת בקרה דיפרנציאלית על אלפי החלבונים שנכנסים לגרעין. בתאים שונים ותחת מצבים שונים (כגון סטרס, רעב או זמינות מזון), קיימות קבוצות חלבונים שכל אחת מהן מתווכת על ידי רצפטור שייחודי לה.
עקרונות כלליים של התנועה הגרעינית
אותו עיקרון פועל גם ביציאה מהגרעין: יש רצפטורים שמתמחים בהכנסת קארגו (מטענים מולקולריים) לגרעין, ורצפטורים שמתמחים בבהוצאה.
כפי שכבר הוזכר:
- mRNA עטוף בחלבונים צריך לצאת מהגרעין.
- תת־יחידות של הריבוזום צריכות לצאת.
הקארגו אינו בהכרח חלבון בודד, אלא יכול להיות:
- קומפלקס של חלבונים.
- קומפלקס של RNA וחלבון.
נפח התנועה
כל התנועה הזאת מתבצעת בו־זמנית — כניסה ויציאה דרך אותם שערים, אותם נוקלאר פורים.
יתרה מכך, כיום ידוע כי בתא פעיל, בנוקלאר פור אחד יכולים להתרחש מאה אירועים של כניסה ויציאה בו־זמנית.
זהו נפח תנועה עצום, אך כל התנועה הזאת היא תנועה מבוקרת — אין כניסה אקראית לגרעין.
התחלנו מכך שחלבונים צריכים להציג תו כניסה, אישור כניסה — NLS — כדי להיכנס לגרעין.
הבקרה הכללית - חלבון Ran
מבט כללי על המערכת
האם קיימת בקרה כללית על נפח התנועה העצום הזה?
תאים אוקריוטיים לא יכולים לשרוד ללא כניסה ויציאה מבוקרת מהגרעין.
התשובה היא כן, והמנגנון מזכיר נושא שכבר נדון.
מדובר בחלבון Ran, “בן-דוד” של Ras. הוא נחשב “מגניב יותר” כי:
- א) הוא קשור לגרעין.
- ב) הוא לא קשור לסרטן.
משפחת חלבוני GTPase הקטנים
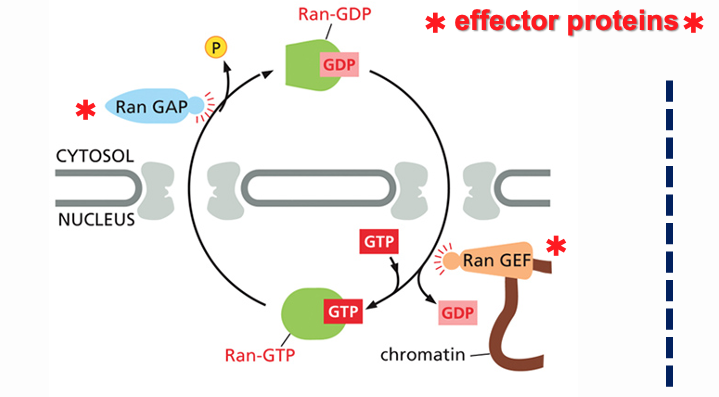
חלבוני GTPase קטנים שייכים למשפחה שלמה שמבקרת תהליכים ביולוגיים רבים. אחד מהם, Ran - הוא חלבון קטן שמבקר את כל מסלולי התנועה הגרעינית.
Ran = Ras-related nuclear protein
עקרון הפעולה של Ran
חלבונים Ran הם מתגים מולקולריים בעלי שני מצבים: ON ו־OFF.
- מצב ON: כאשר Ran קשור ל־GTP (גואנוזין טריפוספט).
- מצב OFF: כאשר Ran קשור ל־GDP (גואנוזין דיפוספט).
כאשר בתוך כיס הנוקלאוטידים קשור GTP — זהו מצב ON. במצב ON חלבון Ran יכול ליצור אינטראקציה עם חלבונים אחרים ולהשפיע על תפקודם.
במצב של GDP הוא ב־OFF.
כמו כל מתג, הוא עובר בין ON ל־OFF.
ההפרדה הייחודית במרחב
במנגנון זה קיימת וריאציה על הנושא: הצורות של GTP ו־GDP מופרדות במרחב התא.
הסכמה מראה:
- בתוך הגרעין, כמעט כל חלבוני Ran נמצאים במצב ON, טעונים ב־GTP. ההבדל הוא של חמישה סדרי גודל — הסיכוי לפגוש מולקולת Ran הקשורה ל־GDP בתוך הגרעין הוא קטן מאוד.
- בציטופלזמה — הפוך - שם כמעט כל מולקולות Ran יהיו במצב GDP (לאחר שאיבדו פוספט אחד).
המנגנון שיוצר את ההפרדה
השאלה נטועה מראש. ל־Ran, כמו לשאר בני משפחתו (כמו Ras), יש חלבוני אפקטור.
מולקולות ה־GTPase הן אנזימים חלשים מאוד. במבחנה, קצב ההידרוליזה של GTP על ידי Ras או Ran הוא איטי ביותר.
חלבוני אפקטור מעלים את קצב ההידרוליזה בכמה סדרי גודל. חלבוני אפקטור אלה ממוקמים:
- מחוץ לנוקלאר פור.
- או בתוך הגרעין.
מיקום זה הוא שיוצר את ההפרדה המרחבית.
שני סוגי האפקטורים
אין צורך לזכור את השמות, אך ראשי התיבות הם:
בצד החיצוני:
- GAP (GTPase Activating Proteins) — חלבונים אלה “דוחפים” את Ran לבצע הידרוליזה ולשחרר פוספט.
בתוך הגרעין:
- חלבון זה (GEF) מוציא את ה־GDP מכיס הקישור ומכניס במקומו GTP.
כלומר, מושקעת אנרגיה במחזור של Ran כדי ליצור הפרדה מרחבית. הפרדה זו מאפשרת להקנות כיווניות לכל מסלולי הטרנספורט שהוזכרו.
מתג זה הוא מעין “מתג-על” המשפיע על עשרות מסלולים של אימפורט ואקספורט (אימפורטינים ואקספורטינים), אם כי לא על כולם.
ההפרדה המרחבית בין שתי הצורות היא המאפשרת לשלוט בכיווניות.
דוגמה קונקרטית - מחזור האימפורט
נבחן דוגמה של אימפורט כדי להבין איך המנגנון פועל. לא נתעמק באקספורט, שפועל בעיקרון דומה.
השקף מראה כיצד הרצפטורים שראינו קודם פועלים ביחס ל־Ran.
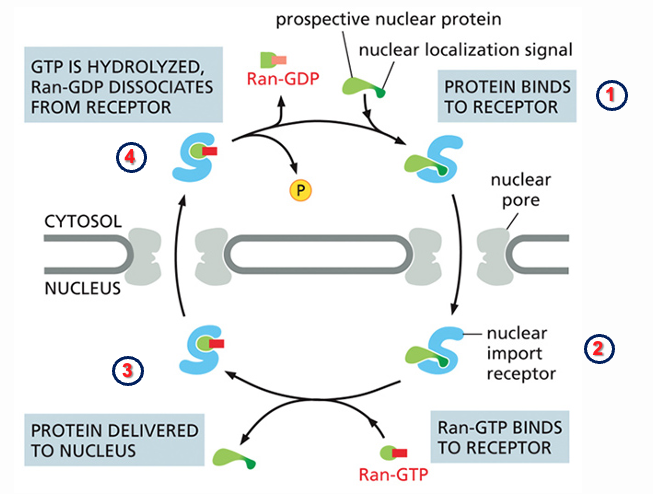
שלבי המחזור
ההסבר מופיע בספר, הוספו מספרים כדי להקל על המעקב.
$\textcolor{green}{Cargo}$ = single protein / protein complex / protein-RNA complex
-
שלב 1: חיבור בציטופלזמה
- החלבון הירוק (קארגו) נושא סיגנל הכוונה לגרעין ונקשר על ידי האימפורט רצפטור (צורת בצבע כחול “S”).
- Ran לא מעורב בשלב זה, מכיוון שבציטופלזמה הוא במצב OFF.
תחילת המסלול מתרחשת ללא מעורבות של Ran.
-
שלב 2: מעבר דרך הנוקלאר פור
- הרצפטור מתווך את המעבר דרך המחסום הסלקטיבי.
- השאטל (הרצפטור - הכחול) נכנס יחד עם המטען שלו.
-
שלב 3: שחרור הקארגו בגרעין (בעקבות קישור הרצפטור ל־Ran)
- בצד הפנימי של הגרעין, הסיכוי לפגוש את Ran במצב ON עולה משמעותית.
- Ran טעון ב־GTP (שלושה פוספטים).
- לרצפטור יש אתר קישור אחד לקארגו ואזור אחר לבקרה אלוסטרית.
- Ran נקשר לאתר השני ברצפטור, גורם לשינוי קונפורמציה ברצפטור ולשחרור הקארגו בגרעין
לכאורה, ניתן היה לעצור כאן, לאחר שהמטרה הושגה.
השלמת המחזור - שלבים 5-4
מדוע נדרשת השלמת המחזור?
הקארגו הובא למדור המטרה, המחסום הסלקטיבי נחצה, והקארגו שוחרר. המטרה הושגה, אך רק פעם אחת.
כדי לצבור חלבון בניגוד למפל הריכוזים במדור היעד (בתוך הגרעין), יש צורך במחזורים רבים. לכן, שלבים 4 ו־5 הם הכרחיים.
-
שלב 4: יציאת הקומפלקס
- כעת, כש־Ran קשור לאימפורט רצפטור, הקומפלקס יוצא החוצה דרך ה־NPC.
- ביציאה מהנוקלאר פור, הוא פוגש את חלבון ה־GAP, הממוקם על הסיבים בצד החיצוני של ה־NPC.
-
שלב 5: הידרוליזה וסיום המחזור
- בשלב זה מתרחשת הידרוליזה של ה־GTP.
- כאשר ה־GTP בכיס של Ran עובר הידרוליזה, פוספט משתחרר, ו־Ran מתנתק.
- האימפורט רצפטור (החלבון הכחול) פנוי כעת להובלה נוספת.
כלומר, השקעת האנרגיה אינה במעבר עצמו, אלא במחזוריות המאפשרת הובלות חוזרות ונשנות.
עקרונות כלליים של המערכת
השקעת האנרגיה
זה עיקרון שחוזר הרבה בביולוגיה. כמו שכבר ראינו:
- חלבוני Ran הם מתגים מולקולריים.
- יש להם שני מצבים: ON (קשור ל־GTP) ו־OFF (קשור ל־GDP).
- השם Ras-related nuclear protein (Ran) מרמז על הקשר למשפחת חלבוני Ras.
במצב ON, Ran יוצר אינטראקציה עם חלבונים אחרים ומשפיע על תפקודם. במצב OFF, הוא אינו פעיל. הצורות השונות (GTP ו־GDP) מופרדות במרחב התא.
תפקיד Ran במערכת - מתג ביולוגי
Ran אינו גורם לתהליך לקרות או לא לקרות, אלא מקנה לו כיווניות.
הקישור הראשוני של הקארגו לרצפטור מתרחש ללא Ran. הרצפטור מזהה אתרי קישור בתוך ה־NPC ומפלס את דרכו פנימה.
התהליך עצמו אינו כיווני במהותו. מטענים בודדים יכולים לנוע פנימה והחוצה. מה שמקנה כיווניות הוא העובדה שבתוך הגרעין, יש סיכוי גבוה שהרצפטור יפגוש מולקולת Ran-GTP, מה שגורם לשחרור הקארגו.
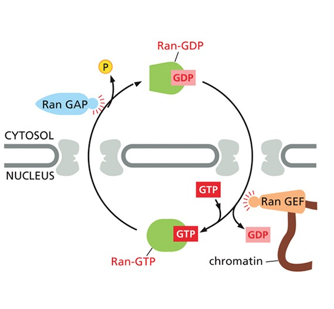
המחזור הנדרש - הידרוליזה של GTP ושחרור Ran
שחרור הקארגו אינו מספיק. כדי שהאימפורט רצפטור יהיה פנוי להובלה נוספת, נדרשת הידרוליזה של GTP ושחרור של Ran.
זהו אחד מהמנגנונים המורכבים שדורשים עיון מעמיק. חשוב להכיר מסלול מורכב כזה כדוגמה ראשונה.
הערות על המורכבות
קיימים מסלולי כניסה ויציאה רבים מהגרעין. חלק גדול מהם נשלט על ידי המתג הביולוגי Ran, הפועל בשני מצבים המופרדים מרחבית.
ההידרוליזה, המקום בו מושקעת אנרגיה, משמשת למחזור הרצפטור. זה מחזיר אותנו להגדרתם כשאטל אימפורט רצפטורים — הם נעים כל הזמן פנימה והחוצה. כאשר המערכת מכוונת כך שהקארגו יועמס במדור אחד וישוחרר במדור אחר, התוצאה נטו היא אימפורט כיווני והיכולת לצבור חלבונים בניגוד למפל הריכוזים במדור היעד.
המורכבות גדלה כאשר חלק מהחלבונים צריכים גם לצאת מהגרעין בשלב מאוחר יותר.
הרצאה 12: מעבר ל־ER - הכוונה לרשתית האנדופלזמטית
מבוא - חזרה למפה הכללית
הדיון התעכב לא מעט על נושא זה. בבחינה, לא יידרשו פרטים קטנים, והנתונים הדרושים יינתנו בשאלה.
כעת, המעבר הוא למצגת 12 — חזרה לרשתית האנדופלזמטית (ER).
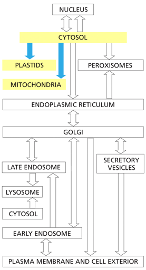
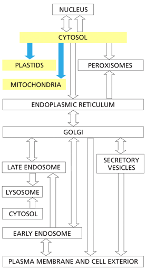
המפה הכללית, שהופיעה גם בתחילת המצגת הקודמת, מסמנת את המסלולים השונים בתא אוקריוטי מורכב. נחזור אליה שוב ושוב.
איפה אנחנו בתמונה הכללית?
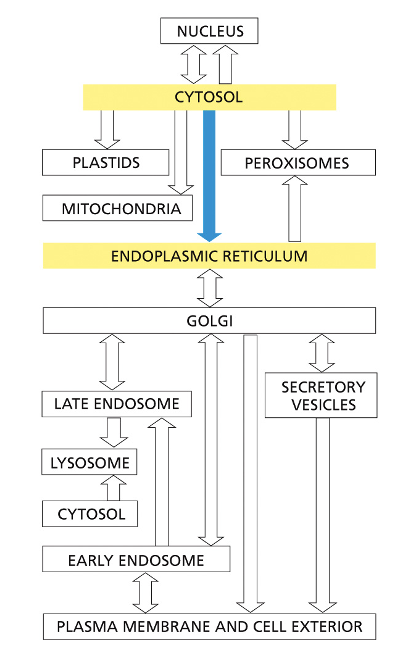
המטרה היא להבין כיצד תאים אוקריוטיים מכוונים חלבונים לאחר התרגום למדורים שונים ובכך משיגים מידור של פעילויותיהם.
מידור הוא מילת מפתח בתאים אוקריוטיים.
הדיון מתמקד כעת בחץ הכחול, מהציטוזול. מדובר בחלבונים שמתורגמים על ריבוזומים חופשיים בציטוזול, המכוונים אל הרשתית האנדופלזמטית (ER). זה כולל מגוון חלבונים:
- חלבונים כמו אינסולין, המופרש החוצה
- חלבונים שיישארו ב־ER
- חלבונים שימשיכו לגולג׳י
כפי שניתן לראות במפה, קיימים יעדים שונים. אנו בדרך לקבל תמונה כללית של תהליכים אלה.
השוואה בין תאים שונים
השקף מציג שתי דוגמאות: תא אנימלי ותא צמחי.
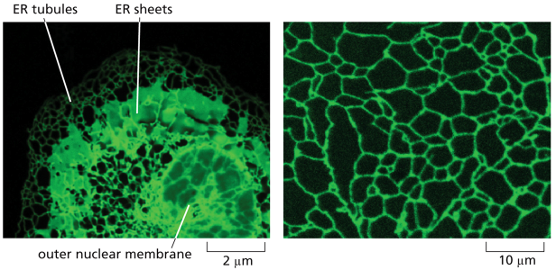
צביעה ומיקרוסקופיה - הבנת המבנה התאי
בשתי הדוגמאות יש צביעה של ה־ER. כיצד היא נעשתה ומדוע היא ירוקה?
מיקרוסקופיה מסורתית מתבססת על קיבוע (פיקסציה) של דוגמאות חיות. בתהליך כימי זה, המערכת מקובעת במקומה, מה שמאפשר צפייה בתמונות מיקרוסקופ אלקטרונים או אור, ובמקרה זה, מיקרוסקופ פלואורסנטי.
מהפכת ה־GFP - מיקרוסקופיה חיה
אחד החידושים הגדולים של סוף המאה ה־20 (שזכה בפרס נובל) הוא האפשרות למיקרוסקופיה חיה (live imaging). דוגמה מרכזית לכך היא השימוש ב־GFP (Green Fluorescent Protein).
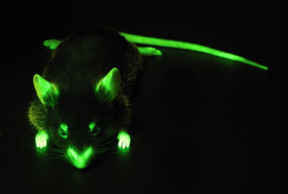
חלבון זה, שבמקור בודד ממדוזה, זוהר באור פלואורסנטי ירוק כאשר מקרינים עליו אור באורך גל מסוים. קיימות וריאציות נוספות, כמו חלבונים הזוהרים באדום.
טכנולוגיה זו מאפשרת להסתכל במיקרוסקופ מותאם ולראות רק את מיקום המולקולה. יתרה מכך, היא מאפשרת מיקרוסקופיה חיה — צפייה בתהליכים דינמיים בזמן אמת. השימוש ב־GFP כסמן מאפשר מעקב בתאים חיים (live tracking) וחושף את הדינמיות של המערכות התאיות.
שוני במבנה ER בין סוגי תאים
התמונות המוצגות הן תמונות רגע (snapshot). ניתן לראות כמה המבנה שונה בין התאים:
- בתא אחד: צינורות ארוכים עם צורת חיבורים משולשת אופיינית.
- בתא השני: מבנים צינוריים, אך גם משטחים רבים יותר.
הבדל זה קשור לשאלה שהועלתה בעבר: מבנה המשטחים מאפשר שטח פנים גדול יותר של ה־ER במקומות שבהם הוא נדרש. הצורות השונות מרמזות על תפקידים שונים.
עיקרון המבנה־תפקיד בתאים אוקריוטיים
זה מחזיר אותנו לעיקרון חשוב שיחזור בקורסים רבים:
תאים אוקריוטיים משתמשים באותו סט בסיסי של:
- אברונים תוך־תאיים.
- ציטוסקלטון.
- מנועים מולקולריים.
- GTPase קטנים.
אותו סט כלים משמש למטרות שונות.
על ידי וריאציות בשטח הפנים ובשימוש בכלים השונים, ניתן לקבל תאים בעלי פונקציות שונות. העיקרון של מבנה־תפקיד הוא עיקרון יסוד.
שני סוגי ER ותפקידיהם
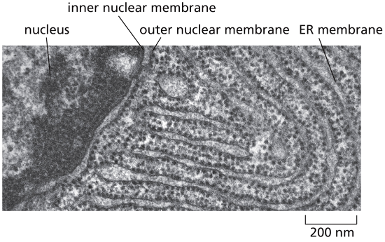
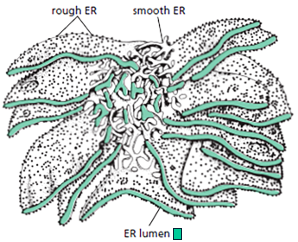
התמונה מהספר מראה את שני סוגי ה־ER, המוכרים עוד מלימודי התיכון.

ER גס (Rough ER)
ה־ER הגס (מחוספס, מגורגר) מכוסה בהמון ריבוזומים. הדוגמה היא מתא אקסוקריני בלבלב, המפריש אנזימים בכמות אדירה. לכן, רוב שטח הציטופלזמה שלו נתפס על ידי ER גס.
ER חלק (Smooth ER)
לעומת זאת, ה־ER החלק נטול ריבוזומים. הדוגמה היא מתא באשכים, העוסק באינטנסיביות בסינתזה של ההורמון הסטרואידי טסטוסטרון.
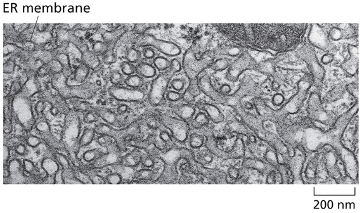
הסינתזה של כל ההורמונים הסטרואידיים מתחילה מכולסטרול. המשטחים החלקים של ה־ER מסמנים סינתזה חזקה של ליפידים:
- כלל סינתזת הליפידים.
- פוספוליפידים.
- כולסטרול.
- הורמונים סטרואידיים.
כל אלה מרוכזים ב־ER החלק.
חלוקת המרחב בתא הכבד
מימין נראה שחזור תלת־ממדי של החלוקה בין ER חלק למחוספס בתא כבד. הדבר מציין שתא הכבד עוסק בשני התפקידים וזקוק לשני הסוגים. התמונה מראה כיצד הם מחולקים במרחב.
ניתן לראות את גבול הגרעין ואת הממברנה החיצונית שלו, שגם עליה יש ריבוזומים. כל המבנה הזה מציין את חלוקת העבודה בין המדורים.
הניסויים של בלובל - הבסיס להיפותזת הסיגנל
כעת, נבחן את הניסויים שהובילו לתגליות הגדולות. חוקרים לא עבדו בוואקום; תיאוריות השתנו בעקבות ניסויים, והמסקנות לא הושגו במהירות. הספר מנסה לתת תמונה סכמטית של התהליך.
הפולס-צ’ייס אקספרימנט
בשיעור הקודם דובר על ניסוי הפולס-צ’ייס (Pulse-Chase Experiment). הסרטון שהוצג מסביר היטב את הניסוי, אך אין צורך לשנן אותו לבחינה.
הומוגניזציה ופרקציונציה
מה מראה התמונה? התמונה מהספר מראה ציטופלזמה של תא עם תערובת של ER חלק ומחוספס.
הניסוי של גינתר בלובל (שזכה בפרס נובל על עבודתו) הוביל להיפותזת הסיגנל, הגורסת שחלבונים נושאים רצפים קצרים של חומצות אמינו (סיגנלים) המכוונים אותם ליעדיהם.
תהליך ההומוגניזציה (Homogenization)
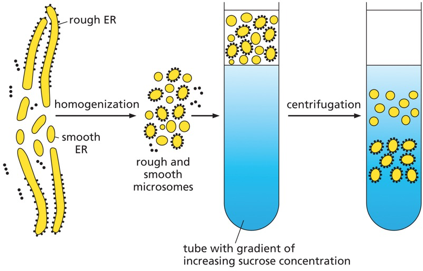
כיצד עוברים מהתא השלם לתערובת? באמצעות “הומוגניזציה”. בדומה לשימוש בבלנדר במטבח, במעבדה משתמשים בהומוגנייזר.
מכשיר זה, הדומה לכלי מהמאה ה־17, קורע את התאים ויוצר תערובת הומוגנית. התהליך גורם לממברנות להיסגר על עצמן וליצור וסיקולות, הנקראות מיקרוזומים.
פרקציונציה וצנטריפוגציה
העיקרון השני הוא פרקציונציה — הפרדת מרכיבי התערובת. המטרה היא להפריד בין המיקרוזומים החלקים לאלה המעוטרים בריבוזומים.
ההפרדה מתבצעת באמצעות צנטריפוגציה. כאשר מריצים את התערובת בצנטריפוגה, למשל על גרדיאנט של סוכרוז (תמיסה צפופה יותר בתחתית ומהולה יותר למעלה), הוסיקולות הצפופות יותר (אלה עם הריבוזומים) שוקעות למטה.
זוהי דוגמה לאופן שבו, באמצעות ניסוי וטעייה, הגיעו להפרדה של מרכיבים תאיים לפרקציות שונות.
הניסוי המכונן של בלובל
מה עושים עם הפרקציות המופרדות? בתמונה מהרצאת הנובל של גינתר בלובל, נראית תוצאה ממיקרוסקופ אלקטרוני הדומה לתמונה מהספר. הניסויים בוצעו, ככל הנראה, על לבלב של כלב.

העיקרון המהפכני
הגדולה של בלובל ואנשיו הייתה הניסיון הראשון לשחזר במבחנה (in vitro) תהליכים המתרחשים בתא. הגישה הייתה דומה לפירוק שעון לחלקיו והרכבתו מחדש: לקחת רכיבים שונים, לערבב אותם ולראות מה קורה.
תיאור הניסוי הספציפי
התמונה בספר, המתארת את “הבסיס הניסויי להיפותזת הסיגנל”, מציגה ניסוי אחד מתוך סדרה.
ישנם שני מצבים:
- למעלה: ביקורת.
- למטה: ניסוי.
ההבדל הוא שבניסוי הוסיפו מיקרוזומים של ER.
בביקורת יש רק ציטוזול, המכיל ריבוזומים חופשיים. בשני המקרים, הוסיפו mRNA המקודד לחלבון מופרש, שסונתז במבחנה.
תוצאות הניסוי ומסקנותיו
המפתח להבנת הניסוי והיפותזת הסיגנל הוא הרצף הראשוני של החלבון (“התולעת”) המציץ מהריבוזום בתחילת התרגום.

- בתחילת התרגום, הרצף הראשוני (N-טרמינוס) של החלבון מבצבץ מהריבוזום.
- בשלב זה, קורה משהו שמוביל לתוצאה שונה בין הביקורת לניסוי.
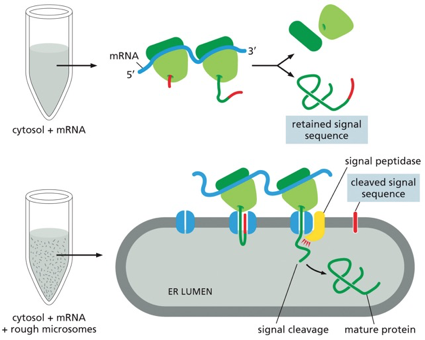
הסיגנל הזה הוא הרצף שבלובל הסיק שנחתך.
- בניסוי (עם מיקרוזומים): החלבון השלם נכנס לתוך הלומן של המיקרוזומים, והסיגנל נחתך ממנו. החלבון אינו נמצא בציטוזול.
- בביקורת (ללא מיקרוזומים): החלבון המלא, כולל הסיגנל, משוחרר לציטוזול.
ההבדל נגרם מצירוף של גורם בציטוזול וגורם על ממברנת המיקרוזום.
החלבון הבשל (לאחר החיתוך) נמצא בתוך המיקרוזום. רוב מוחלט של החלבון נכנס פנימה, והסיגנל שלו נחתך.
המסקנות מהניסוי
ההיפותזה של בלובל מ־1975 התבררה כנכונה. הוא ראה שהחלבון שנוצר בניסוי קצר יותר, והסיק שקיים מנגנון חיתוך.

המסקנה היא שגורם כלשהו מכוון את הריבוזומים. בשתי המבחנות יש ריבוזומים, אך רק בנוכחות מיקרוזומים, הריבוזומים מכוונים לממברנה, והחלבון המסונתז נדחף פנימה.
זה היה קונספט פורץ דרך. הניסוי מדגים כיצד הגיעו להיפותזת הסיגנל.
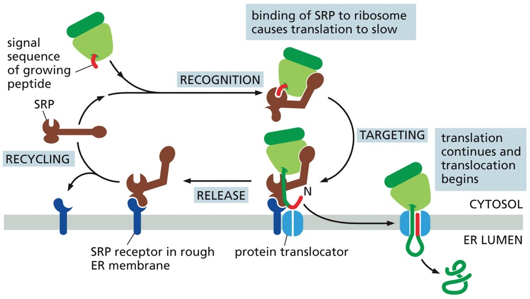
SRP - Signal Recognition Particle
המכונה הביולוגית שמכוונת ריבוזומים
מי מכוון את הריבוזום בתחילת התרגום? גורם כלשהו צריך לזהות ש”כאן מסונתז חלבון שאמור לצאת מהתא” ולכוון אותו ללומן של ה־ER. הניסוי הצליח לשחזר זאת במבחנה.
המכונה הביולוגית שעושה זאת נקראת SRP - Signal Recognition Particle.
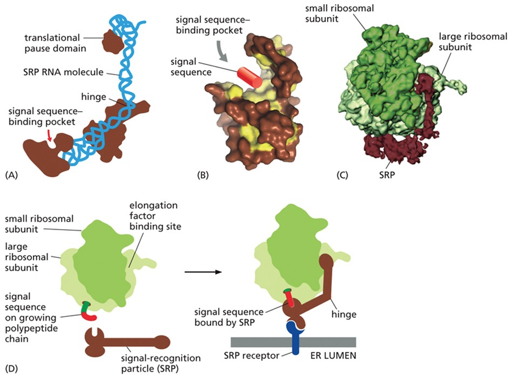
מבנה ה־SRP
מכונה ביולוגית זו, בדומה לדוגמאות אחרות, מורכבת מ־RNA ומחלבון:
- ה־RNA (בכחול) מתקפל על עצמו ויוצר מבנה דמוי מנוף או מלקחיים.
- מבנה זה מחבק את הריבוזום ומוביל אותו ליעדו.
מנגנון הזיהוי הראשוני
הכל מתחיל בכיס קישור באחת מהיחידות החלבוניות של ה־SRP (החלבונים בחום).
תת־יחידה חלבונית זו מכילה כיס קישור המזהה את רצף הסיגנל (signal sequence).
כפי שנראה, רצף הסיגנל (באדום) מופיע בתחילת הסינתזה של החלבון. זהו רצף של חומצות אמינו הידרופוביות, המזוהה על ידי כיס קישור תלת־ממדי ב־SRP.
ברגע שמתרחש זיהוי זה, מתחילה שרשרת פעולות.
מדובר במכונה ביולוגית המורכבת מחלבון ו־RNA, שתפקידה לזהות חלבונים חדשים בתחילת הסינתזה שלהם.
המשך עיבוד חלבונים ב־ER
עיבוד נוסף של חלבונים - דוגמת האינסולין
לאחר חיתוך פפטיד הסיגנל, מתרחשים אירועי עיבוד נוספים, כפי שראינו בדוגמת האינסולין (יצירת קשרי דיסולפיד ושני חיתוכים נוספים) עד לקבלת אינסולין פעיל ובשל (mature).

קיימת מערכת שלמה, הפועלת כמעין “סרט נע”, הדואגת לביצוע מודיפיקציות על החלבון עוד בזמן שהסינתזה שלו נמשכת. תהליכים אלה מתרחשים במהירות.
היגיון הפרדת המדורים
העובדה שמאות ואלפי חלבונים מכוונים לתוך החלל הפנימי של ה־ER יוצרת סביבה מוגנת ומופרדת משאר התא, שבה ריאקציות אנזימטיות יכולות להתרחש בסדר מסוים.
ההיגיון מאחורי המורכבות של התא האיקריוטי הוא “הפרד ומשול”. החלבונים המיועדים לשלבים הבאים עוברים שלבי מודיפיקציות עוד תוך כדי המעבר ל־ER.
יצירת גשרים דיסולפידיים - דוגמה קונקרטית
דוגמה אחת היא יצירת גשרים דיסולפידיים. החלבון האחראי לכך הוא PDI (Protein Disulfide Isomerase).
מה זה אומר?
זהו אנזים היוצר קשרי S-S בחלבונים אחרים. גם הוא עצמו זקוק למחזור פעילות.
- הוא מתחיל במצב מחומצן, כשאצלו יש גשר דיסולפידי.
- הוא פועל על חלבון המטרה תוך כדי כניסתו ללומן.
תהליך יצירת הגשר
התהליך כולל מצב ביניים של קשר קוולנטי בין האנזים לחלבון המטרה. בסופו של דבר, חלבון המטרה מקבל את הגשר הדיסולפידי (למשל, שלושה גשרים באינסולין).
האנזים עצמו עובר למצב מחוזר וזקוק לחלבוני עזר בלומן של ה־ER כדי לחזור למצבו הפעיל ולהתחיל סיבוב נוסף.
זהו רצף שלם של מודיפיקציות החל על שני הסוגים הכלליים של חלבונים:
שני סוגי החלבונים הנפוצים
1. חלבונים מסיסים:
- חלבונים המשוחררים לחלל המימי (לומן) של ה־ER.
- אינסולין הוא דוגמה טובה.
- אנזימים פרוטאוליטיים המופרשים למערכת העיכול הם דוגמה נוספת.
2. חלבונים ממברנליים:
- נשארים משולבים בממברנה.
- החלקים הבולטים ללומן יעברו מודיפיקציות, כמו גליקוזילציות.
שיווי משקל אנרגטי
מדובר בשיווי משקל חמצון-חיזור שהוא ייחודי לסביבת ה־ER. באופן כללי, תהליכים אלה דורשים אנרגיה.
גליקוזילציה - הוספת קבוצות סוכר
ה”קקטוסים” בתמונה מייצגים שרשראות סוכריות — מודיפיקציות סוכריות. סוכרים וליפידים מוספים לחלבונים, לעיתים קרובות לאלה המיועדים למשלוח הלאה. השלב הראשון מתרחש ב־ER, והשלבים הבאים בתחנות אחרות.

הגליקוזילציה הנפוצה ביותר
המודיפיקציה הנפוצה ביותר מתרחשת על כשני שלישים מהחלבונים (מסיסים או ממברנליים) המכוונים ל־ER.
כל השרשרת הסוכרית המסועפת (ה”קקטוס”) מועברת כיחידה אחת. היא כוללת סוכרים כמו גלוקוז, מנוז ו־N-אצטילגלוקוזאמין. זוהי הגליקוזילציה הנפוצה ביותר, המתרחשת על חומצת האמינו אספרגין.
המנגנון הביוכימי
השרשרת הצדדית של חומצת האמינו אספרגין (המכילה קבוצת $NH_2$) היא אתר הקישור. אנזים ספציפי מחבר את כל השרשרת הסוכרית המסועפת לחלבון תוך כדי כניסתו ללומן.
האנזים האחראי הוא Oligosaccharyl transferase.
תהליך מדורג ומורכב
זהו רק השלב הראשון. התהליך מתרחש בזמן שהריבוזום עדיין מסנתז את החלבון. חלבון יכול להיות באורך מאות חומצות אמינו:
- היה לו פפטיד סיגנל.
- הוא כוון לממברנה.
- הוא עבר דרך הטרנסלוקון (למשל, Sec61).
- הוא מתחיל להיכנס ללומן.
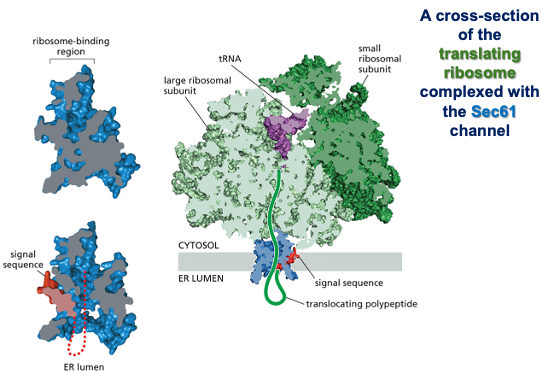
אנזים היושב בממברנה ופונה ללומן מזהה רצפי אספרגין מסוימים (לפי קוד ספציפי).
חומר המוצא
חומר המוצא מצומד לממברנה. זהו סוכר המחובר דרך שני פוספטים לשרשרת ליפידית.
מדוע? חומר המוצא מחובר לממברנה וממתין בסביבת האנזים. כך, לאנזים יש את כל מה שהוא צריך: הפרקורסור (חומר המוצא) צמוד לתעלה. ברגע שמגיע הרצף המתאים, האנזים חותך את השרשרת הסוכרית מהליפיד ומעביר אותה לחלבון. גם כאן, אקטיבציה באמצעות פוספט היא עיקרון חוזר.
שלבים נוספים - גיזום ועיבוד
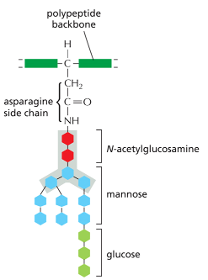
זהו רק השלב הראשון. לאחר הוספת השרשרת הסוכרית, היא עוברת “גיזום” (trimming).
כמחצית מהחלבונים העוברים דרך התעלה עוברים עיבוד זה. זוהי הצורה הנפוצה של גליקוזילציה, הנקראת N-linked glycosylation.
השפעה על פעילות החלבונים
למודיפיקציות סוכריות יש השפעה גדולה מאוד על פעילותם של חלבונים ממברנליים, במיוחד אלה הפונים אל מחוץ לתא.
יצירת מגוון ביולוגי
האם המודיפיקציה זהה בכל החלבונים? לא. ניתן לקבל מגוון ביולוגי על ידי סוגים שונים של מודיפיקציות נוספות על הסוכר הראשוני.
לדוגמה:
- נוגדנים
- רצפטורים
- חלבונים רבים הפועלים מחוץ לסביבה התאית.
חלק גדול מפעילותם מוכתב על ידי האתרים הסוכריים. זהו פתח למגוון ביולוגי עצום, שכולו מתחיל מהכוונה ל־ER.
למה תהליך כל כך מורכב?
מדוע התהליך כה רב־שלבי ודורש אנרגיה כה רבה? זוהי שאלת “ביצה ותרנגולת”.
יצירת תהליך רב־שלבי העובר בין תחנות בתא האיקריוטי מאפשרת:
- שלבי בקרה.
- מערכת בקרת איכות.
כפי שנשאל בעבר, מה קורה כשהתהליך משתבש? קיימת מערכת בקרת איכות הבודקת שהשלבים הקודמים בוצעו כראוי. אם חלבון אינו מקופל נכון או לא קיבל את המודיפיקציות הנדרשות, הוא לא ימשיך הלאה. בתאים אוקריוטיים קיימות רמות רבות של בקרה.
טרנספורט למיטוכונדריה
הדיון בטרנספורט למיטוכונדריה נועד בעיקר לציין את קיומו, ולא להעמיק בפרטים.
מבנה המיטוכונדריה
במפה הכללית, יש חץ המוביל למיטוכונדריה. המבנה המורכב של המיטוכונדריה כבר נדון:
- ממברנה חיצונית.
- ממברנה פנימית עם קיפולים (cristae).
תהליכים ביוכימיים רבים מתרחשים במיטוכונדריה, והיא חיונית לא רק לייצור אנרגיה.
חלוקה למדורים
שחזור תלת־ממדי מראה את הקיפולים הרבים של הממברנה הפנימית, היוצרים שטח פנים גדול. מבנה זה יוצר מדורים שונים:
- ממברנה חיצונית.
- ממברנה פנימית.
- חלל בין-ממברנלי (intermembrane space).
- מטריקס (החלל הפנימי ביותר).
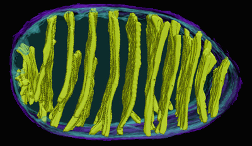
במטריקס הפנימי מתרחשים תהליכים כמו מעגל קרבס. לכן, יש צורך לכוון חלבונים למדורים השונים בתוך המיטוכונדריה.
מורכבות ההכוונה למיטוכונדריה
בדומה לבובות בבושקה, זהו מדור בתוך מדור. חלבון חדש צריך לדעת לא רק שהוא מיועד למיטוכונדריה, אלא לאיזה תת־מדור בדיוק:
- בין הממברנות.
- בתוך אחת הממברנות.
- אל תוך המטריקס.
נדרש מידע הכוונה רב המפוענח על ידי מערכת ייעודית.

דוגמה קונקרטית למנגנון
השמות אינם חשובים, אך הם הגיוניים:
- TOM: Translocon of the Outer Membrane.
- TIM: Translocon of the Inner Membrane.
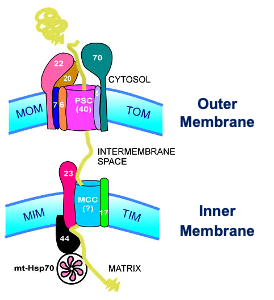
הדוגמה מראה חלבון המגיע מבחוץ:
- הוא קודד בגרעין ותורגם על ריבוזומים חופשיים בציטופלזמה.
- החלבון המלא מגיע למיטוכונדריה.
- שפרונים פורסים אותו (לא נראה בתמונה).
- במקרה הספציפי הזה, הוא עובר דרך טרנסלוקון בממברנה החיצונית (TOM), חוצה את החלל הבין-ממברנלי, עובר דרך טרנסלוקון נוסף בממברנה הפנימית (TIM), ובעזרת שפרון נוסף (HSP70), משוחרר למטריקס.
זוהי רק דוגמה אחת.
הגנום המיטוכונדריאלי
כפי שדובר, המיטוכונדריה התפתחה מחיידק אירובי ששולב בתא.
למיטוכונדריה יש גנום עצמאי, הדומה לגנום פרוקריוטי:
- הוא קטן ועצמאי.
- הוא עובר בתורשה אימהית (מטרנית).
- הוא מכיל מספר קטן של גנים.
הרוב המכריע של החלבונים שהמיטוכונדריה צריכה מקודד בגרעין ומגיע מבחוץ.
אך בפנים, בתוך המטריקס, יש גם:
- גנום.
- ריבוזומים בעלי אופי פרוקריוטי.
- אלה מתרגמים את מעט החלבונים המקודדים מקומית, בעיקר חלבונים מורכבים הפועלים במיטוכונדריה.
המורכבות המלאה של המערכת
לסיום, וכדי לתת טעימה מהמורכבות, התמונה 12.48 מהספר מראה כמה תהליכים שונים מתרחשים.
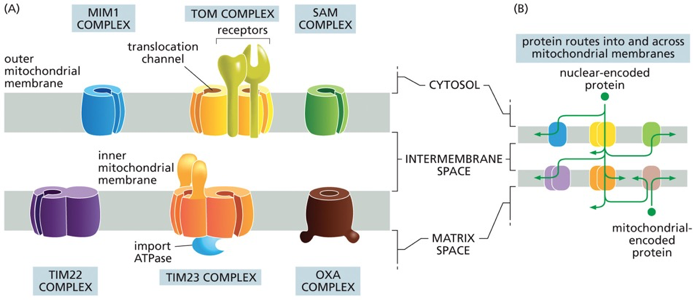
חלבון המקודד בגרעין ומגיע מבחוץ יכול:
- להיכנס לממברנה החיצונית.
- לעבור לחלל הבין-ממברנלי.
- להשתלב בממברנה הפנימית (למשל, ATP סינתאז).
- לעבור פנימה למטריקס.
בנוסף, ישנו המיעוט הקטן של חלבונים המקודדים בגנום המיטוכונדריאלי, המסונתזים בפנים ואינם צריכים לעבור במערכת זו.
התמונה מראה קשרים אפשריים בין הטרנסלוקונים בממברנות השונות.
המיטוכונדריה אינה פשוטה כלל, והמנגנונים מכוונים חלבונים לתת־מדורים שונים.
הגדרת טרנסלוקונים
טרנסלוקונים הם מערכות של תעלות מתוחכמות היושבות בממברנה. בדרך כלל, לטרנסלוקון נלווים חלבוני עזר, כמו רצפטורים.
הדוגמה נועדה להמחיש את מורכבות המערכת.
סיכום והמשך
כמעט בכל תא בגופנו יש מיטוכונדריה, והיא מעורבת בתהליכים ביולוגיים רבים.
רוב החלבונים שלה מקודדים בגרעין:
- סינתזה על ריבוזום בציטוזול.
- שחרור והובלה למיטוכונדריה.
- שפרונים מסייעים בתהליך.
התמונה הכללית מראה עד כמה האבולוציה התקדמה, וקשה לדמיין כיצד מערכת זו התפתחה בשלבים. היא החלה כנראה מאקטו־סימביונט שהפך לאנדו־סימביונט — יצור החי בתוך יצור אחר, כאשר שני הצדדים מרוויחים.
סיום וכיווני המשך
עם זה נסיים. המשך הדרך, בהרצאות הבאות, יעסוק במסלול מ־ER לגולג׳י וליעדים נוספים, כפי שנראה במפה.