תוכן העניינים:
- חזרה על השיעור הקודם
- Bulky DNA lesions
- Pyrimidine dimers ו־UV
- Photoreactivation ופתרונות שאינם קיימים באדם
- Nucleotide Excision Repair - NER
- Xeroderma Pigmentosum - XP
- שכפול DNA - כשבעיות קטנות הופכות לגדולות
- Translesion synthesis - TLS
- XP-V
- TLS in Cancer
- Template switching
- Mismatch Repair - MMR
חזרה על השיעור הקודם
השיעור נפתח בחזרה קצרה על נזקי DNA ברמת הבסיס ועל BER.
הנקודות החשובות:
- מוטציות $\mathrm{C \to T}$ צפויות במיוחד באזורים שבהם ציטוזין עבר מתילציה. אם
5-methylcytosineעובר דיאמינציה (deamination), התוצר הוא תימין, ולכן קשה יותר לזהות שמדובר בטעות.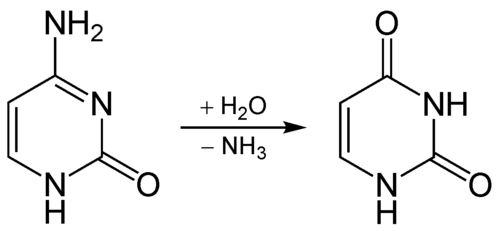
- איבוד בסיס קורה בעיקר בפורינים, אבל גם ציטוזין יכול להופיע כאתר חסר בסיס כשלב ביניים בתיקון דיאמינציה.
- אוקסידציה קשורה באופן ישיר לנשימה תאית ולמיטוכונדריה, דרך יצירת ROS.
- בתאי B צפויה רמה גבוהה יותר של דיאמינציה, בגלל האנזים AID שמשתתף בתהליך יצירת וריאציה בנוגדנים.
- AID יוצר דיאמינציה, ובהמשך מגויסים מנגנונים פחות מדויקים, ולכן מתקבלת רמת מוטציות גבוהה יותר.
- הגורם המרכזי ליצירת AP sites הוא הידרוליזה של הקשר הגליקוזידי.
- בתיקון 8-oxoG האנזים הראשון הוא OGG1.
- ההבדל בין BER של דיאמינציה לבין BER של אוקסידציה הוא בגליקוזילאז הראשון: UNG בדיאמינציה ו־OGG1 באוקסידציה.
- במיפוי אתרי 8-oxoG משתמשים ב־OGG1 לפני שלב הבידים, כדי להפוך את אתרי האוקסידציה ל־AP sites שאפשר לבודד.
מכאן עברנו מנזקים קטנים ברמת הבסיס ל־bulky lesions.
Bulky DNA lesions
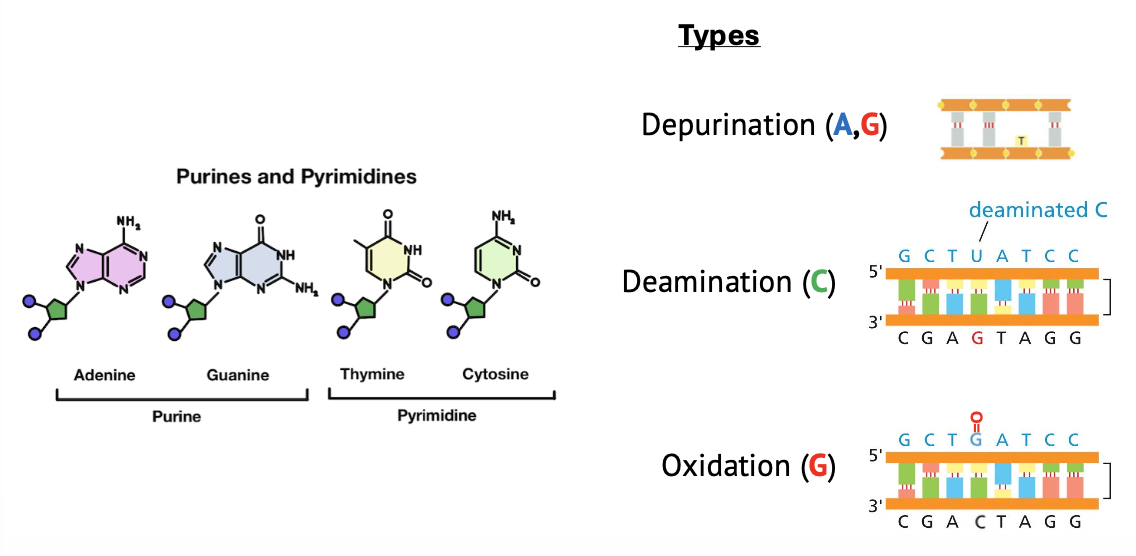
Bulky DNA lesions הם נזקי DNA שנוצרים בדרך כלל מחיבור קוולנטי של מולקולה ריאקטיבית גדולה לאחד מבסיסי ה־DNA.
ההבדל העיקרי בינם לבין non-bulky lesions הוא בגודל ובהשפעה המבנית:
- ב־non-bulky lesions הנזק קטן יחסית, בדרך כלל ברמת בסיס יחיד, והשלד הסוכרי-פוספטי נשאר שלם.
- ב־bulky lesions הנזק גדול מספיק כדי לשנות את מבנה ההליקס של ה־DNA.
השינוי במבנה ההליקס מפריע לתהליכים שדורשים קריאה מסודרת של ה־DNA, בעיקר:
- Replication
- Transcription
דוגמאות ל־bulky lesions:
- Pyrimidine dimers, בעיקר thymine dimers, בעקבות חשיפה ל־UV.
- מולקולות גדולות וריאקטיביות כמו platinum agents, למשל cisplatin.
- מולקולות מעישון, כמו benzopyrene, שיכולות להיקשר קוולנטית ל־DNA.
Pyrimidine dimers ו־UV
Pyrimidine dimer
Pyrimidine dimer הוא חיבור קוולנטי לא תקין בין שני פירימידינים סמוכים. הדוגמה הקלאסית היא חיבור בין שני בסיסי תימין סמוכים, כלומר thymine dimer.
למשל, CPD - Cyclobutane Pyrimidine Dimer.
הנזק הזה נוצר בעיקר בעקבות UV radiation. ככל שהחשיפה ל־UV חזקה יותר או ממושכת יותר, נוצרים יותר thymine dimers.
Thymine dimer מפריע לשכפול DNA, משום שהוא משנה את המבנה המקומי של ההליקס ומפריע לפולימראז להתקדם.
מיפוי thymine dimers בגנום
האם כל אתרי ה־TT בגנום רגישים באותה מידה ליצירת thymine dimers?
כדי לבדוק את זה צריך למפות אתרים שבהם באמת נוצרו thymine dimers, ולא רק לדעת איפה יש רצף TT בגנום.
העיקרון של השיטה:
- מקרינים תאים ב־UV כדי לאפשר יצירת thymine dimers.
- חותכים את ה־DNA באופן אקראי, למשל בסוניקציה.
- מחברים אדפטורים למקטעים. באדפטור יש ddNTP בקצה כדי לחסום המשך חיבור לא רצוי.
- משתמשים ב־T4 endonuclease וב־APE1 כדי לחתוך באזור ה־thymine dimer ולחשוף $\ce{OH}$ חופשי.
- מחברים אדפטור נוסף לאזור שבו נחשף ה־$\ce{OH}$.
- מבצעים PCR וריצוף.
- תחילת הקריאה מסמנת את מיקום הנזק.
כך אפשר להגיע לרזולוציה גבוהה מאוד של מיקום הנזק עצמו.
העשרה באתרי קישור של ETS transcription factors
התוצאה לא טריוויאלית: יש העשרה של thymine dimers באתרי קישור של פקטורי שעתוק ממשפחת ETS.
לא מדובר בכך שהרצף עצמו לבדו רגיש יותר. כשעושים את הניסוי על naked DNA, כלומר DNA ללא חלבונים שקשורים אליו, ההעשרה לא מופיעה.
ההסבר הוא שהקישור של פקטור השעתוק ל־DNA משנה מעט את המבנה המרחבי של ה־DNA. הוא מקרב את שני בסיסי התימין זה לזה, וכך מגביר את הסיכוי שהם יתחברו בקשר קוולנטי לאחר חשיפה ל־UV.
במילים פשוטות: החלבון לא יוצר את הנזק בעצמו, אבל מסדר את ה־DNA כך שהנזק ייווצר בקלות רבה יותר כאשר יש UV.
Photoreactivation ופתרונות שאינם קיימים באדם
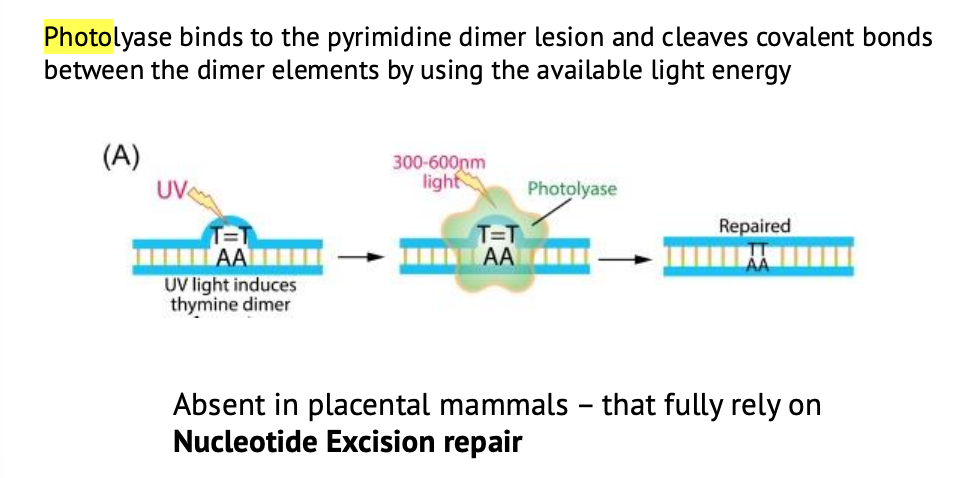
במהלך האבולוציה הופיעו כמה פתרונות לתיקון thymine dimers.
Photoreactivation repair
פתרון אחד הוא photoreactivation בעזרת האנזים photolyase.
Photolyase מופעל על ידי אנרגיית אור, ומתקן את החיבור הקוולנטי בין שני התימינים. הוא לא מסיר מקטע DNA שלם ולא מבצע סינתזה מחדש, אלא מפרק ישירות את הקשר הלא תקין בין הבסיסים.
זה פתרון יעיל מאוד, אבל הוא לא קיים באדם וביונקים בעלי שליה.
ייתכן שהאבות הקדמונים של יונקים בעלי שליה היו פחות חשופים ל־UV, ולכן לא היה לחץ סלקטיבי חזק לשמר את photolyase. מאחר שכל אנזים עולה אנרגטית לתא, מנגנון שאינו מספיק נחוץ עלול להיעלם במהלך האבולוציה. זאת רק השערה.
T4 glycosylase / endonuclease
פתרון נוסף הוא T4 glycosylase / endonuclease, שקיים בבקטריופאג’ים.
המנגנון דומה ברעיון ל־BER: יש אנזים שמזהה thymine dimer באופן ספציפי, מסיר או חותך באזור הנזק, וכך מאפשר תיקון.
גם הפתרון הזה לא קיים בבני אדם.
בבני אדם, התיקון המרכזי של thymine dimers ושל bulky lesions בכלל הוא Nucleotide Excision Repair - NER.
Nucleotide Excision Repair - NER
NER הוא מנגנון תיקון שמתאים לנזקים גדולים יחסית, כאלה שמשנים את מבנה ההליקס. בניגוד ל־BER, שמסיר בסיס פגוע יחיד, NER מסיר מקטע DNA סביב הנזק.
אפשר לחשוב עליו שוב לפי שלושה שלבים:
- Recognition - זיהוי הנזק
- Processing - פתיחת האזור וחיתוך סביב הנזק
- Repair - השלמת המקטע החסר וסגירת השרשרת
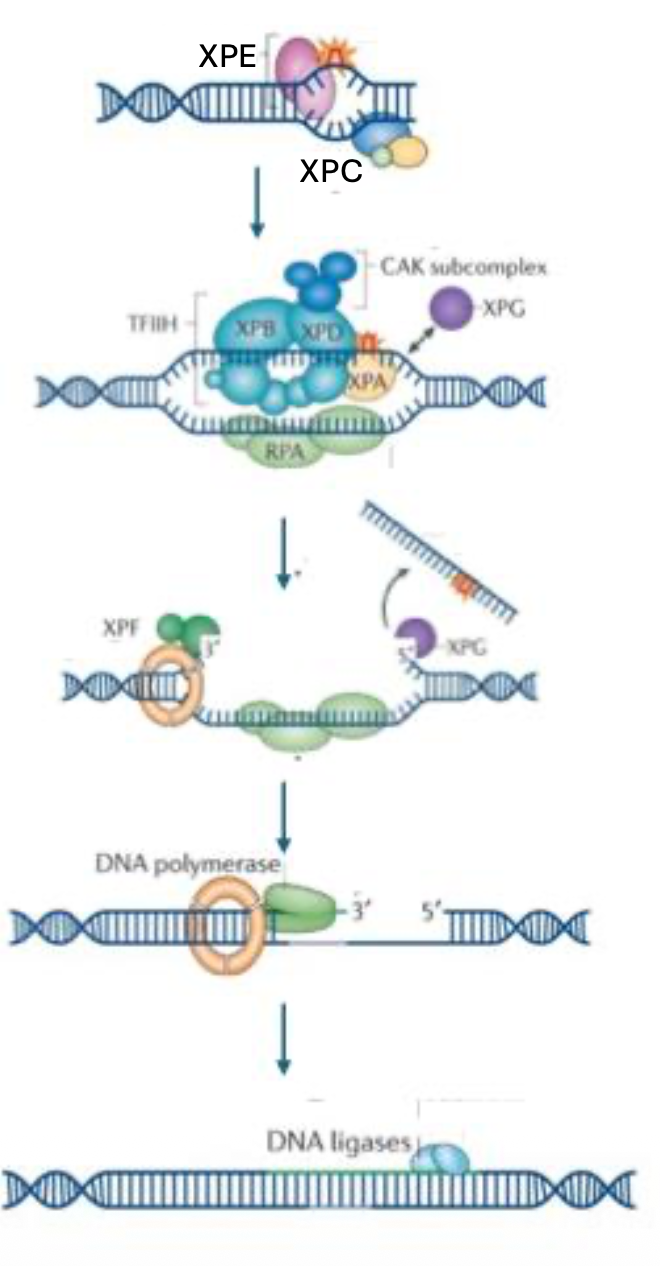
זיהוי הנזק
ב־Global Genome NER, הזיהוי נעשה בעיקר על ידי חלבוני XPC ו־XPE.
הם לא מזהים בהכרח “כימיה” של בסיס מסוים, אלא מבנה לא תקין של DNA. לכן הם מתוארים כ־structure-specific proteins: חלבונים שיודעים לזהות עיוות במבנה ה־DNA.
העיוות יכול להיות אזור שבו ההליקס לא תקין, למשל מעבר מקומי למצב פחות דו־גדילי בגלל bulky lesion.
פתיחת האזור
לאחר הזיהוי מגויסים חלבונים נוספים. האזור סביב הנזק צריך להיפתח, ולכן נדרשות הליקאזות:
- XPB
- XPD
הוזכר גם RPA, שתפקידו לשמור על הגדיל החד־גדילי שנפתח, כדי שלא יתפרק או ייסגר בצורה לא רצויה.
חיתוך סביב הנזק
לאחר פתיחת האזור, צריך להסיר מקטע DNA סביב הנזק.
החיתוך נעשה על ידי אנדונוקלאזות:
- XPF
- XPG
המקטע הפגוע מוסר, ואז נשאר פער ב־DNA.
השלמת המקטע
בשלב האחרון:
- פולימראז מסנתז מחדש את המקטע החסר
- ליגאז מחבר את הקצוות וסוגר את השרשרת
| שלב | חלבונים מרכזיים | תפקיד |
|---|---|---|
| זיהוי | XPC, XPE | זיהוי עיוות מבני ב־DNA |
| פתיחה | XPB, XPD | פתיחת ההליקס סביב הנזק |
| ייצוב | RPA | הגנה על הגדיל החד־גדילי שנפתח |
| חיתוך | XPF, XPG | חיתוך סביב הנזק והסרת המקטע הפגוע |
| תיקון | DNA polymerase, ligase | סינתזה מחדש וסגירת השרשרת |
Xeroderma Pigmentosum - XP
Xeroderma Pigmentosum - XP הוא סינדרום גנטי נדיר שנובע מפגיעה בגנים הקשורים ל־NER.
המאפיינים המרכזיים:
- רגישות גבוהה ל־UV
- נטייה מוגברת מאוד לסרטן עור
- סיכון מוגבר גם לגידולים פנימיים, משום ש־NER אינו מתקן רק thymine dimers, אלא גם bulky lesions אחרים שאינם קשורים בהכרח לחשיפה ל־UV.
סיכון מוגבר מאוד לסרטן עור, בסדר גודל של פי 2,000.
קבוצות חולים שונות
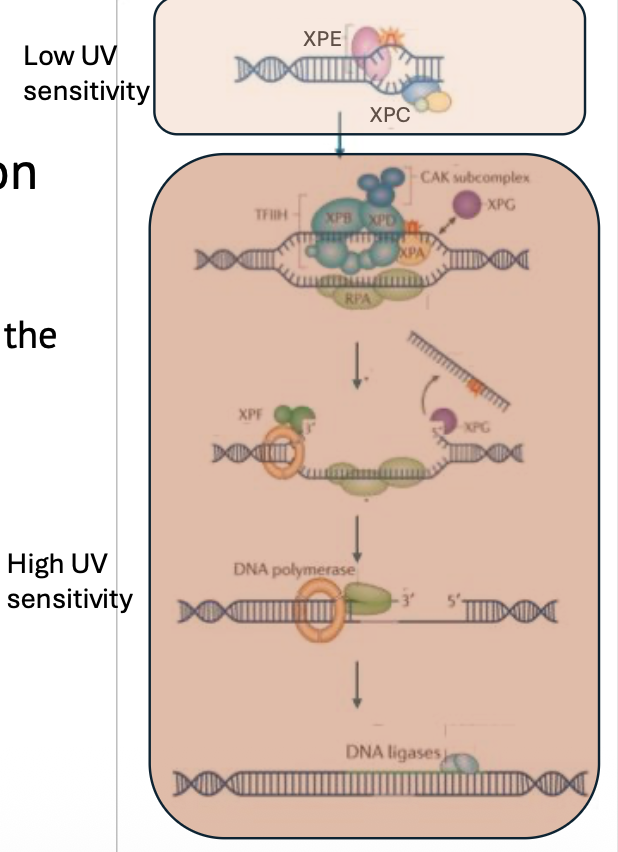
חולי XP מתחלקים לקבוצות לפי הגן שנפגע:
- XPA עד XPG - פגיעה באחד הגנים הקשורים ל־NER.
- XP-V - קבוצה חריגה, שתוסבר בהמשך. אין בה פגיעה בגנים XPA-XPG, אלא במנגנון אחר.
לכל הקבוצות יש נטייה מוגברת לסרטן, אבל יש הבדלים ברגישות ל־UV.
קבוצות שבהן הפגיעה היא בחלבונים downstream יותר בתהליך, כמו XPA, XPB, XPD, XPF ו־XPG, נוטות לרגישות גבוהה יותר ל־UV. לעומת זאת, XPC ו־XPE קשורים לזיהוי הראשוני ב־Global Genome NER, ולכן הפגיעה בהם יכולה להיות מעט קלה יותר מבחינת UV sensitivity.
Global Genome NER לעומת Transcription-Coupled NER
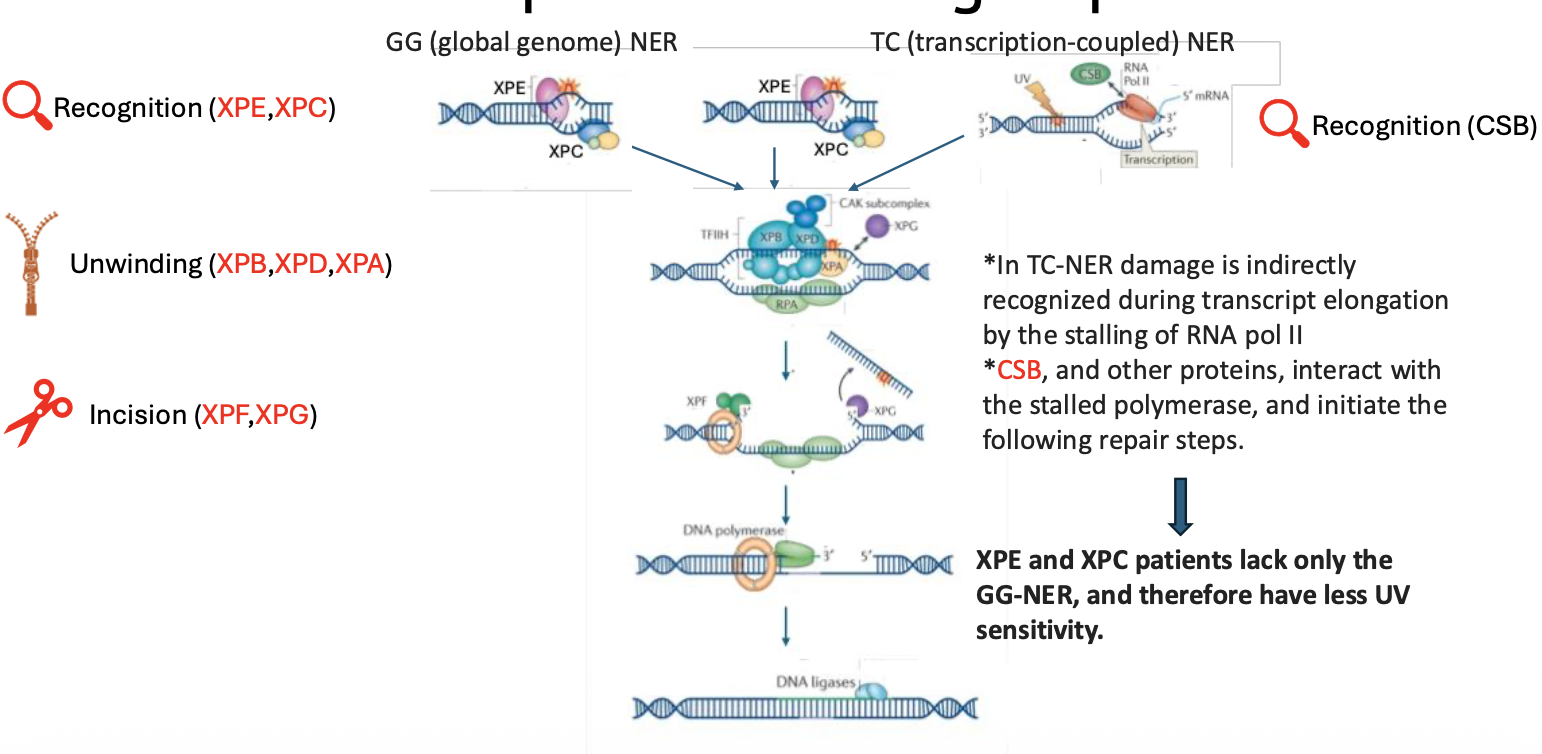
יש שני מסלולים של NER:
Global Genome NER - GG-NER
המסלול הכללי, שמחפש נזקים ברחבי הגנום. הזיהוי הראשוני בו נעשה על ידי XPC ו־XPE.
Transcription-Coupled NER - TC-NER
מסלול שמתמקד באזורים שעוברים שעתוק פעיל.
הזיהוי לא מתחיל מחלבון שמזהה את העיוות ב־DNA, אלא ממצב שבו RNA polymerase נתקע על הנזק. כאשר RNA polymerase נעצר, מגויס חלבון כמו CSB, והוא מוביל לגיוס שאר מנגנון התיקון.
הנקודה החשובה: אחרי שלב הזיהוי, שאר המנגנון משותף לשני המסלולים.
לכן:
- אם הפגיעה היא ב־XPC או XPE, עדיין נשאר TC-NER באזורים שעוברים שעתוק.
- אם הפגיעה היא בחלבונים downstream, כמו ההליקאזות או האנדונוקלאזות, שני המסלולים נפגעים.
זו הסיבה שבפגיעות ב־XPC/XPE הרגישות ל־UV יכולה להיות קלה יותר יחסית לקבוצות אחרות.
שכפול DNA - כשבעיות קטנות הופכות לגדולות
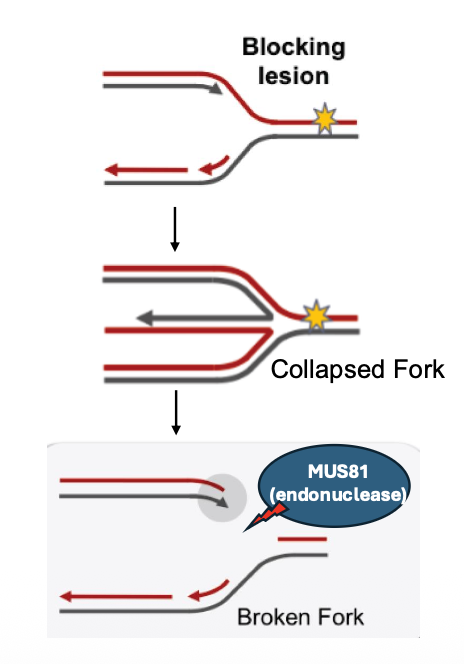
שכפול DNA הוא שלב שבו נזקים קטנים יכולים להפוך לבעיות גדולות.
מזלג השכפול צריך DNA תקין כדי להתקדם. כאשר יש bulky lesion, מבנה שניוני, R-loop או מחסור במשאבים כמו dNTPs, הפולימראז יכול להיתקע. מצב כזה נקרא replication stress.
דוגמאות למצבים שיכולים ליצור replication stress:
- מחסור ב־dNTPs
- יותר מדי origins פעילים או התחלת שכפול ביותר מדי אתרים
- מבנים שניוניים ב־DNA
- R-loops
- DNA lesions, במיוחד bulky lesions שלא תוקנו
כשמזלג השכפול נעצר וקורס, נוקלאזות יכולות לזהות את המבנה ולחתוך את ה־DNA. כך נוצרים שברי DNA, כולל שברים דו־גדיליים, שהם מהנזקים המסוכנים ביותר.
לכן התא צריך מנגנונים שמאפשרים לו להמשיך שכפול גם כאשר יש נזק. לא תמיד מדובר בתיקון מלא; לפעמים מדובר בסבילות לנזק.
Translesion synthesis - TLS
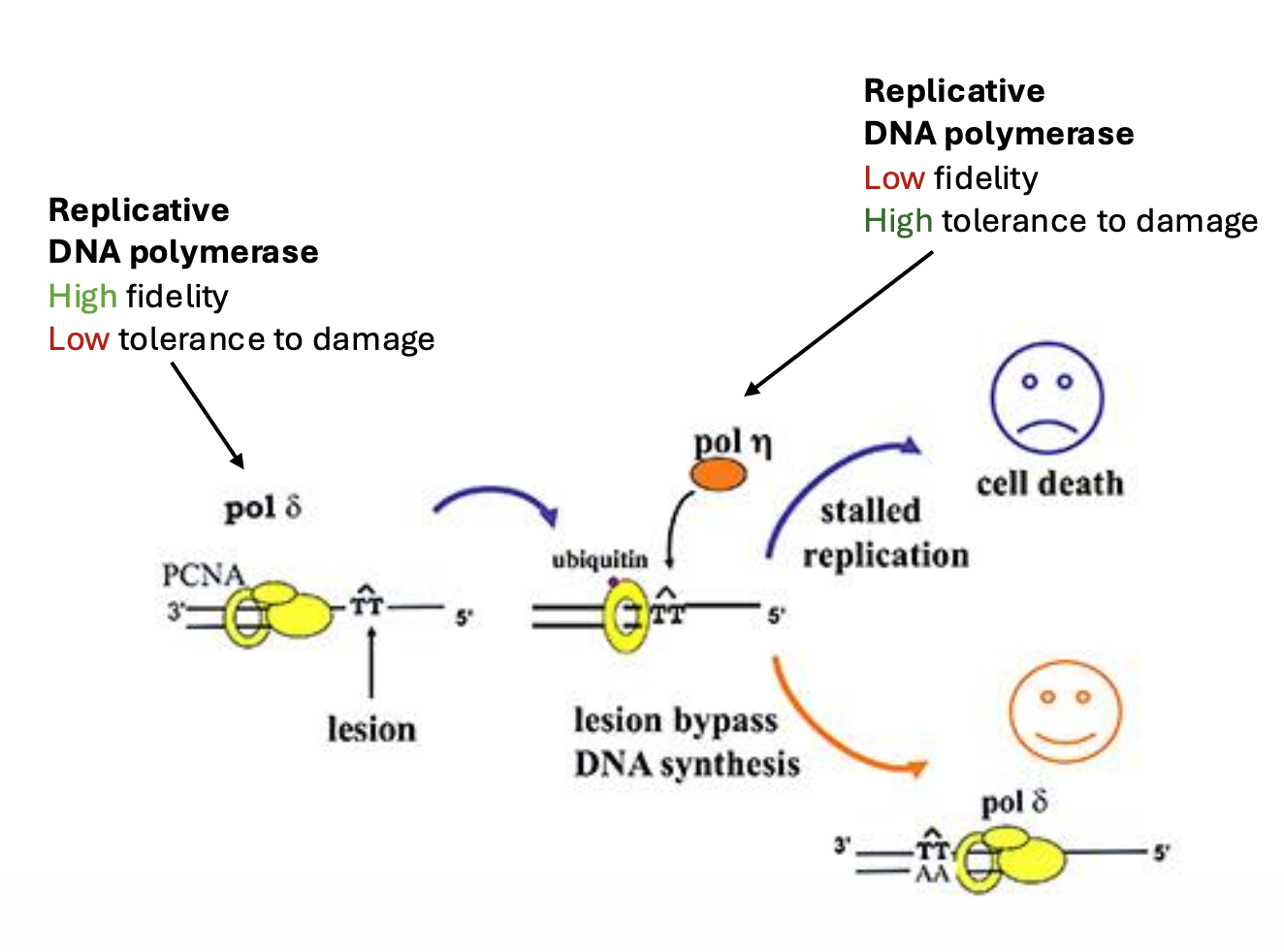
Translesion synthesis - TLS הוא מנגנון של סבילות לנזק, לא מנגנון תיקון קלאסי.
המטרה היא לא להסיר את הנזק, אלא לאפשר לשכפול להמשיך למרות שהנזק עדיין נמצא על ה־DNA.
הרעיון:
- הפולימראז הרפליקטיבי נתקע בנזק
- התא מגייס פולימראז TLS
- פולימראז TLS מסוגל לסנתז מעל הנזק
- לאחר מעבר הנזק, הפולימראז הרפליקטיבי יכול לחזור ולהמשיך
היתרון: השכפול ממשיך, ומזלג השכפול לא בהכרח קורס.
החיסרון: פולימראזות TLS פחות מדויקות, ולכן הן יכולות להכניס מוטציות.
למה פולימראזות TLS פחות מדויקות?
פולימראזות רפליקטיביות רגילות מיועדות לדיוק גבוה. הן פועלות טוב כאשר ה־DNA תקין. לעומת זאת, הן מתקשות כאשר יש bulky lesion.
פולימראזות TLS שונות מהן בכמה מאפיינים:
- אין להן proofreading כמו לפולימראזות רפליקטיביות.
- האתר הפעיל שלהן רחב יותר, ולכן הוא יכול להכיל DNA עם נזק גדול או מעוות.
- הן עובדות באופן מהיר ופחות מדויק - פתרון של “fast and dirty”.
פולימראזות TLS לדוגמה
- Pol η - Polymerase eta: מתמחה בסינתזה מעל thymine dimers שנוצרים בעקבות UV. יחסית לפולימראזות TLS אחרות, היא מדויקת יותר בהקשר הזה.
- Pol ι - Polymerase iota: משמשת כגיבוי כאשר Pol η לא פועלת, אבל היא יותר error-prone.
- Pol κ - Polymerase kappa: מתמחה ב־bulky adducts שאינם thymine dimers. רמת הדיוק שלה בינונית.
- Pol ζ - Polymerase zeta: משתתפת בהמשך הסינתזה לאחר שפולימראז TLS אחר התחיל לעבור את הנזק.
- Rev1: יודע בעיקר להכניס C, ומשמש בעיקר בהקשרים של AP sites שבהם אין מידע ברור מה צריך להיכנס.
הדגש בשיעור היה בעיקר על Pol η, בגלל הקשר שלה ל־UV ול־XP-V.
מנגנון TLS סביב thymine dimer
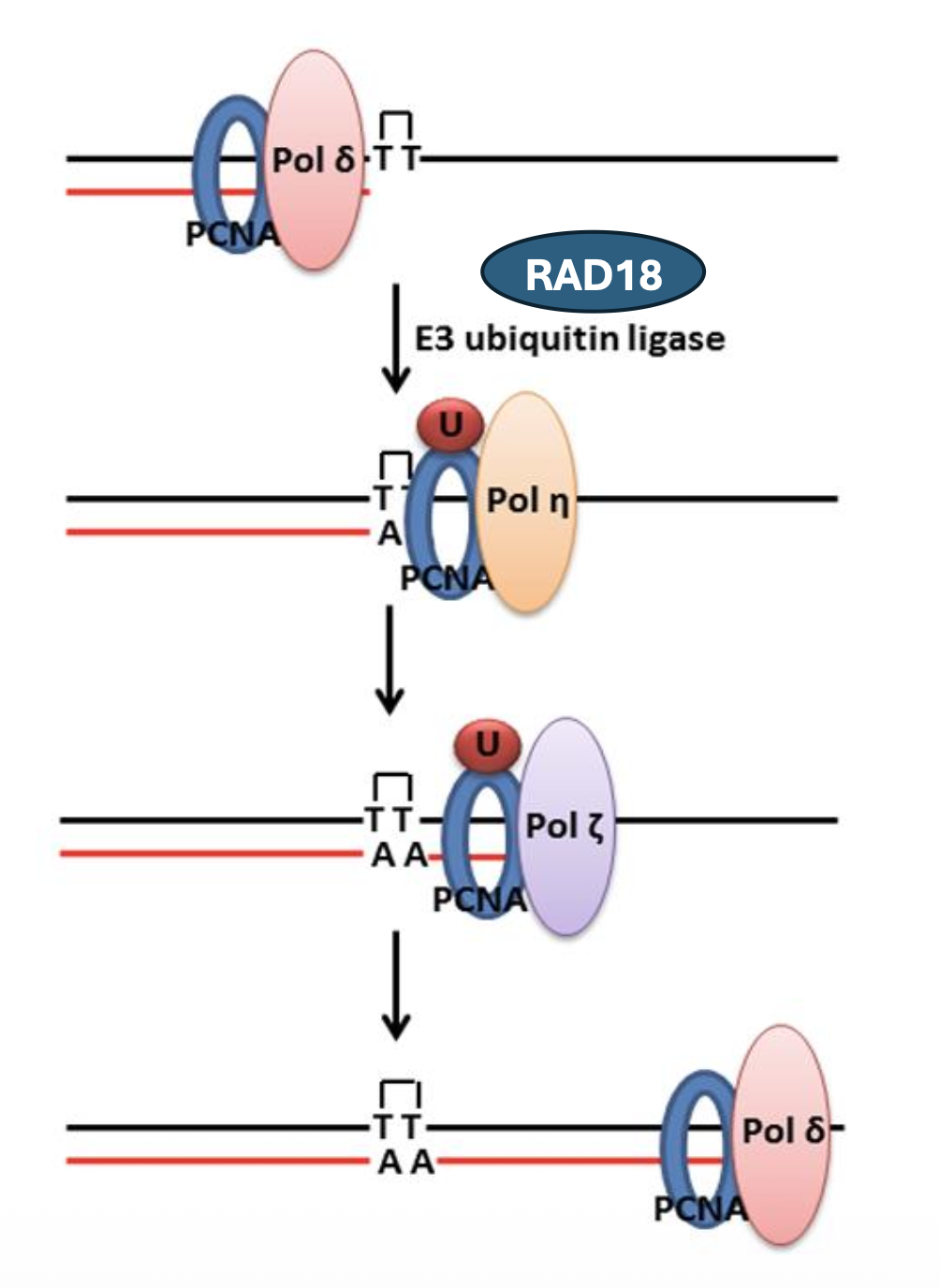
במצב רגיל, פולימראז רפליקטיבי כמו Pol δ מסנתז את ה־DNA יחד עם PCNA.
כאשר Pol δ נתקע ב־thymine dimer:
- הפולימראז נעצר.
- PCNA עובר mono-ubiquitination.
- היוביקוויטינציה אינה מסמנת לפירוק, אלא משמשת כסיגנל לגיוס TLS.
- Pol η מגויס לאזור ומסנתז מעל ה־thymine dimer.
- Pol ζ ממשיך עוד כמה נוקלאוטידים.
- הפולימראז הרפליקטיבי חוזר ולוקח מחדש את ההובלה.
PCNA מתפקד כאן כמעין פלטפורמה שמקבלת ומעבירה סיגנלים למנגנון השכפול.
XP-V
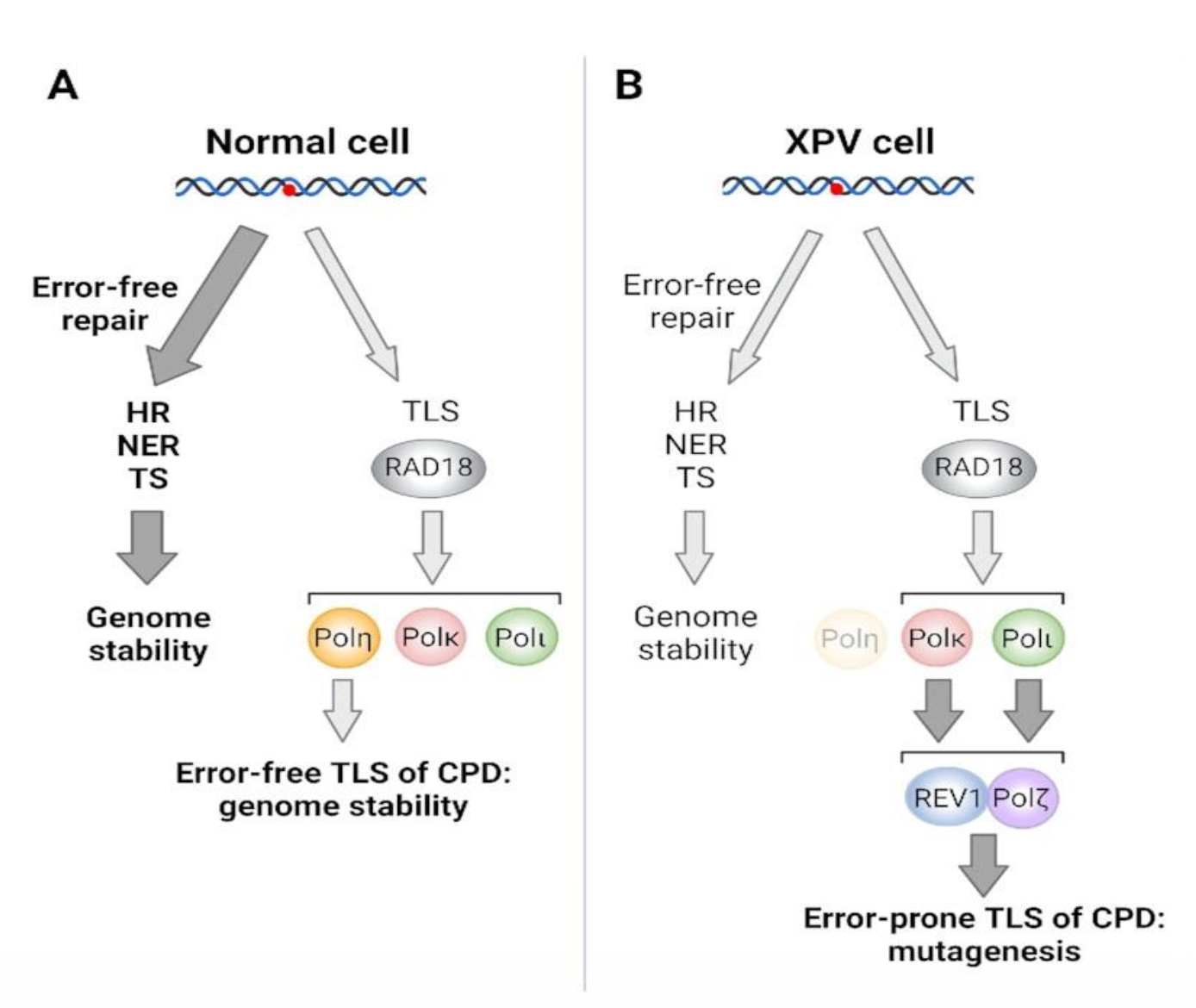
XP-V היא קבוצה חריגה בתוך Xeroderma Pigmentosum.
בחולי XP-V אין פגיעה בגנים XPA-XPG של NER. במקום, יש פגיעה בגן שמקודד ל־Polymerase η.
לכן:
- NER עצמו יכול להיות תקין.
- אבל אם thymine dimer לא תוקן לפני השכפול, התא צריך TLS כדי לעבור מעליו.
- בלי Pol η, התא משתמש בפולימראזות TLS אחרות שהן יותר error-prone.
- התוצאה היא יותר טעויות לאחר חשיפה ל־UV ונטייה מוגברת לסרטן עור.
כלומר, XP-V מלמדת ש־NER הוא לא שכבת ההגנה היחידה. גם מנגנוני סבילות לנזק בזמן שכפול חשובים מאוד למניעת מוטציות.
TLS in Cancer
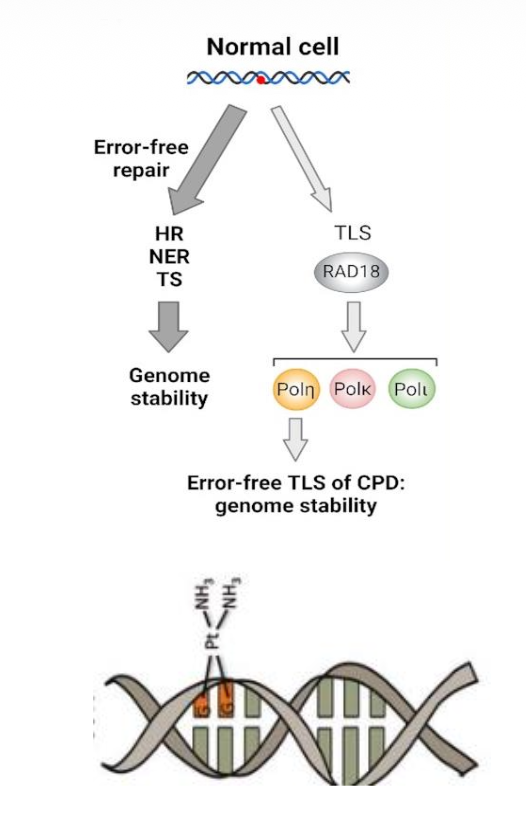
TLS קשור לסרטן בכמה רמות.
חסר ב־TLS תקין
ב־XP-V, חסר Pol η. לכן סינתזה מעל נזקי UV נעשית על ידי פולימראזות פחות מדויקות, ויש יותר מוטציות. זה תורם לנטייה לסרטן עור.
TLS היפראקטיבי
מצד שני, גם TLS פעיל מדי יכול להיות בעייתי.
אם TLS פועל יותר מדי, התא נוטה להמשיך לשכפל מעל נזקים במקום לעצור, לתקן או לעבור אפופטוזיס. זה יכול לגרום לשני דברים:
- עלייה במוטציות.
- ירידה באפופטוזיס למרות עומס נזק גבוה.
בהקשר של טיפול אנטי-סרטני, זה חשוב במיוחד. תרופות כמו cisplatin יוצרות נזקי DNA כדי לעצור שכפול ולהוביל למוות תאי. אם TLS פעיל מדי, התא הסרטני יכול לסבול את הנזק ולהמשיך להתחלק. כך נוצרת סבילות לטיפול.
לכן TLS יכול גם להגן על התא מנזק נקודתי, אבל גם לעזור לתא סרטני לשרוד נזק שהיינו רוצים שיהרוג אותו.
Template switching
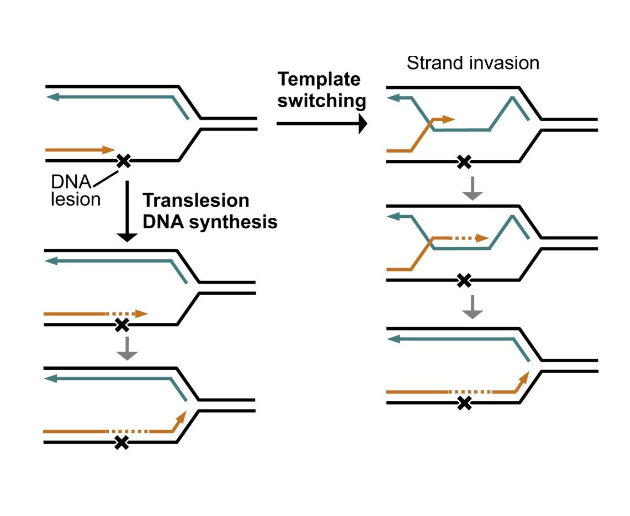
לצד TLS קיים מנגנון נוסף שמאפשר להתמודד עם נזק בזמן שכפול: template switching.
במקום לסנתז ישירות מעל הנזק, התא משתמש בגדיל מהכרומטידה האחות כתבנית זמנית.
הרעיון:
- הפולימראז נתקע בנזק על גדיל האב.
- במקום לגייס TLS, אפשר להשתמש ב־DNA שכבר סונתז בכרומטידה האחות.
- לאחר שעוברים את האזור הבעייתי, חוזרים לתבנית המקורית.
זה מנגנון שפועל לצד TLS. הוא דורש זמינות של כרומטידה אחות ולכן רלוונטי בהקשר של שכפול DNA.
Mismatch Repair - MMR
כאן כבר לא מדובר בהכרח ב־bulky lesion או בנזק כימי ברור. לפעמים ה־DNA נראה רגיל מבחינה מבנית, אבל יש בו בסיס לא נכון: mismatch.
Mismatch יכול להיווצר מכמה סיבות:
- פולימראז הכניס בסיס לא נכון בזמן שכפול
- TLS סינתז מעל נזק והכניס בסיס שגוי
- נזק כמו דיאמינציה או אוקסידציה גרם לזיווג לא תקין
MMR מוריד משמעותית את שיעור הטעויות בגנום.
נתונים:
- פולימראז ללא proofreading מכניס טעות בערך בשיעור של $1:10^5$
- Proofreading מוריד את שיעור הטעויות בעוד כשני סדרי גודל, בערך ל־$1:10^7$
- MMR מוריד את שיעור הטעויות בעוד בערך פי 1,000, עד סדר גודל של $1:10^{10}$
שלבי MMR
כמו במנגנוני תיקון אחרים, גם כאן יש:
- זיהוי
- עיבוד
- תיקון
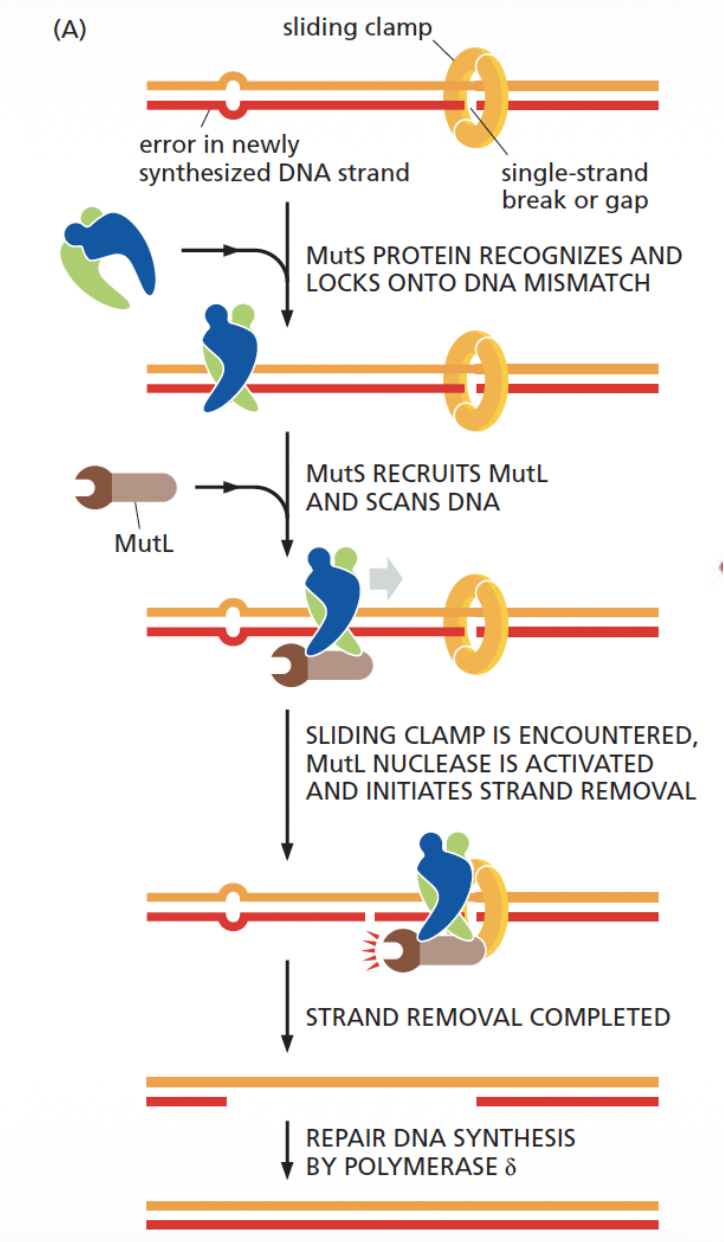
באופן עקרוני:
- MutS מזהה את ה־mismatch.
- MutL מגויס ומסייע בעיבוד האתר.
- צריך לזהות איזה גדיל הוא החדש ואיזה הוא הישן.
- מסירים את האזור השגוי.
- מסנתזים מחדש את המקטע התקין.
- ליגאז סוגר את השרשרת.
באיקריוטים השמות שונים, למשל MSH הוא ההומולוג של MutS, אבל העיקרון דומה.
האתגר המרכזי - Strand discrimination
הבעיה הקשה ב־MMR היא לא רק לזהות שיש mismatch. צריך לדעת איזה גדיל לתקן.
אם יש A מול C, למשל, מי הטעות? האם ה־A נכון וה־C שגוי, או להפך?
התא צריך לזהות את הגדיל החדש, כי שם סביר שהטעות נכנסה בזמן שכפול.
הפתרון של E. coli - מתילציה
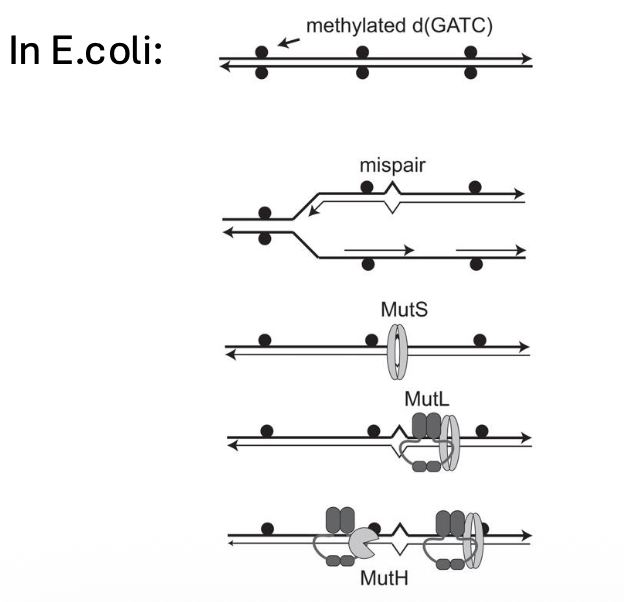
ב־E. coli הפתרון מבוסס על מתילציה של אדנין.
מיד לאחר שכפול DNA, הגדיל הישן כבר ממותל, אבל הגדיל החדש עדיין לא הספיק לעבור מתילציה. לכן אפשר לזהות את הגדיל החדש לפי היעדר מתילציה.
העיקרון:
- הגדיל הממותל הוא הישן
- הגדיל הלא ממותל הוא החדש
- מתקנים את הגדיל החדש
הפתרון באאוקריוטים - PCNA וניקים בגדיל החדש
באאוקריוטים אין את אותו מנגנון של מתילציית אדנין לצורך MMR. לכן הזיהוי נעשה אחרת.
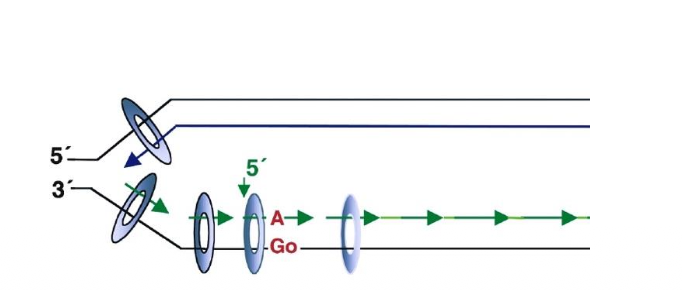
בגדיל החדש יש מאפיינים שמבדילים אותו:
- ב־lagging strand יש מקטעי אוקזקי, ולכן יש ניקים / גאפים זמניים בין המקטעים.
- גם ב־leading strand יש קצה חדש באזור מזלג השכפול.
PCNA מזהה או מסמן את אזורי הסינתזה החדשה, וכך עוזר לכוון את מנגנון MMR לגדיל החדש.
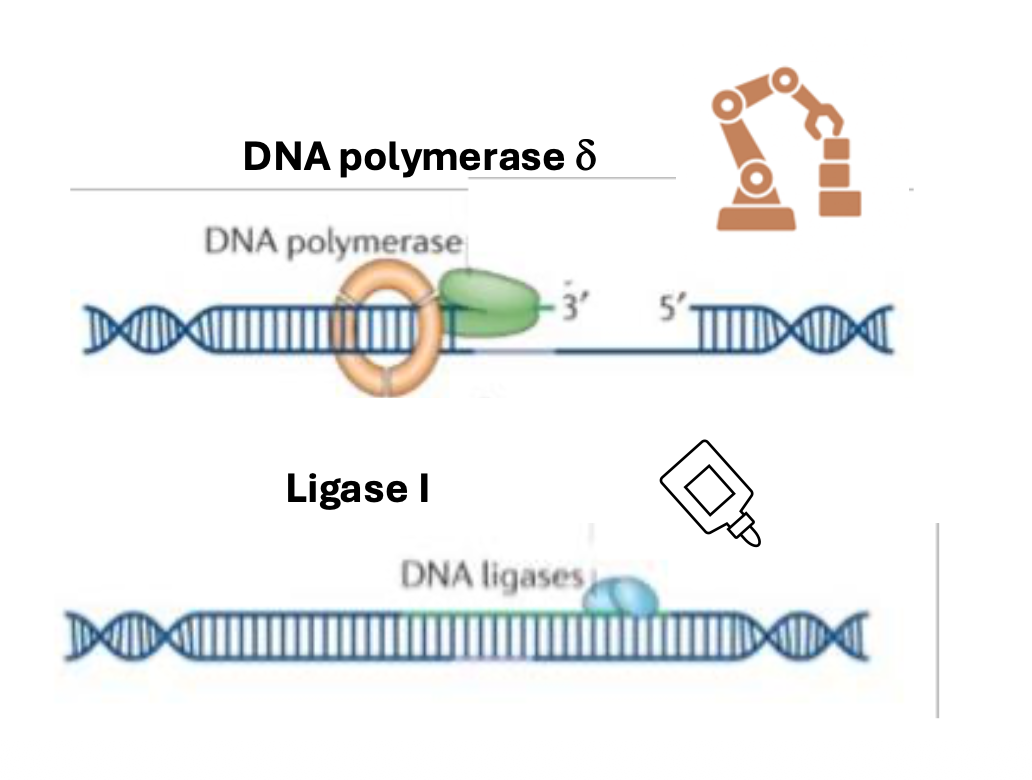
לאחר זיהוי הגדיל הנכון, האזור סביב ה־mismatch מוסר, ואז:
- DNA polymerase δ מסנתז מחדש את המקטע
- Ligase I סוגר את השרשרת
החלק הסופי דומה ברעיון למנגנוני תיקון אחרים: מסירים אזור בעייתי, מסנתזים מחדש, וסוגרים את ה־DNA.
דור פסקל