תוכן עניינים:
- חלק א’: חזרה על פרויקט הגנום האנושי ושיטות מחקר
- חלק ב’: גישות מחקר בגנטיקה - Forward vs. Reverse Genetics
- חלק ג’: גנומיקה השוואתית (Comparative Genomics)
- חלק ד’: תכונות מורכבות (Complex Traits)
- חלק ה’: גנטיקה של אוכלוסיות (Population Genetics)
- חלק ו’: מבוא להנדסה גנטית (Genetic Engineering)
- סיכום כללי
- שאלות תרגול מג׳ונרטות
- שאלות בנושא גנטיקה של אוכלוסיות
חלק א’: חזרה על פרויקט הגנום האנושי ושיטות מחקר
שיטות ריצוף הגנום האנושי
שיטת הליכת כרומוזום (Chromosome Walking)
שיטה זו התבססה על שימוש בסמנים גנטיים (Genetic Markers) שזוהו לאורך הגנום עוד לפני השלמת הריצוף. התהליך כלל:
- שיבוט (Cloning) של מקטעי DNA שונים לתוך וקטורים
- ריצוף כל מקטע בנפרד
- איתור סמן ידוע במקטע המרוצף
- חיפוש מקטע נוסף בספריית הגנום המכיל את אותו הסמן
- חיבור המקטעים וחיפוש הסמן הבא
- בנייה הדרגתית של הגנום השלם
חסרונות השיטה: תהליך איטי ביותר שארך שנים רבות ודרש מאמץ בינלאומי משותף של מדינות רבות.
שיטת הירייה (Shotgun Sequencing)
חברת Celera הציגה גישה חדשנית ויעילה יותר:
- פירגמנטציה - שבירת הגנום לחתיכות קטנות באמצעות סוניקציה (Sonication) - גלי קול, ללא ידיעה מוקדמת על תוכן החתיכות
- הוספת אדפטורים (Adapters) - רצפים ידועים מראש המשמשים לעיגון פריימרים
- ריצוף מקבילי - ריצוף כל המקטעים בו־זמנית באמצעות הפריימרים
- הרכבה ממוחשבת - שימוש באלגוריתמים לזיהוי חפיפות (Overlaps) ובניית הגנום השלם
יתרונות: מהירות, יעילות, פחות תלות בכוח אדם, שימוש מרבי בכוח מחשוב.
בסופו של דבר, שתי השיטות שולבו - כל אחת השלימה פערים של השנייה, ויחד אפשרו את פענוח הגנום האנושי.
פרויקט אלף הגנומים (1000 Genomes Project)
כהרחבה לפרויקט הגנום האנושי, פרויקט זה ריצף 1,092 גנומים של אנשים ממוצאים שונים. הממצאים העיקריים:
- שונות בין־אישית: לכל אדם 100-50 וריאנטים ייחודיים
- חישוב שיעור המוטציה: הנתונים אפשרו הערכה מדויקת יותר של קצב המוטציות בגנום האנושי
חלק ב’: גישות מחקר בגנטיקה - Forward vs. Reverse Genetics
Forward Genetics - מפנוטיפ לגנוטיפ
גישה מחקרית המתחילה מתצפית על פנוטיפ (מחלה, תכונה פיזית, התנהגות) ושואלת: אילו רצפים גנטיים אחראים לפנוטיפ זה?
שיטה 1: מחקרי GWAS (Genome-Wide Association Studies)
עיקרון השיטה:
- גיוס קבוצת מקרה (Case) - אנשים עם הפנוטיפ הנחקר (למשל: חולי סוכרת, אנשים גבוהים)
- גיוס קבוצת ביקורת (Control) - אנשים ללא הפנוטיפ
- השוואת הגנומים וחיפוש אתרים גנטיים המשותפים לקבוצת המקרה
נקודות חשובות:
- ככל שהמדגם גדול יותר (Sample Size), המידע מדויק ואיכותי יותר מבחינה סטטיסטית
- ממצאי GWAS מצביעים על קורלציה (Correlation) ולא בהכרח על קשר סיבתי (Causation)
- האתר שנמצא עשוי להיות קשור לפנוטיפ באופן עקיף - למשל דרך אפיסטזיס (Epistasis) - אינטראקציה בין גנים שבה גן אחד מווסת פעילות של גן אחר
שיטה 2: מוטגנזה אקראית (Random Mutagenesis) וסריקה (Screening)
עיקרון השיטה:
- יצירת מוטציות אקראיות באורגניזם מודל (חיידקים, זבובי פירות, עכברים)
- שיטות ליצירת מוטציות: קרינת UV, חומרים מוטגניים
- הערה חשובה: ניתן להשבית את מנגנון ה־Photolyase כדי שהמוטציות לא יתוקנו
- סריקת הפנוטיפים - זיהוי פרטים עם פנוטיפ שונה/חריג
- חזרה לזיהוי המקטע הגנטי שנפגע
יתרון: יעילות גבוהה - במקום לבדוק גן-גן, מזהים ישירות את הגן שגרם לפנוטיפ.
דוגמה מזבובי פירות (Drosophila): הכנסת טרנספוזונים עם גן GFP, איתור אתרי ביטוי שונים בלרוות (זחלים) ובזבובים בוגרים.
Reverse Genetics - מגנוטיפ לפנוטיפ
גישה מחקרית המתחילה מגן ידוע ושואלת: מהו תפקידו של גן זה?
שיטה 1: ביטוי אקטופי (Ectopic Expression)
ביטוי גן במקום, בזמן או בכמות שאינם הרגילים לו.
אפשרות א’ - הגברת ביטוי:
- הכנסת הגן תחת פרומוטור (Promoter) חזק יותר
- תוצאה: ייצור מוגבר של mRNA וחלבון
- מאפשר זיהוי פנוטיפ שלא נראה בביטוי הרגיל (הנמוך)
אפשרות ב’ - ביטוי ברקמה שונה:
- הכנסת גן לרקמה/אורגניזם שבו הוא לא מתבטא באופן טבעי
דוגמה קלאסית - GFP (Green Fluorescent Protein):
- מקור: מדוזות - זקוקות למנגנון זוהר לחיים במעמקי הים
- שימוש: הכנסת הגן לחיידקים באמצעות הנדסה גנטית
- תוצאה: חיידקים זוהרים בירוק
- יישום: אם לא היינו יודעים את תפקיד הגן, הכנסתו לחיידק והצפייה בפנוטיפ הייתה מלמדת אותנו
שיטה 2: מוטגנזה מכוונת (Targeted Mutagenesis)
פגיעה מכוונת בגן ספציפי ליצירת מצב של Loss of Function.
שימוש ברקומבינציה הומולוגית (Homologous Recombination):
- מנגנון שהכרנו בתיקון DNA ובמיוזה (תהליך השחלוף/Crossing Over)
- החלפת הגן המקורי בסמן סלקציה או ברצף ריק
- יצירת עכבר Knockout - עכבר נעדר ביטוי של הגן הספציפי
דוגמה: פגיעה בגן מסוים בעכבר גרמה להיעדר פרווה בחזה ← מסקנה: הגן אחראי לצמיחת פרווה.
הערה היסטורית: בעבר תהליך זה היה ארוך ומסורבל. כיום, שיטות כמו CRISPR (יילמד בשיעור הבא) מקצרות משמעותית את התהליך.
שיטה 3: שימוש בטרנספוזונים (Transposons)
- אלמנטים גנטיים ניידים (שנלמדו בשיעור קודם) היכולים להשתלב בגנום
- אם טרנספוזון נכנס לתוך גן - הוא משבש את פעילותו
- יתרון: ניתן לעקוב אחר מיקום הכניסה באמצעות רצף הטרנספוזון הידוע כסמן
שילוב הגישות: מקורלציה לקשר סיבתי
שאלה שנשאלה בשיעור: לאחר שמחקר GWAS מצא קשר בין אתר בכרומוזום 15 לסיכון מוגבר למחלת לב - איך מוכיחים קשר סיבתי ישיר?
תשובה: שילוב גישות:
- GWAS מזהה קורלציה (Forward Genetics)
- Reverse Genetics - פגיעה מכוונת בגן החשוד ובדיקת ההשפעה על הפנוטיפ
- מחקרים בתאים, במודלים של עכברים ובמערכות נוספות
חלק ג’: גנומיקה השוואתית (Comparative Genomics)
מה לומדים מהשוואת גנומים?
השוואת גנומים של אורגניזמים שונים (אדם, שימפנזה, עכבר, זבוב, עגבנייה) מאפשרת:
- זיהוי שינויים אבולוציוניים - מוטציות שהתקבעו לאורך הזמן
- זיהוי רצפים שמורים (Conserved Sequences) - רצף המופיע בכל האורגניזמים הנבדקים מעיד על חיוניות ולחץ סלקטיבי לשמרו
- זיהוי גנים שאיבדו תפקוד - היו פעילים באבות קדמונים ואינם מתפקדים כיום
- גילוי פתוגנים חדשים וניבוי התפתחותם האבולוציונית
סוגי שינויים גנטיים (Genetic Variations)
| סוג השינוי | תיאור | הערות |
|---|---|---|
| Point Mutations / SNPs | שינוי, הוספה או מחיקה של נוקלאוטיד בודד | השכיחות ביותר; רובן מתוקנות או ניטרליות |
| Duplications | הכפלה של מקטע DNA | לא תמיד מגבירה ביטוי - לפעמים יוצרת בקרה שלילית וחוסר תפקוד |
| Deletions | מחיקה/חסר של מקטע DNA | |
| Inversions | היפוך של מקטע DNA | נוצר משבר דו־גדילי (DSB) בשני אתרים, היפוך והדבקה |
מנגנון יצירת Inversions
שאלה שנשאלה: איזה מנגנון תיקון עשוי ליצור Inversion?
תשובה: NHEJ (Non-Homologous End Joining) - מנגנון “לא חכם” שמדביק קצוות DNA שבורים ללא התייחסות לרצף ההומולוגי. אם ההדבקה מתרחשת לאחר שהמקטע התהפך, נוצרת Inversion.
הבהרה: Homologous Recombination פחות תיצור Inversion כי היא משתמשת בכרומוזום ההומולוג כתבנית לתיקון.
שאלה נוספת: האם ב־Inversion נשמרת כיווניות 5’-3’?
תשובה: כן, הכיווניות הכימית נשמרת, אך סדר הגנים מתהפך, מה שעלול לשנות את הביטוי הגנטי.
שימושים בגנומיקה השוואתית
בניית עצים פילוגנטיים (Phylogenetic Trees)
השוואת גנומים מאפשרת מיפוי קרבה גנטית בין מינים.
דוגמה: השוואת גנומים של פרה, כבש וחזיר מראה דמיון גנטי גדול יותר בין פרה לכבש מאשר לחזיר.
שאלה שנשאלה: איך יכול להיות שלמינים קרובים יש מספר שונה של כרומוזומים?
תשובה: תהליכים אבולוציוניים כוללים:
- הכפלת כרומוזומים שלמים
- דופליקציות של גנים הנכנסים לאתרים חדשים
- טרנספוזונים המכניסים מקטעים לאזורים חדשים
- מוטציות כולל Insertions הגורמות לשינויים מבניים
הסבר: ההנחה היא שבמהלך האבולוציה, כרומוזום הכפיל את עצמו, ואז כל אחד משני העותקים עבר מוטציות שונות עד שהפכו לכרומוזומים נפרדים עם תכונות שונות.
יישומים נוספים
- מיפוי גיאוגרפי-אבולוציוני: הבנת תהליכי נדידה והתפתחות
- השוואת טמפרטורות גידול: זיהוי גנים הקשורים להסתגלות לסביבות שונות
- זיהוי זנים חדשים: למשל, זנים חדשים של וירוסים והתאמת חיסונים
- חיזוי שפעת עונתית: ניבוי זנים חדשים על בסיס מגמות אבולוציוניות
דמיון גנטי בין בני אדם
בני אדם דומים מאוד גנטית זה לזה, וגם לשימפנזים. מסקנה חשובה: רוב השונות בין בני אדם נובעת לא רק מרצפי DNA אלא מ:
- בקרת ביטוי גנים - אילו גנים מתבטאים, מתי ובאיזו כמות
- אפיגנטיקה - תוספות כימיות על בסיסי DNA והיסטונים המשפיעות על ביטוי
חלק ד’: תכונות מורכבות (Complex Traits)
הגדרה
תכונות מורכבות הן:
- תכונות פוליגניות (Polygenic) - מעורבים בהן שלושה גנים או יותר (בניגוד לשני גנים שנלמדו בהקשר של אינטראקציות גנים)
- או תכונות עם השפעה משמעותית של גורמים סביבתיים
- לרוב - שילוב של שניהם
הבדלים מתכונות מונוגניות
| מאפיין | תכונה מונוגנית | תכונה מורכבת |
|---|---|---|
| מספר גנים | גן אחד | שלושה ומעלה |
| פנוטיפים | שניים (או ארבעה בשני גנים) | ספקטרום רציף |
| התפלגות | דיסקרטית | התפלגות פעמון (Normal Distribution) |
| ניבוי | קל יחסית | מורכב מאוד |
| דוגמה | אנמיה חרמשית, קבוצת דם | גובה, משקל, דיכאון |
Nature vs. Nurture - גנטיקה מול סביבה
שאלה שנשאלה: תנו דוגמאות לתכונות גנטיות לחלוטין ולתכונות סביבתיות לחלוטין.
תכונות גנטיות (כמעט) לחלוטין:
- קבוצת דם ABO
- מחלות מונוגניות כמו אנמיה חרמשית
תכונות סביבתיות (כמעט) לחלוטין:
- מחלות זיהומיות ויראליות (אם מישהו לא היה באזור - לא נדבק)
- חשיפה לרעלים
אולם - גם כאן יש ניואנסים:
- דוגמת הקורונה: אנשים רבים נחשפו לנגיף, אך לא כולם חלו באותה חומרה ← יש רכיב גנטי המשפיע על מערכת החיסון
- לחץ דם, IQ, נטייה לסטרס - כולן תכונות מורכבות עם גם וגם
מסקנה: רוב התכונות והמחלות נמצאות “באמצע” - שילוב של גנטיקה וסביבה.
מדד תורשתיות - Heritability (H²)
היחס בין השונות הגנטית חלקי השונות הפנוטיפית נקרא מדד התורשתיות (H²) או Heritability.
מדד המבטא את החלק היחסי של השונות בתכונה המוסבר על ידי גורמים גנטיים.
- H² = 1 ← התכונה נקבעת גנטית בלבד
- H² = 0 ← התכונה נקבעת סביבתית בלבד
- ערכים ביניים ← שילוב
| תכונה | H² | פרשנות |
|---|---|---|
| סוג דם | 1.0 | גנטי לחלוטין |
| אוטיזם | 0.90 | גנטי ברובו |
| גובה | 0.88 | גנטי ברובו |
| צבע שיער | 0.89 | גנטי ברובו |
| IQ | 0.69 | גנטי חלקית, סביבתי משמעותית |
הערה חשובה: H² מבטא קורלציה, לא סיבתיות. IQ גבוה לא “נגרם” ישירות מגנים - ייתכן שהגנים משפיעים על יכולת למידה, שבתורה מושפעת מסביבה.
שיטת המחקר: השוואת תאומים (Twin Studies)
עיקרון:
- תאומים זהים (Monozygotic): 100% DNA משותף
- תאומים לא זהים (Dizygotic): ~50% DNA משותף (כמו אחים רגילים)
- שתי הקבוצות חולקות סביבה דומה (באותה משפחה)
לוגיקה: אם תכונה גנטית לחלוטין - נצפה ל־100% התאמה בתאומים זהים. אם סביבתית לחלוטין - לא נצפה להבדל בין סוגי התאומים.
דוגמה - סוג דם:
- תאומים זהים: 100% התאמה
- תאומים לא זהים: התאמה לפי חוקי מנדל
דוגמה - צבע שיער:
- תאומים זהים: 89% התאמה (לא 100%!)
- תאומים לא זהים: התאמה נמוכה משמעותית
- מסקנה: רכיב גנטי חזק, אך לא בלעדי
שאלה שנשאלה: האם היו ניסויים על תאומים שגדלו בנפרד?
תשובה: כן, היו מחקרים (חלקם בעייתיים אתית) על תאומים זהים שהופרדו בלידה וגדלו בסביבות שונות. הממצאים תמכו בהשפעה גנטית משמעותית על תכונות רבות, אך גם הראו השפעות סביבתיות.
דוגמה מורחבת: דיכאון קליני (Major Depressive Disorder)
האם דיכאון גנטי או סביבתי?
תשובה: גם וגם - תכונה מורכבת קלאסית.
גנים מעורבים
זוהו למעלה מ־80 גנים הקשורים לדיכאון, במסלולים מגוונים:
| מסלול | הסבר |
|---|---|
| סרוטונין ונוירוטרנסמיטורים | מסלול הטריפטופן, ייצור סרוטונין |
| ציר HPA (Hypothalamic-Pituitary-Adrenal) | תגובה לסטרס |
| מחזור יום-לילה (Circadian Rhythm) | דיכאון חורף, רגישות לשעות אור |
| מערכת החיסון | קשר הדדי בין דלקת למצב רוח |
| פעילות מיטוכונדריאלית | ייצור אנרגיה תאית משפיע על תפקוד כללי |
מחקר אינטראקציה גן-סביבה
מחקר קלאסי בחן גן ספציפי עם שני אללים: אלל קצר (כחול בגרף) ואלל ארוך (ירוק בגרף).
ממצאים:
- ללא אירועים טראומטיים: אין הבדל משמעותי בשכיחות דיכאון בין נשאי האללים
- אירוע טראומטי אחד או שניים: עדיין אין הבדל משמעותי
- שלושה־ארבעה אירועים טראומטיים: הבדל דרמטי - נשאי האלל הקצר בסיכון גבוה משמעותית
מסקנה: האלל עצמו אינו “גורם” לדיכאון, אך הוא מגביר את הרגישות לגורמי סטרס סביבתיים. זו דוגמה מובהקת ל־Gene-Environment Interaction.
שאלה שנשאלה: האם אפשר לעשות בדיקה גנטית לדיכאון?
תשובה: מורכב מאוד. גם אם נבדוק את כל 80+ הגנים:
- לא ברור כיצד לשקלל את התוצאות
- ייתכן שאדם נושא אללי סיכון בחלק מהגנים ואללי הגנה באחרים
- הגורמים הסביבתיים אינם ניתנים לניבוי
שאלה נוספת: האם הגנים האלה ספציפיים לדיכאון?
תשובה: לא בהכרח. גנים רבים משפיעים על מסלולים מרובים - שינוי בהם עשוי להשפיע על תפקודים נוספים מעבר לדיכאון.
דוגמה מורחבת: צבע עור ולבקנות (Albinism)
צבע עור - תכונה מורכבת
מלנין (Melanin): פיגמנט המיוצר בתאים ייעודיים - מלנוציטים (Melanocytes).
תפקידי המלנין:
- הגנה מפני נזקי קרינת UV
- שימור וספיגת ויטמין B9 (פולאט)
- מעורבות ביצירת ויטמין D
שאלה שנשאלה: איך מלנין קשור ליצירת ויטמין D?
תשובה: המלנין מגן מפני UV אך גם “חוסם” חלק מהקרינה הדרושה לסינתזת ויטמין D בעור. לכן:
- באזורים עם קרינה חזקה ← יתרון למלנין רב (הגנה מסרטן עור)
- באזורים עם קרינה חלשה ← יתרון למלנין מועט (ייצור ויטמין D)
מפת צבע העור העולמית: התפלגות צבע העור משקפת התאמה אבולוציונית לעוצמת הקרינה - עור כהה יותר באזורים קרובים לקו המשווה.
לבקנות (Albinism)
הגדרה: פגיעה בייצור מלנין הגורמת לצבע עור, שיער ועיניים בהיר מאוד.
שכיחות: 1:17,000
תסמינים:
- צבע עור ושיער בהיר מאוד
- צבע עיניים בהיר (לפעמים אדמדם)
- רגישות גבוהה לשמש (שריפות ללא שיזוף)
- לעיתים - פגיעה בראייה
גנים מעורבים:
| גן | תפקיד |
|---|---|
| TYR (Tyrosinase) | אנזים במסלול ייצור המלנין - ממיר טירוזין למלנין |
| OCA2 | בקרה על כמות ייצור המלנין |
שאלה שנשאלה: מה הקשר למחלת PKU?
תשובה: במסלול המטבולי, ההמרה של פנילאלנין לטירוזין (הפגועה ב־PKU) נמצאת מעל מסלול ייצור המלנין. אולם יש מסלולים חלופיים, ולכן חולי PKU אינם בהכרח לבקנים.
האם לבקנות היא תכונה מורכבת?
שאלה שנשאלה בשיעור: אם לבקנות יכולה לנבוע מפגיעה בגנים שונים, האם היא תכונה מורכבת?
תשובה: לא. לבקנות היא דוגמה ל־Genetic Heterogeneity (הטרוגניות גנטית) - אותו פנוטיפ יכול לנבוע מפגיעה בגנים שונים, אך מספיקה פגיעה בגן אחד כדי לגרום למצב. זה שונה מתכונה מורכבת/פוליגנית שבה נדרשת תרומה של מספר גנים יחד.
הערה חברתית-תרבותית
במדינות מסוימות באפריקה (כולל אוגנדה), לבקנים נרדפו היסטורית מתוך אמונות תפלות שייחסו להם כוחות מיסטיים או מזיקים. זוהי תזכורת שלגנטיקה יש השלכות חברתיות רחבות.
דוגמה נוספת: Retinitis Pigmentosa (RP)
הגדרה: מחלה גנטית הגורמת לאובדן ראייה פרוגרסיבי עקב פגיעה ברשתית.
גנים מעורבים: למעלה מ־70 גנים שונים - הטרוגניות גנטית נרחבת.
סוגי מוטציות שנמצאו:
- Missense (החלפת חומצה אמינית)
- Frameshift (הזזת מסגרת הקריאה)
- Nonsense (קודון עצירה מוקדם)
- Splicing mutations (פגיעה בעיבוד RNA)
- מוטציות באינטרונים הפוגעות ברגולציה
המלצת צפייה: הסרט “Blink” בנטפליקס - על משפחה שבה מספר ילדים חולים ב־RP ומחליטים לטייל בעולם כדי לחשוף אותם לחוויות ויזואליות לפני אובדן הראייה.
טיפוח סלקטיבי (Selective Breeding)
עיקרון: בחירת פרטים מקצוות ההתפלגות של תכונה רצויה להכלאה, במטרה להסיט את הממוצע בדורות הבאים.
דוגמה מהשיעור: שחקן הכדורסל הגבוה ביותר בהיסטוריה (מנוט בול, 2.31 מ’) לצד שחקן גולף נמוך יחסית - הפרשי גובה ניכרים כתוצאה מתורשה.
יישום בחקלאות:
- זיהוי התפלגות תכונה (למשל: גודל עגבנייה, תכולת פרו־ויטמין A בתירס)
- בחירת פרטים מהקצה הרצוי להכלאה
- לאורך דורות - הסטת הממוצע לכיוון הרצוי
- כך פותחו זנים שונים של עגבניות: שרי קטנות או עגבניות ענק
הבהרה חשובה: טיפוח סלקטיבי אינו הנדסה גנטית - לא מכניסים או מוציאים רצפי DNA, רק בוחרים אילו פרטים יתרבו.
חלק ה’: גנטיקה של אוכלוסיות (Population Genetics)
מעבר מפרט לאוכלוסייה
עד כה עסקנו בגנטיקה ברמת:
- הפרט (אללים, גנוטיפ, פנוטיפ)
- המשפחה (עצי משפחה, חישובי הסתברות)
כעת נעבור לשאלות ברמת האוכלוסייה:
- מה השכיחות של אלל מסוים באוכלוסייה?
- מה הסיכון לחלות במחלה גנטית באוכלוסייה מסוימת?
- האם הסיכון שווה בכל האוכלוסיות בעולם?
התשובה: לא - יש שונות משמעותית בין אוכלוסיות.
תהליכים המשפיעים על הרכב גנטי של אוכלוסיות
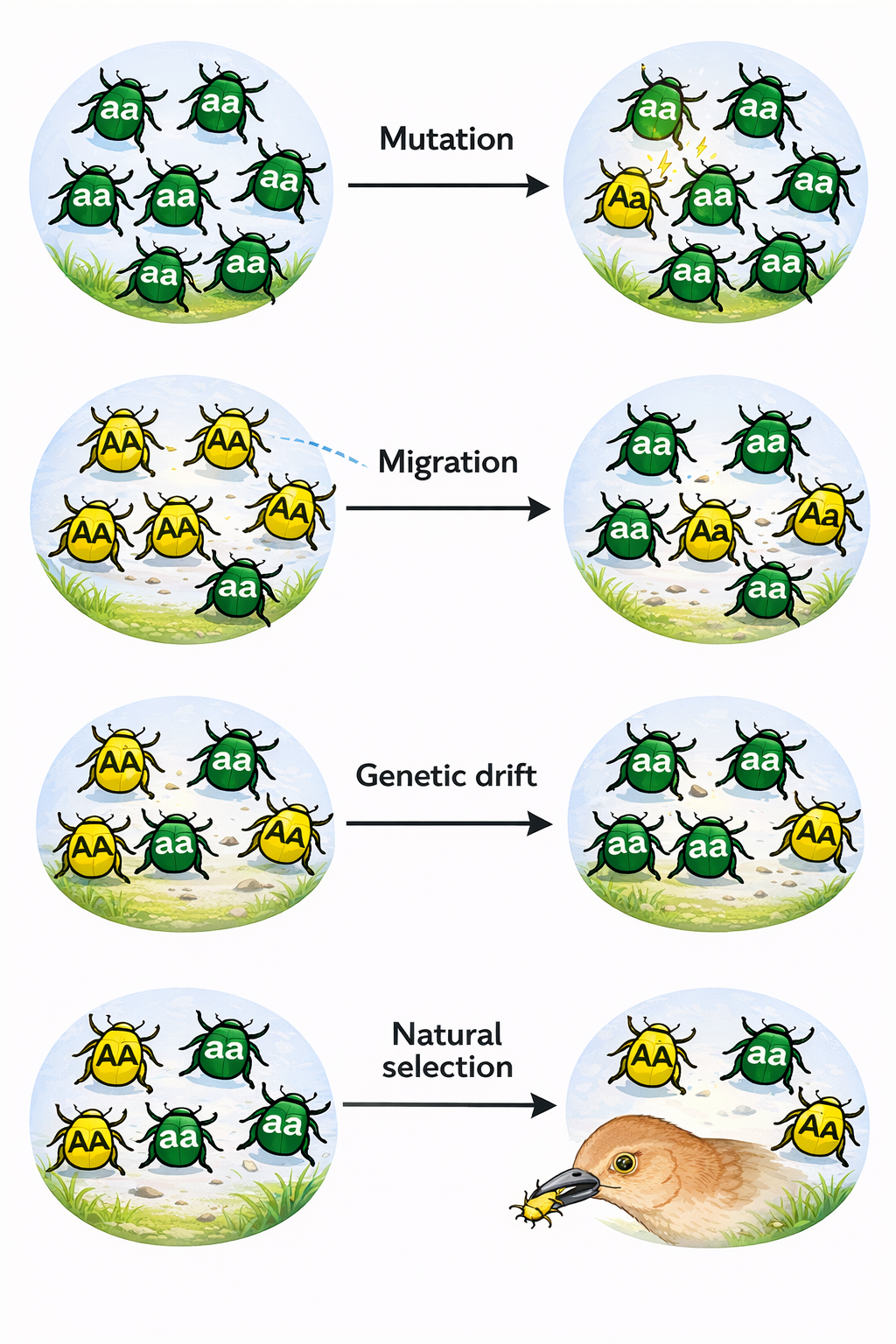
1. מוטציות (Mutations)
שינויים אקראיים ב־DNA. רובן ניטרליות או מתוקנות; חלקן גורמות ל־Loss of Function, ולעיתים נדירות - Gain of Function.
2. הגירה (Migration / Gene Flow)
תנועת אנשים בין אוכלוסיות משנה את ההרכב הגנטי.
3. ברירה טבעית (Natural Selection)
תכונות המעניקות יתרון הישרדותי ורבייתי יתפשטו באוכלוסייה; תכונות מזיקות יפחתו.
4. סחיפה גנטית (Genetic Drift)
שינויים אקראיים בשכיחות אללים, משמעותיים במיוחד באוכלוסיות קטנות.
משוואות הארדי-ויינברג (Hardy-Weinberg Equilibrium)
שני חוקרים - Hardy ו־Weinberg - פיתחו באופן עצמאי את העקרונות המתמטיים המתארים הרכב גנטי באוכלוסיות יציבות.
משוואה ראשונה: שכיחות אללים
\[p + q = 1\]כאשר:
- p = שכיחות האלל הדומיננטי (A)
- q = שכיחות האלל הרצסיבי (a)
משוואה שנייה: שכיחות גנוטיפים
\[p^2 + 2pq + q^2 = 1\]כאשר:
- p² = שכיחות הומוזיגוט דומיננטי (AA)
- 2pq = שכיחות הטרוזיגוט (Aa) - מכפילים ב־2 כי יש שתי דרכים לקבל הטרוזיגוט (A מאמא ו־a מאבא, או להפך)
- q² = שכיחות הומוזיגוט רצסיבי (aa)
הקשר בין המשוואות:
\[(p + q)^2 = p^2 + 2pq + q^2 = 1\]דוגמה: חצי־דומיננטיות בפרחים
רקע: בחצי־דומיננטיות (Incomplete Dominance), להטרוזיגוט יש פנוטיפ ביניים ייחודי.
| גנוטיפ | פנוטיפ |
|---|---|
| A₁A₁ | סגול |
| A₁A₂ | ורוד |
| A₂A₂ | לבן |
נתונים משדה: מתוך 200 פרחים שנדגמו:
- 98 סגולים (A₁A₁)
- 84 ורודים (A₁A₂)
- 18 לבנים (A₂A₂)
חישוב שכיחות אללים:
| אלל | חישוב | תוצאה |
|---|---|---|
| A₁ | (98×2 + 84) / 400 | 280/400 = 0.70 (70%) |
| A₂ | (18×2 + 84) / 400 | 120/400 = 0.30 (30%) |
אימות: p + q = 0.70 + 0.30 = 1 ✓
חישוב שכיחות גנוטיפים (צפויה):
| גנוטיפ | חישוב | תוצאה |
|---|---|---|
| A₁A₁ | p² = 0.70² | 49% |
| A₁A₂ | 2pq = 2×0.70×0.30 | 42% |
| A₂A₂ | q² = 0.30² | 9% |
אימות: 49% + 42% + 9% = 100% ✓
דוגמה קלינית: מחלת טיי-זקס (Tay-Sachs Disease)
רקע: מחלה מונוגנית רצסיבית קשה, גורמת לנזק נוירולוגי פרוגרסיבי ומוות בגיל צעיר.
שכיחות:
| אוכלוסייה | שכיחות חולים |
|---|---|
| יהודים אשכנזים | 1:3,500 |
| קנדים צרפתים | 1:35,000 |
| ממוצע עולמי | 1:320,000 |
חישוב עבור האוכלוסייה האשכנזית:
נתון: q² = 1/3,500 (שכיחות הומוזיגוט רצסיבי = חולים)
שלב 1 - חישוב q: \(q = \sqrt{1/3500} = 0.017\)
שלב 2 - חישוב p: \(p = 1 - q = 1 - 0.017 = 0.983\)
שלב 3 - חישוב שכיחות נשאים (2pq): \(2pq = 2 \times 0.017 \times 0.983 = 0.033 \approx 3.3\%\)
מסקנה: כ־3% מהאוכלוסייה היהודית האשכנזית הם נשאים למחלת טיי-זקס.
יישום קליני
שאלה שנשאלה: למה הנתון הזה חשוב?
תשובות:
- החלטות על בדיקות סקר: כדי להצדיק בדיקת סקר אוכלוסייתית, המחלה צריכה להיות:
- חמורה מספיק (טיי-זקס - בהחלט)
- שכיחה מספיק (3% נשאים - מצדיק השקעה)
- ייעוץ גנטי: אם אדם מהאוכלוסייה האשכנזית מתחתן עם בן/בת זוג מאותה אוכלוסייה, הסיכוי ששניהם נשאים הוא 3% × 3% = 0.09%, והסיכוי לילד חולה הוא 0.09% × 25% ≈ 0.02%.
תנאים לשיווי משקל הארדי-ויינברג
המשוואות תקפות רק כאשר מתקיימים כל התנאים הבאים:
| תנאי | הסבר | למה זה חשוב |
|---|---|---|
| אוכלוסייה גדולה | מספיק פרטים למדגם מייצג | באוכלוסייה קטנה - סחיפה גנטית אקראית |
| זיווגים אקראיים | ללא העדפה לפי מצב גנטי | אם חולים מתחתנים עם חולים - משתנה השכיחות |
| אין הגירה משמעותית | לא נכנסות/יוצאות קבוצות גדולות | הגירה משנה את ההרכב הגנטי |
| אין מוטציות חדשות משמעותיות | קצב מוטציה נמוך | מוטציות חדשות מוסיפות אללים |
| אין ברירה טבעית | אין יתרון/חיסרון לאלל מסוים | סלקציה משנה שכיחויות |
שאלה שנשאלה: אם האוכלוסייה האשכנזית סגורה יחסית, למה לא צפויות יותר מוטציות?
תשובה: אוכלוסייה סגורה לא מגבירה את קצב המוטציות, אלא מגבירה את הסיכוי שמוטציה קיימת תופיע במצב הומוזיגוטי (כי שני ההורים עלולים לרשת את אותו אלל מאב קדמון משותף).
מסקנה מעשית: במציאות, אף אוכלוסייה לא נמצאת בשיווי משקל מושלם. המשוואות נותנות אומדן - טוב יותר מ”הסיכוי קטן”, אך לא מדויק לחלוטין.
סחיפה גנטית (Genetic Drift)
שינויים אקראיים בשכיחות אללים, משמעותיים במיוחד באוכלוסיות קטנות.
אפקט מייסד (Founder Effect)
הגדרה: כשקבוצה קטנה מאוכלוסייה גדולה נודדת ומקימה אוכלוסייה חדשה, ההרכב הגנטי שלה עשוי להיות שונה מהאוכלוסייה המקורית.
מנגנון: מיעוט באוכלוסייה המקורית הופך לרוב באוכלוסייה החדשה.
דוגמה - איי טריסטן דה קוניה:
- קבוצת איים מרוחקת בדרום האוקיינוס האטלנטי
- 2,800 ק”מ מדרום אפריקה, 3,300 ק”מ מדרום אמריקה
- אוכלוסייה נוכחית: 238 תושבים (נכון ל־2024)
- רוב התושבים צאצאים של משפחה סקוטית אחת שהגיעה ב־1817
- פיתחו ניב שפה ייחודי
- שכיחות גבוהה של מחלות מורכבות: גלאוקומה ואסתמה
אפקט צוואר בקבוק (Bottleneck Effect)
הגדרה: כשאוכלוסייה מצטמצמת דרמטית (מגפה, אסון טבע, רדיפות), ההרכב הגנטי של השורדים עשוי להיות שונה מהאוכלוסייה המקורית.
מנגנון: מיעוט באוכלוסייה המקורית הופך לרוב בקרב השורדים.
נישואי קרובים (Consanguinity) וסיכון גנטי
הבעיה הגנטית
בנישואי קרובים, שני ההורים עלולים לרשת את אותו אלל נדיר מאב קדמון משותף. לכן:
- עולה הסיכוי למצב הומוזיגוטי רצסיבי (שני עותקים של האלל הפגום / מוטנטי) אצל הילדים
- מחלות גנטיות נדירות הופכות שכיחות יותר
שכיחות עולמית
נישואי קרובים נפוצים באזורים שונים בעולם:
- מדינות המזרח התיכון
- מדינות באפריקה
- קהילות מבודדות מסיבות דתיות או גיאוגרפיות
נתון: קיים קשר סטטיסטי ברור בין שיעור נישואי קרובים לשיעור מומים מולדים.
פתרון: תוכנית “דור ישרים”
הרקע: באוכלוסייה החרדית הייתה התנגדות ראשונית לבדיקות סקר גנטיות - חשש מ”תיוג” של נשאים ופגיעה בסיכויי שידוך.
הפתרון:
- בדיקות גנטיות לכל המעוניינים
- התוצאות נשמרות במאגר ללא חשיפה לנבדק
- כשבני זוג פוטנציאליים פונים למאגר, הם מקבלים תשובה בינארית:
- “התאמה” - אינם נשאים לאותה מחלה
- “אי־התאמה” - שניהם נשאים (לא מפרטים לאיזו מחלה)
יתרונות:
- מניעת לידת ילדים חולים
- ללא תיוג של יחידים כ”נשאים”
- התאמה תרבותית לאוכלוסייה
יתרון ההטרוזיגוט (Heterozygote Advantage)
לפעמים נשאות באלל מחלה מקנה יתרון אבולוציוני, מה שמפר את שיווי המשקל.
דוגמה קלאסית: חסר ב־G6PD
| מצב | תיאור |
|---|---|
| הומוזיגוט תקין | רגיש למלאריה |
| הטרוזיגוט (נשא) | עמיד יחסית למלאריה + סיכון נמוך לאנמיה |
| הומוזיגוט פגוע | עמיד למלאריה אך סיכון גבוה לאנמיה המוליטית |
תוצאה: באזורים אנדמיים למלאריה (כמו אגן הים התיכון), שכיחות המוטציה גבוהה יותר מהצפוי - כי ההטרוזיגוטים שרדו בשיעור גבוה יותר.
משמעות להארדי-ויינברג: במצב כזה, לא ניתן להניח “אין ברירה טבעית” - האלל “הפגום” דווקא מועדף בסביבה מסוימת.
חלק ו’: מבוא להנדסה גנטית (Genetic Engineering)
הגדרה
הנדסה גנטית: שינוי מכוון בחומר הגנטי ביד אדם, באופן מלאכותי.
כוללת:
- העברת DNA בין אורגניזמים שונים
- שינוי ברצף גן קיים
- יצירת שילובים חדשים של רצפים גנטיים
אינה כוללת:
- השבחה קלאסית / טיפוח סלקטיבי (בחירת פרטים להכלאה)
- בחירת עוברים (PGD) - בדיקה ובחירה, לא שינוי
שלושת סוגי השינויים העיקריים
| סוג | תיאור | דוגמה |
|---|---|---|
| הפעלת גן | ביטוי גן שלא היה פעיל/קיים | הכנסת GFP ממדוזות לחיידקים |
| השתקת גן | מניעת ביטוי גן פעיל | השתקת גן סרטני |
| שינוי רמת ביטוי | הגברה או הפחתה של ביטוי | הגברת ייצור חלבון תרופתי |
יישומים בתחומים שונים
חקלאות
מטרות (זהות להשבחה קלאסית, אך בשיטות שונות):
- הארכת חיי מדף
- הגדלת יבול
- העשרת ערך תזונתי
- עמידות למזיקים ולתנאי סביבה
דוגמאות תיאורטיות/מעשיות:
| יבול | בעיה | פתרון מוצע |
|---|---|---|
| עגבניות | רגישות לקור | הכנסת גנים מדגי קוטב לעמידות לקפיאה |
| תירס | נזקי מזיקים (60%+ מהיבול בארה”ב) | הכנסת גנים מחיידקים לעמידות למזיקים |
| אורז | ערך תזונתי נמוך | אורז מוזהב (Golden Rice) - הכנסת גנים לייצור בטא-קרוטן (פרו־ויטמין A) |
הבהרה חשובה:
- בישראל אין גידולים מהונדסים גנטית בחקלאות (יש מחקר, אין שימוש מסחרי)
- התנגדות ציבורית להנדסה גנטית קיימת, אך חלק מהטענות מבלבלות בין הנדסה גנטית להשבחה קלאסית
- המטרות זהות - השיטות שונות
רפואה
ריפוי גני (Gene Therapy):
- זיהוי מוטציה ספציפית בעובר או בחולה
- תיקון המוטציה או הכנסת עותק תקין של הגן
- פוטנציאל לריפוי מחלות מונוגניות
נטרול גנים מזיקים:
- השתקת גנים סרטניים (אונקוגנים)
- שיבוש ביטוי של גנים הגורמים למחלה
ייצור חלבונים תרופתיים:
| חלבון | שימוש | שיטה ישנה | שיטה חדשה |
|---|---|---|---|
| אינסולין | טיפול בסוכרת | הפקה מלבלב חזירים | ייצור בחיידקים מהונדסים |
יתרונות הייצור בחיידקים:
- זול פי 600
- נקי יותר (ללא סיכון להעברת פתוגנים מחזירים)
- אספקה בלתי מוגבלת
שאלה שנשאלה: האם אפשר לבחור מאפיינים של תינוק (צבע עיניים, גובה)?
תשובה:
- טכנית - מתחיל להיות אפשרי במקומות מסוימים בעולם
- לא בישראל - אסור חוקית
- יש להבחין: בחירת עוברים (PGD) ≠ הנדסה גנטית
- PGD = בדיקה ובחירה של עובר קיים, לא שינוי הגנום
מחקר
- הבנת תפקודי גנים (Forward & Reverse Genetics)
- יצירת מודלים למחלות (עכברי Knockout)
- פיתוח טכנולוגיות חדשות
תעשייה
תעשיית מזון:
- ייצור אנזימים להכנת גבינות
- אנזימים לריכוך בשר
- אנזימים להצללת מיצים
תעשיות אחרות:
- אורגניזמים עם תכונות ייחודיות (למשל: צמחים זוהרים לנוי)
- ייצור חומרים ביולוגיים
שאלות אתיות (לדיון בשיעורים הבאים)
- מהם הסיכונים של שחרור אורגניזמים מהונדסים לסביבה?
- האם יש גבול למה שמותר לשנות בגנום האדם?
- מי מחליט אילו שינויים “לגיטימיים”?
- מהן ההשלכות החברתיות של היכולת “לעצב” צאצאים?
סיכום כללי
השיעור עסק במעבר משלושה מישורים:
-
מפרט לאוכלוסייה: הבנה שגנטיקה פועלת לא רק ברמת הפרט והמשפחה, אלא גם ברמת אוכלוסיות שלמות, עם דינמיקות ייחודיות.
-
מתכונות פשוטות למורכבות: רוב התכונות והמחלות אינן מונוגניות אלא משלבות השפעות של גנים רבים וגורמים סביבתיים.
-
מטבע למלאכותי: הידע הגנטי שנצבר מאפשר כיום התערבות מכוונת בגנום - הנדסה גנטית - עם יישומים בחקלאות, רפואה, מחקר ותעשייה.
נקודות מפתח:
- משוואות הארדי-ויינברג מאפשרות חישוב שכיחויות גנטיות, אך תקפות רק בתנאים מסוימים
- תכונות מורכבות דורשות גישות מחקר משולבות ומקשות על ניבוי
- הנדסה גנטית היא כלי, לא מטרה - המטרות (יבול, בריאות) זהות לשיטות קלאסיות
- לכל התערבות גנטית יש השלכות אתיות הדורשות דיון ציבורי
בשיעור הבא: טכנולוגיית CRISPR ויישומיה.
שאלות תרגול מג׳ונרטות
נושאים מרכזיים: H² ופרשנותו, קונקורדנציה בתאומים, סלקציה מלאכותית ו־QTL, GWAS ו־Manhattan Plot, אינטראקציה G×E (סרוטונין ודיכאון), מסלול מלאנין ואפיסטזיס, הטרוגניות לוקוס בלבקנות, RP כהטרוגניות גנטית
שאלה 1: מדד תורשתיות (H²) - פרשנות
מדד התורשתיות (H²) לגובה באדם הוא כ־0.88. חוקר טוען שמשמעות הדבר היא ש־88% מגובהו של כל אדם נקבע על־ידי הגנטיקה. האם הטענה נכונה?
- כן - H²=0.88 משמעו שאצל כל אדם, 88% מהגובה נקבע גנטית ו־12% נקבע סביבתית
- לא - H² מתאר את החלק מתוך השונות הפנוטיפית באוכלוסייה שמוסבר על־ידי שונות גנטית, ולא את הקביעה הגנטית אצל פרט בודד
- לא - H²=0.88 מציין שלגובה יש 88 אללים תורמים, ולכן מדובר בתכונה פוליגנית ולא במדד של שונות
- כן - H² מודד את מקדם המתאם בין הורים לצאצאים, ולכן 0.88 פירושו מתאם כמעט מושלם שמראה קביעה גנטית
פתרון
התשובה הנכונה היא (2).
H² (Broad-Sense Heritability) מוגדר כיחס בין השונות הגנטית לשונות הפנוטיפית הכוללת באוכלוסייה: H² = Vg / Vp. ערך של 0.88 אומר ש־88% מהשונות בגובה בין אנשים באוכלוסייה מוסבר על־ידי הבדלים גנטיים ביניהם. זה לא אומר שגובהו של אדם ספציפי נקבע ב־88% גנטית - אדם שגדל בתת־תזונה קיצונית ייפגע בגובהו ללא קשר לגנוטיפ. H² הוא מדד אוכלוסייתי, לא פרטני, ותלוי בתנאי הסביבה הספציפיים של האוכלוסייה הנמדדת.
למה האחרות שגויות:
- (א) זו בדיוק הטעות הנפוצה - יישום של מדד אוכלוסייתי על פרט בודד.
- (ג) H² אינו מונה אללים - הוא מדד של שונות.
- (ד) H² אינו מקדם מתאם בין הורים לצאצאים (זה h², narrow-sense heritability, שמחושב אחרת).
מקור: שקף 8
שאלה 2: H² ואינטראקציה גן-סביבה
מחקר מראה ש־H² של BMI הוא 0.70 באוכלוסייה אחת ו־0.40 באוכלוסייה אחרת. מה ניתן להסיק?
- באוכלוסייה הראשונה הגנום האנושי שונה ביסודו מזה של השנייה, ולכן יש יותר גנים הקשורים ל־BMI
- ההבדל עשוי לנבוע מכך שבאוכלוסייה השנייה השונות הסביבתית (Ve) גדולה יותר - למשל הבדלים גדולים יותר בתזונה, פעילות גופנית או מצב כלכלי - מה שמגדיל את Vp ומקטין את היחס H²
- ההבדל מוכיח ש־BMI באוכלוסייה הראשונה נקבע גנטית ובאוכלוסייה השנייה נקבע סביבתית בלבד
- H² יכול להשתנות רק אם נעשתה טעות מדידה - מדד תורשתיות הוא קבוע ביולוגי לכל תכונה ואינו תלוי באוכלוסייה
פתרון
התשובה הנכונה היא (2).
H² = Vg / Vp = Vg / (Vg + Ve). אם השונות הסביבתית (Ve) גדלה - למשל הבדלים רחבים יותר בגישה למזון, בתרבות אכילה, בפעילות גופנית - אזי Vp גדל, ו־H² קטן, גם אם Vg (השונות הגנטית) זהה בשתי האוכלוסיות. לכן H² אינו מדד קבוע לתכונה אלא תלוי באוכלוסייה הספציפית ובתנאי הסביבה שלה. תכונה היא “גנטית בלבד” רק כאשר H²=1.
למה האחרות שגויות:
- (א) הגנום האנושי דומה מאוד בין אוכלוסיות - ההבדל הוא בסביבה, לא בגנום.
- (ג) H²=0.40 עדיין אומר שחלק ניכר מהשונות גנטי - לא “סביבתי בלבד”.
- (ד) H² תלוי מאוד באוכלוסייה ובסביבה - אינו קבוע ביולוגי.
מקור: שקפים 7–8
שאלה 3: מחקרי תאומים - פרשנות קונקורדנציה
עבור סכרת, שיעור הקונקורדנציה בתאומים מונוזיגוטיים (MZ) הוא 65% ובתאומים דיזיגוטיים (DZ) הוא 18%. עבור יד-שמאלנות (Handedness), ה־MZ הם 79% וה־DZ הם 77%. מה ניתן להסיק מההשוואה?
- בשני המקרים יש רכיב גנטי דומיננטי חזק כי ערכי ה־MZ גבוהים מ־50% בשניהם
- יד-שמאלנות היא תכונה גנטית יותר מסכרת כי הקונקורדנציה ב־MZ שלה גבוהה יותר (79% מול 65%)
- בסכרת הפער הגדול בין MZ ל־DZ (65% מול 18%) מעיד על רכיב גנטי משמעותי, בעוד שביד-שמאלנות הפער הזניח (79% מול 77%) מעיד שהסביבה המשותפת או גורמים אקראיים תורמים יותר מהגנטיקה
- הנתונים סותרים זה את זה ואינם ניתנים לפרשנות, כי בתכונה מורכבת אי־אפשר להשתמש בנתוני תאומים
פתרון
התשובה הנכונה היא (3).
המפתח לפרשנות מחקרי תאומים הוא הפער בין MZ ל־DZ, לא הערך המוחלט. תאומים MZ חולקים 100% מה־DNA, ותאומים DZ חולקים ~50%. אם תכונה גנטית מאוד - ה־MZ צפויים להיות הרבה יותר קונקורדנטיים מ־DZ. בסכרת: 65% מול 18% = פער של 47 נקודות → רכיב גנטי חזק + רכיב סביבתי (כי לא 100% ב־MZ). ביד-שמאלנות: 79% מול 77% = פער של 2 נקודות → הגנטיקה כמעט לא מסבירה את הקונקורדנציה, אלא סביבה משותפת או מקריות.
למה האחרות שגויות:
- (א) הערך המוחלט ב־MZ לא מעיד על עוצמת הרכיב הגנטי - רק ההפרש מול DZ קובע.
- (ב) הקונקורדנציה המוחלטת הגבוהה ביד-שמאלנות אינה מעידה על גנטיקה - הפער מ־DZ הוא המדד הרלוונטי.
- (ד) מחקרי תאומים הם כלי מרכזי ומבוסס לחקר תכונות מורכבות.
מקור: שקפים 9, 15
שאלה 4: מחקרי תאומים - קונקורדנציה של 100% ב־MZ
בטבלת הקונקורדנציה, סוג דם (Blood type) מראה 100% ב־MZ ו־66% ב־DZ. מדוע הקונקורדנציה ב־MZ היא בדיוק 100% ולא פחות?
- כי סוג הדם מושפע גם מגורמי סביבה, אך במקרה של תאומים זהים הם חולקים גם סביבה זהה ולכן תמיד קונקורדנטיים
- כי סוג הדם נקבע בלעדית על ידי הגנוטיפ ללא השפעה סביבתית כלל - ולכן תאומים שחולקים 100% מהגנום יהיו תמיד זהים בתכונה זו (H²=1)
- כי הבדיקה לסוג דם אינה רגישה מספיק כדי להבחין בהבדלים קטנים בין תאומים MZ
- כי 100% הוא ערך מעוגל - בפועל יש מקרים בודדים של MZ שאינם קונקורדנטיים בסוג דם בגלל מוטציות סומטיות
פתרון
התשובה הנכונה היא (2).
סוג הדם (ABO) נקבע אך ורק על ידי הגנוטיפ - אין לסביבה השפעה עליו. מכיוון שתאומים MZ חולקים 100% מה־DNA שלהם, הם תמיד יהיו קונקורדנטיים בסוג דם. זוהי דוגמה לתכונה עם H²=1 - השונות הפנוטיפית נובעת כולה מהשונות הגנטית. ה־66% ב־DZ נובע מכך שתאומים DZ חולקים ~50% מהגנום ויכולים לרשת אללים שונים מהוריהם.
למה האחרות שגויות:
- (א) סוג דם אינו מושפע מסביבה - זו תכונה גנטית טהורה.
- (ג) בדיקות סוג דם מדויקות מאוד - זו לא בעיית רגישות.
- (ד) קונקורדנציה של 100% היא אמיתית - מוטציות סומטיות לא משנות סוג דם באופן מעשי.
מקור: שקפים 8–9
שאלה 5: סלקציה מלאכותית ו־H²
באיור מהשיעור, מגדלי צמחים בחרו צמחי תירס עם ריכוז פרו־ויטמין A גבוה (ממוצע 1.63 μg/g מתוך אוכלוסיית מקור עם ממוצע 1.25 μg/g). הדור הבא הראה ממוצע של 1.44 μg/g. מדוע הממוצע בדור הבא לא הגיע ל־1.63 כמו הפרטים שנבחרו?
- כי הפער בין 1.25 ל־1.63 נבע כולו מגורמי סביבה ולא מגנטיקה, ולכן לא עבר לדור הבא
- כי חלק מהפער שנצפה בפרטים שנבחרו נבע מרכיב סביבתי (לא־תורשתי), ורק הרכיב הגנטי של הפער עבר בתורשה - לכן התגובה לסלקציה קטנה מדיפרנציאל הסלקציה
- כי התירס עובר רגרסיה ספונטנית לממוצע האוכלוסייה בכל דור, ללא קשר לגנטיקה
- כי המגדלים טעו ובחרו פרטים שהריכוז הגבוה שלהם היה כולו גנטי, ובכל זאת הדור הבא ירד כי המוטציות אינן יציבות
פתרון
התשובה הנכונה היא (2).
זוהי הדגמה קלאסית של הקשר בין H² לתגובה לסלקציה. כאשר בוחרים פרטים בעלי פנוטיפ קיצוני, חלק מהפנוטיפ שלהם נובע מגנטיקה (תורשתי) וחלק מסביבה (לא־תורשתי). רק הרכיב הגנטי עובר לצאצאים. לכן: R (Response) = H² × S (Selection differential). ממוצע ההורים הנבחרים 1.63, ממוצע האוכלוסייה 1.25, S = 0.38. אם הדור הבא הגיע ל־1.44, R = 0.19. לכן H² ≈ 0.19/0.38 = 0.50.
למה האחרות שגויות:
- (א) לא כולו סביבתי - הדור הבא כן עלה (מ־1.25 ל־1.44), אז חלק גנטי.
- (ג) רגרסיה לממוצע היא תופעה סטטיסטית שמוסברת על ידי H² - לא “ספונטנית”.
- (ד) אין קשר ליציבות מוטציות - זהו עניין של שונות גנטית מול סביבתית.
מקור: שקף 10
שאלה 6: GWAS - עקרון ופרשנות
מחקר GWAS מצא קשר מובהק (p < 5×10⁻⁸) בין SNP מסוים באינטרון הראשון של גן FTO לבין BMI מוגבר. מה ניתן להסיק מממצא זה?
- המוטציה ב־FTO גורמת ישירות להשמנה - כלומר זוהי מוטציה קאוזלית שדי בה לבדה לגרום למחלה
- ה־SNP מראה אסוציאציה סטטיסטית עם BMI באוכלוסייה, אך אינו בהכרח קאוזלי - ייתכן שהוא סמן (marker) ל־linkage disequilibrium עם הווריאנט הפונקציונלי האמיתי, וגם אם הוא קאוזלי - כרכיב אחד מתוך רבים, השפעתו על פרט בודד קטנה
- ה־SNP נמצא באינטרון ולכן אין לו שום משמעות ביולוגית אפשרית - הממצא הוא חיובי שקרי
- ממצא GWAS עם p < 5×10⁻⁸ מוכיח שהגן FTO הוא הגורם היחיד והמספיק להשמנה באוכלוסייה שנבדקה
פתרון
התשובה הנכונה היא (2).
GWAS מזהה אסוציאציות (קורלציות) סטטיסטיות בין SNPs לבין פנוטיפים באוכלוסייה - לא סיבתיות ישירה. ה־SNP ב־FTO הוא הלוקוס עם ההשפעה המשמעותית ביותר על BMI שנמצא עד כה, אך: (1) ייתכן שה־SNP עצמו אינו הווריאנט הפונקציונלי אלא נמצא ב־LD עמו; (2) גם אם הוא קאוזלי, השפעתו על פרט בודד קטנה - השמנה היא תכונה מורכבת שמושפעת ממאות לוקוסים ומסביבה. האלל T (BMI-increasing) של rs17817964 מראה תדירויות שונות בין אוכלוסיות שונות.
למה האחרות שגויות:
- (א) GWAS לא מוכיח סיבתיות, ותכונה מורכבת כמו BMI אינה נקבעת על ידי גן יחיד.
- (ג) SNPs באינטרונים יכולים להשפיע על רגולציה, שחבור, ואינהנסרים - אינם חסרי משמעות.
- (ד) FTO הוא רכיב אחד מתוך אלפי לוקוסים שתורמים ל־BMI - לא “גורם יחיד ומספיק”.
מקור: שקפים 18–21
שאלה 7: אינטראקציה גן × סביבה - דיכאון קליני
במחקר של Caspi ו־Moffitt (2003), נמצא שאנשים עם שני עותקים של האלל הקצר (Short) של גן טרנספורטר הסרוטונין, שחוו ארבעה אירועי חיים סטרסוגניים או יותר, היו בסיכון כפול לדיכאון בהשוואה לנושאי שני עותקים של האלל הארוך. מה מדגים ממצא זה?
- שהאלל הקצר גורם לדיכאון באופן דטרמיניסטי ללא קשר לסביבה - כלומר מי שנושא אותו יפתח דיכאון בהכרח
- שהסביבה בלבד קובעת דיכאון ולגנטיקה אין תפקיד - כי ללא אירועים סטרסוגניים גם בעלי האלל הקצר לא חלו
- אינטראקציה גן × סביבה (Gene-Environment Interaction) - הגנוטיפ לבדו או הסביבה לבדה אינם מספיקים; הסיכון עולה משמעותית רק בשילוב של רגישות גנטית עם חשיפה סביבתית
- שהאלל הארוך הוא מגן מפני כל מחלה פסיכיאטרית ולכן נושאיו לעולם לא יפתחו דיכאון
פתרון
התשובה הנכונה היא (3).
ממצא Caspi & Moffitt הוא דוגמה קלאסית לאינטראקציה גן × סביבה (G×E): הגנוטיפ (אלל קצר של טרנספורטר סרוטונין) לא גורם לדיכאון לבדו, והסביבה (אירועים סטרסוגניים) לא גורמת לדיכאון זהה בכל הגנוטיפים - רק השילוב של שניהם מגביר את הסיכון באופן משמעותי. ביטוי נוסף למורכבות: מעל 80 גנים קשורים בדיכאון, ורבים מהם אינם ספציפיים לדיכאון - יש חפיפה גנטית עם חרדה (Shared genetic associations between depressive and anxiety symptoms).
למה האחרות שגויות:
- (א) האלל הקצר מגביר סיכון אך אינו דטרמיניסטי - ללא סטרס, השיעור נמוך.
- (ב) הגנטיקה משנה - נושאי האלל הקצר הגיבו אחרת לאותם אירועים.
- (ד) גם נושאי האלל הארוך יכולים לפתח דיכאון, רק בשיעור נמוך יותר.
מקור: שקפים 22–25
שאלה 8: מדד תורשתיות - השוואה בין תכונות
לפי הטבלה מהשיעור, H² של Fingerprint ridge count הוא 0.97 ו־H² של Major Depression הוא 0.37. חוקרת טוענת: “אי אפשר להשפיע על טביעת אצבע, ואפשר להשפיע על דיכאון - לכן אלו תוצאות צפויות.” האם הפרשנות שלה מדויקת?
- כן - H² גבוה פירושו שהתכונה לא ניתנת לשינוי, ו־H² נמוך פירושו שניתן לשנות אותה על ידי התערבות
- באופן חלקי - H² משקף את יחס השונות הגנטית לפנוטיפית באוכלוסייה, לא את יכולת השינוי של התכונה אצל פרט. אפשר להתערב בתכונה גם כש־H² גבוה (למשל PKU - H² גבוה אך ניתן לדיאטה), אך האינטואיציה שלה נכונה בכך שתכונות מושפעות-סביבה נוטות ל־H² נמוך יותר
- לא - H² קובע רק את מספר הגנים המעורבים, ותכונה עם H² נמוך פשוט מעורבים בה פחות גנים
- לא - H² של 0.37 פירושו שהדיכאון אינו גנטי כלל, והסביבה בלבד אחראית
פתרון
התשובה הנכונה היא (2).
H² הוא מדד אוכלוסייתי של שונות ולא מדד של “יכולת שינוי” (malleability) אצל פרט. דוגמה חשובה: PKU (Phenylketonuria) - H² גבוה מאוד כי ההבדל בפנוטיפ נובע כמעט לגמרה מגנוטיפ, אך ניתן לשנות את הפנוטיפ באופן דרמטי על ידי התערבות סביבתית (דיאטה ללא פנילאלנין). עם זאת, האינטואיציה נכונה בכיוון הכללי: תכונות שבהן השונות הסביבתית תורמת הרבה (כמו דיכאון, שמושפע מאירועי חיים) יראו H² נמוך יותר.
למה האחרות שגויות:
- (א) H² גבוה אינו אומר “לא ניתן לשינוי” - ראו דוגמת PKU.
- (ג) H² אינו מונה גנים - תכונה עם H² נמוך יכולה להיות מאוד פוליגנית.
- (ד) H²=0.37 עדיין אומר ש־37% מהשונות גנטית - לא “אינו גנטי כלל”.
מקור: שקף 8
שאלה 9: מסלול ביוסינתזת מלאנין - אפיסטזיס
בגן TYR מקודד האנזים טירוזינאז, שהופך DOPA למלאנין. בגני OCA (כמו OCA2, OCA4) מקודדים חלבונים המווסתים את כמות ייצור המלאנין. אם ל־TYR יש מוטציה הומוזיגוטית (TYR‑/‑) אך גני OCA תקינים - מה יהיה הפנוטיפ, ומהי האינטראקציה הגנטית?
- פנוטיפ תקין - כי גני OCA תקינים יפצו על חוסר TYR ויווסתו ייצור מלאנין חלופי
- צבע עור כהה - כי חוסר TYR מוביל לצבירת DOPA שהופכת למלאנין באופן ספונטני
- לבקנות מלאה (Albinism) - כי ללא טירוזינאז אין ייצור מלאנין כלל, ולגני OCA אין על מה לווסת. זוהי דוגמה לאפיסטזיס - TYR אפיסטטי ל־OCA כי הוא נמצא בשלב מוקדם יותר במסלול
- הפחתה חלקית בצבע - כי TYR אינו האנזים היחיד שמייצר מלאנין, ולכן מסלולים אלטרנטיביים יפצו באופן חלקי
פתרון
התשובה הנכונה היא (3).
TYR (טירוזינאז) הוא האנזים המרכזי ליצירת מלאנין מ־DOPA. ללא TYR תקין - אין ייצור מלאנין כלל, גם אם כל מווסתי ה־OCA תקינים. לגני OCA אין על מה לפעול כי אין מצע (מלאנין) לווסת. זוהי אפיסטזיס (Epistasis): TYR הוא אפיסטטי ל־OCA - המוטציה ב־TYR “מסתירה” את ההשפעה של OCA. מוטציה ב־TYR (כרומוזום 11, OCA1) גורמת ללבקנות מהסוג החמור ביותר. שכיחות לבקנות: 1:17,000.
למה האחרות שגויות:
- (א) גני OCA אינם יכולים “לפצות” על חוסר TYR - הם לא מייצרים מלאנין בעצמם.
- (ב) DOPA לא הופכת למלאנין ספונטנית - נדרש אנזים טירוזינאז (שלב 4 במסלול).
- (ד) TYR הוא האנזים העיקרי - אין מסלול חלופי משמעותי ליצירת מלאנין.
מקור: שקפים 33–35
שאלה 10: לחץ סלקציה על צבע עור - ויטמין D מול פולאט
צבע עור כהה מגן מפני קרינת UV ומשמר פולאט (B9), אך מעכב ייצור ויטמין D. חוקר שואל: מדוע לאוכלוסיות בצפון אירופה עור בהיר? מהו ההסבר האבולוציוני?
- עור בהיר מגן טוב יותר מפני קור - ולכן נבחר בסלקציה באזורים קרים
- באזורים עם קרינת UV נמוכה, עור בהיר מאפשר ייצור מספיק ויטמין D גם בחשיפה מועטה, והפולאט אינו מפורק כי ה־UV חלש - ולכן עור בהיר מעניק יתרון סלקטיבי בסביבות אלו
- עור בהיר הוא סימפטום של חוסר מלאנין כתוצאה ממוטציות מזיקות שהצטברו בהעדר לחץ סלקציה - ולא תוצאה של סלקציה חיובית
- כל האוכלוסיות האנושיות היו בעלות עור בהיר במקור, ורק אלו שנדדו לאזורים טרופיים פיתחו עור כהה - לכן צפון אירופה שמר על המצב הקדום
פתרון
התשובה הנכונה היא (2).
יש התאמה גאוגרפית ברורה בין עוצמות UV לצבע עור: יותר קרינה = יותר מלאנין. בסביבות עם UV נמוך (צפון אירופה), פחות מלאנין מאפשר ייצור מספיק ויטמין D גם בחשיפה מועטה לשמש. במקביל, בסביבה עם UV נמוך אין סכנה לפירוק פולאט. לכן: עור בהיר = יתרון סלקטיבי באזורים עם UV נמוך. עור כהה = יתרון סלקטיבי באזורים עם UV גבוה (הגנה על פולאט + הגנה מנזקי UV, כאשר הגוף מייצר מספיק ויטמין D בגלל עוצמת הקרינה).
למה האחרות שגויות:
- (א) צבע עור אינו קשור להגנה מקור - הקשר הוא לקרינת UV.
- (ג) עור בהיר אינו “מזיק” - הוא מעניק יתרון ייצור ויטמין D בסביבת UV נמוך.
- (ד) המחקר מראה שהמצב הקדום היה עור כהה (מוצא אפריקאי), ועור בהיר התפתח בסלקציה חיובית.
מקור: שקפים 26–28
שאלה 11: לבקנות - הטרוגניות לוקוס
שני הורים עם לבקנות (Albinism) מביאים לעולם ילד עם פיגמנטציה תקינה. כיצד ניתן להסביר זאת?
- לבקנות היא תמיד דומיננטית, ולכן שני הורים חולים יכולים להביא ילד בריא בסיכוי 25%
- לבקנות יכולה להיגרם ממוטציות בגנים שונים (TYR, OCA2, OCA3, OCA4 ועוד) - אם כל הורה הומוזיגוט לגן אחר, הילד יהיה הטרוזיגוט בשני הגנים ויייצר מלאנין תקין דרך המסלול השלם
- הילד ירש מוטציה de novo מתקנת (Reversion mutation) שהחזירה את הגן למצב תקין
- אי־אפשר ששני הורים עם לבקנות יביאו ילד בעל פיגמנטציה תקינה - ההסבר היחיד הוא Non-paternity
פתרון
התשובה הנכונה היא (2).
לבקנות (Albinism) מדגימה הטרוגניות לוקוס (Locus heterogeneity) - אותו פנוטיפ (חוסר מלאנין) יכול להיגרם ממוטציות בגנים שונים על כרומוזומים שונים. למשל: OCA1 בכרומוזום 11 (TYR), OCA2 בכרומוזום 15, OCA3 בכרומוזום 9, OCA4 בכרומוזום 5, ועוד. אם אם הומוזיגוטית ל־OCA2 (OCA2⁻/⁻, TYR⁺/⁺) ואב הומוזיגוט ל־OCA1 (TYR⁻/⁻, OCA2⁺/⁺), הילד יהיה OCA2⁺/⁻ TYR⁺/⁻ - הטרוזיגוט בשני הגנים, עם עותק תקין אחד של כל אחד → ייצור מלאנין תקין.
למה האחרות שגויות:
- (א) לבקנות היא רצסיבית (AR), לא דומיננטית.
- (ג) מוטציה de novo מתקנת אפשרית תאורטית אך נדירה ביותר - ההסבר של הטרוגניות שכיח הרבה יותר.
- (ד) זה בהחלט אפשרי כאשר הגנים השונים - ואינו דורש הנחת Non-paternity.
מקור: שקפים 34–36
שאלה 12: Retinitis Pigmentosa - הטרוגניות גנטית
Retinitis Pigmentosa (RP) מערבת כ־70 גנים שונים ומראה דפוסי תורשה מגוונים. מה מייחד את RP כדוגמה למחלה גנטית מורכבת?
- RP היא תכונה פוליגנית קלאסית - כל חולה נושא מוטציות בעשרות גנים במקביל, ורק הצטברות של מספיק מוטציות גורמת למחלה
- RP מדגימה הטרוגניות אלילית ולוקוסית - אותו פנוטיפ (אבדן ראייה הדרגתי) יכול להיגרם ממוטציות בגנים שונים, בכרומוזומים שונים, ובדפוסי תורשה שונים (AR, AD, X-linked), כאשר אצל כל חולה בדרך כלל מוטציה אחת עיקרית אחראית
- RP מורשת תמיד בדפוס X-linked recessive כי רוב הגנים המעורבים נמצאים על כרומוזום X
- RP מדגימה אפיסטזיס בלבד - כל 70 הגנים פועלים במסלול ליניארי אחד, ופגיעה בכל שלב גורמת לאותו פנוטיפ
פתרון
התשובה הנכונה היא (2).
RP מדגימה הטרוגניות גנטית מרשימה: כ־70 גנים שונים, על כרומוזומים שונים, עם דפוסי תורשה מגוונים. מתוך המקרים הפתורים: ~62% AR, ~24% AD, ~14% X-linked. אצל כל חולה בדרך כלל יש מוטציה עיקרית אחת בגן אחד שאחראית לפנוטיפ. סוגי המוטציות מגוונים: Missense, Frameshift, Nonsense, Splicing, CNV, ועוד. הגן השכיח ביותר הוא USH2A (13 מקרים מתוך הנתונים). זהו הבדל חשוב מתכונה “פוליגנית” שבה מוטציות רבות במקביל תורמות כל אחת מעט.
למה האחרות שגויות:
- (א) RP אינה פוליגנית - בדרך כלל מוטציה אחת בגן אחד אחראית אצל כל חולה.
- (ג) רוב המקרים (62%) הם AR, לא X-linked.
- (ד) 70 הגנים אינם במסלול ליניארי אחד - הם בגנים שונים הקשורים לרשתית.
מקור: שקפים 37–38
שאלה 13: QTL Mapping - עיקרון
בניסוי מיפוי QTL, הכליאו עגבניות Beefmaster (גדולות) עם Sungold (קטנות), וב־Backcross (BC₁) קיבלו מנעד רציף של גדלים. כיצד השתמשו בנתונים אלה לזיהוי אזורים גנומיים שתורמים לגודל הפרי?
- זיהו גן יחיד שאחראי לגודל הפרי על ידי חיפוש יחסים מנדליאניים (3:1) ב־BC₁
- השתמשו בסמנים גנטיים (Markers) לאורך הגנום - בדקו עבור כל סמן אם יש קשר סטטיסטי בין הגנוטיפ בסמן לבין גודל הפרי; סמנים שהראו קורלציה מובהקת מצביעים על אזור גנומי שמכיל QTL
- ריצפו את כל הגנום של כל צמח ב־BC₁ וזיהו את כל ההבדלים ברצף בין צמחים גדולים לקטנים
- חיתכו כל כרומוזום באנזימי רסטריקציה ובדקו באיזה כרומוזום יש את הלהקה הגדולה ביותר
פתרון
התשובה הנכונה היא (2).
QTL Mapping מבוסס על שימוש בסמנים גנטיים (כמו SNPs, מיקרוסטליטים) הפזורים לאורך הגנום. עבור כל סמן, בודקים האם יש קורלציה סטטיסטית בין הגנוטיפ בסמן (בהורשה מ־Beefmaster או מ־Sungold) לבין ערך התכונה הכמותית (גודל הפרי). סמנים שמראים קשר מובהק ממוקמים בקרבת QTL - לוקוסים שתורמים לתכונה הכמותית. סמנים על כרומוזומים שונים יכולים לזהות לוקוסים מרובים. לאחר איפיון, ניתן לנבא תכונות לפי רצפים גנטיים - שימוש חשוב בחקלאות.
למה האחרות שגויות:
- (א) גודל פרי הוא תכונה כמותית/פוליגנית - אין יחסים מנדליאניים פשוטים.
- (ג) ריצוף גנום שלם של כל צמח לא היה ריאלי בטכנולוגיה הקלאסית, וגם כיום QTL mapping מבוסס על סמנים.
- (ד) שיטה זו לא מאפשרת מיפוי QTL.
מקור: שקפים 11–14
שאלה 14: GWAS - Manhattan Plot
בגרף Manhattan Plot ממחקר GWAS, ציר ה־X מציג את מיקום ה־SNPs לאורך 23 כרומוזומי האדם, וציר ה־Y מציג -log₁₀(p-value). חוקרת מבחינה שעבור Rheumatoid Arthritis (RA) ו־Type 1 Diabetes (T1D) יש שיאים בולטים באותו אזור בכרומוזום 6. מה ניתן להסיק?
- מדובר במחלה אחת עם שני שמות - RA ו־T1D הן למעשה ביטויים שונים של אותו גן
- הממצא מעיד על פליאוטרופיה - אותו אזור גנומי (HLA-DRB1) קשור לרגישות למחלות אוטואימוניות שונות, כי הוא מקודד לחלבוני MHC שמעורבים בזיהוי חיסוני
- מדובר בשגיאה סטטיסטית - אם שתי מחלות מראות אותו שיא, סימן שה־SNP אינו ספציפי
- השיא בכרומוזום 6 מעיד על כך ש־GWAS אינו יכול להבחין בין מחלות ולכן אינו שיטה אמינה
פתרון
התשובה הנכונה היא (2).
ב־Manhattan Plot מהשיעור, גם RA וגם T1D מראים שיא בולט באזור HLA-DRB1 על כרומוזום 6, וגם PTPN22 על כרומוזום 1. זהו ממצא חשוב ביולוגית: אזור ה־HLA מקודד לחלבוני MHC Class II שמעורבים בהצגת אנטיגנים למערכת החיסון. מוטציות באזור זה יכולות לגרום לתגובה אוטואימונית - ולכן הן מגבירות רגישות למחלות אוטואימוניות שונות. זוהי דוגמה לפליאוטרופיה: אותו לוקוס גנטי משפיע על מספר תכונות/מחלות שונות.
למה האחרות שגויות:
- (א) RA ו־T1D הן מחלות שונות בבירור (מפרקים מול לבלב) - אך חולקות רגישות גנטית משותפת.
- (ג) זו לא שגיאה - זוהי תובנה ביולוגית על מנגנון משותף.
- (ד) GWAS יכול להבחין היטב בין מחלות; העובדה שיש חפיפה היא ממצא ולא כשל.
מקור: שקף 14
שאלה 15: הבחנה בין תכונה מונוגנית לפוליגנית
חוקר רוצה להבדיל בין מחלה מונוגנית (כמו Sickle Cell Anemia) לבין מחלה מורכבת/פוליגנית (כמו מחלת עורקים כליליים). מהם הקריטריונים שיעזרו לו?
- מחלה מונוגנית מראה קונקורדנציה נמוכה ב־MZ ומחלה פוליגנית קונקורדנציה גבוהה ב־MZ
- מחלה מונוגנית עוקבת אחרי דפוסי תורשה מנדליאניים ברורים, נגרמת מווריאנט יחיד בעל אפקט גדול, וניתנת לאבחון ישיר; מחלה פוליגנית מושפעת ממספר רב של ווריאנטים בעלי אפקט קטן ומגורמי סביבה, ולא מראה דפוס מנדליאני
- מחלה מונוגנית תמיד חמורה ומחלה פוליגנית תמיד קלה - זה הקריטריון העיקרי
- הקריטריון היחיד הוא האם המחלה תורשתית או לא - מחלה מונוגנית תורשתית ומחלה פוליגנית אינה תורשתית
פתרון
התשובה הנכונה היא (2).
כפי שמודגם באיור מהשיעור: Sickle Cell Anemia - וריאנט גנומי אחד (על כרומוזום 11) אחראי למחלה כולה (Single gene disease). מחלת עורקים כליליים (Coronary artery disease) - ווריאנטים רבים על כרומוזומים רבים, כל אחד תורם מעט, בשילוב עם סביבה (Complex disease). ההבדלים: מחלה מונוגנית מראה דפוסי מנדל (AD/AR/XL), יחסים צפויים (3:1, 1:1), ואבחון על ידי זיהוי מוטציה אחת. מחלה פוליגנית יוצרת מנעד פנוטיפים, לא עוקבת אחרי דפוס מנדליאני, ומושפעת מסביבה.
למה האחרות שגויות:
- (א) להפך - מחלה מונוגנית נוטה לקונקורדנציה גבוהה יותר ב־MZ (אם גנטית טהורה).
- (ג) חומרה אינה הקריטריון - יש מחלות פוליגניות חמורות (סרטן) ומונוגניות קלות.
- (ד) שתיהן תורשתיות - ההבדל הוא באופן התורשה ובמספר הגנים.
מקור: שקפים 2–3
שאלות בנושא גנטיקה של אוכלוסיות
שאלות תרגול בגנטיקה של אוכלוסיות: חוק הרדי-ויינברג, חישובי שכיחות אללים וגנוטיפים, הנחות יסוד, סחיפה גנטית, אפקט מייסד, צוואר בקבוק, נישואי קרובים, ברירה טבעית, פאביזם G6PD.
שאלה 1: חישוב שכיחות נשאים - הטעות הנפוצה
Tay-Sachs היא מחלה אוטוזומלית רצסיבית. בקרב יהודים אשכנזים, 1 מכל 3,500 תינוקות נולד חולה. בהנחת שיווי-משקל HW, מה שכיחות הנשאים (Carriers) באוכלוסייה זו?
- שכיחות הנשאים היא 2q = 2×(1/3500) = 0.00057, כלומר כ־1 מתוך 1,750
- שכיחות הנשאים היא q² = 1/3500, ולכן q = 1/59, ושכיחות הנשאים 2pq ≈ 2×(1/59)×(58/59) ≈ 1/30 - כלומר כ־3 מכל 100 אנשים
- שכיחות הנשאים היא √(1/3500) = 1/59, כלומר כ־1 מתוך 59 - בלי צורך לכפול ב־2pq
- שכיחות הנשאים היא 2q² = 2/3500 = 1/1750, כי הנשאים שכיחים פי שניים מהחולים
פתרון
התשובה הנכונה היא (2).
הנתון: שכיחות חולים (aa) = q² = 1/3500. מכאן: q = √(1/3500) ≈ 1/59 ≈ 0.017. שכיחות האלל הדומיננטי: p = 1 - q = 1 - 0.017 = 0.983. שכיחות נשאים (Aa): 2pq = 2 × 0.017 × 0.983 ≈ 0.0334, כלומר כ־3 מכל 100 (או 1 מכל 30). זה ממצא מפתיע: למרות שרק 1/3500 חולים, כ־1/30 הם נשאים - כלומר הנשאים שכיחים פי ~117 מהחולים.
למה האחרות שגויות:
- (א) הטעות כאן היא שימוש ב־2q במקום 2pq. הנוסחה 2q אינה נכונה - צריך קודם לחלץ q מתוך q², כלומר לבצע שורש.
- (ג) √(1/3500) = q = שכיחות האלל, לא שכיחות הנשאים. שכיחות הנשאים היא 2pq, לא q.
- (ד) הכפלת q² ב־2 אינה נותנת את שכיחות הנשאים - 2pq ≠ 2q².
מקור: שקפים 12–13
שאלה 2: חישוב שכיחות אללים מתוך תורשה קו־דומיננטית
בפרחי Mirabilis, אלל A₁ נותן צבע סגול (A₁A₁), אלל A₂ נותן לבן (A₂A₂), והטרוזיגוט (A₁A₂) נותן ורוד. במדגם של 200 פרחים: 98 סגולים, 84 ורודים, 18 לבנים. מה שכיחות האלל A₁?
- p(A₁) = 98/200 = 0.49, כי שכיחות האלל שווה לשכיחות ההומוזיגוטים
- p(A₁) = (98 + 84) / 200 = 0.91, כי כל מי שנושא לפחות עותק אחד של A₁ תורם לשכיחותו
- p(A₁) = (2×98 + 84) / (2×200) = 280/400 = 0.70, כי כל פרט תורם שני אללים ולכן יש 400 אללים בסך הכל
- p(A₁) = √(98/200) = √0.49 = 0.70, כי לפי HW שכיחות ההומוזיגוטים שווה ל־p² ולכן p = √(p²)
פתרון
התשובה הנכונה היא (3).
בתורשה קו־דומיננטית, כל גנוטיפ ניתן לזיהוי ישיר, ולכן ניתן לספור אללים ישירות: סה”כ אללים = 2 × 200 = 400 (כי כל פרט דיפלואידי תורם 2 אללים). אללי A₁: כל A₁A₁ תורם 2, כל A₁A₂ תורם 1: (2×98) + (1×84) = 196 + 84 = 280. לכן p(A₁) = 280/400 = 0.70. בדיקה: q(A₂) = (2×18 + 84)/400 = 120/400 = 0.30. p + q = 1 ✓.
למה האחרות שגויות:
- (א) שכיחות הפנוטיפ הסגול (98/200) = p² = 0.49, לא p. מבלבלים בין שכיחות גנוטיפ לשכיחות אלל.
- (ב) לא כל נושא A₁ תורם אותו דבר - הומוזיגוט תורם 2 אללים והטרוזיגוט רק 1.
- (ד) התוצאה המספרית זהה (0.70), אך השיטה שגויה עקרונית: שיטת השורש תקפה רק בהנחת HW, בעוד ספירה ישירה עובדת תמיד בקו־דומיננטיות ואינה דורשת הנחת שיווי-משקל.
מקור: שקפים 6–7
שאלה 3: הנחות הרדי-ויינברג - זיהוי הפרה
חוקרת בודקת אוכלוסיית ציפורים באי קטן ומוצאת שהגנוטיפים בלוקוס מסוים אינם עומדים בשיווי-משקל HW - יש עודף הומוזיגוטים וחוסר הטרוזיגוטים ביחס לציפייה. מהו ההסבר הסביר ביותר?
- ברירה טבעית פועלת נגד ההטרוזיגוטים - כלומר לבעלי הגנוטיפ ההטרוזיגוטי כושר הישרדות נמוך יותר
- מוטציות חדשות יוצרות אללים נוספים שמגדילים את שיעור ההומוזיגוטים באוכלוסייה
- הזיווגים אינם אקראיים - ייתכן שהציפורים בוחרות בני זוג דומים להן פנוטיפית (Assortative mating) או שבאי קטן יש נישואי קרובים (Inbreeding), מה שמגביר את שיעור ההומוזיגוטים
- גודל האוכלוסייה גדול מדי ולכן הסיכוי למפגש בין אללים שונים נמוך, מה שגורם לעודף הומוזיגוטים
פתרון
התשובה הנכונה היא (3).
עודף הומוזיגוטים + חוסר הטרוזיגוטים הוא הסימן ההיכר הקלאסי של זיווג לא־אקראי (Non-random mating), ובפרט Inbreeding (נישואי קרובים). באי קטן, הפרטים קרובים גנטית זה לזה, ולכן סיכוי גבוה שהצאצאים יהיו הומוזיגוטיים. Assortative mating (בחירת בן זוג דומה) גם מגביר הומוזיגוטיות. שני המנגנונים מפרים את הנחת ה”זיווגים אקראיים” של HW.
למה האחרות שגויות:
- (א) ברירה נגד הטרוזיגוטים (Underdominance) אפשרית תאורטית אך נדירה בטבע; Inbreeding באי קטן הוא הסבר סביר הרבה יותר ופשוט יותר.
- (ב) מוטציות חדשות יוצרות אללים חדשים אך לא גורמות באופן ישיר לעודף הומוזיגוטים - להפך, הן מגבירות שונות.
- (ד) להפך - אוכלוסייה גדולה מקיימת HW טוב יותר. אוכלוסייה קטנה רגישה לסחיפה ול־Inbreeding.
מקור: שקפים 14–15, 18
שאלה 4: הנחות HW - איזו הנחה מופרת?
באוכלוסיית טריסטן דה קונייה (238 תושבים, צאצאי משפחה סקוטית מ־1817), נמצאו שיעורים גבוהים של גלאוקומה ואסתמה. חוקר טוען שהאוכלוסייה “אינה בשיווי-משקל HW”. כמה מתוך חמש הנחות היסוד של HW מופרות באוכלוסייה זו?
- הנחה אחת בלבד - גודל אוכלוסייה קטן (הפרה של “מספר פרטים גדול/אינסופי”)
- שתי הנחות - גודל אוכלוסייה קטן + היעדר הגירה (האי מבודד)
- לפחות שלוש הנחות - גודל אוכלוסייה קטן (סחיפה גנטית), היעדר הגירה (בידוד גאוגרפי), וזיווגים אינם אקראיים (אוכלוסייה קטנה שבהכרח מתחתנת בתוך עצמה)
- כל חמש ההנחות מופרות - כי באוכלוסייה קטנה כל ההנחות נופלות אוטומטית
פתרון
התשובה הנכונה היא (3).
טריסטן דה קונייה מפרה לפחות שלוש הנחות: (1) אוכלוסייה קטנה - 238 תושבים, רחוק מ”אינסופי”, → סחיפה גנטית חזקה; (2) אין הגירה - האי מרוחק 2,816 ק”מ מדרום אפריקה ו־3,360 ק”מ מדרום אמריקה, כמעט ללא הגירה פנימה; (3) זיווגים אינם אקראיים - באוכלוסייה כה קטנה, כולם קרובי משפחה במידה מסוימת → Inbreeding בלתי נמנע. השיעור הגבוה של גלאוקומה ואסתמה נובע מאפקט מייסד + סחיפה + Inbreeding.
למה האחרות שגויות:
- (א) גודל האוכלוסייה אינו ההפרה היחידה - הבידוד הגאוגרפי וה־Inbreeding הם הפרות נוספות משמעותיות.
- (ב) חסרה ההפרה של זיווגים לא־אקראיים - שהיא קריטית באוכלוסייה כה קטנה.
- (ד) לאו דווקא כל חמש - עדיין יכולות להתרחש מוטציות חדשות, וברירה טבעית לא בהכרח פועלת על כל לוקוס.
מקור: שקפים 14–15, 25–27
שאלה 5: אפקט מייסד מול צוואר בקבוק
מה ההבדל המהותי בין אפקט מייסד (Founder Effect) לבין צוואר בקבוק גנטי (Bottleneck Effect)?
- אפקט מייסד מתרחש כאשר קבוצה קטנה נודדת ומקימה אוכלוסייה חדשה במיקום חדש, ואילו צוואר בקבוק מתרחש כאשר אוכלוסייה קיימת עוברת צמצום דרסטי (כמו אסון טבע) ואז מתאוששת - בשניהם, ההרכב הגנטי של האוכלוסייה הקטנה שנותרה אינו מייצג את האוכלוסייה המקורית
- אפקט מייסד חל רק על אוכלוסיות אנושיות וצוואר בקבוק חל רק על בעלי חיים, אך המנגנון הגנטי זהה
- באפקט מייסד שכיחות האללים משתנה כי הנודדים בוחרים אללים מסוימים (סלקציה), בעוד שבצוואר בקבוק השינוי הוא אקראי לחלוטין
- צוואר בקבוק מגביר שונות גנטית כי רק האללים ה”חזקים” שורדים, בעוד אפקט מייסד מפחית שונות
פתרון
התשובה הנכונה היא (1).
שניהם סוגים של סחיפה גנטית (Genetic Drift) - שינוי אקראי בשכיחות אללים עקב גודל אוכלוסייה קטן. ההבדל: אפקט מייסד - קבוצה קטנה נודדת ומקימה אוכלוסייה חדשה (כמו המשפחה הסקוטית שהגיעה לטריסטן דה קונייה ב־1817). צוואר בקבוק - אוכלוסייה קיימת עוברת צמצום חד (אסון טבע, מגפה) ורק מעטים שורדים. בשני המקרים, האוכלוסייה הקטנה שנותרת/נוצרת אינה מייצגת את השונות הגנטית המקורית, ואללים מסוימים עלולים להיעלם או להיות מיוצגים ביתר.
למה האחרות שגויות:
- (ב) שני התהליכים חלים על כל אורגניזם - אין הגבלה לסוג.
- (ג) באפקט מייסד השינוי הוא גם אקראי - הנודדים לא “בוחרים” אללים; ההרכב שלהם מקרי.
- (ד) צוואר בקבוק מפחית שונות גנטית (אובדן אללים), לא מגביר.
מקור: שקפים 26–27
שאלה 6: נישואי קרובים - ההשפעה על שכיחות מחלות רצסיביות
נתונים ממשרד הבריאות הישראלי מראים שבכפר ערבי-מוסלמי אחד (~10,000 תושבים) אובחנו 43 משפחות עם חירשות (Connexin 26), 27 משפחות עם Retinitis Pigmentosa, ו־9 משפחות עם תלסמיה. רוב המחלות הן אוטוזומליות רצסיביות. מדוע שיעור המחלות הרצסיביות גבוה באופן יחסי דווקא באוכלוסייה זו?
- כי באוכלוסייה קטנה וסגורה עם שיעור גבוה של נישואי קרובים (67% בקרב בדואים בנגב), בני הזוג חולקים שכיחות גבוהה יותר של אללים זהים מאב־קדמון משותף - ולכן הסיכוי שצאצאיהם יהיו הומוזיגוטים רצסיביים (aa) גבוה הרבה יותר מאשר באוכלוסייה פתוחה
- כי באוכלוסייה קטנה שיעור המוטציות גבוה יותר, ולכן נוצרים יותר אללים רצסיביים חדשים בכל דור
- כי ברירה טבעית באוכלוסייה קטנה פועלת לטובת האלל הרצסיבי - נשאים הטרוזיגוטיים מקבלים יתרון הישרדות
- כי נישואי קרובים משנים את שכיחות האלל הרצסיבי (q) באוכלוסייה ומגדילים אותה, ולכן גם q² עולה
פתרון
התשובה הנכונה היא (1).
נישואי קרובים (Consanguinity) מגדילים את שיעור ההומוזיגוטיות, לא את שכיחות האלל. כשבני דודים ראשונים מתחתנים, הם חולקים 1/8 מהגנום שלהם. אם אלל רצסיבי נדיר קיים במשפחה, הסיכוי ששני בני הזוג הם נשאים גבוה בהרבה מאשר בזיווג אקראי. הנתונים מישראל מראים שיעורי נישואי קרובים גבוהים: בדואים בנגב 67% (35% בני דודים ראשונים), דרוזים 54% (33% בני דודים ראשונים). התוצאה: עלייה במחלות AR ובמומים מולדים.
למה האחרות שגויות:
- (ב) שיעור המוטציות אינו תלוי בגודל האוכלוסייה - Inbreeding אינו מגביר מוטציות.
- (ג) אין יתרון הטרוזיגוטי ידוע עבור חירשות או RP - אלה פשוט מצטברות בגלל Inbreeding.
- (ד) נישואי קרובים אינם משנים את שכיחות האלל (q) - הם משנים את שכיחות הגנוטיפים (מגדילים הומוזיגוטים על חשבון הטרוזיגוטים) בלי לשנות את p ו־q עצמם.
מקור: שקפים 20–22
שאלה 7: נישואי קרובים - השפעה על שכיחויות אללים מול שכיחויות גנוטיפים
באוכלוסייה שבה p=0.9 ו־q=0.1, ויש שיעור גבוה של נישואי קרובים, מה צפוי לקרות לשכיחויות הגנוטיפים בהשוואה לציפיות HW?
- שכיחות AA תעלה מעל p², שכיחות aa תעלה מעל q², ושכיחות Aa תרד מתחת ל־2pq - כי Inbreeding מגביר הומוזיגוטיות על חשבון הטרוזיגוטיות, בעוד p ו־q עצמם נשארים ללא שינוי
- שכיחות q תעלה ושכיחות p תרד - כי Inbreeding מעדיף את האלל הרצסיבי
- כל הגנוטיפים ישארו בהתאם לציפיות HW - כי HW תלוי רק בשכיחות אללים ולא באופן הזיווג
- שכיחות aa תעלה אך שכיחות AA תרד - כי Inbreeding מגביר רק את ההומוזיגוטים לאלל הנדיר
פתרון
התשובה הנכונה היא (1).
Inbreeding מגביר הומוזיגוטיות - של שני הסוגים (AA וגם aa) - על חשבון הטרוזיגוטים (Aa). הסיבה: כשבני זוג קרובים גנטית, סיכוי גבוה שהצאצא יקבל שני עותקים של אותו אלל (IBD - Identical by descent). חשוב: שכיחויות האללים p ו־q עצמן אינן משתנות - רק ההתפלגות בין גנוטיפים משתנה. עם מקדם Inbreeding (F): שכיחות AA = p² + Fpq, שכיחות Aa = 2pq - 2Fpq, שכיחות aa = q² + Fpq.
למה האחרות שגויות:
- (ב) Inbreeding לא משנה את p ו־q - הוא משנה רק את חלוקת הגנוטיפים.
- (ג) HW דורש זיווג אקראי - Inbreeding הוא הפרה ישירה שמשנה שכיחויות גנוטיפים.
- (ד) Inbreeding מגביר את שני סוגי ההומוזיגוטים (AA וגם aa), לא רק את aa.
מקור: שקפים 14–15, 18–20
שאלה 8: ברירה טבעית - פאביזם ויתרון ההטרוזיגוט
פאביזם (חסר G6PD) היא מחלה רצסיבית מקושרת ל־X, השכיחה באזור הים התיכון. החוסר באנזים G6PD גורם לאנמיה המוליטית בחשיפה לפול, זיהומים או תרופות. למרות הנזק, המוטציה שכיחה מאוד באזורים מסוימים. מדוע?
- כי המוטציה היא ניטרלית - אנמיה המוליטית קלה מספיק כדי לא להפחית כושר הישרדות, ולכן אין ברירה נגדה
- כי המוטציה מעניקה עמידות למלריה - תאי דם אדומים עם חוסר G6PD מהווים סביבה פחות מתאימה לטפיל הפלסמודיום, ולכן באזורים אנדמיים למלריה יש יתרון סלקטיבי לנושאי המוטציה שמפצה על הנזק מאנמיה המוליטית (ברירה מאזנת)
- כי סחיפה גנטית באוכלוסיות קטנות באזור הים התיכון העלתה את שכיחות המוטציה באופן אקראי - ללא כל יתרון סלקטיבי
- כי המוטציה נוצרת שוב ושוב (Recurrent mutation) בשיעור גבוה באזור הים התיכון בגלל גורמים סביבתיים כמו קרינה, ולכן היא שכיחה למרות שהיא מזיקה
פתרון
התשובה הנכונה היא (2).
זוהי דוגמה קלאסית לברירה מאזנת (Balancing Selection) / יתרון ההטרוזיגוט - בדומה לאנמיה חרמשית. החוסר ב־G6PD מעניק עמידות למלריה. באזורים שבהם מלריה אנדמית (אזור הים התיכון, אפריקה, דרום-מזרח אסיה), היתרון בעמידות למלריה מפצה על הנזק מאנמיה המוליטית. לכן הברירה הטבעית שומרת על האלל הפגום בשכיחות גבוהה - זהו מצב שבו ברירה טבעית מפרה את HW ומונעת מהאלל המזיק להיעלם.
למה האחרות שגויות:
- (א) אנמיה המוליטית אינה ניטרלית - ללא יתרון המלריה, המוטציה הייתה פוחתת בשכיחותה בגלל ברירה שלילית.
- (ג) סחיפה לבדה לא מסבירה את ההתפלגות הגאוגרפית שחופפת לאזורי מלריה - זה מצביע על ברירה.
- (ד) שיעור מוטציות אינו תלוי באזור גאוגרפי באופן שמסביר שכיחות כה גבוהה.
מקור: שקפים 32–35
שאלה 9: ארבעת כוחות האבולוציה - זיהוי תהליך
באיור מהשיעור מוצגות ארבע אוכלוסיות חיפושיות: באחת מופיע אלל חדש A שלא היה קיים (Aa אחד מופיע בין aa), בשנייה חיפושיות מאוכלוסייה צהובה (AA) מגיעות לאוכלוסייה ירוקה (aa), בשלישית אוכלוסייה קטנה מאבדת אללים באקראי, וברביעית ציפור טורפת חיפושיות ירוקות ומשאירה צהובות. התאם:
- 1=מוטציה, 2=הגירה, 3=ברירה טבעית, 4=סחיפה גנטית
- 1=הגירה, 2=מוטציה, 3=סחיפה גנטית, 4=ברירה טבעית
- 1=מוטציה, 2=הגירה, 3=סחיפה גנטית, 4=ברירה טבעית
- 1=סחיפה גנטית, 2=הגירה, 3=מוטציה, 4=ברירה טבעית
פתרון
התשובה הנכונה היא (3).
- (1) מוטציה - אלל חדש (A) נוצר באוכלוסייה שבה כולם היו aa; מוטציה היא המקור היחיד לשונות גנטית חדשה.
- (2) הגירה (Gene flow) - פרטים עם גנוטיפ AA מאוכלוסייה אחרת מגיעים לאוכלוסייה של aa; ההגירה משנה שכיחויות אללים.
- (3) סחיפה גנטית - באוכלוסייה קטנה, אללים אובדים באופן אקראי (לא על בסיס כושר); זה תוצאה של גודל אוכלוסייה קטן.
- (4) ברירה טבעית - ציפור טורפת חיפושיות ירוקות (aa) ← שורדות הצהובות (AA, Aa) ← שכיחות A עולה בגלל כושר הישרדות.
למה האחרות שגויות:
- (א) מבלבל בין ברירה טבעית (4) לסחיפה (3): סחיפה = אקראית, ברירה = לא־אקראית (על בסיס כושר).
- (ב) מבלבל בין מוטציה (אלל חדש נוצר) להגירה (אלל קיים מגיע מבחוץ).
- (ד) מוטציה = אלל חדש, לא אובדן אקראי.
מקור: שקף 2
שאלה 10: חישוב HW - שימוש קליני
לזוג הורים בריאים נולד ילד חולה במחלה אוטוזומלית רצסיבית נדירה (שכיחות 1/10,000). לזוג גם בת בריאה. הבת מתחתנת עם גבר בריא מהאוכלוסייה הכללית. מה הסיכוי שייוולד להם ילד חולה?
- הסיכוי הוא (2/3) × (2q) × (1/4) - הסיכוי שהבת נשאית הוא 2/3 (ולא 1/2, כי ידוע שהיא בריאה), הסיכוי שהחתן נשא הוא 2pq ≈ 2q (כאשר q=1/100), והסיכוי לילד חולה מזיווג Aa×Aa הוא 1/4
- הסיכוי הוא (1/2) × (1/100) × (1/4) = 1/800 - הסיכוי שהבת נשאית הוא 1/2, הסיכוי שהחתן נשא הוא q=1/100, והסיכוי לילד חולה 1/4
- הסיכוי הוא (2/3) × (1/100) × (1/4) - כי הסיכוי שהחתן נשא הוא q ולא 2pq
- הסיכוי הוא (2/3) × (1/50) × (1/4) = 1/300 - הסיכוי שהבת נשאית 2/3, שכיחות נשאים 2pq ≈ 1/50, סיכוי לילד חולה 1/4
פתרון
התשובה הנכונה היא (4).
שלב 1 - שכיחות אללים: שכיחות חולים = q² = 1/10,000, לכן q = 1/100 = 0.01, p = 0.99.
שלב 2 - סיכוי שהבת נשאית: ההורים שניהם Aa. הצאצאים האפשריים: AA (1/4), Aa (2/4), aa (1/4). אך ידוע שהבת בריאה, לכן מתוך 3 אפשרויות (AA, Aa, Aa): הסיכוי שהיא Aa = 2/3.
שלב 3 - סיכוי שהחתן נשא: הוא בריא מאוכלוסייה כללית. שכיחות נשאים = 2pq = 2 × 0.99 × 0.01 ≈ 0.02 = 1/50.
שלב 4 - סיכוי לילד חולה (אם שניהם נשאים): 1/4.
סה”כ: (2/3) × (1/50) × (1/4) = 2/600 = 1/300.
למה האחרות שגויות:
- (א) שכיחות נשאים היא 2pq ≈ 1/50 ולא 2q = 2/100. (כי 2pq = 2×0.99×0.01 ≈ 0.0198 ≈ 1/50, לא 2×0.01 = 0.02 - במקרה זה הערכים קרובים, אך הנוסחה ב־א כותבת “2q” בלי p).
- (ב) הסיכוי שהבת נשאית הוא 2/3 (לא 1/2) כי ידוע שהיא בריאה, ו־q=1/100 הוא שכיחות האלל, לא שכיחות הנשאים.
- (ג) שכיחות הנשאים היא 2pq (לא q) - q הוא שכיחות האלל הרצסיבי.
מקור: שקפים 3, 12–13
שאלה 11: מוטציה כגורם להפרת HW
מה יקרה לשכיחויות האללים באוכלוסייה אם מתרחשות מוטציות חדשות בשיעור קבוע?
- המוטציות ישנו את שכיחויות הגנוטיפים אך לא את שכיחויות האללים - כי מוטציה משנה את האלל בתוך הפרט אך לא את סך האללים באוכלוסייה
- המוטציות יכניסו אללים חדשים לאוכלוסייה ויגדילו את השונות הגנטית - אך בפועל, שיעור המוטציות הטבעי נמוך מאוד (כ־10⁻⁶ לכל לוקוס לדור), ולכן לבדן הן משנות שכיחויות אללים באופן איטי ביותר, וההשפעה משמעותית רק בשילוב עם כוחות אחרים כמו ברירה או סחיפה
- המוטציות תמיד יגרמו לעלייה בשכיחות האלל הרצסיבי כי רוב המוטציות הן loss-of-function
- מוטציות אינן מפרות שיווי-משקל HW כלל - רק הגירה, סחיפה וברירה טבעית מפרות אותו
פתרון
התשובה הנכונה היא (2).
מוטציות הן המקור היחיד לשונות גנטית חדשה - הן מכניסות אללים חדשים שלא היו קיימים באוכלוסייה. עם זאת, שיעור המוטציות הטבעי נמוך מאוד (~10⁻⁵–10⁻⁶ לכל לוקוס לכל דור), ולכן לבדן הן משנות שכיחויות אללים לאט מאוד. השפעתן המשמעותית היא ביצירת החומר הגולמי (שונות) שעליו פועלים כוחות אחרים: ברירה טבעית יכולה לקדם או להדחיק אלל חדש, סחיפה יכולה לקבע אותו באוכלוסייה קטנה.
למה האחרות שגויות:
- (א) מוטציה כן משנה שכיחות אללים - היא יוצרת אלל חדש ומשנה את p ו־q (גם אם מעט).
- (ג) מוטציות יכולות להיות gain-of-function, loss-of-function, או ניטרליות - לא תמיד “רצסיביות”.
- (ד) מוטציות הן אחת מחמש ההנחות של HW (“אין מוטציות חדשות”) - הפרתן מפרה HW.
מקור: שקפים 14, 29–31
שאלה 12: הכלאה עצמית בצמחים - ההשפעה על הטרוזיגוטיות
בצמח המבצע הכלאה עצמית (Self-fertilization), מה קורה לשיעור ההטרוזיגוטים לאורך דורות?
- שיעור ההטרוזיגוטים נשאר יציב - כי בכל דור ההטרוזיגוטים מייצרים הטרוזיגוטים חדשים ביחס 1:2:1, ולכן ההטרוזיגוטיות מתחדשת
- שיעור ההטרוזיגוטים יורד בחצי בכל דור - כי הכלאה עצמית של Aa נותנת 1/4 AA, 1/2 Aa, 1/4 aa, כך שבכל דור מחצית מההטרוזיגוטים הופכים להומוזיגוטים, עד שההטרוזיגוטיות שואפת לאפס
- שיעור ההטרוזיגוטים עולה - כי הכלאה עצמית מגבירה מגוון גנטי על ידי שחלוף (Crossing-over) בזמן מיוזה
- ההשפעה תלויה באלל הדומיננטי - הטרוזיגוטיות יורדת רק אם האלל הרצסיבי מזיק, כי אז ברירה פועלת נגד ההומוזיגוטים הרצסיביים
פתרון
התשובה הנכונה היא (2).
הכלאה עצמית (Self-fertilization) היא צורה קיצונית של Inbreeding. כשצמח Aa מפרה את עצמו: הצאצאים הם 1/4 AA, 1/2 Aa, 1/4 aa. כלומר - מ־100% הטרוזיגוטים בדור 0, נשארים 50% הטרוזיגוטים בדור 1. בדור 2, שוב מחציתם הופכים להומוזיגוטים → 25%. וכן הלאה: 12.5%, 6.25%… הסדרה שואפת לאפס. בסופו של תהליך, כמעט כל הפרטים הומוזיגוטיים - AA או aa. שכיחויות האללים p ו־q אינן משתנות, רק ההתפלגות בין גנוטיפים.
למה האחרות שגויות:
- (א) ההטרוזיגוטים כן מייצרים הטרוזיגוטים, אך רק מחציתם - לכן יש ירידה נטו.
- (ג) שחלוף (Crossing-over) משנה קישור בין לוקוסים שונים, לא שיעור הטרוזיגוטיות בלוקוס אחד.
- (ד) הירידה בהטרוזיגוטיות היא מתמטית-מכנית ולא תלויה בברירה.
מקור: שקף 28
שאלה 13: דור ישרים - עיקרון ואתיקה
תוכנית “דור ישרים” מבצעת בדיקות התאמה גנטית באוכלוסייה החרדית. מה העיקרון הייחודי של התוכנית?
- בדיקת נשאות נעשית לכל אחד מבני הזוג הפוטנציאליים, התוצאות נשמרות במאגר אנונימי (מספרי זיהוי בלבד, ללא שמות או ת.ז.), והתשובה ניתנת כ”יש התאמה” או “אין התאמה” - מבלי לפרט מי נשא ולאיזו מחלה
- בדיקת נשאות לזוג בלבד לאחר אירוסין, עם פירוט מלא של סטטוס הנשאות של כל אחד מבני הזוג לכל מחלה
- בדיקה גנומית מלאה (Whole Genome Sequencing) שמאפשרת לכל אדם לדעת את כל המוטציות שהוא נושא, והתוצאות נשמרות במאגר ציבורי
- בדיקה שמתבצעת רק לאחר לידת ילד חולה, כדי לזהות את המוטציה הספציפית ולמנוע לידות נוספות
פתרון
התשובה הנכונה היא (1).
דור ישרים היא תוכנית ייחודית שמשלבת מניעה רפואית עם שמירה על פרטיות ועל ערכי הקהילה: (1) בדיקת נשאות לכל אחד - לא רק לזוגות. (2) מאגר אנונימי - מספרי זיהוי אקראיים בלבד, ללא שמות או ת.ז. (3) התשובה בינארית: “יש התאמה” (שניהם נשאים לאותה מחלה - אין לשדך) או “אין התאמה” (אפשר לשדך). (4) לא מפרטים מי נשא ולאיזו מחלה - כדי למנוע סטיגמה. כך, זוגות שאינם מתאימים גנטית לא ישודכו, אך אף אחד לא “מתויג” כנשא.
למה האחרות שגויות:
- (ב) הבדיקה נעשית לפני שידוך (לא לאחר אירוסין), ואינה מפרטת פרטים ספציפיים.
- (ג) אין ריצוף גנומי מלא - רק בדיקות נשאות ממוקדות, והמאגר אנונימי, לא ציבורי.
- (ד) הבדיקה היא מניעתית (לפני נישואין) - לא לאחר לידת ילד חולה.
מקור: שקף 23
שאלה 14: יישום HW - חישוב שכיחות נשאים בקו־דומיננטיות
באוכלוסיית פרחי Mirabilis עם p(A₁) = 0.7 ו־q(A₂) = 0.3, חוקר רוצה לדעת: אם אבחר פרח ורוד (A₁A₂) ואכליא אותו עם פרח ורוד אחר, מה ההסתברות לקבל פרח לבן (A₂A₂)?
- 1/4 - כי הכלאת Aa × Aa נותנת 1/4 aa לפי מנדל, וזה לא תלוי בשכיחויות באוכלוסייה
- q² = 0.09 - כי ההסתברות לקבל A₂A₂ באוכלוסייה היא תמיד q² לפי HW
- (0.3)² = 0.09 - כי גם בהכלאה ספציפית ההסתברות נקבעת לפי שכיחויות האללים באוכלוסייה
- 1/2 × 1/2 = 1/4 - כי כל הורה ורוד (A₁A₂) מעביר A₂ בהסתברות 1/2, וההסתברות שגם מהאב וגם מהאם יגיע A₂ היא 1/4 (כמו ב־א’, אך הנימוק שונה)
פתרון
התשובה הנכונה היא (א) (ו־(ד) - שתיהן מגיעות לאותה תוצאה בנימוקים שונים אך תקפים).
כאשר מכליאים פרח ורוד (A₁A₂) × פרח ורוד (A₁A₂), זוהי הכלאה ספציפית - לא דגימה אקראית מהאוכלוסייה. לכן שכיחויות האוכלוסייה (p ו־q) אינן רלוונטיות. לפי חוק ההפרדה של מנדל: כל הורה הטרוזיגוט מעביר A₁ בהסתברות 1/2 ו־A₂ בהסתברות 1/2. הצאצאים: 1/4 A₁A₁ (סגול), 1/2 A₁A₂ (ורוד), 1/4 A₂A₂ (לבן). לכן ההסתברות ל־A₂A₂ = 1/4. תשובה (ד) מגיעה לאותה תוצאה בנימוק מפורט זהה.
למה האחרות שגויות:
- (ב) q² = 0.09 היא שכיחות A₂A₂ באוכלוסייה, לא בהכלאה ספציפית בין שני ורודים.
- (ג) אותה טעות - שימוש בשכיחויות אוכלוסייה להכלאה ספציפית.
מקור: שקפים 5–10
שאלה 15: אינטגרציה - זיהוי התהליך מתוך תרחיש
באוכלוסייה של 500,000 אנשים, מחלה אוטוזומלית רצסיבית מופיעה בשכיחות q²=1/40,000 (q≈0.005). קבוצה של 200 מתיישבים מתוך אוכלוסייה זו מקימה יישוב מבודד. לאחר 10 דורות, שכיחות המחלה ביישוב עולה ל־1/2,500. אילו תהליכים עלולים להסביר זאת?
- ברירה טבעית בלבד - האלל הרצסיבי מעניק יתרון הטרוזיגוטי ביישוב החדש
- מוטציות חדשות בלבד - שיעור מוטציות גבוה ביישוב החדש יצר אללים רצסיביים חדשים
- שילוב של אפקט מייסד (ייתכן שהמתיישבים המקוריים כללו שיעור נשאים גבוה מהממוצע), סחיפה גנטית (אוכלוסייה קטנה → שינויים אקראיים גדולים), ו־Inbreeding (ביישוב קטן ומבודד, נישואי קרובים בלתי נמנעים → עלייה בהומוזיגוטיות)
- הגירה בלבד - אנשים עם שכיחות גבוהה של האלל הרצסיבי הגיעו ליישוב מאוכלוסיות אחרות
פתרון
התשובה הנכונה היא (3).
התרחיש מתאר עלייה דרמטית בשכיחות מחלה רצסיבית: מ־1/40,000 ל־1/2,500 (פי 16). שלושה תהליכים משלימים מסבירים זאת:
(1) אפקט מייסד: 200 מתיישבים אינם מייצגים את שכיחויות האללים באוכלוסייה הגדולה. אם במקרה כללו שיעור נשאים (2pq) גבוה מהממוצע, q ביישוב גבוה מ־0.005.
(2) סחיפה גנטית: באוכלוסייה של 200 (ואפילו כמה אלפים לאחר צמיחה), שינויים אקראיים בשכיחות אללים משמעותיים - q עלול לעלות באקראי.
(3) Inbreeding: ביישוב קטן ומבודד, לאחר מספר דורות כולם קרובי משפחה → נישואי קרובים → עלייה בהומוזיגוטיות → יותר aa.
למה האחרות שגויות:
- (א) אין סיבה להניח יתרון הטרוזיגוטי ללא ראיות ספציפיות - ההסבר הפשוט הוא סחיפה + Inbreeding.
- (ב) שיעור מוטציות לבדו (~10⁻⁵-10⁻⁶) אינו מסביר עלייה כה דרמטית ב־10 דורות.
- (ד) נאמר שהיישוב מבודד - אין הגירה משמעותית.
מקור: שקפים 14, 25–27