תוכן העניינים:
- חזרה על שיעור הקודם - שאלות פתיחה
- חלק א: צנטרומרים
- חלק ב: קוהזין וסגרגציה
- חלק ג: תסמונת דאון וגיל האם
- חלק ד: הכפלת DNA - מבוא
- חלק ה: DNA פולימראז - מאפיינים ומנגנון
חזרה על שיעור הקודם - שאלות פתיחה
הטרוכרומטין ואאוכרומטין: הטרוכרומטין הוא המבנה הדחוס (הסגור) והאאוכרומטין הפתוח. כשמסתכלים על גרעין במיקרוסקופ אלקטרוני, הגרעינון (nucleolus) נראה צפוף ועל כן דומה מבחינה ויזואלית להטרוכרומטין - אך זאת תוצאה של צפיפות גבוהה של DNA, ולא של דחיסה פונקציונלית. חשוב לזכור: במיקרוסקופ אלקטרוני בוחנים צפיפות ולא מצב פתיחה/סגירה של כרומטין. לכן אזורים פעילים ביותר כמו הגרעינון, שיש בהם הרבה טרנסקריפציה, עשויים להיראות כהים על אף שהכרומטין שלהם פתוח.
מחלת פרוגריה (Progeria): הבעיה שם היא בחיבור הלמינה לממברנת הגרעין - ניתוק בין קישור הכרומטין ל־lamina (חומר מביולוגיה של התא).
TADs ו־CTCF: CTCF נקשר לרצפים ספציפיים ב־DNA, וכי גודל ה־TAD נקבע לפי ה־scaffold של CTCF כשהוא פועל בכיווניות הפוכה על שני קצות הלולאה (קישור בכיוון מנוגד הוא התנאי לסגירת הלולאה). אם CTCF קשור באותה כיווניות, לולאה לא תיסגר.
מדורים (Compartments A ו־B): המדורים נקבעים על פי תדירות האינטראקציות בין TADs שונים. TADs שמתקיימות ביניהם אינטראקציות רבות נמצאים באותו מדור, ואילו אזורים ללא אינטראקציות משותפות מוקצים למדורים שונים.
טריטוריות כרומוזומליות (Chromosome Territories): כל כרומוזום מתמקם באזור מוגדר בגרעין, תלוי בסוג התא וגורמים נוספים.
קונדנסציה במיטוזה: בתהליך הדחיסה המיטוטית, תדירות האינטראקציות בין TADs קטנה ולא גדלה - כיוון שבמיטוזה מבנה ה־TAD למעשה מתפרק לחלוטין. הכרומוזום מקבל מבנה מוגדר, והצנטרומר נראה דחוס.
Ki-67: חלבון שמצפה את הכרומוזומים במיטוזה, מעניק להם מטען חיובי, ובכך מונע אגרגציה של כרומוזומים. ללא Ki-67 הסגרגציה עצמה תקינה, אך היציאה ל־G1 בתום החלוקה לקויה. בקליניקה הוא משמש כמרקר לפרוליפרציה ומשמש רבות באבחון גידולים סרטניים.
חלק א: צנטרומרים
חשיבות הצנטרומר
אחד העקרונות הבסיסיים בביולוגיה הוא הצורך לחלק את המטען הגנטי בצורה שוויונית בין תאי הבת בחלוקה. לאחר שמולקולת ה־DNA הדו־גדילית עוברת הכפלה, נוצרות שתי מולקולות זהות הנקראות כרומטידות אחיות (sister chromatids). הן נשארות מחוברות זו לזו מרגע יצירתן ועד לנקודת הסגרגציה. הצנטרומר הוא האלמנט המולקולרי המרכזי המבטיח שהסגרגציה תתבצע בצורה נכונה.
הצנטרומר הוא אחד משלושה אזורים חיוניים לקיום עצמאי של כרומוזום:
- הצנטרומר - לסגרגציה
- הטלומרים - בקצות הכרומוזום, מגנים עליו (ייידונו בשיעור הבא)
- אתרי ראשית ההכפלה (Origins of replication) - מהם מתחילה ההכפלה בשלב S
מהו צנטרומר?
הצנטרומר מוגדר ברמת רצף הבסיסים ב־DNA - זה אזור ספציפי בגנום שמאמץ מבנה דחוס וייחודי. מבחינת הכרומטין, הוא שייך לקטגוריה של הטרוכרומטין קונסטיטוטיבי. בנוסף לצפיפות, מאפיין אותו נוקלאוזום מיוחד עם וריאנט היסטון ייחודי (ראו להלן).
תפקידו: לשמש כנקודת הקישור של הקינטוכור (Kinetochore). הקינטוכור הוא קומפלקס חלבוני גדול ומורכב שמתווך בין ה־DNA לבין סיבי המיקרוטובול של ציר ההפרדה. כלומר: דנ״א ← צנטרומר ← קינטוכור ← מיקרוטובול.
ביטוי מורפולוגי: ההיצרות האופיינית הנראית בכרומוזום בזמן מיטוזה (ה”מותניים”) נובעת מהצפיפות הגבוהה מאוד של הצנטרומר, בנוסף לנוכחות מסיבית של קוהזין באזור זה.
מיקום הצנטרומר
הצנטרומר יכול להימצא בכל מקום לאורך הכרומוזום. מיקומו אינו משפיע על תקינות הסגרגציה, אך כן נותן לנו מאפיין מורפולוגי לזיהוי וסיווג כרומוזומים:
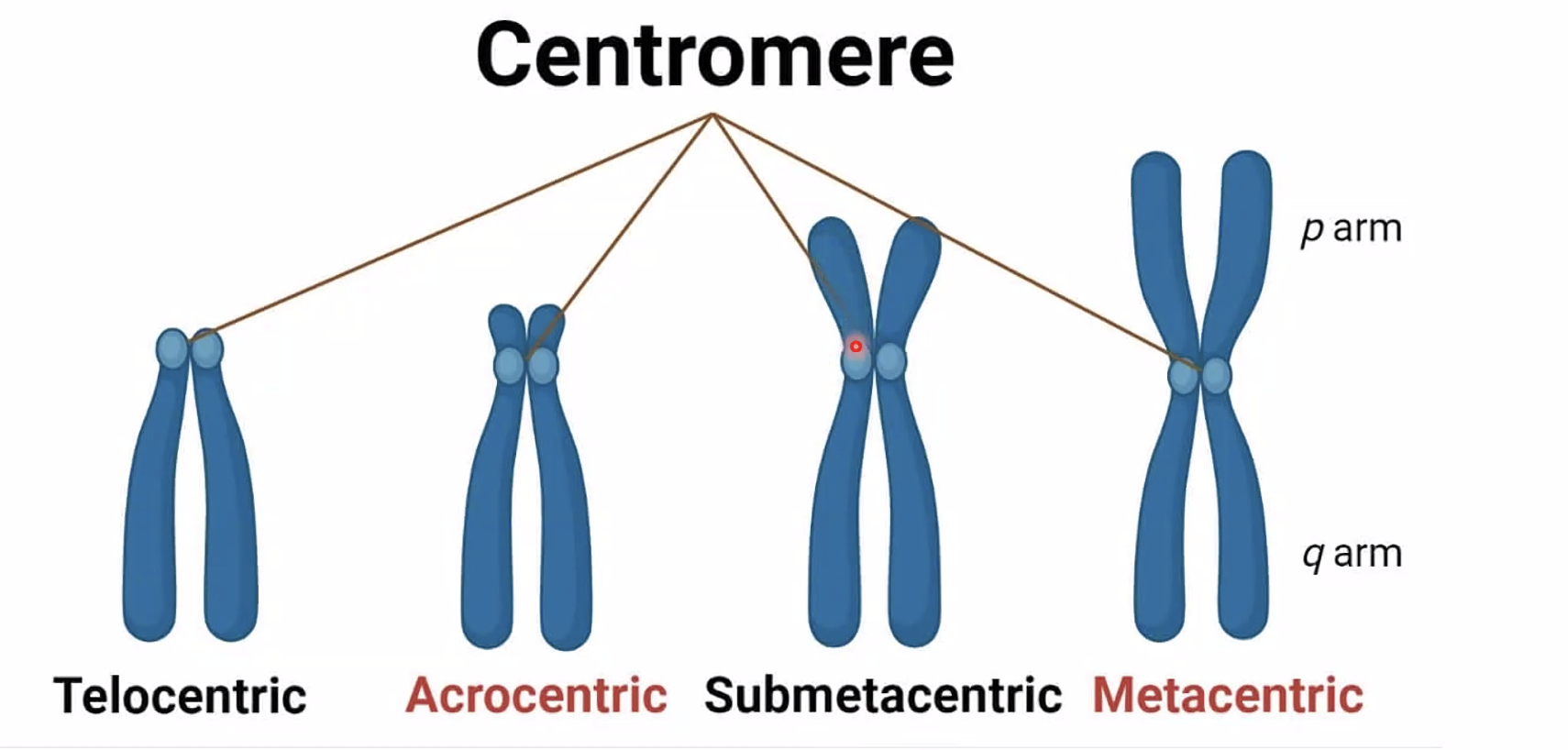
| שם | מיקום הצנטרומר | זרועות |
|---|---|---|
| מטאצנטרי (metacentric) | במרכז | p ו־q שוות |
| סאב־מטאצנטרי (submetacentric) | קרוב למרכז | p קצרה, q ארוכה |
| אקרוצנטרי (acrocentric) | קרוב לקצה | p קצרה מאוד |
| טלוצנטרי (telocentric) | בקצה הכרומוזום | - |
כלל בסיסי: צנטרומר אחד בלבד לכרומוזום
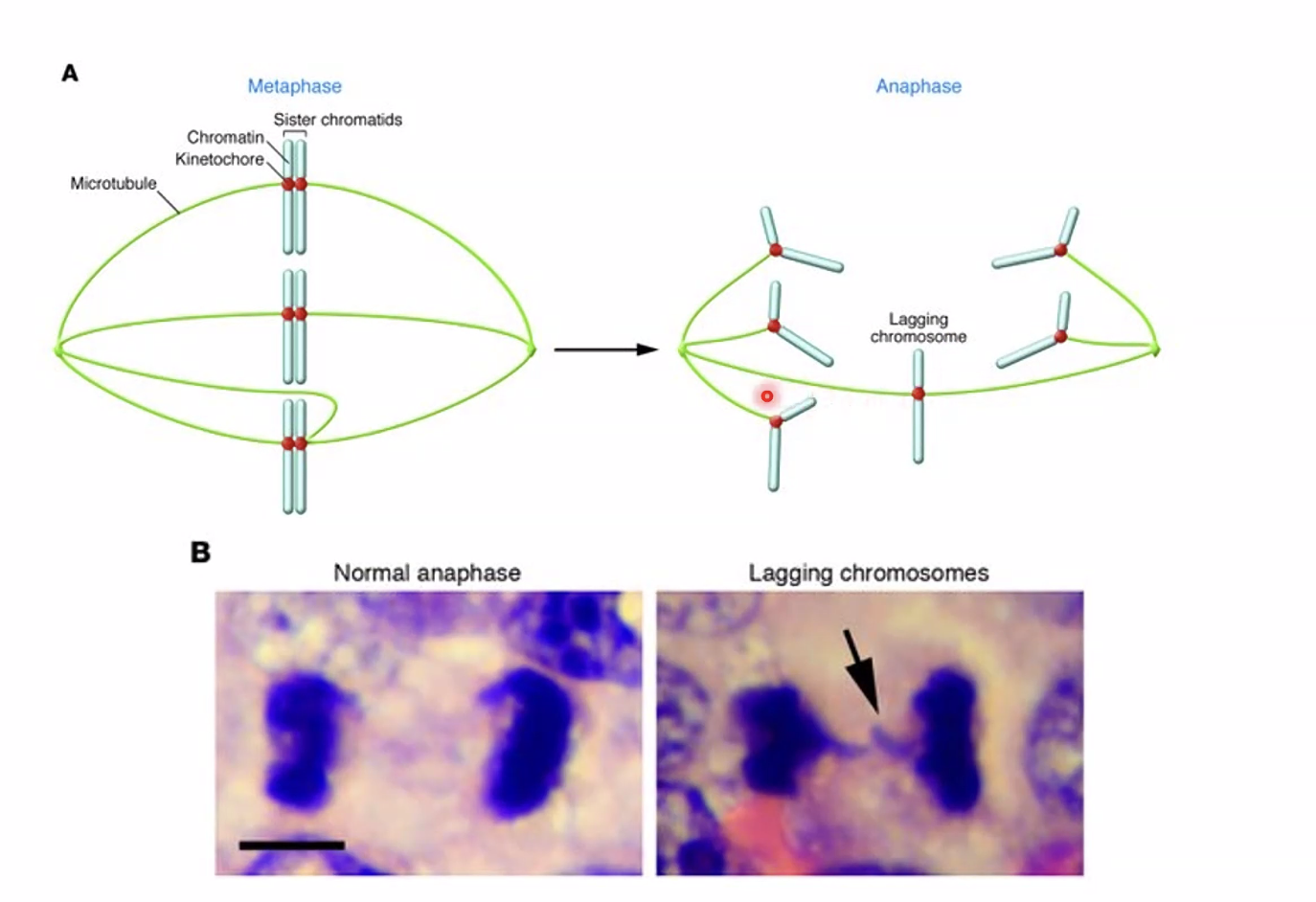
לכל כרומוזום יש צנטרומר אחד ואחד בלבד. הסיבה קריטית: אם יהיה יותר מצנטרומר אחד, כרומטידה יכולה להיקשר למיקרוטובולים מהכיוון הנכון וגם מהכיוון השגוי. במצב כזה, כוחות מנוגדים יפעלו על הכרומוזום בו־זמנית ויגרמו לו להישאר תקוע במרכז התא (תופעה הנקראת lagging chromosome), ובסופו של דבר לאנאופלואידיה (אחד מתאי הבת יקבל כרומוזום עודף, השני חסר) - או לשבירה פיזית של הכרומוזום. תופעה זו נצפית לעיתים קרובות בתאים סרטניים.
הגדרה אפיגנטית של הצנטרומר הפעיל
מעניין שרצפי האלפא-סאטלייט (alpha satellite) שמהווים את הצנטרומר אינם ייחודיים לצנטרומר - הם יכולים להופיע גם במקומות אחרים על הכרומוזום. ובכל זאת, בכל כרומוזום יש צנטרומר אחד פעיל בלבד. המשמעות היא שההגדרה של צנטרומר פעיל היא אפיגנטית: התא מדכא את פעילות כל רצפי האלפא-סאטלייט האחרים על גבי הכרומוזום, פרט לאחד. הגורם המרכזי המגדיר פעילות זו הוא וריאנט ההיסטון CENP-A (ראו להלן), בשילוב עם סמנים אפיגנטיים של הטרוכרומטין כמו H3K9me3.
כראיה לכך, כאשר כרומוזום נשבר ונוצרת חתיכה ללא צנטרומר, ניתן לראות לעיתים הפעלה של נאוצנטרומר (Neocentromere) - רצפי אלפא-סאטלייט שעד כה לא שימשו כצנטרומר פעיל עוברים אקטיבציה וממלאים את התפקיד. אך גם במצב זה, לעולם לא יתקיימו שני צנטרומרים פעילים על אותו כרומוזום.
מבנה הצנטרומר - השוואה בין שמרים לאדם
צנטרומר בשמרים (מודל פשוט)
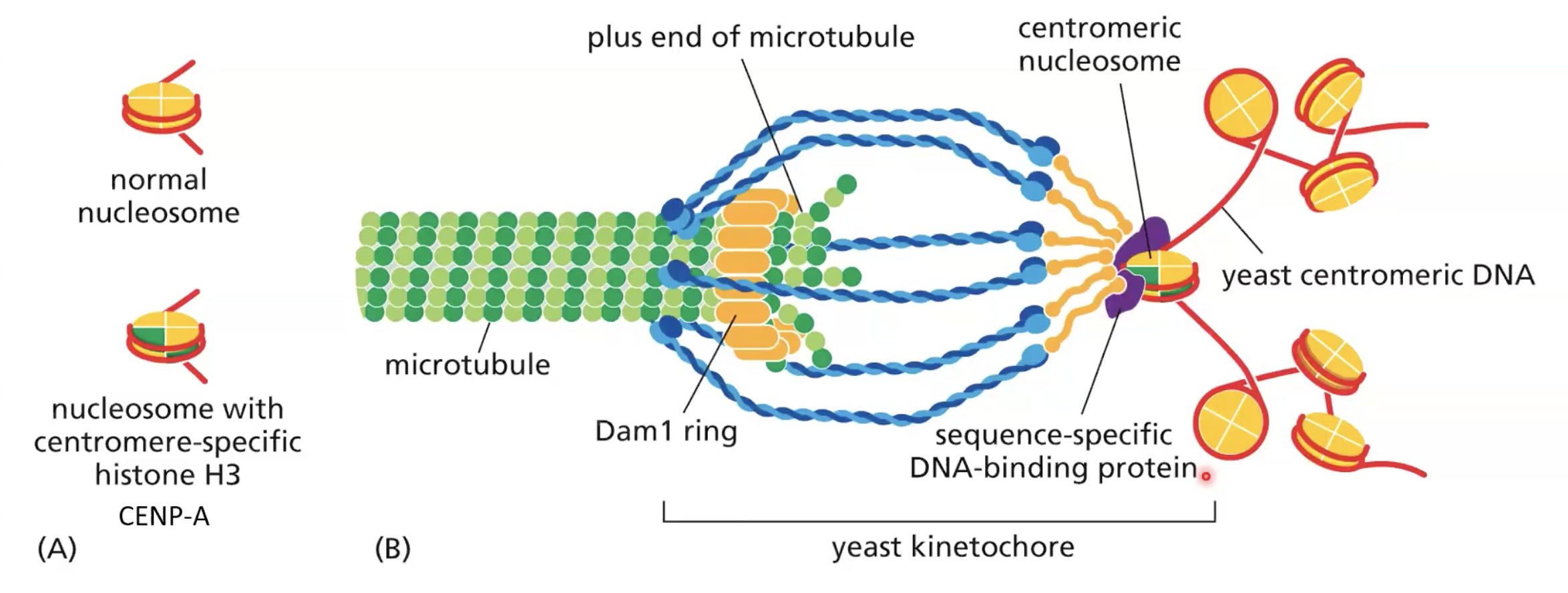
בשמרים, הצנטרומר בנוי מנוקלאוזום בודד. הנוקלאוזום הזה מיוחד: במקום היסטון H3 רגיל, הוא מכיל וריאנט שנקרא CENP-A (בשמרים: Cse4). הנוקלאוזום הזה משמש כמרקר מולקולרי שעליו נבנה הקינטוכור. הקינטוכור מורכב מתת־יחידות שנקשרות ספציפית לנוקלאוזום המכיל CENP-A, ומתת־יחידות שנקשרות למיקרוטובול - ובכך נוצר הגשר בין הכרומטין לציר ההפרדה.
צנטרומר אנושי (מבנה מורכב)
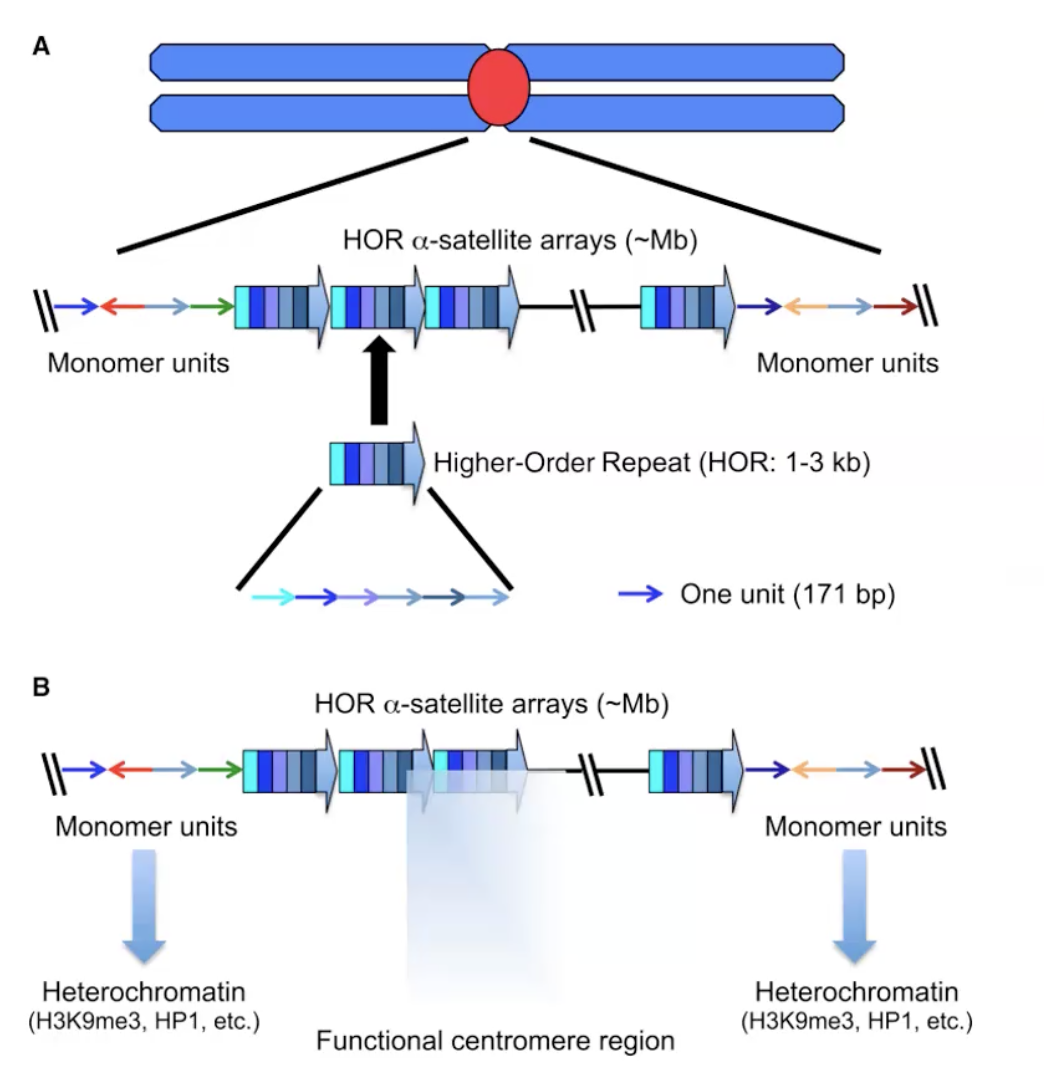
הצנטרומר האנושי גדול בסדרי גודל מהצנטרומר של שמרים: הוא תופס מיליוני בסיסים. הוא בנוי מחזרות של אלפא-סאטלייט (alpha satellite) המסודרות זו אחר זו. כל אלפא-סאטלייט בגודל של 1–3 קילובסיסים, ובתוכו יחידה בסיסית של כ־171 זוגות בסיסים - שווה ערך לנוקלאוזום אחד - וגם כאן, כל יחידה מכילה CENP-A במקום H3.
האזור כולו מסומן בסמנים אפיגנטיים של הטרוכרומטין (כגון H3K9me3), נראה דחוס בצביעות שונות, ומתארגן לתצורה מורכבת של לולאות מדורגות. גם כאן, בסופו של דבר, הקצוות שמורכבים מאלפא-סאטלייטס הנושאים CENP-A משמשים כבסיס לבניית הקינטוכור. מבחינה פונקציונלית - העבודה זהה לזו שבשמרים, גם אם המבנה הרבה יותר מורכב ופחות מוגדר בפרטיו.
הרכב הקינטוכור כולל גם קוהזין (cohesin) שמייצב את המבנה כולו (מסומן לרוב בצביעה בצבע אדום בשקפים).
הקינטוכור מקשר בין אזור הצנטרומר של הכרומוזום לבין המיקרוטובולים (של כישור החלוקה).
חלק ב: קוהזין וסגרגציה
תפקידי הקוהזין - שתי אוכלוסיות
כבר הוזכר בשיעורים קודמים שקוהזין ממלא תפקיד בארגון הכרומטין לתחומי TAD (loop extrusion). אך לקוהזין יש גם אוכלוסייה שנייה, נפרדת, שתפקידה לגמרי שונה: החזקה פיזית של כרומטידות אחיות. אוכלוסייה זו מתמקמת לאורך זרועות הכרומוזום ובצורה מסיבית במיוחד על הצנטרומר.
מחזור הקוהזין לאורך מחזור התא
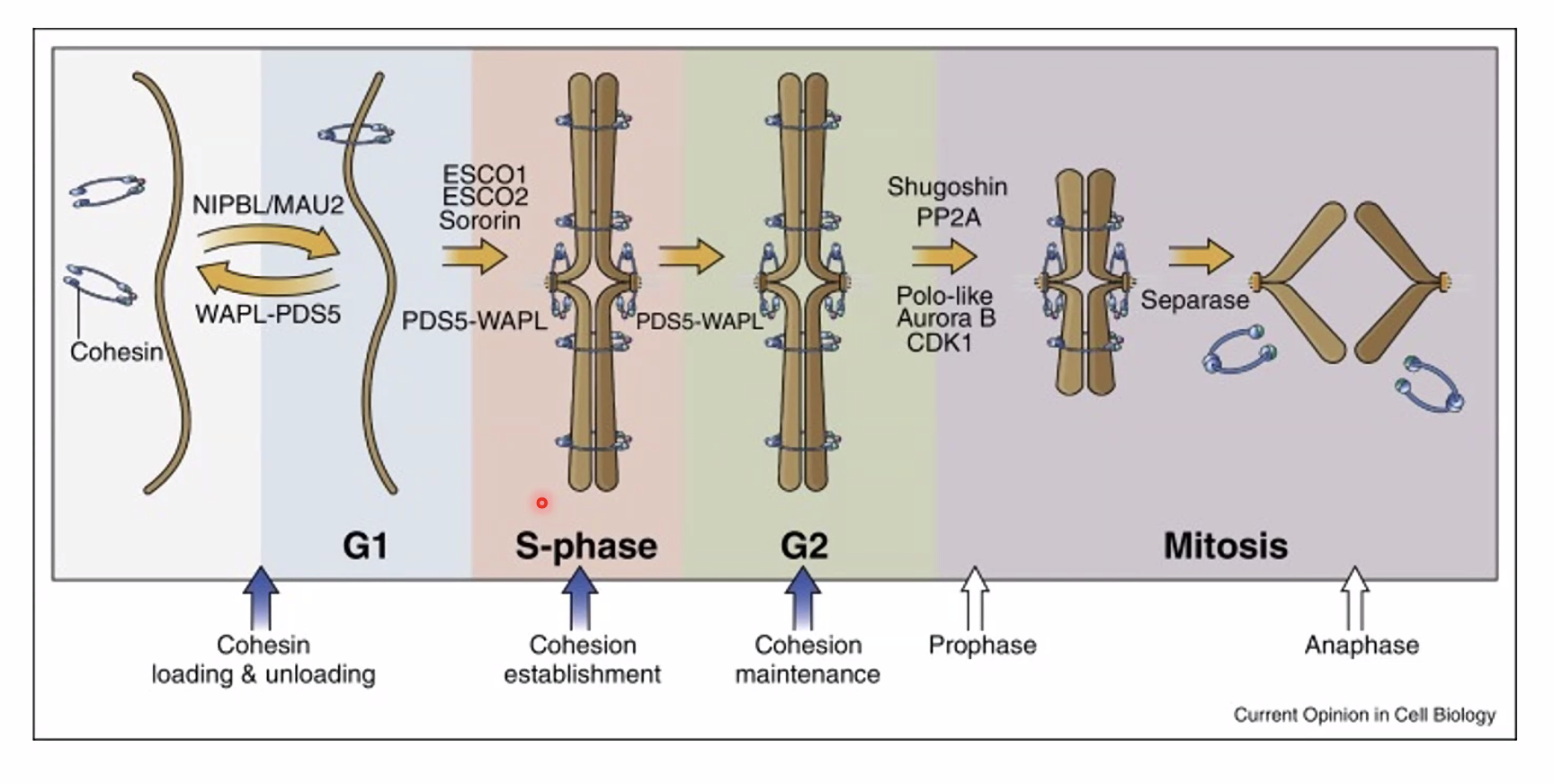
בשלב G1: קוהזין מתחיל לעלות על הכרומוזום, אך הקישור שלו דינמי מאוד - עולה ויורד ואינו יציב.
בשלב S (הכפלת ה־DNA): בד בבד עם הכפלת ה־DNA, מיד עם יצירת הכרומטידה האחות, מתקיימת הלבשה של קוהזין שמחזיק את שתי הכרומטידות האחיות ביחד. הקישור הזה עכשיו יציב. הוא מתרחש הן לאורך הזרועות והן - ביתר שאת - על הצנטרומר.
בשלב G2 עד כניסה למיטוזה: המצב הזה של קוהזין נשמר באופן אקטיבי.
בכניסה למיטוזה: תהליך הדחיסה (condensation) מבוצע על ידי קונדנסין, אך כדי שקונדנסין יפעל כראוי יש דרישה שקוהזין יהיה נוכח. לאחר מכן מתרחש תהליך דו־שלבי של הסרת הקוהזין:
- שלב ראשון (prophase pathway): הקוהזין מוסר מהזרועות, אך נשאר על הצנטרומר. לכן, כרומוזום בפרומטפאזה נראה בצורת X - הכרומטידות צמודות רק בצנטרומר.
- שלב שני (אנאפאזה): כאשר ה־APC/C (Anaphase Promoting Complex) מסמן שהצ’ק-פוינט עבר, הוא מפעיל פרוטאז שנקרא ספראז (separase). הספראז חותך את הקוהזין שנותר על הצנטרומר. פעולה זו מתוארת כ”מכה בפטיש” - אגרסיבית במכוון, כי חשוב להבטיח שלא יישאר אפילו קוהזין אחד שיעכב את הסגרגציה.
הצ’ק-פוינט של הסגרגציה - מנגנון המתח
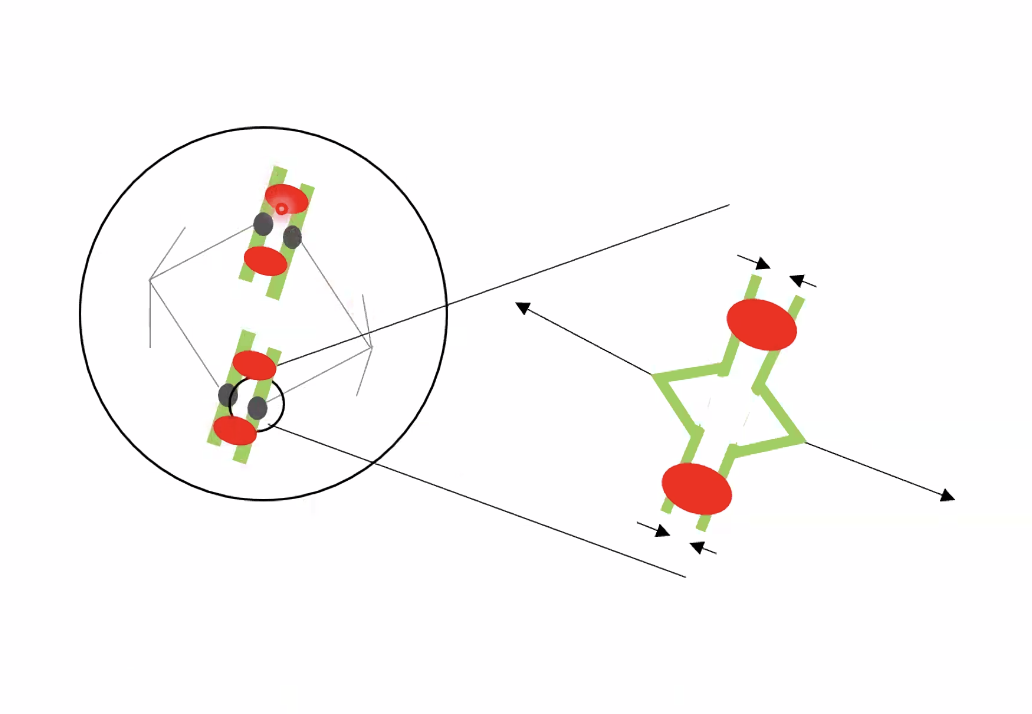
לפני שהסגרגציה מתאפשרת, יש לוודא שכל כרומטידה נקשרה למיקרוטובולים משני הצדדים הנכונים (bipolar attachment). המנגנון פועל כך:
- מצד אחד: המיקרוטובולים מנסים למשוך את הכרומטידות כלפי קטבים מנוגדים של התא.
- מצד שני: הקוהזין מחזיק פיזית את שתי הכרומטידות האחיות ומונע מהן להיפרד.
ניתן לדמות זאת לגומייה: המיקרוטובולים מושכים שתי כרומטידות לשני כיוונים, אך הגומייה (הקוהזין) לא מרשה להן להיפרד. מה שכן קורה הוא שנוצר רווח פיזי קטן בין הכרומטידות בצנטרומר. רווח זה - של מספר ננומטרים - הוא הסיגנל לתא שהקישור הביפולרי הצליח. רק כשהרווח נוצר נפסק תהליך “השחרור מהמיקרוטובול”, מה שמאפשר לקישור להתייצב. כל עוד הכרומטידות צמודות (ללא רווח), הקישור נחשב לא־ביפולרי ומשוחרר שוב ושוב.
ברגע שהצ’ק-פוינט עבר בצורה תקינה, ה־APC/C מאשר את הסגרגציה, הספראז מופעל, הקוהזין נחתך - וכוחות המיקרוטובולים מושכים את הכרומטידות לשני תאי הבת.
תקלות שיכולות להתרחש:
- אם הקוהזין לא יוסר בצורה נכונה ← שתי הכרומטידות עוברות לאותו תא ← אנאופלואידיה (aneuploidy).
- אם כרומוזום נקשר למיקרוטובולים משני הכיוונים בצנטרומר אחד ← lagging chromosome, ובסופו שבירה פיזית או אנאופלואידיה.
חלק ג: תסמונת דאון וגיל האם
הגרף הקליני
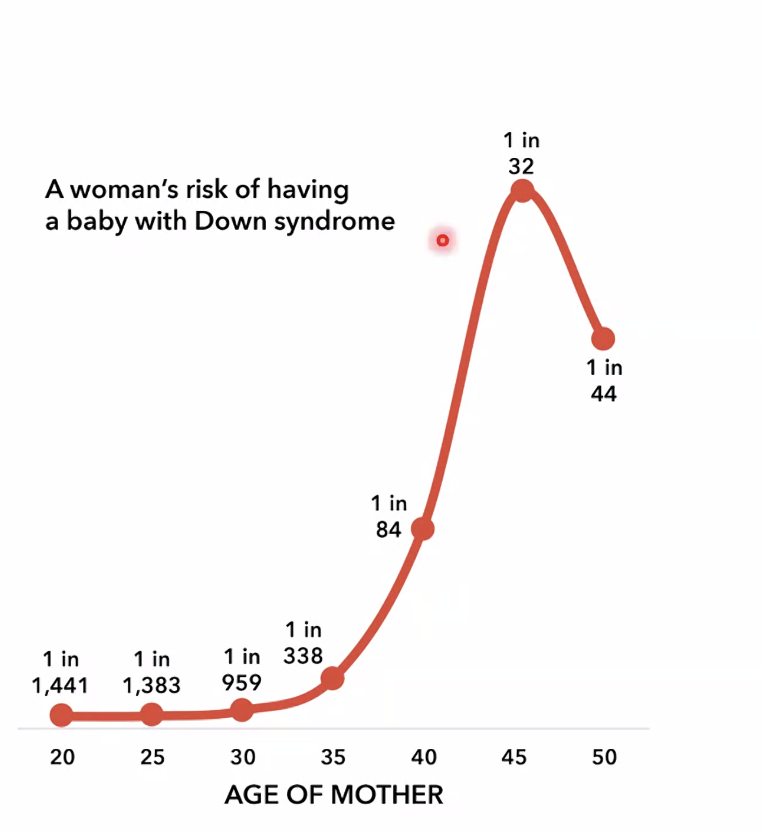
הסיכון להולדת תינוק עם תסמונת דאון (Trisomy 21 - שלושה עותקים של כרומוזום 21) גדל כפונקציה של גיל האם. עד גיל 30, הסיכון נמוך מאוד (בסדר גודל של יותר מ־1 ל־1,000). בגיל 35 יש קפיצה ברורה. בגיל 40 הקפיצה גדולה עוד יותר. בגיל 45 הסיכוי גבוה מאוד: כ־1 מכל 3 הריונות יהיה עם תסמונת דאון. הנתונים בגיל 50 פחות אמינים סטטיסטית בגלל מיעוט המקרים (הרבה נשים כבר עברו מנופאוזה), ולכן ה”ירידה” שנראית שם היא ככל הנראה ארטיפקט סטטיסטי.
למה גברים לא מראים תופעה זו?
בגברים, תאי זרע מתחדשים כל הזמן לאורך החיים. לכן הגיל הממוצע של תא הזרע הוא פחות או יותר קבוע בכל גיל של הגבר.
מדוע אצל נשים מבוגרות הסיכון עולה?
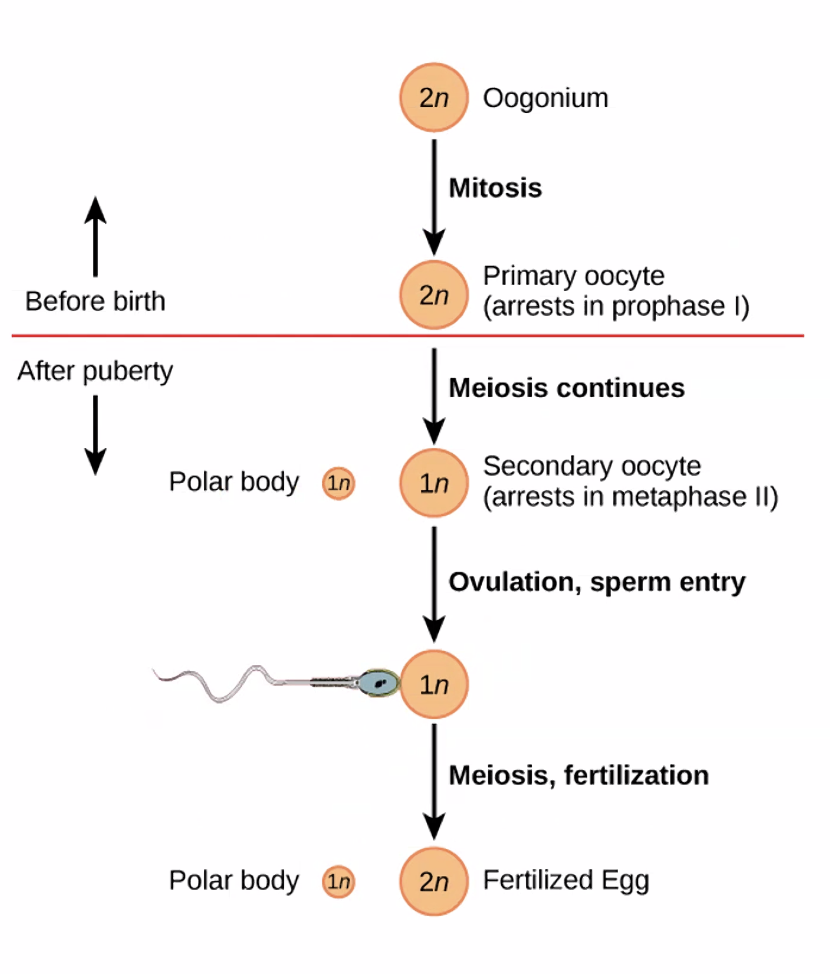
תהליך יצירת הביציות מחולק לשני שלבים:
- שלב עוברי: תאי ביצית עוברים מיוזה ראשונה (חלוקת ההפחתה שבה כרומוזומים הומולוגיים מופרדים, אך כרומטידות אחיות נשארות יחד) - ונעצרות בנקודה זו. הן “מחכות” כך שנים רבות.
- גיל הפוריות ואילך: כל חודש, ביצית אחת מקבלת סיגנל הורמונלי, עוברת מיוזה שנייה, ומבשילה להפריה.
כלומר, הביצית עשויה לשהות בשלב הביניים של המיוזה הראשונה שנים עד עשרות שנים, עד שהיא “מופעלת”. הקוהזין שהוטל על הכרומטידות האחיות בשלב העוברי צריך להחזיק ביניהן במשך כל הזמן הזה.
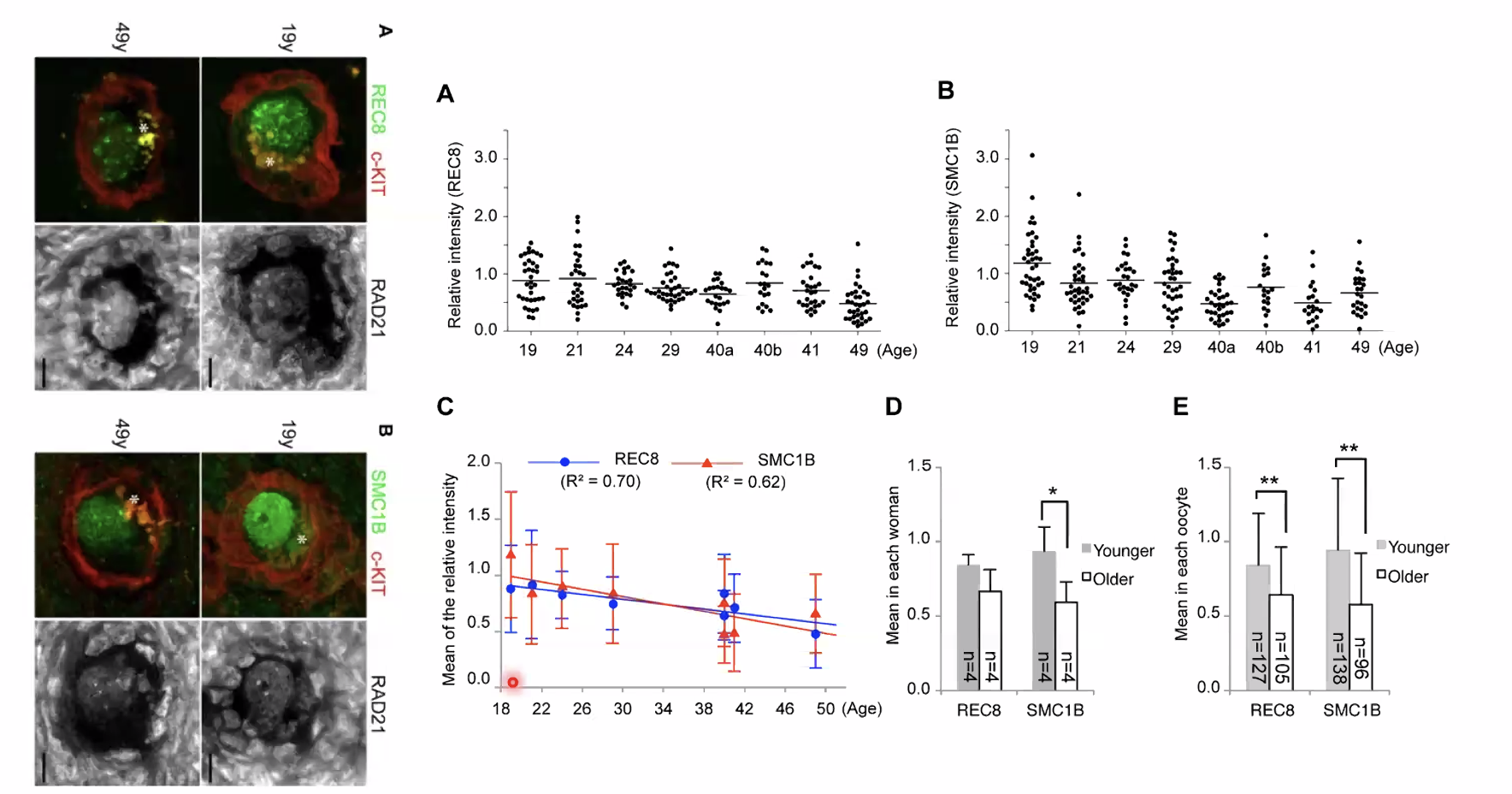
עם השנים, הקוהזין מתפרק: תהליכים טבעיים של מחצית חיי חלבון, ונזקים סביבתיים (קרינה קוסמית, מזהמים, עישון, אלכוהול ועוד), גורמים לירידה בכמות הקוהזין הפונקציונלי בתאי הביצית. מחקרים שנמדדו בנשים בגיל 18 עד 50 הראו ירידה ברורה וקבועה בכמות תת־יחידות קוהזין (SMC1β ו־RAD21/REC8) לאורך השנים.
כתוצאה מכך: ככל שהאישה מבוגרת יותר, יש פחות קוהזין בתאי הביצית שלה, ובמיוזה השנייה הסגרגציה פחות מדויקת - הסיכוי לאי־הפרדה (Nondisjunction) ולטריזומיה 21 עולה. זה הסבר מולקולרי חלקי לתופעה הקלינית של עליית שכיחות תסמונת דאון עם גיל האם.
חלק ד: הכפלת DNA - מבוא
הבסיס: עיקרון ההכפלה הסמי-קונסרבטיבית
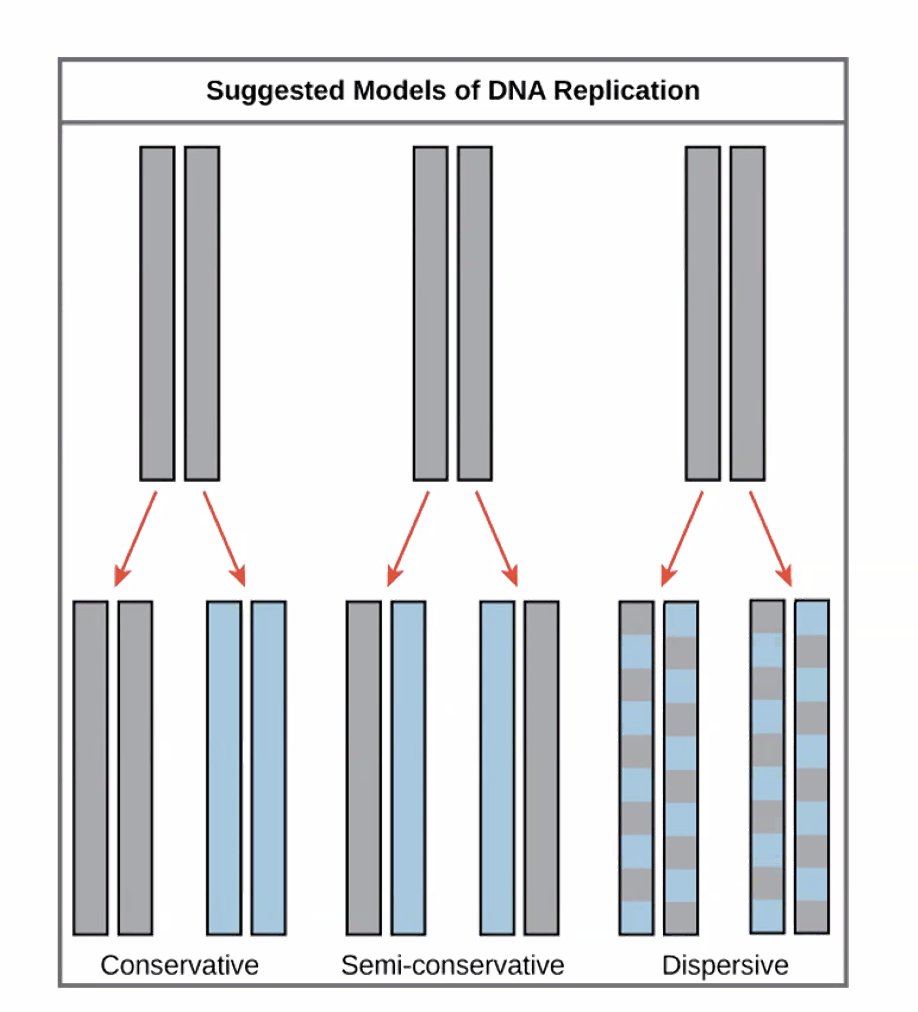
כאשר חוקרים בשנות ה־50 החלו לחשוב על מנגנון הכפלת ה־DNA, הוצעו שלושה מודלים תיאורטיים:
-
קונסרבטיבי (conservative): מולקולת ה־DNA המקורית נשמרת שלמה, ונוצרת מולקולה חדשה לחלוטין. בסוף מקבלים: מולקולה ישנה + מולקולה חדשה.
-
דיספרסיבי (dispersive): כל מולקולת DNA בסופו של דבר מכילה תערובת של חומר ישן וחומר חדש, מפוזרים ברחבי כל הגדיל (אזורים ישנים ואזורים חדשים על אותו גדיל).
-
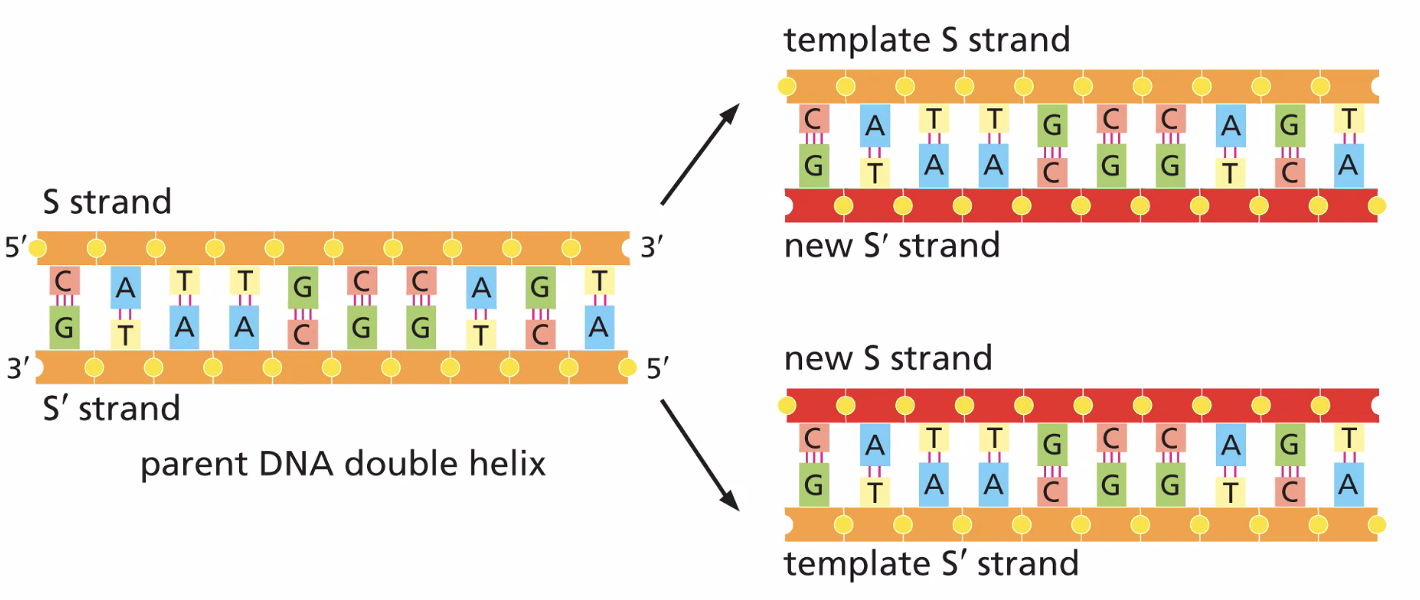
סמי-קונסרבטיבי (semi-conservative): כל אחד מהגדילים הישנים משמש כתבנית לגדיל חדש. בסוף ההכפלה, כל מולקולת DNA מכילה גדיל אחד ישן וגדיל אחד חדש.
המודל הנכון הוא הסמי-קונסרבטיבי. הבסיס המאפשר אותו הוא עיקרון זיווג הבסיסים (G-C, A-T): כאשר אנחנו “פותחים” את הדו־גדיל, כל גדיל מכיל מידע מלא לבניית הגדיל המשלים שלו.
ניסוי מסלסון ושטאל (Meselson-Stahl, 1958)
ניסוי זה, שנחשב לאחד הניסויים היפים ביותר בביולוגיה מולקולרית, הוכיח אמפירית את ההכפלה הסמי-קונסרבטיבית באמצעות כלים מוגבלים יחסית לזמנו.
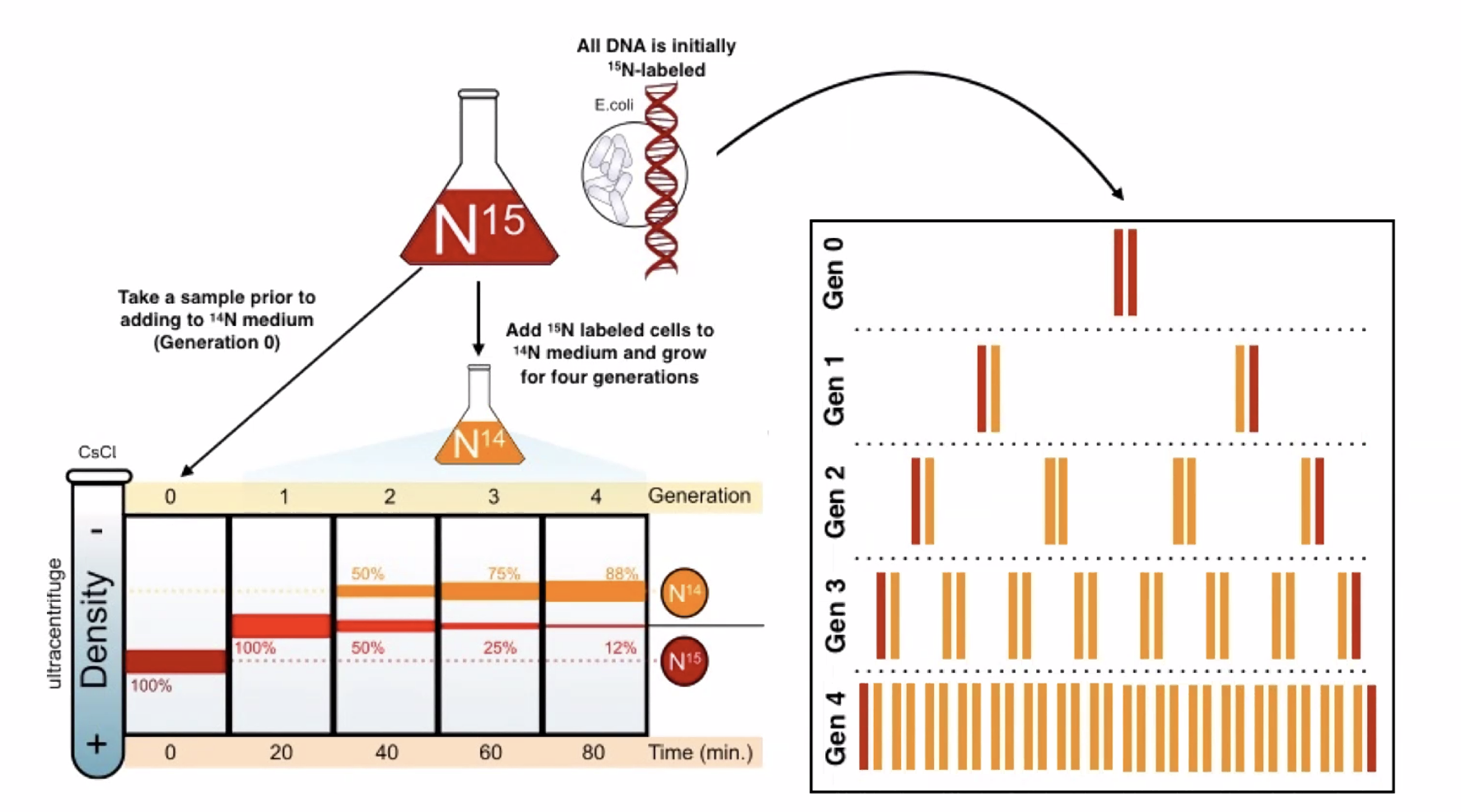
עיקרון הניסוי:
- גידול חיידקי (E. coli) למספר מחזורי חלוקה בנוכחות חנקן כבד (N¹⁵), עד שכל ה־DNA של החיידקים הכיל אך ורק N¹⁵.
- העברת החיידקים לגידול עם חנקן קל (N¹⁴) - כך שכל נוקלאוטיד חדש שיוכנס לDNA יהיה קל יותר.
- מדידת משקל מולקולות ה־DNA לאחר כל מחזור חלוקה באמצעות גרדיאנט צסיום כלוריד (CsCl) - שיטת הפרדה המבוססת על שקיעה לפי משקל.
תוצאות:
-
אחרי מחזור אחד: כל ה־DNA בעל משקל אחיד ואמצעי (היברידי - גדיל אחד N¹⁵ וגדיל אחד N¹⁴). זאת תוצאה עקבית עם המודל הסמי-קונסרבטיבי ועם המודל הדיספרסיבי, ולכן לא מבחינה ביניהם.
-
אחרי שני מחזורים: מופיעות שתי אוכלוסיות בגרדיאנט - מולקולות היברידיות (N¹⁵/N¹⁴, כמו בדור הראשון) ומולקולות קלות (N¹⁴/N¹⁴, מכילות שני גדילים חדשים) - ביחס של 50%:50%. תוצאה זו אינה עקבית עם המודל הדיספרסיבי (שהיה מנבא מולקולות בעלות משקל אחיד יותר ויותר), ועקבית לחלוטין עם המודל הסמי-קונסרבטיבי.
-
אחרי שלושה מחזורים: יחס המולקולות ההיברידיות ממשיך לרדת יחסית למולקולות הקלות - בדיוק כצפוי.
על בסיס ניסוי זה נקבע שהכפלת ה־DNA היא סמי-קונסרבטיבית.
ארתור קורנברג ובידוד DNA פולימראז
לפני שנסביר איך ה־DNA פולימראז פועל, ניתן קצת הקשר היסטורי:
- 1956: ארתור קורנברג בודד לראשונה אנזים מ־E. coli עם יכולת לסנתז DNA על בסיס תבנית - ונתן לו את השם DNA פולימראז (היום: DNA פולימראז I). בזמנו חשבו שזהו האנזים הרֶפּלִיקָטִיבִי (Replicative) הראשי, אך כיום ידוע שה־Pol I משתתף בעיקר בסיום רפליקציה ובתיקון.
- 1959: קורנברג קיבל על כך פרס נובל.
- 1968: קורנברג הצליח לראשונה לשחזר הכפלת DNA במבחנה - כלומר לגרום לאנזימים מנוקים לסנתז DNA מחוץ לתא. פרק זמן של 12 שנה בין בידוד האנזים לבין הרפליקציה המוצלחת במבחנה מעיד על המורכבות הרבה של הריאקציה.
חלק ה: DNA פולימראז - מאפיינים ומנגנון
ארבעת המאפיינים של DNA פולימראז
כאשר מדברים על DNA פולימראז (ובאופן כללי על אנזימים), מגדירים ארבעה מושגים:
-
פעילות (Activity): מה הפעילות הביוכימית של האנזים? עבור DNA פולימראז - פולימריזציה של נוקלאוטידים לרצף DNA. לשם השוואה: טופואיזומרזות מסירות Super-coiling; אקסונוקלאז חותך מהקצוות; אנדונוקלאז חותך בתוך רצף; ספראז חותך חלבונים; ליגאז יוצר מחדש קשר פוספודיאסטרי; RNA פולימראז מסנתז RNA.
- מהירות (Speed): כמה נוקלאוטידים מוכנסים בשנייה. קיים הבדל עצום בין אורגניזמים:
- E. coli: כ־1,000 בסיסים לשנייה
- תאי אדם: כ־50 בסיסים לשנייה (שני סדרי גודל פחות)
ההבדל קשור בחלקו לנושא הדיוק: בדרך כלל יש פשרה (trade-off) בין מהירות לדיוק - ככל שהפולימריזציה מהירה יותר, הסיכוי לטעויות עולה (פחות זמן מושקע בכל נקודה).
-
פרוססיביות (Processivity): מספר הנוקלאוטידים שמסונתזים מרגע שהאנזים נקשר לDNA ועד שהוא נופל ממנו. DNA פולימראז רֶפּלִיקָטִיבִי, שצריך לסנתז מקטעים ארוכים, מאופיין בפרוססיביות גבוהה מאוד (יכול לסנתז אלפי ועד מיליוני בסיסים בכל מחזור פעולה). לעומת זאת, DNA פולימראז של תיקון מסנתז מקטעים קצרים, ולכן פרוססיביות נמוכה יותר מספיקה.
- דיוק / נאמנות (Accuracy / Fidelity): מספר הבסיסים הנכונים שהוכנסו ביחס לטעויות, לכל מחזור פעולה. מחושב כמספר הטעויות חלקי מספר הבסיסים שסונתזו.
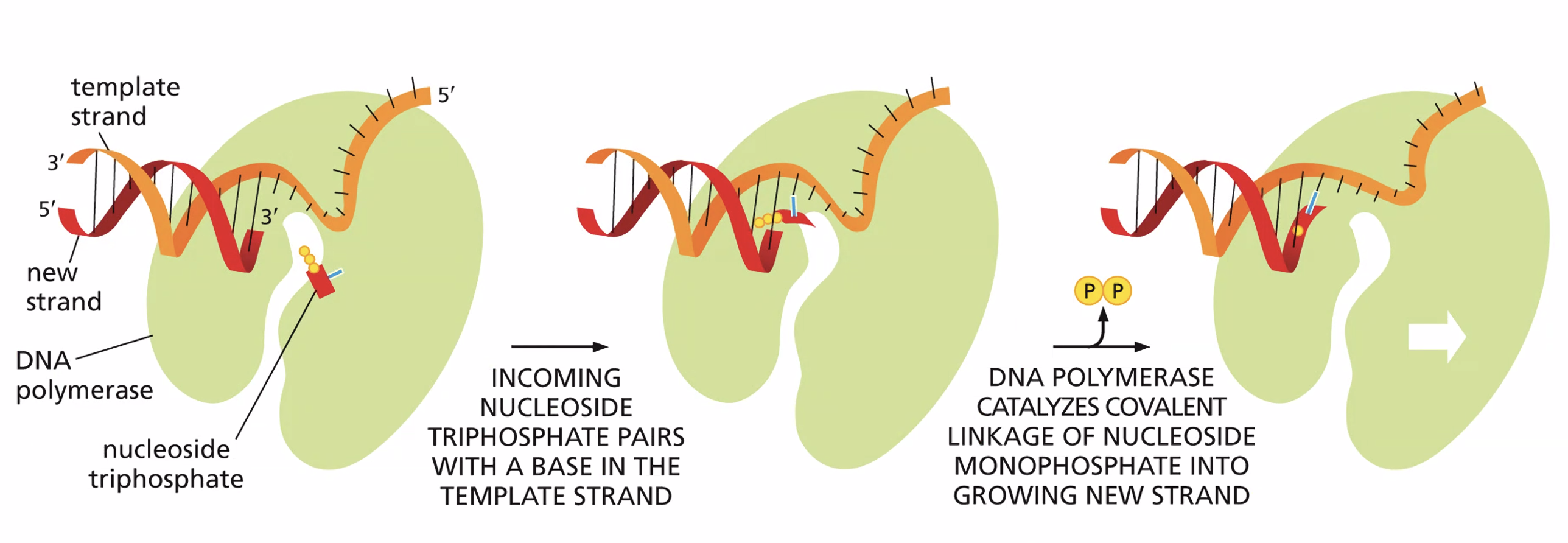
מנגנון הפולימריזציה
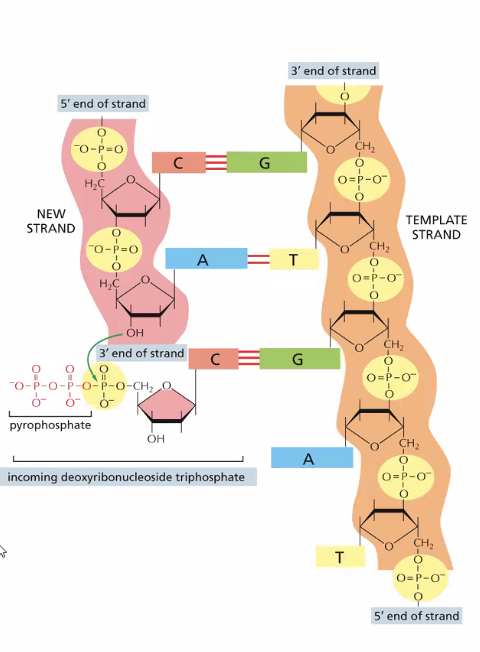
הכימיה הבסיסית: כדי לחבר נוקלאוטיד חדש לשרשרת הגדלה, מתרחשת התקפה נוקלאופילית: קבוצת ה־OH על פחמן 3 (קצה 3’) של הנוקלאוטיד האחרון בשרשרת תוקפת את פוספט α (קצה 5’) של הנוקלאוטיד הנכנס (שהוא טריפוספט, dNTP). נוצר קשר פוספודיאסטרי חדש ומשתחרר פירופוספט. התהליך ספונטני מבחינה אנרגטית - הקשר בטריפוספט עתיר-אנרגיה, ולכן לא נדרש מקור אנרגיה חיצוני.
מה עושה ה־DNA פולימראז אם הכימיה ספונטנית? שני תפקידים:
-
קיצוב מרחב: ה־DNA פולימראז מחזיק את הנוקלאוטיד הנכנס באוריינטציה שבה קצה ה־5’-פוספט שלו נמצא קרוב מספיק לקצה 3’-OH של השרשרת הגדלה, כדי לאפשר את ההתקפה. ללא הקרבה הזאת הכימיה הספונטנית לא תתרחש.
-
סלקציה לפי זיווג בסיסים: ל־DNA פולימראז אין ספציפיות לנוקלאוטיד מסוים - כל ארבעת הנוקלאוטידים (A, T, G, C) יכולים להיכנס לאתר הקטליטי בסיכוי שווה (1/4). אולם: רק נוקלאוטיד שיוצר זיווג בסיסים נכון עם הנוקלאוטיד בגדיל התבנית יגרום לשינוי קונפורמציה ב־DNA פולימראז. שינוי קונפורמציה זה הוא שמקרב את הפוספט ל־OH ומאפשר את הקישור הקוולנטי. נוקלאוטיד לא־משלים לא יוצר זיווג, לא מושרה שינוי קונפורמציה - ולכן הוא פשוט משתחרר.
כיווניות הסינתזה: ה־DNA פולימראז עובד תמיד בכיוון 5’←3’. אין DNA פולימראז בעולם שיודע לסנתז בכיוון 3’←5’. לפיכך, גדיל התבנית נקרא בכיוון 3’←5’, והגדיל הנבנה נמשך בכיוון 5’←3’.
אי־יכולת לפתוח שרשרת חדשה: כל ה־DNA פולימראזות המוכרות יכולות רק להמשיך שרשרת קיימת - הן מחברות נוקלאוטיד לנוקלאוטיד קיים, אך לא יודעות להניח את הנוקלאוטיד הראשון. זה יוצר בעיה ביצירת שרשרת חדשה, ופתרונה ייסקר בשיעורים הבאים.
מנגנון ההגהה (Proofreading) - פעילות 3’←5’ אקסונוקלאז
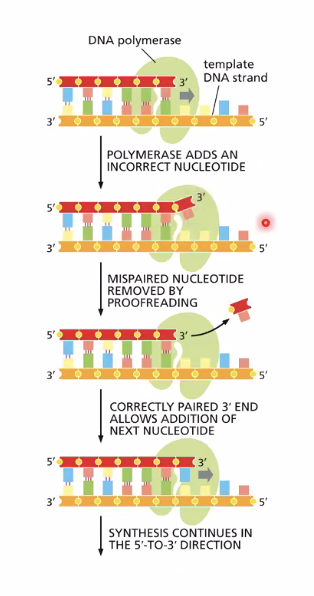
זוהי תכונה המאפיינת בעיקר DNA פולימראז רֶפּלִיקָטִיבִי; DNA פולימראזות של תיקון בדרך כלל אינן מכילות מנגנון זה.
הבעיה שהמנגנון פותר: לעיתים נוקלאוטיד נכנס לאתר הקטליטי בקונפורמציה לא־יציבה (בעל אנרגיה גבוהה). בקונפורמציה כזו, הנוקלאוטיד הלא־נכון יכול לחקות זיווג בסיסים ולעורר שינוי קונפורמציה בפולימראז - וייכנס לשרשרת. לאחר שנוצר הקשר הקוולנטי, הנוקלאוטיד “חוזר” לקונפורמציה האנרגטית הנמוכה שלו - הקונפורמציה שלא־יוצרת זיווג. כעת הוא תקוע בשרשרת אך לא יוצר קשרי מימן עם הבסיס שמולו.
כיצד הפולימראז מזהה את הטעות: המצב שבו נוקלאוטיד תקוע בשרשרת ללא זיווג בסיסים יוצר עיוות (kink) בשלד של ה־DNA. שינוי מבני זה הוא הטריגר שהאתר האקסונוקלאזי של הפולימראז מזהה.
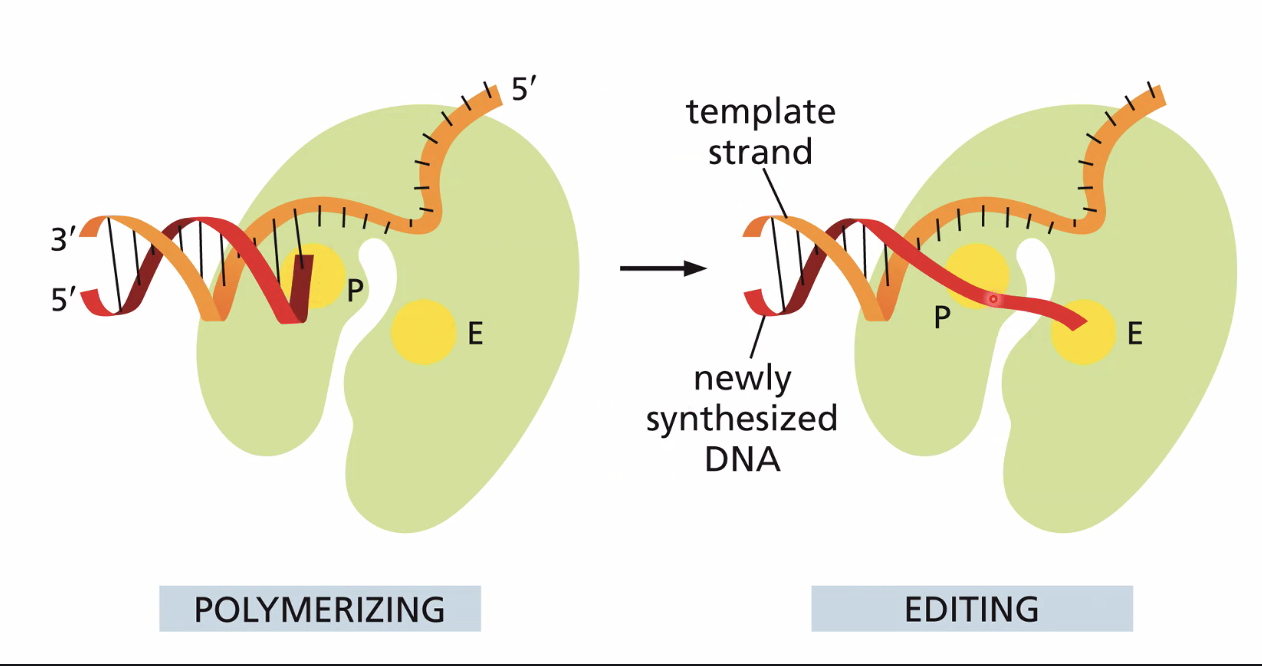
תיקון הטעות: הנוקלאוטיד האחרון בשרשרת עובר מאתר הפולימריזציה לאתר של אקסונוקלאז 3’←5’ שנמצא על אותו פולימראז (אך נפרד ממנו). אתר האקסונוקלאז חותך את הנוקלאוטיד האחרון. הנוקלאוטיד משתחרר, הקונפורמציה של שלד ה־DNA חוזרת לנכונה, והפולימראז חוזר למצב של פולימריזציה - ומנסה שוב עם נוקלאוטיד חדש.
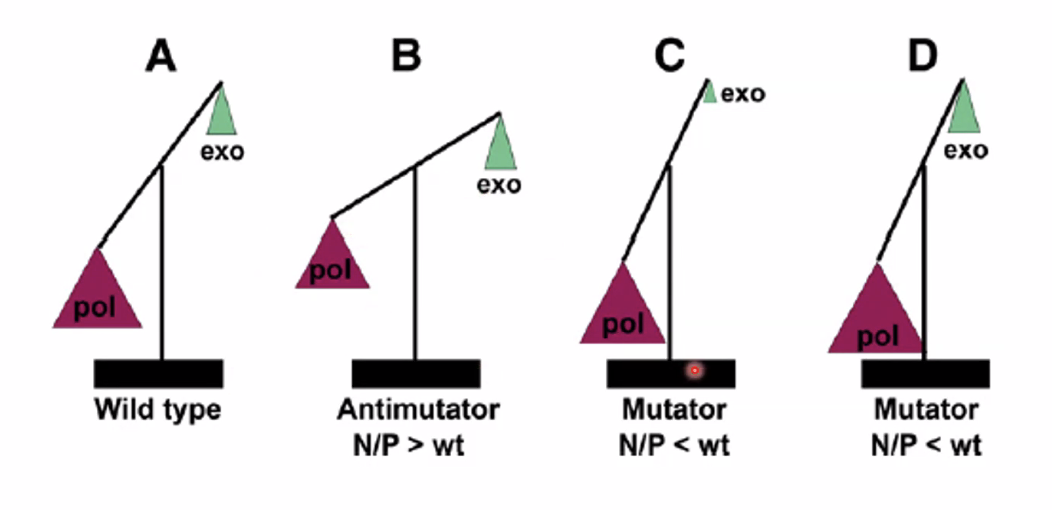
שיווי משקל עדין: קיים איזון בין שני התהליכים המנוגדים - פולימריזציה (מאריכה שרשרת) ואקסונוקלאז (מקצרת שרשרת). הפרת האיזון לכל כיוון היא בעייתית:
- עודף פולימריזציה (אקסונוקלאז מוחלש, או פולימריזציה מהירה מדי) ← יותר טעויות בשרשרת.
- עודף אקסונוקלאז (פולימריזציה מוחלשת) ← הרפליקציה האיטית מאוד, השלמת ה־S phase עלולה לקחת שעות במקום שעה, התאים יתעכבו מאוד.
רמות הדיוק של הרפליקציה
בסופו של דבר, הרפליקציה מבוטחת בשלוש רמות:
| רמה | מנגנון | דיוק (שגיאה אחת לכל…) |
|---|---|---|
| 1 | זיווג בסיסים בלבד | 1:10,000 |
| 2 | + הגהה (proofreading) בזמן הרפליקציה | 1:10,000,000 (10⁷) |
| 3 | + מערכות תיקון לאחר רפליקציה | 1:10,000,000,000 (10¹⁰) |
זה דיוק עצום ביחס לגודל הגנום. הדיוק הזה הוא הסיבה שאנחנו מצליחים לתפקד כבני אדם בריאים למרות שיש לנו כמויות עצומות של DNA להכפיל. כאשר מערכות התיקון פגומות - למשל כתוצאה ממוטציה הפוגעת בפעילות האקסונוקלאז, בפרוססיביות, או במנגנוני התיקון שלאחר רפליקציה - הסיכוי לפגיעה בגנים קריטיים עולה, ועמו הסיכון להתמרה סרטנית.
ה־DNA פולימראזות האנושיות
בגנום האנושי קיימים 17 אנזימים הנמנים על קטגוריית ה־DNA פולימראז. רק לשלושה מהם יש פעילות הגהה (3’←5’ אקסונוקלאז), ואלה הם ה־DNA פולימראזות הרֶפּלִיקָטִיבִיות:
- Pol ε (פול־אפסילון) - פולימראז רֶפּלִיקָטִיבִי בגרעין, בעיקר על ה־leading strand
- Pol δ (פול־דלתא) - פולימראז רֶפּלִיקָטִיבִי בגרעין, בעיקר על ה־lagging strand
- Pol γ (פול־גמא) - ה־DNA פולימראז המיטוכונדריאלי
שאר הפולימראזות, בעיקר אלו של תיקון, מסנתזות מקטעים קצרים יחסית - ולכן מנגנון ההגהה, שמאט את התהליך, אינו נחוץ להן.
דור פסקל