תוכן העניינים:
- Schwann Cells
- The Oligodendrocyte
- Chemical Synapses vs. Electrical Synapses
- Communication Between Neurons - Release of Presynaptic Vesicles
- Receptors on Postsynaptic Membrane
- Excitatory and Inhibitory Postsynaptic Potentials (
EPSP/IPSP) - Axon Hillock - נקודת ההחלטה
- Temporal and Spatial Summation
- Example - Integration of Information (שובע)
- Synapse - Clearance of Neurotransmitters
- Clinical Application - Lidocaine / Benzocaine
- Different Types of Action Potentials
- אצטילכולין (Acetylcholine)
- Neuromuscular Junction
- Cardiomyocytes - תאי שריר הלב
- EEG
- Synaptic Plasticity - פלסטיות סינפטית
- Hebb’s Rule: “Neurons that fire together, wire together”
- המנגנון המולקולרי - קולטן NMDA
- Long-Term Potentiation (
LTP) ו־Long-Term Depression (LTD)
חזרנו על החומר הקודם - פוטנציאל מנוחה, פוטנציאל פעולה, הדפולריזציה והריפולריזציה, והקפיצה של פוטנציאל הפעולה מנוד ראנוויה לנוד ראנוויה לאורך האקסון. פוטנציאל הפעולה מתחיל בתחילת האקסון (ה־Axon Hillock) ומתקדם לסוף האקסון.
Schwann Cells
תאי שוואן הם תאי גְלִייָה (תאי תמיכה לא־עצביים לנוירונים) של מערכת העצבים הפריפרית. הם ״מחבקים״ את האקסון בשכבות רבות של ממברנה ומבודדים אותו - זו שכבת המיאלין (Myelin Sheath). השם “מיאלין” נגזר מחלבון מסוים שנמצא בתוך השכבה השומנית. בין כל שני תאי שוואן עוקבים מפרידים צמתי ראנוויה (Nodes of Ranvier) שבהם האקסון חשוף, ושם מתחדש פוטנציאל הפעולה בהולכה קופצנית (Saltatory conduction). ניתן לזהות תא שוואן בחתך רוחב של עצב - הגרעין שלו הוא חלק ממעטפות האקסון, ורואים את גוף התא עוטף אותו מסביב.
The Oligodendrocyte
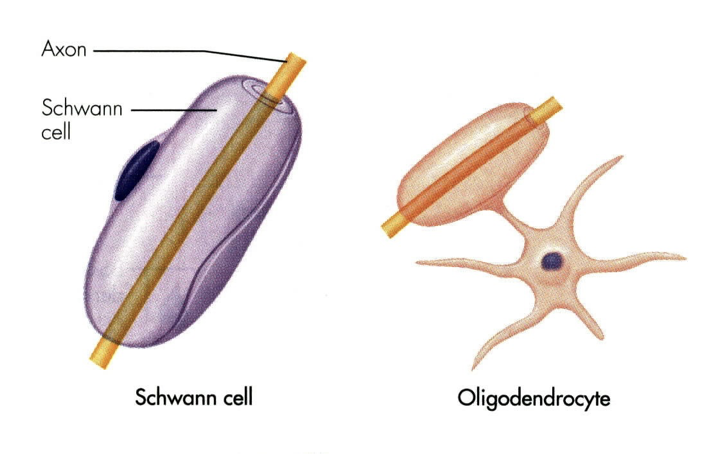
תא האוליגודנדרוציט ממלא תפקיד זהה של בידוד - אך שייך למערכת העצבים המרכזית (מוח וחוט השדרה), בעוד תאי שוואן נמצאים רק בפריפריה.
ההבדל המבני המשמעותי הוא שתא האוליגודנדרוציט לא נצמד לגוף האקסון - יש לו גוף תא, וממנו יוצאות שלוחות רבות שמסתובבות סביב אקסונים שונים. כלומר, אוליגודנדרוציט יחיד מסוגל לבודד מספר אקסונים שונים באותו אזור בו־זמנית - יתרון ניכר על פני תאי שוואן, שכל אחד מהם מכסה קטע יחיד של אקסון יחיד.
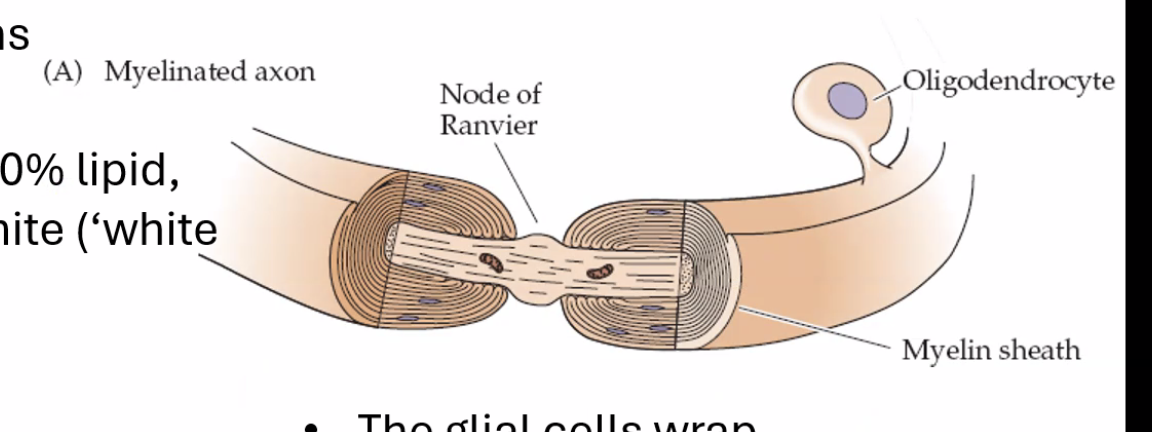
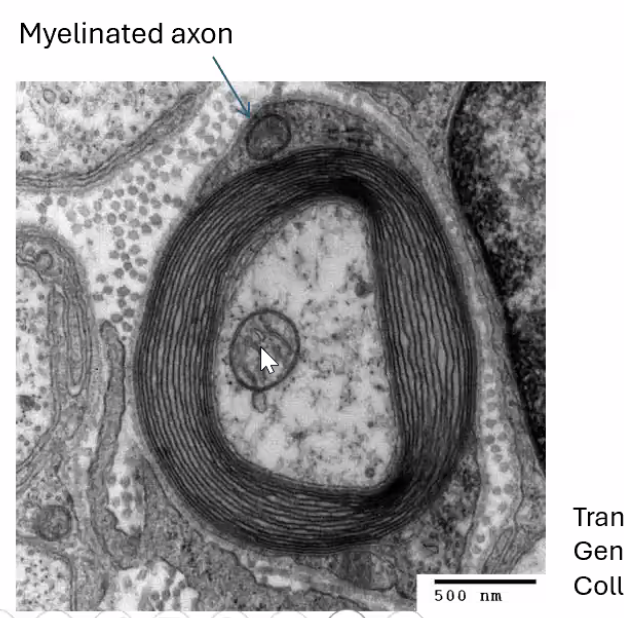
בתמונת מיקרוסקופ אלקטרוני זו רואים חתך רוחב של אקסון. מסביבו שכבת המיאלין. כאשר שואלים מה הגוף הגדול שנמצא בתוך האקסון עצמו - זו מיטוכונדריה, הניכרת במאפיין האופייני לה: קיפולי הממברנה הפנימית (ה־Inner membrane).
לגבי זיהוי סוג הבידוד: בתמונה זו ניתן לזהות שמדובר בתא שוואן ולא באוליגודנדרוציט, מכיוון שרואים את גוף התא עצמו צמוד ומחבק את האקסון.
ייחוס קליני - מחסור במיאלין
אצל חולים עם מחלות דמיאלינציה (Demyelination) כמו טרשת נפוצה (MS), ניתן למדוד את האטת ההולכה העצבית על ידי הצגת גירוי ויזואלי ומדידת הזמן עד להגעת האות לקליפת הראייה (Visual Evoked Potentials). גם הבדל של כ־20% בלבד בהולכה גורם לפתולוגיה קלינית ניכרת.
סיבי C - אקסונים ללא מיאלין
לא כל סיבי העצב בגוף עטופים במיאלין. קיימים סוגים נוספים, כמו סיבי C (C-fibers) - אקסונים דקים ללא שכבת מיאלין. הם אחראים בעיקר לתחושת כאב מאוחרת (כמה שניות לאחר הפגיעה) ולהולכה איטית בהרבה. נלמד עליהם בהרחבה בסמסטר ג’ בהקשר של פיזיולוגיה של הכאב.
Chemical Synapses vs. Electrical Synapses
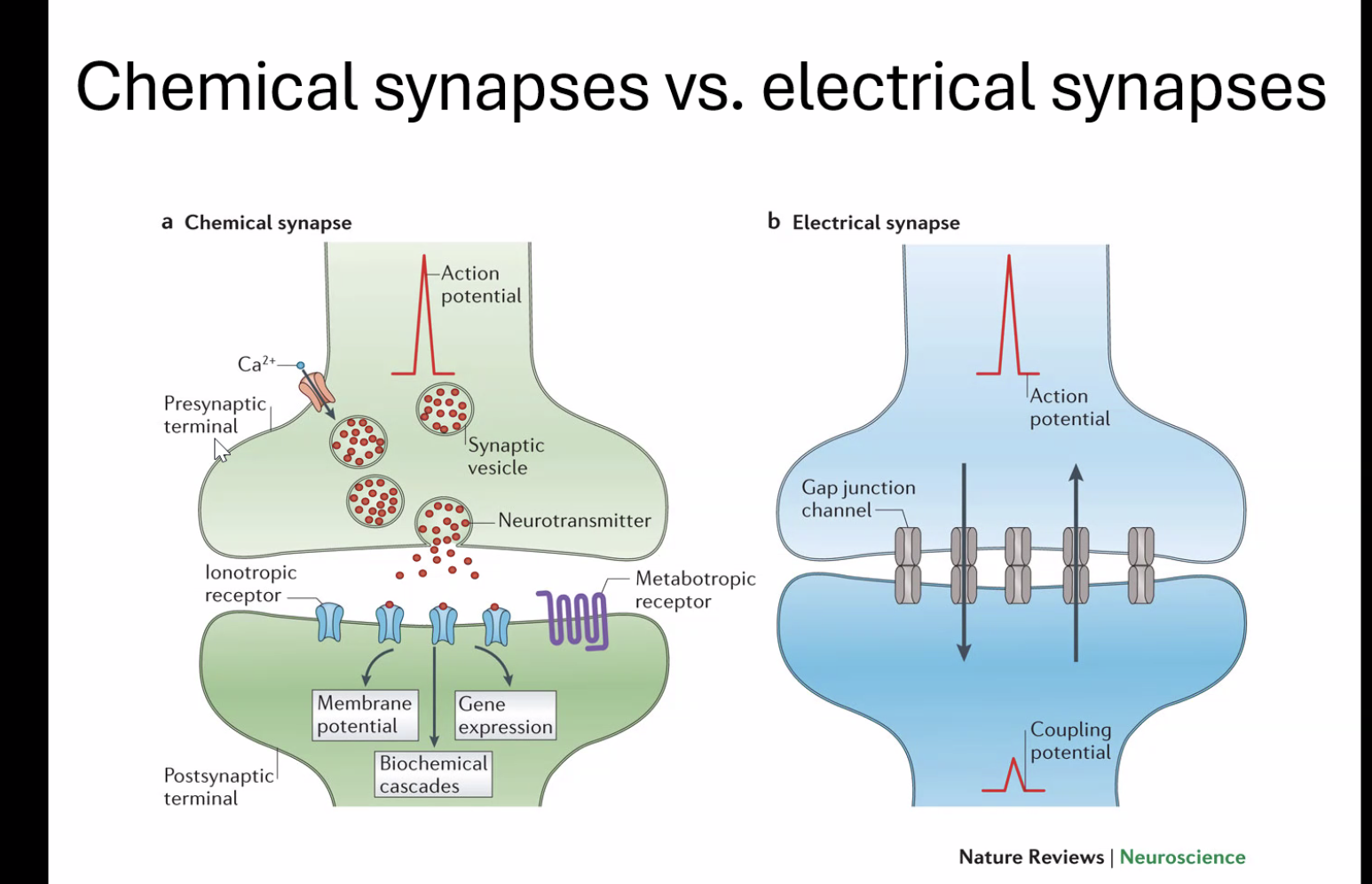
כשפוטנציאל הפעולה מגיע לסוף האקסון - לפריסינפסה - הוא יכול לתקשר עם התא הבא בתור, או עם תא אחר בגוף (כמו תא שריר). לתקשורת הזאת קוראים סינפסה, ויש שני סוגים עיקריים:
-
סינפסה חשמלית (Electrical synapse): ערוצים ישירים (Gap junctions) מחברים בין שני תאי העצב, ויונים (בעיקר נתרן) עוברים ישירות מתא לתא. המנגנון פשוט ומהיר, אך דווקא בגלל פשטותו - הוא נדיר יחסית, כי אין בו כמעט יכולת בקרה.
-
סינפסה כימית (Chemical synapse): זה הסוג הנפוץ ביותר, ובו נתמקד.
Communication Between Neurons - Release of Presynaptic Vesicles
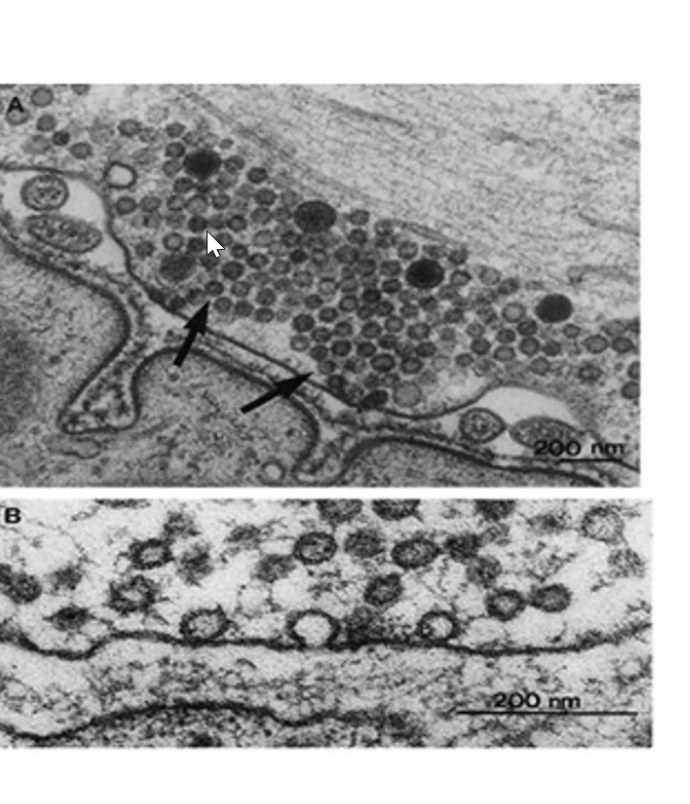
בפריסינפסה קיימות וסיקולות (שלפוחיות) רבות, הממתינות טעונות בנוירוטרנסמיטרים לשחרור. כשהאות החשמלי מגיע לסוף האקסון, הוא פותח תעלות סידן תלויות מתח (Voltage-gated Ca²⁺ channels) הייחודיות לפריסינפסה - לא תעלות נתרן כמו לאורך האקסון, אלא ספציפית תעלות סידן. הסידן נכנס מהמרחב החוץ־תאי לתוך הפריסינפסה, ושם מפעיל את מנגנון השחרור.
המנגנון המולקולרי מתבסס על SNARE proteins: חלבון Synaptobrevin שנמצא על הווסיקולה וחלבון Syntaxin שנמצא על ממברנת הפריסינפסה נקשרים זה לזה בנוכחות סידן - קירוב הממברנות גורם לאיחוי (Fusion) ולשחרור של הנוירוטרנסמיטרים אל הרווח הסינפטי (Synaptic cleft).
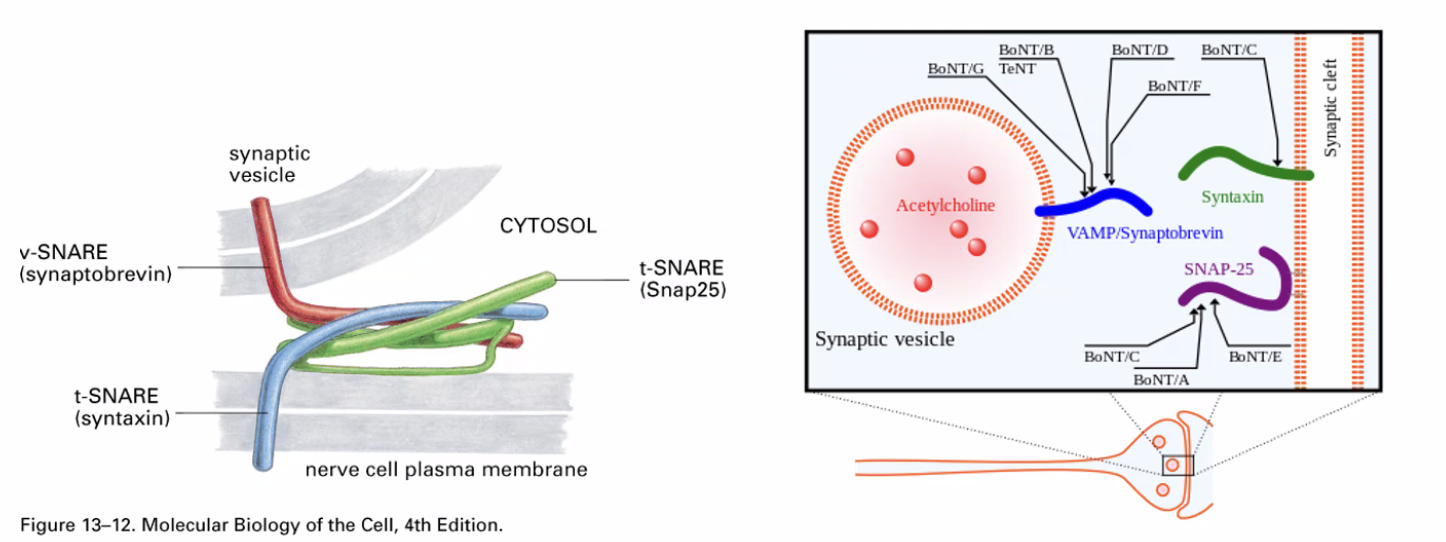
הנוירוטרנסמיטרים עוברים דיפוזיה אל הפוסט-סינפסה ונקשרים לקולטנים הנמצאים על ממברנת הדנדריט של תא העצב הבא.
חשיבות ה
סידן: הסידןהוא המתווך הקריטי ביותר לתקשורת סינפטית. חסימה מלאה שלו בתרביות תאים מפסיקה כמעט לחלוטין את כל הפעילות הסינפטית.
לכל תא עצב תדירות פוטנציאל פעולה
תא עצב אינו “שקט” בין אירועים - הוא כל הזמן יורה פוטנציאלי פעולה בתדירות כלשהי. אם התא מפסיק לגמרי לירות לאורך זמן, הוא מתחיל בתהליכים של אפופטוזיס (מוות מתוכנת). השאלה אינה “אם” - אלא באיזו תדירות הוא יורה.
Receptors on Postsynaptic Membrane
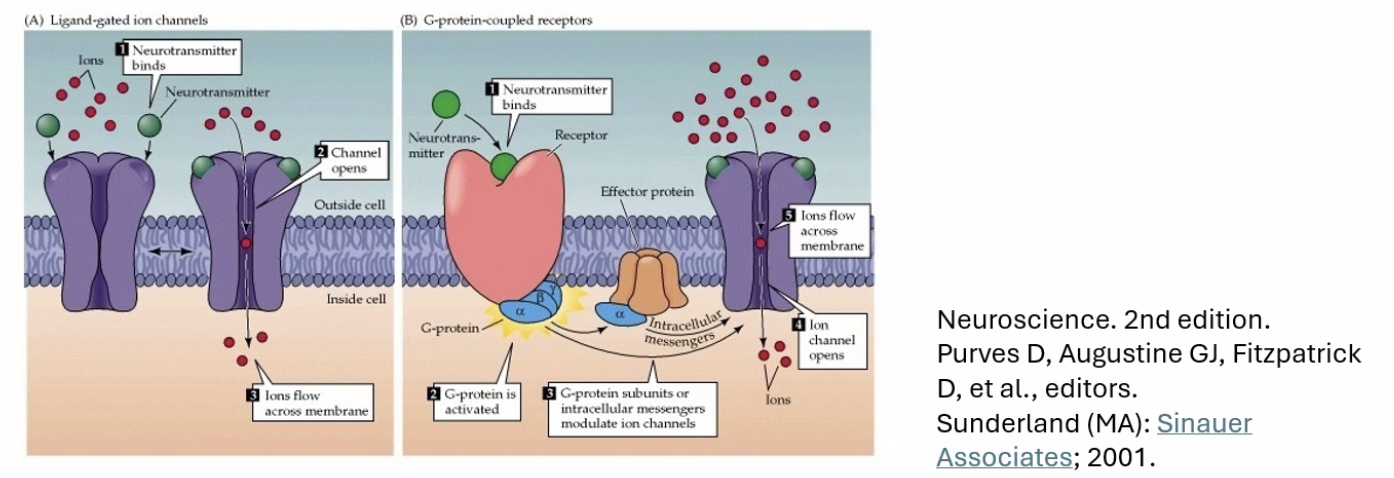
קולטני הפוסט-סינפסה מתחלקים לשני סוגים עיקריים:
-
Ionotropic receptors (קולטנים יונוטרופיים): הקולטן עצמו הוא תעלה. קישור הנוירוטרנסמיטר פותח את התעלה ישירות - יונים נכנסים או יוצאים. מהיר יחסית.
-
Metabotropic receptors (קולטנים מטבוטרופיים): הקולטן מחובר לחלבון G. קישור הנוירוטרנסמיטר גורם לשחרור חלבון G, שבתורו פותח תעלות אחרות או מפעיל שפעולי איתות תוך־תאיים, שינוי ביטוי גנים ועוד. איטי יותר, אך עם מגוון השפעות גדול הרבה יותר.
Excitatory and Inhibitory Postsynaptic Potentials (EPSP / IPSP)
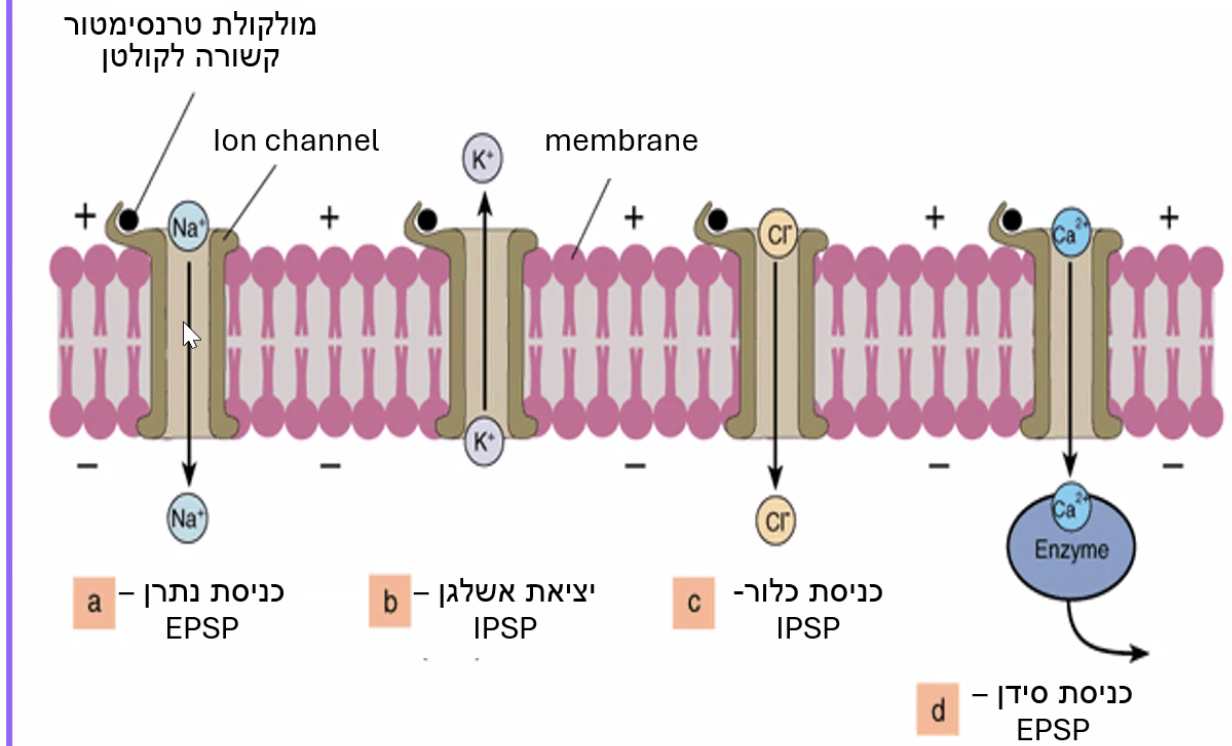
קישור נוירוטרנסמיטר לקולטן יגרום לאחד משני מצבים:
-
EPSP(Excitatory Postsynaptic Potential): עלייה במתח הממברנה (דפולריזציה). לדוגמה - אם הקולטן הוא תעלת נתרן, נתרן נכנס לתא, המתח בפנים נהייה חיובי יותר -EPSP. -
IPSP(Inhibitory Postsynaptic Potential): ירידה במתח הממברנה (היפרפולריזציה). לדוגמה - אם הקולטן הוא תעלת אשלגן, אשלגן יוצא מהתא (מכיוון שמתח השיווי משקל שלו שלילי מאוד), המתח בפנים יורד -IPSP. באותו אופן, כניסת כלור (שלילי) גורם גם היא ל־IPSP.
ההיגיון: מה שנקבע הוא לא סוג היון (כי גם נתרן וגם אשלגן חיוביים), אלא כיוון התנועה בהתאם להפרש מתח השיווי משקל (Equilibrium potential) של כל יון.
פרופגציה של EPSP/IPSP בדנדריטים
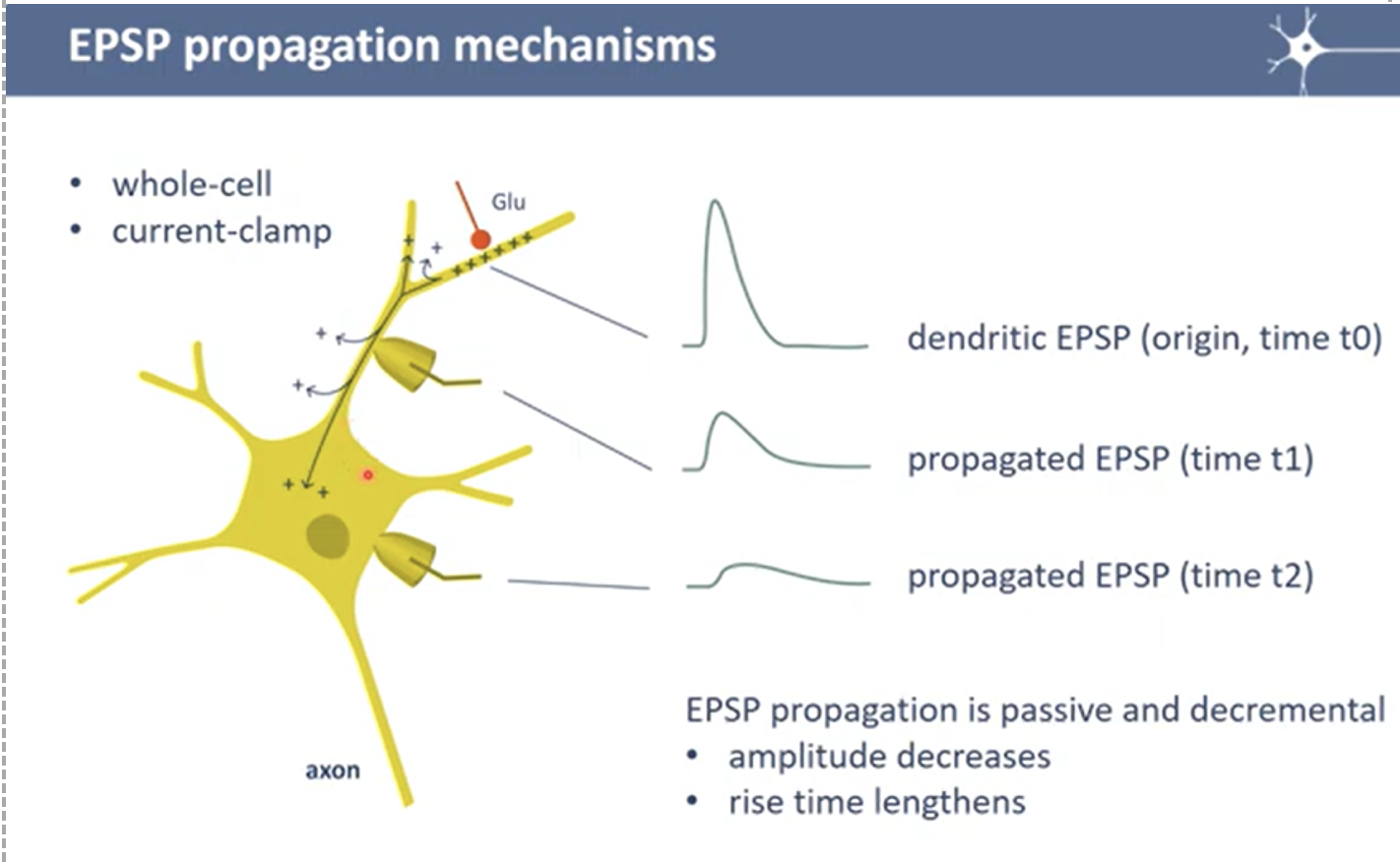 | 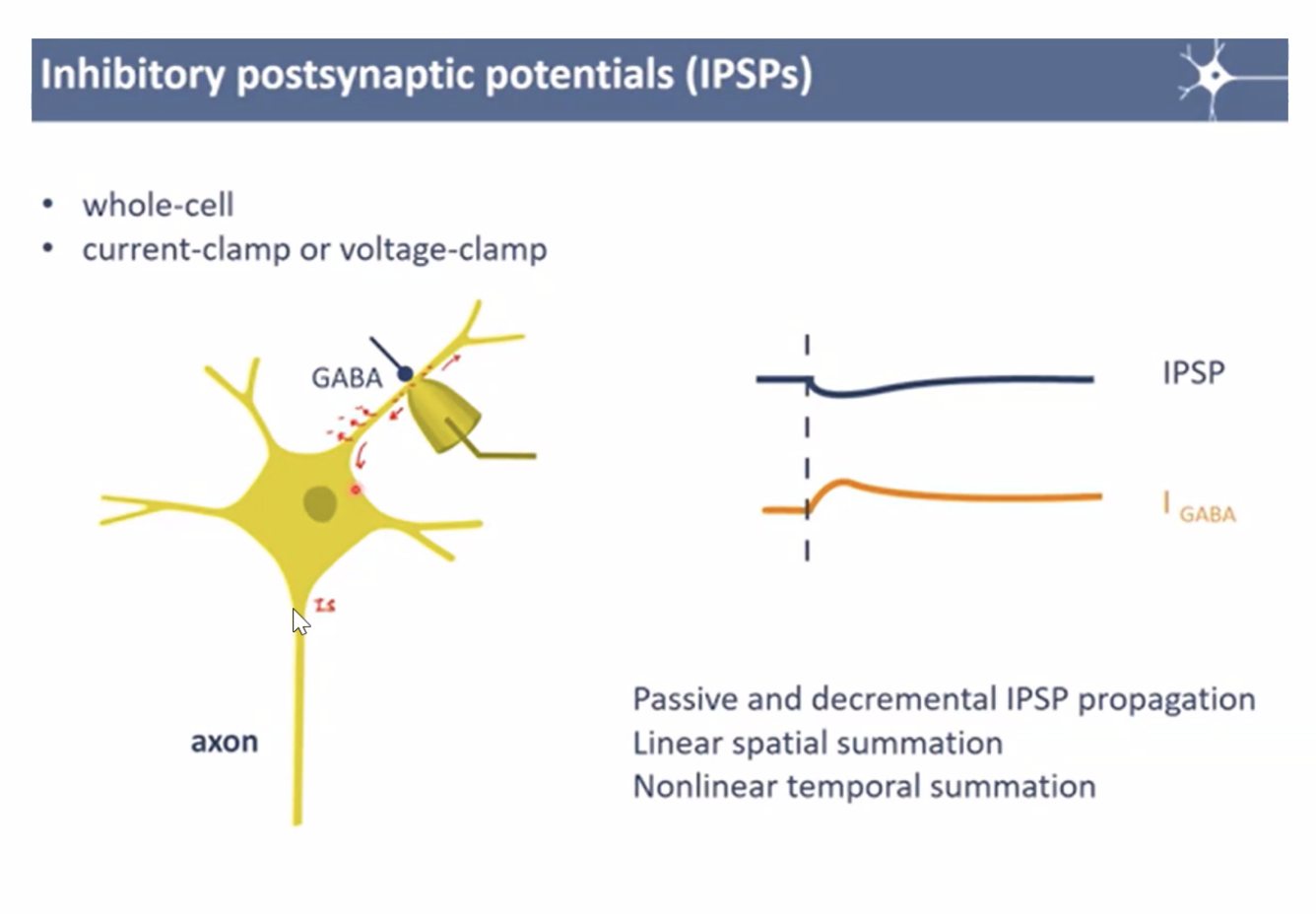 |
EPSP הוא לא פוטנציאל פעולה - בדנדריטים אין תעלות נתרן תלויות מתח. לכן, שינוי המתח שנוצר בסינפסה לא מתחדש, אלא עובר דיפוזיה פסיבית לאורך הדנדריט, ודועך ככל שמתרחק. עד שמגיע ל־Axon Hillock, ה־EPSP שהיה אולי $−40 \, \mathrm{mV}$ בסינפסה, יגיע אולי רק לבערך $−65\, \mathrm{mV}$.
באותו אופן עובד ה־IPSP - ירידה במתח שעוברת בדיפוזיה לאורך הדנדריט ומגיעה (לאחר דעיכה) ל־Axon Hillock.
Axon Hillock - נקודת ההחלטה
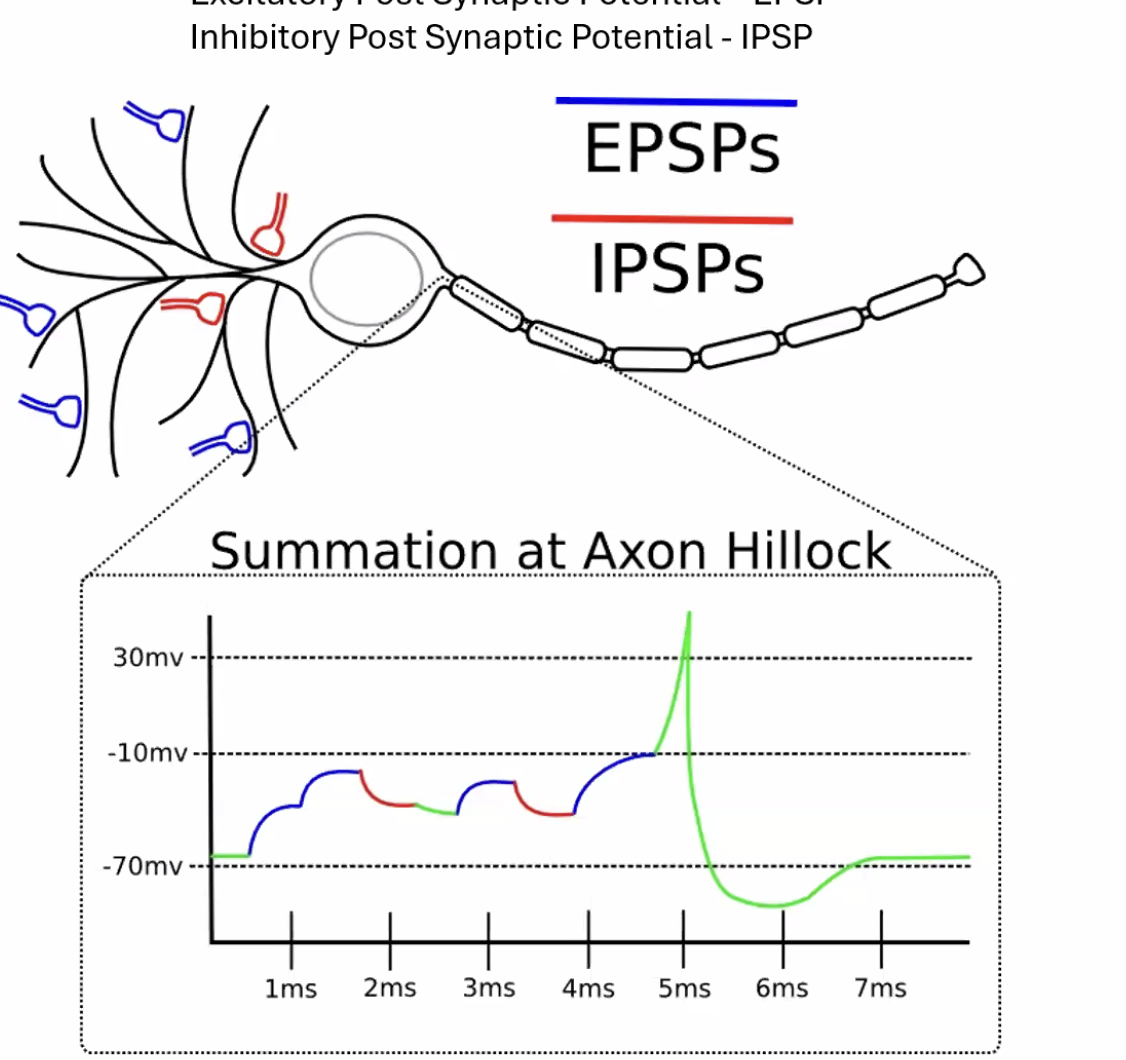
ה־Axon Hillock הוא נקודת האינטגרציה של כל המידע שתא העצב מקבל. מאות סינפסות יכולות לפעול על אותו תא בו־זמנית - חלקן מייצרות EPSPs וחלקן IPSPs - וכולן מתכנסות ל־Axon Hillock.
אם הסכום של כל ה־EPSPs מנצח את כל ה־IPSPs ומגיע לסף (Threshold) הנדרש לפתיחת תעלות נתרן תלויות מתח - מתחיל פוטנציאל פעולה, שעובר את האקסון עד סופו. ברגע שהתחיל - הוא ימשיך עד הסוף. אין “פוטנציאל פעולה חזק” או “חלש” - פוטנציאל פעולה הוא עקרון “הכל או לא כלום” (All-or-Nothing), בדיוק כמו ביט בינארי: 0 או 1.
אז איך מבטאים עוצמה? לא בחוזק הפוטנציאל, אלא בתדירות שלו. ההבדל בין להרים כוס לבין להרים משקל של 20 ק”ג הוא התדירות של פוטנציאלי הפעולה המגיעים לאותו שריר - לא חוזקם.
Temporal and Spatial Summation
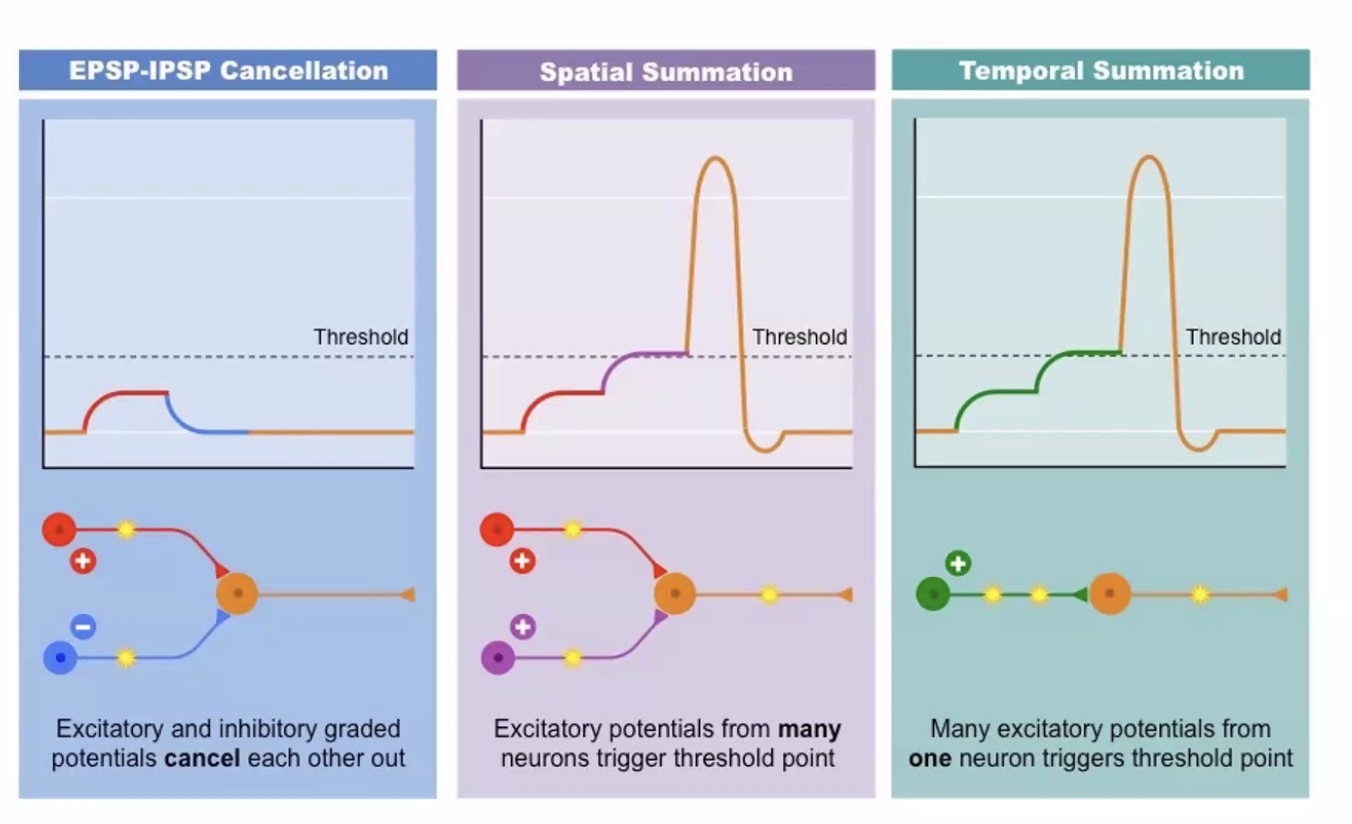
שני מנגנוני סכימה שמאפשרים ל־Axon Hillock להגיע לסף:
-
Spatial Summation (סכימה מרחבית): שתי סינפסות שונות על שני דנדריטים שונים מופעלות בו־זמנית - ה־
EPSPsשלהן מסתכמים ב־Axon Hillock. -
Temporal Summation (סכימה זמנית): סינפסה בודדת אחת יורה בתדירות כל כך גבוהה, שה־
EPSPשל הירייה הבאה מגיע לפני שה־EPSPהקודם דעך לגמרי - ומצטבר עליו.
Example - Integration of Information (שובע)
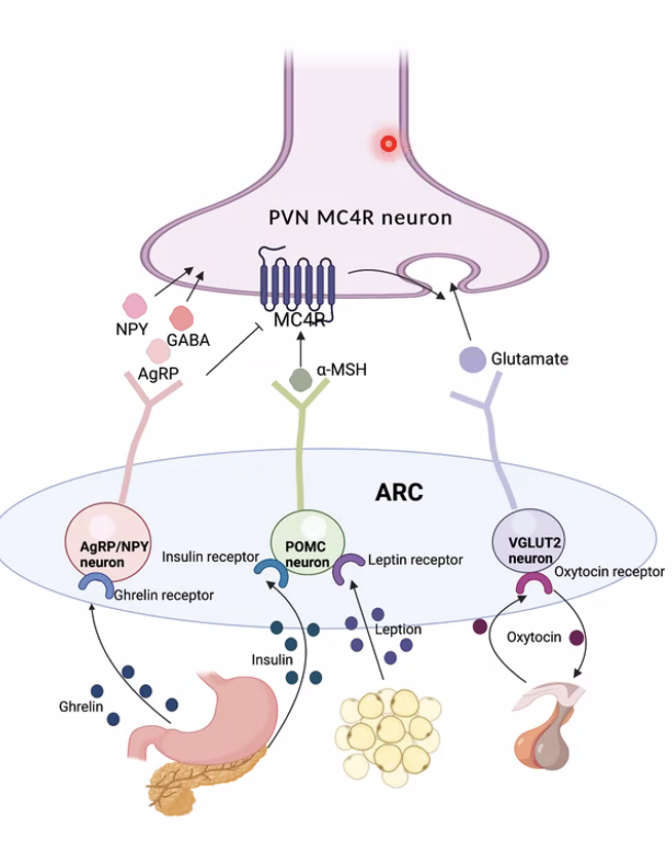
דוגמה יפה לאינטגרציה: תא עצב שאחראי על תחושת שובע מקבל קלט מכמה מקורות במקביל. ההורמון לפטין (שמופרש מרקמת שומן) מפעיל תאי עצב שמשחררים נוירוטרנסמיטר הגורם ל־EPSP - ומעלה סיכוי לתחושת שובע. ההורמון גרלין (שמופרש כשלא אכלנו זמן רב) מפעיל נתיב אחר הגורם ל־IPSP - ומוריד את הסיכוי לשובע ומגביר רעב. כל ההורמונים האלה מגיעים ל־Axon Hillock של אותו תא עצב, ושם מתקבלת ה”החלטה” האם אני שבע עכשיו.
Synapse - Clearance of Neurotransmitters
Clearance of Neurotransmitters is important to stop the signal!
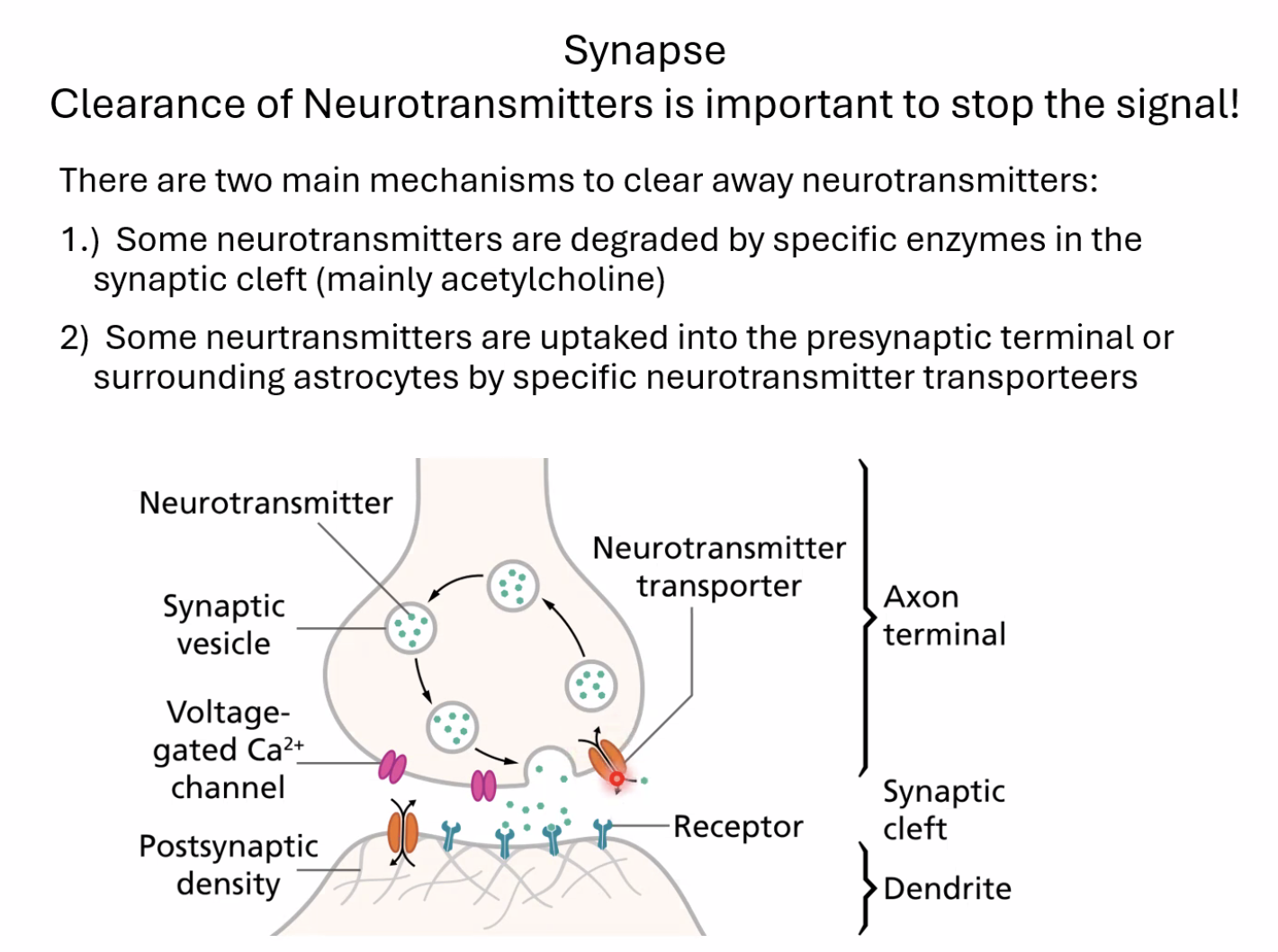
לאחר שהנוירוטרנסמיטר נקשר לקולטן ועשה את עבודתו, הוא חייב לעזוב את הרווח הסינפטי - אחרת האות לא ייפסק. שני מנגנונים עיקריים:
-
פירוק אנזימטי: חלק מהנוירוטרנסמיטרים (בעיקר אצטילכולין) מפורקים על ידי אנזים ספציפי ישירות ברווח הסינפטי. מה שנשאר לאחר הפירוק (הרכיבים) נקלט חזרה ומשמש לייצור מחדש.
-
קליטה חזרה (Reuptake): רוב הנוירוטרנסמיטרים נקלטים חזרה לפריסינפסה (ולעיתים לאסטרוציטים שכנים) דרך טרנספורטרים - תעלות ייחודיות לכל נוירוטרנסמיטר. שם הם נארזים מחדש לווסיקולות לשימוש עתידי - מחזור (Recycling) יעיל.
תרופות רבות פועלות בדיוק על הטרנספורטרים האלה - למשל, תרופות נוגדות דיכאון מסוג SSRI חוסמות את טרנספורטר הסרוטונין, מה שגורם לסרוטונין להישאר זמן רב יותר ברווח הסינפטי.
Clinical Application - Lidocaine / Benzocaine
לידוקאין ובנזוקאין (נמצאים למשל ב”קל־גרון”) הם תרופות משככי כאבים מקומיות שפועלות על ידי חסימת תעלות נתרן תלויות מתח. ללא פתיחת תעלות נתרן, אין פוטנציאל פעולה - ואין העברת אות כאב. עצבי החישה (Sensory neurons) באותו אזור פשוט מפסיקים לתקשר עם המוח.
Different Types of Action Potentials
פוטנציאל פעולה יכול להיראות שונה בין רקמות שונות, בהתאם לצורך הפיזיולוגי. הדוגמה המרכזית: תאי שריר הלב (Cardiomyocytes).
אצטילכולין (Acetylcholine)
הנוירוטרנסמיטר אצטילכולין מיוצר על ידי חיבור של שתי מולקולות:
- Acetyl-CoA - מגיע ממסלול הגליקוליזה
- Choline - מגיע מהתזונה, או מפירוק אצטילכולין קודם
האנזים Choline Acetyltransferase (ChAT) מחבר בין השתיים ויוצר אצטילכולין. ניתן לזהות תאי עצב כולינרגיים בחתך מוח על ידי צביעה לאנזים הזה.
פירוק אצטילכולין - אצטילכולין אסטראז
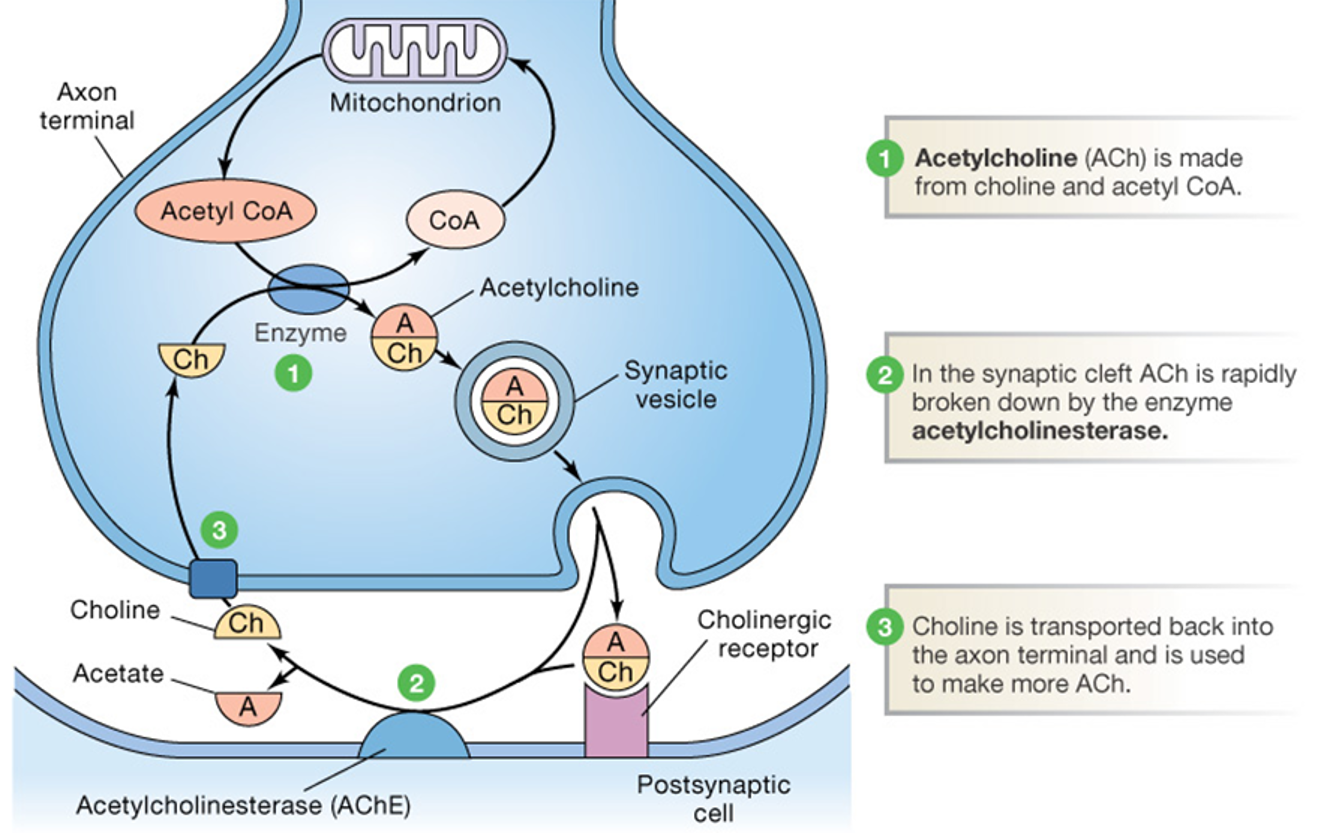
שלא כמו רוב הנוירוטרנסמיטרים שנקלטים חזרה שלמים, אצטילכולין מפורק ברווח הסינפטי על ידי האנזים Acetylcholinesterase. הפירוק מחזיר לפריסינפסה רק את ה־Choline, שממוחזר לייצור אצטילכולין חדש.
גזים עצביים (כמו גז סרין) פועלים על ידי עיכוב אצטילכולין אסטראז - הצטברות אצטילכולין ברווח הסינפטי גורמת לעירור מוגזם ולשיתוק.
קולטן ניקוטיני (Nicotinic Receptor)
קולטן יונוטרופי - תעלה ישירה לנתרן. קישור אצטילכולין פותח את התעלה, נתרן נכנס - EPSP. שמו נגזר מכך שניקוטין אף הוא קושר ומפעיל קולטן זה, וכך פועל רוב האפקט הפרמקולוגי שלו.
קולטן מוסקריני (Muscarinic Receptor)
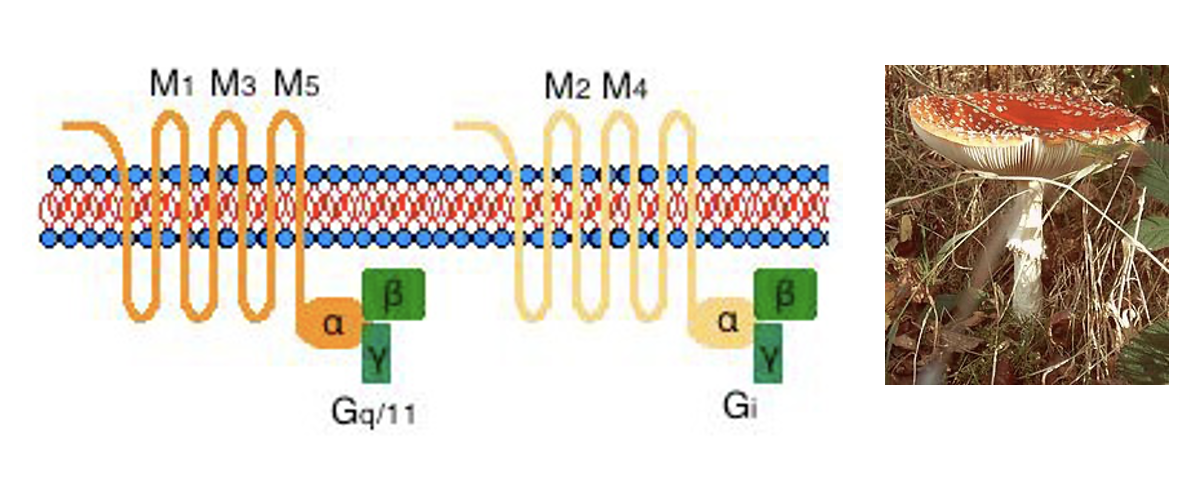
קולטנים מטבוטרופיים המחוברים לחלבון G. קיימים חמישה תתי-סוגים (M1–M5), כל אחד מקודד בגן שונה:
- M1, M3, M5 - מחוברים לחלבון Gq; הפעלתם גורמת בסופו של דבר ל־
EPSP. - M2, M4 - מחוברים לחלבון Gi; הפעלתם פותחת תעלות אשלגן וגורמת ל־
IPSP.
המסקנה החשובה: אצטילכולין יכול לגרום גם EPSP וגם IPSP - הכל תלוי בסוג הקולטן שנמצא על הפוסט-סינפסה. העיקרון הזה נכון לרוב הנוירוטרנסמיטרים.
Neuromuscular Junction
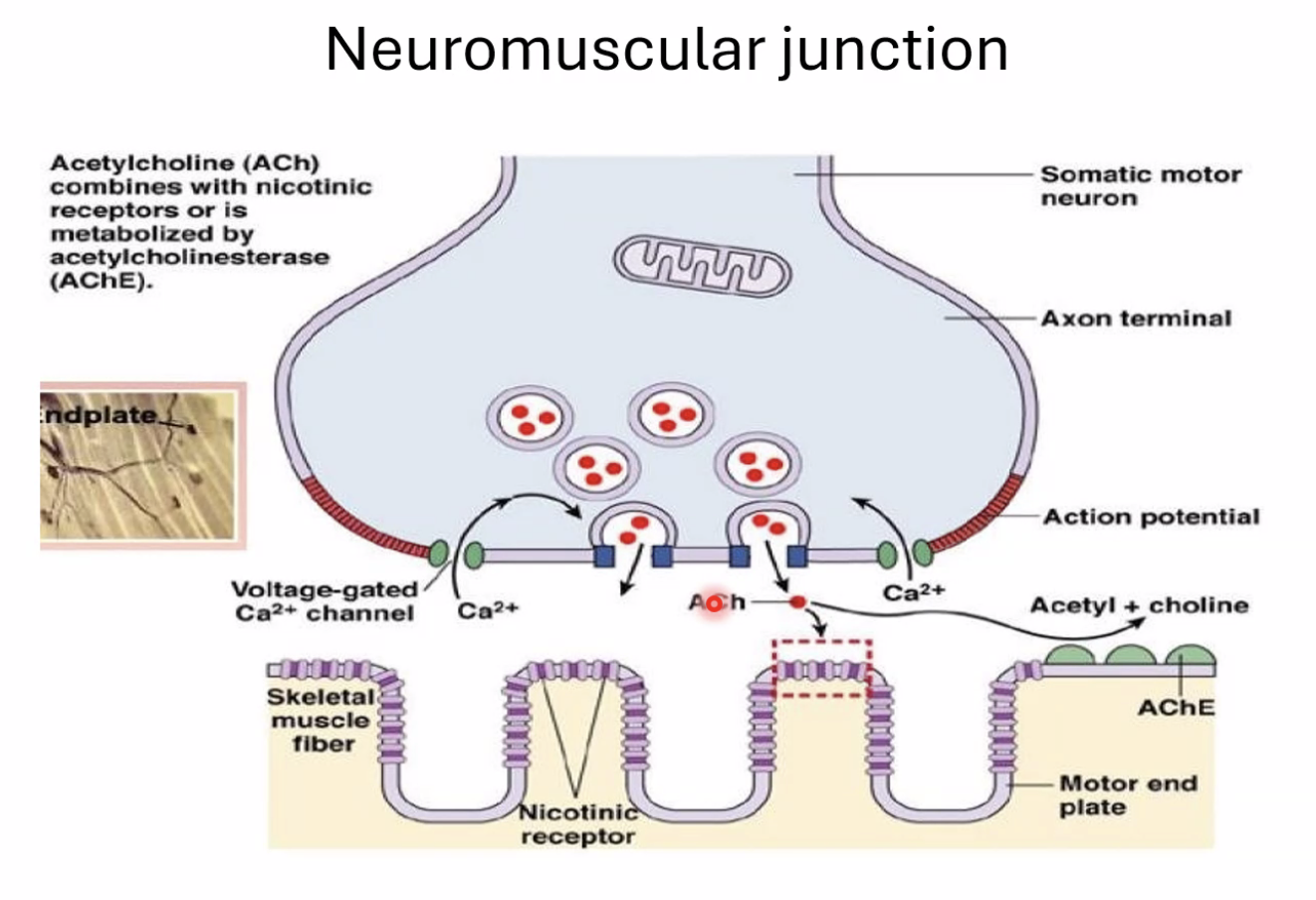
ה־Neuromuscular Junction הוא הסינפסה בין מוטונוירון (תא עצב מוטורי) לבין תא שריר. בסוף האקסון משתחרר אצטילכולין, שנקשר לקולטנים ניקוטיניים בלבד (אין כאן קולטנים מוסקריניים) על ממברנת תא השריר, גורם ל־EPSP, ומפעיל את מנגנון הכיווץ. ככל שתדירות פוטנציאלי הפעולה גבוהה יותר - כיווץ חזק יותר על ידי Summation.
Cardiomyocytes - תאי שריר הלב
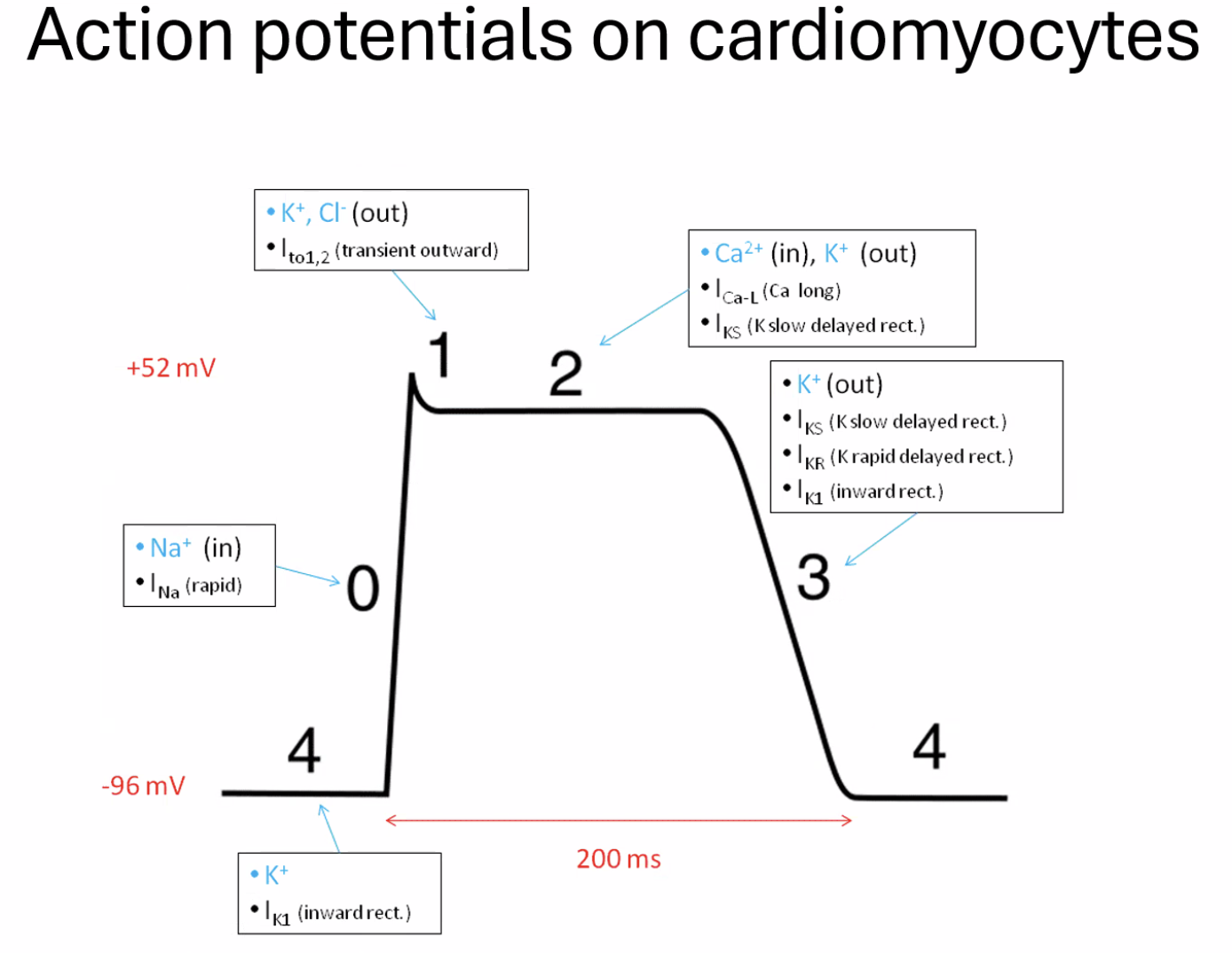
לתאי שריר הלב יש פוטנציאל פעולה משלהם, שנראה שונה בצורה מהותית. המאפיין הבולט הוא הפלאטו (Plateau): לאחר הדפולריזציה הראשונית, המתח לא יורד מיד, אלא נשאר גבוה לאורך זמן (כ־200–300 מילישניות). מה שגורם לפלאטו הוא פתיחה של Slow Ca²⁺ channels - תעלות סידן שנפתחות ונסגרות לאט, ויוצרות מצב שבו כניסת סידן ויציאת אשלגן מאזנות זו את זו.
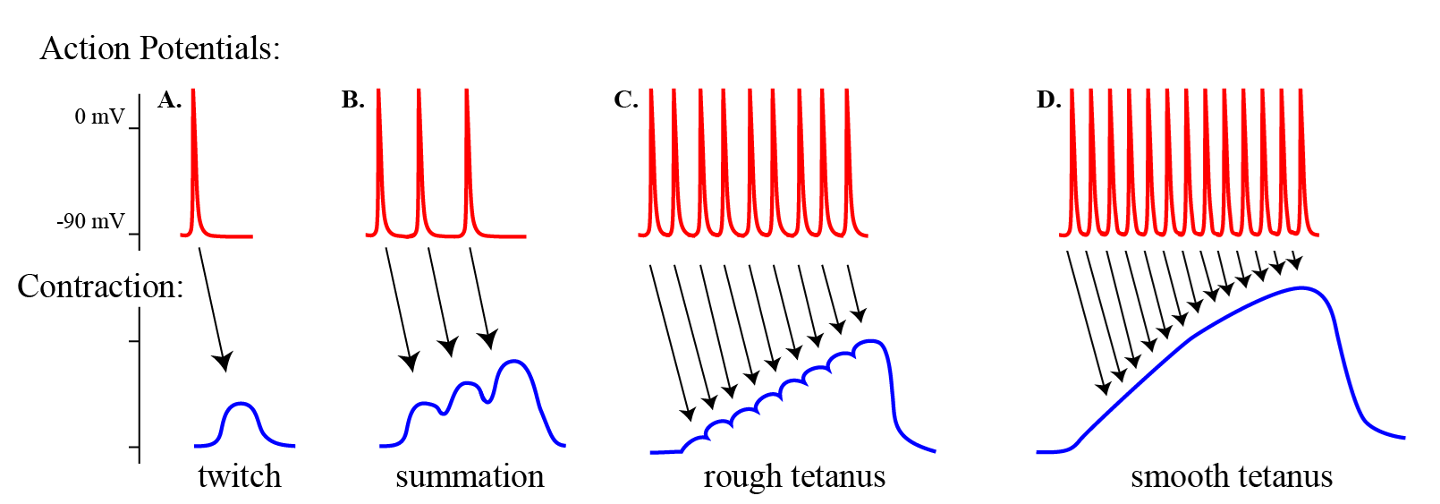
המשמעות הפיזיולוגית: תקופת הרפרקטוריות (Refractory period) הרבה יותר ארוכה, מה שאומר שלא ניתן להגיע לטטנוס לבבי. בשריר שלד, אם התדירות גבוהה מספיק, ניתן להגיע לכיווץ מתמשך (Tetanus). בלב - המנגנון הזה נמנע, כי הלב חייב להרפות בין פעימה לפעימה כדי להתמלא שוב בדם. הפלאטו הארוך מבטיח זאת.
EEG
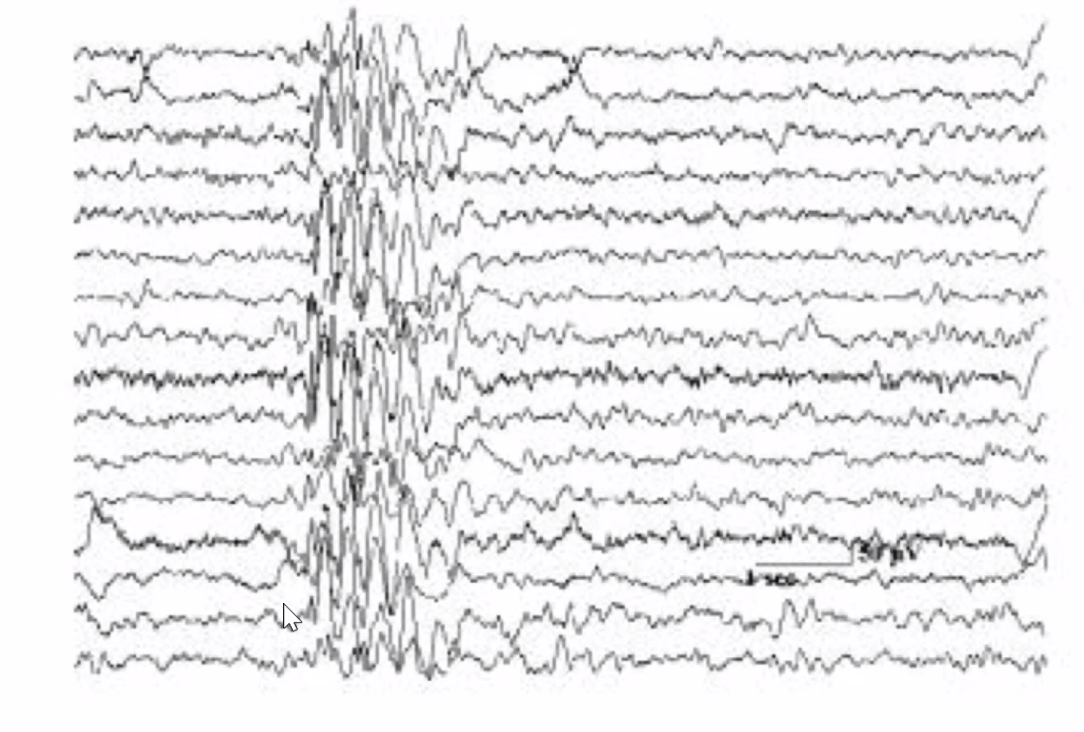
EEG (Electroencephalography) הוא מדידה של הפעילות החשמלית על פני הקרקפת. אלקטרודות המוצמדות לאזורים שונים בראש מודדות כל אחת את “הממוצע החשמלי” של מיליוני תאי עצב מתחתיה בקליפת המוח (Cortex).
הגדולה שב־EEG היא לא במדידה של תא עצב בודד, אלא בסינכרוניזציה - כמה תאי עצב פועלים באותו זמן:
- כשתאי עצב פועלים לא סינכרונית (כל אחד בתדירותו הייחודית, כמו בזמן ערות ועיסוק קוגניטיבי) - ה־EEG מראה אמפליטודות נמוכות ותדירות גבוהה (גלי ביתא).
- כשתאי עצב פועלים בסינכרוניזציה גבוהה (כולם יחד) - האמפליטודה עולה.
שינה עמוקה (Slow wave sleep, Stage 4): גלי דלטה עם אמפליטודה גבוהה - מרבית קליפת המוח פועלת בסינכרוניזציה.
אפילפסיה: במהלך התקף, פתאום כל תאי העצב באזור מסוים יורים יחד בצורה חריגה. ה־EEG מראה עלייה פתאומית ודרמטית באמפליטודה - זה בדיוק מה שרואים בתמונה.
Synaptic Plasticity - פלסטיות סינפטית
פלסטיות סינפטית היא היכולת לשנות את חוזק הסינפסות - לחזק או להחליש אותן - בתגובה לפעילות. זהו המנגנון הבסיסי של זיכרון ולמידה.
זיכרון ולמידה
Non-associative Memory - Habituation & Sensitization
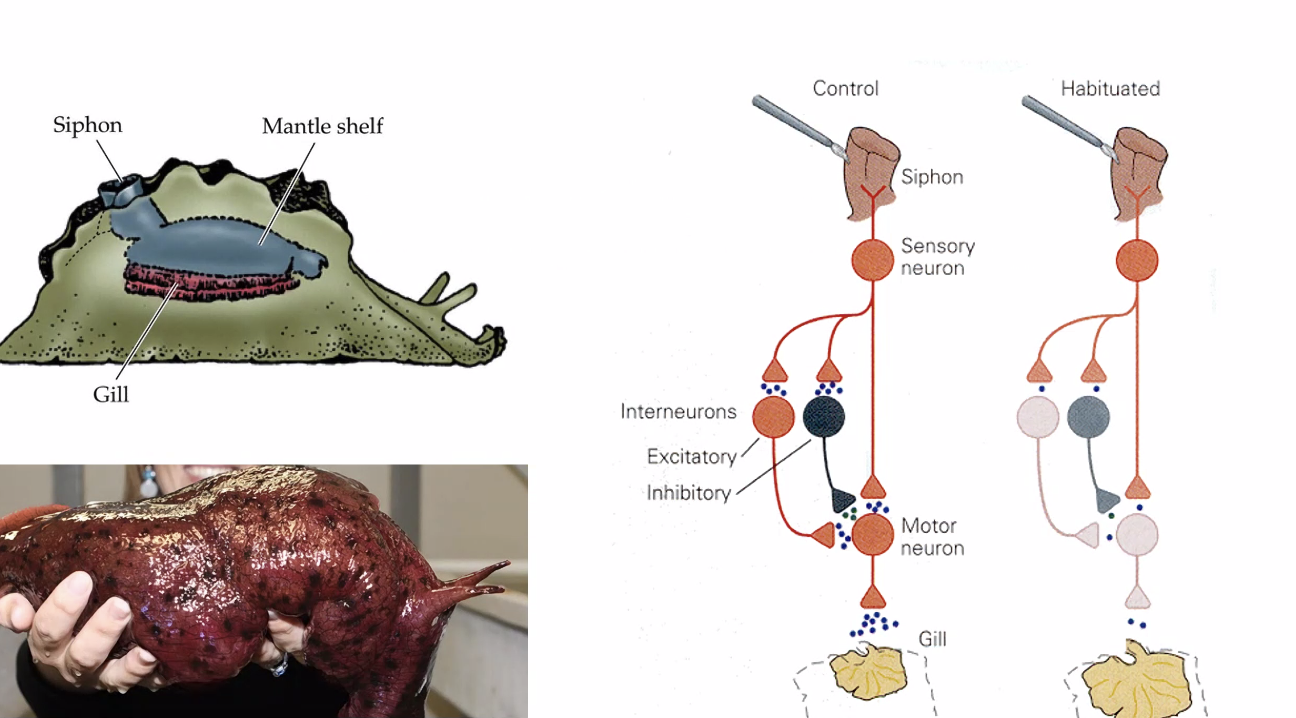
המודל הניסויי המפורסם הוא Aplysia - חילזון ים גדול שנחקר רבות. לאפליזיה יש איבר בשם Siphon, שכאשר נוגעים בו גורם לריפלקס של כיווץ כלי הנשימה (Gill withdrawal reflex). המסלול הוא פשוט: נוירון חישה ← סינפסה ← מוטונוירון ← כלי הנשימה.
-
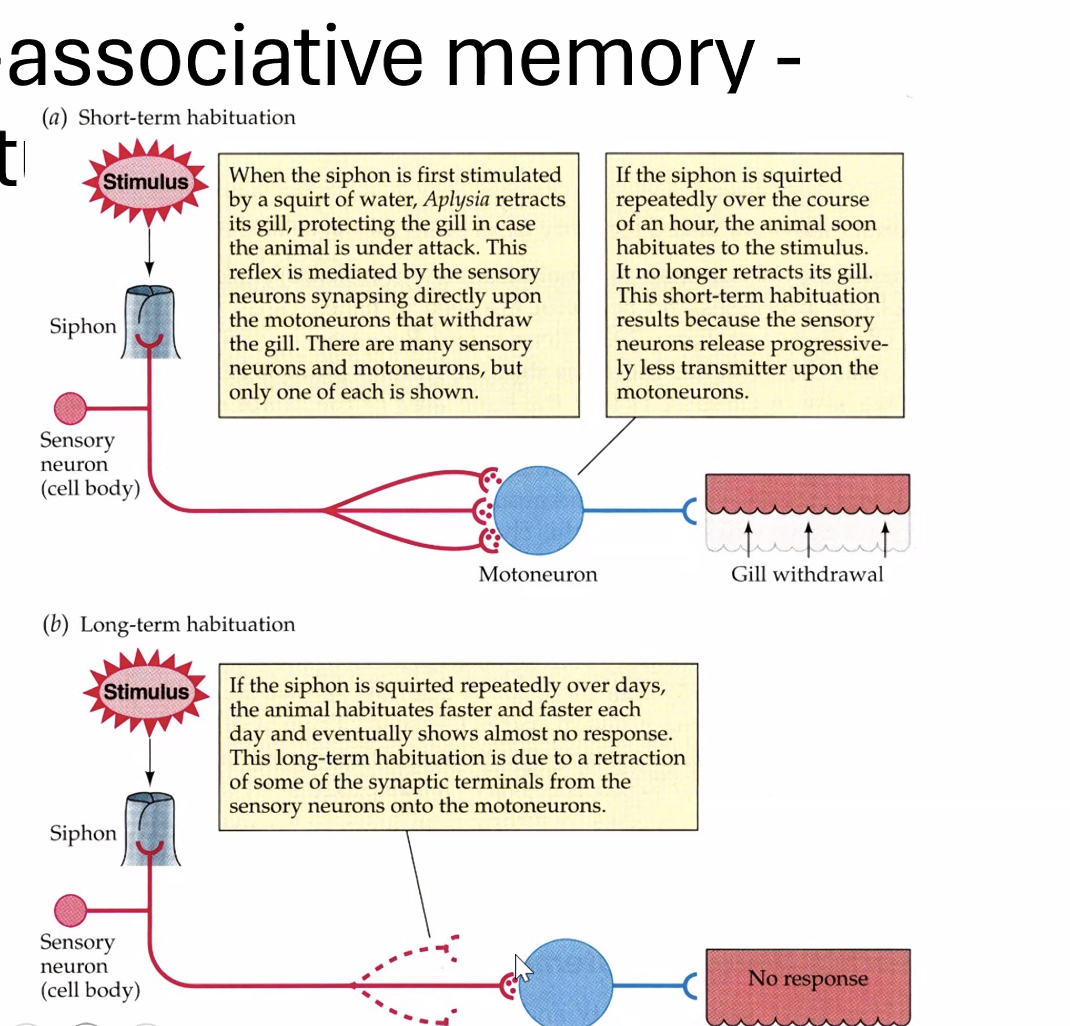
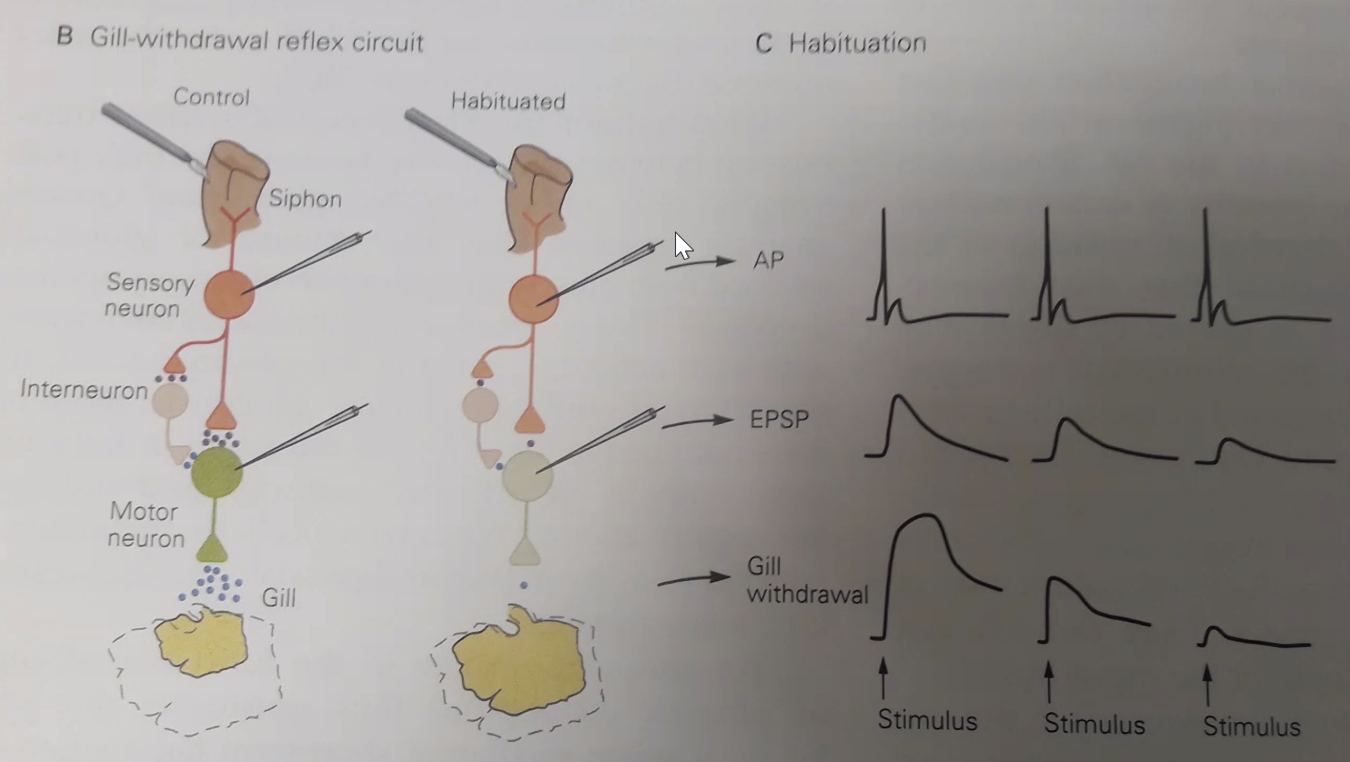
Habituation (הביטואציה): גירוי חוזר ונשנה של ה־Siphon גורם לתגובה פוחתת. בטווח הקצר - הפריסינפסה מיצתה את מאגר הנוירוטרנסמיטרים שלה. בטווח הארוך - חלק מהסינפסות נעלמות, אחרות נחלשות. ביום למחרת, התגובה עדיין מופחתת. זהו אחד מסוגי הזיכרון הפשוטים ביותר - הגוף “זכר” שהגירוי הזה לא מסוכן ולא חשוב. בדיוק כמו רעש לבן: נכנסים לחדר עם שעון מתקתק - אחרי רגע כבר לא שומעים אותו.
-
Sensitization (סנסיטיזציה): גירוי חזק במיוחד גורם לתגובה מוגברת. תא העצב החישתי אינו משתנה - אבל השינוי בסינפסה (חיזוקה) גורם ל־
EPSPחזק יותר בפוסט-סינפסה, וסיכוי גבוה יותר לפוטנציאל פעולה.
Hebb’s Rule: “Neurons that fire together, wire together”
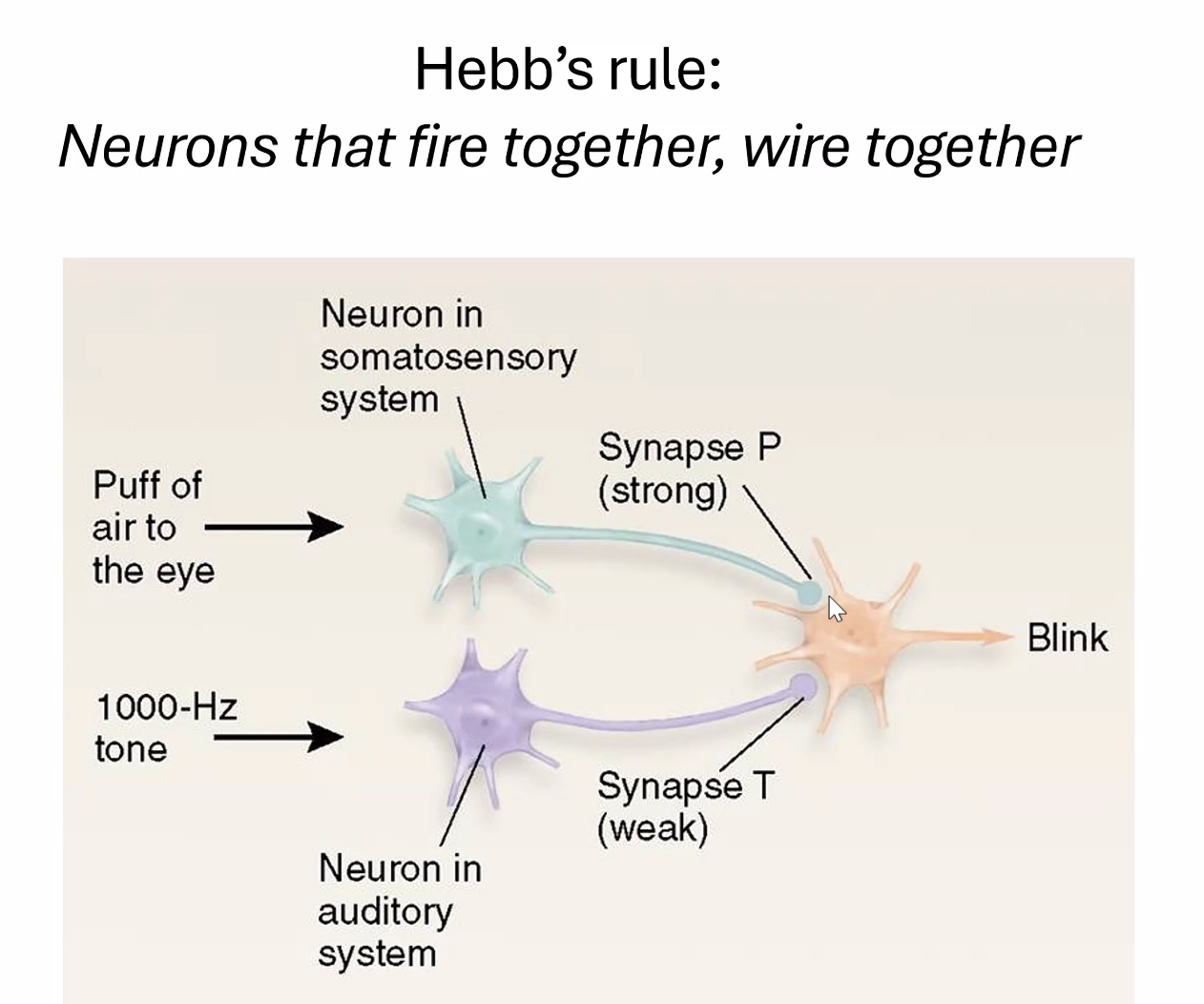
עיקרון הב: כאשר שתי סינפסות מופעלות בו־זמנית - הסינפסה החלשה מחוזקת. זהו הבסיס לזיכרון אסוסיאטיבי - קישור בין שני גירויים שהתרחשו יחד. בדיוק כמו ניסויי פבלוב: כלב שמשמיע צליל + מקבל אוכל ← בסופו של דבר הצליל לבד מפריש רוק. ברמה הנוירונלית: הסינפסה החלשה (מהמסלול השמיעתי) חוזקה בגלל הפעלה בו־זמנית עם הסינפסה החזקה (מהמסלול הויזואלי).
המנגנון המולקולרי - קולטן NMDA
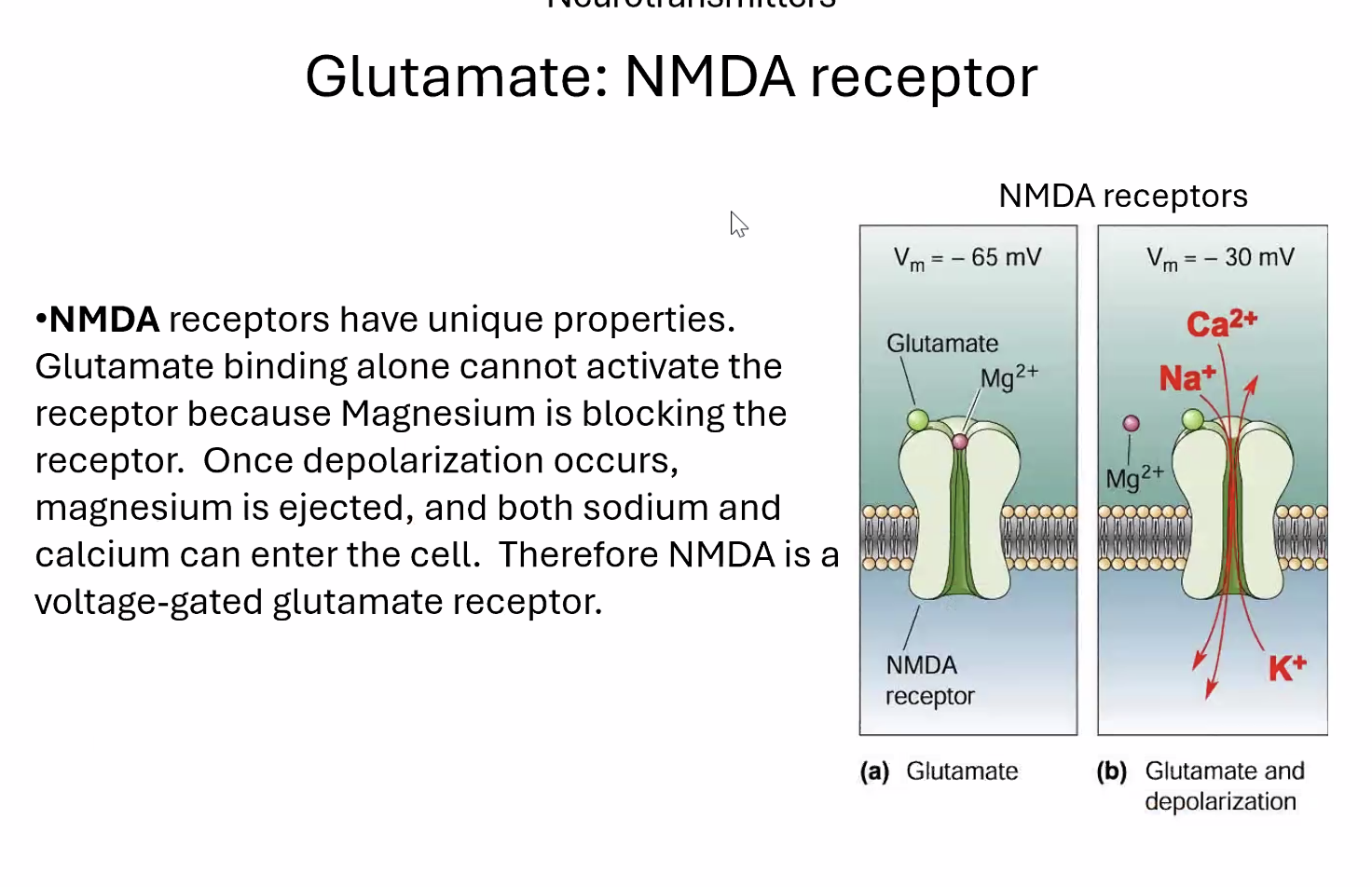
קולטן NMDA הוא קולטן יונוטרופי לגלוטמט, ומאפיינו הייחודי הוא שהוא דורש שני תנאים בו־זמנית כדי להיפתח:
- קישור של גלוטמט - הנוירוטרנסמיטר הנפוץ ביותר.
דפולריזציהמספקת של הממברנה (בסביבות $−30 \, \mathrm{mV}$) - כלומר, הסינפסה צריכה להיות מופעלת בו־זמנית עם פוטנציאל פעולה בתא.
הסיבה לדרישה השנייה: בתוך תעלת ה־NMDA נמצא יון מגנזיום החוסם אותה כאשר המתח שלילי. רק כאשר המתח עולה מספיק - המגנזיום מסולק והתעלה נפתחת.
מה נכנס דרכה? גם נתרן וגם סידן - דבר נדיר ביותר, כי לרוב תעלות יונוטרופיות סלקטיביות ליון אחד.
תפקיד הסידן: הסידן הנכנס קושר את החלבון Calmodulin, שמפעיל את האנזים CaMKII (Calcium/Calmodulin-dependent Protein Kinase II). CaMKII מזרחן קולטני AMPA (קולטן יונוטרופי נוסף לגלוטמט), שגורם לגיוסם מווסיקולות תוך־תאיות אל ממברנת הסינפסה. כתוצאה - יש יותר קולטני AMPA על הפוסט-סינפסה.
בנוסף לכך: כניסת סידן יכולה לגרום לשינוי מבני של הסינפסה - הרחבת שטח המגע בין פריסינפסה לפוסט-סינפסה, מה שמגביר עוד יותר את היעילות.
קולטן NMDA כ”חיישן הזדמנות”: הוא בעצם מגלה האם הסינפסה הנוכחית פעלה בו־זמנית עם פוטנציאל פעולה של התא - סימן לכך שהסינפסה הזו היתה חלק מהפעילות הכוללת. במצב כזה, מתקיים חיזוק (LTP).
Long-Term Potentiation (LTP) ו־Long-Term Depression (LTD)
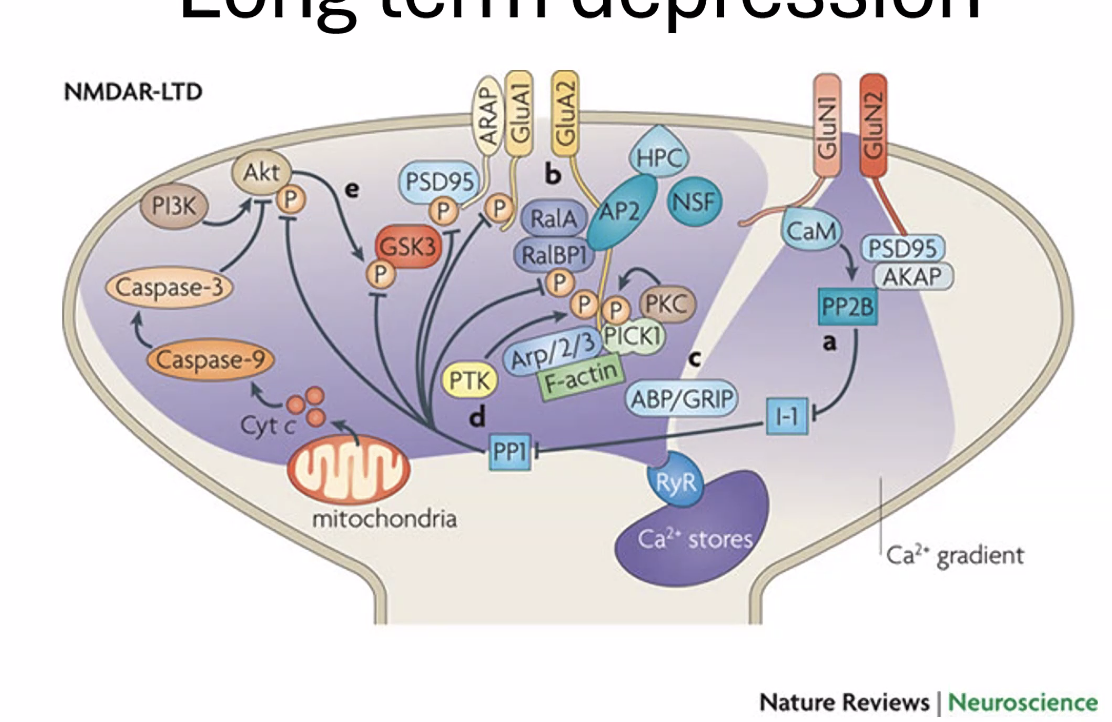
-
LTP(Long-Term Potentiation): כאשר NMDA מופעל בחוזק (כניסתסידןגבוהה) - CaMKII מזרחן AMPA, מגייס קולטנים לסינפסה, ומחזק אותה. הסינפסה תגיב חזק יותר בפעמים הבאות. -
LTD(Long-Term Depression): כאשר NMDA מופעל בחלש - רק מעטסידןנכנס. ריכוז נמוך זה מפעיל פוספטאז PP1 (Phosphatase), שמוריד את הזרחון מקולטני AMPA - גורם לסילוקם מהממברנה, ולהחלשת הסינפסה.
המפתח: אותו קולטן NMDA - אם הוא מופעל חזק (הרבה סידן) ← LTP; אם חלש (מעט סידן) ← LTD. כך הסינפסה יכולה להתחזק או להיחלש לפי צורך.
דור פסקללסיכום: הפלסטיות הסינפטית - ובפרט
LTP- היא המנגנון הנוירוביולוגי המרכזי של זיכרון ולמידה. אזורי מוח כמו ההיפוקמפוס (Hippocampus) עשירים במיוחד בקולטני NMDA, ולכן פלסטיים במיוחד. השינויים במוח אינם בעיקרם יצירת נוירונים חדשים (דבר נדיר), אלא חיזוק והחלשה של קשרים סינפטיים קיימים.