מבוא
בשיעור זה נעסוק במחזור החיים של וירוסים, החל מהתהליך שבו הווירוס מדביק תא ועד לשחרור וירוסים חדשים. נדון במושגים חשובים כגון תאים רגישים ומתירניים, דרכי העברה שונות של וירוסים, מדדי הדבקה ($R$), ושיטות זיהוי מעבדתיות מתקדמות.
שלבי מחזור החיים של וירוסים
1. Attachment (היצמדות)
הווירוס צריך להגיע לתא המארח ולהיצמד לרצפטור ספציפי על פני התא. תהליך ההיצמדות הוא ספציפי ביותר – כל וירוס בחר בתהליך האבולוציה רצפטור מסוים.
2. Penetration (חדירה)
לאחר ההיצמדות, הווירוס חודר לתוך התא. תהליך זה יכול להתבצע בדרכים שונות:
- Fusion – התמזגות עם ממברנת התא
- Endocytosis – בליעה לתוך וזיקולה תאית
3. Uncoating (חשיפת החומר הגנטי)
הקפסיד (Capsid) נפתח ומשחרר את החומר הגנטי ($\ce{DNA}$ או $\ce{RNA}$) לתוך התא. תהליך זה מתרחש לרוב בעקבות שינוי ב־pH או פעולת אנזימים תאיים.
4. Expression (ביטוי גנים)
החומר הגנטי הוויראלי מתורגם לחלבונים על ידי מנגנוני התא המארח.
5. Replication (הכפלת הגנום)
הגנום הוויראלי מוכפל באמצעות אנזימים וויראליים או תאיים. תהליך זה תלוי בסוג החומר הגנטי של הווירוס.
6. Assembly (הרכבה)
חלבונים וויראליים וגנומים חדשים מתאספים ליצירת וירוסים שלמים (virions).
7. Maturation (הבשלה)
הווירוסים עוברים שינויים סופיים הנחוצים לתפקודם.
8. Release (שחרור)
הווירוסים החדשים משתחררים מהתא באחת משתי דרכים:
- Lysis – פיצוץ התא
- Budding – שחרור הדרגתי דרך הממברנה
תאים רגישים ומתירניים
הגדרות
- תא רגיש (Susceptible) – תא שיש לו רצפטור שהווירוס יכול להיצמד אליו ולחדור דרכו.
- תא מתירני (Permissive) – תא שמאפשר את התרבות הווירוס בתוכו, כלומר יש בו את כל המנגנונים הנדרשים לשכפול הוויראלי.
דוגמאות
- HIV – מדביק תאי T (CD4+), אך אם מוכנס באופן מלאכותי לתאי עכבר, לא יתרבה שם (לא מתירני).
- Hepatitis B – מדביק רק תאי כבד (הפטוציטים), שהם גם רגישים וגם מתירניים לווירוס זה.
חשיבות: כדי שוירוס יתרבה בתא, התא חייב להיות גם רגיש וגם מתירני.
דרכי העברה של וירוסים
העברה אופקית (Horizontal Transmission)
מעבר של וירוס ממארח למארח באותה הדור:
- אוויר – טיפות רוק (Droplets), אירוסולים
- מגע ישיר – דם, רוק, יחסי מין
- וקטורים – יתושים, קרציות
העברה אנכית (Vertical Transmission)
מעבר מאם לעובר או לתינוק:
- דרך השליה (Transplacental)
- במהלך הלידה
- הנקה
זואונוזות (Zoonotic Diseases)
מחלות שמקורן בבעלי חיים:
- West Nile Virus – מציפורים דרך יתושים
- Rabies – מבעלי חיים נגועים
- Avian Flu (H5N1) – מעופות
- Ebola – מקופים
- SARS-CoV-2 – כנראה מעטלפים
וירמיה (Viremia)
הגדרה: מצב שבו וירוסים נמצאים בזרם הדם.
משמעות: וירמיה מאפשרת לווירוס להתפשט מאיבר ההדבקה הראשוני לאיברים נוספים בגוף, מה שעלול להוביל לסיבוכים מערכתיים.
Entry site is not necessarily the final target!
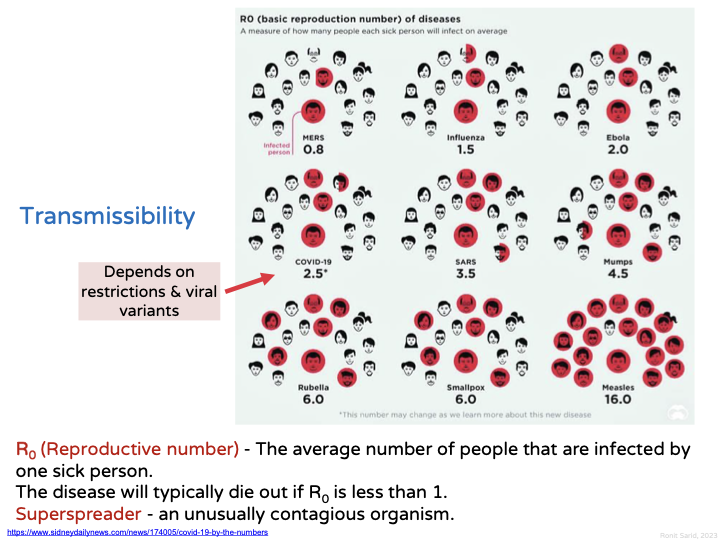
מדדי הדבקה – Reproductive Number ($R$)
הגדרה: מספר האנשים הממוצע שאדם חולה אחד מדביק.
דוגמאות
- $R < 1$ – המחלה אינה מתפשטת (דוגמה: MERS, $R \approx 0.7$)
- $R = 1$ – המחלה יציבה
- $R > 1$ – המחלה מתפשטת באוכלוסייה
- Ebola: $R \approx 2$
- SARS-CoV-2: $R \approx 2-3$ (משתנה לפי וריאנט)
- Measles (חצבת): $R \approx 16$ – אחת המחלות המדבקות ביותר!
חשיבות: ערך $R$ גבוה מחייב אחוזי חיסון גבוהים יותר להשגת חסינות עדר.
יציבות וירוסים מחוץ לגוף
גורמים המשפיעים על יציבות
- חום – טמפרטורות גבוהות מפרקות חלבונים וויראליים
- לחות – משפיעה על יציבות הקפסיד והממברנה
- קרינת UV – פוגעת בחומר הגנטי
- מעטפת – וירוסים ממוטפים (Enveloped) רגישים יותר לתנאי סביבה
דוגמאות
- HIV – בר-קיימא מספר שעות בלבד מחוץ לגוף
- Hepatitis B – יכול לשרוד שבועות על משטחים
- Norovirus – עמיד מאוד לתנאי סביבה
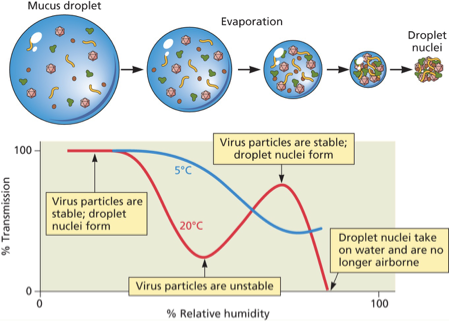
עקומת יציבות וטמפרטורה־לחות
- לחות נמוכה (<30%) – וירוסים יציבים בכל טמפרטורה
- לחות בינונית (50%) – יציבות גבוהה בטמפרטורות נמוכות (~5°C), יציבות נמוכה בחום (>20°C)
- לחות גבוהה (>80%) – וירוסים מתפרקים במהירות
משמעות קלינית: מרק חם בחורף יכול לעזור – החום והלחות מפחיתים את יציבות הווירוסים בדרכי הנשימה.
התפרצויות עונתיות (Seasonal Outbreaks)
גורמים
- תנאי אקלים – טמפרטורה ולחות מעדיפות
- התנהגות אנושית – שהייה במקומות סגורים בחורף
- מחזורי החיים של וקטורים – פעילות יתושים בקיץ
דוגמאות
- Influenza – פיק בחורף במדינות ממוזגות
- Poliovirus – דווקא בקיץ (תנאים חמים)
- West Nile Virus – קיץ (תלוי בפעילות יתושים)
שיטות זיהוי מעבדתיות
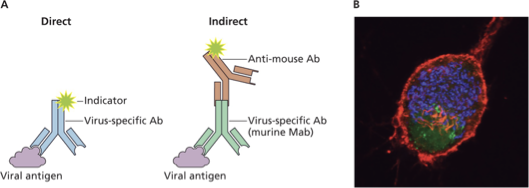
1. Immunofluorescence (אימונופלואורסצנציה)
Direct Method
- נוגדן ספציפי לאנטיגן וויראלי, מסומן בצבע פלואורסצנטי
- קושר ישירות לווירוס בדגימה
Indirect Method
- נוגדן ראשוני (לא מסומן) כנגד הווירוס
- נוגדן משני מסומן (למשל Anti-Mouse Antibody) כנגד הנוגדן הראשוני
- יתרון: חסכוני – נוגדן משני אחד לכל נוגדני העכבר
2. ELISA (Enzyme-Linked Immunosorbent Assay)
עיקרון
- נוגדן קשור למשטח
- הוספת דגימה (עם אנטיגן וויראלי)
- הוספת נוגדן שני מסומן באנזים
- הוספת סובסטרט שמייצר צבע
- מדידת עוצמת הצבע = כמות הווירוס
שימושים
- כימות וירוסים בדגימות
- בדיקות סרולוגיות (נוגדנים בדם)
3. Rapid Antigen Tests (בדיקות אנטיגן מהירות)
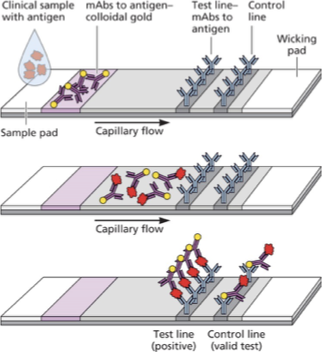
מבנה
- Control Line – נוגדן כנגד הנוגדן המסומן (תמיד חיובי אם הבדיקה תקינה)
- Test Line – נוגדן כנגד אנטיגן וויראלי ספציפי
תוצאות
- קו אחד (Control) – שלילי
- שני קווים (Control + Test) – חיובי
- אין קווים – הבדיקה פגומה
4. PCR (Polymerase Chain Reaction)
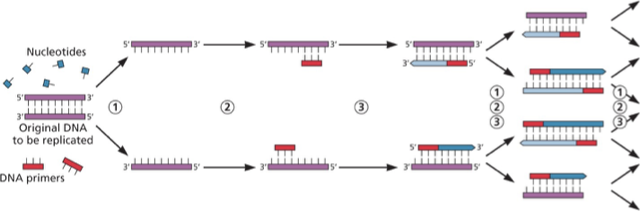
עיקרון בסיסי
PCR מאפשר הכפלה מעריכית של רצף $\ce{DNA}$ ספציפי.
שלבים
- Denaturation (95°C) – הפרדת גדילי $\ce{DNA}$
- Annealing (50-60°C) – היצמדות Primers
- Extension (72°C) – הארכת הגדיל על ידי DNA Polymerase
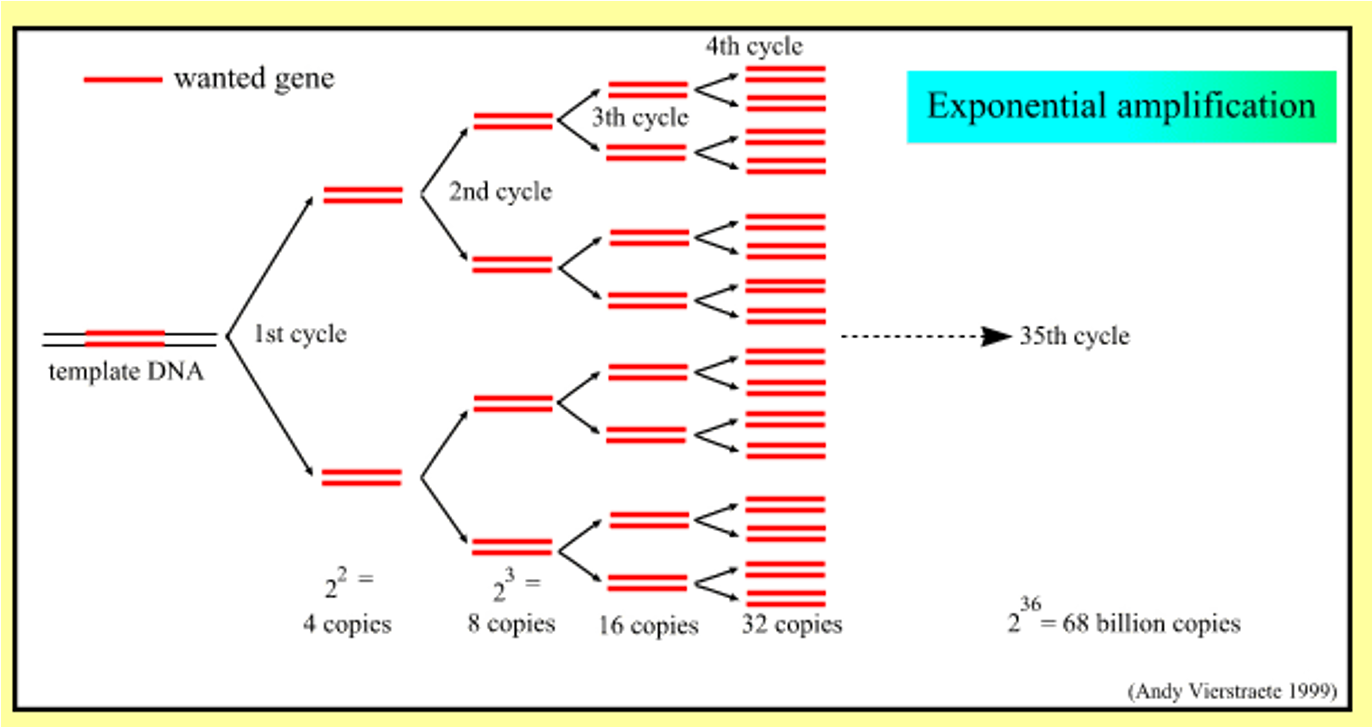
מחזור ההכפלה
- מחזור 1: 2 מולקולות
- מחזור 2: 4 מולקולות
- מחזור n: $2^n$ מולקולות
- 36 מחזורים: כ־68 מיליארד מולקולות
Taq Polymerase
- אנזים מחיידק Thermus aquaticus מעיינות רותחים
- עמיד לטמפרטורות גבוהות (עד 95°C)
- מאפשר ביצוע מחזורים חוזרים ללא הוספת אנזים חדש
5. RT-PCR (Reverse Transcription PCR)
שימוש
זיהוי וירוסי $\ce{RNA}$ (כמו SARS-CoV-2, Influenza)
שלבים
- Reverse Transcription – המרת $\ce{RNA}$ ל־$\ce{cDNA}$ באמצעות Reverse Transcriptase
- PCR רגיל על ה־$\ce{cDNA}$
דוגמה: אבחון COVID-19
- שני זוגות Primers לשני אזורים שונים בגנום
- שני פסים – חיובי
- פס אחד – אפשרי מוטציה באחד האזורים
- אפס פסים – שלילי
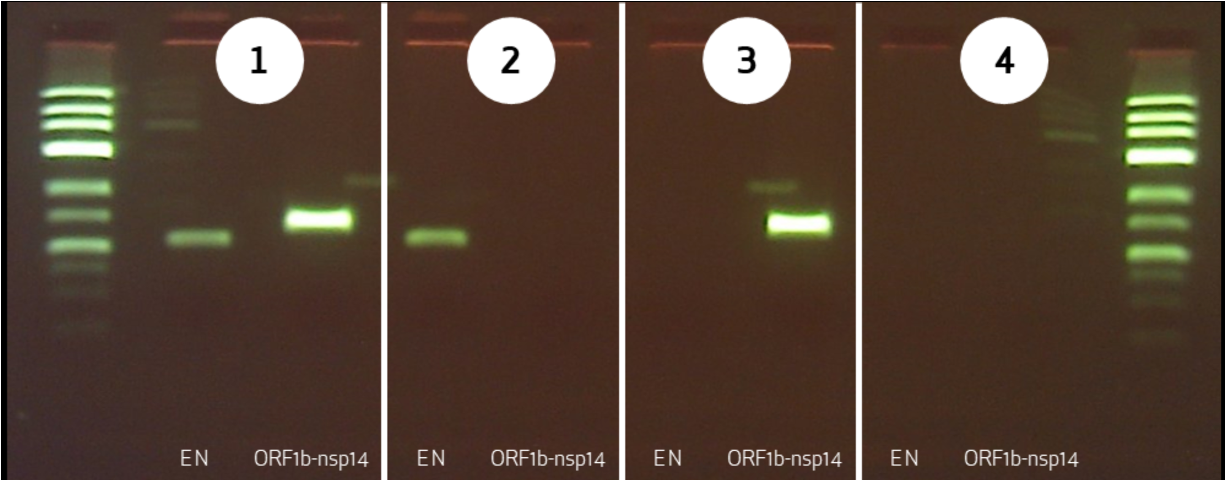
חשיבות: Primers הם רצפים ספציפיים לווירוס מסוים. PCR לגילוי קורונה לא יזהה וירוס שפעת!
שיטות תרבית וירוסים
1. תרבית תאים (Cell Culture)
- תאים בתרבית מדוגמה או שרה אחת של תאים
- מאפשרת מחקר ושכפול וירוסים במעבדה
2. ביצים מעוברות (Embryonated Eggs)
- הזרקת וירוס לאזורים שונים בביצה
- שימוש נפוץ בייצור חיסוני שפעת
- בעיה נוכחית (2023): מחסור בביצים בארה”ב בשל Avian Flu – הובילה לעלייה דרמטית במחיר (מדולר אחד, לשבע ולתריסר)
3. מודלים של בעלי חיים
- עכברים, אוגרים, פרימטים
- שימוש במחקר פתוגנזה וחיסונים
- דוגמה: עכברים מהונדסים עם רצפטור ACE2 אנושי למחקר COVID-19
מדידת כמות וירוסים – Plaque Assay
עיקרון
- שכבה של תאים (Monolayer)
- כיסוי בשכבת אגר חצי־מוצקה
- הדבקה בווירוס
- וירוס הורג תאים מקומיים ויוצר “חור” (Plaque)
חישוב
\[\text{Viral titer (PFU/ml)} = \frac{\text{Number of plaques} \times \text{Dilution factor}}{\text{Volume plated (ml)}}\]דוגמה
- דילול $10^{-7}$
- 10 Plaques
- נפח $0.1 \, \mathrm{ml}$
יתרון
מודד רק וירוסים אינפקטיביים – שונה מ־PCR (מודד גם $\ce{DNA}$ של וירוסים מתים) ו־ELISA (מודד גם קפסידים ריקים).
ייצור חיסונים מבוסס ביצים
תהליך
- בידוד זן שפעת מקומי
- שילוב (Reassortment) עם זן מעבדה שגדל היטב בביצים
- גנום שפעת מורכב מ־8 סגמנטים של $\ce{RNA}$
- הדבקת תא בשני זנים גורמת לערבוב סגמנטים
- הדבקת ביצים רבות בזן ההיברידי
- איסוף וירוסים
- Inactivation (השבתה)
- ניקוי וביקורת איכות
- אריזה להזרקה

Reassortment בשפעת
- 8 סגמנטים של $\ce{RNA}$ בגנום
- מאפשר שילוב מהיר של חומר גנטי בין זנים
- סיבה מרכזית לשונות הגבוהה והצורך בחיסון שנתי
תופעות מיוחדות בדינמיקה של וירוסים
Eclipse Phase
- תקופה שבה אין וירוסים זמינים מחוץ לתא
- הווירוס נמצא בתהליך שכפול בתוך התא
- משך: שעות עד ימים (תלוי בווירוס)
Burst vs. Budding Release
- Burst (Multiple Cycle): נפיחת תא משחררת וירוסים חדשים פתאום ← פיק שני אם לא כל התאים נדבקו בפעם הראשונה
- One-Step Growth: כל התאים נדבקו מלכתחילה ← פיק אחד
נקודות מרכזיות לזכור
- מחזור חיים וויראלי מורכב מ־8 שלבים: Attachment → Penetration → Uncoating → Expression → Replication → Assembly → Maturation → Release
- תא רגיש ≠ תא מתירני – נדרשים שניהם להדבקה מוצלחת
- העברה אופקית (בין אנשים) שונה מהעברה אנכית (אם-עובר)
- $R$ (Reproductive Number) – מדד קריטי להבנת התפשטות מגיפות
- PCR – הכפלה ספציפית של $\ce{DNA}$; עבור וירוסי $\ce{RNA}$ נדרשת RT-PCR
- Plaque Assay – השיטה היחידה למדידת וירוסים אינפקטיביים
- לחות וטמפרטורה משפיעות באופן דרמטי על יציבות וירוסים
- Reassortment בשפעת – מנגנון מרכזי לשונות גנטית מהירה