תוכן העניינים:
- פתיחה - חזרה על השיעורים הקודמים
- אי יציבות גנומית - למה זה חשוב?
- הגורמים לנזקי DNA
- נזקי DNA ברמת הבסיס
- Base Excision Repair - BER
- דיאמינציה יזומה במערכת החיסון ובתגובה אנטי-ויראלית
- Guanine oxidation ו־8-oxoG
- מיפוי AP sites ו־8-oxoG בגנום
פתיחה - חזרה על השיעורים הקודמים
השיעור נפתח בחזרה קצרה על NGS וספריות DNA דרך שאלות Kahoot. הנקודות שעלו בחזרה:
- היתרונות של NGS לעומת Sanger כוללים ריצוף תוך כדי סינתזה, ריצוף מקבילי ומהירות. שימוש ב־reads ארוכים יותר אינו יתרון טיפוסי של NGS לעומת Sanger.
- סלקציה שלילית של rRNA נעשית בעזרת RNase H, שמזהה RNA בתוך היבריד DNA-RNA.
- תיקון קצוות של מקטעי DNA לפני חיבור אדפטורים קשור להכנת המקטע לחיבור האדפטור.
- אם מתקבלים מקטעים קטנים מדי בספרייה, הבעיה קשורה ל־Size selection, ובפרט לשימוש לא מתאים ב־carboxyl beads.
- Genome indexing נועד להפוך את החיפוש בגנום ליעיל יותר.
- האתגר הייחודי במיפוי RNA-seq הוא gapped reads, בגלל שחבור: ה־read מגיע מ־cDNA, אבל רפרנס DNA גנומי כולל אינטרונים.
- Protein A משמש לצימוד ביד מגנטי לנוגדן, דרך הקישור לחלק הקבוע של הנוגדן.
- הרזולוציה של ChIP-seq תלויה בגודל המקטעים בספרייה: ככל שהמקטע קטן יותר, קל יותר למקם את אתר הקישור המדויק.
מכאן עברנו לנושא המרכזי של החלק הזה בקורס: נזקי DNA ואי יציבות גנומית.
אי יציבות גנומית - למה זה חשוב?
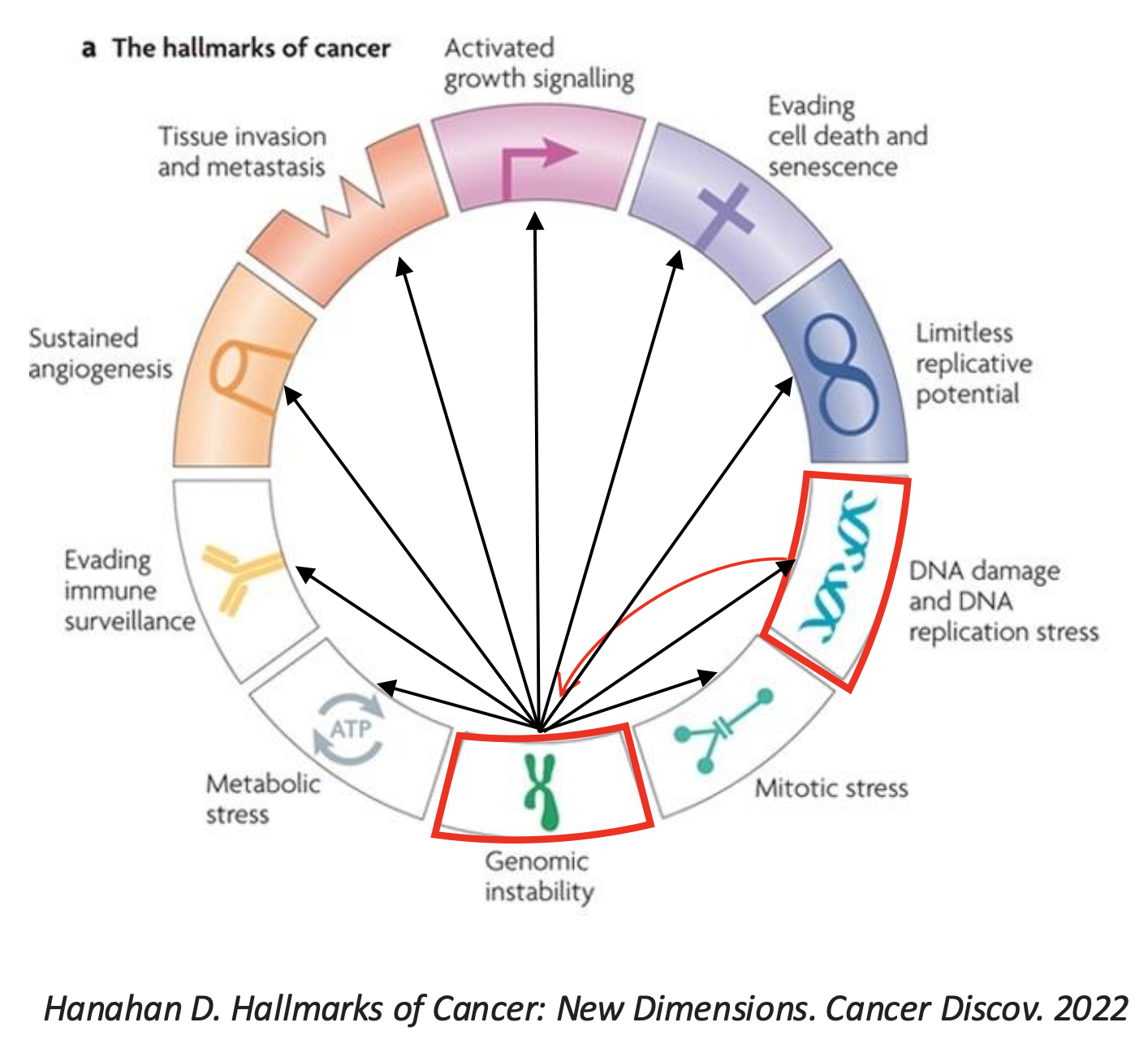
אי יציבות גנומית קשורה ישירות לפתולוגיות שונות, ובעיקר לסרטן. בתמונה מתוך המאמר The Hallmarks of Cancer, נזקי DNA ואי יציבות גנומית מופיעים כחלק ממאפייני התא הסרטני.
המרצה הדגיש הבחנה חשובה:
- DNA damage - נזק שמתרחש בזמן אמת במולקולת DNA, כתוצאה מגורם מסוים.
- Genome instability - תוצר אפשרי של נזקי DNA: שינויים כרומוזומליים ארוכי טווח שיכולים לעבור לתאי הבת.
כלומר, נזק ל־DNA לא בהכרח הופך מיד לשינוי קבוע. ברוב המקרים הנזק מתוקן. הוא הופך לבעיה יציבה יותר כאשר הוא שורד את שכפול ה־DNA. אחרי השכפול, השינוי כבר יכול לעבור לתאי הבת.
אי יציבות גנומית כמאפיין-על בסרטן
אי יציבות גנומית היא לא רק עוד מאפיין של סרטן. היא יכולה להיחשב מאפיין-על, משום שהיא מאפשרת לתא לרכוש תכונות סרטניות נוספות.
כדי שתא ירכוש תכונה חדשה, כמו חלוקה מוגברת, התחמקות מאפופטוזיס או התחמקות ממערכת החיסון, צריך שינוי גנטי כלשהו: מוטציה, מחיקה, טרנסלוקציה או שינוי כרומוזומלי אחר.
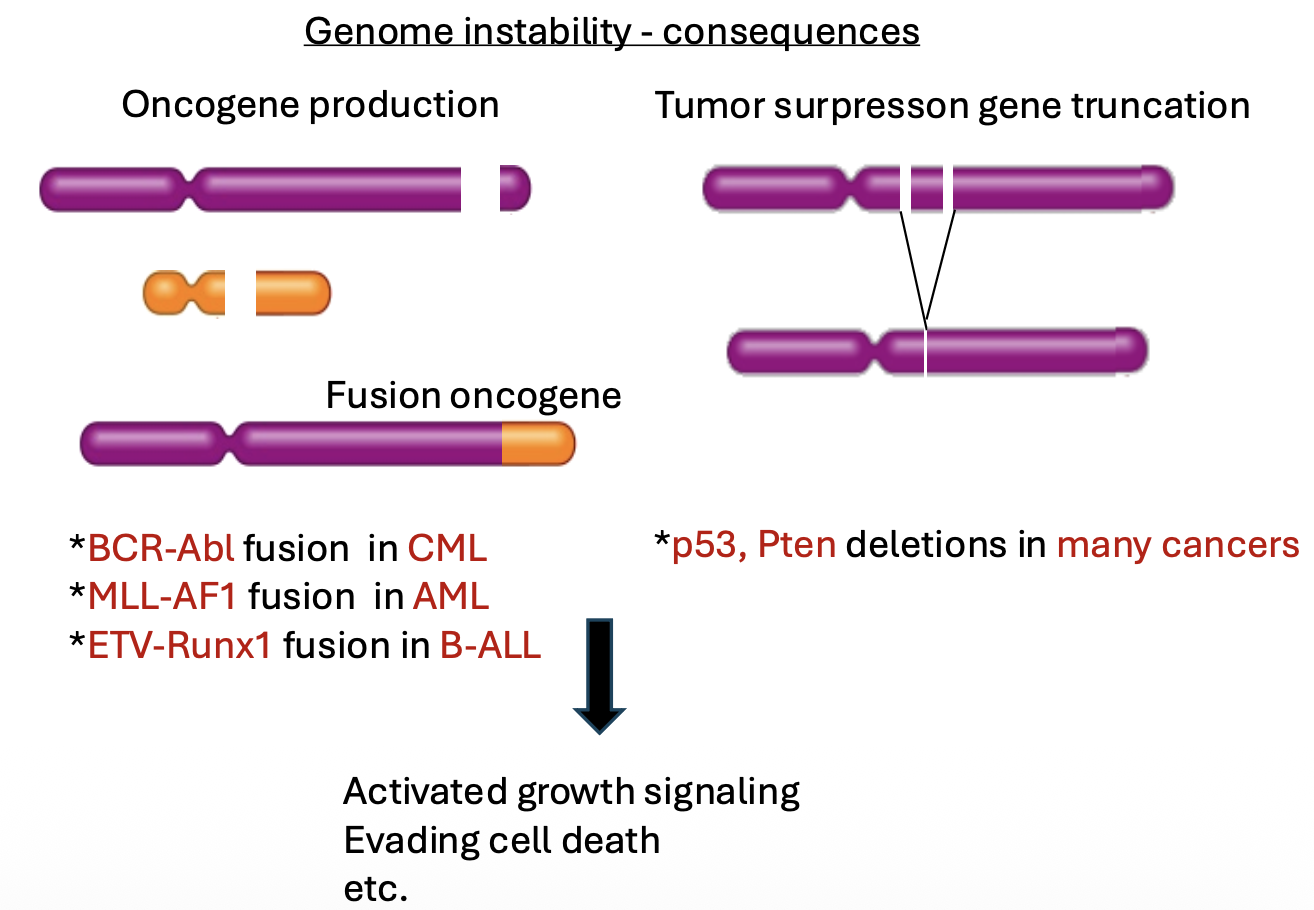
דוגמאות לתוצרים של אי יציבות גנומית:
- יצירה או הפעלה של אונקוגן - גן שהתוצר שלו מקדם תכונות סרטניות, למשל חלוקה מוגברת או מניעת אפופטוזיס.
- פגיעה ב־tumor suppressor gene - גן שתפקידו למנוע התפתחות סרטנית. כאשר הוא נמחק או עובר מוטציה, התא מאבד מנגנון הגנה.
דוגמה מרכזית היא p53: זהו tumor suppressor חשוב, שמזהה נזקי DNA ויכול להוביל את התא לאפופטוזיס. לכן בתאים סרטניים יש יתרון באיבוד או פגיעה ב־p53: התא מאבד את “השומר”, ויכול לצבור עוד ועוד שינויים.
הזדקנות
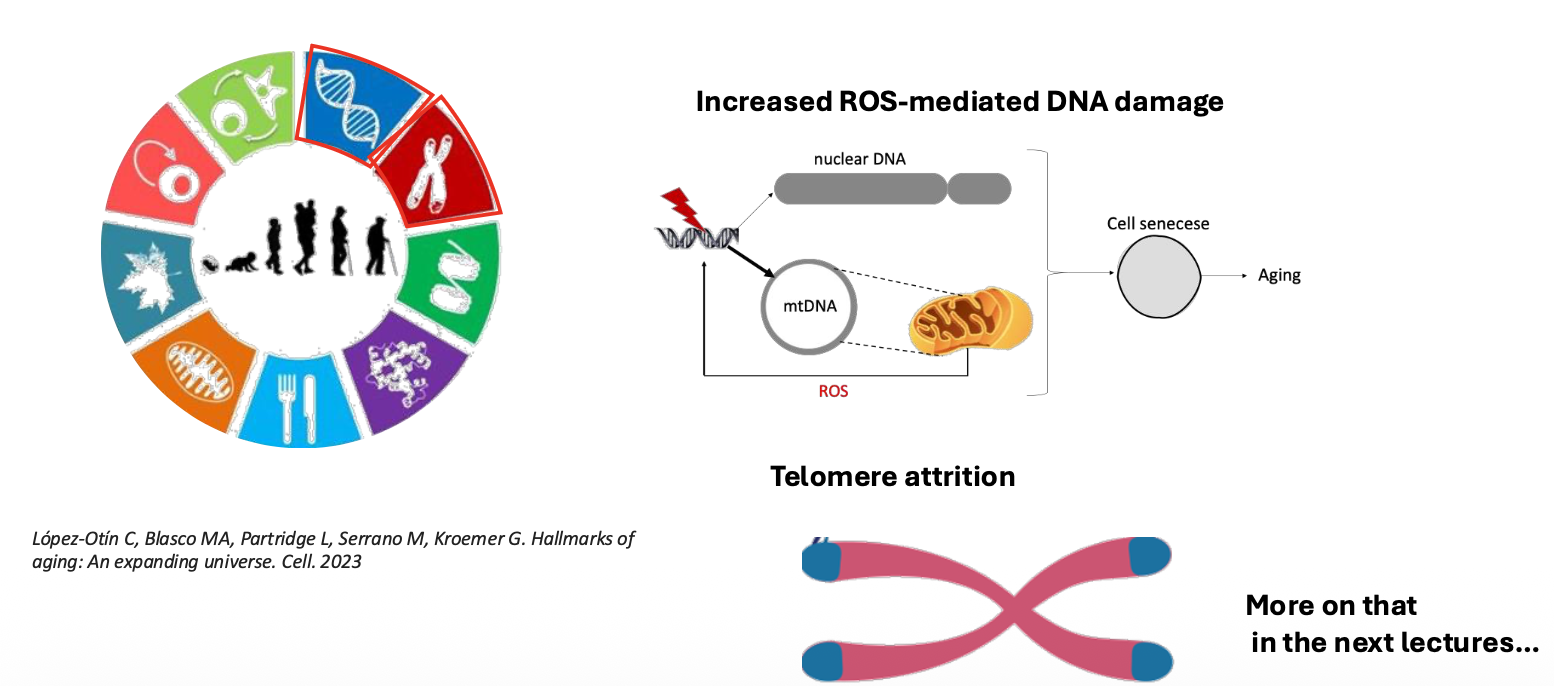
אי יציבות גנומית קשורה גם להזדקנות. אחד המקורות לנזקי DNA במהלך ההזדקנות הוא המיטוכונדריה.
המיטוכונדריה מייצרת ATP, אבל כתוצר לוואי נוצרים גם Reactive Oxygen Species - ROS. ככל שהמיטוכונדריה מזדקנת ונעשית פחות יעילה, יש פחות יצירת ATP ויותר יצירת ROS.
ROS יכולים להגיב עם ה־DNA וליצור נזקים. כך נוצר מעגל שבו הזדקנות מיטוכונדריאלית מגבירה נזקי DNA, ונזקי DNA תורמים להזדקנות תאית.
נזקי DNA קשורים גם לשחיקת טלומרים - תהליך שמתרחש גם באופן טבעי עם הגיל, אבל נזקי DNA יכולים להגביר את הקצב שלו.
מחלות גנטיות וטיפולים אנטי-סרטניים
הוזכרו גם מחלות שבהן הבעיה היא פגם במנגנוני תיקון DNA, למשל Xeroderma Pigmentosum - XP, וכן דוגמאות כמו BRCA בהקשרים של תיקון נזקי DNA.
מהצד השני, הרבה טיפולים אנטי-סרטניים משתמשים דווקא בהשריה מכוונת של נזקי DNA. הרעיון הוא לגרום מספיק נזק כך שהתא הסרטני ימות. לעיתים הטיפול משלב השריה של נזקי DNA יחד עם פגיעה ביכולת של התא לתקן את הנזק.
הגורמים לנזקי DNA
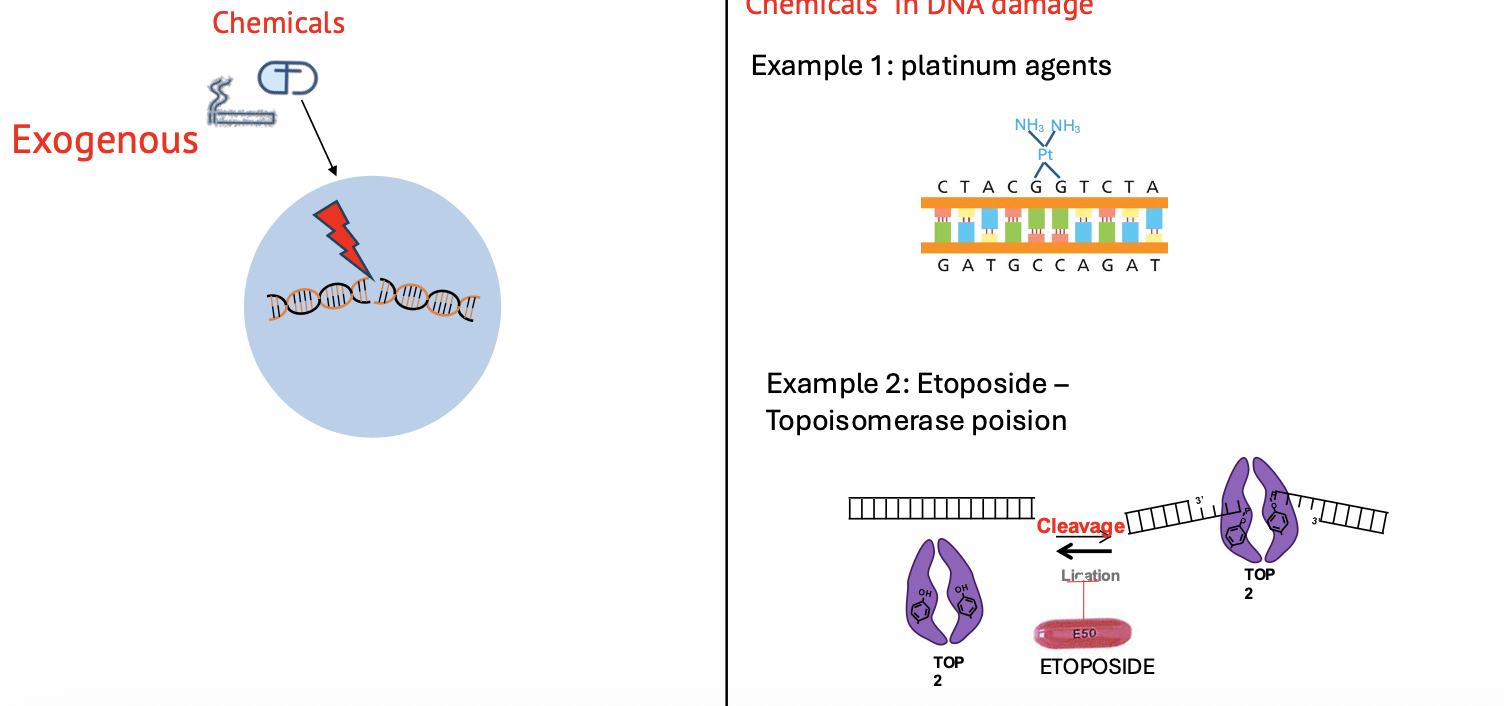
נזקי DNA יכולים להיגרם מגורמים חיצוניים או מגורמים פנימיים.
גורמים חיצוניים
גורמים חיצוניים כוללים כימיקלים וקרינה.
Platinum agents הם דוגמה לכימיקלים שמגיבים עם DNA ויוצרים נזקים גדולים יותר מבחינה מבנית.
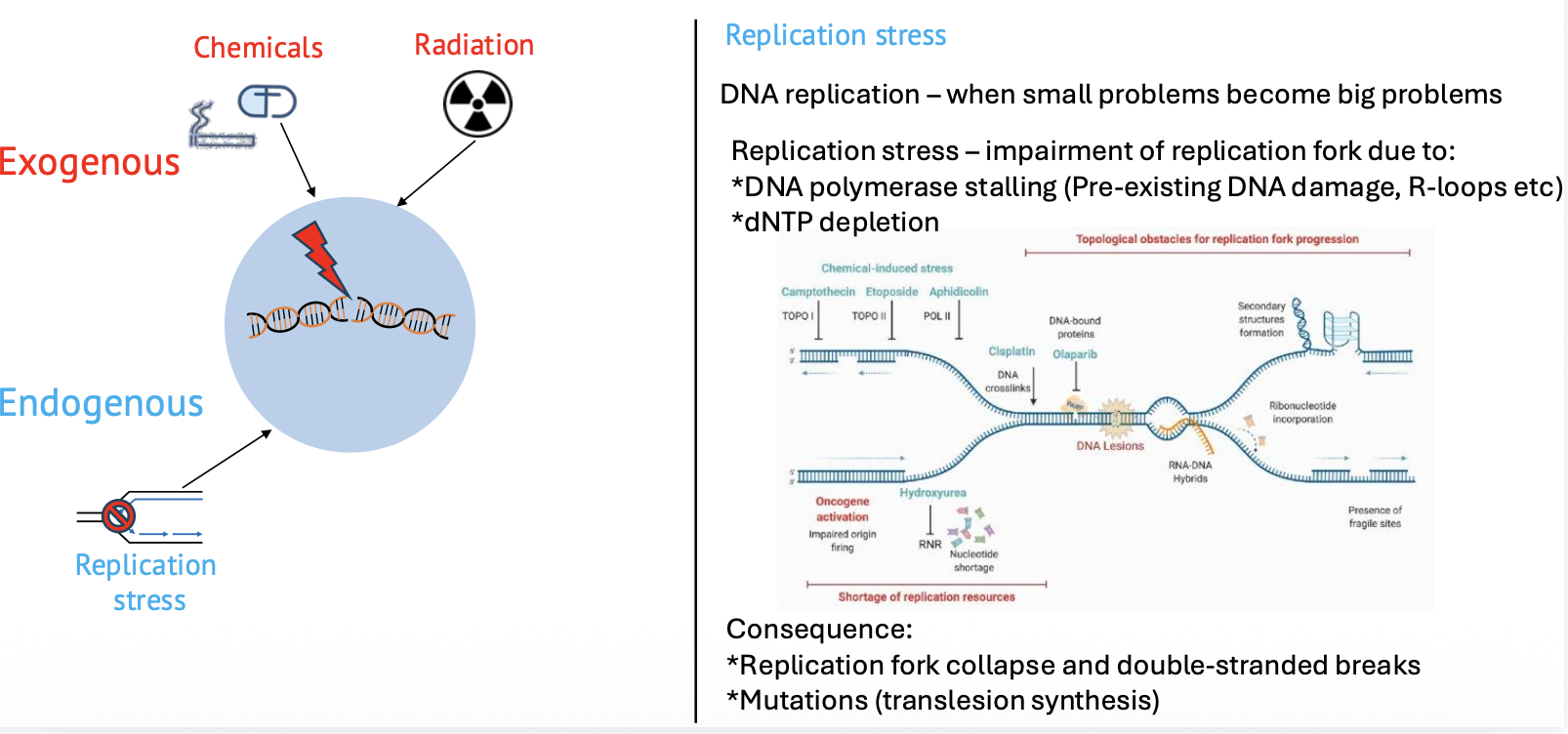
קרינה היא גורם חיצוני נוסף:
- UV radiation יכולה ליצור דימרים של תימין.
- Ionizing radiation יכולה לגרום לנזקים שונים, כולל שברי DNA.
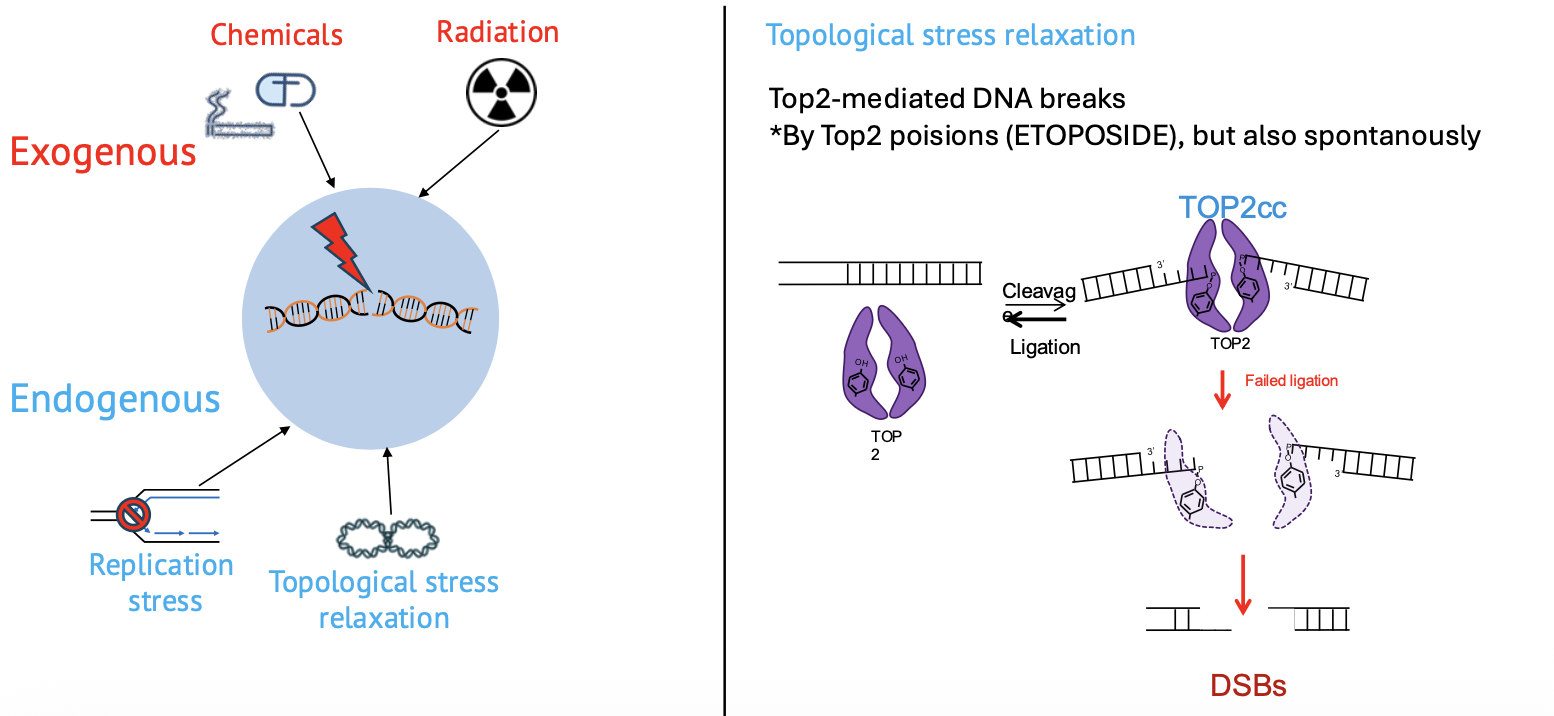
הוזכר גם Toposide, כתרופה אנטי-סרטנית שפועלת דרך פגיעה בפעילות של topoisomerase. העיקרון הוא שעיכוב או הרעלה של topoisomerase יכולים להוביל ליצירת נזקי DNA.
גורמים פנימיים
גם בלי גורמים חיצוניים, DNA יכול להינזק. התא עצמו מייצר מצבים שבהם ה־DNA מאוים.
שכפול DNA
אחת מנקודות התורפה המרכזיות היא שכפול DNA. מזלג השכפול צריך “כביש נקי” כדי להתקדם. אם יש נזק, מבנה שניוני או מכשול אחר, מזלג השכפול יכול להיתקע.
שכפול DNA הוא המקום שבו בעיות קטנות יכולות להפוך לבעיות גדולות. כאשר מזלג השכפול קורס, נוקלאזות יכולות לחתוך את ה־DNA כדי לשחרר את המבנה התקוע, וכך נוצרים שברי DNA.
Topoisomerase
גם פעילות תקינה של topoisomerase מאתגרת את היציבות הגנומית. Topoisomerase II משחרר מתח טופולוגי על ידי יצירת שבר זמני והפיך ב־DNA, מעבר של מקטע DNA וחיבור מחדש.
בדרך כלל זה תהליך מבוקר ומהיר, אבל מכיוון שהוא מתרחש בתדירות גבוהה, יש סיכוי סטטיסטי שמשהו ישתבש והחיבור מחדש לא יקרה כראוי.
יצירת הרפרטואר החיסוני
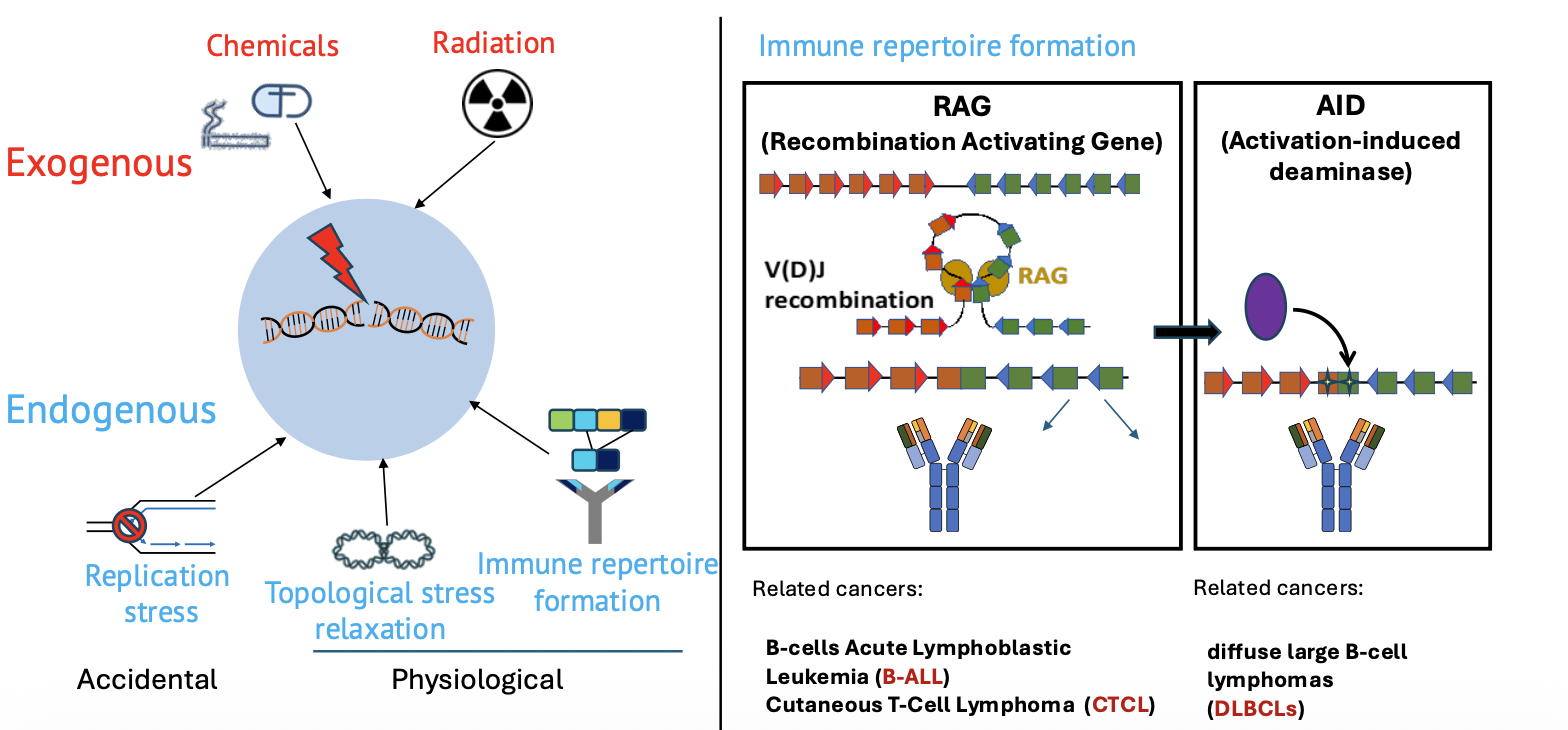
דוגמה נוספת היא יצירת נוגדנים ורצפטורים לאנטיגן. כדי ליצור מגוון עצום של נוגדנים ושל T-cell receptors, תאי מערכת החיסון מבצעים עריכה של DNA.
ברמת ה־DNA זה דומה ל־cut and paste: חותכים את ה־DNA ומחברים אותו מחדש כדי ליצור רצפים שונים. זה הכרחי ליצירת מערכת חיסון אדפטיבית מגוונת, אבל זה גם מסוכן, כי מדובר ביצירת שברי DNA באופן יזום.
המנגנון אמור להיות מבוקר מאוד, אבל הוא לא מושלם. לכן יש לו גם קשר להתפתחות סרטני דם, למשל לימפומות.
Translesion synthesis - סבילות לנזק במקום תיקון
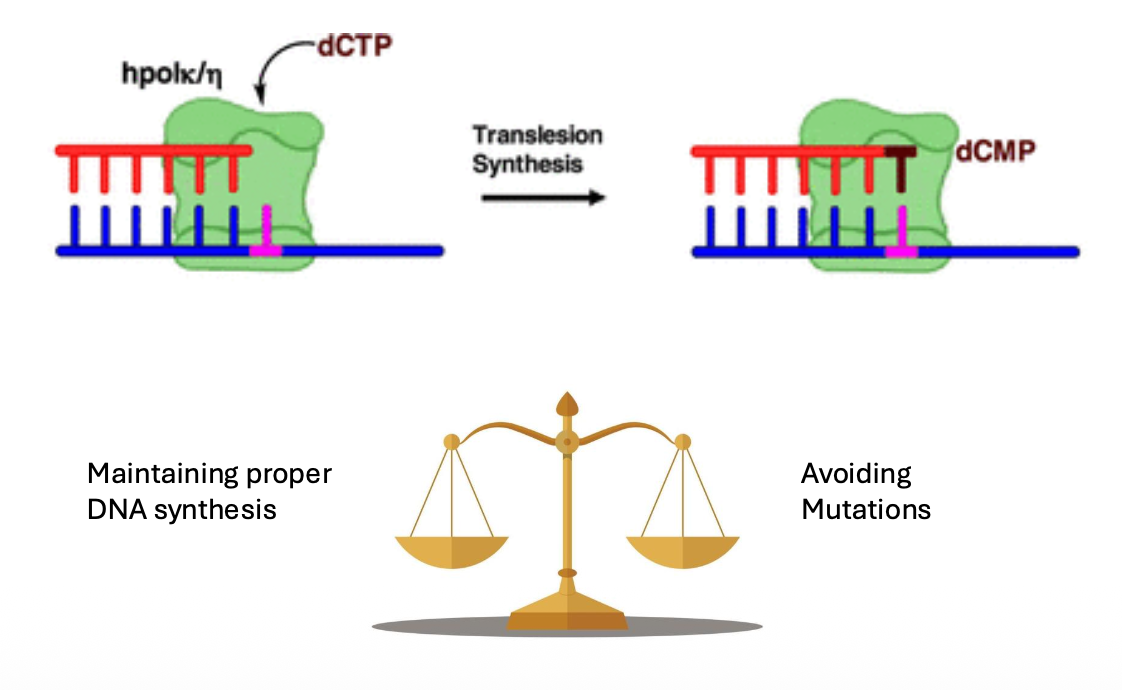
לא תמיד התא מתקן את הנזק לפני שהוא ממשיך; לפעמים הוא “סובל” את הנזק כדי לא לעצור את השכפול. זה נקרא Translesion synthesis.
במנגנון הזה התא מסנתז DNA מעל נזק קיים. היתרון הוא שהשכפול יכול להמשיך והתא יכול לשרוד. החיסרון הוא שזה מנגנון פחות מדויק, ולכן הוא יכול להכניס מוטציות.
זה אחד ההסברים לקשר בין נזקי DNA לבין מוטציות שעוברות לתאי הבת: אם התא משכפל מעל נזק במקום לתקן אותו, הוא עלול לקבע מוטציה.
שינויים כרומוזומליים
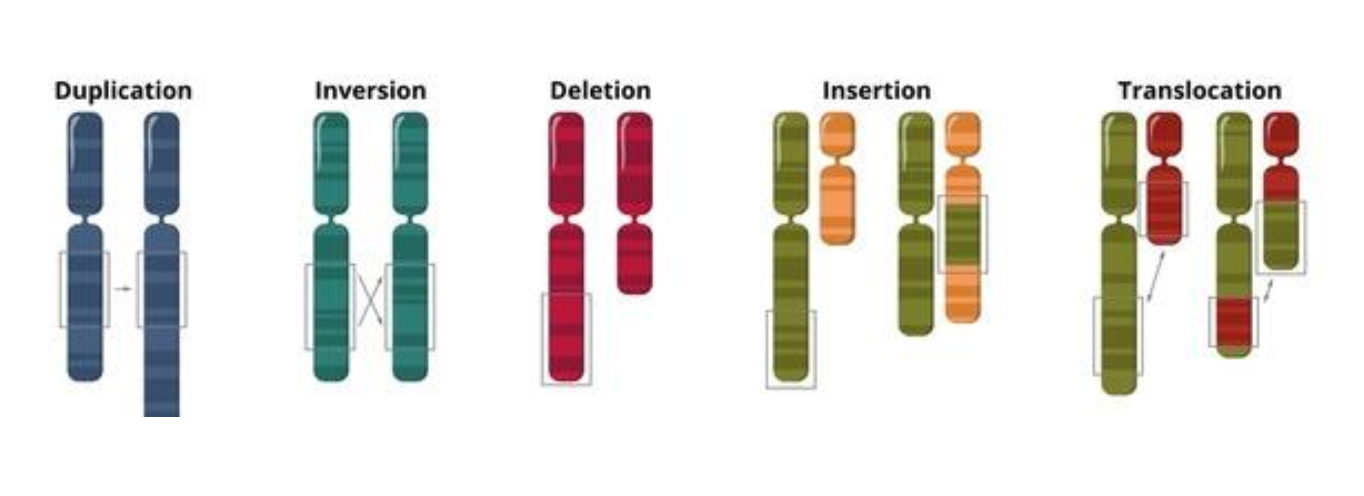
תוצר אפשרי של נזקי DNA ואי יציבות גנומית הוא chromosomal aberrations - שינויים כרומוזומליים.
לדוגמה:
- מחיקות
- דופליקציות
- אינסרציות
- טרנסלוקציות
הוזכרו גם transposable elements ו־transposase, כמרכיבים שמקורם האבולוציוני קשור ל־DNA ויראלי ושיכולים לגרום לבלגן גנומי אם אינם מבוקרים.
זיהוי נזקי DNA במעבדה
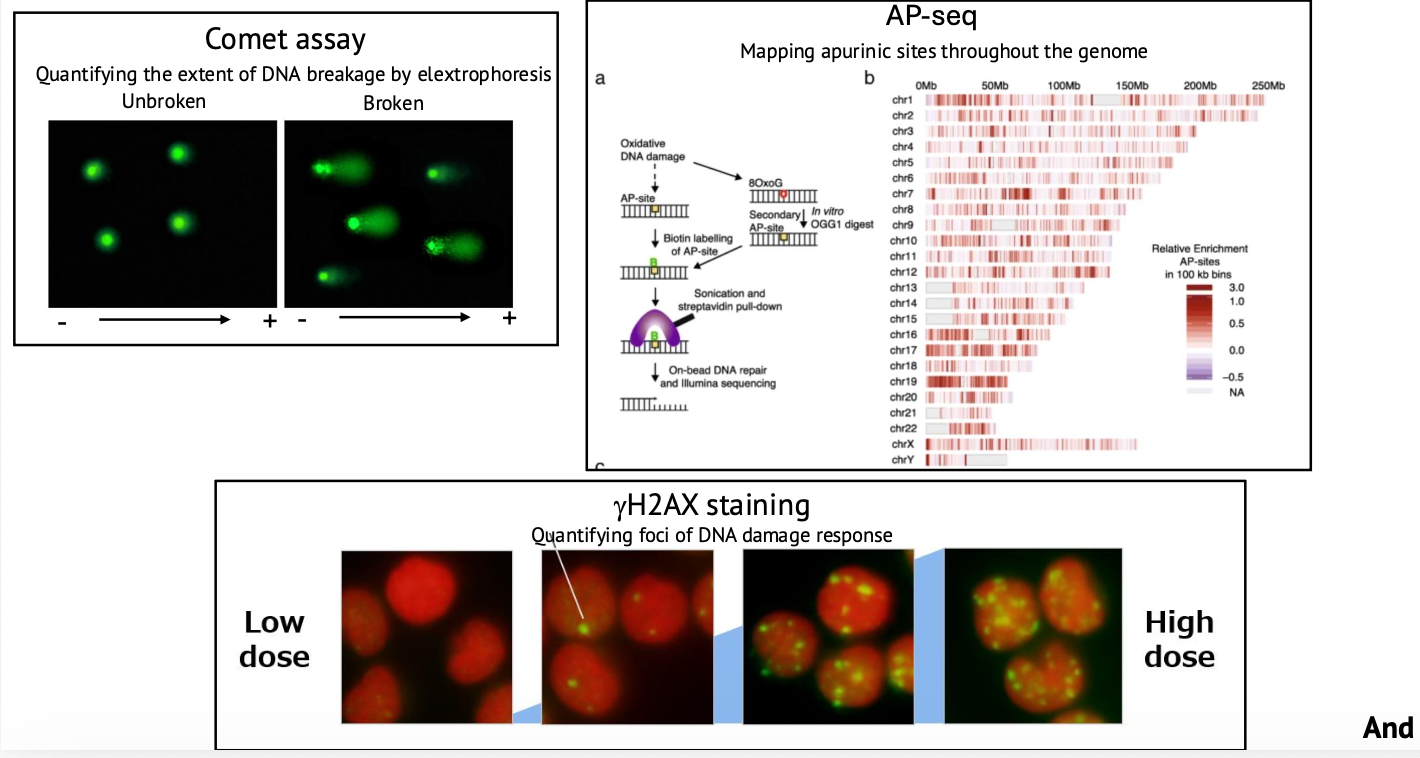
אחת הדרכים לזהות שברי DNA היא Comet assay.
בבדיקה זו צובעים DNA בצביעה פלואורסצנטית ומריצים באלקטרופורזה. אם ה־DNA שלם, הוא נשאר יותר כגוש עגול. אם יש שברים, המקטעים הקטנים נודדים ויוצרים “זנב” שנראה כמו כוכב שביט.
ככל שהזנב גדול או אינטנסיבי יותר, יש יותר נזקי DNA.
הוזכרו גם דרכים נוספות לזיהוי נזקים, כמו ספריות DNA שמזהות שברים או נזקים אחרים, צביעה של γH2AX לזיהוי אזורים הקשורים לתיקון שברי DNA, ומיפוי של אתרים חסרי בסיס.
נזקי DNA ברמת הבסיס
בחלק העיקרי של השיעור התמקדנו ב־Base-level DNA damage או Non-bulky DNA lesions.
אלו נזקים שבהם השלד הסוכרי-פוספטי נשאר שלם, אבל הבסיס עצמו נפגע, משתנה או נעלם. זה שונה מ־bulky lesions, שבהם נזק גדול יותר משנה את המבנה המרחבי של ה־DNA.
שלושת הנזקים המרכזיים:
- Depurination - איבוד בסיס פוריני
- Deamination - הסרה של קבוצת אמין
- Oxidation - חמצון של בסיס, בעיקר גואנין
| סוג הנזק | בסיסים שנפגעים בעיקר | מה קורה? | מנגנון תיקון |
|---|---|---|---|
| Depurination | פורינים: A ו־G | איבוד הבסיס ויצירת אתר חסר בסיס | BER |
| Deamination | בעיקר C | הסרת קבוצת אמין, למשל C → U | BER |
| Oxidation | בעיקר G | יצירת 8-oxoG | BER |
Depurination
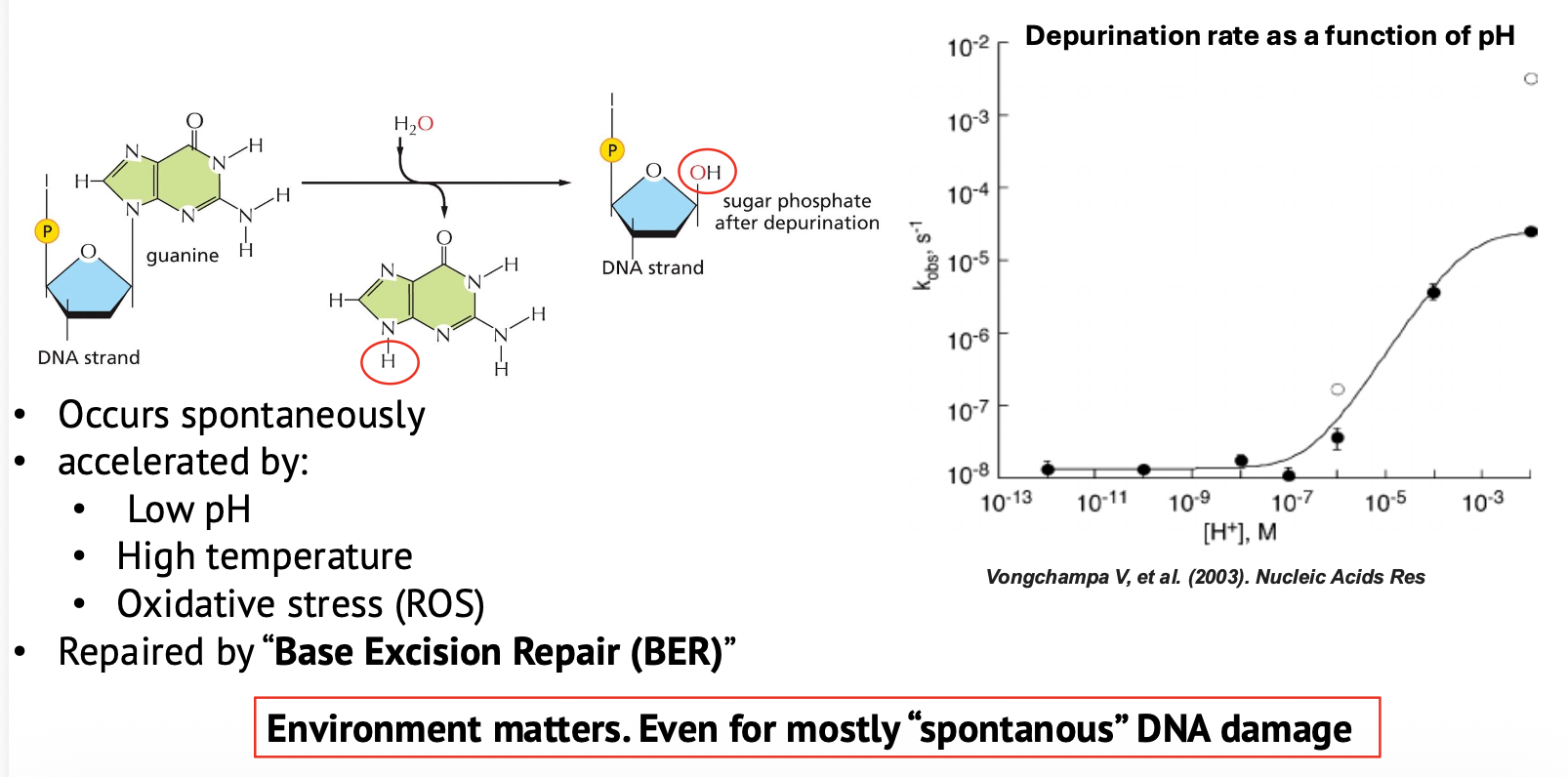
Depurination היא איבוד של בסיס פוריני, כלומר A או G. האיבוד מתרחש על ידי הידרוליזה של הקשר ה־N-glycosidic שמחבר בין הבסיס לבין הסוכר.
לאחר איבוד הבסיס נשאר שלד סוכרי-פוספטי, אבל בלי בסיס. אתר כזה נקרא AP site, כלומר אתר א-פוריני או באופן כללי אתר חסר בסיס.
דפורינציה שכיחה הרבה יותר מדה־פירימידינציה, כי הקשר בין פורין לסוכר חלש יותר מהקשר המקביל בפירימידינים.
- Depurination: בערך 18,000 מקרים ביום, בערך 5 בשנייה.
- Depyrimidination: בערך 600 מקרים ביום.
דפורינציה יכולה לקרות באופן ספונטני, כי יש מים ויש תנאים שמאפשרים הידרוליזה. היא מוגברת בתנאים של pH נמוך וטמפרטורה גבוהה. היא יכולה להיות מושפעת גם מ־oxidative stress.
Deamination
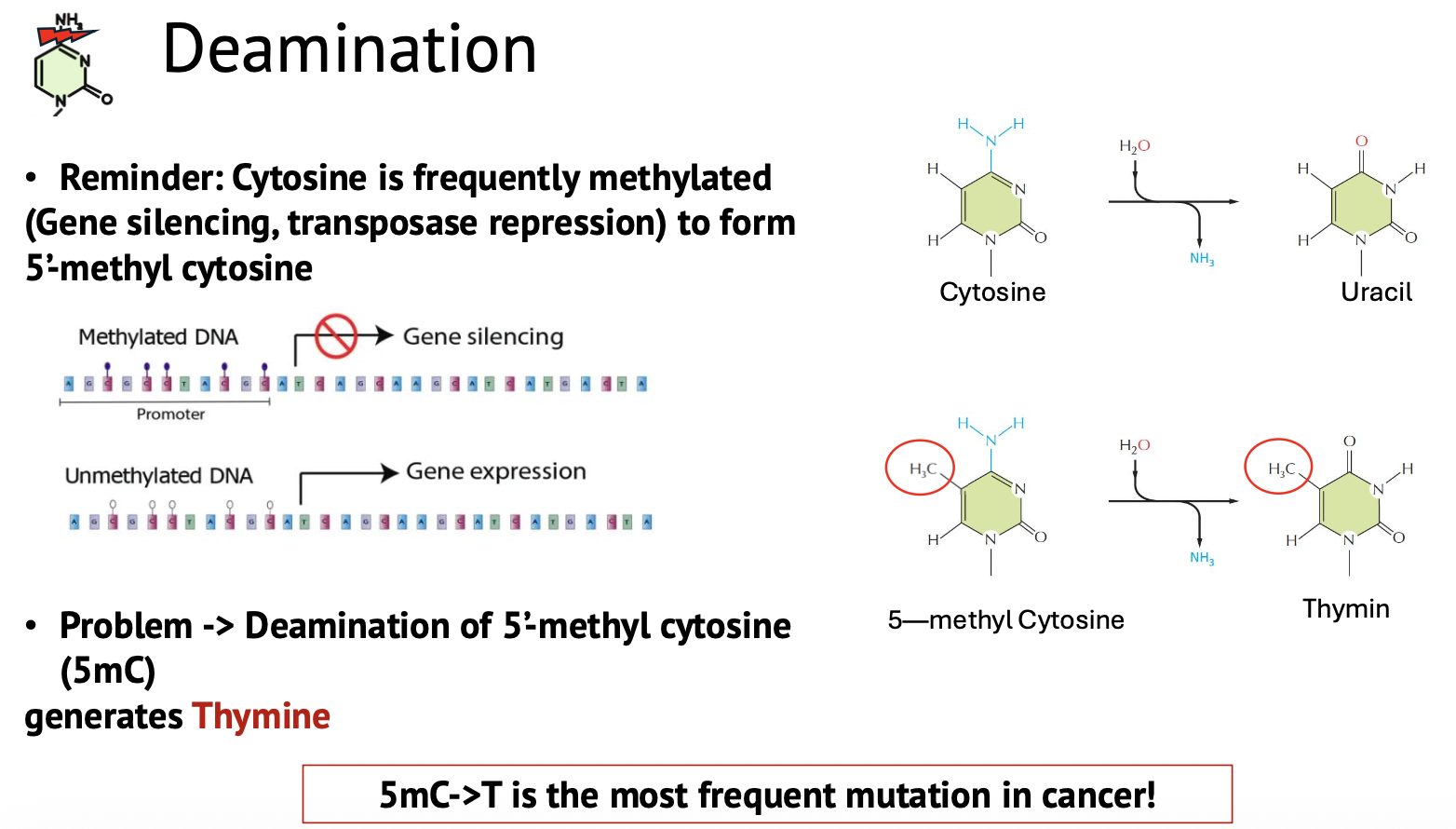
Deamination היא הסרה של קבוצת אמין מהבסיס.
הדוגמה המרכזית היא:
\[\ce{C -> U}\]כלומר, ציטוזין הופך לאורציל. זה פחות שכיח מדפורינציה (סדר גודל של בערך 100 מקרים ביום).
כאן מופיעה אחת הסיבות לכך שב־DNA יש תימין (T) ולא אורציל (U): אם ציטוזין עובר דיאמינציה והופך לאורציל, התא יכול לזהות שאורציל לא אמור להיות ב־DNA ולתקן אותו.
אבל יש מקרה בעייתי יותר: ציטוזין יכול לעבור מתילציה ל־5-methylcytosine. אם 5-methylcytosine עובר דיאמינציה, התוצר הוא תימין ולא אורציל.
זו בעיה, כי תימין הוא בסיס תקין ב־DNA. לכן קשה יותר לתא לזהות שמדובר בטעות. המוטציה של 5-methylcytosine ל־T היא אחת המוטציות הנפוצות בסרטן.
דיאמינציה יכולה לקרות באופן ספונטני, והיא מוגברת גם בתנאים כמו pH נמוך וטמפרטורה גבוהה. בנוסף לכך, יש אנזימים שעושים דיאמינציה באופן פעיל.
Base Excision Repair - BER
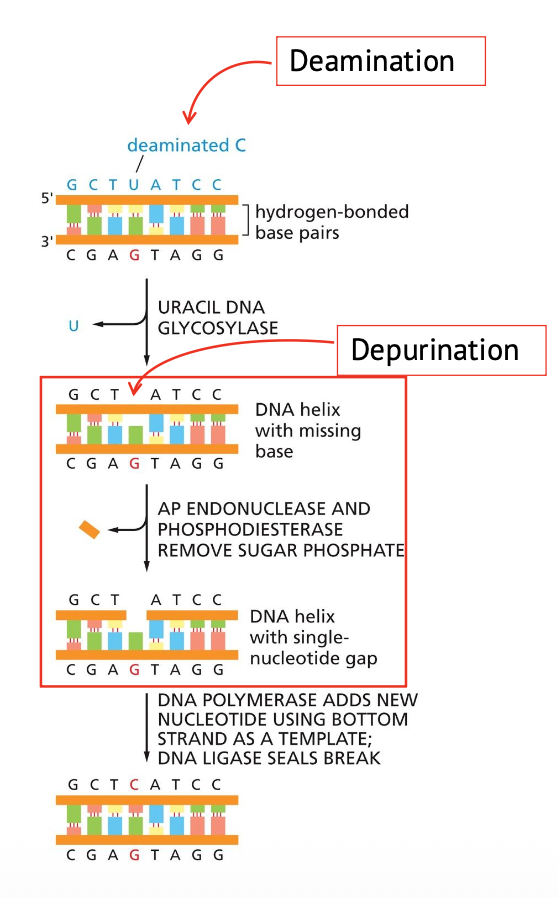
Base Excision Repair - BER הוא מנגנון התיקון המרכזי לנזקים קטנים ברמת הבסיס.
המנגנון עובד בשלושה שלבים כלליים שחוזרים גם במנגנוני תיקון אחרים:
- Recognition - זיהוי הנזק
- Processing - עיבוד הנזק והכנת האתר לתיקון
- Repair - השלמת הנוקלאוטיד החסר וסגירת השלד
השלב הראשון - יצירת אתר חסר בסיס
במקרה של דפורינציה, כבר יש אתר חסר בסיס, כי הבסיס נעלם.
במקרה של דיאמינציה, קודם צריך לזהות את האורציל ולהסיר אותו. האנזים שעושה זאת הוא: UNG - Uracil DNA Glycosylase
UNG מזהה אורציל בתוך DNA, מסיר אותו, וכך יוצר אתר חסר בסיס (כמו “שן חסרה” ב־DNA).
הסרת הסוכר החסר בסיס
אחרי שנוצר AP site, צריך להסיר את החלק הסוכרי-פוספטי שבו חסר בסיס. אי אפשר פשוט “להכניס בסיס” לתוך הסוכר הקיים; צריך להכניס נוקלאוטיד שלם.
האנזים שעושה את החיתוך הוא: APE1 / AP endonuclease
APE1 מזהה AP site וחותך את השלד, כך שנוצר nick חד־גדילי.
השלמת הנוקלאוטיד וסגירת השרשרת
לאחר מכן:
- DNA polymerase β מוסיף את הנוקלאוטיד החסר.
- Ligase סוגר את ה־nick ומחבר מחדש את השלד הסוכרי-פוספטי.
לדימוי: פולימראז β הוא כמו פינצטה שמניחה את הנוקלאוטיד במקום, וליגאז הוא כמו דבק שסוגר את השרשרת.
מה קורה אם לא מתקנים בזמן?
“הטוב, הרע והמכוער”:
- הטוב - BER מתקן בזמן, והבסיס התקין משוחזר.
- הרע - אם אתר חסר בסיס עובר שכפול לפני תיקון, יכולה להיווצר מחיקה באזור הזה.
- המכוער - Translesion synthesis יכול לסנתז מעל האתר הפגוע בצורה פחות מדויקת, וכך להכניס מוטציה.
גם בדיאמינציה, אם לא מתקנים בזמן, שינוי כמו C→U עלול להפוך לאחר שכפול לשינוי קבוע בזוג הבסיסים.
דיאמינציה יזומה במערכת החיסון ובתגובה אנטי-ויראלית
אחרי שהוצגה דיאמינציה כנזק, עלתה השאלה: למה שהתא יעשה דיאמינציה באופן יזום?
AID בתאי B
במערכת החיסון, תאי B צריכים לשפר את האפיניות של הנוגדנים שלהם לאנטיגן. התהליך נקרא Affinity maturation.
כדי לעשות זאת, נוצרים שינויים בגנים המקודדים לנוגדנים. המוטציות נוצרות באופן אקראי, ואז יש סלקציה לתאים שבהם הנוגדן נקשר טוב יותר לפתוגן.
האנזים המרכזי הוא: AID - Activation-Induced Deaminase
AID עושה דיאמינציה לציטוזין. הוא לא “מכניס מוטציה” ישירות, אלא יוצר שינוי שמוביל למנגנוני תיקון פחות שמרניים וליצירת מוטציות באזורי הנוגדנים.
זה חשוב ליצירת תגובה חיסונית טובה יותר, אבל יש לזה גם צד מסוכן: אנזים שמייצר מוטציות ב־DNA עלול לתרום לסרטני דם, כמו לימפומות.
APOBEC
הוזכרו גם דיאמינזות ממשפחת APOBEC, שהן קרובות משפחה של AID.
התפקיד שלהן קשור לתגובה אנטי-ויראלית: הן יכולות לבצע דיאמינציה ב־DNA או RNA ויראלי, וכך לפגוע בו כחלק מהתגובה נגד וירוסים.
גם כאן יש צד בעייתי: אם פעילות כזו מתרחשת במקום הלא נכון או בעוצמה לא מבוקרת, היא יכולה לתרום לנזק גנומי.
Guanine oxidation ו־8-oxoG
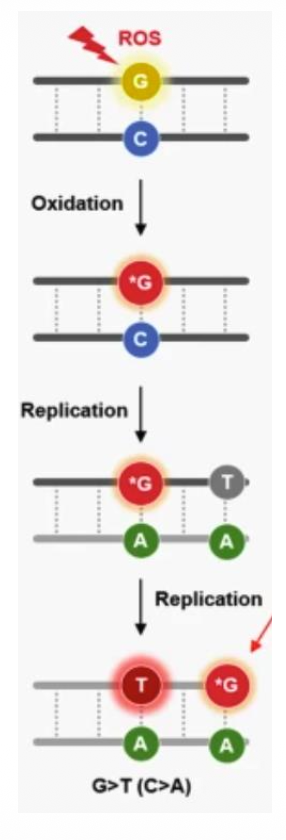
הנזק השלישי הוא Oxidation, בעיקר של גואנין.
Reactive Oxygen Species נוצרים באופן טבעי במיטוכונדריה, בעיקר כתוצר לוואי של שרשרת מעבר האלקטרונים. הם יכולים לעלות גם בעקבות גורמים חיצוניים כמו קרינה מייננת, תרופות או הדבקות חיידקיות וויראליות.
אחד הנזקים הנפוצים שהם יוצרים הוא: 8-oxoGuanine - 8-oxoG
זהו גואנין שעבר חמצון בעמדה 8 (בערך 1,500 מקרים ביום).
אם 8-oxoG לא מתוקן, הוא עלול לגרום למוטציה, משום שהוא יכול להזדווג בצורה לא תקינה עם אדנין. לכן חשוב להסיר אותו לפני שכפול DNA.
למה טלומרים פגיעים במיוחד?
כל ה־DNA חשוף לנזקי חמצון, אבל הטלומרים פגיעים במיוחד ל־8-oxoG.
הסיבה היא שהטלומרים עשירים מאוד בגואנין. הרצף הטלומרי מורכב מחזרות של:
\[\text{TTAGGG}\]כלומר, חלק גדול מהרצף הוא G. מכיוון ש־8-oxoG נוצר מגואנין, אזורים עשירים בגואנין חשופים יותר לנזק הזה.
תיקון 8-oxoG
כמו דיאמינציה ודפורינציה, גם 8-oxoG מתוקן על ידי BER.
אבל בשלב הראשון צריך אנזים שיודע לזהות ולהסיר 8-oxoG. האנזים הזה הוא: OGG1 - 8-oxoguanine glycosylase 1
OGG1 מקביל בתפקידו ל־UNG, אבל הוא מזהה 8-oxoG במקום אורציל. לאחר יצירת AP site, המשך התיקון דומה: APE1, פולימראז β וליגאז.
| נזק | אנזים זיהוי/הסרה ראשון | המשך תיקון |
|---|---|---|
| דיאמינציה C→U | UNG | APE1 → Polymerase β → Ligase |
| אוקסידציה ל־8-oxoG | OGG1 | APE1 → Polymerase β → Ligase |
| דפורינציה | כבר נוצר AP site | APE1 → Polymerase β → Ligase |
מיפוי AP sites ו־8-oxoG בגנום
בחלק האחרון של השיעור דיברנו על הדרך לזהות ולמפות אתרים חסרי בסיס בגנום.
המטרה היא לא רק לדעת שיש נזק, אלא לשאול:
- האם טיפול מסוים מעלה את מספר ה־AP sites?
- איפה בגנום הם נוצרים?
- האם הם מפוזרים באופן אחיד או מועשרים באזורים מסוימים?
הרעיון הכללי של AP-seq
השיטה היא AP-seq - מיפוי של אתרים א-פוריניים / אתרים חסרי בסיס.
השלבים הכלליים:
- חותכים את ה־DNA באופן אקראי למקטעים.
- מבצעים סלקציה למקטעים שמכילים AP site.
- מרצפים את המקטעים.
- ממפים את הקריאות לגנום.
השלב החשוב הוא הסלקציה: איך מזהים דווקא מקטעים שיש בהם אתר חסר בסיס?
Isolate the apurinic sites
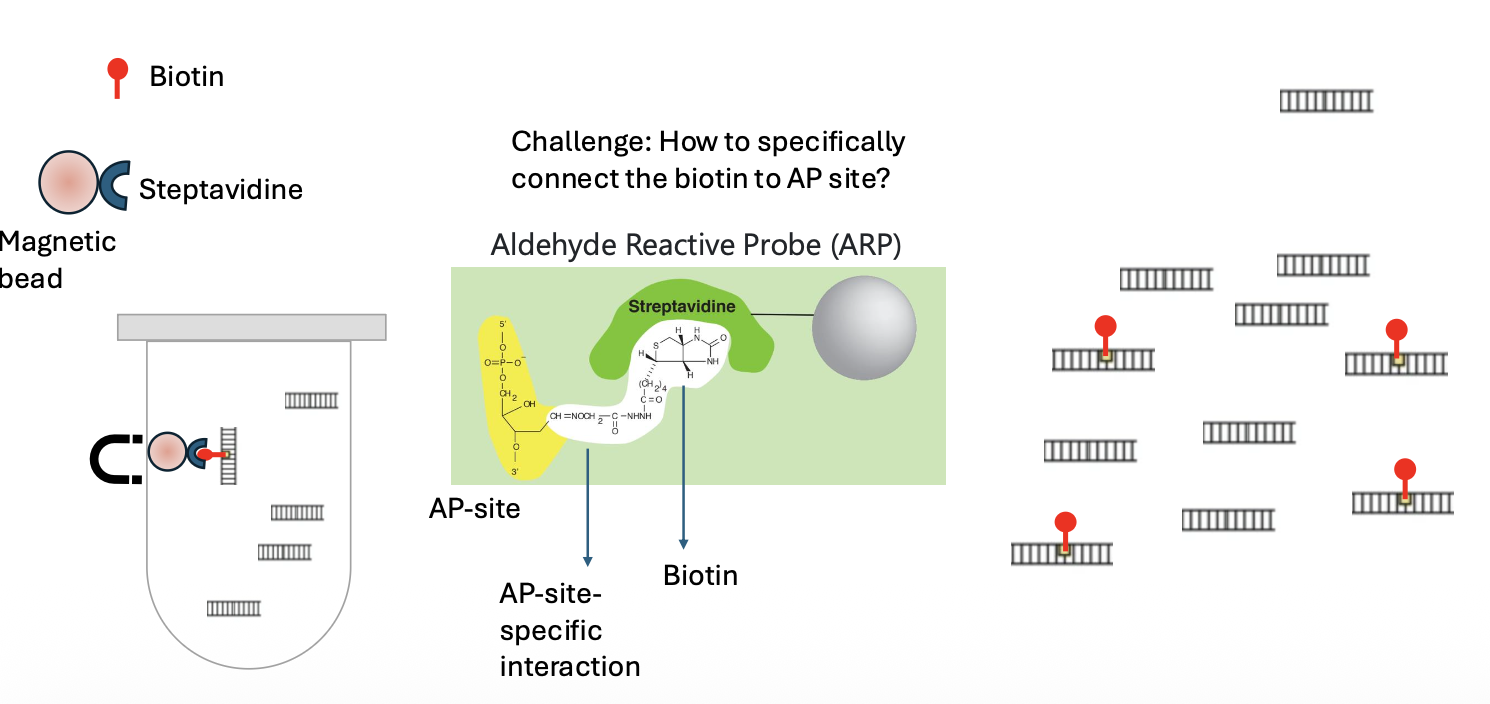
כדי לזהות AP sites משתמשים במערכת Biotin-Streptavidin.
העיקרון:
- משתמשים ב־aldehyde-reactive probe שמזהה את הסוכר באתר חסר בסיס.
- הפרוב מחובר ל־biotin.
- כך AP sites מקבלים סימון ביוטין.
- משתמשים בבידים מגנטיים המצופים streptavidin.
- Streptavidin נקשר לביוטין בצורה מאוד ספציפית.
- בעזרת מגנט מבודדים את מקטעי ה־DNA שמכילים AP sites.
אם יש נוגדן או חלבון שמזהה את התכונה הרצויה, אפשר להשתמש בו. אם אין, צריך לבנות מערכת זיהוי. כאן המערכת היא ביוטין-סטרפטאבידין.
שלבים 3 ו־4 - Sequencing and alignment
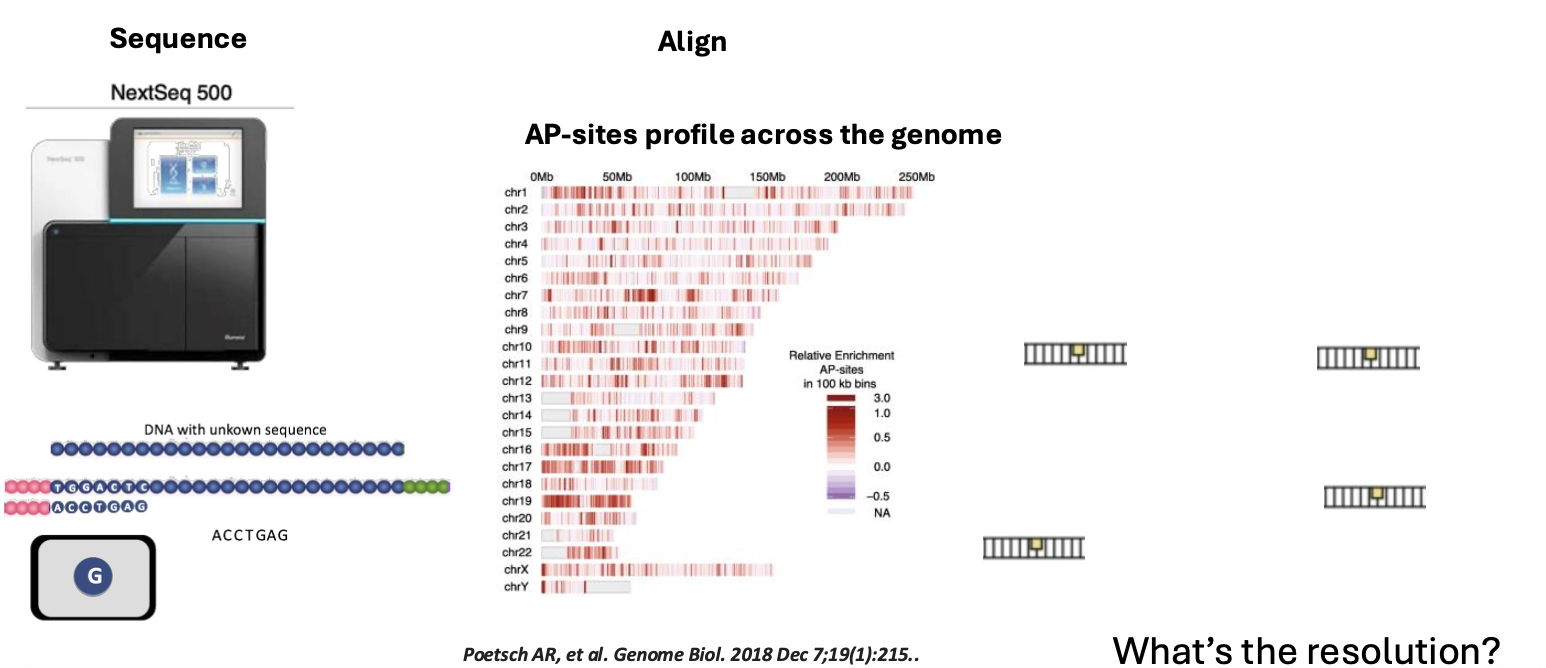
אחרי בידוד המקטעים, ממשיכים כמו בספריות DNA אחרות:
- חיבור אדפטורים
- ריצוף
- alignment לגנום
- ניתוח פיזור האתרים לאורך הגנום
התוצאה היא מיפוי של AP sites. בתמונה למעלה (צד ימין) יש מפה, שבה רואים שהנזק אינו מפוזר באופן אחיד: יש אזורים שבהם יש יותר AP sites ואזורים שבהם יש פחות.
איך ממפים 8-oxoG?
אם רוצים למפות אתרי 8-oxoG ולא רק AP sites קיימים, אפשר להשתמש בידע ממנגנון התיקון.
הרעיון:
- לוקחים את ה־DNA.
- מטפלים בו ב־OGG1.
- OGG1 מזהה 8-oxoG ומסיר אותו.
- ההסרה יוצרת AP site.
- עכשיו אפשר להשתמש באותה שיטת AP-seq כדי למפות את האתרים.
כלומר, OGG1 הופך את אתרי האוקסידציה לאתרים חסרי בסיס שניתן למפות בשיטה שתוארה.
ניסוי עם X-ray
ניסוי שבו השוו בין תאי ביקורת לתאים שטופלו ב־X-ray; מכיוון ש־X-ray משרה oxidative stress, מצפים לראות יותר נזקי חמצון.
ההשוואה הראתה:
- לאחר X-ray יש עלייה ב־AP sites לאורך הגנום.
- באתרים שהועשרו בעזרת OGG1, כלומר אתרים שמייצגים 8-oxoG, ההשפעה של X-ray בולטת יותר.
זה מתאים לרעיון ש־X-ray מעלה oxidative stress, ולכן מעלה בעיקר נזקי חמצון.
העשרה בטלומרים
בסוף השיעור הוצגה דוגמה לניתוח של העשרה באזורים גנומיים מסוימים.
הנקודה שהודגשה: בטלומרים יש העשרה של AP sites שמקורם בנזק חמצוני, במיוחד באתרים שהועשרו בעזרת OGG1.
זה מתאים למה שנאמר קודם: טלומרים עשירים בגואנין, ולכן הם רגישים יותר ל־8-oxoG.
דור פסקל