תוכן העניינים:
- חזרה על השיעור הקודם
- ראשית הכפלה - Origin of Replication
- יצירת מזלג הכפלה
- מרכיבי מזלג הרפליקציה
- מקטעי אוקזקי
- סגירת מקטעי אוקזקי - החלפת הפריימר
- ליגציה ואריזה חזרה לכרומטין
- תהליך מזלג הרפליקציה - סיכום
- מחלות Trinucleotide Repeat
חזרה על השיעור הקודם
בשיעור הקודם דיברנו על DNA פולימראז. הסינתזה היא תהליך ספונטני מבחינה כימית, כיוון שהנוקלאוטיד נושא את האנרגיה הדרושה בקבוצת הטרי-פוספט שלו, והיא מתבצעת תמיד בכיוון 5’←3’: הנוקלאוטיד החדש מתחבר לקבוצת ההידרוקסיל החופשית שעל פחמן 3’ של הגדיל הגדל. לא קיימת שום מערכת ביולוגית שבה הסינתזה הולכת בכיוון הפוך. בנוסף לכך, DNA פולימראז יודע רק להאריך שרשראות קיימות ואינו יכול להתחיל שרשרת חדשה De Novo, בניגוד ל־RNA פולימראז.
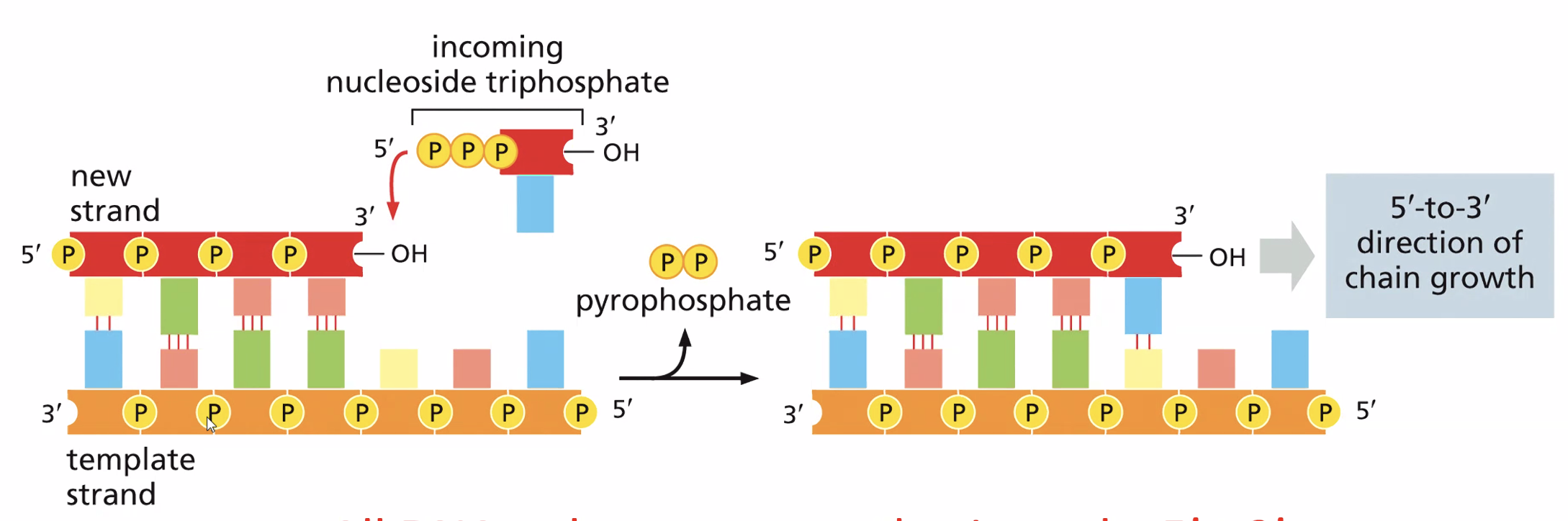
תכונת ה־Proofreading (הגהה)
ל־DNA פולימראז שני אתרים פעילים:
-
האתר הראשון - פולימריזציה: האפיניות לכל הנוקלאוטידים זהה, ומה שקובע איזה נוקלאוטיד יסונתז הוא זיווג הבסיסים עם הטמפלייט. נוקלאוטיד נכון יוצר קשרי מימן עם הטמפלייט, מה שגורר שינוי קונפורמציה שמקרב את קצה 5’ של הנוקלאוטיד לקבוצת ה־OH של השרשרת הגדלה ומאפשר את הפולימריזציה.
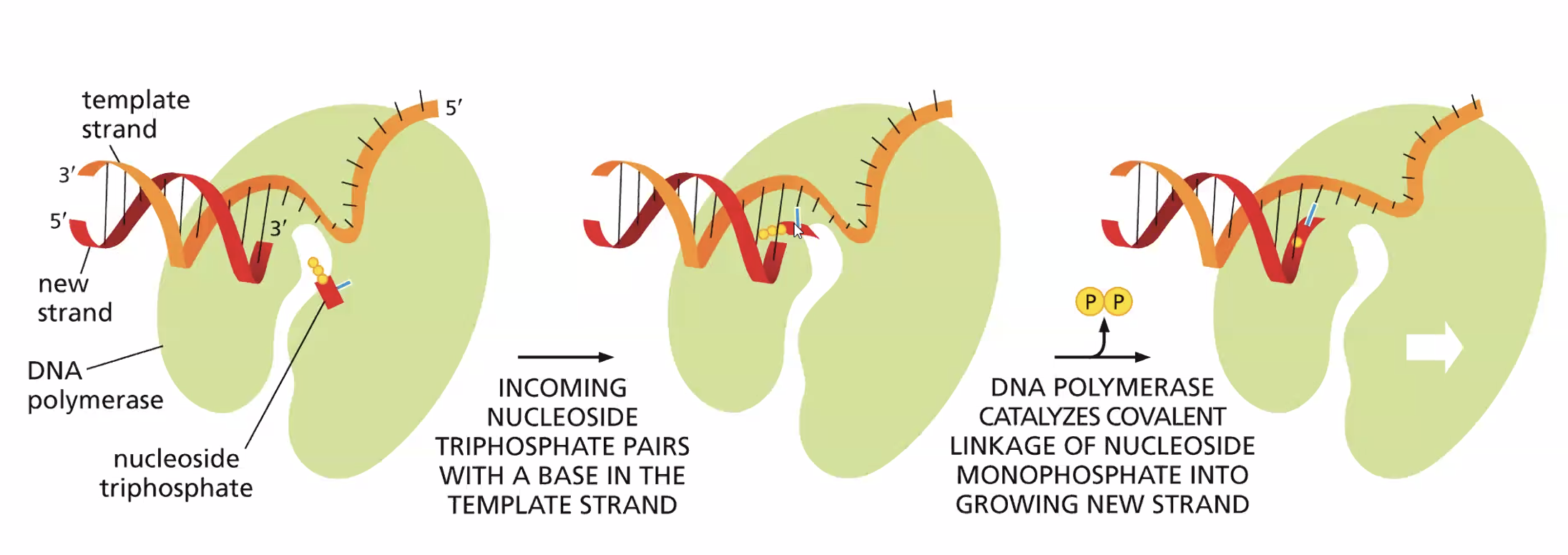
-
האתר השני - אקסונוקלאז 3’←5’: יודע לפרק נוקלאוטיד אחד מקצה המולקולה. האפיניות שלו גבוהה לחד־גדיל בלבד. כשנכנס נוקלאוטיד שגוי, הוא חוזר במהרה לקונפורמציה האנרגתית הנמוכה שלו, הדו־גדיל “נפתח” מקומית, וה־DNA פולימראז קופץ לאתר האקסונוקלאז ומסלק את הנוקלאוטיד השגוי.
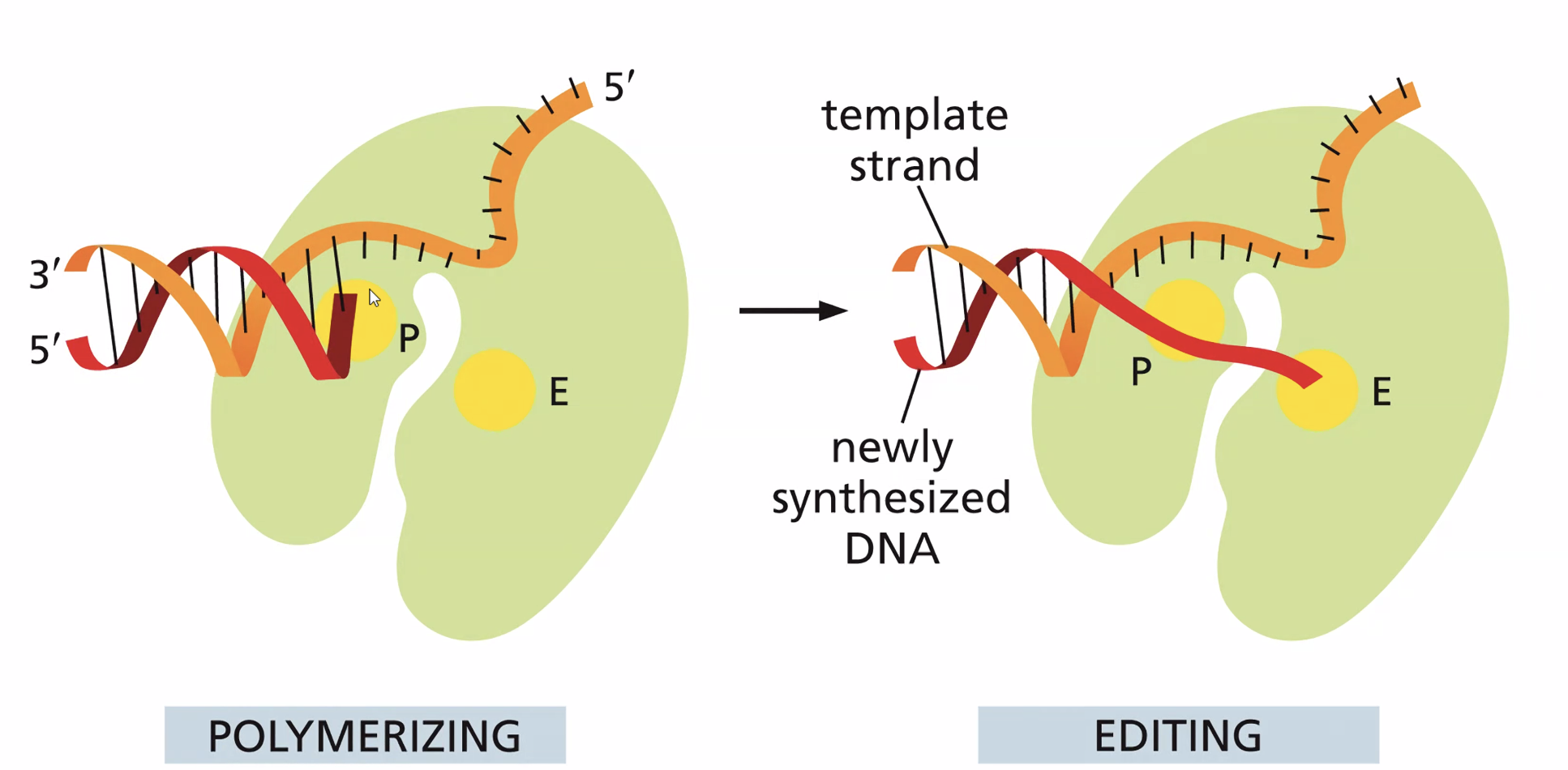
נקודה קלינית: קיים שיווי-משקל עדין בין קצב הפולימריזציה לקצב פעילות האקסונוקלאז.
מוטציה שמגבירה את קצב הפולימריזציה תאיץ את הרפליקציה אך תגדיל את אחוז הטעויות.
מוטציה שמבטלת את הפעילות האקסונוקלאזית תטה את שיווי המשקל לכיוון טעויות מוגברות.
לאחר סיום הרפליקציה פועלת גם מערכת תיקון נוספת (Post-Replication Repair) שנדון בה בהמשך הקורס.
ראשית הכפלה - Origin of Replication
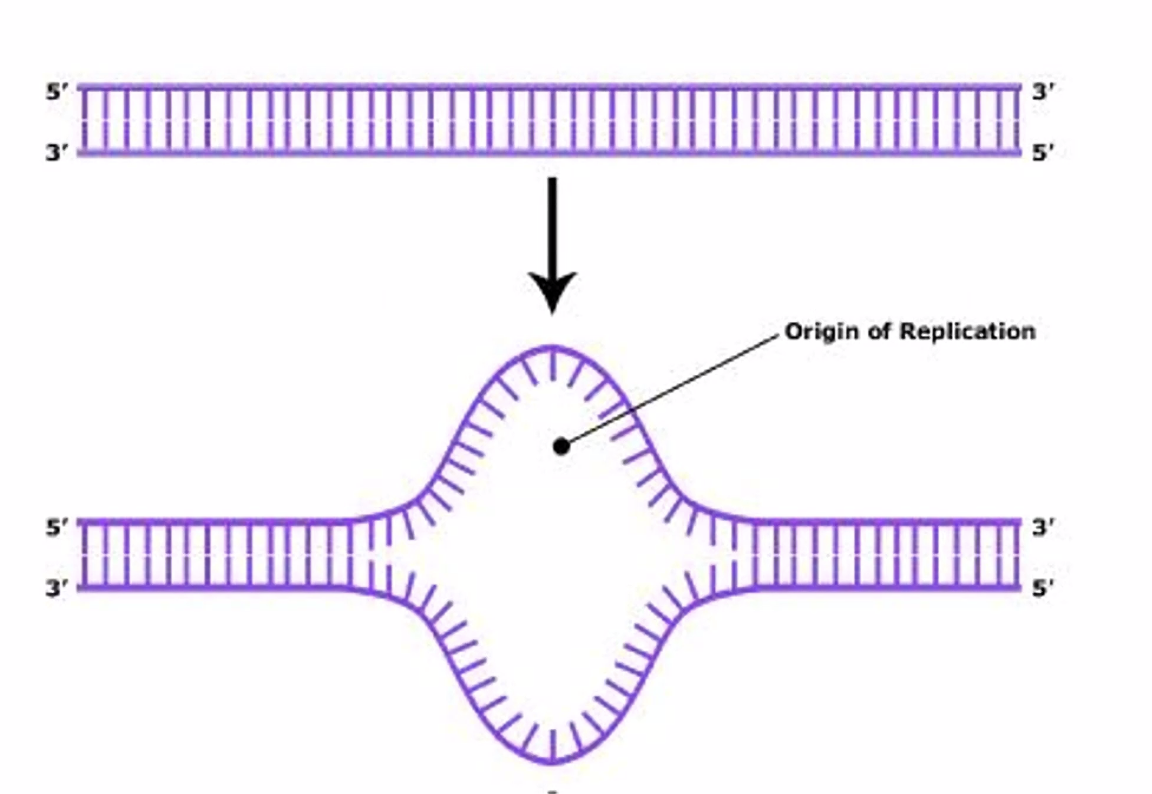
אזורי ראשית הכפלה (Origins of Replication) מפוזרים לאורך הכרומוזום ומתאפיינים במספר תכונות פיזיקליות שמקלות על פתיחת הדו־גדיל:
- עשיר ב־AT: לזיווג A-T יש רק שני קשרי מימן (לעומת שלושה לזיווג G-C), ולכן קל יותר לפתוח אותו.
- בנוסף לכך, רצפי A ארוכים יוצרים כיפוף (Bent) של הדו־גדיל, שמסייע ליצירת לולאה ומקל על הפתיחה.
- ללא נוקלאוזומים (Nucleosome-free): הנוקלאוזומים מוסרים מהאזור באופן אקטיבי על־ידי קומפלקסי Remodelers. הנוקלאוזומים שכן קיימים בסמוך לאתר תורמים למתח פיתולי שלילי (Negative Supercoiling) המרפה את קשרי הגדיל.
- Negative Supercoiling: המתח הפיתולי השלילי שנוצר בין נוקלאוזומים סמוכים מחליש את קשרי הגדיל ומקל מאוד על פתיחת הדו־גדיל (בתוך היסטון המתח הפיתולי הוא חיובי, אך מחוץ להיסטון הוא שלילי לצורך איזון).
השוואה: חיידקים מול תאים אאוקריוטים
גודל הגנום של חיידק E. Coli הוא כ־$4.6 \, \mathrm{Mb}$, וקצב הכפלת ה־DNA הוא 1,000 בסיסים לשניה. מה זמן הכפלת ה־DNA של E. Coli?
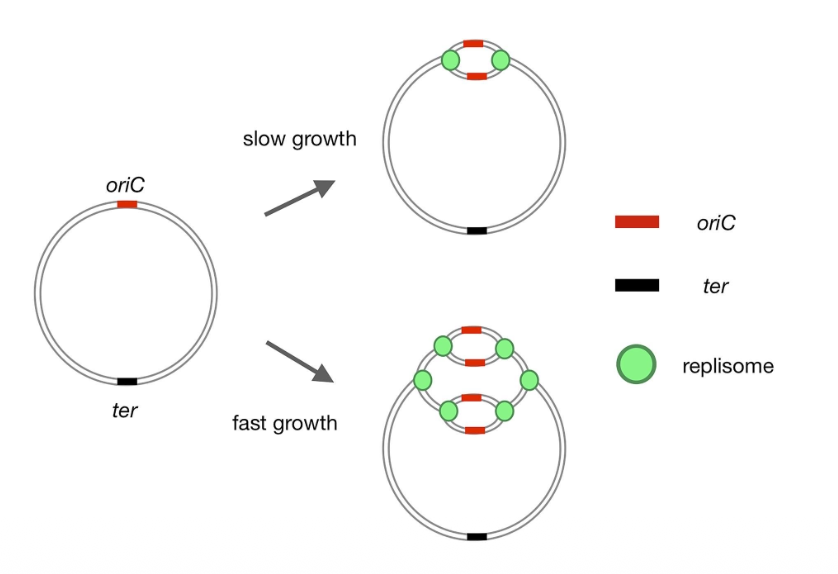
בחיידק E. coli יש אתר ראשית הכפלה אחד בלבד, ממנו הרפליקציה מתקדמת בשני כיוונים. מכיוון שהגנום הוא $4.6 \, \mathrm{Mb}$ וקצב הפולימראז הוא $1,000$ בסיסים/שנייה, החישוב התיאורטי נותן בערך $40$ דקות - אך בפועל E. coli מסוגל להשלים את הרפליקציה תוך 20 דקות, בגלל שהוא מתחיל מחזור רפליקציה חדש עוד לפני שסיים את הקודם (“Re-firing”). באיור למטה זה המצב התחתון.
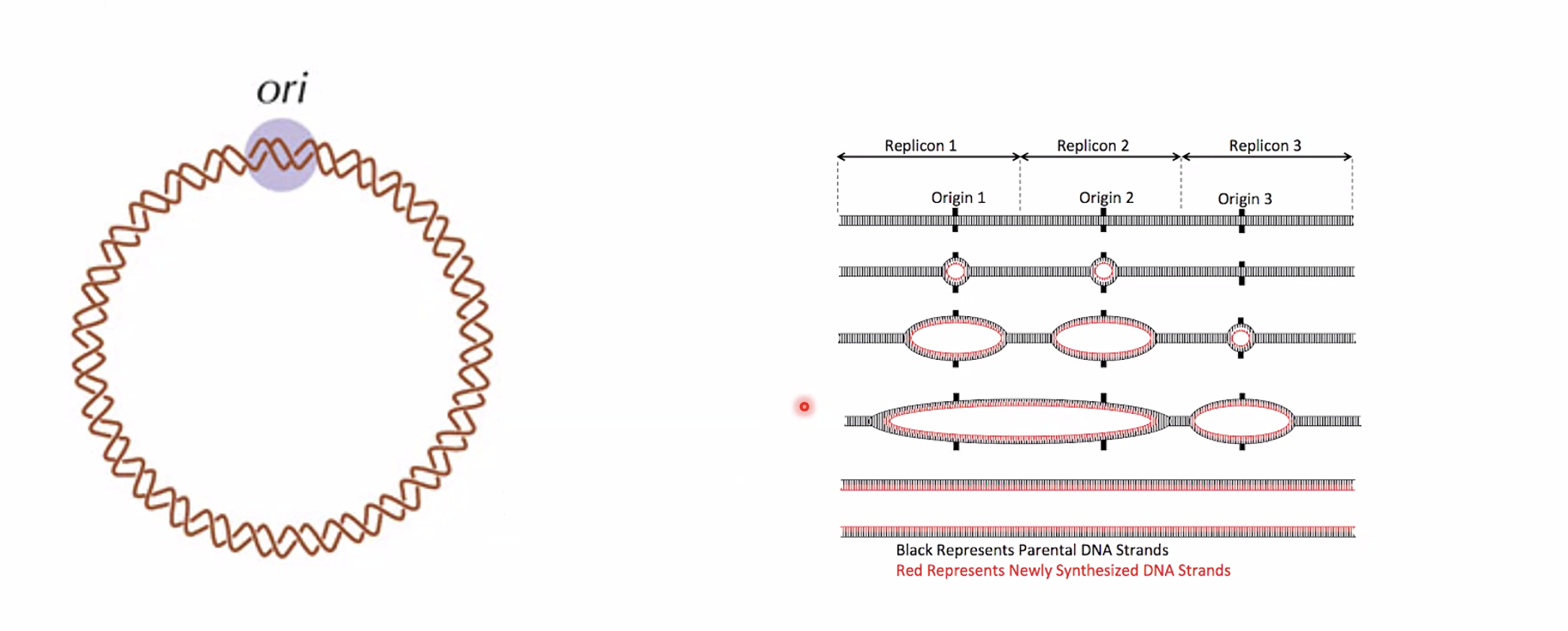
גודל הגנום האנושי הוא $3200 \, \mathrm{Mb}$ וקצב ההכפלה של DNA polymerase הוא 50 בסיסים/שניה. מהו זמן ההכפלה הצפוי של של הגנום האנושי?
תשובה: 178,000 שעות. אבל בפועל זמן הכפלת ה־DNA הוא 10-8 שעות. כיצד?
באאוקריוטים, לעומת זאת:
- הגנום האנושי גדול בסדרי גודל מגנום חיידקי.
- קצב ה־DNA פולימראז הוא רק כ־50 בסיסים/שנייה.
- אסור לאתר ראשית הכפלה “לירות” יותר מפעם אחת בכל מחזור תא.
- הפתרון: אתרי ראשית הכפלה רבים שיורים במקביל לאורך כל כרומוזום. לא כולם יורים בו־זמנית - יש Early Origins ו־Late Origins, בהתאם למצב הכרומטין, לתעתוק פעיל ועוד.
באיור - תא אנושי מצד ימין ותא חיידקי מצד שמאל.
יצירת מזלג הכפלה
הרכבת מזלג הרפליקציה
בכל Origin נבנים שני מזלגות רפליקציה.
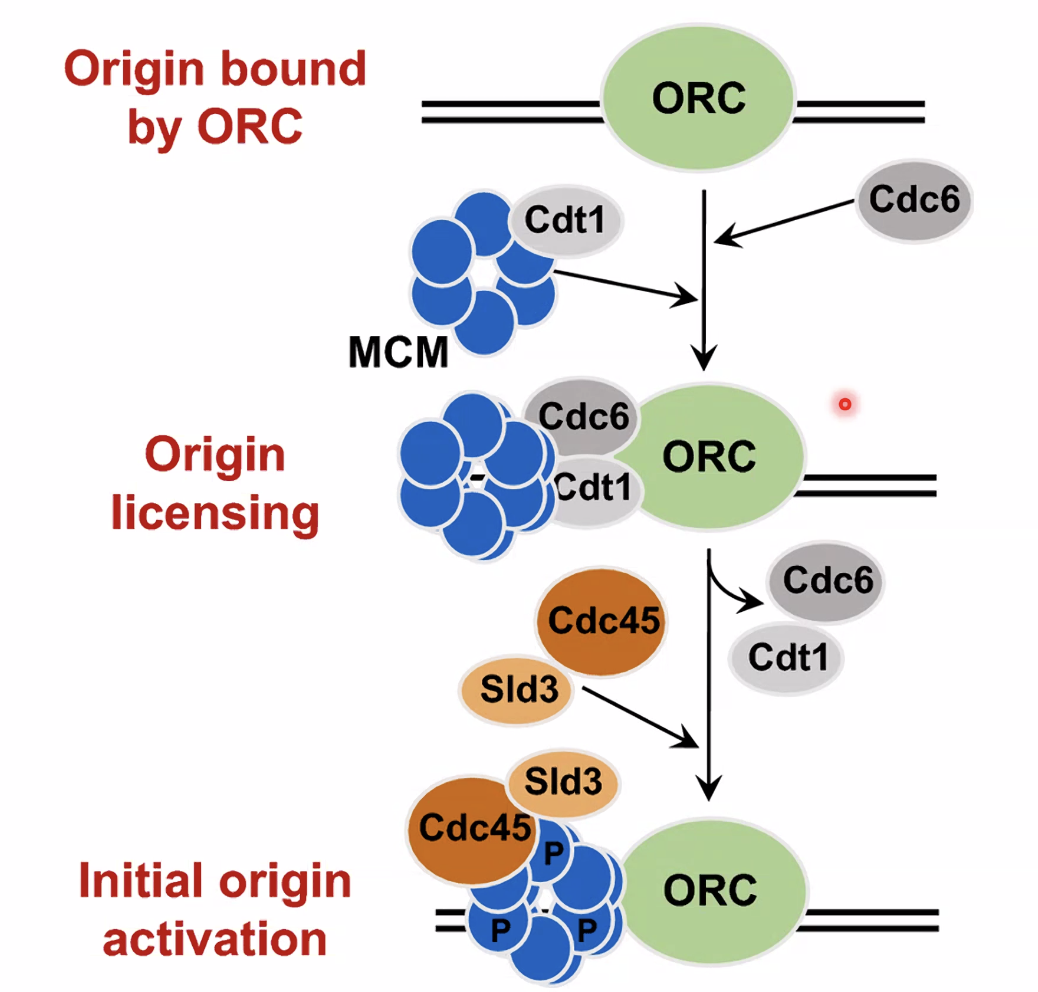
תהליך הרכבת המזלג בתאים אאוקריוטים:
- ORC (Origin Recognition Complex) - קומפלקס חלבוני שנקשר לאתר ראשית הכפלה מיד עם סיום המיטוזה, בתחילת G1. הוא ה”סמן” של האתר.
- ה־ORC מגייס את MCM (Mini Chromosome Maintenance) - קומפלקס הליקאז שנשאר לא־פעיל, “נטען” על ה־DNA בשלב G1 בנוכחות גורמי בקרה CDC6 ו־CDT1.
- בכניסה לשלב S, קסקדה של פוספורילציות ודה־פוספורילציות (בהשתתפות CDC45 ו־SLD3) משחררת את ה־MCM מה־ORC ומפעילה אותו (ה־Origin “יורה”).
- ה־MCM מנצל את הפתיחה הראשונית שנוצרה באתר ה־ORC ומתחיל לפתוח את הדו־גדיל.
התהליך: ה־ORC מסמן את האתר ← קושר MCM ← קסקדת פוספורילציה משחררת ומפעילה את ה־MCM ← האתר “יורה”.
MCM - ההליקאז
Roles of DNA helicase
- Helicase activity is ATP-dependent.
- Melts the dsDNA into ssDNA.
- Remove secondary structures (triplexes, quadruplexes, G4 loops).
- Displace DNA-bound proteins
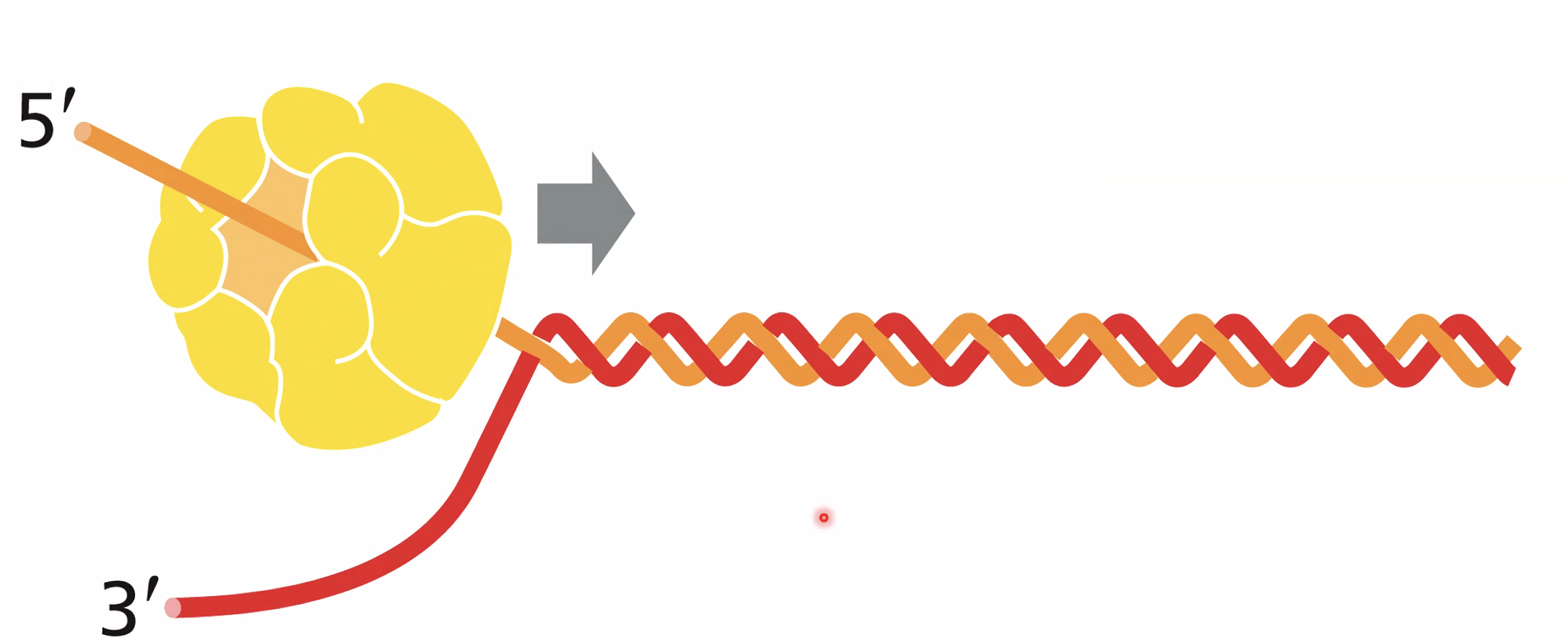
ההליקאז (MCM) הוא אנזים שמבצע “התכה” - פתיחת הדו־גדיל לשני חד־גדילים. מקור האנרגיה: הידרוליזה של ATP (ATP הופך ל־ADP). ההליקאז מתגבר על קשרי המימן ועל קשרי הוואן-דר-ואלס שמחזיקים את הדו־גדיל, ובנוסף:
- מפרק מבנים שניוניים (טריפלקסים, קוואדרופלקסים, לולאות G4).
- מסלק חלבונים שיושבים על ה־DNA (RNA פולימראז, היסטונים ועוד) - פועל כ”מכבש” שנכנס עם אנרגיה גבוהה ומפנה הכל מפניו.
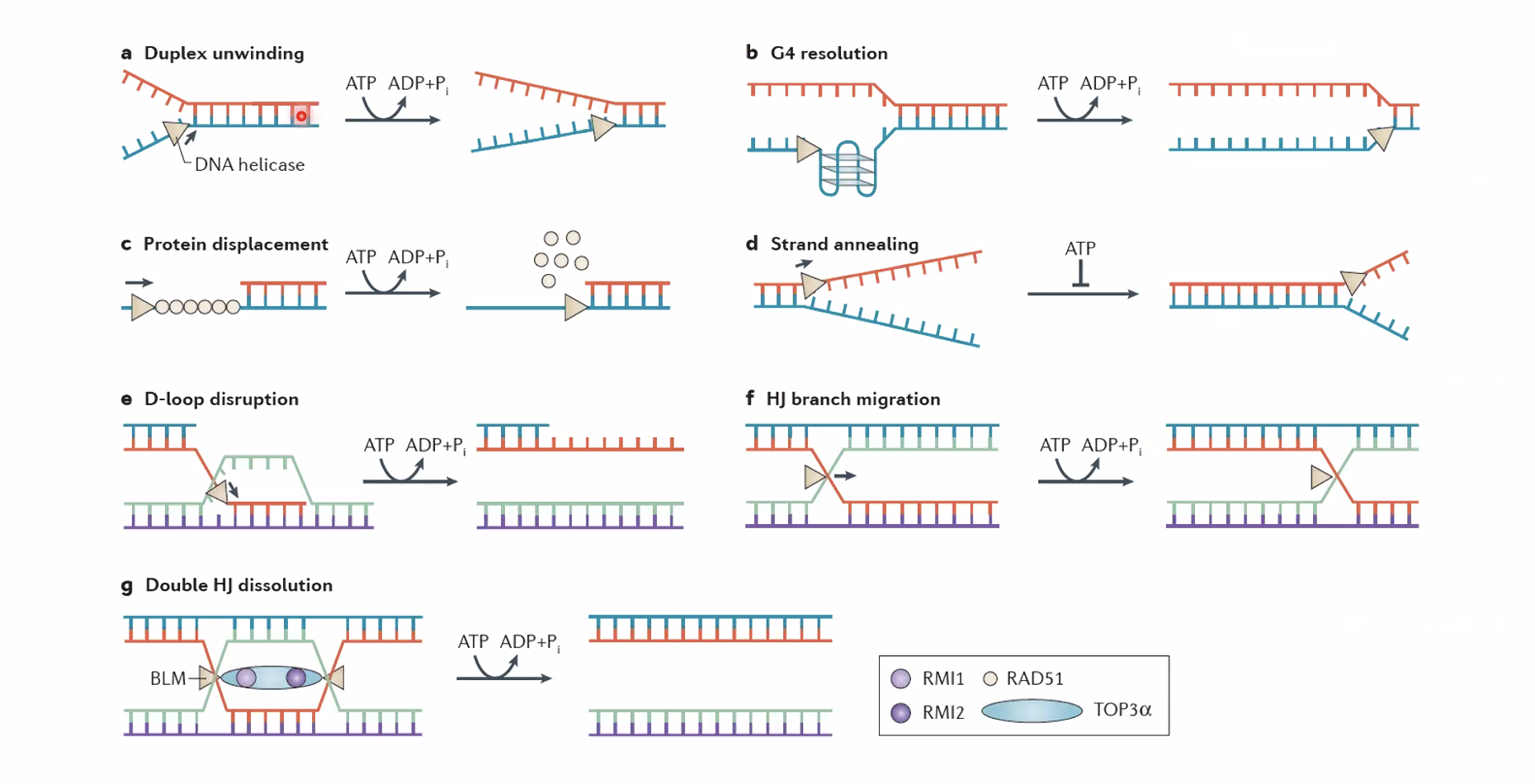
משפחת ההליקאזות היא אחת הגדולות ביותר בתא, ויש לה תפקידים גם ב־DNA Repair, בטרנסקריפציה ובסגירת Holliday junctions (קשור לרקומבינציה, ניתן כדוגמה אגבית).
טופואיזומרז - שחרור מתח הסופרקוילינג
פתיחת הדו־גדיל על־ידי ההליקאז יוצרת Positive Supercoiling (Wr) מלפנים. אם המתח לא מוסר, הוא יכול להתנגד לפעולת ההליקאז ועלול לעצור אותו או לגרום לשבירת ה־DNA. טופואיזומרז מסיר את המתח על־ידי שינוי ה־Linking Number של ה־DNA, ופעילותו חיונית לקידום הרפליקציה.
מרכיבי מזלג הרפליקציה
DNA פולימראז אלפא (פרימאז)
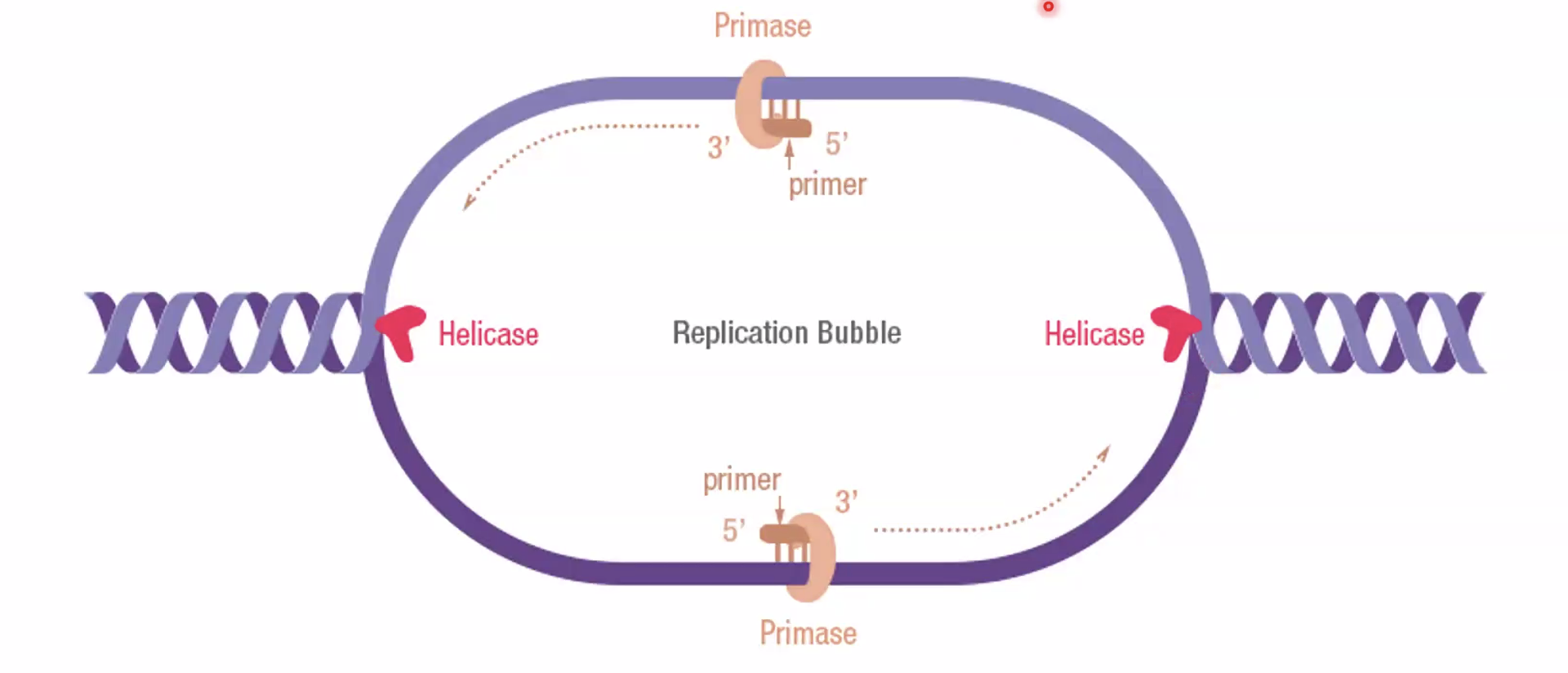 | 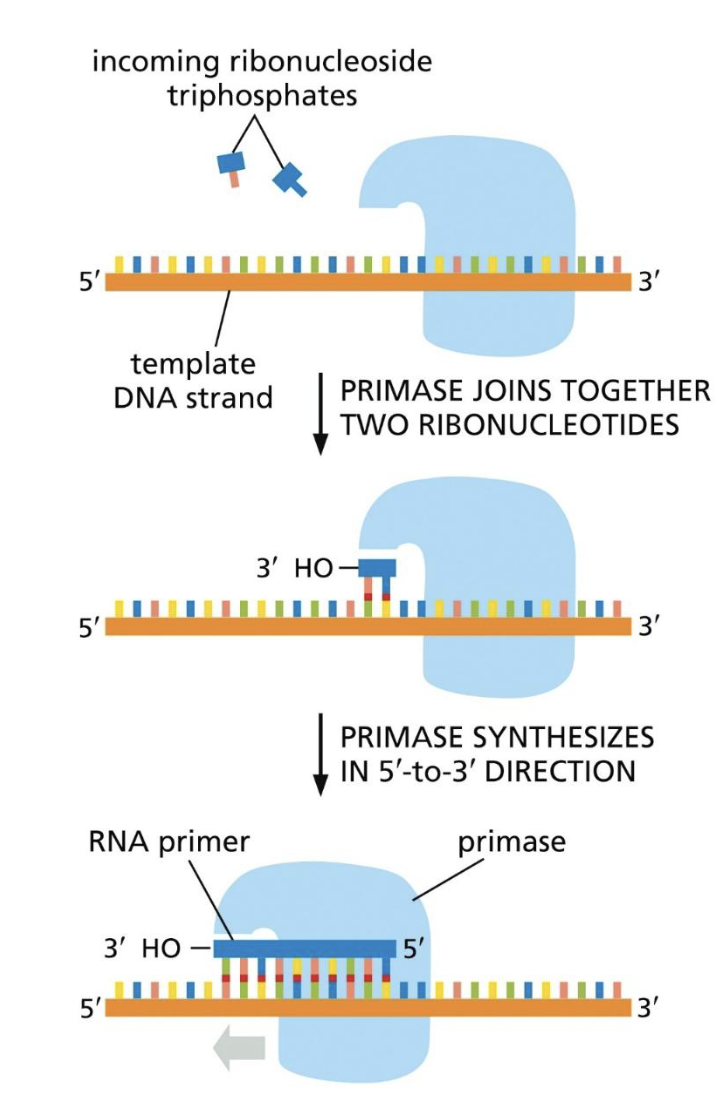 |
DNA פולימראז לא יכול להתחיל שרשרת חדשה, לכן נדרש פריימר קיים (קצה $\ce{3’-OH}$) שממנו ניתן להמשיך. בחיידקים, האנזים שמסנתז פריימרים הוא פרימאז; באאוקריוטים זהו DNA פולימראז אלפא (DNA polymerase alpha).
תכונות DNA פולימראז אלפא:
- יודע להתחיל שרשראות De Novo.
- מסנתז תחילה כ־8–10 ריבונוקלאוטידים (RNA), ואז ממשיך בעוד כ־10–20 דאוקסיריבונוקלאוטידים (DNA) - סך הכול כ־18–30 נוקלאוטידים.
- פרוססיביות נמוכה מאוד - נופל אחרי סיום הפריימר.
- דיוק (Fidelity) נמוך - אין לו מנגנון Proofreading (הפריימר הוא מולקולה זמנית שתוחלף בהמשך).
DNA פולימראז אלפא מתיישב, מסתנז דה־נובו RNA, לאחר מכן DNA ואז נופל.
להלן הבהרות מ־ChatGPT
פריימר הוא מקטע קצר, לרוב RNA, שמספק קצה 3’-OH חופשי כדי ש־DNA פולימראז יוכל להתחיל להאריך שרשרת.
יש גם הבדל חשוב:
- ב־leading strand צריך פריימר אחד
- ב־lagging strand צריך הרבה פריימרים, אחד לכל מקטע אוקזאקי
הבלבול הנפוץ: הפריימר הוא לא הוא כל הגדיל החדש. רק התחלה זמנית, ובהמשך מחליפים אותו.
Polymerization initiation by replicative DNA polymerases δ and ε
RPA / SSB - Single-Strand Binding Protein
לאחר פתיחת הדו־גדיל, ה־DNA החד־גדילי עלול להיסגר חזרה. החלבון RPA (באאוקריוטים) / SSB (בחיידקים) מצפים את ה־DNA החד־גדילי, ממסכים את הבסיסים ומונעים היווצרות מחדש של הדו־גדיל. כך נשמרת “בועת ההכפלה” פתוחה.
Processivity - ה־Sliding Clamp/PCNA
Sliding Clamp (PCNA)
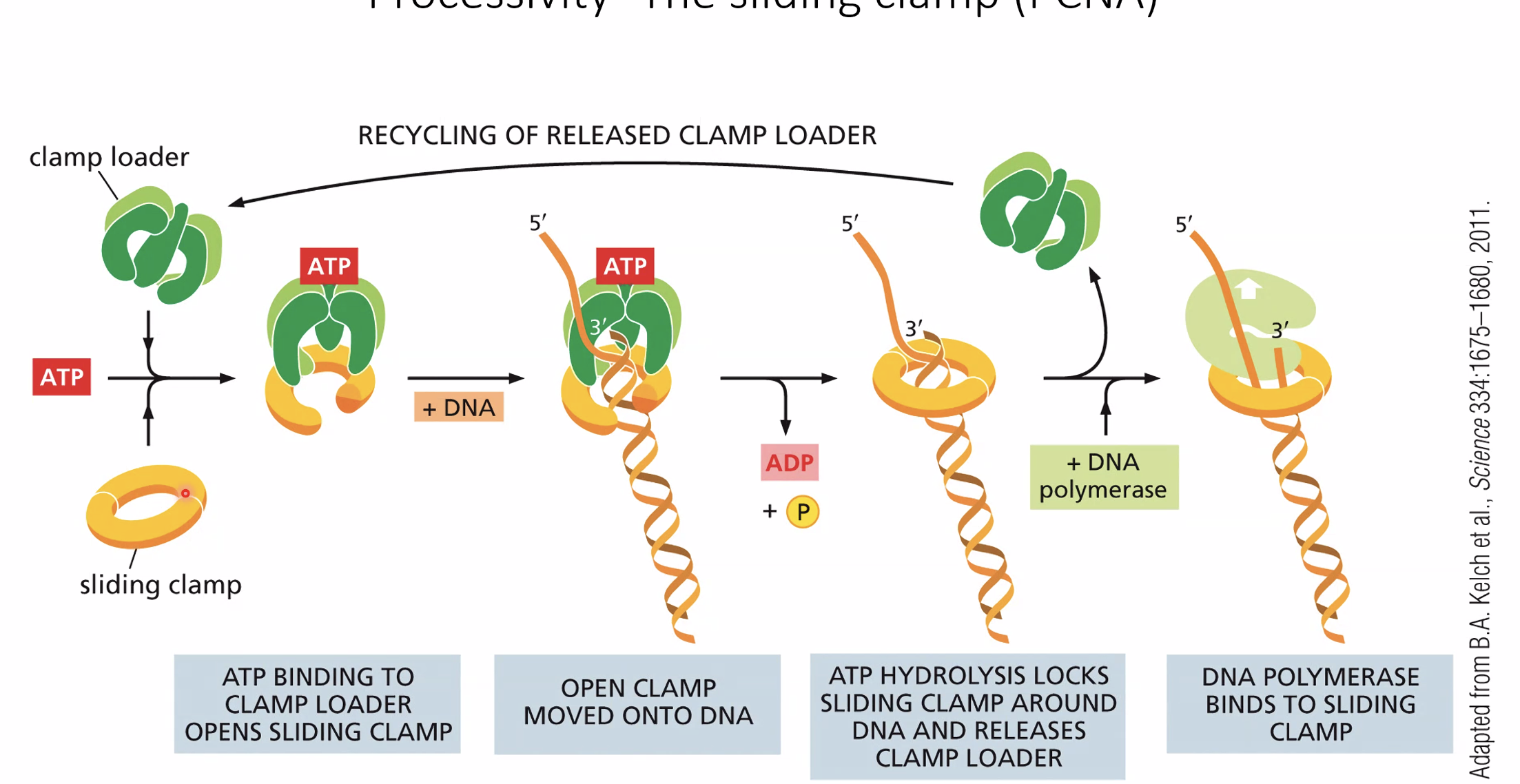
ה־DNA פולימראז הרֶפּלִיקָטִיבִי (Pol ε ו־Pol δ) חייב לסנתז מיליוני בסיסים בלי ליפול. הדבר מושג על־ידי PCNA (Proliferating Cell Nuclear Antigen) - חלבון בצורת טבעת שנועלת פיזית את ה־DNA פולימראז על ה־DNA.
מנגנון הפעולה:
- קישור של ATP גורם לפתיחת הטבעת.
- ה־PCNA מתיישב על ה־DNA עם ה־DNA פולימראז בתוכו.
- הידרוליזה של ATP ל־ADP גורמת לסגירת הטבעת.
- ה־DNA פולימראז נעול ואינו יכול ליפול - פרוססיביות גבוהה מאוד.
גם אם ה־DNA פולימראז מתנתק רגעית מהתבנית, ה־PCNA מחזיק אותו קרוב ומאפשר לו לחזור ולהמשיך. דומה קונספטואלית לקוהיזין.
מקטעי אוקזקי
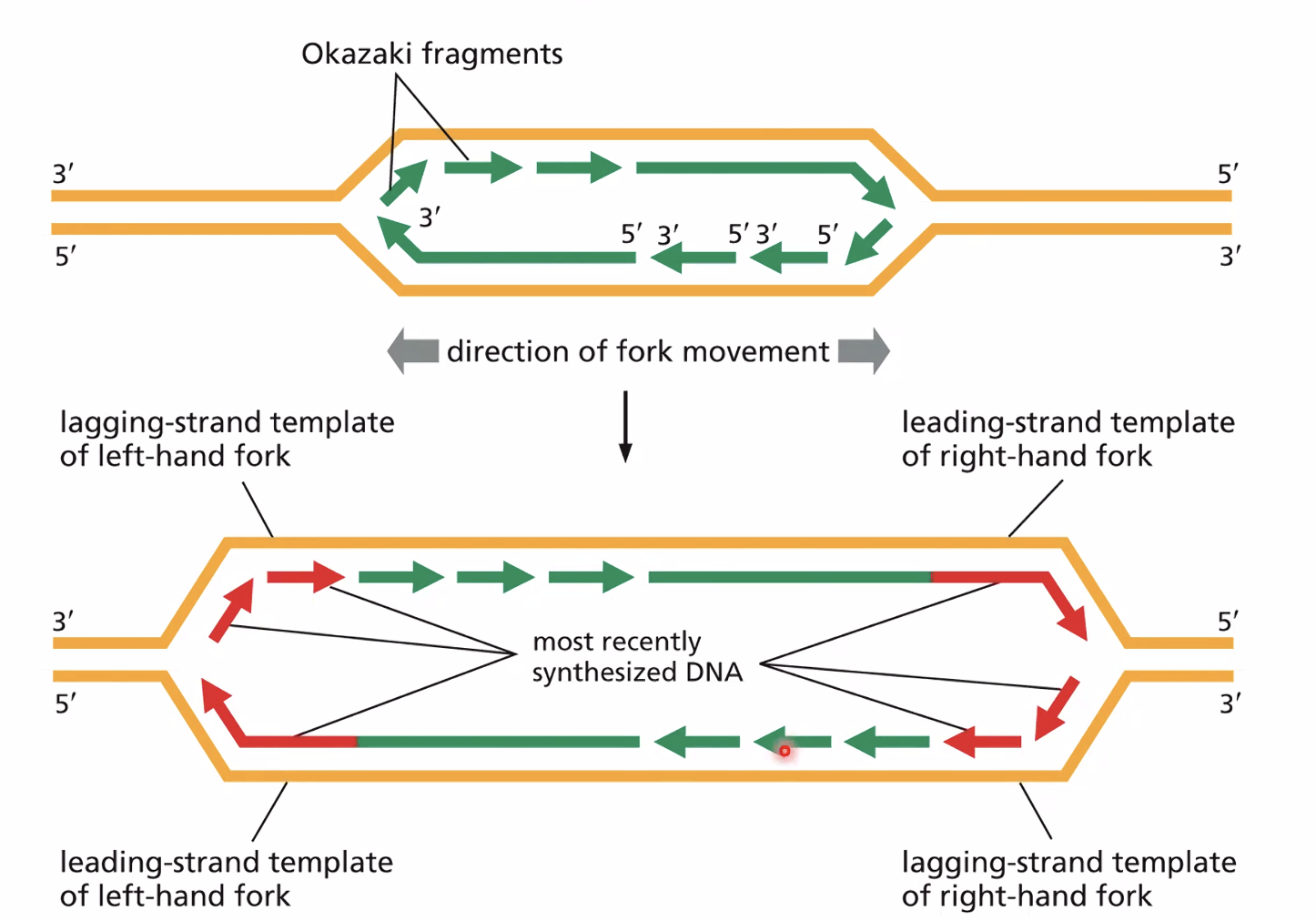
מכיוון שסינתזה של DNA חייבת להיות בכיוון 5’←3’, ואחד משני גדילי הטמפלייט פונה בכיוון 3’←5’ ביחס לכיוון התקדמות המזלג - הגדיל הזה (ה-Lagging Strand) לא יכול להיות מסונתז בצורה רציפה. הפתרון: מקטעי אוקזקי - סינתזה מקוטעת על־ידי היפוך מקומי של ה־Lagging Strand במזלג הרפליקציה, ליצירת אוריינטציה 5’←3’ זמנית.
מה קובע את גודל מקטעי אוקזקי?
- בחיידקים: 1,000–2,000 נוקלאוטידים (אין נוקלאוזומים).
- באדם ובתאים אאוקריוטים: 100–200 נוקלאוטידים - הגודל מוגבל על־ידי גודל הנוקלאוזום (147 נ”ק + לינקר ≈ 200 נ”ק).
נקודה קלינית: בכל ערך בין 100 ל־200 נוקלאוטידים בהקשר של ביולוגיה מולקולרית - חשוב לחשוב מיד על גודל של נוקלאוזום אחד. למשל, ה־circulating cell-free DNA בדם נמצא גם הוא בסדר גודל זה.
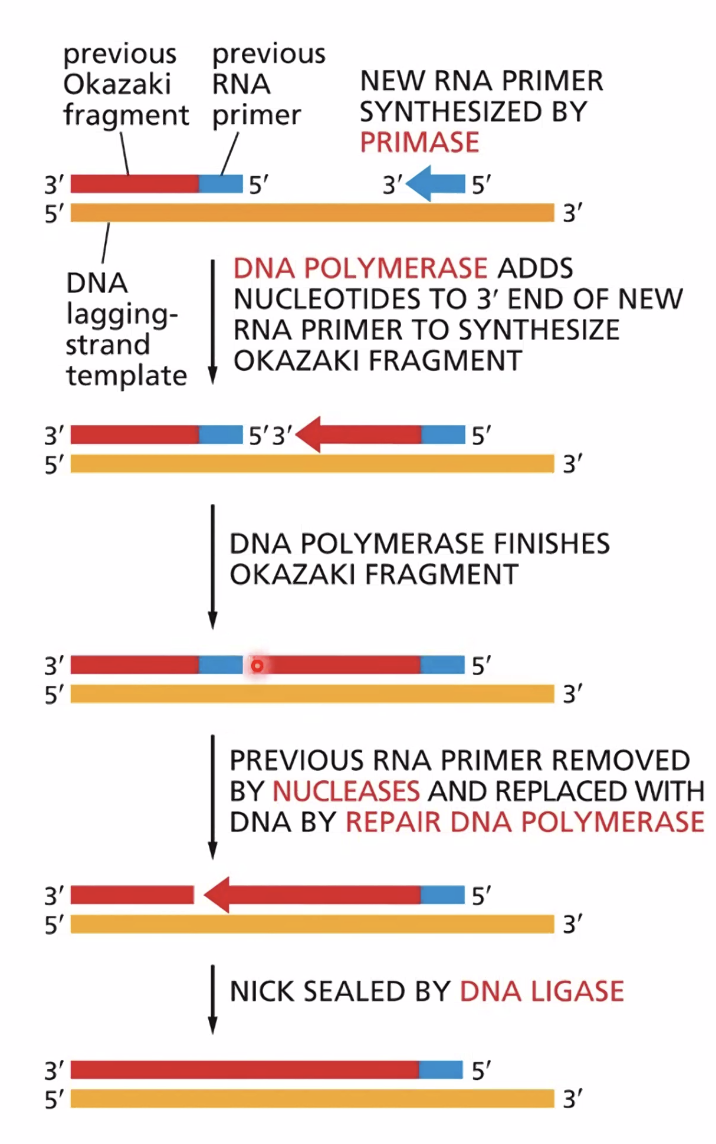
DNA פולימראז רֶפּלִיקָטִיבִי עוצר כאשר הוא נתקל באזור דו־גדילי - כלומר בפריימר של מקטע האוקזקי הבא. זאת הנקודה שבה נוצר Nick (שבר חד־גדילי) ומתחיל תהליך החלפת הפריימר.
סגירת מקטעי אוקזקי - החלפת הפריימר
בחיידקים - E. coli DNA Polymerase I, פעילות 5’←3’ אקסונוקלאז
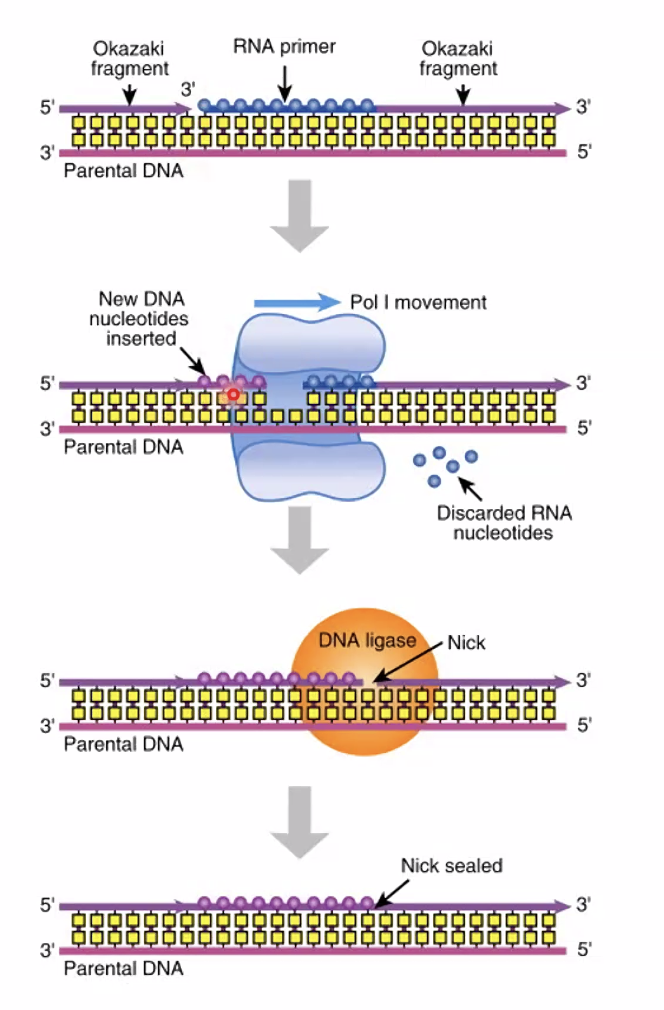
ב־E. coli, DNA פולימראז I (הראשון שבודד על־ידי ארתור קורנברג ב־1958) הוא לא הפולימראז הרֶפּלִיקָטִיבִי - הוא בעל פרוססיביות נמוכה יחסית. תפקידו הייחודי: פעילות אקסונוקלאז 5’←3’ בנוסף לפולימראז ולאקסונוקלאז 3’←5’. כלומר: הוא מפרק מלפניו ומסנתז מאחוריו בו־זמנית, ובכך:
- מפרק את הפריימר (RNA + DNA בדיוק נמוך).
- מחליף אותו ב־DNA בדיוק גבוה.
- לבסוף, DNA ליגאז (עם אנרגיה מ־ATP) סוגר את ה־Nick האחרון.
באאוקריוטים - FEN1 (Flap Endonuclease)
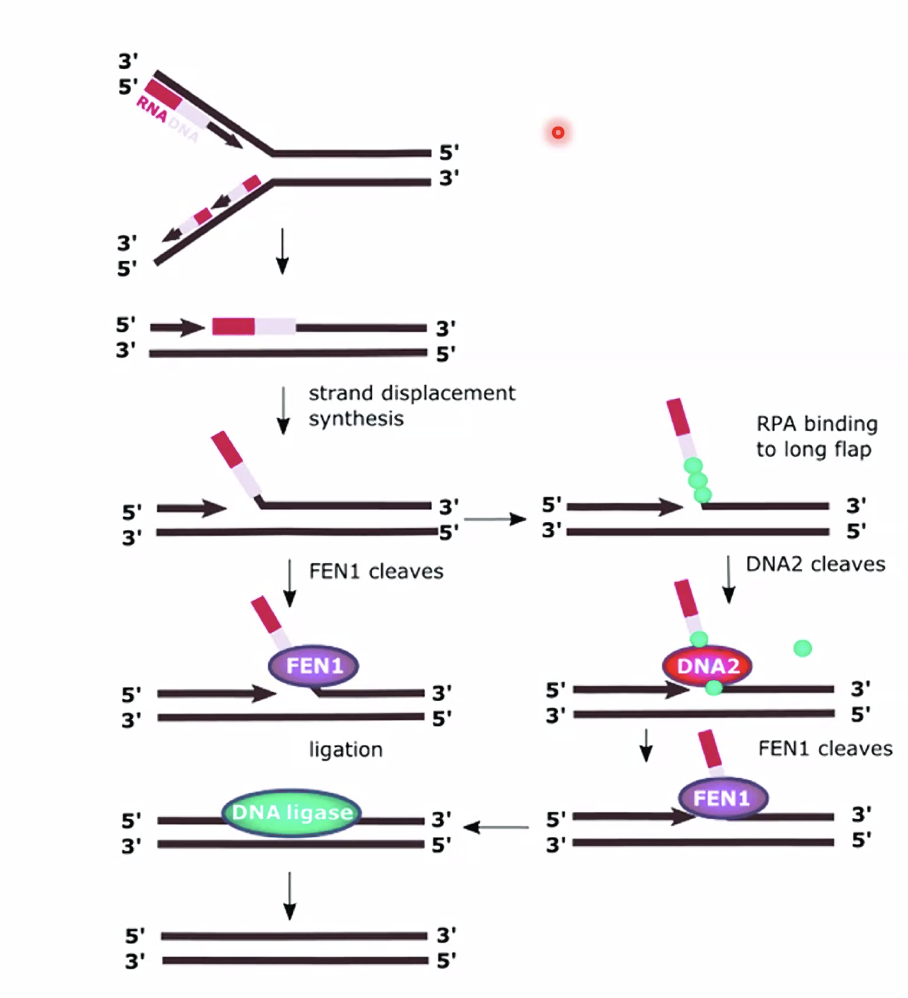
באאוקריוטים, ל־DNA פולימראז δ יש פעילות חלקית של הליקאז, ולכן כאשר הוא מגיע לפריימר של המקטע הבא, הוא דוחף את הפריימר הישן ויוצר Flap - חד־גדיל שמסתדר כלפי חוץ. ה־FEN1 (Flap Endonuclease 1) (וגם DNA2) חותכים את ה־Flap, ואז DNA פולימראז ממלא את הפער, וליגאז סוגר את ה־Nick.
ההבדל:
- בחיידקים - אקסונוקלאז 5’←3’ של Pol I (מפרק את אזור הפריימר)
- באאוקריוטים - אנדונוקלאז (FEN1) שחותך לאחר יצירת Flap (דחיקת האזור על־ידי Pol δ וחיתוך החתיכה החוצה על ידי FEN1, סגירת הניק האחרון על ידי Ligase)
ליגציה ואריזה חזרה לכרומטין
כרומטיניזציה לאחר הרפליקציה
מיד לאחר מעבר מזלג הרפליקציה, ה־DNA החשוף נארז חזרה לכרומטין על־ידי קומפלקס FACT. חלק מההיסטונים ממוחזרים (מהגדיל הישן) וחלק חדשים (שהסינתזה שלהם מוגברת בשלב S). תהליך האריזה מוסיף סמנים אפיגנטיים שמאפשרים להבדיל בין הגדיל הישן לחדש - מידע חיוני למנגנוני תיקון פוסט-רפליקציה (MMR, שיידון בהמשך הקורס).
קוהיזין מתיישב מיד לאחר הרפליקציה על הכרומטידות האחיות ומחזיק אותן יחד עד לאנאפאזה של המיטוזה, שם ספראז מסיר אותו.
טבלת השוואה: פרוקריוטים מול אאוקריוטים
| תכונה | פרוקריוטים (E. coli) | אאוקריוטים (אדם) |
|---|---|---|
| אתרי ראשית הכפלה | 1 | אלפים, לאורך כל הכרומוזומים |
| יריות | מספר פעמים בסייקל | פעם אחת בלבד לכל אתר |
| מיקום | ציטופלזמה | גרעין |
| קצב DNA פולימראז | כ־1,000 בסיסים/שנייה | כ־50 בסיסים/שנייה |
| גודל מקטעי אוקזקי | 1,000–2,000 נ”ק | 100–200 נ”ק |
| החלפת פריימר | Pol I - אקסונוקלאז 5’←3’ | FEN1 - flap endonuclease |
| כרומטין | ללא נוקלאוזומים (בעיקר) | ארוז בנוקלאוזומים |
תהליך מזלג הרפליקציה - סיכום
- ORC נקשר לאתר ראשית הכפלה (AT-rich, nucleosome-free, negative supercoiling).
- ה־ORC גייס MCM (הליקאז), שנשאר לא־פעיל עד שלב S.
- בשלב S, קסקדת פוספורילציות (CDC45, SLD3) מפעילה את ה־MCM, שמתנתק מה־ORC ופותח את הדו־גדיל.
- טופואיזומרז מסיר Positive supercoiling שנוצר מלפני ההליקאז.
- RPA מצפה את ה־DNA החד־גדילי ומונע היסגרות.
- DNA פולימראז אלפא (פרימאז) מסנתז פריימרים (תחילה כ־8–10 ריבונוקלאוטידים (RNA), ואז ממשיך בעוד כ־10–20 דאוקסיריבונוקלאוטידים (DNA) , פידליטי נמוך).
- ה־PCNA (sliding clamp) נועל את ה־DNA פולימראז הרֶפּלִיקָטִיבִי על ה־DNA.
- Pol ε מסנתז את ה־Leading Strand באופן רציף (5’←3’).
- Pol δ מסנתז את ה־lagging Strand במקטעי אוקזקי (100–200 נ”ק באדם), כל אחד לאחר פריימר של Pol α.
- FEN1 מסלקת flaps של פריימרים, Pol δ ממלאת, DNA ליגאז סוגר Nicks
- Pol δ - האנזים שמסנטז את מקטעי האוקזקי
- Ligase - מבצע את הפעולה האחרונה בהכפלת ה־DNA
- מיד לאחר מעבר המזלג - FACT וקומפלקסים נוספים אורזים בחזרה לכרומטין; קוהיזין מחבר את הכרומטידות האחיות.
מחלות Trinucleotide Repeat
מחלות אלה (Trinucleotide Repeat Diseases, TRDs) נגרמות מהתארכות בלתי-נורמלית של רצפים חוזרים בני שלושה נוקלאוטידים בגנום. בכל מחזור רפליקציה, מספר החזרות עשוי לגדול, מה שמוביל לפתולוגיה.
Fragile X (תסמונת X שביר)

מחלה מהשכיחות ביותר לפיגור שכלי, מופיעה בסל הבדיקות של משרד הבריאות בישראל. המאפיינים:
- רצף חוזר: CGG
- מיקום החזרה: בפרומוטור של הגן FMR1 (הגן המעורב במחלה)
- מצב תקין: בערך עד 50–70 חזרות
- מצב נשאות (premutation): מאות שאינן גורמות למחלה אך מתארכות בכל דור
- מצב פתולוגי: מעל 200 חזרות CGG ← היפרמתילציה של הפרומוטור (CpG islands) ← השתקת הגן ← לא מתקבל חלבון FMR1 ← הגן חיוני להתפתחות מוחית עוברית ← פיגור שכלי קשה
מנגנון המתילציה: CG/CpG הם האות לאנזימי המתילציה. כאשר יש יותר מ־200 חזרות, ריכוז ה־CpG גדול מאוד והאזור הופך להיות hypermethylated ומושתק.
הנטינגטון (Huntington’s Disease)
- רצף חוזר: CAG (מקודד לגלוטמין)
- מיקום: בתוך האזור המקודד של הגן
- עודף חזרות CAG יוצר שרשרת פוליגלוטמין ארוכה בחלבון הנטינגטין ← קיפול לקוי, אגרגציה של חלבונים ← חוסר בחלבון פונקציונלי ← מחלה ניוונית עצבית ושרירית עם הופעה מאוחרת.
מיוטוניה דיסטרופית (Myotonic Dystrophy)
- רצף חוזר: CTG
- מנגנון: החזרות משפיעות על Alternative Splicing של ה־RNA ← פגיעה בתפקוד שרירי.
מנגנון ההתארכות - Slippage
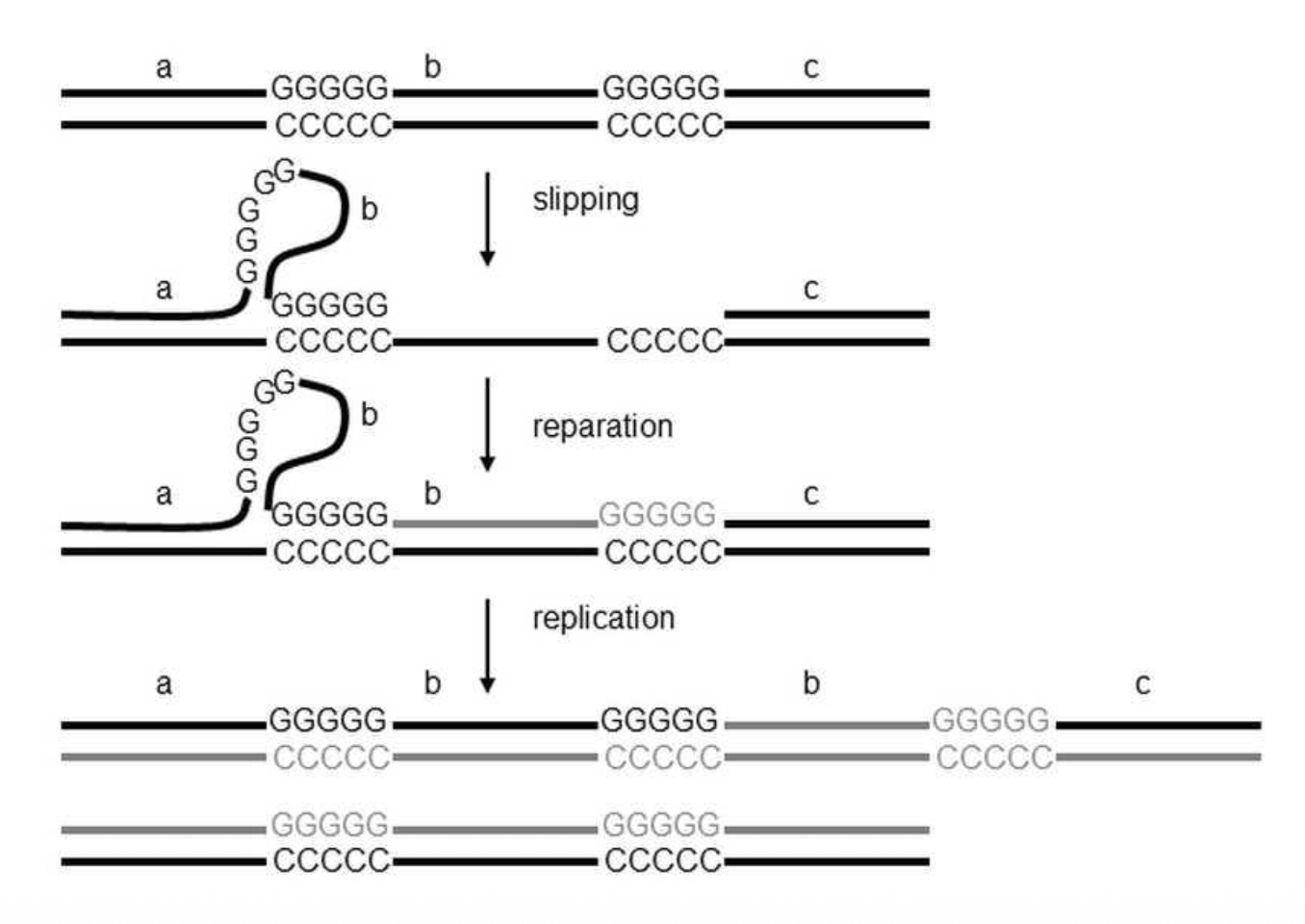
כאשר ה־DNA נפרם ונוצר אזור חד־גדילי, רצפים חוזרניים עלולים להתקפל על עצמם וליצור מבנה של גבעול־לולאה (stem-loop/hairpin).
במצב כזה יכולים לקרות שני דברים:
- אם ה־DNA פולימראז מדלג על הלולאה, מתקבלת התקצרות של הרצף.
- אם ה־DNA פולימראז מחליק לאחור ומסנתז שוב חלק מן הרצף, מתקבלת התארכות של הרצף (expansion).
תהליך זה, הנקרא slippage, שכיח במיוחד בנשאיות של premutation, ועלול לגרום להתארכות הדרגתית של הרצף מדור לדור, עד לחציית הסף הפתולוגי.
דור פסקל