נושאים:
- חזרה
- מסלול Wnt
- BMP Signaling - TGF-β Superfamily
- Rspondin (RSPO) - חלבון שמגביר Wnt ומעכב BMP
- FGF Signaling - RTK superfamily
- Cross-talk בין מסלולים - FGF ו־Wnt דרך E-cadherin
- לקראת השיעור הבא - Sonic Hedgehog (Shh)
חזרה
בשיעור הקודם למדנו עקרונות כלליים של התפתחות עוברית, ובמרכזם - תאים אמבריוניים מדברים אחד עם השני ובעקבות זאת מאפשרים תהליכים התפתחותיים. דיברנו על חמישה מסלולים עיקריים (בפועל קיימים יותר) שהם השפה המולקולרית שבה תאים עובריים מתקשרים:
WntBMP(TGF-β superfamily)FGF(RTK superfamily)- Shh
- Notch
מסלול Wnt
ייצור והפרשה של Wnt Ligand
O-acylation - תוספת חומצת שומן
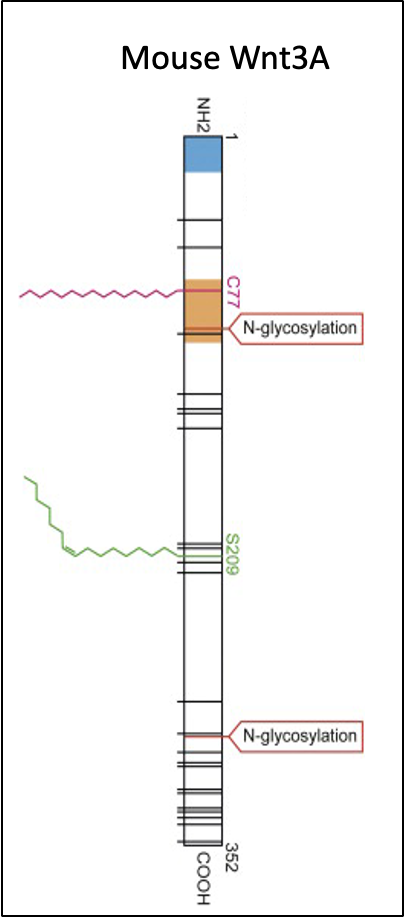
כמעט בכל Wnt ligand יש סרין במיקום מסוים שעליו מתרחש תהליך של O-acylation: הוספת חומצת שומן מסוג חומצה פלמיטית (Palmitic acid), באמצעות הקבוצה הקרבוקסילית שלה, על הידרוקסיל של הסרין. במקרה של Wnt3A זה סרין 209.
את ה־O-acylation מבצע האנזים Porcupine (PORCN), שנמצא תמיד ב־ER - אנזים גדול וטרנס־ממברנלי שחוצה את ממברנת ה־ER מספר פעמים.
התוספת הזאת חיונית לשני דברים:
- הפרשת הליגנד מהתא
- קישור הליגנד לרצפטור
Frizzled(כי ב־Frizzledיש כיס ייחודי שחומצת השומן נכנסת לתוכו - בלי זה אין סיגנלינג)
בנוסף לכך, לאחר ה־O-acylation יכול להתרחש גם S-acylation (תוספת פלמיטט על ציסטאין) - תהליך פחות חיוני שלא מתרחש בכל Wnt.
מסע הליגנד מה־ER ועד להפרשה
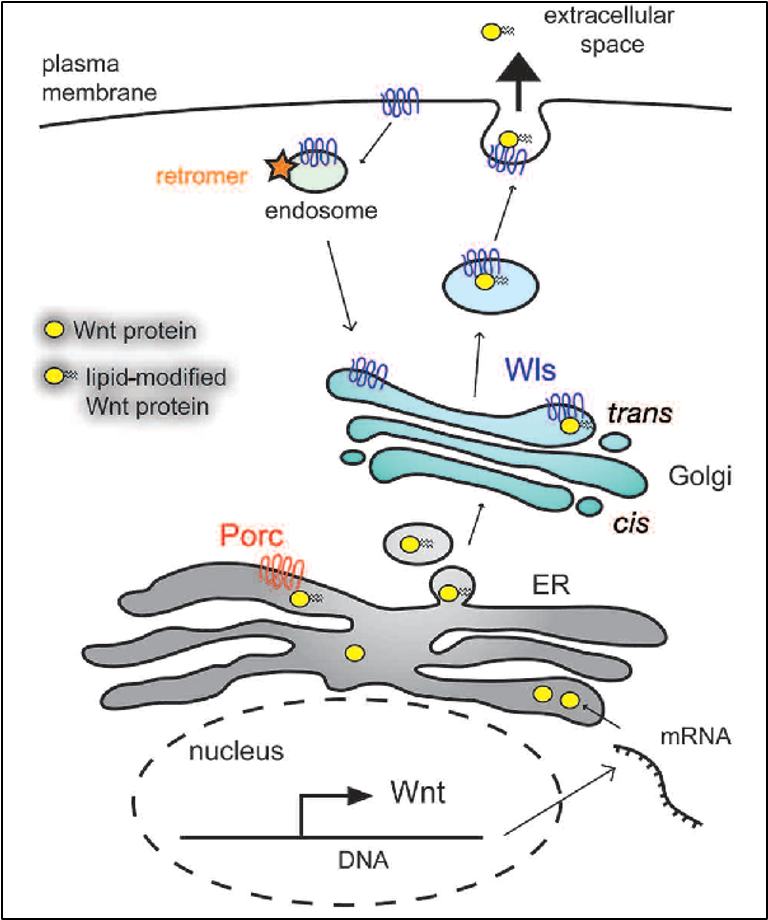
- ה־DNA מתועתק ל־mRNA שיוצא מהגרעין
- mRNA מתיישב על ריבוזומים שיושבים על ה־ER; סינתזת
Wntנעשית אל תוך ה־ER - Porcupine מבצע O-acylation ב־ER
Wnt ligandעובר לגולג’י- בגולג’י מחכה
Wntless(Wls) - חלבון טרנס־ממברנלי שיושב בממברנת הגולג’י, והכרחי הן להעברת ה־Wntמהגולג’י אל הממברנה, והן לשחרור הליגנד לחלל הבין־תאי. Wls גם מגיש את הליגנד לחלבונים שיסייעו לו לנדוד.
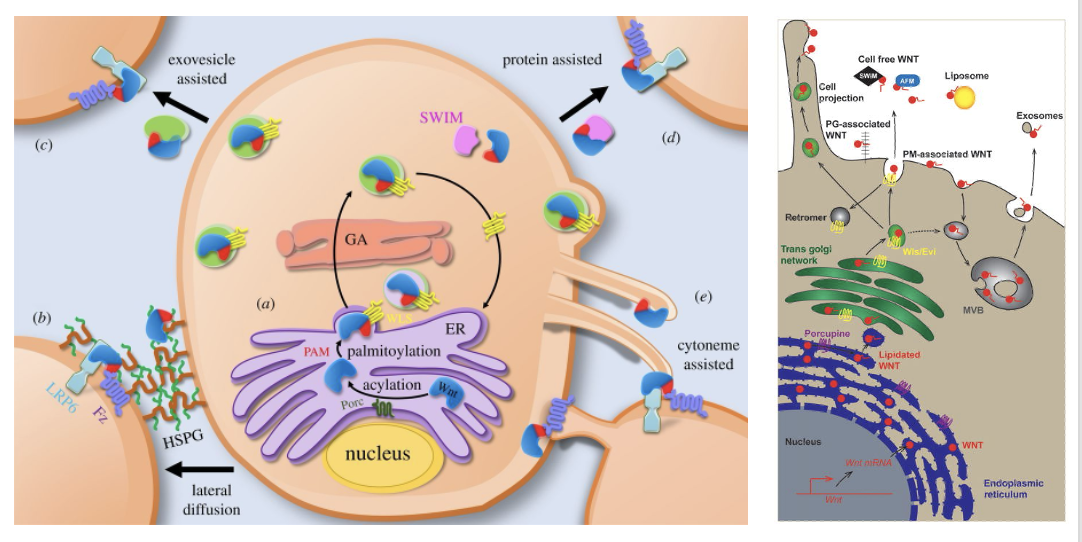
הדרכים לתנועת Wnt Ligand בין תאים
הבעיה המרכזית: מכיוון שיש על הליגנד חומצת שומן, הוא לא מסיס ואינו יכול פשוט לעבור דיפוזיה. נדרש מנגנון שיאפשר לו להגיע לתא המטרה.
דרך 1 - קישור ל־sFRP
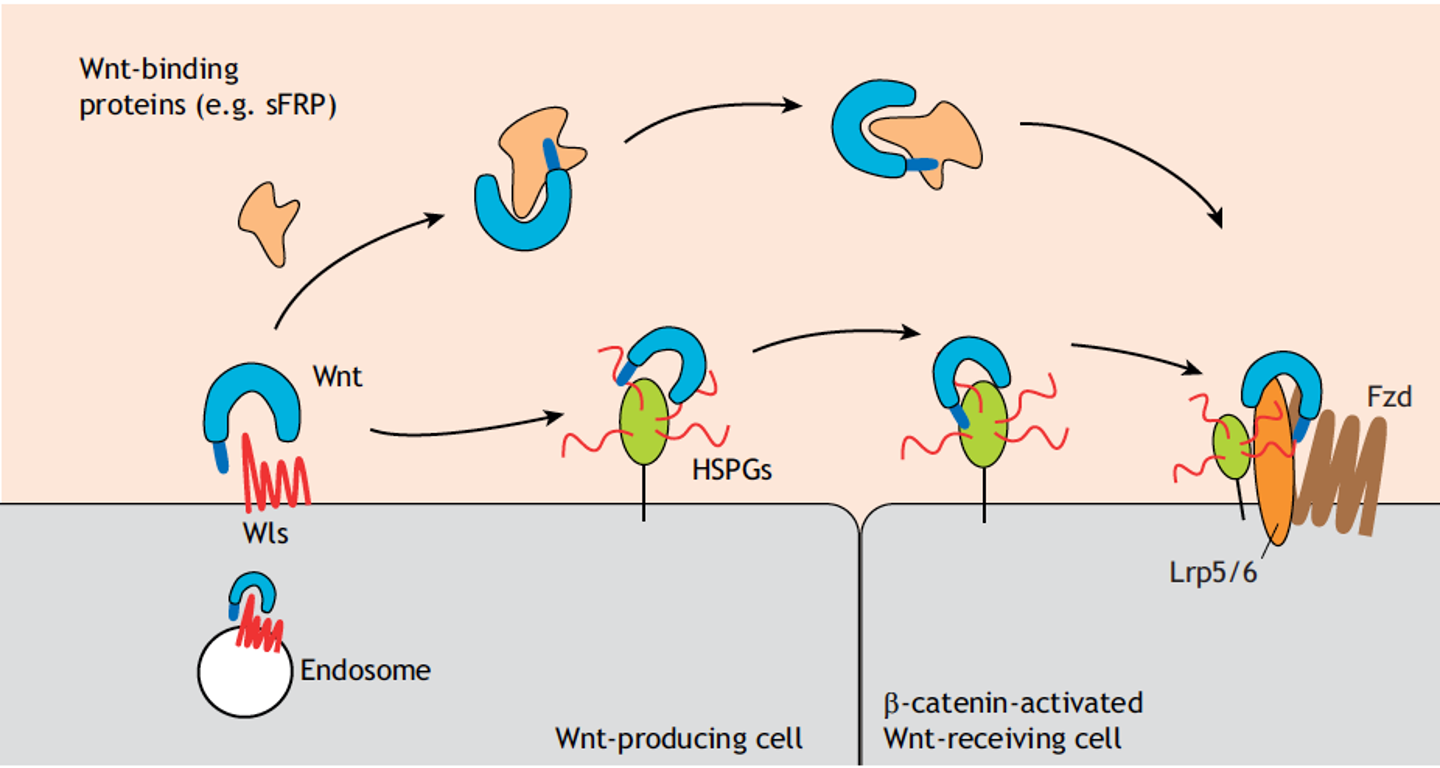
sFRP (Secreted Frizzled-Related Proteins) - חלבונים מופרשים שמכילים דומיין דמוי Frizzled ולכן יכולים לקשור Wnt. ב־sFRP יש “כיסים” שבתוכם חומצת השומן יכולה להיקשר באפיניות נמוכה יחסית.
Wls מגיש את ה־Wnt ל־sFRP ונוצר קומפלקס של sFRP + Wnt Ligand, שיכול כעת לעבור דיפוזיה, להתרחק מהתא המייצר ולהגיע לתא המטרה - כי ה־sFRP “מסתיר” את חומצת השומן.
באזור תא המטרה ה־sFRP מתנתק מהליגנד (לפי $K_D$, כמו כל אינטראקציה יש association ו־dissociation), ואז Wnt חופשי יכול להיקשר ל־Frizzled ולהפעיל את המסלול.
שימו לב: sFRP שנחשב “אינהיביטור” של
Wnt, משמש כאן דווקא כפרומוטור - הוא מאפשר לליגנד להתרחק מהתא ולהגיע ליעד.
דרך 2 - קישור ל־HSPGs
Wls יכול גם לשחרר את Wnt ישירות לחלל הבין־תאי. שם, HSPG (Heparan Sulfate Proteoglycans) - חלבונים עם שרשראות סוכר - יכולים לקשור את Wnt, שנודד לאורך “יער” ה־HSPGs ומגיע לתא המטרה.
דרך 3 - ליגנד קשור לממברנה
Wls יכול לשחרר את ה־Wnt ligand אל תוך ממברנת התא המייצר - הליגנד “תקוע” בממברנה בזכות חומצת השומן. במצב הזה:
- אין דיפוזיה מעבר לדיפוזיה פנימית בממברנה
- אך אם תא אחר נמצא ממש סמוך (מגע ממברנה־ממברנה),
Wntיכול להיקשר ל־Frizzledשלו - נדרש מנגנון שמוציא את חומצת השומן מהממברנה ומשבץ אותה לתוך כיס ה־
Frizzled
זאת דרך שהיא אפשרית אך לא נפוצה - מחייבת קרבה פיזיקלית מאוד גדולה.
דרך 4 - אקסוזומים
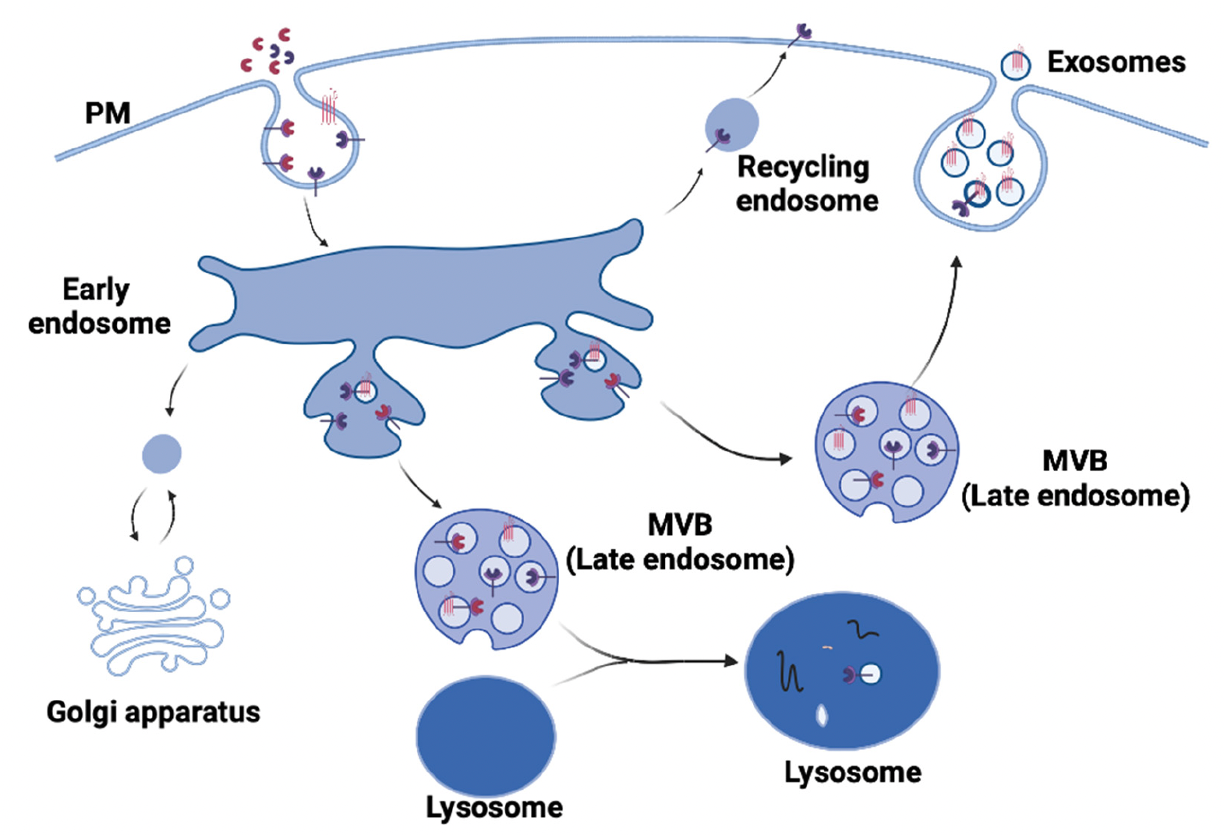
אקסוזומים הם וסיקולות (בועיות) קטנות שתאים מפרישים החוצה. על גבי האקסוזומים יכול לשבת Wnt ligand (עם Wls), ובדרך זו הוא יכול להגיע לתא המטרה.
איך נוצרים אקסוזומים:
בדרך כלל, כשחלבון טרנס־ממברנלי שאיבד את הפונקציה שלו נכנס לאנדוזום, הוא לא יכול להתפרק ישירות על ידי הליזוזום (כי הוא קשור לממברנה ומוגן). הדרך לטפל בו היא ליצור וסיקולות פנימיות בתוך האנדוזום - זה יוצר MVB (Multivesicular Body).
- הנתיב הרגיל: MVB ← איחוי עם ליזוזום ← כל הווסיקולות הפנימיות מתפרקות.
- הנתיב האחר (שיוצר אקסוזומים): MVB ← איחוי עם ממברנת התא ← כל הווסיקולות הפנימיות מופרשות החוצה - כל וסיקולה כזו שמופרשת היא אקסוזום.
שימו לב לאוריינטציה: מה שהיה בפנים (צד ציטופלסמי) הופך עכשיו לצד חיצוני.
אם מביאים אל תוך האנדוזום את ה־Wnt ligand עם Wls, ניתן ליצור אקסוזומים שהליגנד יושב עליהם. האקסוזומים “מסתירים” את חומצת השומן ומאפשרים לליגנד לנדוד אל תא המטרה.
האקסוזומים נוצרים על ידי מנגנון ESCRT - שונה במהותו מתהליך האנדוציטוזה הקלאסי שתלוי בקלתרין.
דרך 5 - סייטונים (Cytonemes)
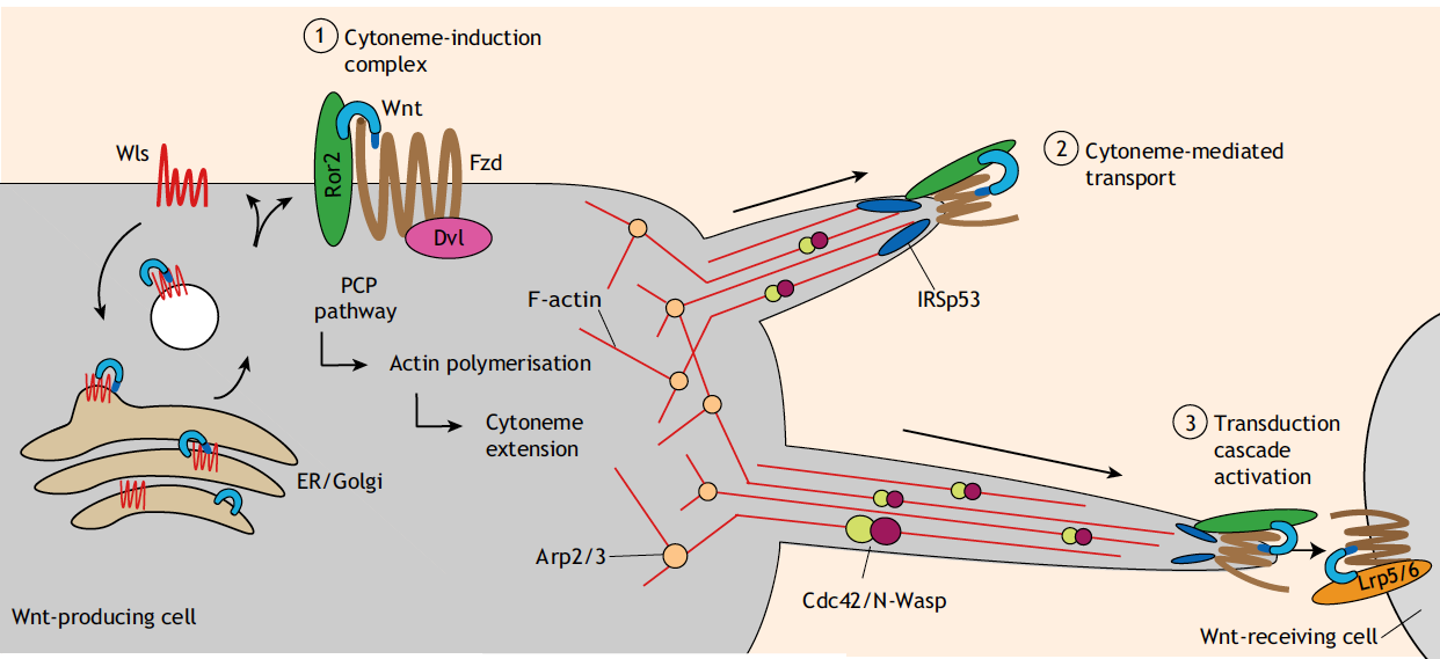
סייטונים הם שלוחות ארוכות של ממברנה שתאים יוצרים כדי לתקשר עם תאים רחוקים יותר. על קצה הסייטון יושבים Frizzled ו־Ror2 (קו־רצפטור לא־קנוני) עם Wnt ligand.
התא המייצר מפעיל Wnt לא־קנוני (ריאורגניזציה של ציטוסקלטון האקטין) שיוצר פילמנטי אקטין שדוחפים את הממברנה ומאריכים את הסייטון. הסייטון גדל ומגיע עד לתא המטרה, שם יש Frizzled + LRP5/6 (קו־רצפטורים לקנוני). מתרחש מעבר הליגנד מה־Frizzled + Ror2 (לא־קנוני) ל־Frizzled + LRP5/6 (קנוני) - וכך Wnt לא־קנוני מפעיל Wnt קנוני בתא המטרה.
סיכום - דרכי ההפרשה
| דרך | מנגנון |
|---|---|
| sFRP | ליגנד + sFRP נודדים יחד כקומפלקס |
| HSPG | ליגנד נודד לאורך שרשראות הסוכר |
| ממברנה | ליגנד קשור לממברנה, מגיע לתאים סמוכים |
| אקסוזומים | ליגנד על וסיקולות מופרשות |
| סייטונים | שלוחות ממברנה ארוכות |
הבחנה: Wnt קנוני לעומת לא־קנוני
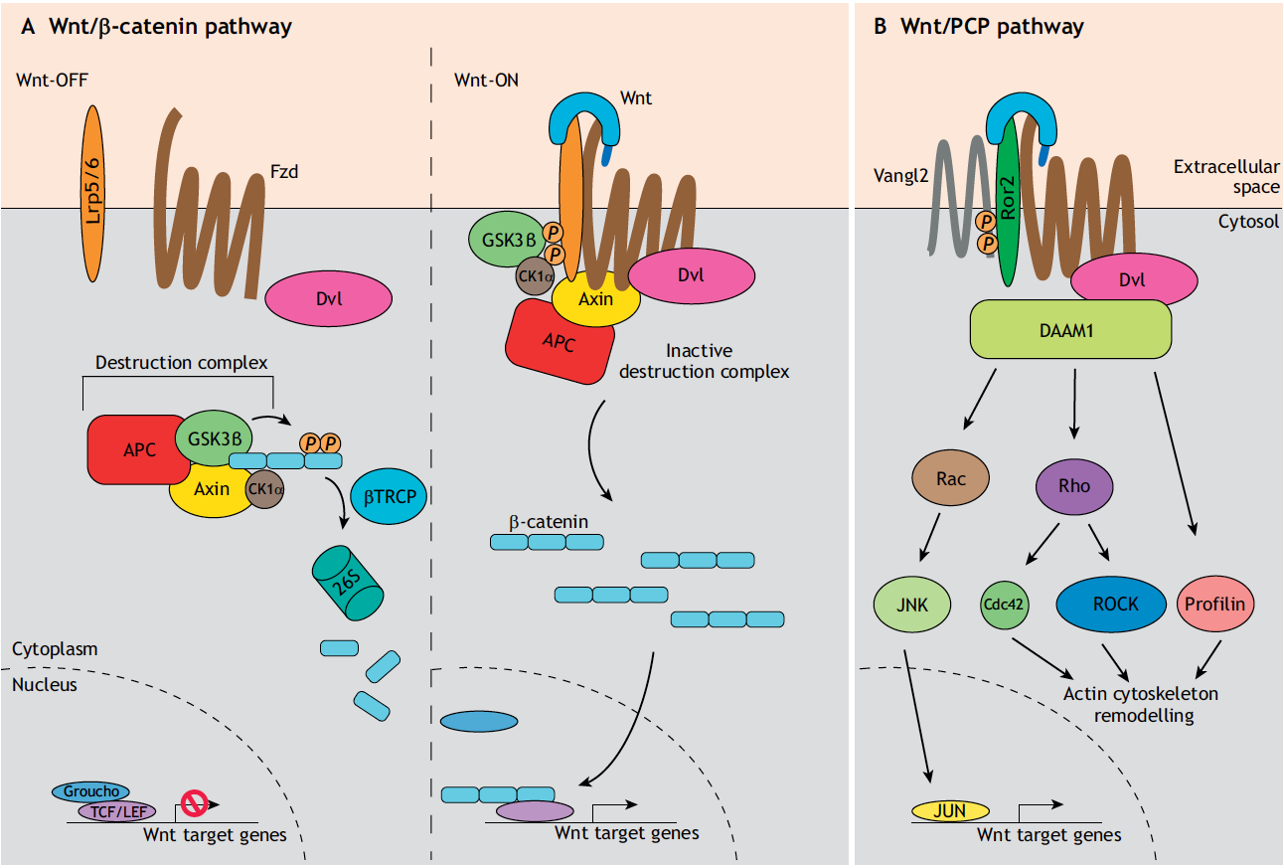
| קנוני | לא־קנוני | |
|---|---|---|
| קו־רצפטור | LRP5/6 | Ror2 / Ryk |
| Destruction complex | כן - מרכזי | לא - לא מעורב |
| יעד מרכזי | β-catenin | ציטוסקלטון אקטין |
תלות ב־β-catenin | כן β-catenin dependent | לא β-catenin independent |
הלא־קנוני חשוב מאוד בהתפתחות: ניידות תאים בעובר, תנועה ממקום למקום, חיבור לתאים אחרים - כל אלה דורשים שליטה בציטוסקלטון. אי אפשר לעשות תנועה בלי לשלוט בציטוסקלטון.
BMP Signaling - TGF-β Superfamily
TGF-β - העץ הפילוגנטי
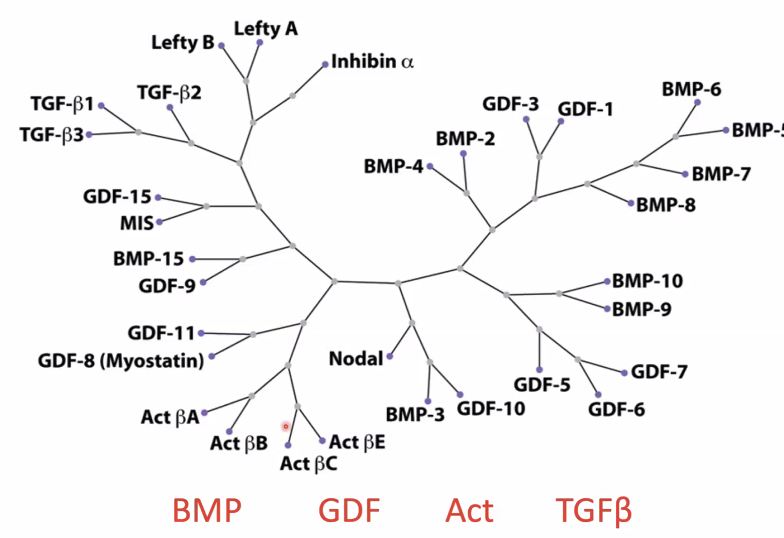
TGF-β Superfamily כוללת ארבע תת־משפחות עיקריות:
BMP- קבוצה גדולה מאוד- GDF - קבוצה גדולה
- Activins - קבוצה קטנה יחסית
- TGF-β - רק שלושה ליגנדים
שלושה חלבונים ייחודיים הם מעכבים (Inhibitors): Nodal, Lefty1 (Lefty A), ו־Lefty2 (Lefty B) - כשהם נקשרים לרצפטור הם מונעים העברת אותות (בניגוד לשאר, שמפעילים).
המסלול הגנרי של BMP
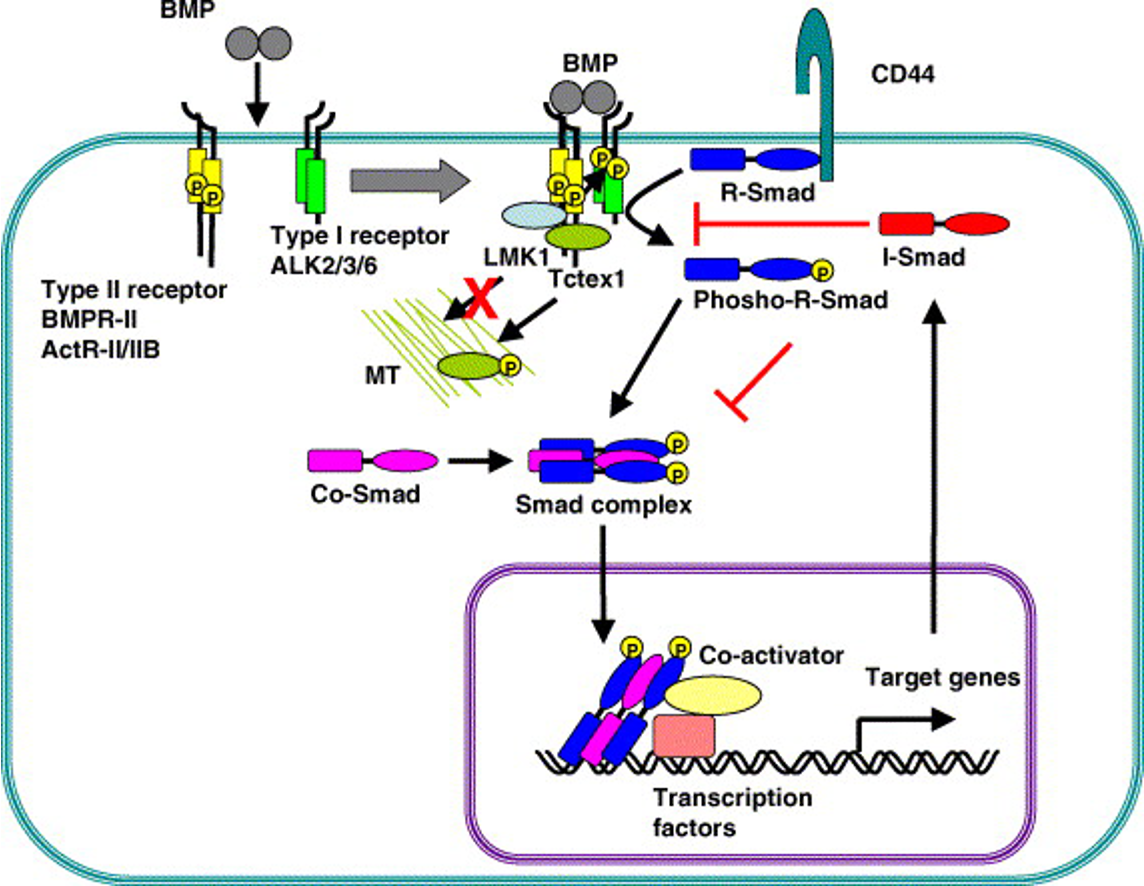
הליגנד BMP הוא דימר (בניגוד ל־Wnt שהוא מונומר).
שני סוגי רצפטורים, גם הם דימרים:
- רצפטור
Type II- קינאז פעיל קונסטיטוטיבי אך מאוד חלש. לא יכול לפעול לבד, צריך קרבה פיזיקלית. - רצפטור
Type I- קינאז לא פעיל כשלעצמו; מופעל על ידיType II.
ללא ליגנד: Type II ו־Type I קיימים כדימרים נפרדים. Type II עושה אוטו־פוספורילציה קונסטיטוטיבית אחד על השני, אך ללא השפעה.
עם ליגנד (BMP): הדימר של BMP מחבר בין Type II לבין Type I, ומביא את Type II לקרבה פיזיקלית מספקת כדי לבצע פוספורילציה על הקינאז דומיין של Type I - זה מאקטב את Type I.
Type I המאוקטב מגייס R-Smad מהציטוזול ועושה עליו פוספורילציה.
התוצאה: R-Smad מאוקטב נקשר לR-Smad נוסף ולCo-Smad (Smad4). הקומפלקס השלישוני נכנס לגרעין, נקשר לפרומוטורים מתאימים ומפעיל טרנסקריפציה של גני מטרה של BMP.
שים לב: לרצפטורים יש פעילות קינאז על סרין ותרואנין - בניגוד ל־
FGFשעושה פוספורילציה על טירוזין.
הבדלים בין תת־המשפחות - R-Smads שונים
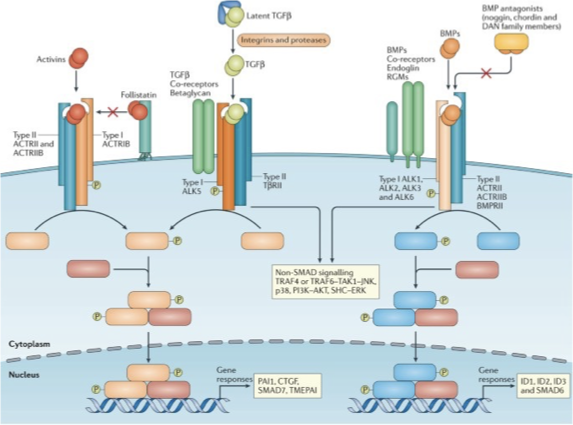
זה הניואנס המרכזי שמסביר למה יש כל כך הרבה ליגנדים שונים:
| ליגנד | קינאז Type I | R-Smads שמופעלים |
|---|---|---|
BMP / GDF | BMPR1 | Smad 1, 5, 8 (אחד מהם או שילובים) |
| Activins / TGF-β | ActR1B / TGF-βR1 | Smad 2, 3 |
מה שמשותף לכולם: Co-Smad = Smad4
לא מדובר באותם גנים שמשופעלים - Smad1/5/8 לעומת Smad2/3 מפעילים גנים שונים. וזאת בדיוק הנקודה: שפה עשירה שמאפשרת תוצאות מגוונות.
הרצפטורים ספציפיים לליגנד - רצפטורי
BMPלא קושרים TGF-β ולהפך.
ביוסינתזה של ליגנדים - TGF-β Superfamily
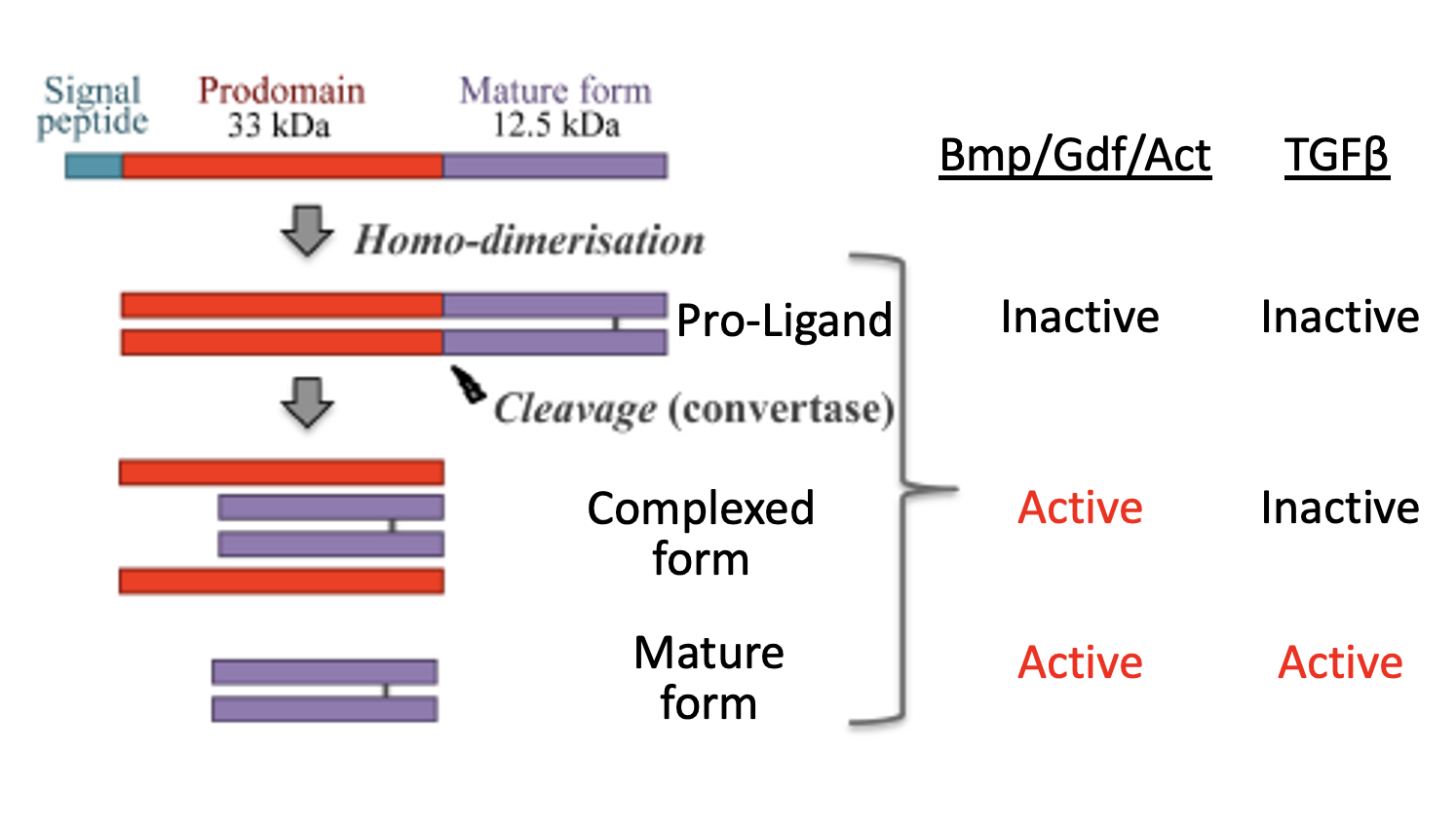
כל הליגנדים של TGF-β Superfamily נוצרים באותה שיטה:
- נוצר מונומר לא־פעיל עם Signal Peptide, Pro-domain (לא פעיל) ו־Mature domain (האזור הפעיל).
- המונומר עובר הומו־דימריזציה - אינטראקציה גם לא־קוולנטית וגם קוולנטית (קשר די-סולפידי באזור הפעיל). לדימר שנוצר קוראים Pro-Ligand.
- ביקוע ב־ER על ידי Convertase בין ה־Pro-domain לבין ה־Mature domain.
התוצאה: Complex Form - שני הדימרים הפעילים קשורים בקשר די-סולפידי, והפרו־דומיין עדיין קשור לא־קוולנטית למולקולה הפעילה.
פעילות ה־Complex Form:
BMP, GDF, Activins← Complex Form פעיל - יכול לקשור רצפטור ולהפעיל מסלול.TGF-β← Complex Form לא פעיל - מופרש תמיד בצורה הסגורה שלו.
Mature Form (הצורה הבוגרת): כאשר הפרו־דומיין מתנתק לגמרי מהאזור הפעיל, מתקבלת הצורה הבוגרת - פעילה בכל הליגנדים, כולל TGF-β.
V-Shape לעומת Closed-Shape
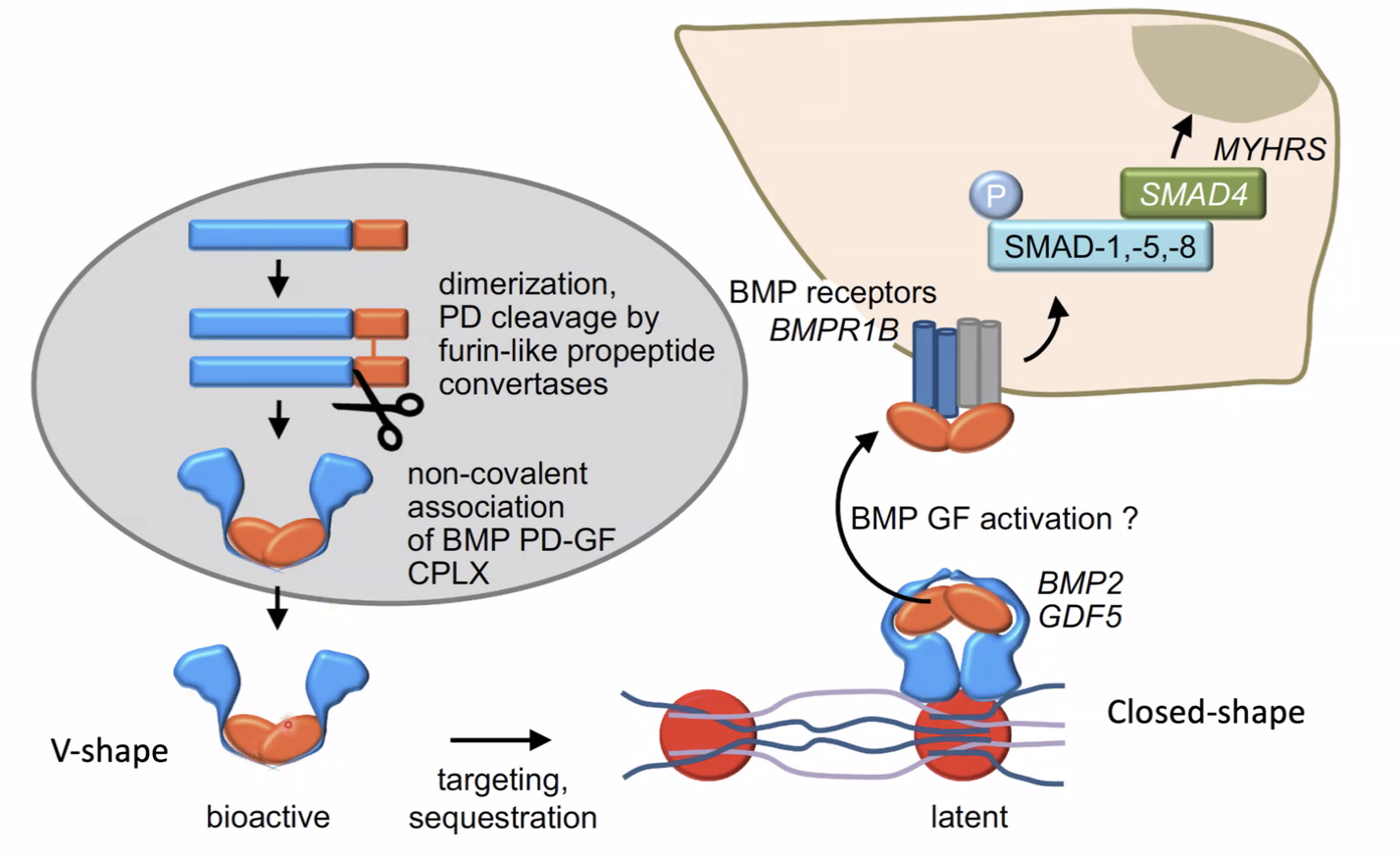
ה־Complex Form יכול להיות בשני מצבים:
- V-Shape (Open) - צורה פעילה; ה־
BMPיכול לקשור רצפטור - Closed-Shape - חלבון מה־Extracellular Matrix (ECM) נקשר ל־V-Shape וסוגר אותו; לא פעיל
כדי לשחרר ולהפעיל Closed-Shape נדרש פרוטאז שמבצע ביקוע פרוטאוליטי ומשחרר את הדימר הפעיל - שיכול כעת לקשור רצפטור.
חשיבות המצב הסגור: TGF-β מופרש מלכתחילה בצורה סגורה ויכול להיות מאוחסן ב־ECM לאורך זמן. כשמגיעים תאים חדשים ויש פרוטאז בסביבה, ה־TGF-β משתחרר ופעיל. התא שייצר את הליגנד יכול כבר להיעלם - הליגנד “מדבר עם העתיד”; תא אחר יכול להפעיל מערכת שנוצרה בעבר. זה נורא חשוב בתהליכים התפתחותיים.
מעכבים של BMP
בדומה ל־Wnt, גם ל־BMP יש מעכבים מופרשים רבים:
Noggin- נגדBMP2,BMP7Gremlin- נגד GDFChordin- נגדBMP2Follistatin,Twisted Gastrulation, Cross-Veinless 2 - ועוד
כולם עובדים באותו עיקרון: נקשרים ל־BMP ומונעים ממנו להיקשר לרצפטור.
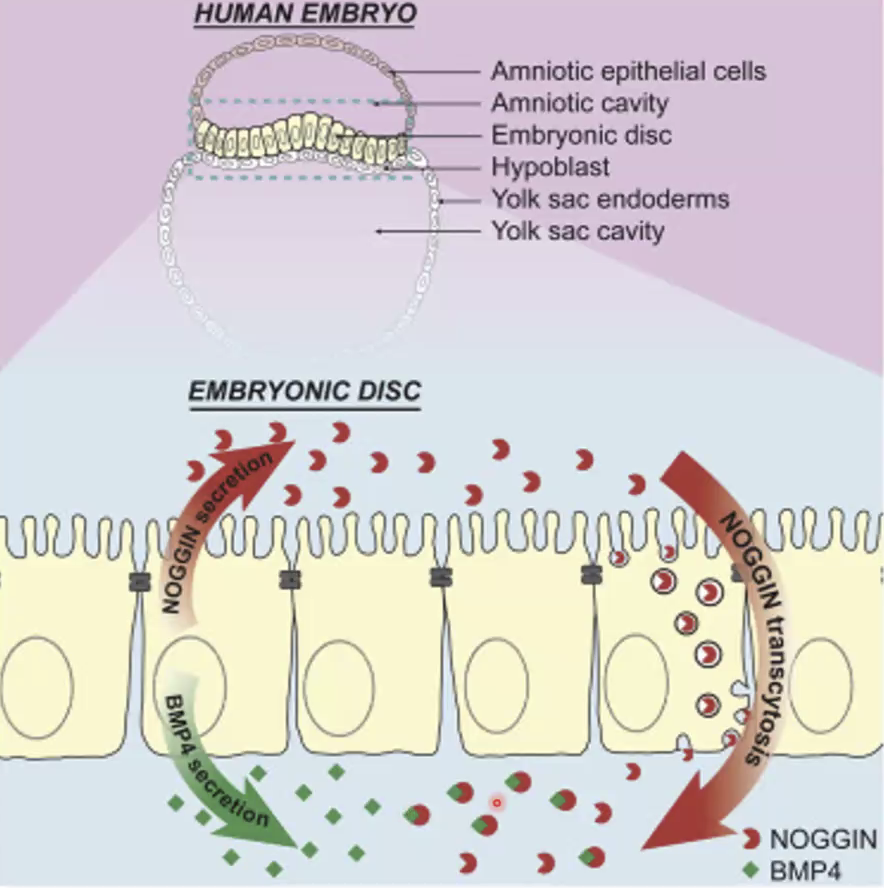
דוגמה קלינית חשובה - גרדיאנט של BMP ב־Epithelium:
אותו תא מייצר גם BMP4 וגם Noggin, אבל לא לאותו צד:
BMP4מופרש לצד הבזליNogginמופרש לצד האפיקלי
תא מסוים אחר לוקח את ה־Noggin, עושה לו Transcytosis (העברה בווסיקולות מצד אחד לצד השני) ומשחרר אותו בצד אחר. בצורה הזאת נוצר גרדיאנט מבוקר של BMP. אם הייתה הפרשה של BMP ו־Noggin לאותו צד מיידית - הכל היה נחסם ולא היה גרדיאנט. זו דרך טובה לקבוע ולשלוט בגרדיאנט ובתלילות שלו.
I-Smads - מעכבים פנימיים
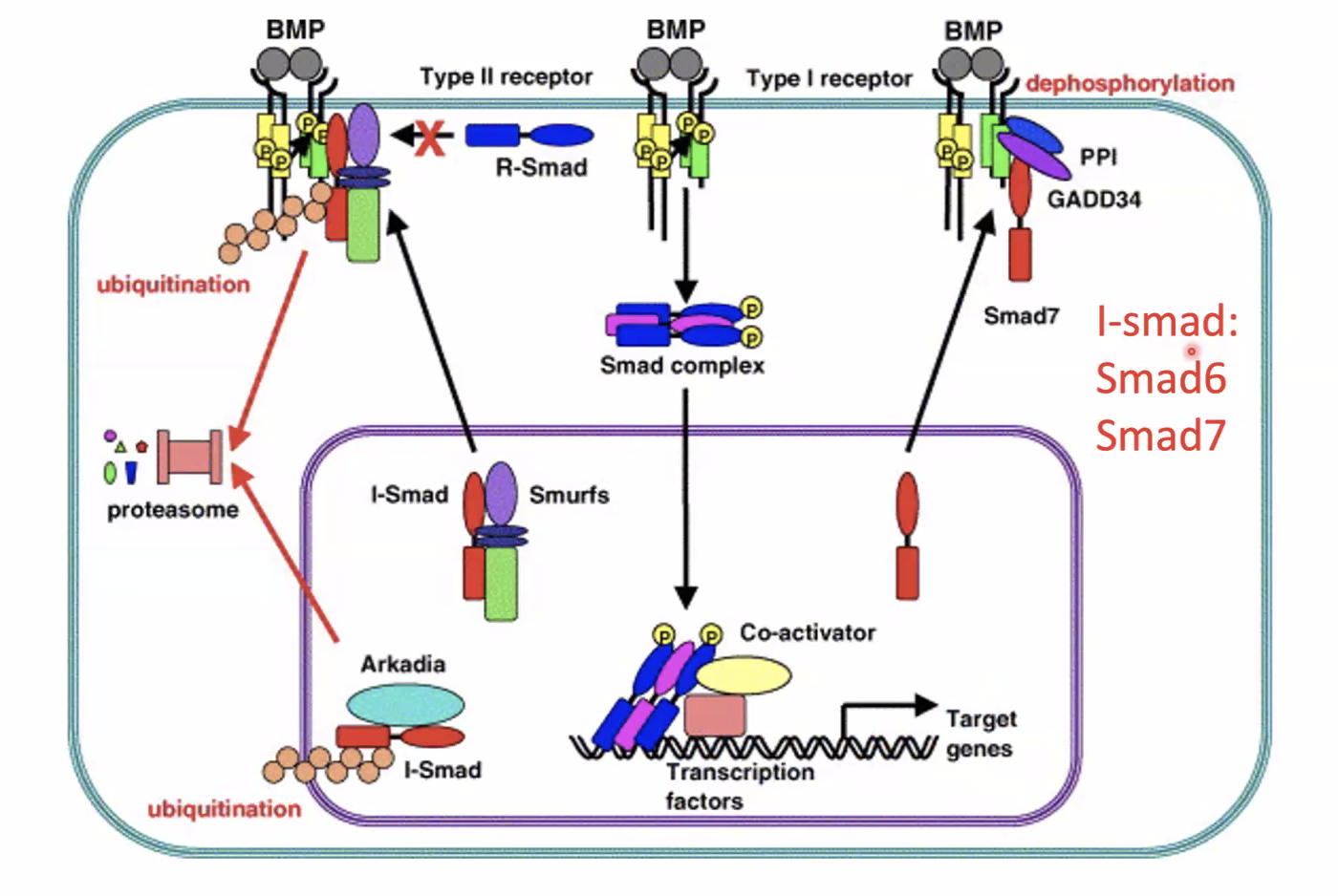
בנוסף למעכבים המופרשים, יש מעכבים פנימיים (Endogenous Inhibitors) - חלק ממשפחת ה־Smad אך פועלים הפוך:
I-Smad6 ו־I-Smad7 נקשרים לרצפטור Type I ומגייסים אליו פוספטאזות (שמורידות פוספט) - מה שמונע מ־Type I לפעול. בנוסף לכך, I-Smad7 יכול לגייס Smurf (E3 Ubiquitin Ligases) שעושים פולי-יוביקוויטינציה לרצפטור Type II ← דגרדציה של הרצפטור מהממברנה.
Rspondin (RSPO) - חלבון שמגביר Wnt ומעכב BMP
Rspondin הוא חלבון שמסוגל להשפיע על שני מסלולי איתות שונים: מצד אחד הוא מחזק את מסלול Wnt, ומצד שני הוא מעכב את מסלול BMP.
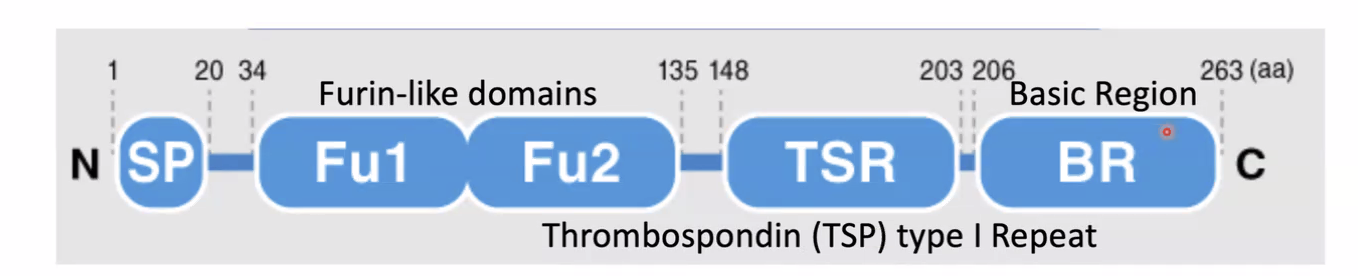
ל־Rspondin יש כמה דומיינים עיקריים:
- Signal Peptide
- Furin-like domain 1 (FU1)
- Furin-like domain 2 (FU2)
- Thrombospondin type 1 repeat (TSP)
- C-terminal
איך Rspondin מחזק את Wnt signaling
כפי שראינו בשיעור הקודם, החלבונים RNF43 ו־ZNRF3 הם E3 ubiquitin ligases טרנסממברנליים. התפקיד שלהם הוא לבצע יוביקוויטינציה ל־Frizzled, וכך לגרום ל־internalization ולדגרדציה שלו. כאשר Frizzled מתפרק, האיתות של Wnt נחלש.
כאשר יש Rspondin:
- הדומיין FU1 נקשר ל־RNF43/ZNRF3
- הדומיין FU2 נקשר לרצפטור LGR
הקישור הזה מעכב את פעילות ה־E3 ubiquitin ligases. כתוצאה מכך Frizzled לא עובר דגרדציה, מצטבר על פני התא, ויכולת התגובה ל־Wnt גדלה.
כלומר: Rspondin מגביר Wnt signaling בכך שהוא מונע את פירוק Frizzled.
איך Rspondin מעכב BMP signaling
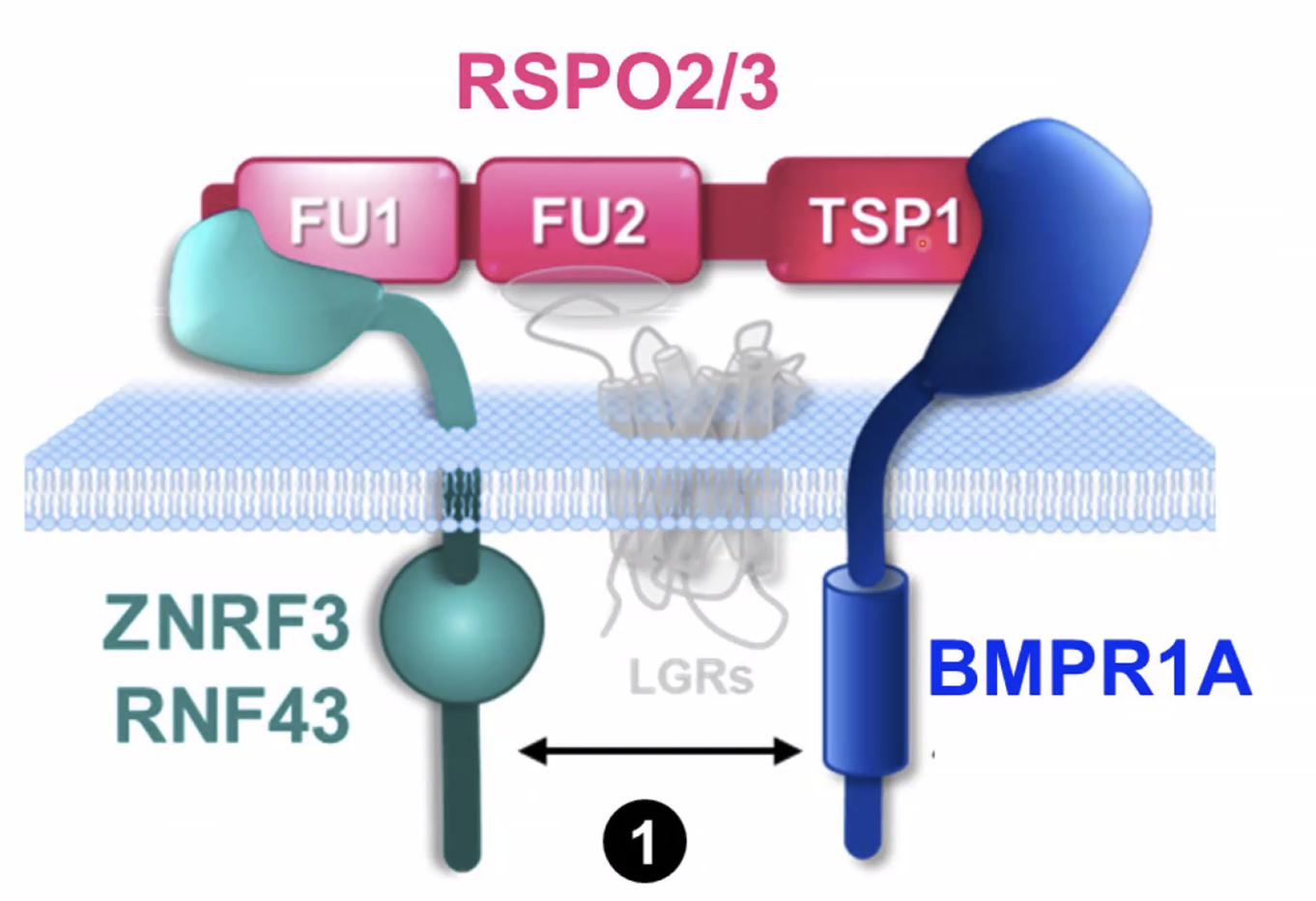
במצב אחר, כאשר אין LGR בסביבה, אבל יש BMP Receptor 1A, אותה מולקולת Rspondin יכולה לפעול אחרת.
במצב הזה:
- הדומיין FU1 עדיין נקשר ל־E3 ubiquitin ligases
- הדומיין TSP נקשר ל־BMP Receptor 1A
כך נוצר קומפלקס שמקרב בין ה־E3 ubiquitin ligase לבין רצפטור BMP. במצב הזה ה־ligases כבר לא מעוכבים, אלא משנים את יעד הפעולה שלהם ופועלים על BMP receptor.
התוצאה היא יוביקוויטינציה של BMP receptor, שמובילה לדגרדציה של הרצפטור ולירידה ב־BMP signaling.
הרעיון המרכזי
היופי ב־Rspondin הוא שאותה מולקולה יכולה לבצע שתי פעולות שונות:
- להגביר Wnt signaling על ידי מניעת דגרדציה של Frizzled
- לעכב BMP signaling על ידי קידום דגרדציה של BMP receptor
בשני המקרים המנגנון קשור ליוביקוויטינציה, אבל הכיוון שונה:
- ב־
Wnt: Rspondin מעכב את פעילות ה־ligases על Frizzled - ב־
BMP: Rspondin מכוון את פעילות ה־ligases אל BMP receptor
FGF Signaling - RTK superfamily
RTK Receptor - Tyrosine Kinases
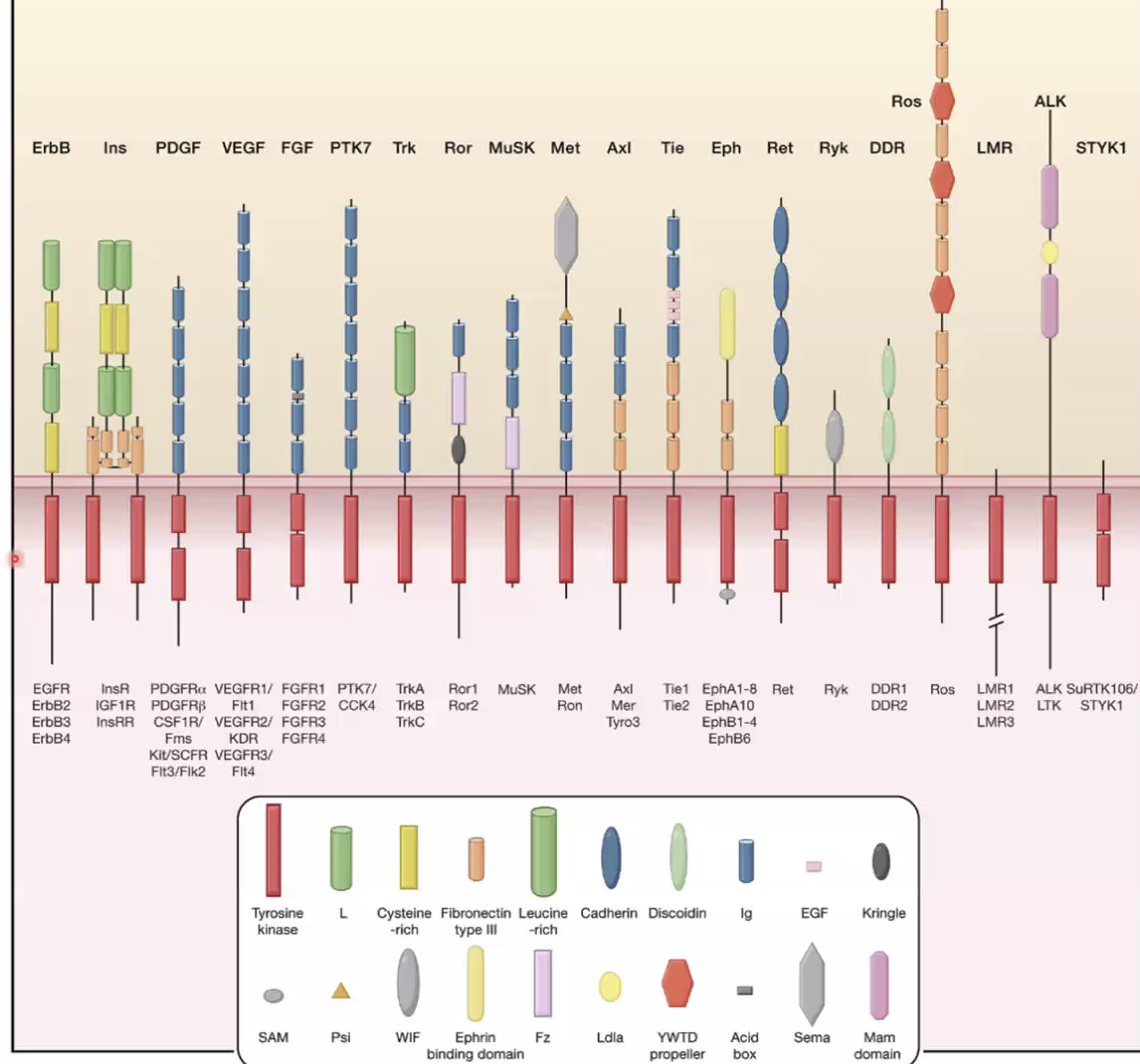
RTK (Receptor Tyrosine Kinase) היא משפחה גדולה מאוד של רצפטורים. מה שמשותף לכולם:
- חוצים את הממברנה פעם אחת
- בצד התוך־תאי (Intercellular): דומיין קינאז שיודע לעשות פוספורילציה על טירוזין (חומצת אמינו)
- ללא ליגנד: הקינאז לא פעיל
מה שמבדיל בין RTKs שונים הוא האזור החוץ־תאי - הוא מקנה את הספציפיות לליגנד השונה.
נתמקד בתת־משפחה FGF (Fibroblast Growth Factor).
FGF Receptor (FGFR)
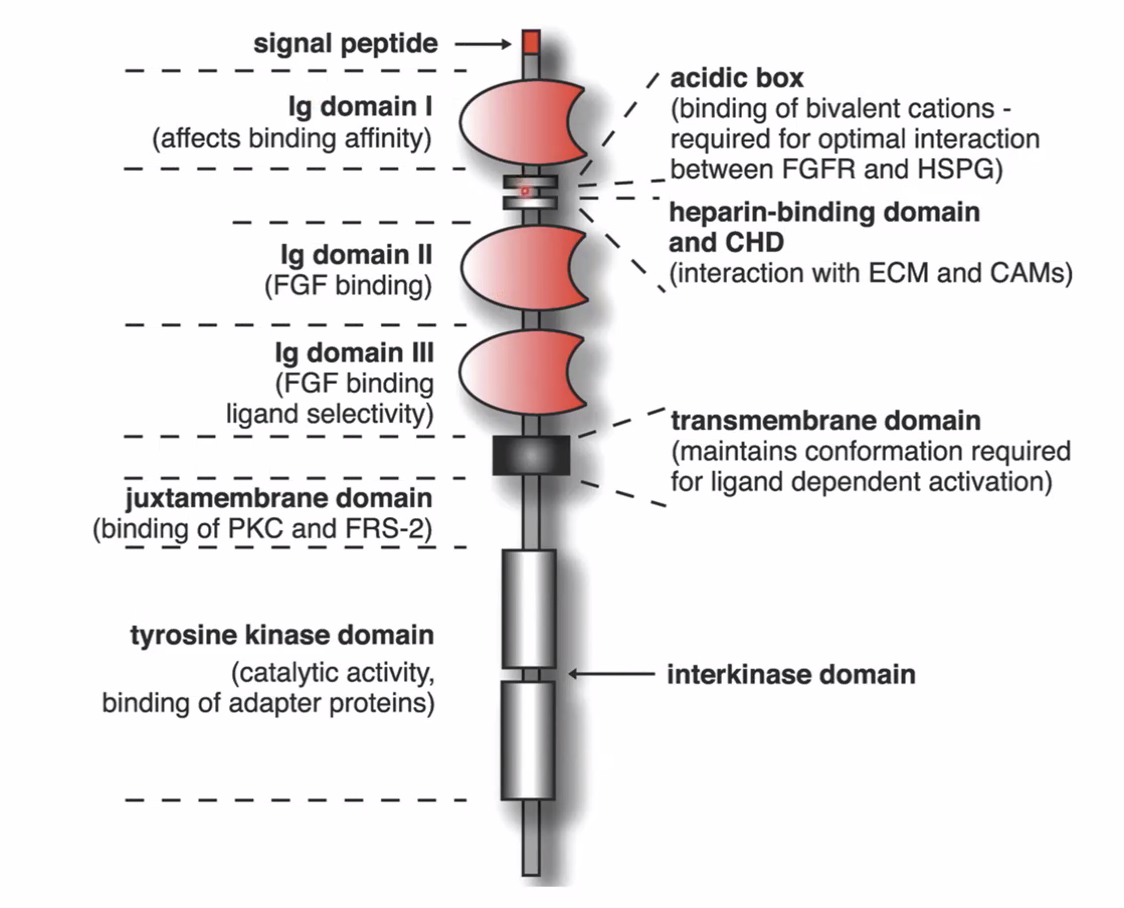
משפחת FGF receptors כוללת ארבעה רצפטורים עיקריים: FGFR1-4. עם זאת, לכל אחד מהם יש וריאנטים רבים של שחבור חליפי (splice variants), ולכן בפועל מתקבל מגוון גדול בהרבה מארבעה רצפטורים בלבד.
למשפחה זו יש גם 22 ליגנדים שונים. המשמעות היא שמערכת ה־FGF יכולה לייצר מגוון רחב של אותות ותוצאות ביולוגיות, בהתאם לשילוב בין הליגנד, הרצפטור והווריאנט הספציפי.
באזור החוץ־תאי (extracellular domain) של הרצפטור יש כמה אזורים חשובים:
D1(Ig domain 1) - דומיין בעל תפקיד אוטו־אינהיביטורי, כלומר, הוא מפחית את האפיניות של הרצפטור לליגנד.D2ו־D3(Ig domains 2–3) - דומיינים האחראים על קישור הליגנד.- מבין שניהם,
D3חשוב במיוחד לקביעת הספציפיות: הוא משפיע לאיזה ליגנד הרצפטור ייקשר ובאיזו אפיניות.
בנוסף לכך, בין D1 ל־D2 נמצא heparin-binding domain. אזור זה מאפשר קישור ל־HSPG (Heparan Sulfate Proteoglycans), שחיוני להפעלת המסלול.
כלומר, גם אם FGF נקשר לרצפטור דרך D2 ו־D3, עדיין נדרש HSPG בסביבה בשביל העברת אותות בצורה תקינה. בלי HSPG, הקישור לבדו אינו מספיק, והאות לא יעבור אל תוך התא.
הפעלת FGF Receptor
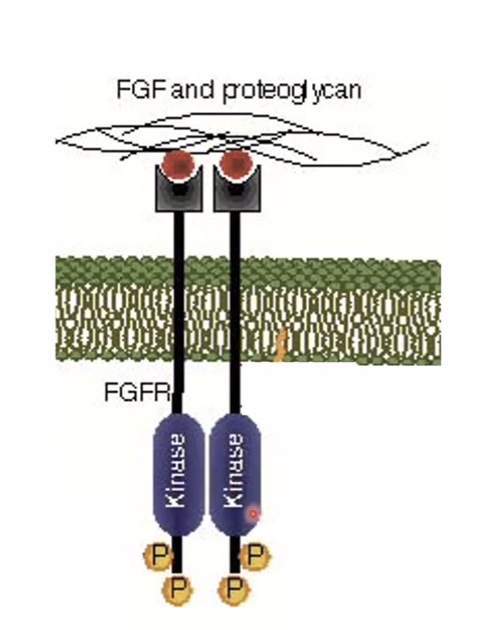
FGF ligandנקשר לשני רצפטורים (כל מולקולת ליגנד לרצפטור אחד)- נוצרת דימריזציה של שני הרצפטורים
- HSPG נקשר גם הוא לרצפטור - גורם לשינוי קונפורמטיבי
- הקינאזות מאוקטבות - מבצעות אוטו־פוספורילציה (כל רצפטור עושה פוספורילציה לשכנו)
- נוצרות נקודות עגינה (Docking Sites) לאנזימים ולאדפטורים שונים על האזור התוך־תאי
שלושת המסלולים שמופעלים כתוצאה מ־FGF Receptor
מסלול 1 - PLC-γ
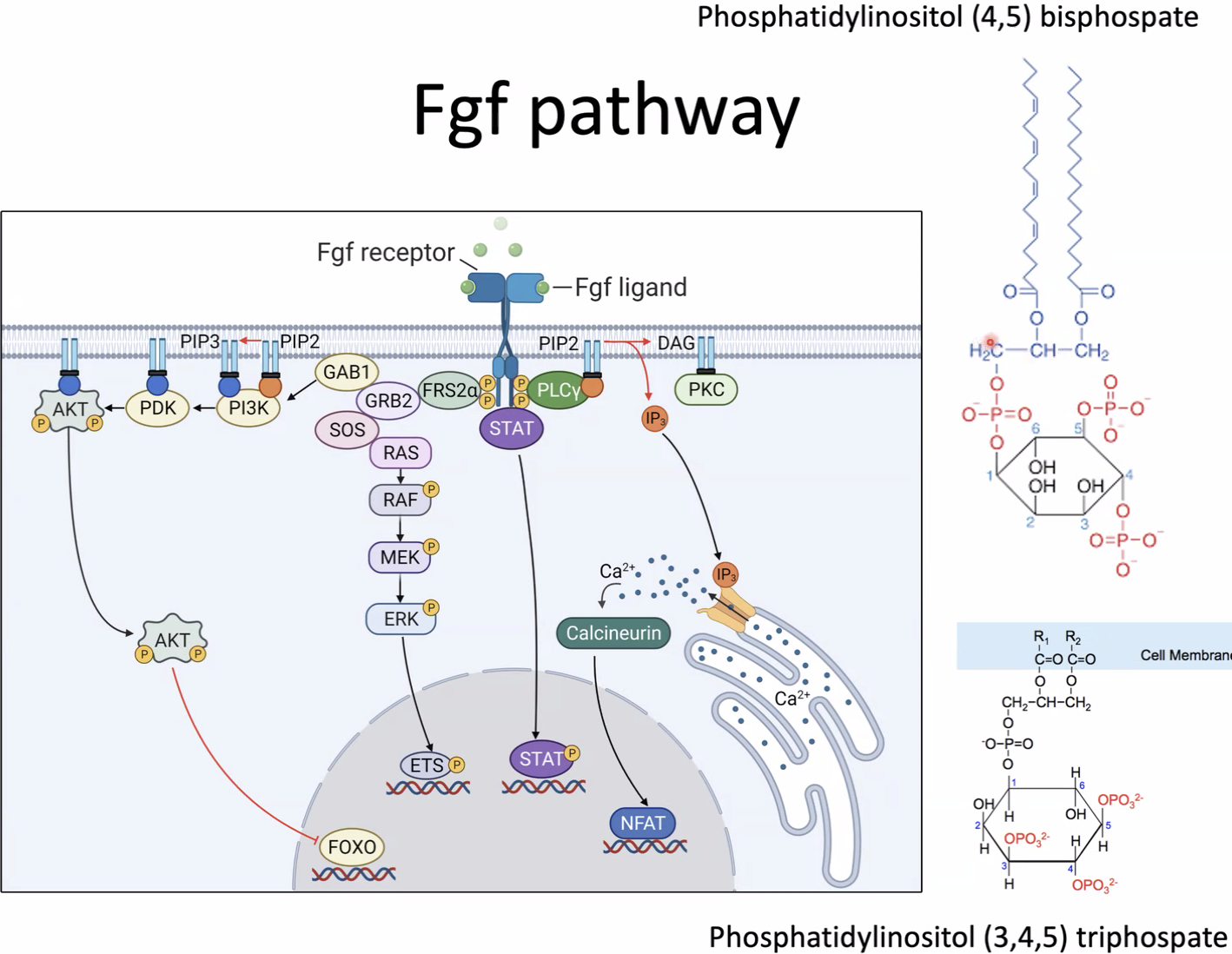
PLC-γ (Phospholipase C-gamma) נקשר לרצפטור המזורחן דרך נקודת עגינה, וכך עובר הפעלה.
הסובסטרט שלו הוא PIP2 (Phosphatidylinositol 4,5-bisphosphate), פוספוליפיד שנמצא בחלק הפנימי של ממברנת התא. המבנה שלו כולל גליצרול, שתי חומצות שומן, פוספט, וקבוצת אינוזיטול שעליה יש שני פוספטים נוספים בעמדות 4 ו־5.
לאחר ההפעלה, PLC-γ מבקע את PIP2 לשני תוצרים: IP3 ו־DAG.
-
IP3 הוא תוצר מסיס, שנע בציטופלסמה ונקשר לתעלות סידן על פני ה־ER. הקישור פותח את התעלות וגורם לשחרור $\ce{Ca^2+}$ לציטופלסמה. הסידן משמש כשליח שניוני ומפעיל מסלולי איתות וגורמי שעתוק.
-
DAG נשאר בממברנה, ושם הוא מפעיל את PKC (Protein Kinase C), שממשיך את העברת האות בתוך התא.
בדיקה עצמיה - מה PLC-γ עושה?
PLC-γ מבקע את PIP2 לשני תוצרים: IP3 ו־DAG.
- IP3 היא מולקולה מסיסה שגורמת לשחרור סידן מה־ER לציטופלסמה, וכך מפעילה מסלולי איתות וגורמי שעתוק.
- DAG נשאר בממברנה ומפעיל את PKC, שממשיך את העברת האות בתא.
מסלול 2 - PI3K
לאחר הפעלת הרצפטור, FRS2-α — שהוא Docking protein — נקשר לרצפטור ועובר פוספורילציה.
בהמשך FRS2-α מגייס את GRB2 ואת GAB1, ודרכם מגויס גם PI3K (Phosphoinositide 3-kinase).
PI3K פועל על PIP2, אך בניגוד ל־PLC-γ הוא לא מבקע אותו, אלא מוסיף פוספט נוסף לפחמן 3 של האינוזיטול, וכך נוצר PIP3 ((PI(3,4,5)P3)).
PIP3 משמש אתר עגינה לקינאזות שונות, שמפעילות בהמשך מסלולי איתות תוך־תאיים ובסופו של דבר מובילות להפעלת גורמי שעתוק.
מסלול 3 - Ras/MAPK
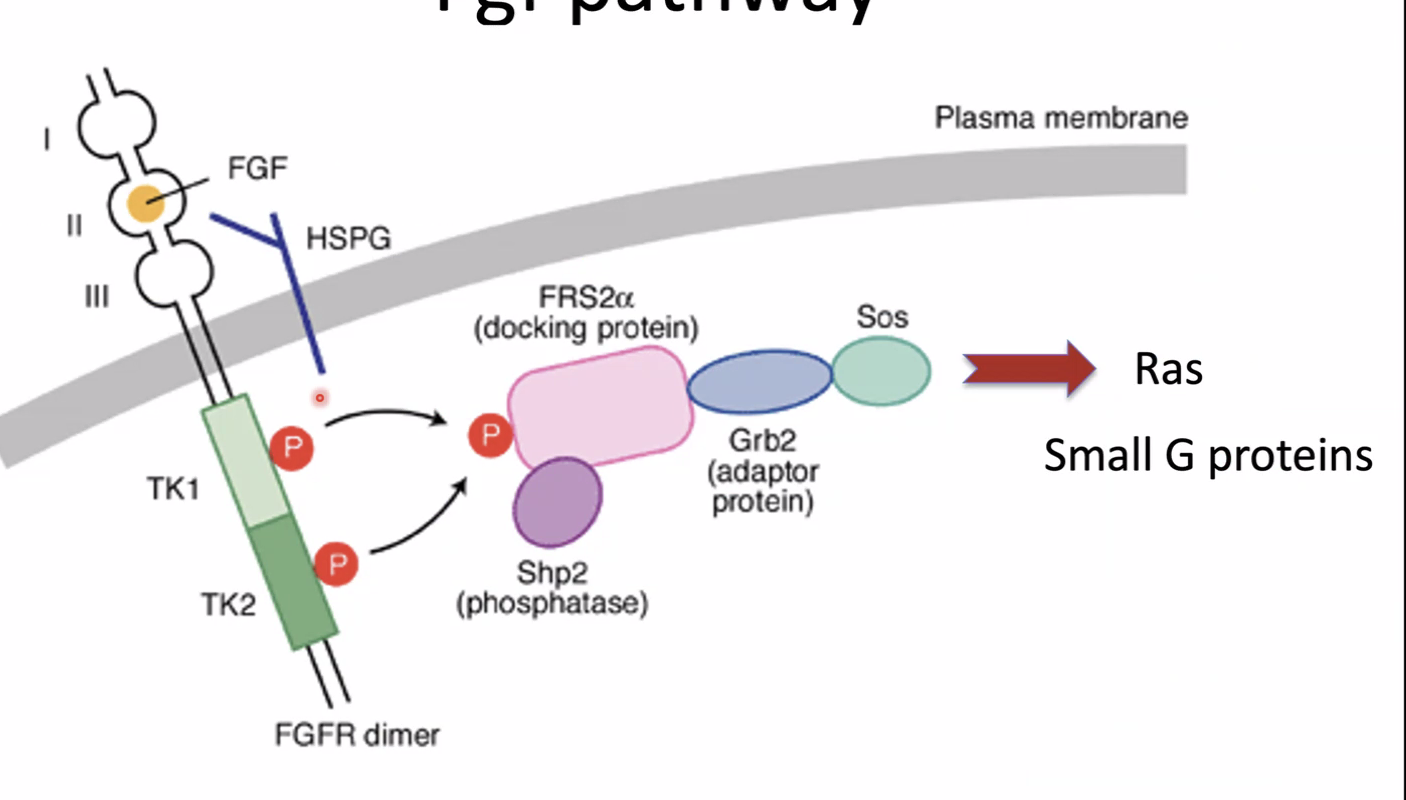
זהו מסלול האיתות הקלאסי של FGF, והוא מעביר את האות מהרצפטור שעל הממברנה עד להפעלת גנים בגרעין.
לאחר ש־FGF receptor מופעל, החלבון FRS2-alpha נקשר אליו ועובר פוספורילציה. לאחר מכן GRB2 נקשר ל־FRS2-alpha, ודרכו מגויס גם SOS.
SOS הוא גורם מסוג GEF (Guanine nucleotide Exchange Factor). התפקיד שלו הוא להחליף את ה־GDP שעל Ras ב־GTP, וכך Ras עובר אקטיבציה.
מרגע ש־Ras הופך לפעיל, מתחילה שרשרת קינאזות מסודרת:
\[\text{Ras} \xrightarrow{\text{activates}} \underset{\text{MAPKKK}}{\text{Raf}} \xrightarrow{\text{phosphorylates}} \underset{\text{MAPKK}}{\text{MEK}} \xrightarrow{\text{phosphorylates}} \underset{\text{MAPK}}{\text{ERK}}\]פירוט השלבים:
- Ras הפעיל מפעיל את Raf
- Raf הוא MAPKKK (קינאז שנמצא שלוש דרגות מעל MAPK בשרשרת), והוא מזרחן את MEK
- MEK הוא MAPKK, והוא מזרחן את ERK
- ERK הוא ה־MAPK הסופי במסלול
לאחר ש־ERK עובר פוספורילציה, הוא נכנס לגרעין ומזרחן גורמי שעתוק כמו ELK ו־FOS. הפוספורילציה הזאת מפעילה אותם, וכך מתחיל שעתוק של גני מטרה.
בדיקה עצמית - מה קורה אחרי ש־FGF מפעיל את הרצפטור?
- FGF מפעיל רצפטור
- FRS2-alpha
- GRB2
- SOS
- Ras
- Raf
- MEK
- ERK
- גורמי שעתוק
- טרנסקריפציה
Small G Proteins - עיקרון כללי
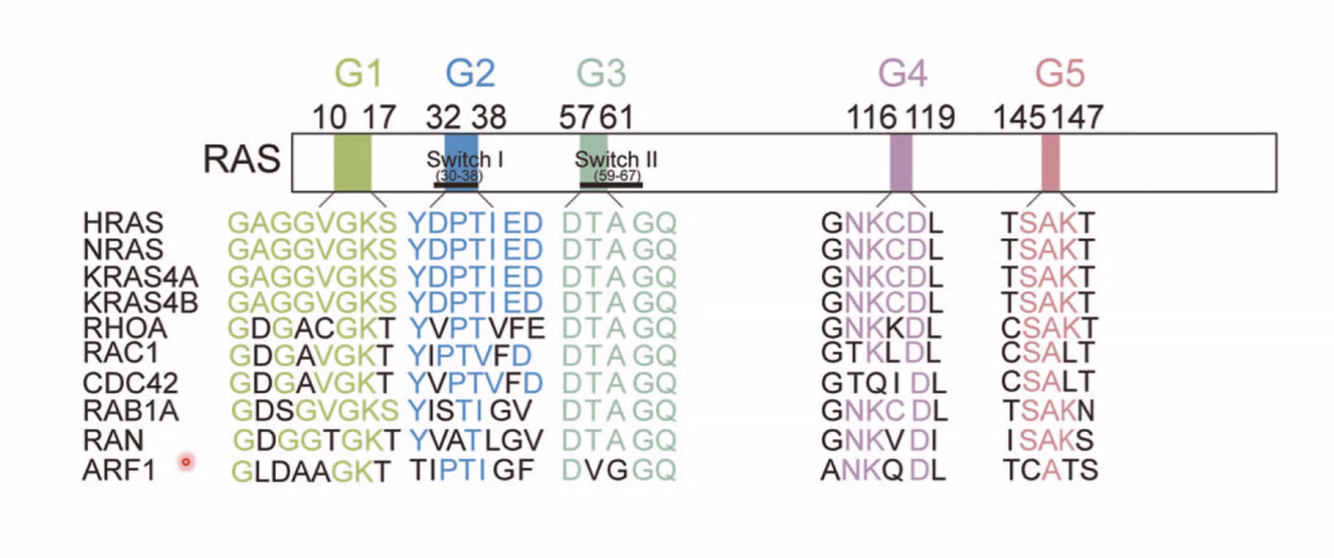
Ras שייך לקבוצה גדולה של Small G Proteins - חלבונים קטנים שיש להם רצפים שמורים (G1-G5). כולם כוללים: H-Ras, N-Ras, Rho, CDC42, Rack1, Ran ועוד.
הפעילות הקטליטית: כל Small G Protein הוא GTPase - מבצע הידרוליזה של GTP ל־GDP. אך זו לא הפונקציה הביולוגית שלהם - זה רק המנגנון שמאפשר להם להיות מופעלים ומעוכבים.
מה הם עושים ביולוגית (תלוי על איזה חלבון):
Ras- מסלולMAPK- Rho - ריאורגניזציה של ציטוסקלטון אקטין
- Rab - תנועה של וסיקולות (אנדוציטוזה)
- Ran - טרנספורט דרך נוקלאופורין (גרעין ↔ ציטופלסמה)
המצב הפעיל והלא פעיל של Small G Proteins
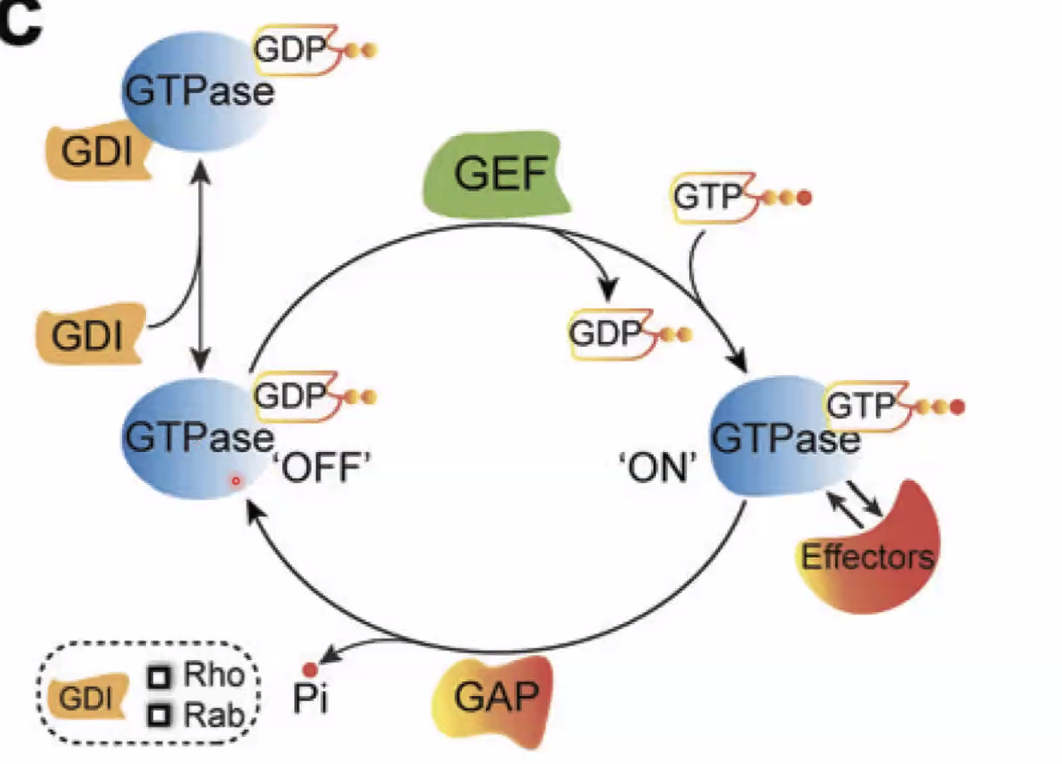
- GDP קשור ← לא פעיל
- GTP קשור ← פעיל - יכול לקשור Effectors ולהפעיל מסלולים
GEF (Guanine nucleotide Exchange Factor): מחליף GDP ב־GTP ← אקטיבציה. GEF של Ras = SOS.
GAP (GTPase Activating Protein): נקשר ל־Small G Protein ומאקטב את פעילות ה־GTPase שלו ← הידרוליזה של GTP ל־GDP ← אינאקטיבציה.
תפקיד SHP2 במסלול Ras
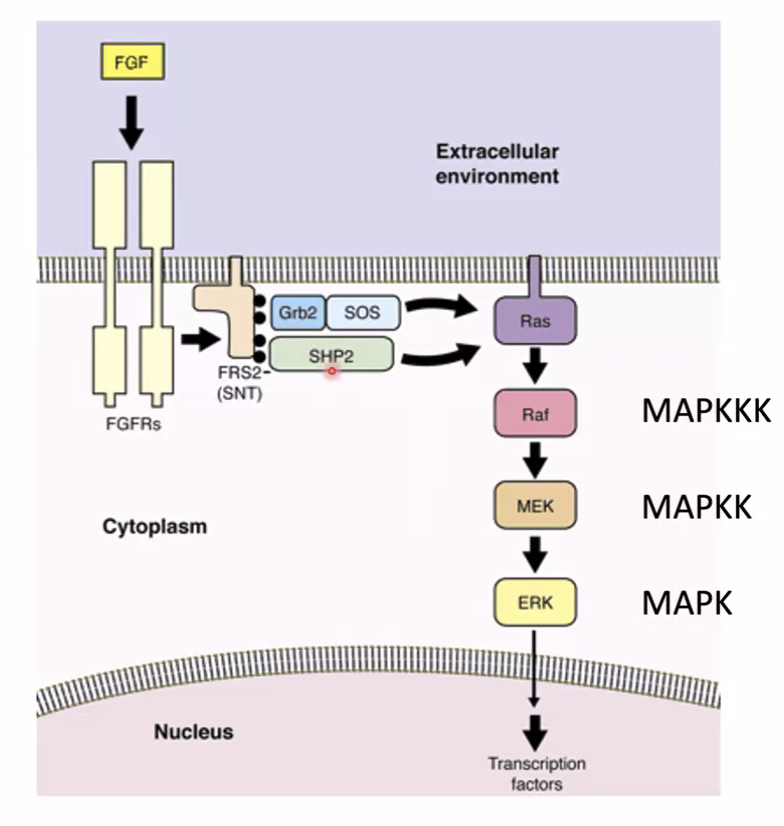
נקודה עדינה אך חשובה: כאשר FRS2-α נקשר לרצפטור המאוקטב, מתרחשת פוספורילציה מסוימת על FRS2-α שיוצרת Docking Site לGAP (ספציפי ל־Ras). קישור של GAP מפסיק את Ras. אבל: רוצים להפעיל את Ras, לא לעצור אותו. לכן מגויס גם SHP2 (פוספטאז) שמוריד את אותו פוספט ספציפי - וכך GAP לא יכול להיקשר, ו־Ras נשאר פעיל.
SHP2הוא פוספטאז שבסיטואציה הזאת מפעילRasבצורה עקיפה - על ידי מניעת גיוס GAP. זה נראה אנטי-אינטואיטיבי (פוספטאז = מעכב?) אבל האפקט הכולל הוא פוזיטיבי.
SHP2 מעורב בעוד מסלולים רבים - זה לא התפקיד הבלעדי שלו.
מעכבים פנימיים של מסלול FGF
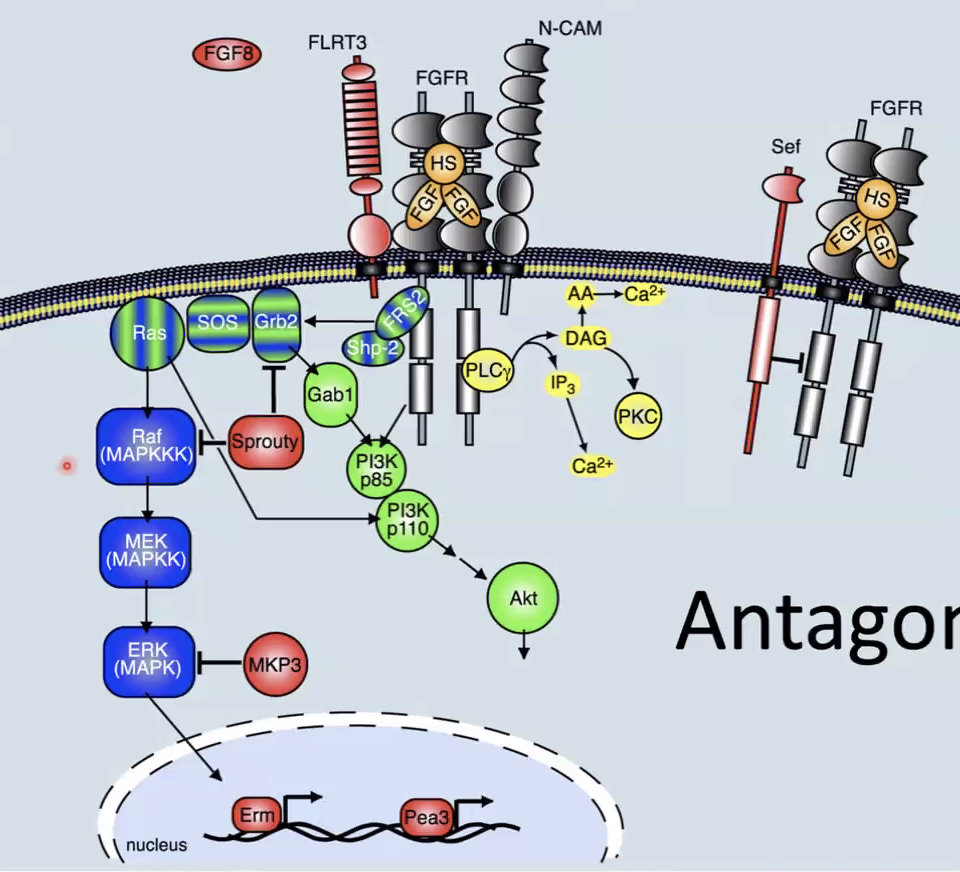
בניגוד למסלולי BMP ו־Wnt, שבהם יש הרבה מעכבים מופרשים מחוץ לתא, במסלול FGF רוב המעכבים הם פנימיים, כלומר פועלים בתוך התא עצמו.
-
Sprouty (SPRY): חלבון שמעכב את המסלול על ידי קישור ל־GRB2 או ל־Raf. כלומר, תא שמקבל אות של FGF יכול לייצר Sprouty, וכך ליצור מנגנון כיבוי עצמי של המסלול.
-
Sef: חלבון טרנסממברנלי שמעודד יוביקוויטינציה של קולטני FGF. כתוצאה מכך הרצפטור הפעיל עובר דגרדציה, ולכן האיתות נחלש או נפסק.
Cross-talk בין מסלולים - FGF ו־Wnt דרך E-cadherin

RTK עושה פוספורילציה על beta-catenin בטירוזין 654
כפי שראינו בשיעור הקודם, ב־Adherens Junctions החלבון E-cadherin קשור ל־beta-catenin, ו־beta-catenin קשור ל־alpha-catenin, שמחבר את כל המבנה לפילמנטים של אקטין. כלומר, הקישור של beta-catenin חשוב ליציבות של E-cadherin ושל הצומת כולו.
כאן נכנס הקשר למסלול FGF:
כאשר רצפטור מסוג RTK כמו FGFR מופעל על ידי FGF, הדומיין הקינאזי שלו מבצע פוספורילציה על beta-catenin בטירוזין 654.
לפוספורילציה הזאת יש שתי תוצאות חשובות:
-
beta-catenin מתנתק מ־E-cadherin
ברגע שהקישור בין beta-catenin ל־E-cadherin נפגע, היציבות של E-cadherin יורדת, הוא עובר דגרדציה, ו־Adherens Junctions מתפרקים. המשמעות היא ששני תאים שהיו צמודים יכולים כעת להיפרד.
-
ה־beta-catenin החופשי יכול להיכנס לגרעין
לאחר שהוא משתחרר מהצומת, הוא נכנס לגרעין ומפעיל גני מטרה של Wnt. הדבר המעניין כאן הוא שזה קורה גם בלי ליגנד Wnt בסביבה (להבנתי גם בלי קשר ל־Destruction Complex).
כלומר, הפעלה של FGF/RTK יכולה גם לפרק את ההיצמדות בין תאים וגם להפעיל תוכנית גנים שמזוהה עם Wnt.
הנקודה המרכזית: מסלול FGF יכול להשפיע על מסלול Wnt דרך beta-catenin. זאת דוגמה ל־cross-talk בין מסלולי איתות: מסלול אחד מפעיל תוצאה שמזוהה בדרך כלל עם מסלול אחר.
Pyk/Fer - שחרור של alpha-catenin
Pyk ו־Fer הן קינאזות שמופעלות downstream ל־RTK.
לאחר ההפעלה, הן נקשרות ל־p120 catenin ומבצעות פוספורילציה על שיירי טירוזין אחרים ב־beta-catenin.
התוצאה היא ש־alpha-catenin מתנתק מהקומפלקס. ברגע ש־alpha-catenin משתחרר, הקישור של פילמנטי האקטין אל ה־Adherens Junction נחלש או אובד.
כלומר, ה־Junction עצמו עדיין קיים, אבל הוא כבר לא מחובר בצורה יציבה ל”חגורה” של האקטין. לכן המבנה נעשה פחות קשיח ויותר גמיש.
לקראת השיעור הבא - Sonic Hedgehog (Shh)
המסלול הבא הוא Sonic Hedgehog (Shh) - נושא כבד שכולל גם אורגנלה ייחודית שיש לה חשיבות רבה הן בגוף הכללי והן בהתפתחות עוברית. יידון בשיעור הבא.
דור פסקל