תוכן העניינים:
- חזרה על השיעור הקודם
- MMR deficiency ו־Microsatellite Instability
- MSI בסרטן ובטיפול אימונותרפי
- MSI test ו־Lynch syndrome
- Single-strand breaks - SSBs
- תיקון SSB ו־PARP1
- PARP inhibitors בטיפול אנטי-סרטני
- Double-strand breaks - DSBs
- Non-Homologous End Joining - NHEJ
חזרה על השיעור הקודם
חזרה על Bulky lesions, NER, TLS ו־MMR:
- בחולי XPC ו־XPE הרגישות ל־UV נמוכה יותר יחסית לקבוצות XP אחרות, כי Transcription-Coupled NER עדיין תקין אצלם. הפגיעה היא בעיקר בזיהוי של Global Genome NER.
- ב־XP-V הגן הפגוע אינו אחד מגני XP הקלאסיים של NER, אלא Polymerase η. לכן הבעיה היא ב־TLS מעל נזקי UV.
- חולי XP יכולים לפתח גם סרטנים פנימיים, לא רק סרטן עור, משום ש־NER מתקן גם bulky lesions ממקורות כימיים פנימיים ולא רק thymine dimers מקרינת UV.
- ביטוי מוגבר של פקטורי שעתוק ממשפחת ETS צפוי לגרום ליותר thymine dimers באתרים שאליהם הם נקשרים, כי הקישור שלהם מקרב את התימינים זה לזה.
- עמידות ל־cisplatin יכולה לנבוע מ־TLS מוגבר: התא מצליח לשכפל מעל הנזק במקום לעצור ולעבור אפופטוזיס.
- באאוקריוטים, strand discrimination ב־MMR נעזר בניקים או ב־DNA חד־גדילי בגדיל המסונתז, ולא במתילציה כמו ב־E. coli.
- PCNA משתתף גם ב־MMR וגם ב־TLS: ב־MMR הוא עוזר לזהות את הגדיל החדש, וב־TLS הוא עובר mono-ubiquitination ומגייס פולימראזות TLS.
- עלייה בביטוי RNase H אינה צפויה לעודד קריסה של מזלג השכפול, כי RNase H מפרק R-loops ובכך יכול להפחית מכשולים לשכפול.
מכאן חזרנו ל־MMR, והפעם התמקדנו בפתולוגיות שקשורות לחסר ב־MMR.
MMR deficiency ו־Microsatellite Instability
חזרה על MMR
Mismatch Repair - MMR מזהה טעויות שנוצרות במהלך שכפול DNA.
החלבון המרכזי בשלב הזיהוי הוא MutS בחיידקים, או MSH באאוקריוטים. הוא מזהה עיוות קטן במבנה ההליקס שנוצר בגלל mismatch, נסגר סביבו, ומגייס את שאר מנגנון התיקון.
האתגר המרכזי הוא strand discrimination: אחרי שנוצר mismatch, צריך לדעת איזה גדיל הוא הישן והתקין, ואיזה גדיל הוא החדש שבו כנראה נפלה הטעות.
שני פתרונות:
- ב־E. coli משתמשים במתילציה של אדנין. הגדיל הישן כבר ממותל, והגדיל החדש עדיין לא.
- באאוקריוטים משתמשים בניקים ובאזורים חד־גדיליים בגדיל המסונתז, בעזרת PCNA. ב־lagging strand יש מקטעי אוקזקי, וב־leading strand יש קצה חדש באזור מזלג השכפול.
בסוף התהליך המקטע שמכיל את הטעות מוסר, ואז DNA polymerase δ מסנתז מחדש ו־ligase סוגר את הקצוות.
Microsatellites
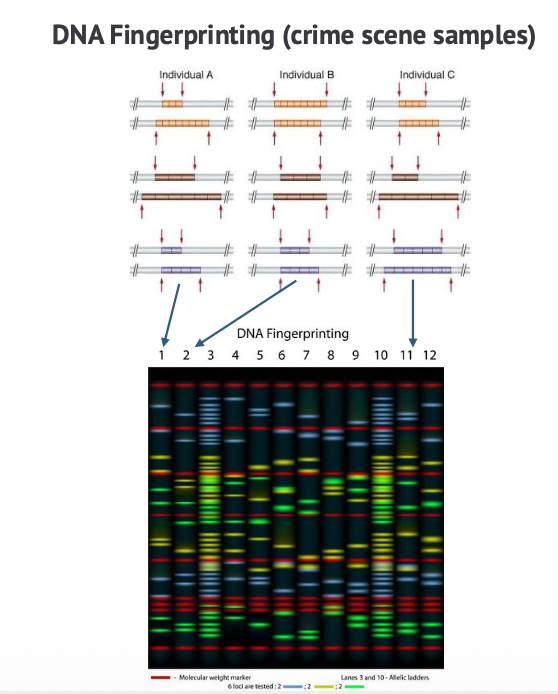
Microsatellites הם אזורי DNA חוזרני קצרים, שבהם אותו רצף קצר חוזר מספר פעמים.
הם נמצאים באזורים מסוימים בגנום, לרוב באזורים לא מקודדים. מה שהופך אותם לשימושיים הוא שמספר החזרות משתנה בין אנשים שונים.
לכן פרופיל של כמה microsatellites יכול לשמש כמו טביעת אצבע גנטית. אם בודקים כמה אתרי microsatellite שונים ומשווים את אורכי החזרות, אפשר לזהות התאמה בין דגימות DNA.
Replication slippage
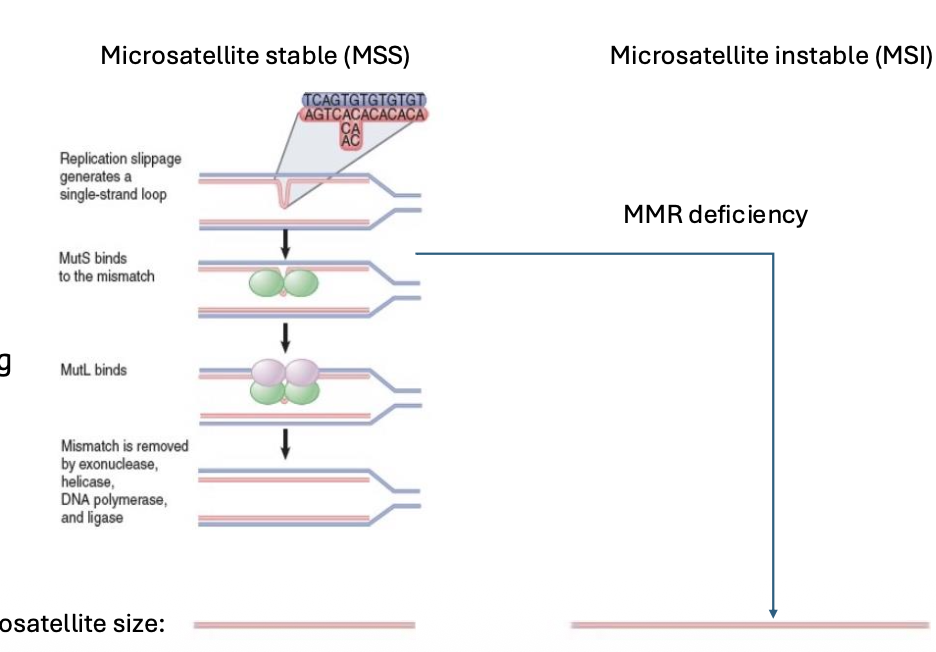
Microsatellites רגישים במיוחד לתופעה שנקראת replication slippage.
הסיבה היא שכל חזרה ברצף יכולה להתאים לכל חזרה אחרת. בזמן שכפול DNA, הגדיל המסונתז וה־template יכולים “להחליק” זה ביחס לזה, ואז נוצרת לולאה.
הלולאה יכולה להיווצר בשני מקומות:
- אם הלולאה נוצרת בגדיל המסונתז, מספר החזרות יכול לגדול.
- אם הלולאה נוצרת בגדיל האב / template, מספר החזרות יכול להתקצר.
MMR מזהה את המבנה הלא תקין, חותך ומתקן אותו. לכן MMR שומר על יציבות מספר החזרות.
כשיש MMR deficiency, ה־slippage לא מתוקן בצורה טובה. התוצאה היא שינוי במספר החזרות במיקרוסטלייטים. קוראים לזה Microsatellite Instability - MSI, או בסרטנים עם רמה גבוהה של התופעה: MSI-high.
MSI בסרטן ובטיפול אימונותרפי
MSI-high נפוץ במיוחד בכמה סוגי סרטן, כמו:
- colorectal cancer
- endometrial cancer
- gastric cancer
כשיש חסר ב־MMR, הטעויות שנוצרות בזמן שכפול אינן מתוקנות. לכן לסרטנים מסוג MSI-high יש בדרך כלל עומס מוטציות גבוה.
החיסרון: עומס מוטציות גבוה יכול לתרום לטרנספורמציה סרטנית, למשל על ידי פגיעה ב־tumor suppressor genes או יצירת שינויים שמקדמים חלוקה והישרדות.
אבל יש גם צד טיפולי חשוב: עומס מוטציות גבוה יכול ליצור הרבה חלבונים חדשים או מקטעי חלבון חדשים שהתא לא הציג קודם. אלו נקראים neoantigens.
Neoantigens
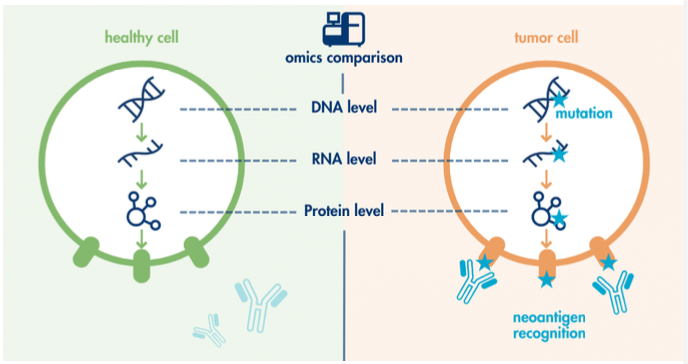
Neoantigens הם אנטיגנים חדשים שנוצרים בעקבות מוטציות.
כשבתא סרטני יש הרבה מוטציות, נוצרים חלבונים או פפטידים שהמערכת החיסונית יכולה לזהות כלא־עצמיים. לכן, מבחינת מערכת החיסון, סרטן MSI-high יכול להיות יותר “בולט”.
זה מסביר למה סרטנים MSI-high יכולים להגיב טוב לטיפול אימונותרפי.
הסרטן מכבה את מערכת החיסון
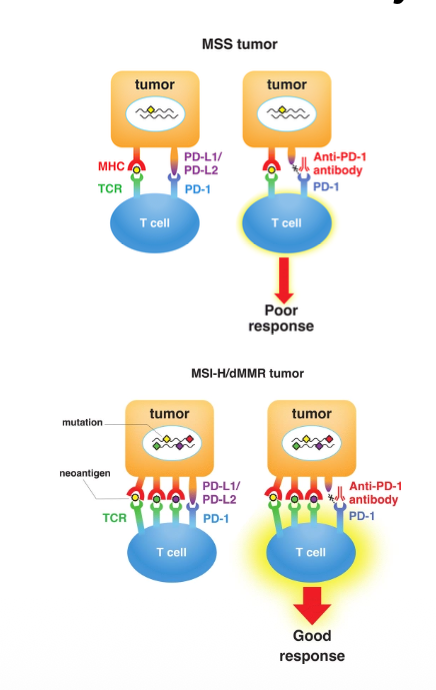
אחד המנגנונים שבאמצעותם תאים סרטניים מתחמקים ממערכת החיסון, הוא דיכוי תגובת מערכת החיסון. מנגנון שקשור ל־PD-1, שהוא רגולטור שלילי של מערכת החיסון.
טיפול אימונותרפי, למשל בעזרת immune checkpoint inhibitors כמו anti-PD-1, מנסה לשחרר את העיכוב ולאפשר למערכת החיסון לפעול נגד התא הסרטני.
לכן בחולה עם סרטן MSI-high, יש היגיון טיפולי להשתמש ב־immune checkpoint inhibitors: מצד אחד יש הרבה neoantigens, ומצד שני הטיפול מסיר את הדיכוי שמונע ממערכת החיסון להגיב אליהם.
MSI test ו־Lynch syndrome
MSI test
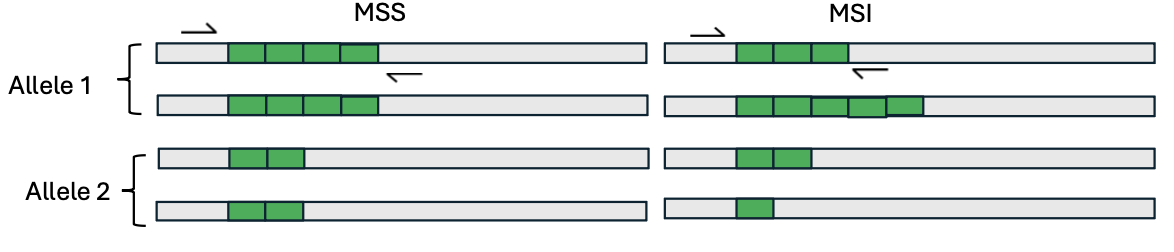
כדי לבדוק אם גידול הוא MSI-high, משווים בין DNA מרקמה בריאה לבין DNA מהרקמה הסרטנית של אותו אדם.
הרעיון:
- בוחרים כמה אתרי microsatellite
- מגבירים אותם ב־PCR בעזרת פריימרים ספציפיים
- בודקים את אורכי המקטעים
- משווים בין הרקמה הבריאה לבין הרקמה הסרטנית
ברקמה הבריאה, פרופיל המיקרוסטלייטים מייצג את המצב המקורי של האדם. אם ברקמה הסרטנית מופיעים פיקים חדשים או שונות באורכים, זה סימן ל־microsatellite instability.
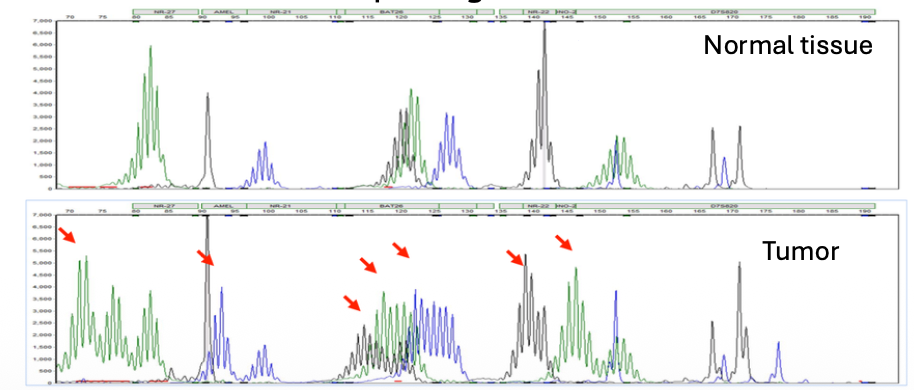
ב־electropherogram אפשר לראות הבדלים באורכי המקטעים. לא בהכרח חשוב איזה שינוי ספציפי קרה בכל microsatellite; מה שחשוב הוא שיש שונות רחבה שמצביעה על חוסר יציבות ועל MMR deficiency.
המידע הזה מאפשר לבחור טיפול מתאים, במיוחד בהקשר של אימונותרפיה.
Lynch Syndrome
Lynch syndrome הוא סינדרום (תסמונת) תורשתי שבו יש נטייה לפתח סרטנים מסוימים, במיוחד colorectal cancer, בגלל פגיעה בגנים של MMR.
הגנים בהקשר זה הם בעיקר:
- MLH
- MSH
כשאדם נושא מוטציה בגנים של MMR, יש לו נטייה מוגברת לפתח גידולים עם MSI-high.
בנוסף ל־Lynch syndrome, MSI יכול להופיע גם באופן נרכש במהלך החיים. לדוגמה:
- Epigenetic misregulation, למשל hypermethylation והשתקה של גן MMR כמו MLH1.
- Over-expression של microRNA, למשל miR-155, שיכול להוריד ביטוי של גנים הקשורים ל־MMR.
הנתונים לגבי colorectal cancer:
- בערך 15% ממקרי colorectal cancer הם MSI-high
- מתוך מקרי MSI-high, בערך 20% קשורים ל־Lynch syndrome
- בערך 80% הם מקרים ספורדיים
Single-strand breaks - SSBs
לאחר סיום החלק על TLS ו־MMR, עברנו לנושא חדש: DNA breaks.
עד עתה דיברנו על:
- נזקים ברמת הבסיס
- bulky lesions
- טעויות זיווג ותיקון MMR
כעת עוברים לשברים ב־DNA:
- Single-strand breaks - SSBs
- Double-strand breaks - DSBs
מהו SSB?
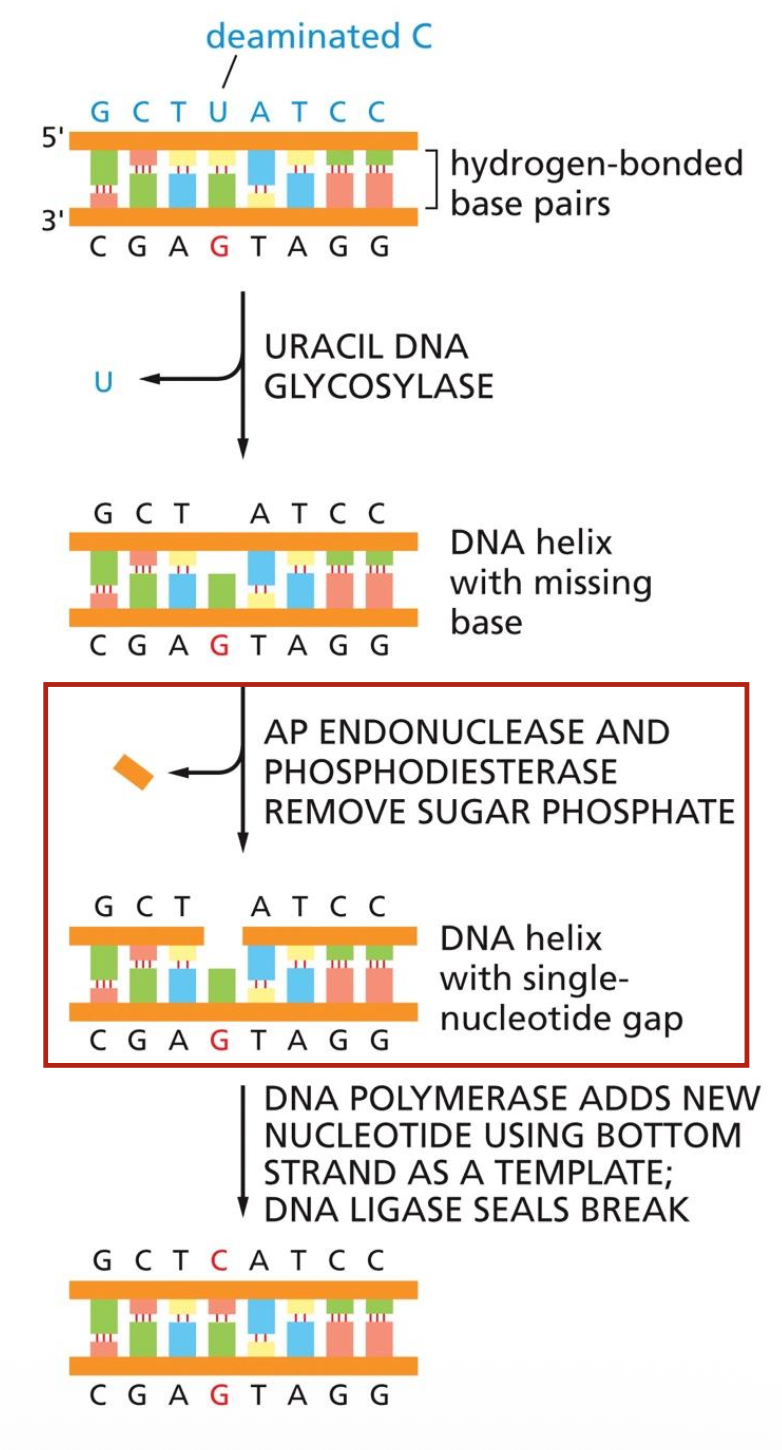
Single-strand break הוא נזק שבו השרשרת הסוכרית-פוספטית נחתכת באחד משני הגדילים של ה־DNA.
זה נזק נפוץ מאוד - סדר גודל של 10,000 עד 100,000 שברים חד־גדיליים לתא ביום.
הוא נפוץ לא רק בגלל גורמים חיצוניים, אלא גם כי הוא מופיע כתוצר ביניים של תהליכים תקינים ותהליכי תיקון אחרים.
מקורות ל־SSBs
מקורות עקיפים:
- Base Excision Repair - למשל אחרי פעילות APE1, נוצר ניק כחלק מהתהליך.
- Nucleotide Excision Repair - חלבונים כמו XPF ו־XPG חותכים את ה־DNA סביב הנזק.
- Mismatch Repair - נדרש חיתוך של הגדיל החדש כדי להסיר את האזור השגוי.
- Okazaki fragments - ב־lagging strand יש ניקים עד שהמקטעים מחוברים.
- Topoisomerase I - יוצר שבר חד־גדילי זמני כחלק משחרור מתח טופולוגי.
מקורות ישירים:
- Ionizing radiation
- Reactive Oxygen Species - ROS
כמעט כל תהליך שמוביל ל־BER, NER או MMR יכול ליצור SSB כתוצר ביניים. לכן SSBs קיימים בכל מקום ונדרשת מערכת תיקון יעילה מאוד.
תיקון SSB ו־PARP1
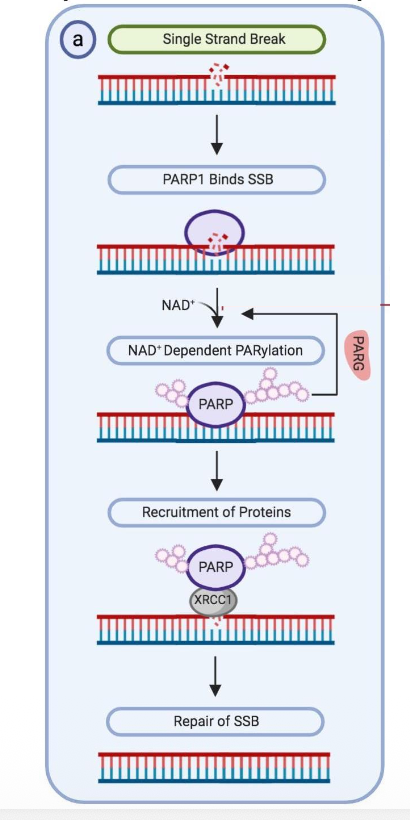
השחקן המרכזי בתיקון שברים חד־גדיליים הוא PARP1.
זיהוי ו־PARylation
PARP1 מזהה single-strand break. לאחר הזיהוי הוא עושה PARylation על עצמו - כלומר מוסיף על עצמו שרשראות של סוכרים / פולימרים של ADP-ribose.
זו מודיפיקציה לאחר תרגום, והיא משמשת כסיגנל לגיוס חלבונים נוספים.
גיוס XRCC1
לאחר PARylation מגויס החלבון XRCC1.
XRCC1 הוא scaffold protein (חלבון פיגום): חלבון שמגייס ומארגן סביבו חלבונים אחרים הדרושים לתיקון.
בשלב הבא XRCC1 מגייס חלבונים שמנקים את הקצוות של השבר, למשל:
- APE1
- PNKP
המטרה להכין קצוות מתאימים לתיקון: צד אחד עם הידרוקסיל וצד שני עם פוספט, כדי שפולימראז וליגאז יוכלו לפעול.
לאחר ניקוי הקצוות:
- פולימראז משלים נוקלאוטידים חסרים, אם יש צורך בכך
- ליגאז סוגר את הניק
הקשר בין SSB repair לבין BER
SSB יכול להיווצר כחלק תקין מ־BER. במקרה כזה אין צורך להפעיל מחדש את כל מנגנון PARP1, כי הנזק כבר זוהה ומנגנון התיקון כבר פועל.
לכן ב־BER יש מעין העברת שרביט: פקטורים של BER מגייסים ישירות את XRCC1, ובכך מדלגים על הצורך בגיוס PARP1.
זה הופך את התהליך ליעיל יותר ומונע בזבוז אנרגיה. אם התהליך נכשל, PARP1 עדיין יכול לזהות את ה־SSB ולהפעיל תיקון מלא.
Topoisomerase I cleavage complex
Topoisomerase I משחרר מתח טופולוגי על ידי יצירת שבר חד־גדילי זמני. בדרך כלל הוא מחזיק את הקצוות ומחבר אותם מחדש בעצמו.
אבל לפעמים נוצר Top1 cleavage complex שלא נפתר. במצב כזה יש חלבון שקשור קוולנטית ל־DNA, וזה יוצר בעיה מורכבת יותר מ־SSB רגיל.
PARP1 פועל גם כאן: הוא מגייס את TDP1, חלבון שיודע להסיר protein-DNA adducts כמו Top1 התקוע על ה־DNA. לאחר הסרת החלבון, ניתן להמשיך לתיקון השבר החד־גדילי.
PARP inhibitors בטיפול אנטי-סרטני
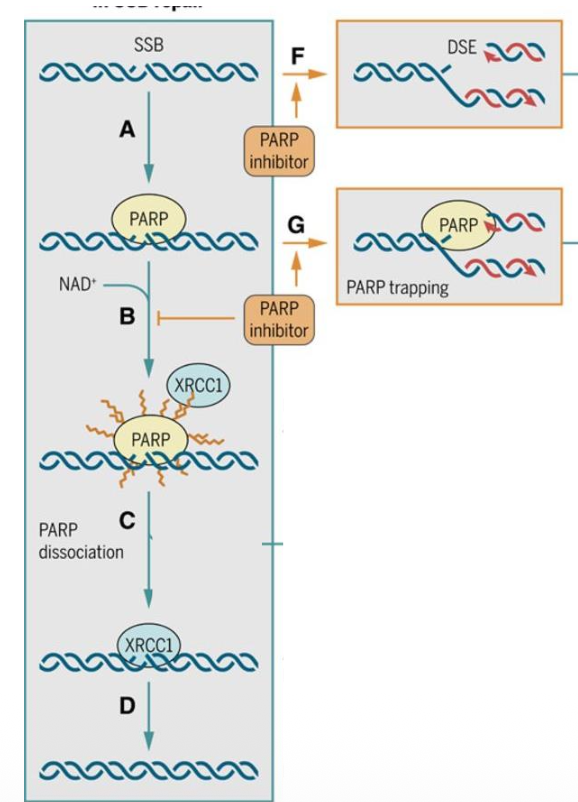
PARP inhibitors הם משפחה חשובה של תרופות אנטי-סרטניות.
הרעיון הוא לעכב את PARP1 וכך לפגוע בתיקון של single-strand breaks.
יש שתי דרכי פעולה מרכזיות:
1. עיכוב קטליטי של PARP1
אם PARP1 מעוכב, SSBs לא מתוקנים בצורה יעילה. חלק מהשברים החד־גדיליים האלה עלולים להפוך בזמן שכפול ל־double-strand breaks.
כשמצטברים הרבה DSBs, התא עלול לעצור שכפול ולעבור אפופטוזיס.
2. PARP trapping
במנגנון נוסף, PARP נשאר “תקוע” על ה־DNA. כשמזלג השכפול מגיע לאזור הזה, PARP התקוע מפריע לפולימראז להתקדם, ויכול לגרום לקריסה של מזלג השכפול ולנזקי DNA חמורים יותר.
Synthetic lethality
PARP inhibitors יעילים במיוחד בהקשרים של synthetic lethality.
הרעיון: פגיעה אחת לבדה לא בהכרח הורגת את התא, אבל שתי פגיעות יחד כן.
לדוגמה:
- מצד אחד, מעכבים PARP ויוצרים עומס של SSBs שיכולים להפוך ל־DSBs.
- מצד שני, אם לתא יש BRCA deficiency, יש לו בעיה בתיקון DSBs.
השילוב בין יצירת שברים לבין חוסר יכולת לתקן אותם מוביל למוות תאי. לכן בחולות עם רקע של BRCA deficiency, PARP inhibitors יכולים להיות יעילים במיוחד.
המנגנון יורחב בשיעור על תיקון double-strand breaks ו־homologous recombination.
Double-strand breaks - DSBs
בחלק האחרון עברנו ל־Double-strand breaks.
Double-strand break הוא קריעה של שני הגדילים של ה־DNA, כלומר שבירה של הכרומוזום לשני חלקים.
זה אחד הנזקים החמורים ביותר שיכולים לקרות ל־DNA, משום שהוא יכול להוביל ל:
- מחיקות
- קיצור של כרומוזום
- טרנסלוקציות
- יצירת גן חדש או אונקוגן חדש
- פגיעה ב־tumor suppressor genes
לדוגמה, Philadelphia chromosome, שבו נוצר fusion בין גנים שונים, והתוצר הוא חלבון עם פעילות שמעודדת תכונות סרטניות.
מקורות ל־DSBs
- Replication fork collapse - קריסה של מזלג השכפול.
- SSB שלא תוקן לפני רפליקציה - כשמזלג השכפול פוגש שבר חד־גדילי, זה יכול להפוך ל־DSB.
- ROS - יכולים ליצור שברים, כולל שברים דו־גדיליים.
- Topoisomerase II - יוצר שבר דו־גדילי זמני כדי לשחרר מתח טופולוגי.
- Programmed recombination - תהליכים פיזיולוגיים שבהם התא יוצר שברים בכוונה, למשל V(D)J recombination במערכת החיסון.
- Meiotic recombination - לפני מיוזה יש שבירה יזומה של DNA, למשל על ידי SPO11, כדי לאפשר שחלוף בין כרומוזומים הומולוגיים.
- Ionizing radiation.
- תרופות כימותרפיות, למשל Toposide, שפוגע בפעולת Topoisomerase II ויכול לגרום ל־DSBs.
גם טיפולים כאלה יכולים ליצור סיכון לסרטן שניוני, משום שהם עצמם גורמים לנזקי DNA. לגבי Toposide סדר גודל של כ־3% סיכון לסרטן שניוני כתוצאה מהטיפול.
מנגנוני תיקון עיקריים ל־DSBs
יש שני מנגנוני תיקון עיקריים:
| מנגנון | עיקרון | מתי פעיל יותר? | דיוק |
|---|---|---|---|
| Non-Homologous End Joining - NHEJ | חיבור ישיר של הקצוות | בעיקר כשאין כרומטידה אחות זמינה, למשל G1 | יחסית error-prone |
| Homologous Recombination - HR | שימוש בכרומטידה אחות כתבנית | S phase ו־G2 | מדויק יותר |
NHEJ אינו משתמש בתבנית, ולכן הוא פחות מדויק. הוא פועל לאורך מחזור התא, אבל הבחירה בו משמעותית במיוחד כשאין כרומטידה אחות זמינה.
HR מבוסס על כרומטידה אחות כתבנית, ולכן הוא מדויק יותר, אבל הוא אפשרי בעיקר אחרי שכפול DNA, כלומר ב־S phase או G2.
תיקון DSB כתגובה מערכתית
כשיש DSB, התא לא רק “מדביק” את הקצוות. הוא צריך לתאם כמה מערכות:
- תיקון DNA
- עצירת מחזור התא
- בחירת מנגנון תיקון לפי שלב מחזור התא
- פתיחת כרומטין סביב האזור
- הגברת הסיגנל כדי שחלבונים רבים יגויסו לאתר הנזק
החלבון שמהווה מתאם מרכזי הוא ATM; מעין “רמטכ״ל” של התגובה ל־DSB, כי הוא מתאם בין תיקון DNA, מחזור התא וכרומטין.
Non-Homologous End Joining - NHEJ
NHEJ חוזר לאותה תבנית כללית של מנגנוני תיקון:
- זיהוי
- עיבוד
- תיקון
זיהוי והגנה על הקצוות
החלבון הראשון שמזהה את הקצוות הוא Ku.
Ku מזהה קצוות של DNA, נקשר אליהם ומגן עליהם. קצוות DNA הם אזורים רגישים במיוחד, ולכן התא צריך לייצב אותם מהר.
לאחר מכן Ku מגייס את DNA-PK, שפועל כמעין גשר בין שני הקצוות ומחזיק אותם קרובים זה לזה.
עיבוד הקצוות
לפני שאפשר לחבר את הקצוות, צריך לנקות אותם ולהכין אותם לליגציה.
דוגמאות לפקטורים רלוונטיים (לכאורה לא נדרש לזכור את כולם):
- Artemis
- פולימראזות שונות
- PNKP
המטרה להגיע לקצוות שניתנים לחיבור: הידרוקסיל בצד אחד ופוספט בצד השני.
חיבור הקצוות
בשלב התיקון:
- XRCC4 פועל כ־scaffold protein, בדומה ל־XRCC1 בתיקון SSBs.
- Ligase IV מחבר את הקצוות.
הדגש הוא ש־XRCC1 קשור ל־SSB repair, ואילו XRCC4 קשור ל־DSB repair דרך NHEJ.
NHEJ deficiency
כשיש חסר ב־NHEJ, למשל בפקטורים כמו ligase, Artemis או DNA-PK, עלולות להופיע כמה בעיות:
- רגישות לקרינה מייננת - כי קרינה מייננת יוצרת DSBs.
- מוות תאי מוגבר - הצטברות DSBs יכולה להוביל לאפופטוזיס.
- סיכון מוגבר לסרטן - בגלל תיקון לקוי ושינויים גנומיים.
- SCID - Severe Combined Immune Deficiency.
הקשר ל־SCID הוא דרך מערכת החיסון. כדי ליצור נוגדנים ו־T-cell receptors יש צורך ב־V(D)J recombination, תהליך שכולל יצירת DSBs וחיבור מחדש של DNA. אם אין תיקון תקין של השברים האלה, לא ניתן ליצור רפרטואר תקין של רצפטורים חיסוניים.
הסיכון הגנומי ב־NHEJ
NHEJ חיוני, אבל הוא גם יכול ליצור בעיות.
מכיוון שהוא מחבר קצוות DNA בלי להשתמש בתבנית, הוא עלול לחבר קצוות לא נכונים. זה נקרא mis-joining.
תוצאה אפשרית:
- מחיקות
- טרנסלוקציות
- חיבור בין קצוות מכרומוזומים שונים
- איבוד או הוספה של כמה נוקלאוטידים באזור החיבור
זה יכול ליצור אונקוגן חדש או לפגוע ב־tumor suppressor gene.
לכן יש פרדוקס מסוים: גם חסר ב־NHEJ וגם פעילות לא מדויקת של NHEJ יכולים לתרום לסרטן.
Alternative NHEJ
אם NHEJ הקלאסי לא עובד, עדיין צריך מנגנון גיבוי כלשהו. למשל, מנגנון בשם Alternative NHEJ.
זה מנגנון גיבוי שמנסה להשתמש בהומולוגיה קצרה בקצוות כדי לחבר אותם. הוא יכול להציל את התא במצב שבו אין פתרון אחר, אבל הוא בעייתי יותר ומועד למחיקות, משום שבדרך כלל צריך להסיר כמה נוקלאוטידים כדי למצוא התאמה בין הקצוות.
גם כאן חוזר עקרון הפשרה: התא מעדיף תיקון לא מושלם על פני השארת שבר בלתי מתוקן.
דור פסקל