תוכן העניינים:
- פתיחה: על מה השיעור
- Cdx2: מה לומדים מניסוי Loss of Function
- תאי אפיתל ו־Tight Junctions
- יצירת ה־Blastocoel
- מה קורה ב־Cdx2 KO?
- ניסוי תרבית: Outgrowth של Trophectoderm
- Cdx2 מדכא Oct4 ו־Nanog ב־Trophectoderm
- Compaction
- siRNA וניסוי E-cadherin
- Polarization
- First cell fate decision: תאים חיצוניים מול תאים פנימיים
- מישור החלוקה: חלוקה סימטרית וא-סימטרית
- Cdx2, פולריות ולוקליזציה של mRNA
- Hippo signaling: איך תא יודע שהוא בפנים?
- Amot, NF2 והקשר ל־Adherens Junctions
- חיבור המודל: Cdx2, פולריות ו־Hippo
- Zygotic Genome Activation וגלי כניסה ל־ICM
- Positive feedback loops ברשת פקטורי השעתוק
- Second cell fate decision ו־FGF signaling
- רצף האירועים המרכזי
- משפטי מפתח
פתיחה: על מה השיעור
בשיעור הקודם הוצגו כמה פקטורי שעתוק חשובים בהתפתחות המוקדמת: Oct4, Nanog, Cdx2, Gata4 ו־Gata6. בשיעור הזה המוקד עובר ל־Cdx2 ולשאלה איך הוא משתתף ב־First cell fate decision, כלומר ביצירת ההבחנה בין תאים חיצוניים שיהפכו ל־Trophectoderm לבין תאים פנימיים שיהפכו ל־ICM.
בהמשך השיעור נכנס גם ה־Second cell fate decision, שבו תאי ה־ICM נפרדים לכיוון Epiblast או Primitive endoderm.
Cdx2: מה לומדים מניסוי Loss of Function
כדי להבין את התפקיד של Cdx2, מסתכלים על עובר תקין לעומת עובר מוטנט שבו Cdx2 חסר.
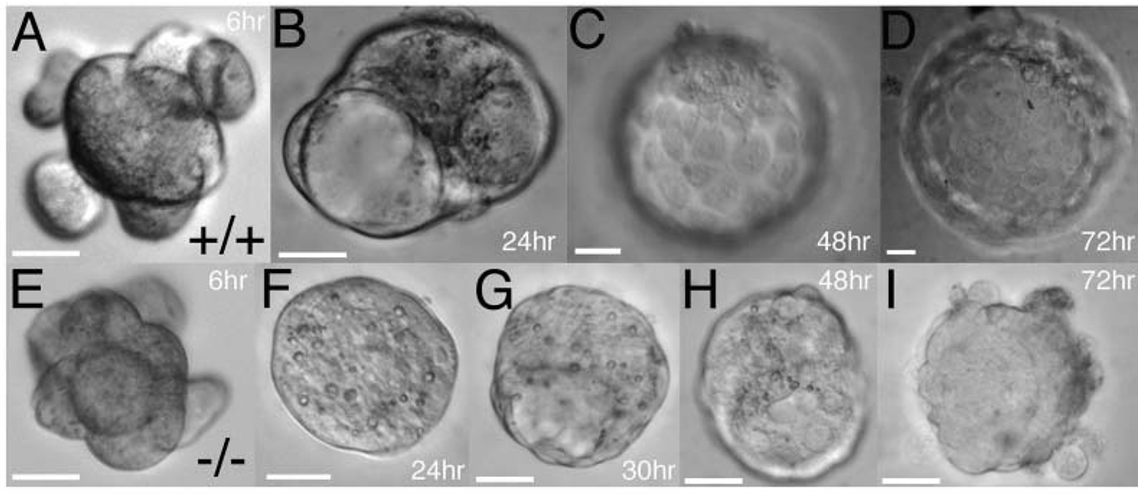
בעובר תקין, לאורך הזמן מתקבל בלסטוציסט עם Trophectoderm, Blastocoel ו־ICM.
במוטנט ל־Cdx2 מתחיל להיווצר Blastocoel, ולכן נראה שהעובר מתחיל להיכנס למסלול של יצירת בלסטוציסט. אבל תוך זמן קצר ה־Blastocoel נעלם, מתרחשת קריסה ומתקבל גוש תאים.
המסקנה הראשונה: העובר מסוגל להתחיל תהליך של יצירת Blastocoel ללא Cdx2, אבל לא לשמר אותו.
כדי להבין למה זה קורה, צריך להבין קודם איך נוצר ה־Blastocoel ומהו מחסום אפיתליאלי.
תאי אפיתל ו־Tight Junctions
תאי אפיתל הם שכבת תאים שמפרידה בין שני חללים. לדוגמה, תאי אפיתל יכולים להפריד בין חלל מערכת העיכול לבין הגוף, או בין לומן של כלי דם לבין הרקמה שסביבו.
לתאי אפיתל יש בדרך כלל שני צדדים:
| צד בתא | משמעות |
|---|---|
| Basal / Basolateral domain | הצד שפונה לממברנה בזלית או לתאים שכנים |
| Apical domain | הצד שפונה לחלל או לסביבה החיצונית |
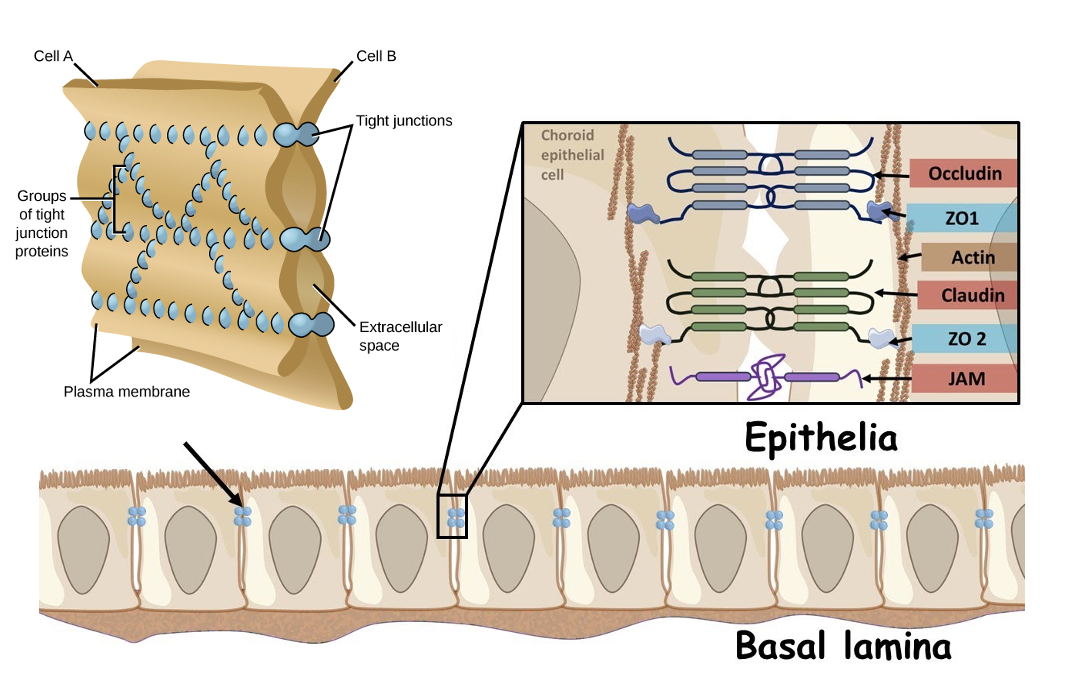
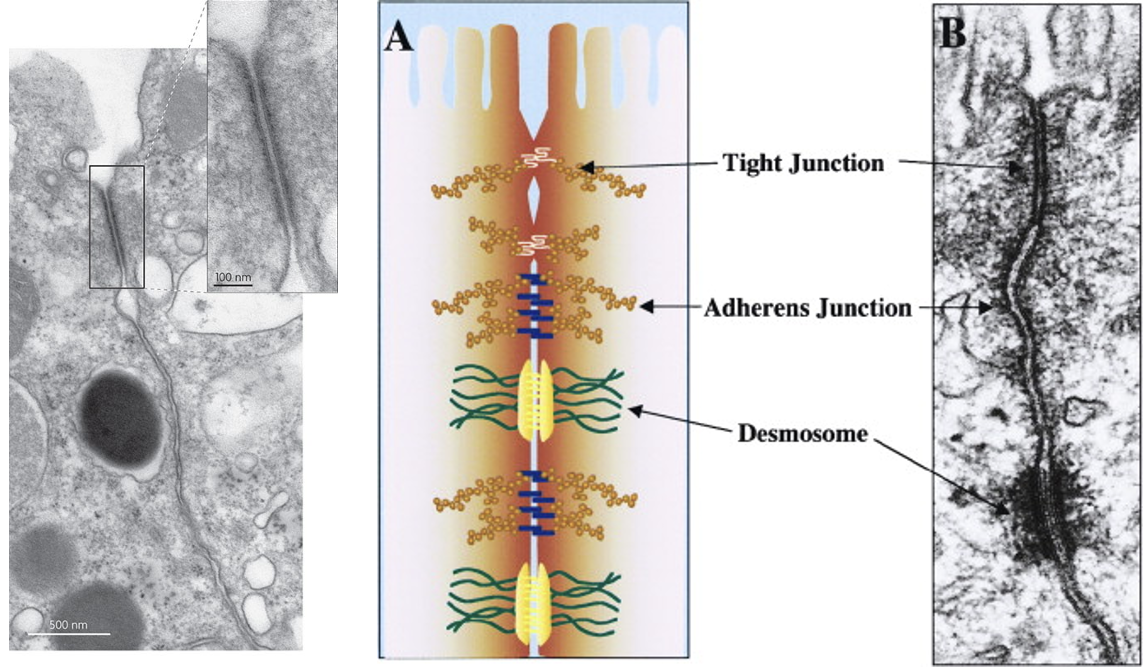
בקצה האפיקלי של תאי אפיתל יכולים להופיע Tight junctions. אלה קומפלקסים של חלבונים שמצמידים את הממברנות של שני תאים שכנים, כך שהמעבר בין התאים נחסם.
ההבדל בין שני סוגי החיבורים:
| מבנה | תפקיד עיקרי בשיעור |
|---|---|
| Adherens junctions | הצמדה מכנית בין תאים, בין היתר דרך E-cadherin |
| Tight junctions | יצירת מחסום שמונע מעבר בין התאים |
הנקודה החשובה היא ש־Tight junctions לא מאפשרים למים, יונים או חומרים אחרים לעבור בין התאים. אם משהו עובר מצד אחד לצד השני, הוא צריך לעבור דרך התא עצמו ולא בין התאים.
יצירת ה־Blastocoel
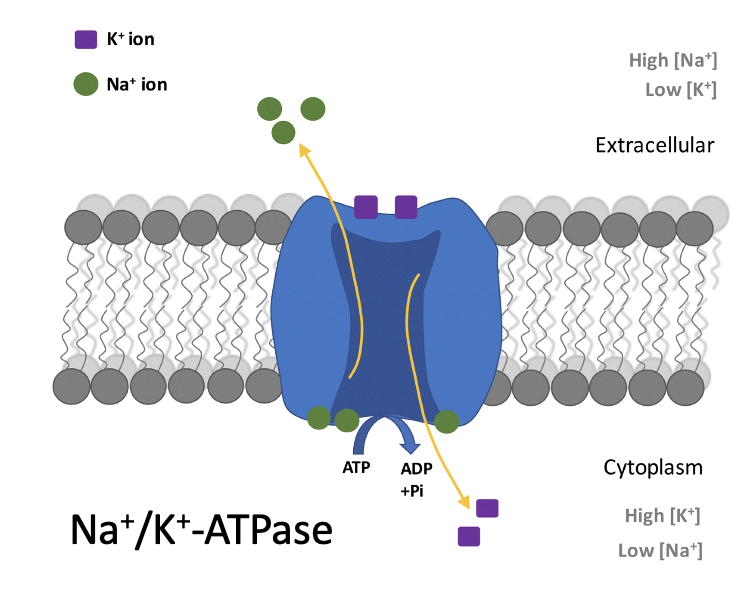
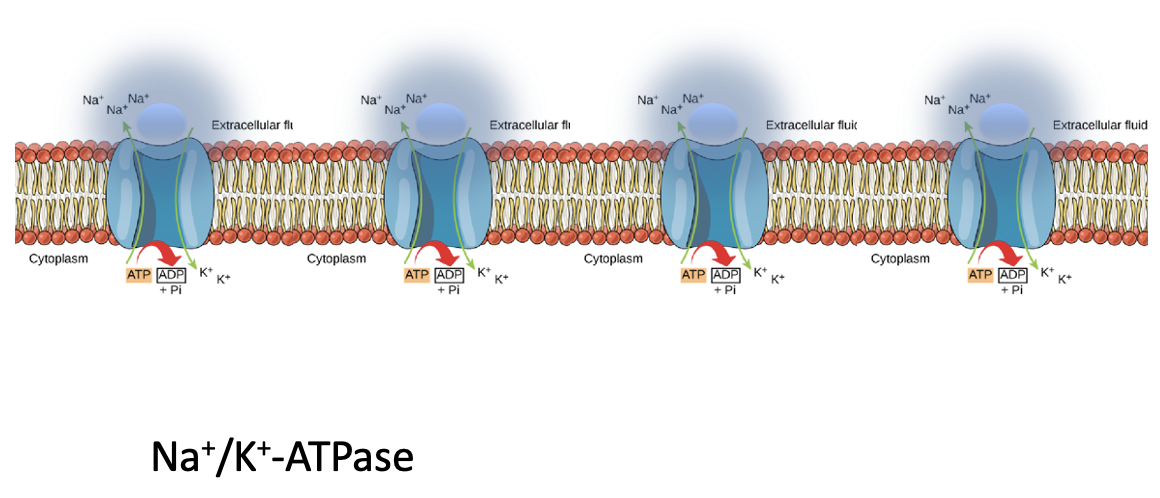
בשלב המורולה יש תאים פנימיים ותאים חיצוניים. כל התאים מחוברים זה לזה דרך Adherens junctions, אבל רק התאים החיצוניים מתנהגים כתאים אפיתליאליים ויוצרים Tight junctions בצד האפיקלי שלהם.
המשאבה בתמונה למעלה מוציאה יוני נתרן ומכניסה יוני אשלגן תוך שימוש ב־ATP. החשיבות כאן אינה בעיקר המטען החשמלי אלא שינוי ריכוז היונים: כאשר ריכוז היונים עולה באזור שבין התאים, נוצר לחץ אוסמוטי שמושך מים.
הסדר הוא כזה:
- המשאבות יוצרות ריכוז יונים גבוה באזור הבזולטרלי, בין התאים.
- מים נעים דרך התאים בעקבות הלחץ האוסמוטי.
- נוצרים חללים קטנים של נוזל בין התאים.
- החללים הקטנים נעים, מתאחדים ויוצרים חללים גדולים יותר.
- בסופו של דבר נוצר חלל מרכזי אחד - Blastocoel.
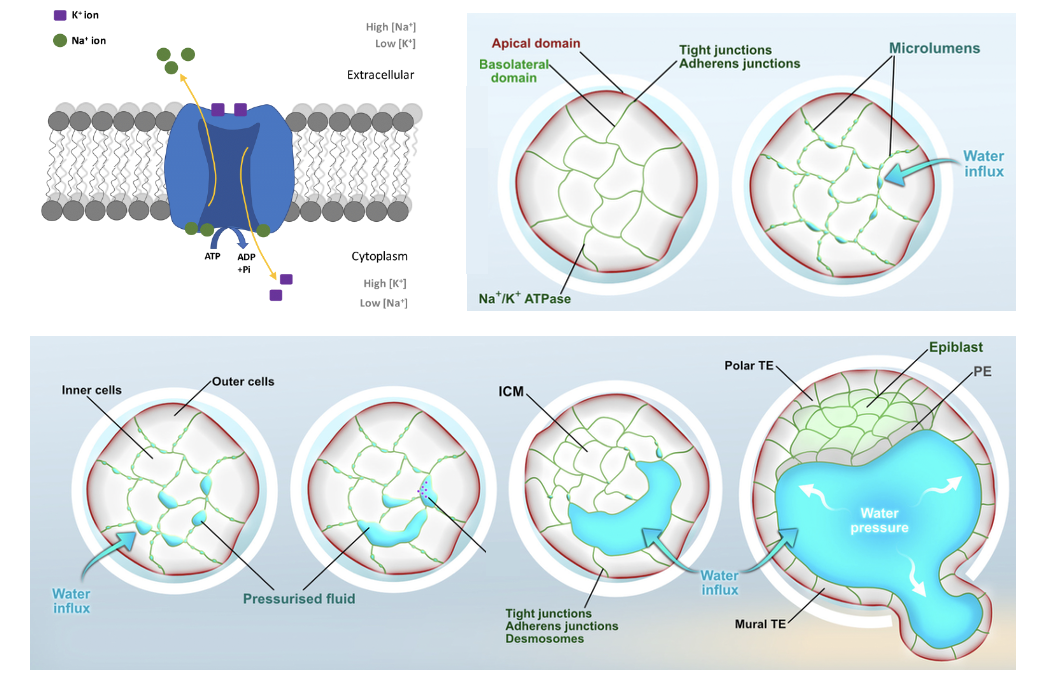
ה־Tight junctions חשובים משום שהם סוגרים את העובר כמערכת. אם לא היה מחסום כזה, הנוזלים היו יכולים לברוח החוצה, והחלל לא היה נשמר.
למה ה־Blastocoel חשוב?
ככל שה־Blastocoel גדל, הוא יוצר לחץ מבפנים כלפי חוץ. בשלב היציאה מה־Zona Pellucida, העובר מפריש פרוטאזות באזור מסוים ויוצר פתח קטן ב־Zona Pellucida. אבל הפתח לבדו אינו מספיק; הלחץ שנוצר על ידי ה־Blastocoel דוחף את העובר החוצה.
ה־Zona Pellucida קשיחה, אבל מים יכולים לעבור דרכה. מה שנשמר הוא המחסום של התאים החיצוניים, דרך ה־Tight junctions.
מה קורה ב־Cdx2 KO?
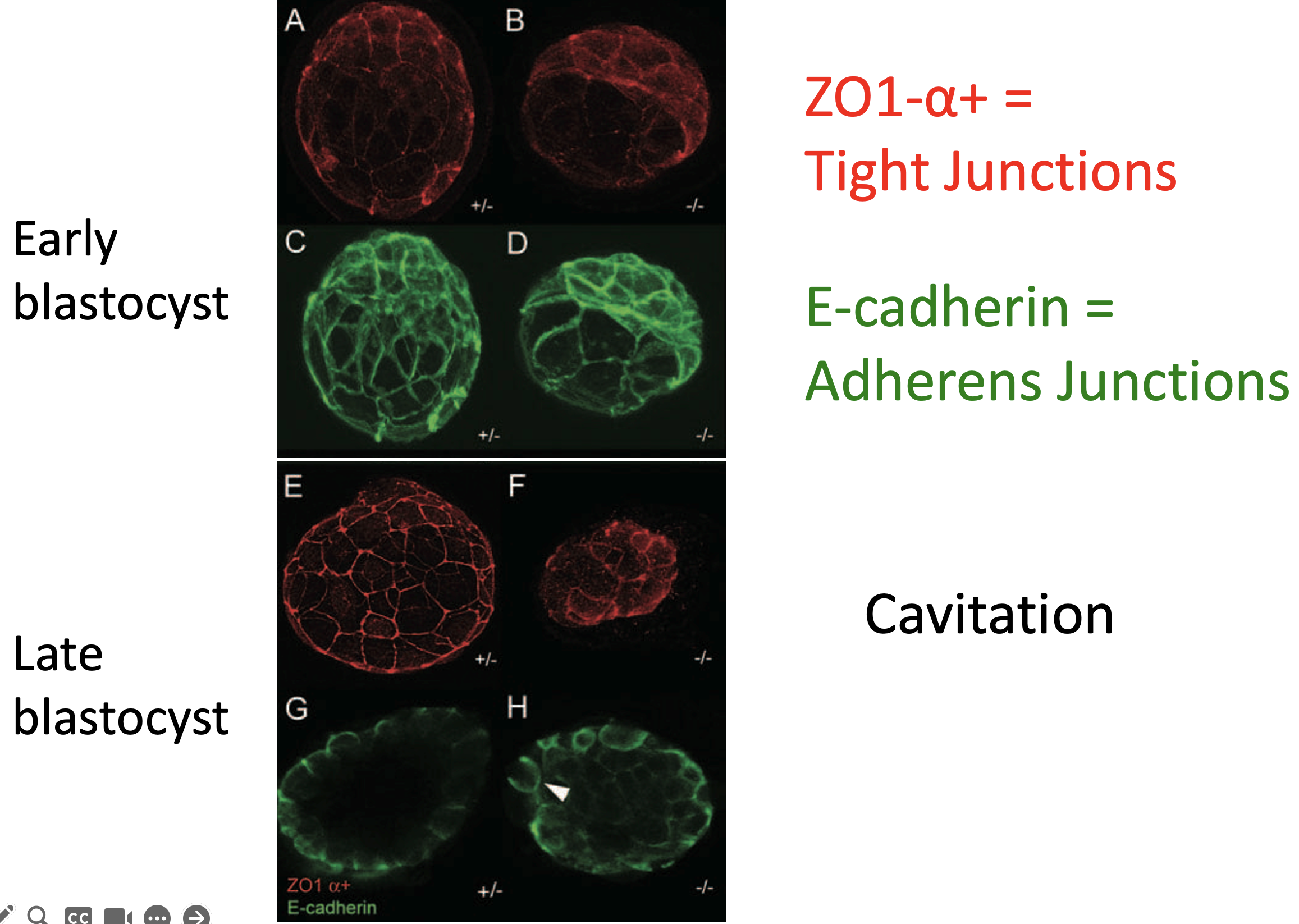
בתמונה, העוברים התקינים נמצאים משמאל, והמוטנטים ל־Cdx2 מימין.
בבלסטוציסט מוקדם, גם במוטנט ניתן לראות התחלה של Tight junctions ו־E-cadherin. אבל בבלסטוציסט מאוחר, בעובר התקין יש Blastocoel ברור ומחסום אפיתליאלי יציב, ואילו במוטנט ה־Tight junctions מתפרקים או נעשים לא תקינים.
המשמעות היא שה־Blastocoel מתחיל להיווצר, אבל אינו מוחזק. ברגע שה־Tight junctions לא יציבים, הנוזלים אינם נשמרים, והחלל קורס.
ללא Cdx2, התאים החיצוניים (outer cells) מאבדים את התכונות האפיתליאליות הדרושות לשימור ה־Blastocoel.
ניסוי תרבית: Outgrowth של Trophectoderm
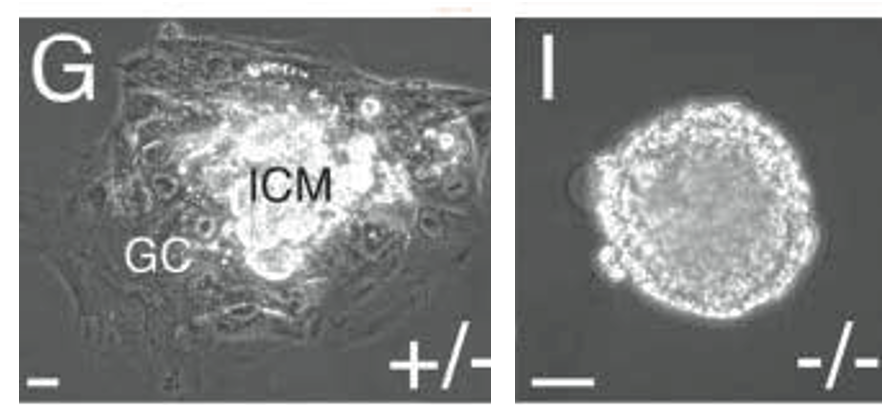
בניסוי נוסף לוקחים את העובר ושמים אותו בצלחת בתנאי תרבית.
בעובר תקין, ה־Trophectoderm נפרס על הצלחת, וה־ICM יושב עליו. במוטנט ל־Cdx2, נראה שאין Trophectoderm מתפקד, אלא בעיקר גוש תאים שנראה כמו ICM.
Cdx2 מדכא Oct4 ו־Nanog ב־Trophectoderm
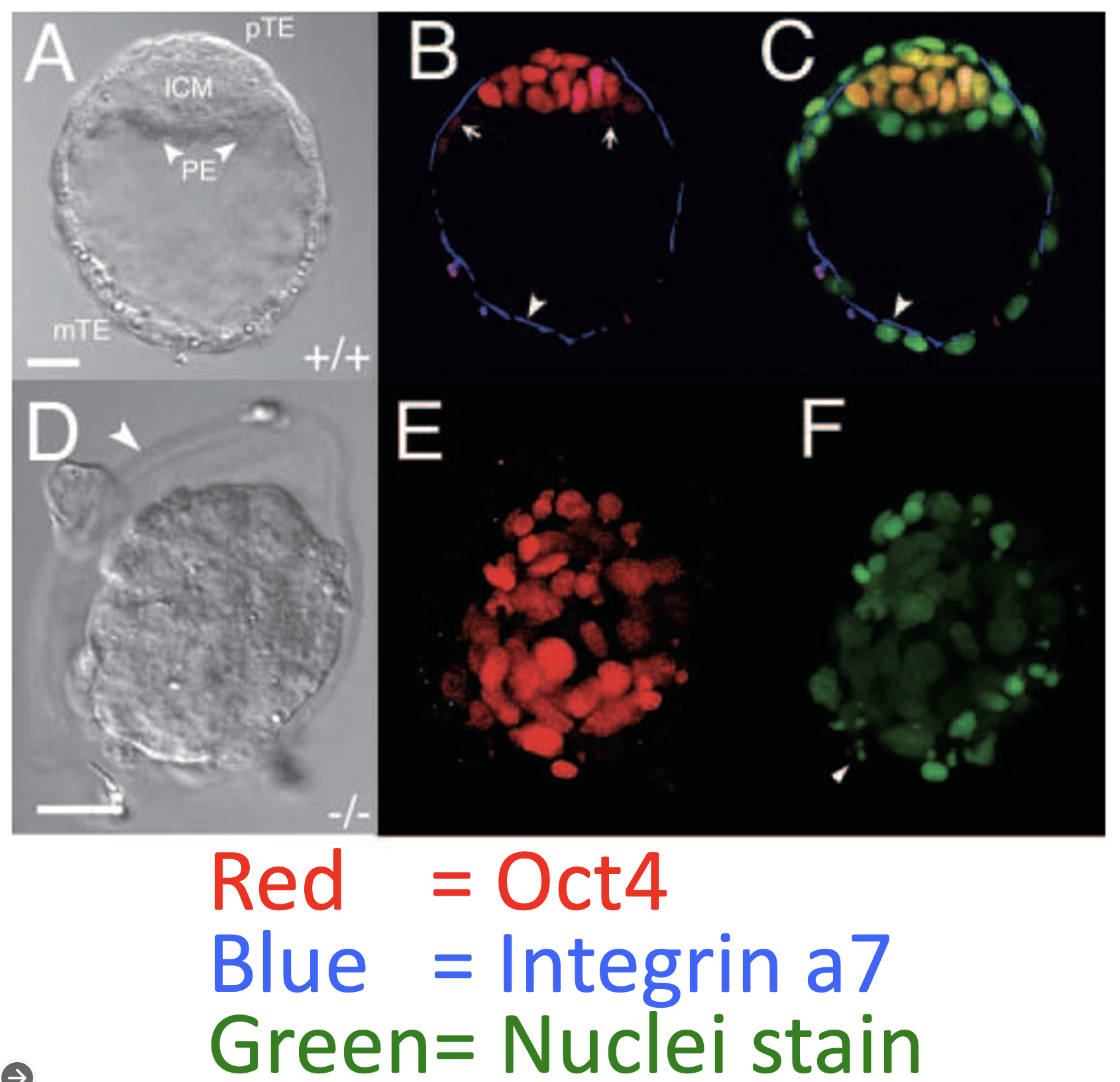
בצביעה שבתמונה השתמשו ב־Integrin α7 (צבע כחול) כמרקר של Trophectoderm וב־Oct4 (צבע אדום) כמרקר שקשור ל־ICM.
במוטנטים ל־Cdx2, כמעט כל התאים מבטאים Oct4 (צבע אדום בתמונה E), בעוד שמרקר ה־Trophectoderm אינו מופיע כמו בעובר התקין (בתמונה E לא רואים את העיגול הכחול שרואים ב־B). המשמעות היא שאין הפרדה תקינה בין תאי ICM לבין Trophectoderm.
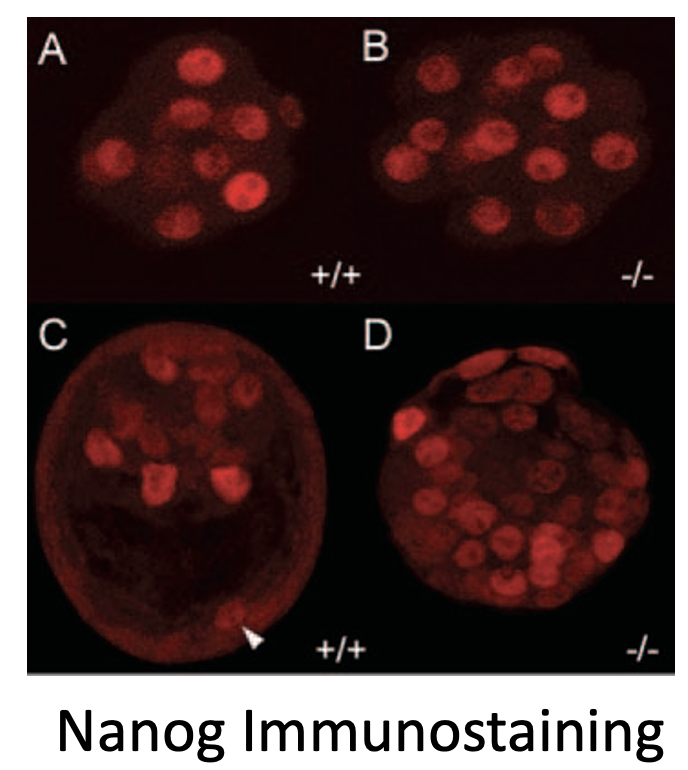
גם בבחינת Nanog מתקבלת תמונה דומה: במוטנט, תאים רבים מבטאים Nanog.
המסקנה החשובה: Cdx2 הוא רפרסור של Oct4 ושל Nanog בתאי ה־Trophectoderm.
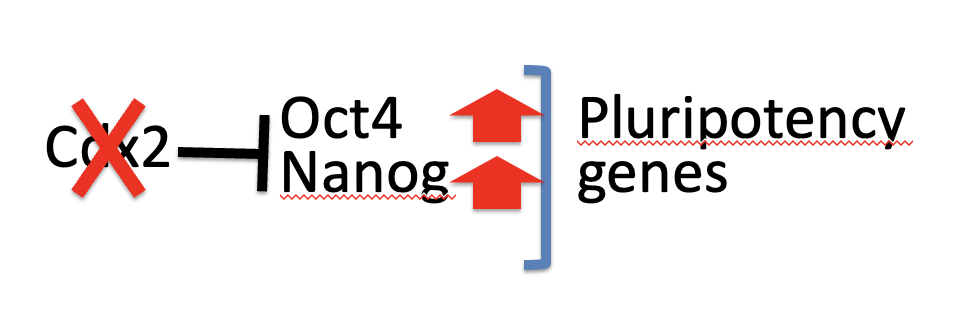
כלומר, כדי שתא חיצוני יהפוך ל־Trophectoderm, צריך למנוע בו ביטוי של Oct4 ו־Nanog. לעומת זאת, כדי שתא יהיה ICM, צריך להוריד את Cdx2 ולאפשר ל־Oct4 ול־Nanog להתבטא (כמו בתמונה למעלה).
Compaction
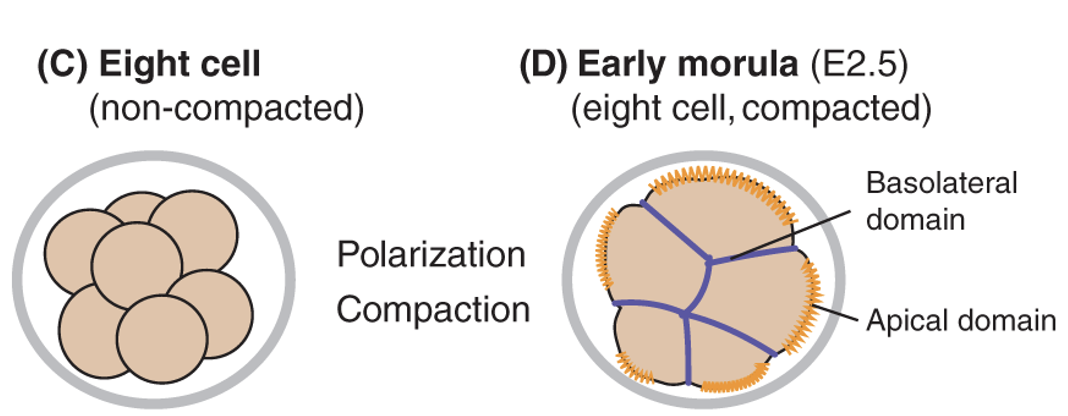
במעבר סביב שלב שמונת התאים מתרחשים שני תהליכים חשובים:
- Compaction - התאים נצמדים זה לזה ונראים פחות כבלסטומרים נפרדים.
- Polarization - התאים מקבלים צד אפיקלי וצד בזולטרלי.
ב־Compaction, הבלסטומרים נצמדים זה לזה בעיקר דרך Adherens junctions, שבהם משתתף E-cadherin.
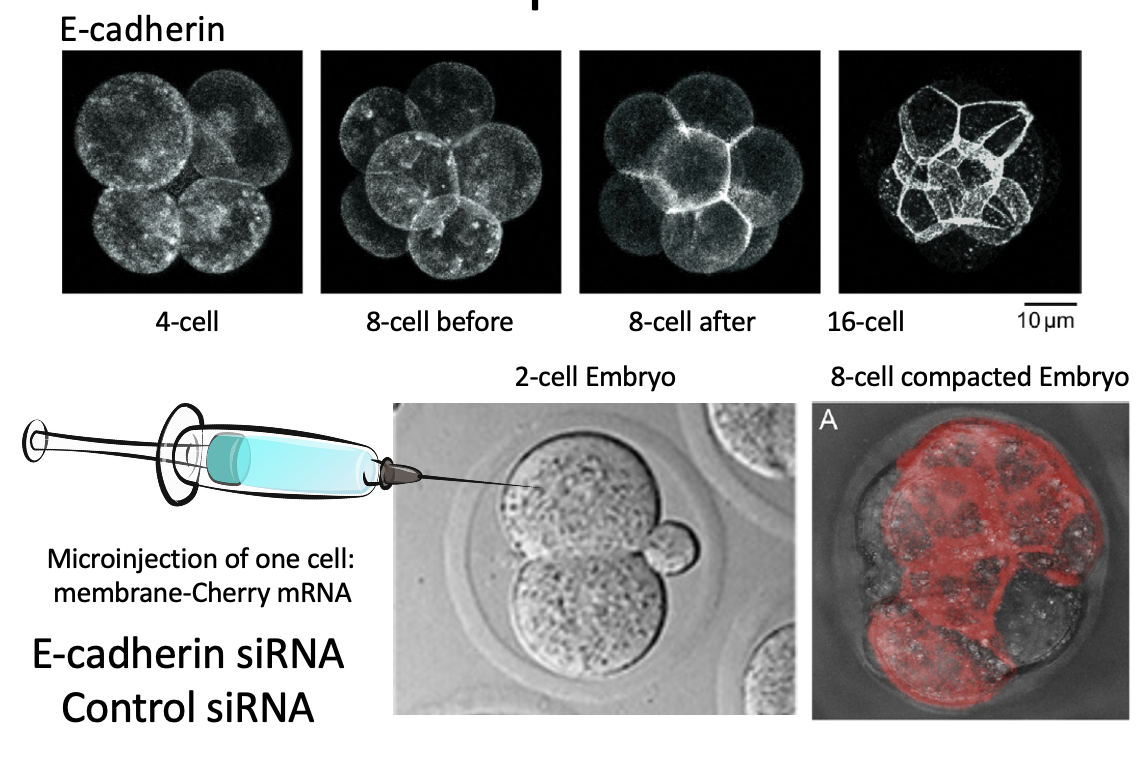
בתחילת הדרך E-cadherin נמצא על פני הממברנה, אבל לאחר Compaction הוא מתרכז באזורי המגע בין התאים. עצם הנוכחות של E-cadherin על הממברנה אינה מספיקה; צריך שייווצרו בין התאים Adherens junctions פעילים.
siRNA וניסוי E-cadherin
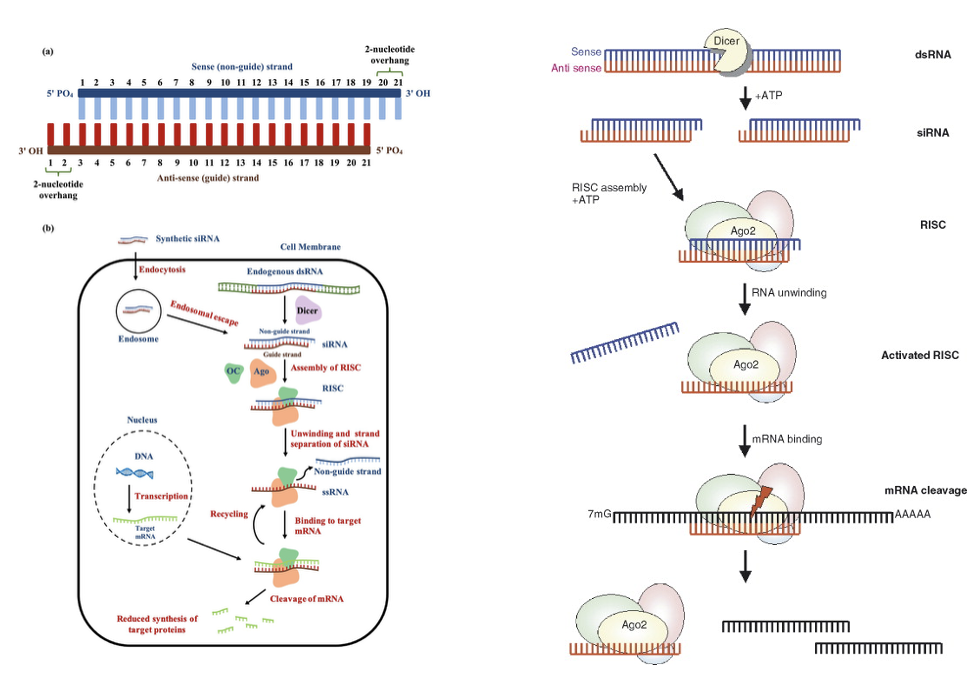
העיקרון של siRNA: מולקולות RNA דו־גדיליות קצרות יכולות להוביל לפירוק RNA מטרה ספציפי, וכך להוריד ביטוי של גן מסוים. המנגנון הביולוגי כולל חיתוך של dsRNA על ידי Dicer, ובהמשך שימוש בקומפלקס שמזהה את ה־RNA המתאים ומוביל לפירוקו.
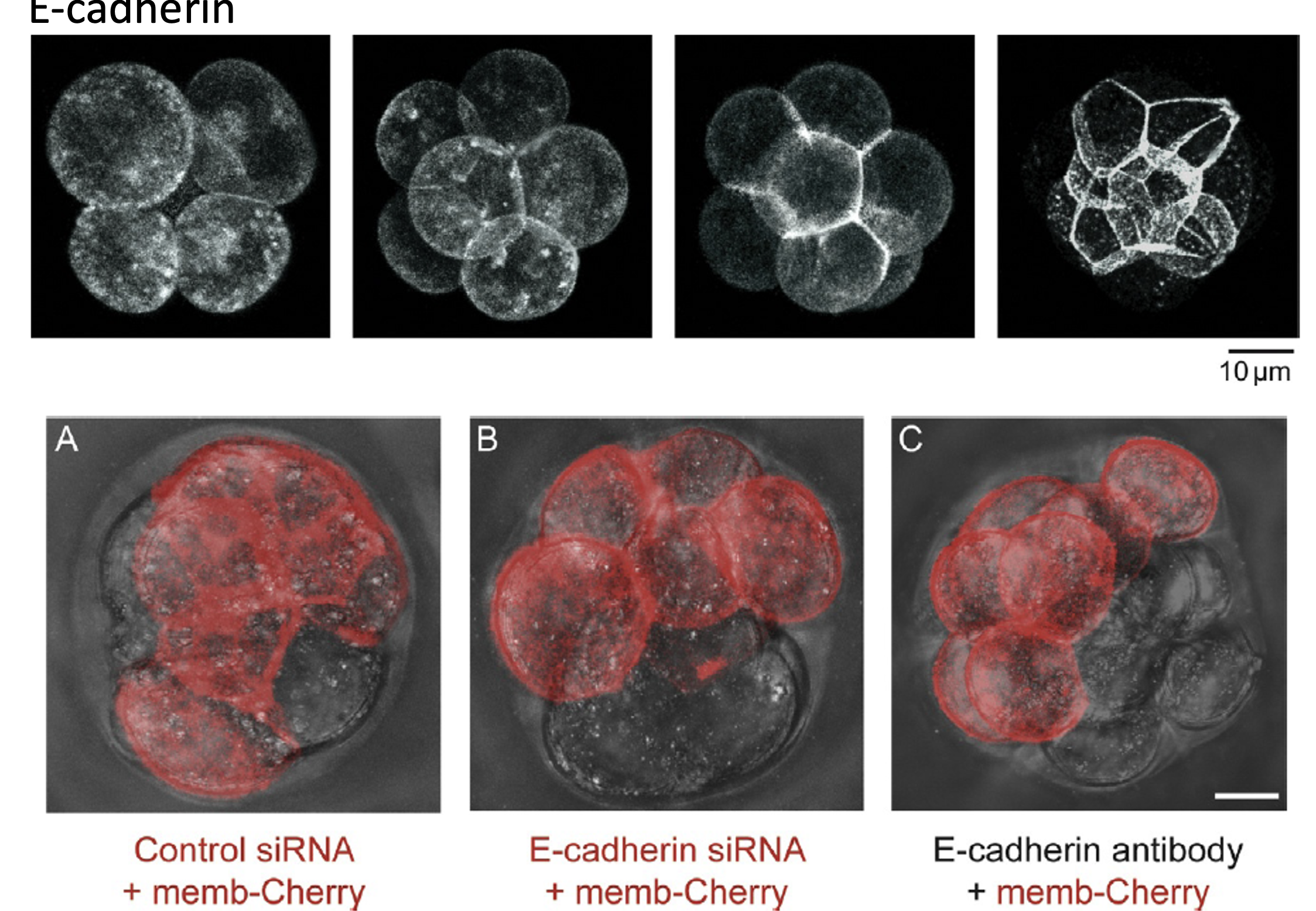
בניסוי הזה מזריקים לתא אחד בלבד בעובר שנמצא בשלב של שני תאים mRNA שמקודד לסמן אדום. מכיוון שרק תא אחד קיבל את ה־mRNA, רק הצאצאים שלו יהיו מסומנים באדום.
אחרי שהעובר ממשיך להתחלק, בודקים איפה נמצאים התאים האדומים. אם רואים שחצי מהעובר אדום וחצי מהעובר לא אדום, המשמעות היא שהצאצאים של כל אחד משני התאים המקוריים נשארו יחסית יחד. כלומר, התאים לא התערבבו באקראיות מלאה בתוך העובר.
במילים פשוטות: הסמן האדום משמש למעקב אחרי “משפחה” אחת של תאים, ומראה שבשלבים האלה עדיין אפשר לזהות מאיזה תא מוקדם הם הגיעו.
השלב הבא הוא להזריק גם siRNA נגד E-cadherin.
הביקורת חשובה: ייתכן שההזרקה עצמה, הסמן האדום, או עצם הכנסת siRNA גורמים להשפעה. לכן משתמשים גם ב־siRNA אקראי שאינו מכוון נגד גן ספציפי.
התוצאות:
| טיפול | מה רואים? | מסקנה |
|---|---|---|
siRNA ביקורת 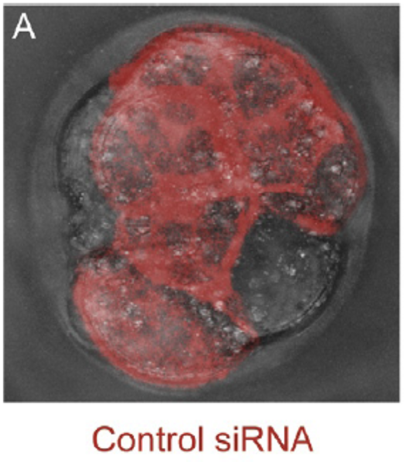 | התאים המסומנים משתלבים בעובר שעובר Compaction | עצם ההזרקה אינה מספיקה כדי לשבש Compaction |
siRNA נגד E-cadherin 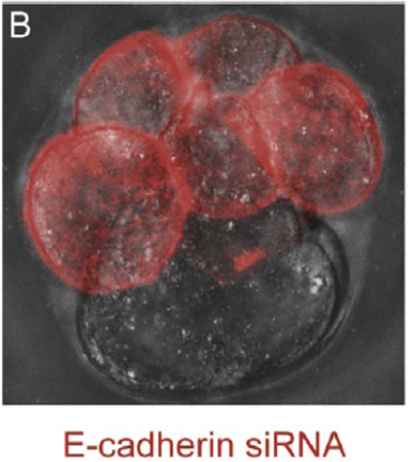 | התאים שבהם הורד E-cadherin נשארים עגולים ואינם משתלבים היטב | E-cadherin דרוש ל־Compaction |
נוגדן חוסם נגד E-cadherin 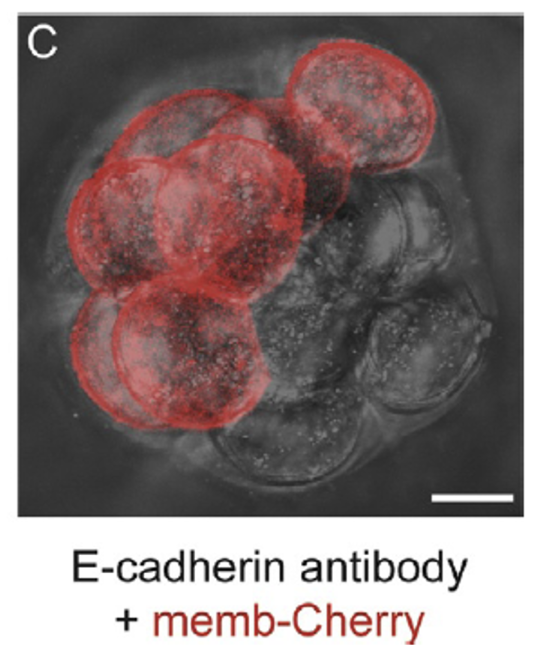 | כל התאים נפגעים ולא עוברים Compaction תקין | הפעילות הישירה של E-cadherin חשובה לתהליך |
איך Compaction נוצר בפועל?
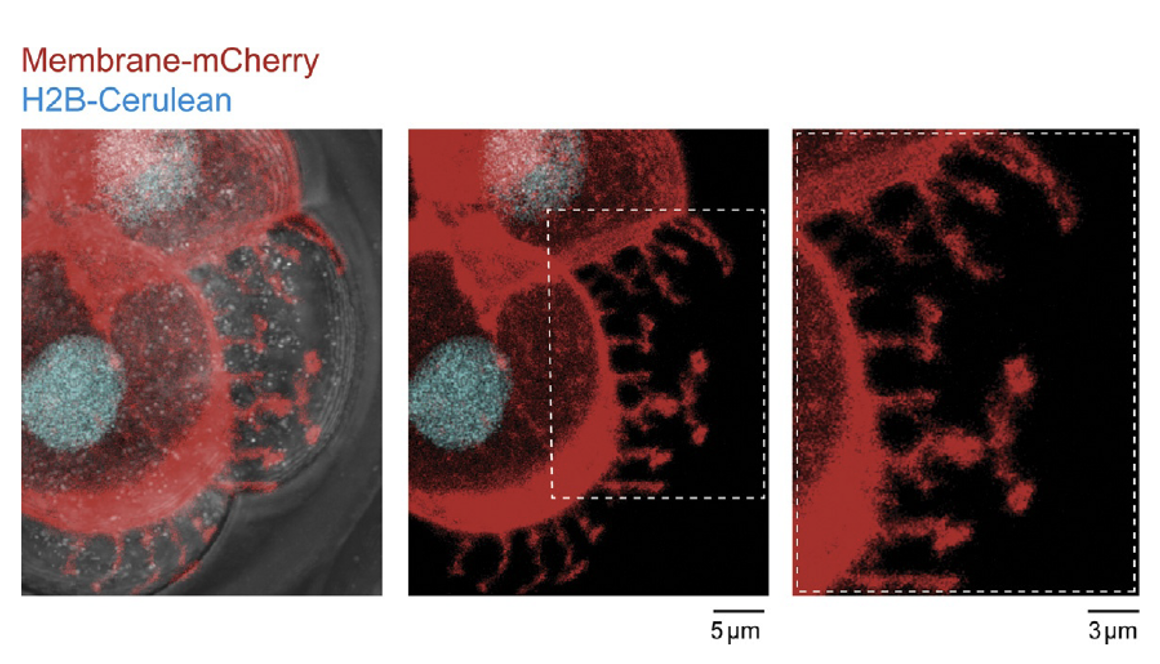
התאים שולחים שלוחות דמויות זרועות, filopodia, שתופסות את הממברנה של תאים שכנים ומקרבות אותם. התהליך תלוי ב־E-cadherin.
Polarization
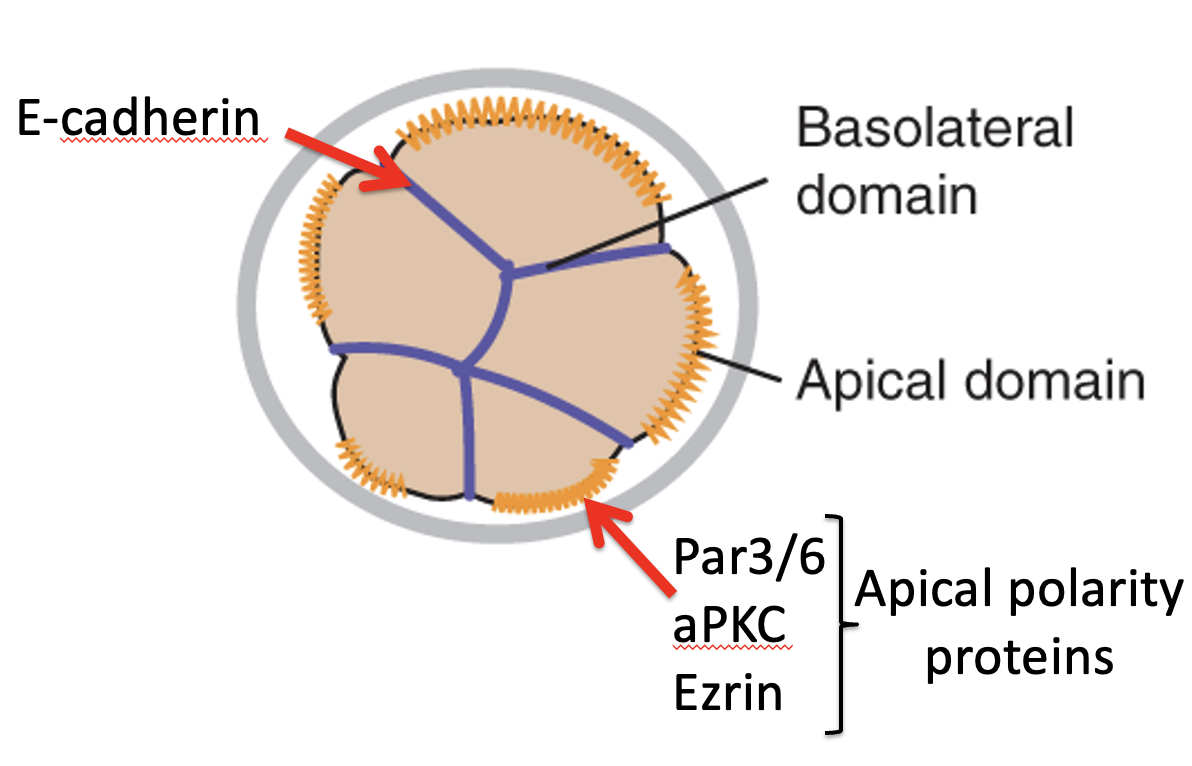
במקביל ל־Compaction, התאים עוברים Polarization. המשמעות היא שהתא כבר אינו אחיד מכל צדדיו: בצד אחד יש קומפלקס אפיקלי, ובצד אחר יש מגעים עם תאים שכנים.
בצד האפיקלי מופיעים חלבונים כמו Par3, Par6, aPKC ו־Ezrin. הם יוצרים את ה־Apical polarity complex.
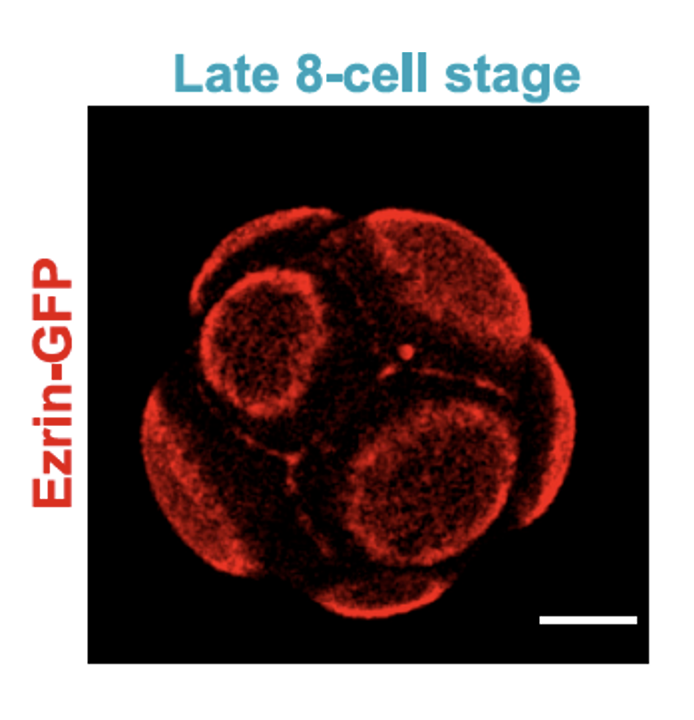
בצביעה של Ezrin ניתן לראות מעין כיפה אפיקלית. הכיפה הזאת מייצגת את האזור שבו מרוכזים חלבוני הפולריות האפיקלית.
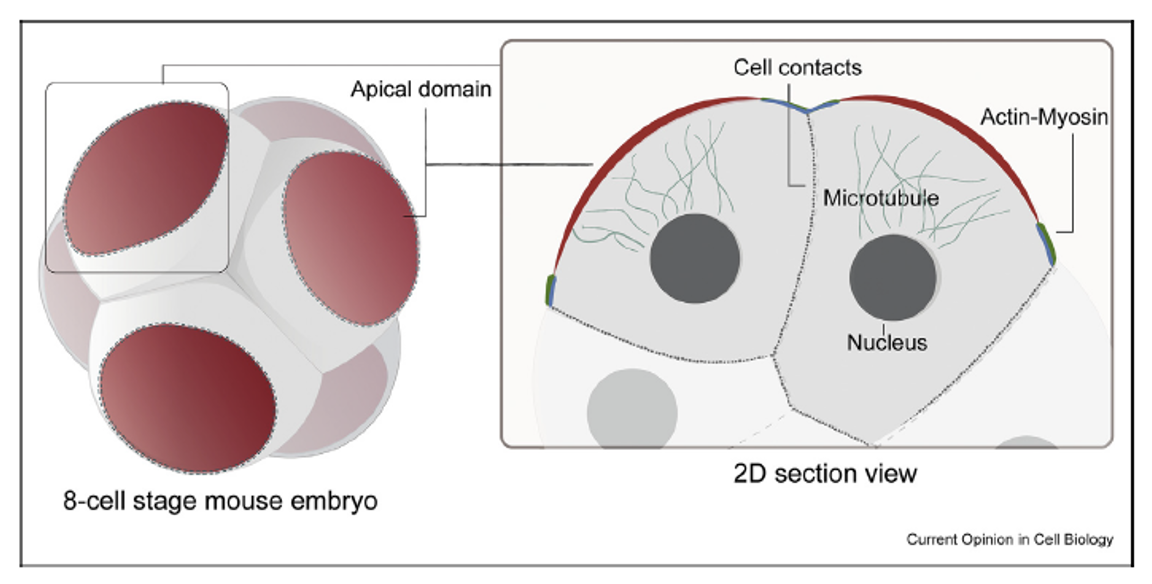
הכיפה האפיקלית מוקפת בטבעת של אקטין-מיוזין. בנוסף לכך, המיקרוטובולים מכוונים מהגרעין לכיוון האזור האפיקלי.
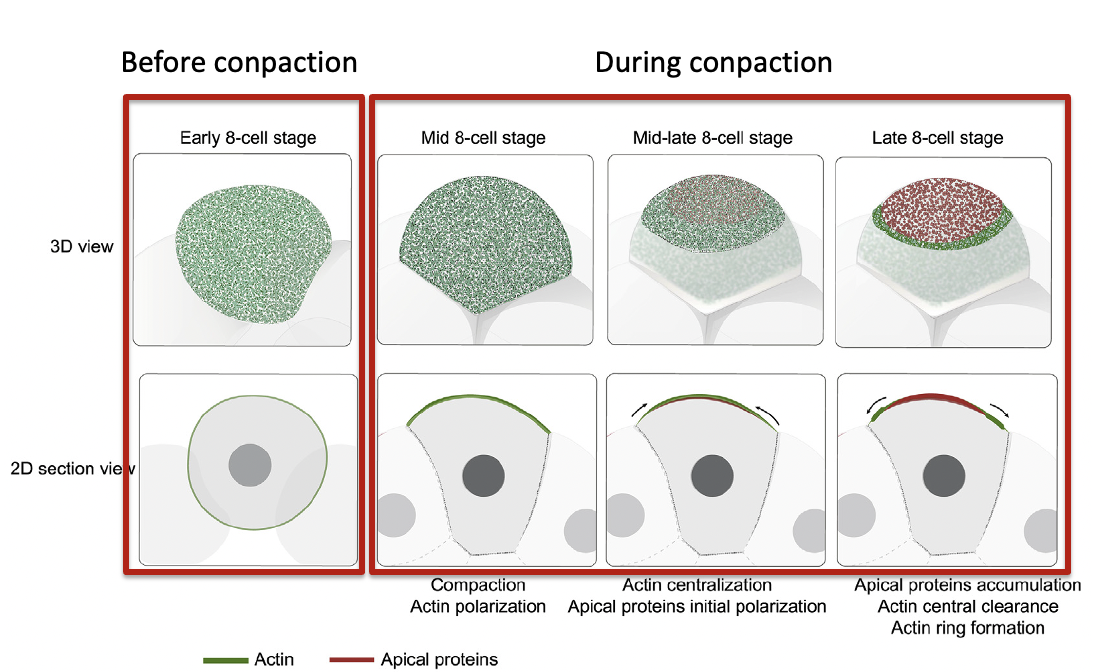
בהתחלה אקטין מתרכז באזור החופשי ממגע עם תאים אחרים. בהמשך, חלבוני הפולריות האפיקלית מתרכזים במרכז האזור, והאקטין נדחק לפריפריה ויוצר טבעת.
Compaction ו־Polarization קשורים זה לזה, אבל אינם תלויים לחלוטין זה בזה.
First cell fate decision: תאים חיצוניים מול תאים פנימיים
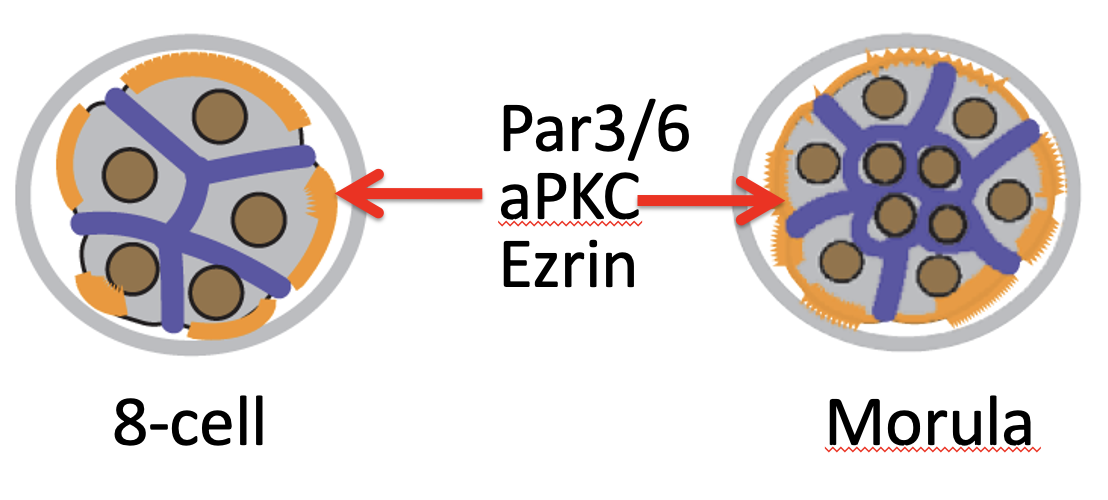
לפני ההבחנה בין תאים פנימיים וחיצוניים, בעובר בן שמונה תאים: התאים פולריים. לאחר מכן מתקבל מצב שבו:
| אוכלוסייה | מצב פולריות | גורל עיקרי |
|---|---|---|
| תאים חיצוניים | פולריים | Trophectoderm |
| תאים פנימיים | לא פולריים | ICM |
השאלה המרכזית היא איך עוברים ממצב סימטרי יחסית למצב שבו יש שתי אוכלוסיות תאים שונות.
שתי היפותזות
| היפותזה | רעיון מרכזי |
|---|---|
| Inside-outside hypothesis | המיקום קובע את הפולריות: תא שבחוץ יהיה פולרי, תא שבפנים יהיה לא פולרי |
| Polarity hypothesis | הפולריות קובעת את המיקום: תא פולרי יישאר בחוץ, תא לא פולרי ייכנס פנימה |
ניסויים שמראים תמיכה בשני הכיוונים:
- אם מזיזים פיזית תא חיצוני פנימה, הוא יכול לאבד פולריות.
- אם מזיזים תא פנימי החוצה, הוא יכול להפוך לפולרי.
- אם מורידים חלבון של הקומפלקס האפיקלי, למשל Par3, התא יכול לעזוב את השכבה החיצונית ולהיכנס פנימה.
- אם גורמים לתא פנימי לבטא מרכיבי פולריות, הוא יכול להפוך לפולרי ולצאת החוצה.
המסקנה: שליטה בפולריות מאפשרת שליטה במיקום התא, ולכן היא חלק מרכזי ב־First cell fate decision.
מישור החלוקה: חלוקה סימטרית וא-סימטרית
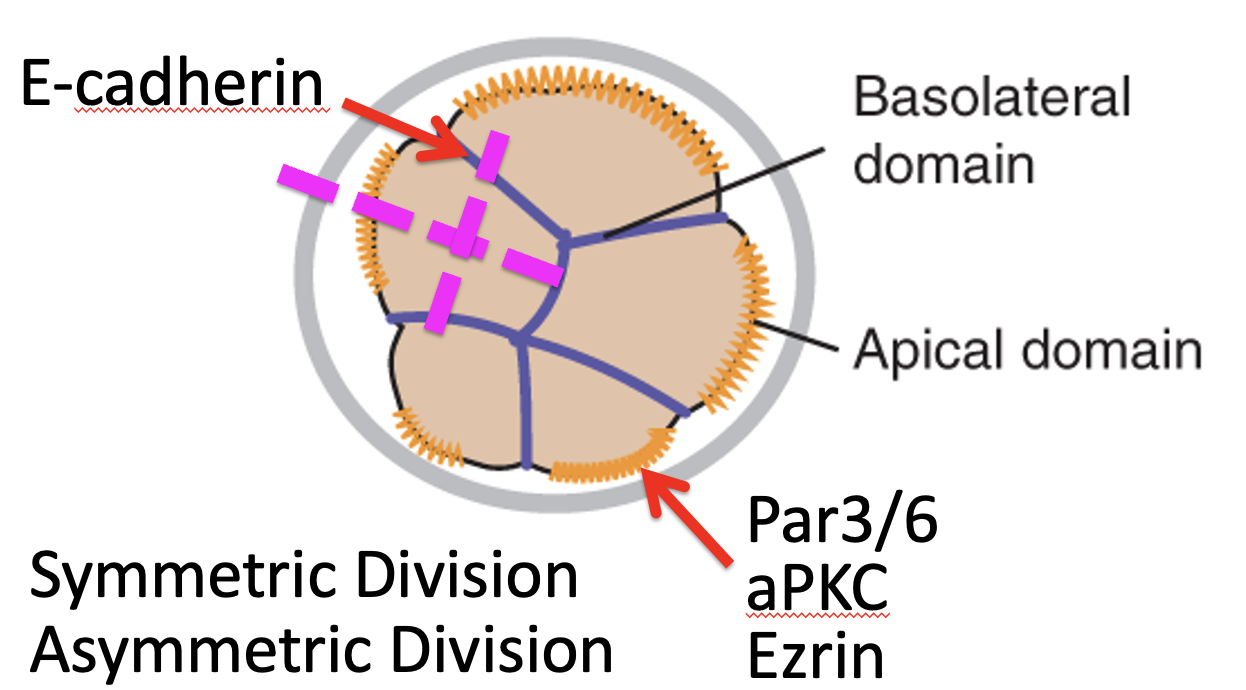
מלבד פולריות, יש פרמטר נוסף: מישור החלוקה.
| סוג חלוקה | מה מתקבל? |
|---|---|
| חלוקה סימטרית | שני תאי בת דומים, שניהם נשארים חיצוניים ופולריים |
| חלוקה א-סימטרית | תא בת אחד מקבל את הקומפלקס האפיקלי ונשאר חיצוני, ותא בת שני אינו מקבל אותו ונכנס פנימה |
לכן, כדי לבצע First cell fate decision צריך לשלוט בשני דברים:
- פולריזציה
- מישור החלוקה
Cdx2, פולריות ולוקליזציה של mRNA
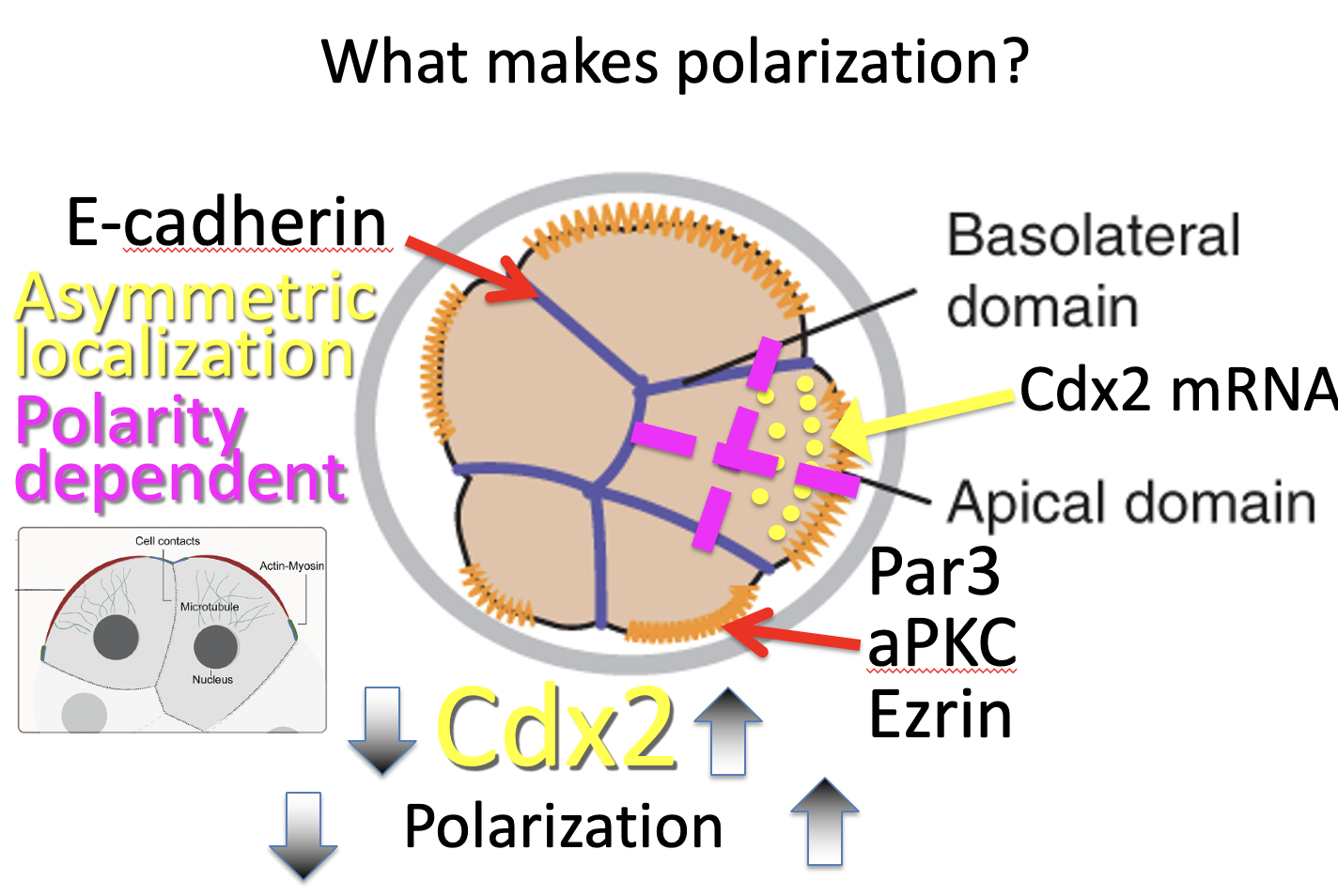
יש קשר בין רמות Cdx2 לבין מידת הפולריות של התא:
- יותר Cdx2 ← יותר פולרי
- פחות Cdx2 ← פחות פולרי
לא צריך לחשוב על פולריות כמצב בינארי של ״פולרי״ או ״לא פולרי״ בלבד, אלא כספקטרום.
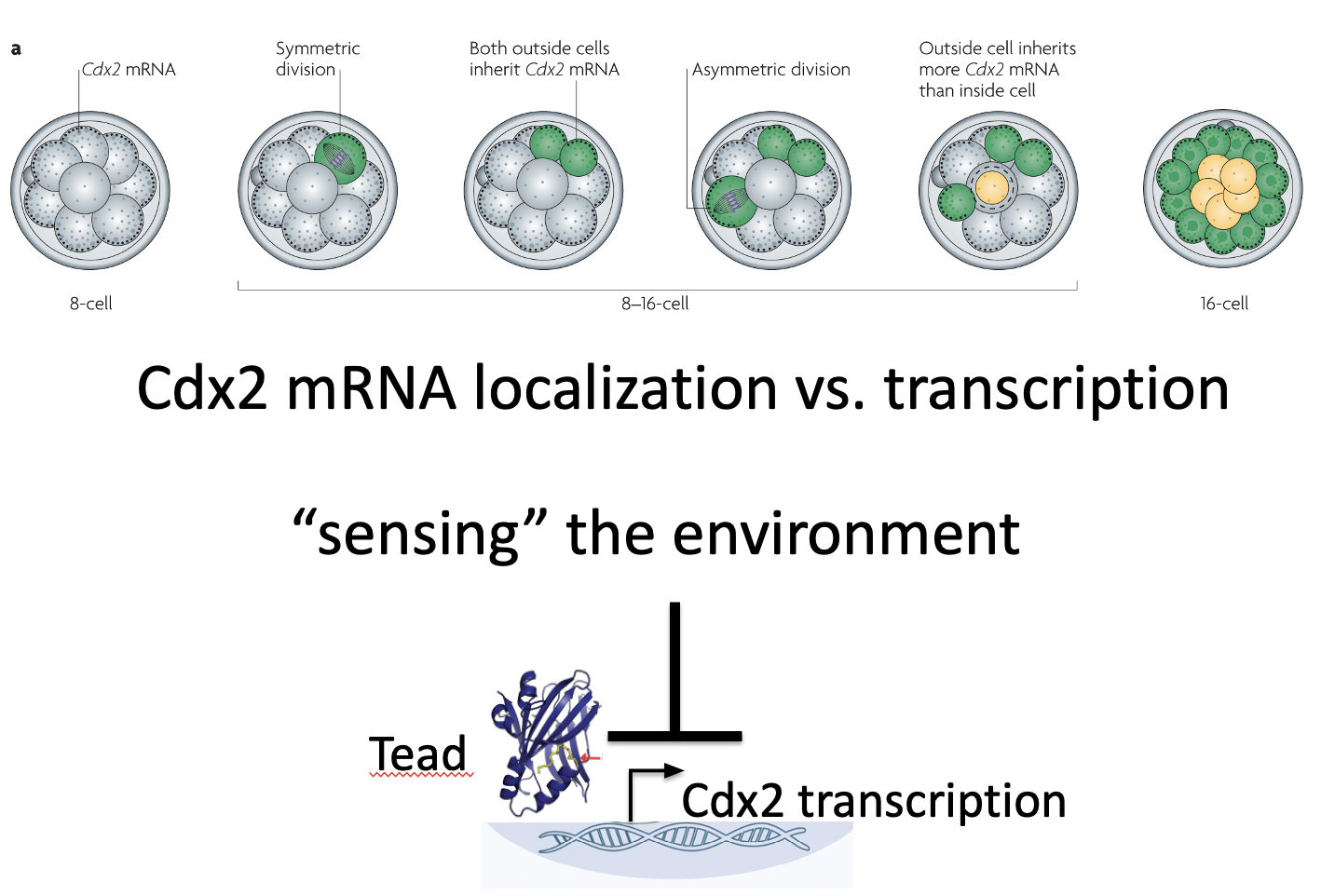
בנוסף לכך, ה־mRNA של Cdx2 לא מפוזר בציטופלזמה באופן אחיד, אלא ממוקם באזור האפיקלי של התא. זו לוקליזציה לא סימטרית של mRNA.
חשוב להפריד בין שני דברים:
| רכיב | איפה הוא רלוונטי? | משמעות |
|---|---|---|
| Cdx2 mRNA | ממוקם בצד האפיקלי | משפיע על מה כל תא בת יקבל בחלוקה |
| Cdx2 protein | פועל בגרעין | פקטור שעתוק שמפעיל תוכנית של Trophectoderm |
כאשר תא פולרי מתחלק א-סימטרית, תא הבת החיצוני מקבל יותר Cdx2 mRNA, ואילו תא הבת הפנימי מקבל מעט מאוד ממנו. כך נוצר חלון זמן שבו בתא הפנימי רמות Cdx2 נמוכות.
אבל זה לא מספיק: אם התא הפנימי ימשיך לשעתק Cdx2, הרמות יעלו שוב והתא עלול להפוך לפולרי ולחזור החוצה. לכן התא הפנימי צריך גם לכבות את השעתוק של Cdx2.
Hippo signaling: איך תא יודע שהוא בפנים?
השאלה הבאה היא איך תא פנימי יודע שהוא בפנים, ולכן צריך לכבות את השעתוק של Cdx2.
התשובה היא Hippo signaling.
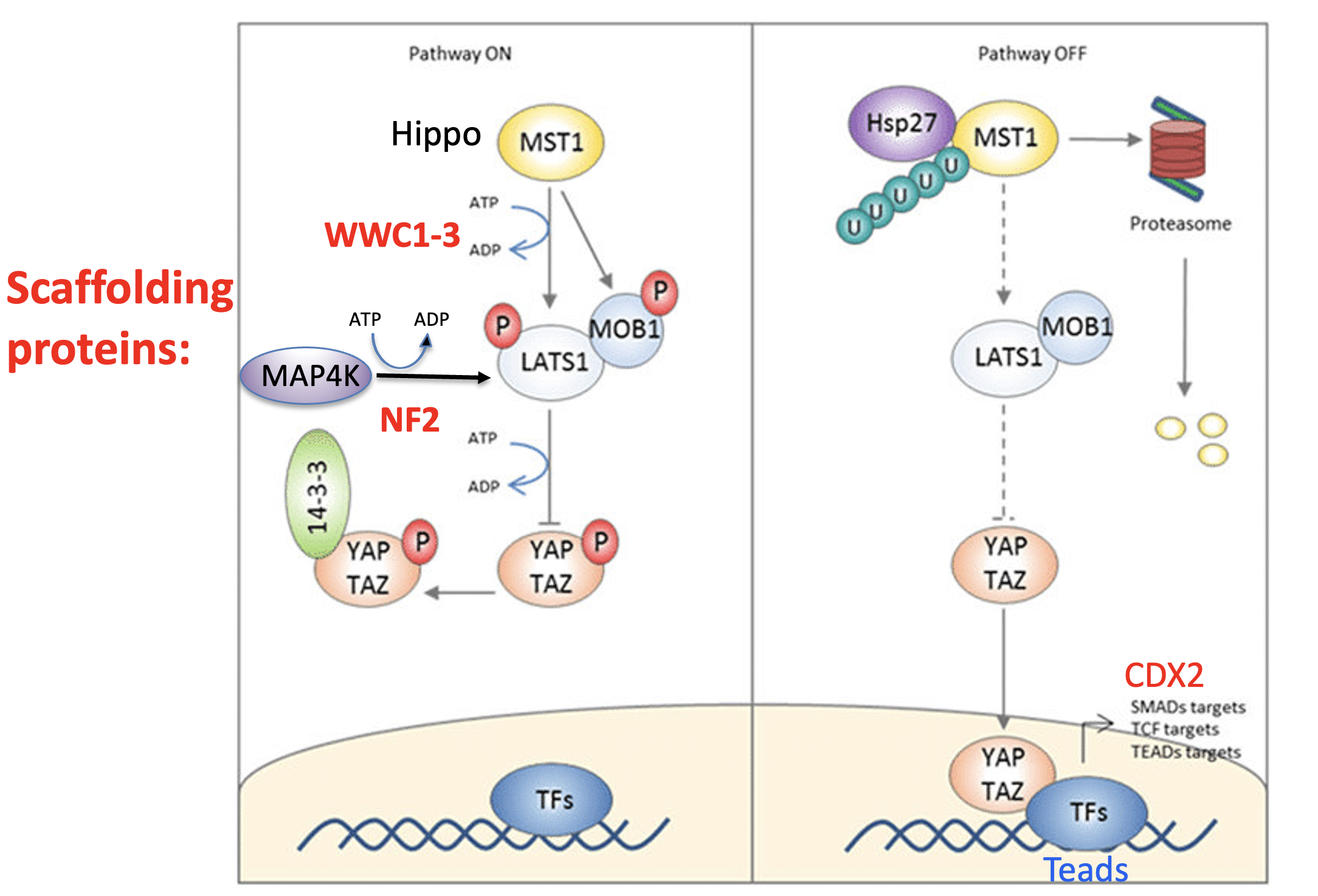
כאשר מסלול Hippo פעיל:
- LATS פעיל.
- LATS מזרחן את YAP/TAZ.
- YAP/TAZ נשארים בציטופלזמה.
- הם לא נכנסים לגרעין.
- אין הפעלה של TEAD.
- אין שעתוק של Cdx2.
זה מצב שמתאים לתאים פנימיים.
כאשר מסלול Hippo כבוי:
- YAP/TAZ אינם מזורחנים באופן שמחזיק אותם בציטופלזמה.
- הם נכנסים לגרעין.
- הם פועלים יחד עם TEAD.
- TEAD מפעיל שעתוק של Cdx2.
זה מצב שמתאים לתאים חיצוניים.
הנקודה המבלבלת במסלול:
- כאשר Hippo פעיל, התוצאה היא דווקא חסימה של שעתוק Cdx2.
- כאשר Hippo כבוי, YAP/TAZ נכנסים לגרעין ומאפשרים שעתוק Cdx2.
Amot, NF2 והקשר ל־Adherens Junctions
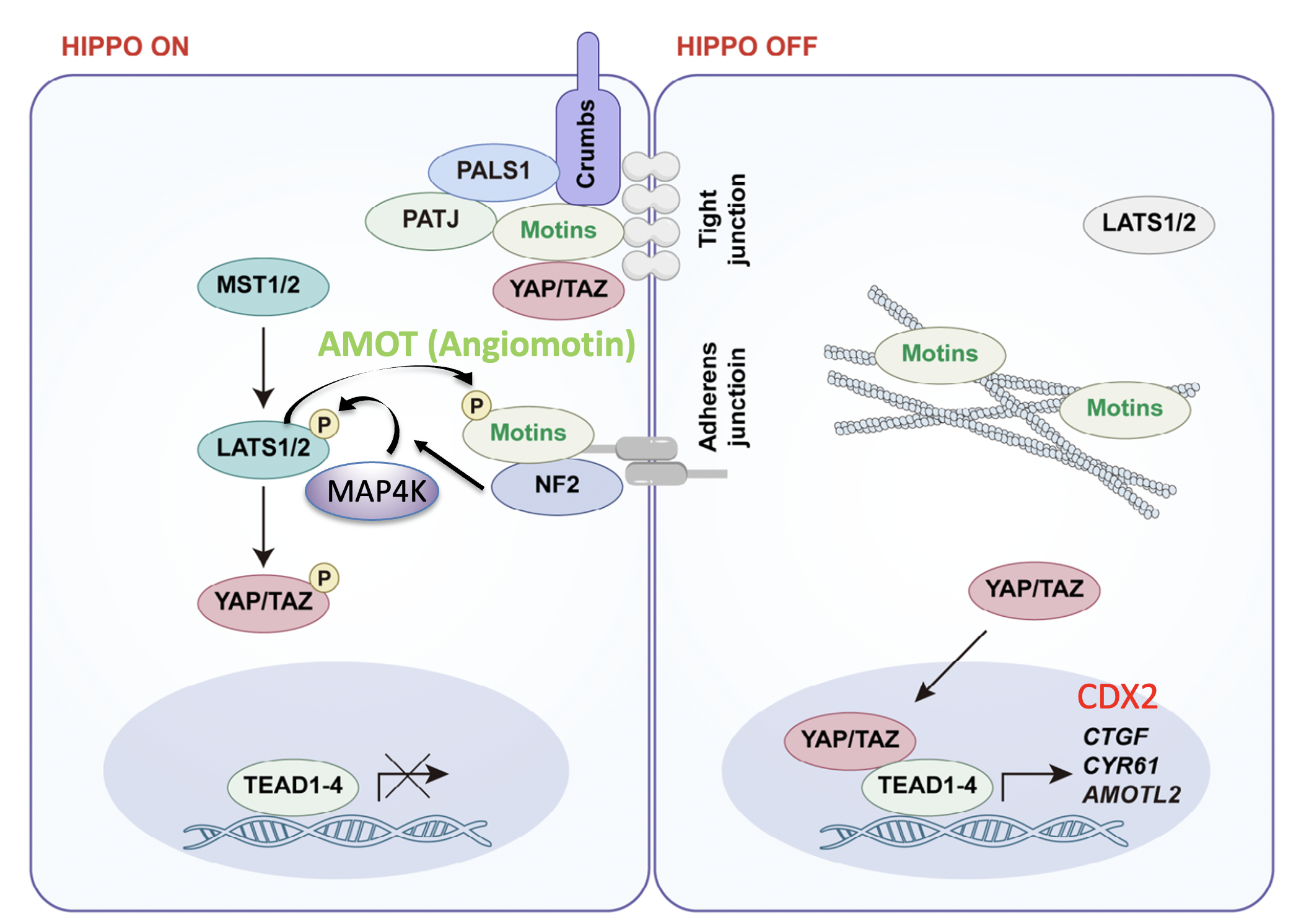
הוזכרו חלבוני Motin, ובעיקר Amot; Amot יכול להשתתף בהפעלת Hippo דרך NF2 ו־LATS.
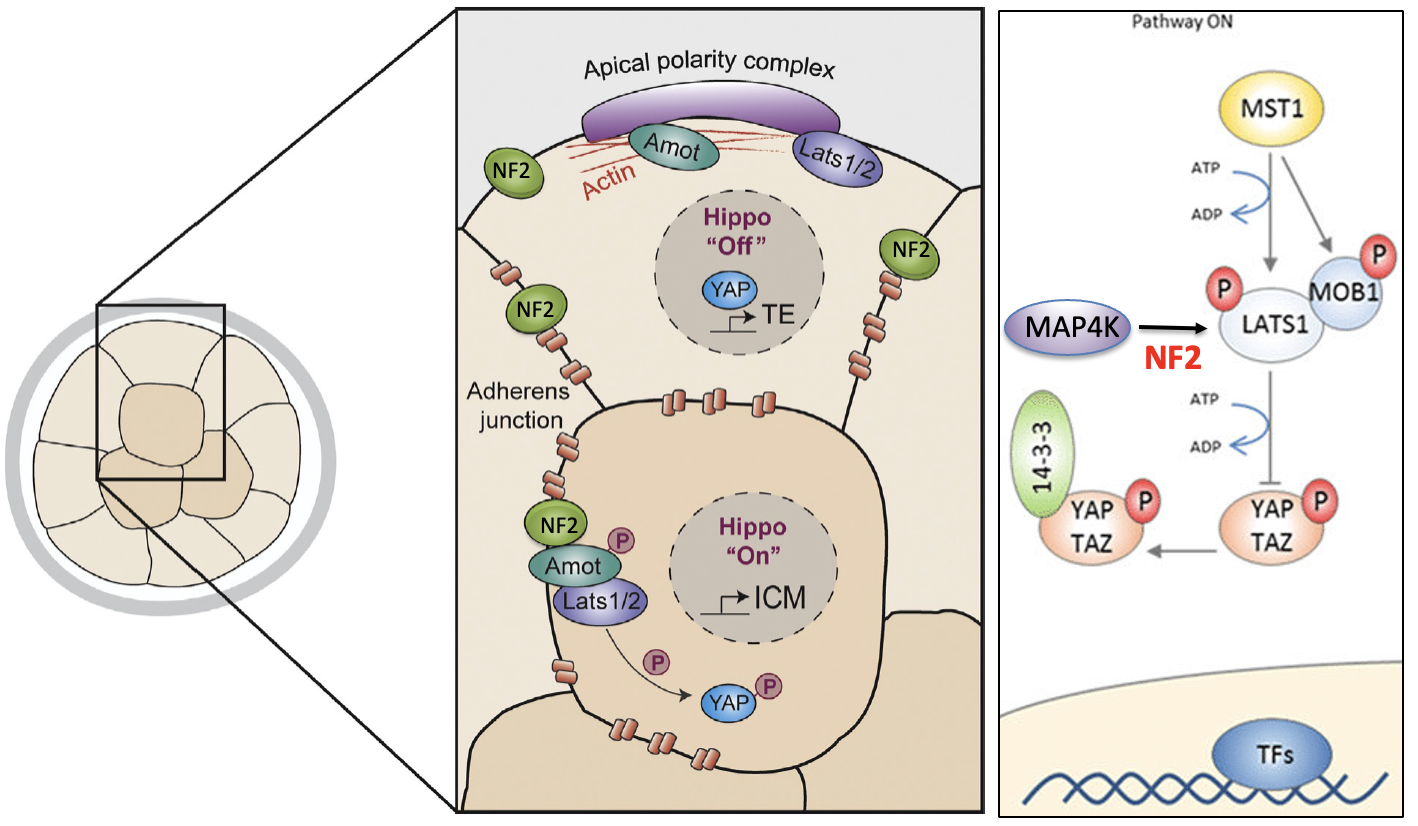
ההבדל בין תאים פנימיים וחיצוניים:
| תא | מצב Hippo | תוצאה |
|---|---|---|
| פנימי | Hippo פעיל | YAP לא נכנס לגרעין ← אין TEAD פעיל ← אין שעתוק Cdx2 |
| חיצוני | Hippo כבוי | YAP נכנס לגרעין ← TEAD פעיל ← יש שעתוק Cdx2 |
בתאים פנימיים יש הרבה מגעים בין תאים ו־Adherens junctions, ולכן יש תנאים להפעלת Hippo. בתאים חיצוניים, הקומפלקס האפיקלי קושר רכיבים כמו Amot ו־LATS והופך אותם לפחות זמינים להפעלת Hippo. לכן בתאים החיצוניים Hippo כבוי, ו־Cdx2 יכול להתבטא.
חיבור המודל: Cdx2, פולריות ו־Hippo
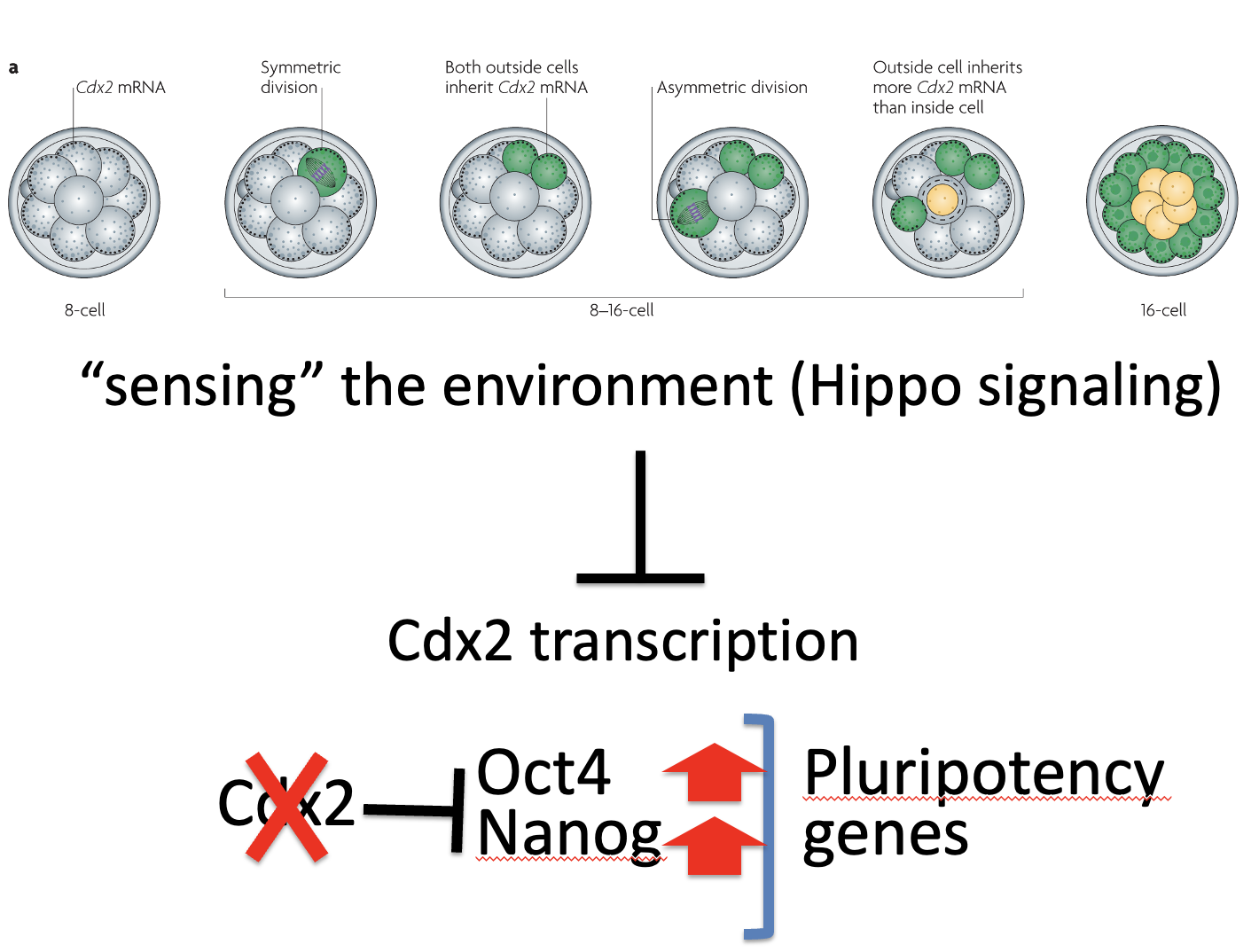
המודל הכללי של First cell fate decision:
- בעובר בן שמונה תאים יש פולריות ולוקליזציה אפיקלית של Cdx2 mRNA.
- בחלוקה סימטרית, שני תאי הבת נשארים חיצוניים, פולריים, וממשיכים לבטא Cdx2.
- בחלוקה א-סימטרית, תא אחד נכנס פנימה ומקבל מעט Cdx2 mRNA.
- בתא הפנימי מופעל Hippo.
- Hippo מונע כניסת YAP/TAZ לגרעין.
- TEAD אינו מפעיל שעתוק של Cdx2.
- רמות Cdx2 נשארות נמוכות.
- Oct4 ו־Nanog יכולים להתבטא, והתא נשמר בכיוון ICM.
Cdx2 ומישור החלוקה
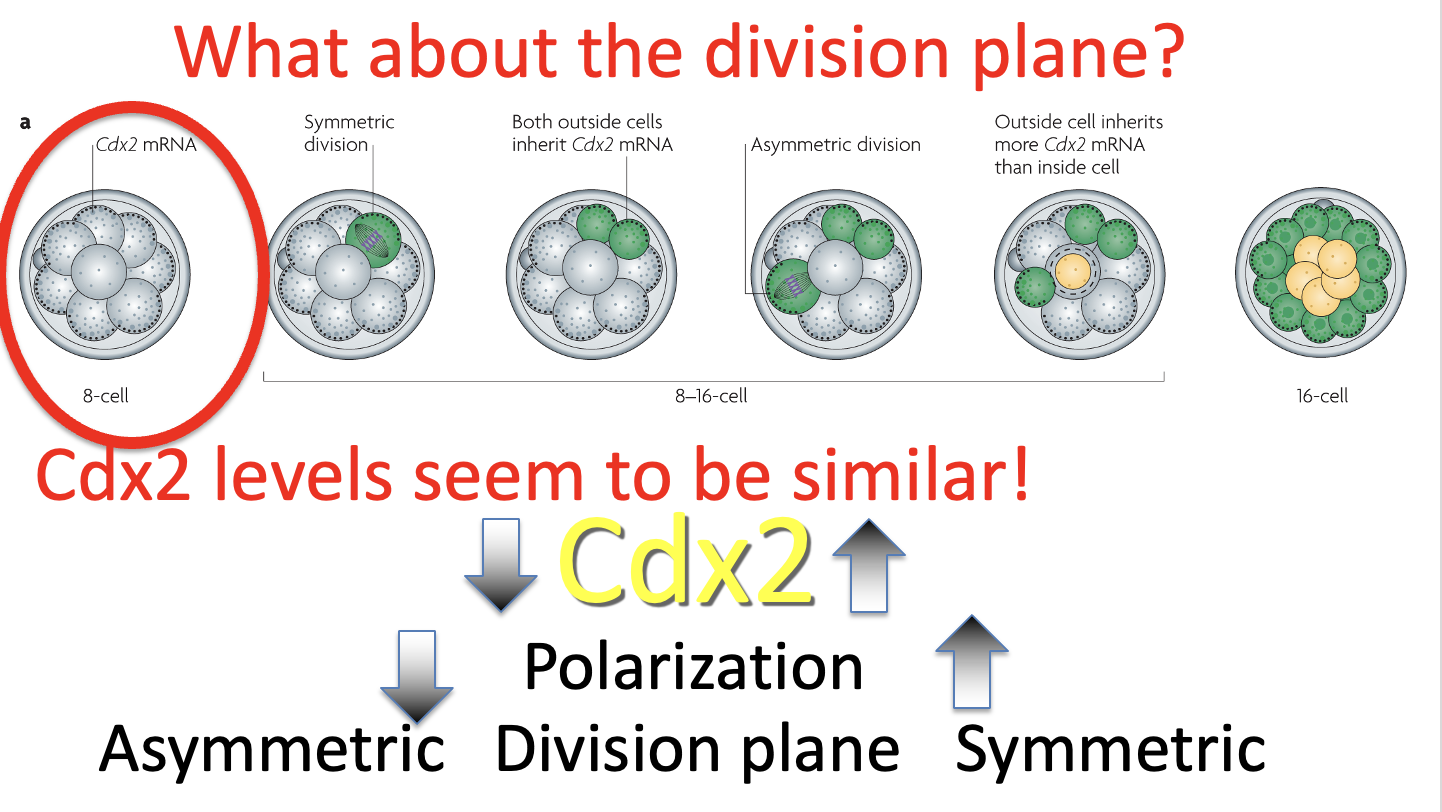
יש גם קשר בין רמות Cdx2 לבין סוג החלוקה:
- רמות גבוהות יותר של Cdx2 ← סיכוי גבוה יותר לחלוקה סימטרית
- רמות נמוכות יותר של Cdx2 ← סיכוי גבוה יותר לחלוקה א-סימטרית
חשוב: מדובר בסיכויים, לא בכלל מוחלט.
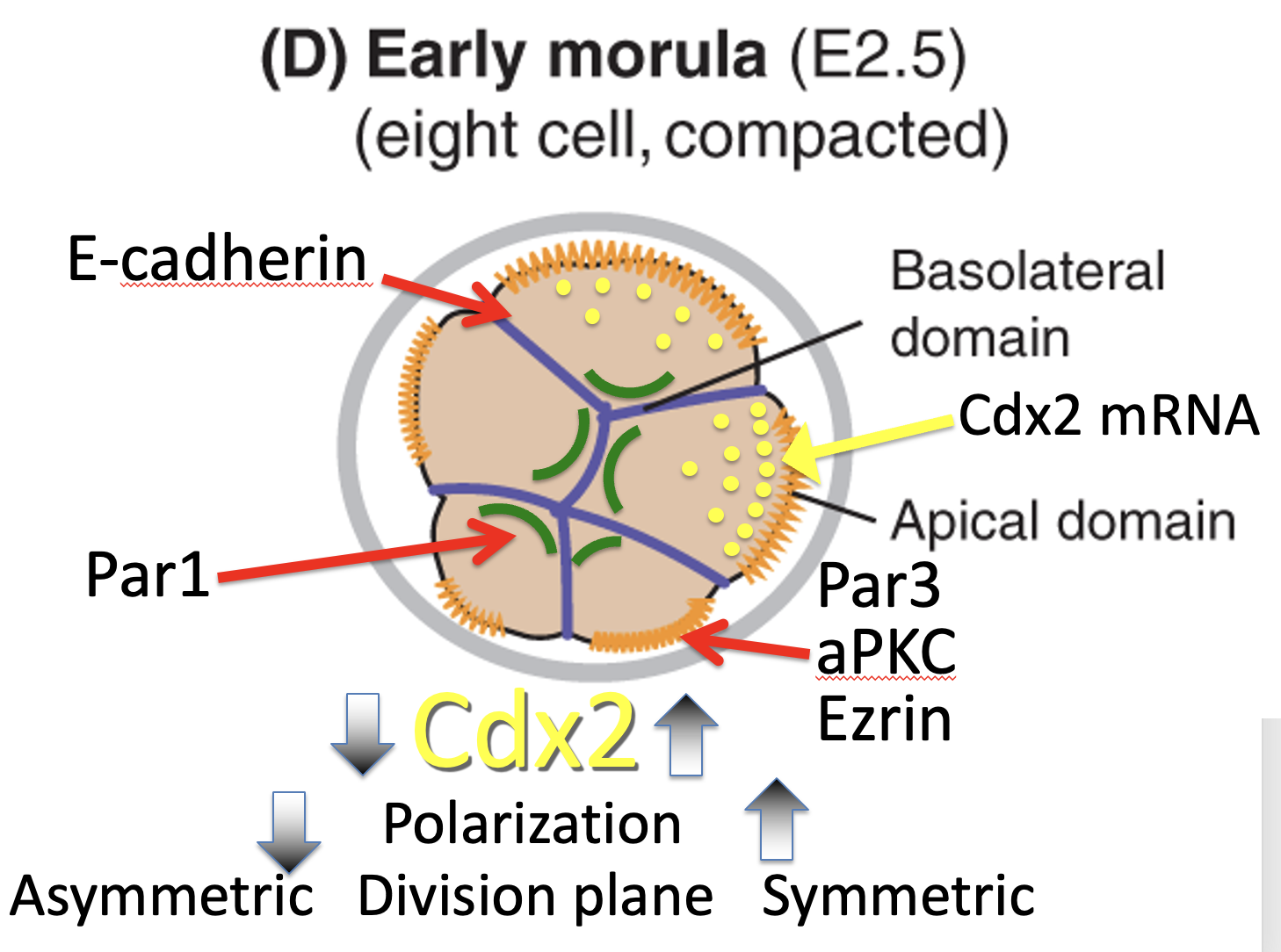
הסכמה בתמונה למעלה, שבה כל התאים בשלב שמונת התאים מבטאים אותה כמות של Cdx2, אינה מדויקת. לפי השיעור, כבר בשלבים האלה יש שונות בין תאים ברמות Cdx2, והשונות יכולה להשפיע על מישור החלוקה ועל יצירת תאים פנימיים.
Zygotic Genome Activation וגלי כניסה ל־ICM
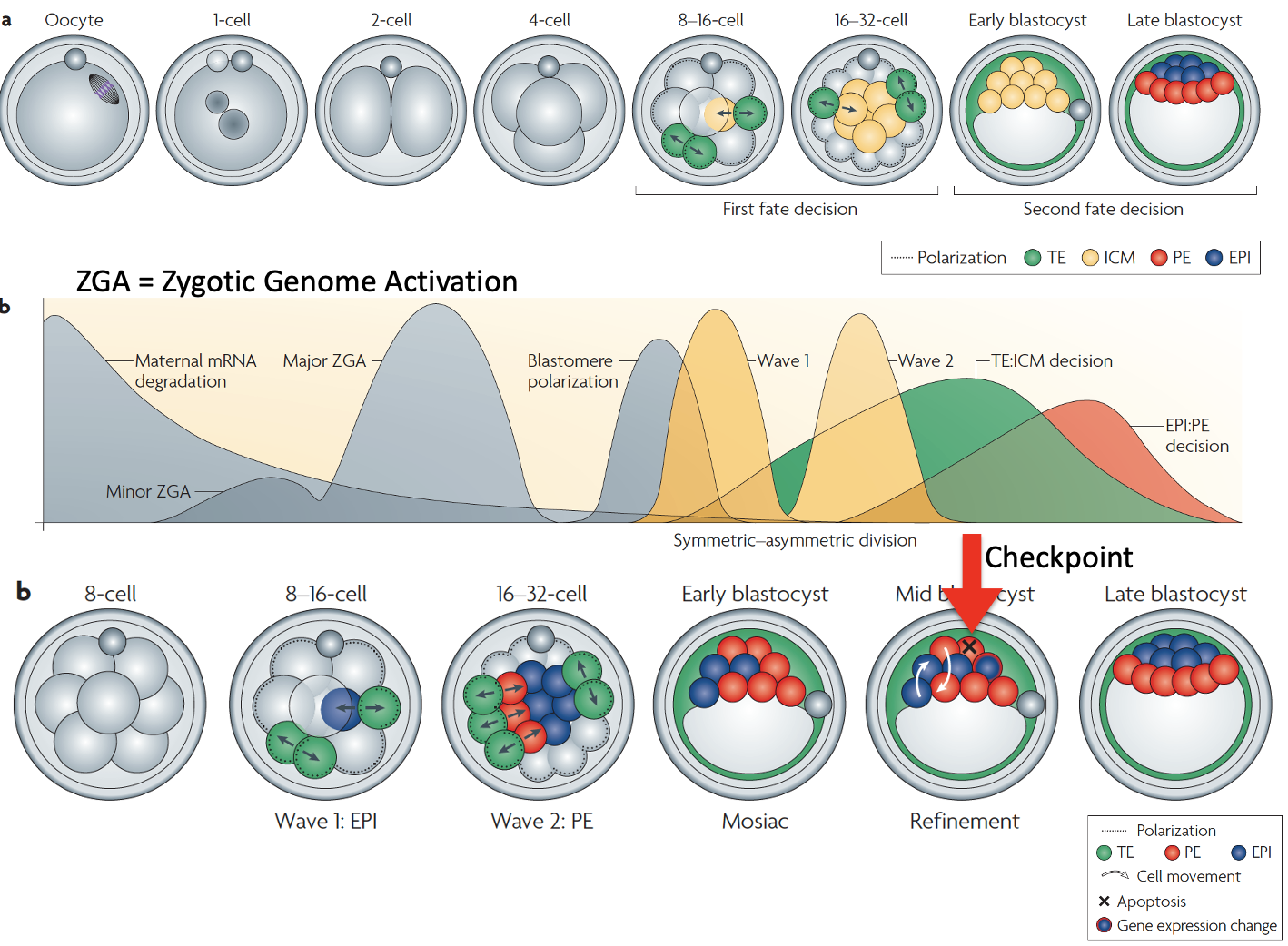
בתחילת ההתפתחות, עד שלב שני התאים, הגנום העוברי מושתק, וה־RNA שמניע את השלבים הראשונים מגיע מהביצית. בשלב שני התאים מתרחשת Zygotic Genome Activation (ZGA), כלומר התחלת הפעילות של הגנום העוברי.
נקודה חשובה: תאי ICM אינם נוצרים כולם בבת אחת. יש שני גלים של חלוקות א-סימטריות:
| גל | מה קורה? | גורל מועדף בהמשך |
|---|---|---|
| 1 | תאים נכנסים מוקדם יותר פנימה | לרוב Epiblast |
| 2 | תאים נכנסים מאוחר יותר פנימה | לרוב Primitive endoderm |
לאחר מכן מתרחש sorting: תאים שאמורים להיות Primitive endoderm מסתדרים באזור המתאים, ותאים שאמורים להיות Epiblast נשארים באזור אחר.
אם תא מבטא תוכנית שאינה מתאימה למיקום שלו, למשל תא שמבטא Gata4 אך נשאר במקום לא מתאים, העובר יכול להפעיל תהליך של אפופטוזיס. זאת מעין נקודת ביקורת חשובה לפני יצירת האפיבלסט, משום שהאפיבלסט ייתן בהמשך את העובר כולו.
Positive feedback loops ברשת פקטורי השעתוק
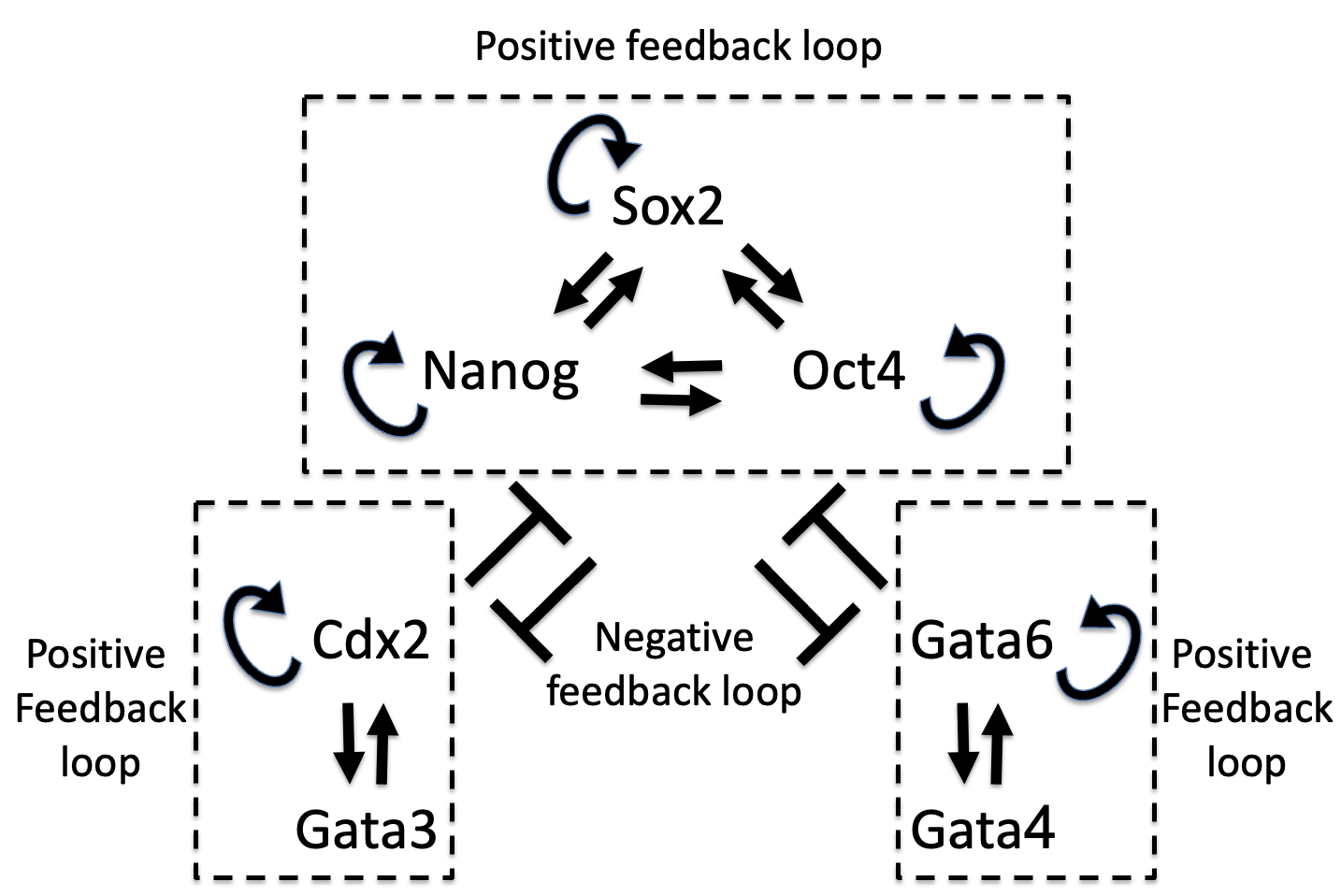
בתמונה למעלה מודל של רשת פקטורי שעתוק. המודל לא נדרש ברמת המשוואות, אלא ברמת ההיגיון: שינוי קטן ברמות של פקטור מסוים יכול לעבור הגברה דרך positive feedback loop.
שלוש קבוצות מרכזיות:
| קבוצה | פקטורים | משמעות |
|---|---|---|
| Pluripotency maintaining genes | Oct4, Nanog, Sox2 | שימור כיוון פלוריפוטנטי / Epiblast |
| Trophectoderm genes | Cdx2, Gata3 | קידום גורל Trophectoderm |
| Primitive endoderm genes | Gata6, Gata4 | קידום גורל Primitive endoderm |
בתוך כל קבוצה יש קשרי הגברה חיוביים. בין קבוצות יש קשרי דיכוי. לכן, כאשר קבוצה אחת מתחילה לקבל יתרון, היא יכולה להגביר את עצמה ולדכא את האחרות.
לדוגמה:
- אם Nanog עולה, הוא יכול לחזק את רשת הפלוריפוטנטיות.
- אם Cdx2 דומיננטי, הוא מחזק את כיוון ה־Trophectoderm ומדכא את Oct4/Nanog.
- אם Gata6 עולה, הוא מקדם את כיוון ה־Primitive endoderm ומדכא את הרשת הפלוריפוטנטית.
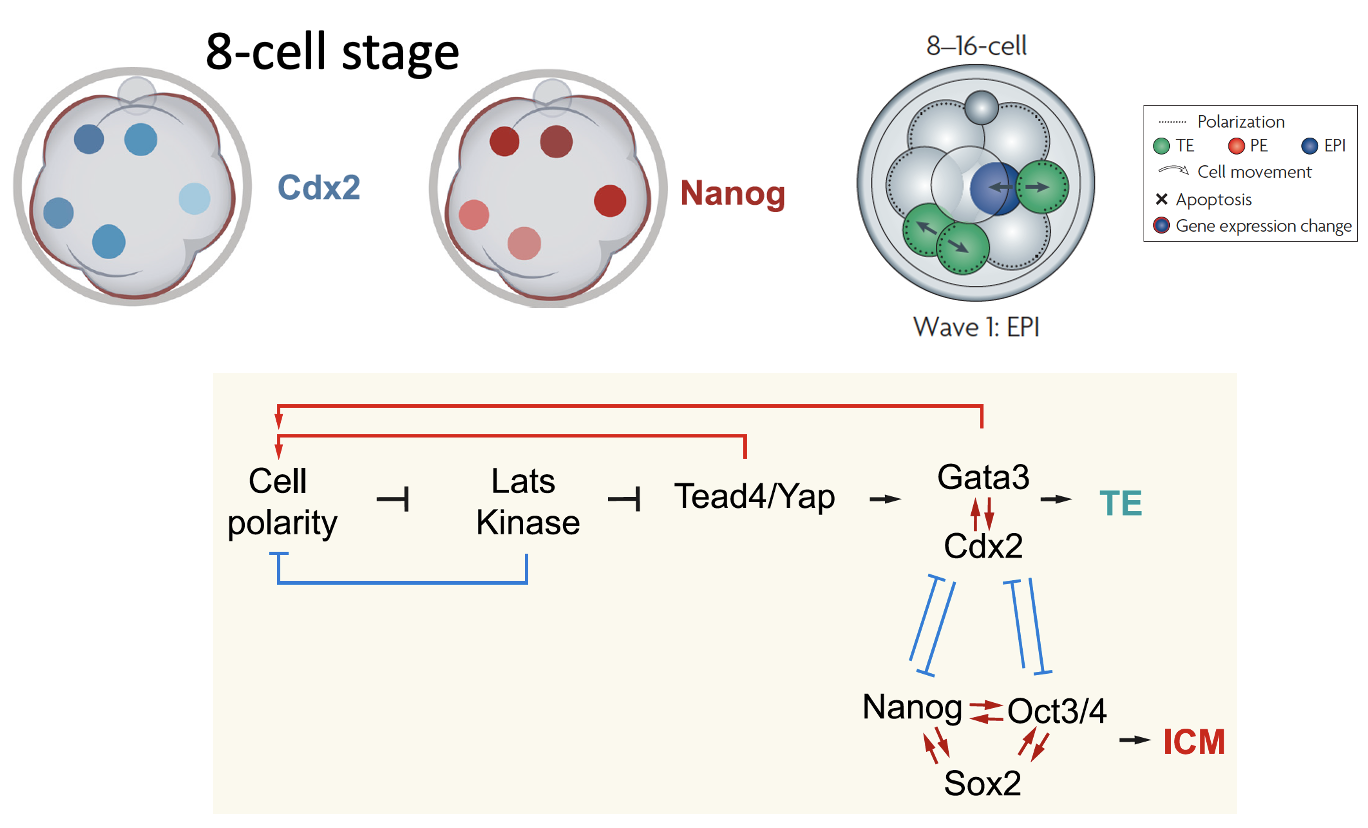
במודל של First cell fate decision, חלוקה א-סימטרית יוצרת חלון זמן שבו תא פנימי מקבל פחות Cdx2. אם בתא הזה יש מעט Nanog, ו־Cdx2 נשאר נמוך בגלל Hippo, רשת הפלוריפוטנטיות יכולה לעבור הגברה ולהשתלט. כך התא נשאר בכיוון ICM.
Second cell fate decision ו־FGF signaling
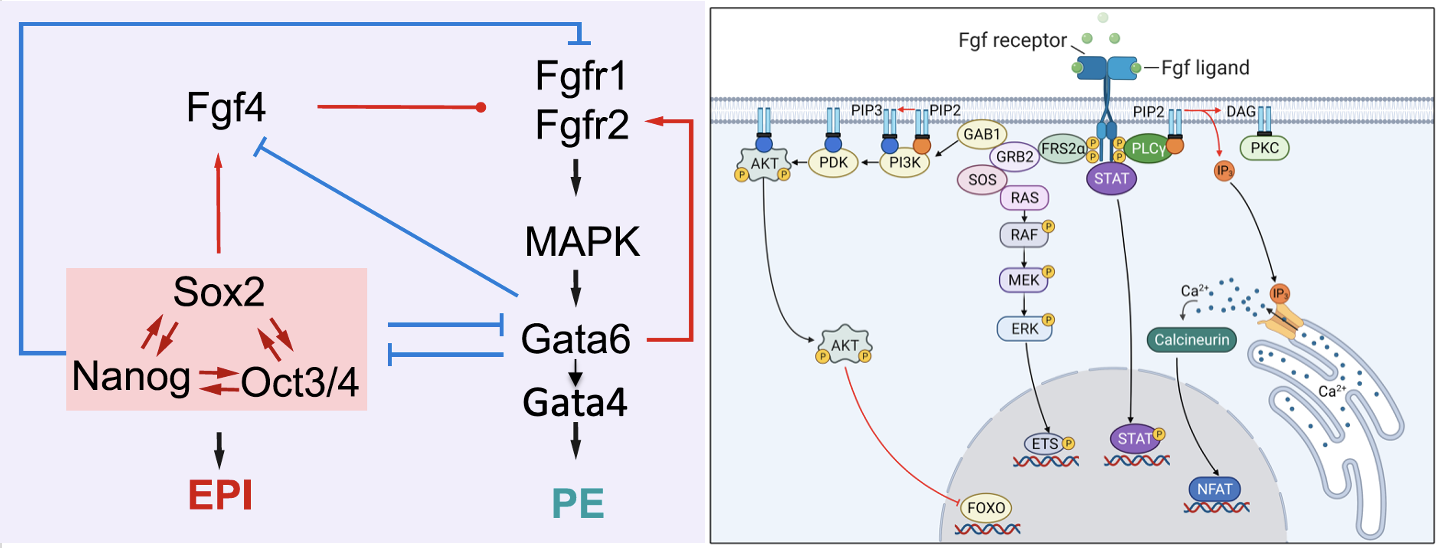
בשלב ה־Second cell fate decision, תאי ה־ICM מתפצלים לשני כיוונים:
| אוכלוסייה | פקטורים מרכזיים | גורל |
|---|---|---|
| תאים עם Nanog / Oct4 / Sox2 | Pluripotency maintaining genes | Epiblast |
| תאים עם Gata6 / Gata4 | Primitive endoderm genes | Primitive endoderm |
כאן נכנס FGF signaling.
- תא שמבטא Oct4, Nanog ו־Sox2 מבטא את הליגנד FGF4.
- אותו תא מדכא את הביטוי של הרצפטורים FGFR1/FGFR2, ולכן הוא בעיקר מייצר את הליגנד ולא מגיב לו.
- תא שהולך לכיוון Gata6 מבטא את הרצפטורים ל־FGF, אבל אינו מבטא את FGF4.
- כאשר FGF4 נקשר לרצפטור בתא מתאים, מופעל מסלול שמעלה את Gata6, ובהמשך Gata4, ומקדם Primitive endoderm.
הגל הראשון
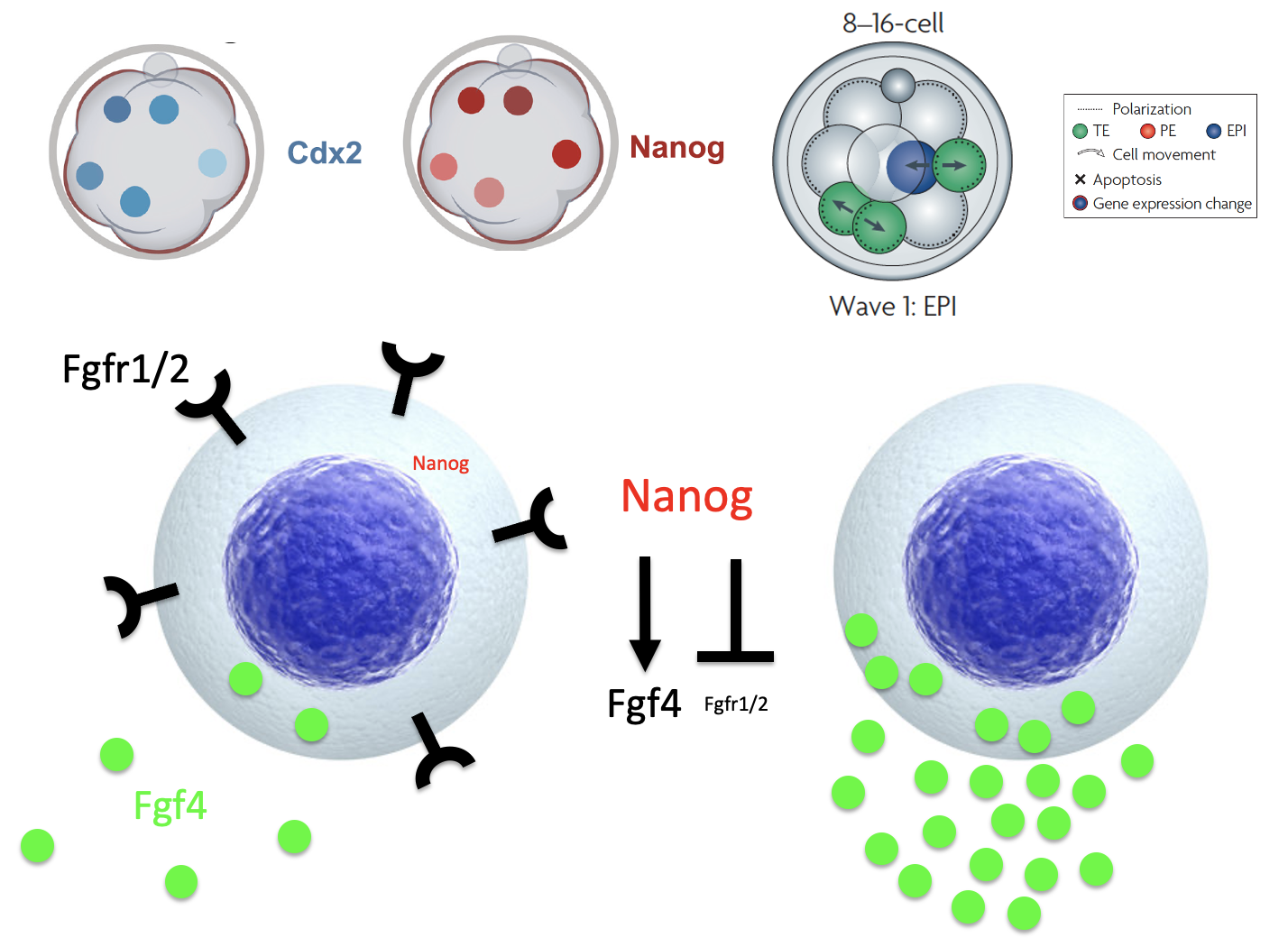
בגל הראשון, התאים שנכנסים פנימה מעלים Nanog. בעקבות זאת הם מבטאים יותר FGF4 ומדכאים את הרצפטורים ל־FGF. לכן הם בעיקר מקור לליגנד, ונוטים להישאר בכיוון Epiblast.
הגל השני
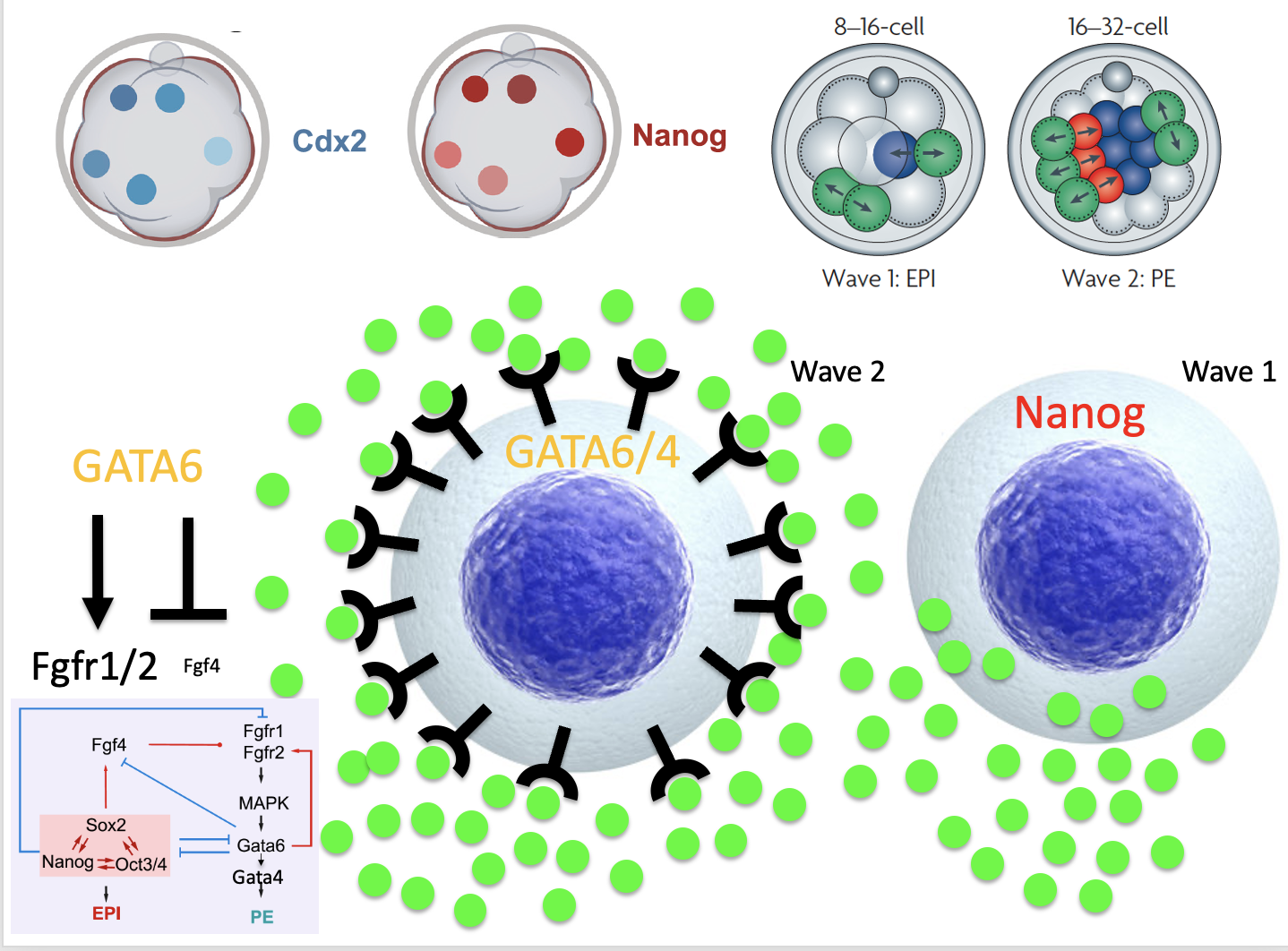
בגל השני, תאים שנכנסים פנימה מגיעים לסביבה שבה כבר יש הרבה FGF4 שהופרש מהתאים של הגל הראשון. גם אם הרצפטורים שלהם בתחילה ברמה נמוכה, כמות הליגנד בסביבה יכולה להפעיל FGF signaling. בעקבות זאת עולה Gata6, שמעלה את רמות הרצפטורים ומדכא את רשת Nanog/Oct4/Sox2. כך התאים האלה נוטים לכיוון Primitive endoderm.
זה ההסבר לכך שתאי Wave 1 נוטים להפוך ל־Epiblast, בעוד שתאי Wave 2 נוטים להפוך ל־Primitive endoderm.
רצף האירועים המרכזי
Zygote
↓
2-cell embryo
↓
Zygotic Genome Activation
↓
4-cell embryo
↓
8-cell embryo
↓
Compaction + Polarization
↓
First cell fate decision
├─ Outer cells
│ ↓
│ Hippo OFF
│ ↓
│ YAP/TAZ + TEAD active
│ ↓
│ Cdx2 ON
│ ↓
│ Trophectoderm
│
└─ Inner cells
↓
Hippo ON
↓
YAP/TAZ kept out of nucleus
↓
Cdx2 OFF
↓
Oct4/Nanog/Sox2 allowed
↓
ICM
↓
Second cell fate decision
├─ Nanog / Oct4 / Sox2
│ ↓
│ FGF4 ligand
│ ↓
│ Epiblast
│
└─ FGF response → Gata6 / Gata4
↓
Primitive endoderm
משפטי מפתח
- Cdx2 חיוני לשימור זהות ה־Trophectoderm וליצירת מחסום אפיתליאלי יציב.
- ללא Cdx2, ה־Blastocoel יכול להתחיל להיווצר, אבל אינו נשמר.
- Tight junctions נמצאים בתאים החיצוניים וחשובים לשימור ה־Blastocoel.
- E-cadherin דרוש ל־Compaction.
- פולריות ומישור חלוקה הם שני מנגנונים מרכזיים ביצירת inner cells ו־outer cells.
- Hippo פעיל בתאים פנימיים ומונע שעתוק של Cdx2.
- Hippo כבוי בתאים חיצוניים ומאפשר שעתוק של Cdx2.
- Cdx2 מדכא את Oct4 ו־Nanog בתאי ה־Trophectoderm.
- בתאי ICM, הורדת Cdx2 מאפשרת ל־Oct4/Nanog/Sox2 לשמר פלוריפוטנטיות.
- ב־Second cell fate decision, FGF4 שמופרש מתאים בכיוון Epiblast משפיע על תאים אחרים ומקדם בהם Gata6/Gata4 ו־Primitive endoderm.