תוכן העניינים:
- התפתחות מוקדמת ותפקיד כללי
- מבנה הלב ומסלול הדם
- מה נדרש מלב מתפקד?
- מבנה סיבי השריר ותנועת הסחיטה של הלב
- תאי הלב והצימוד בין תאים
- מערכת ההולכה של הלב
- SA Node - הקוצב הראשי
- AV Node - השהיה בין עליות לחדרים
- Bundle of His - כבל הולכה מבודד
- Purkinje Fibers - הולכה מהירה לשריר החדר
- רצף ההולכה בלב וקוצבים סמויים
- פוטנציאל הפעולה של תאי קוצב - Nodal Action Potential
- ויסות קצב הלב דרך פוטנציאל הקוצב
- פוטנציאל הפעולה של תאי החדר
- תקופה רפרקטורית
- Excitation–Contraction Coupling
התפתחות מוקדמת ותפקיד כללי
הלב הוא אחד האיברים הראשונים שמתפתחים בעובר. ההתפתחות שלו מתחילה מוקדם מאוד, בערך מיום 16, וניתן לזהות פעילות לבבית כבר אחרי כשלושה שבועות. בשלב הזה הלב עדיין לא נראה כמו הלב הבוגר עם ארבעת המדורים, אבל הוא כבר פונקציונלי ומעביר דם במערכת העוברית. פעילות לבבית מופיעה עוד לפני פעילות נוירונלית ברורה.
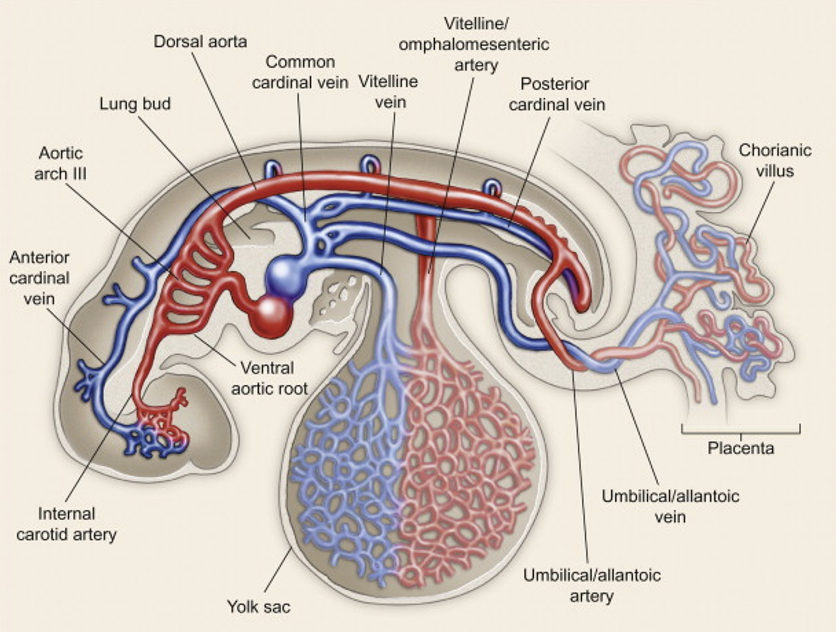
במערכת העוברית קיימת כבר חלוקה למערכת עורקית ולמערכת ורידית. וריד הטבור מביא מהאם דם עשיר בחמצן לעובר, והדם עובר דרך המשאבה הלבבית כדי להגיע לרקמות. עם גדילת העובר, גם הלב וגם מערכת כלי הדם ממשיכים להתפתח: המדורים, כלי הדם, העורקיקים והפרפוזיה לרקמות.
מבנה הלב ומסלול הדם
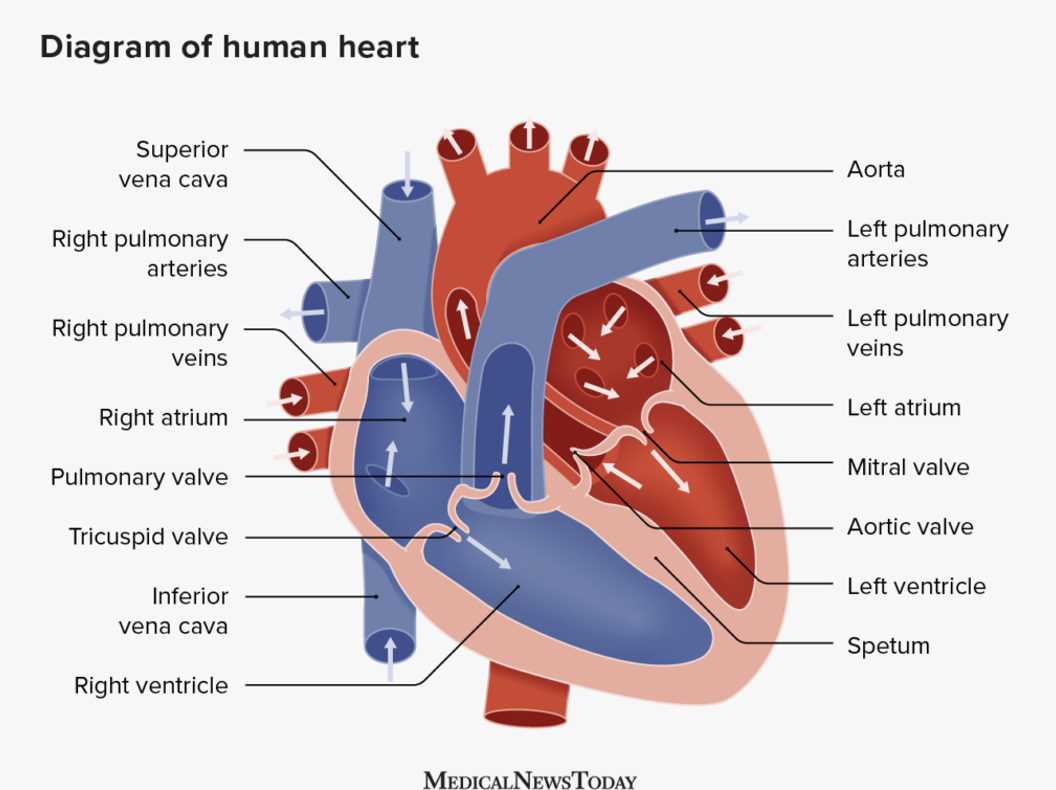
הלב פועל כמשאבה שמחברת בין שתי מערכות זרימה:
- המערכת הריאתית - דם מהמערכת הוורידית מגיע לעלייה הימנית, עובר לחדר הימני ומוזרק לריאות.
- המערכת הסיסטמית - הדם שחוזר מהריאות מגיע לעלייה השמאלית, עובר לחדר השמאלי ומוזרק לגוף דרך אבי העורקים.
החדר הימני קטן ודק יותר מהחדר השמאלי, משום שהוא מזריק דם רק לסירקולציה הריאתית, שבה הלחצים נמוכים יותר. החדר השמאלי צריך להזריק דם לכל הגוף ולכן עבה וחזק יותר. ציורים סכמטיים של הלב לא תמיד משקפים נאמנה את ההבדל בעובי ובגודל בין שני החדרים.
החשיבות של המבנה מתבררת כשחושבים על הלב כמשאבה: העליות צריכות להתכווץ קודם, להזרים דם לחדרים, ורק לאחר מכן החדרים צריכים להתכווץ ולהזריק את הדם הלאה. אם העליות והחדרים היו מתכווצים יחד, מילוי החדרים היה נפגע והדם לא היה מוזרק בצורה יעילה.
מה נדרש מלב מתפקד?
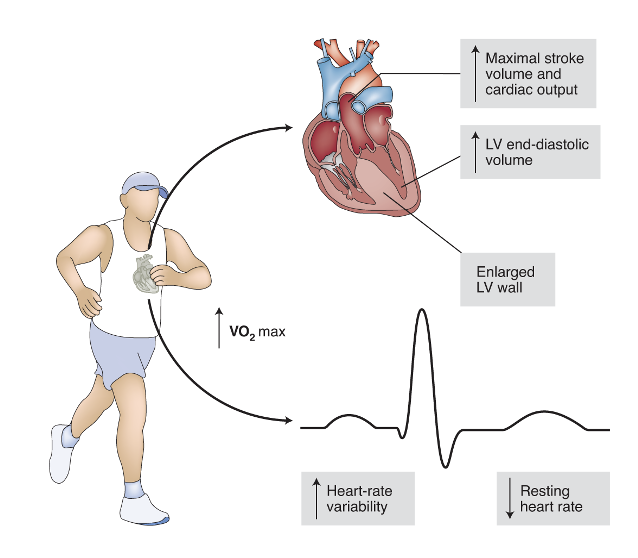 |  |
לב מתפקד צריך לשמור על תפוקה לבבית (cardiac output) תקינה: הזרקת דם בכמות מספקת, בלחץ מתאים, כך שתתקיים פרפוזיה לאיברים - מוח, גפיים ושאר רקמות הגוף.
בנוסף לכך, הלב צריך להיות אדפטיבי; לשנות את פעולתו בהתאם למצב הגוף: מנוחה, שינה, ריצה, סטרס או מצב של fight or flight. היכולת הזאת נשענת על כמה רמות בקרה:
- בקרה לוקלית בתוך שריר הלב ותאי השריר עצמם
- בקרה הורמונלית / הומורלית
- בקרה עצבית דרך המערכת הסימפתטית והפאראסימפתטית
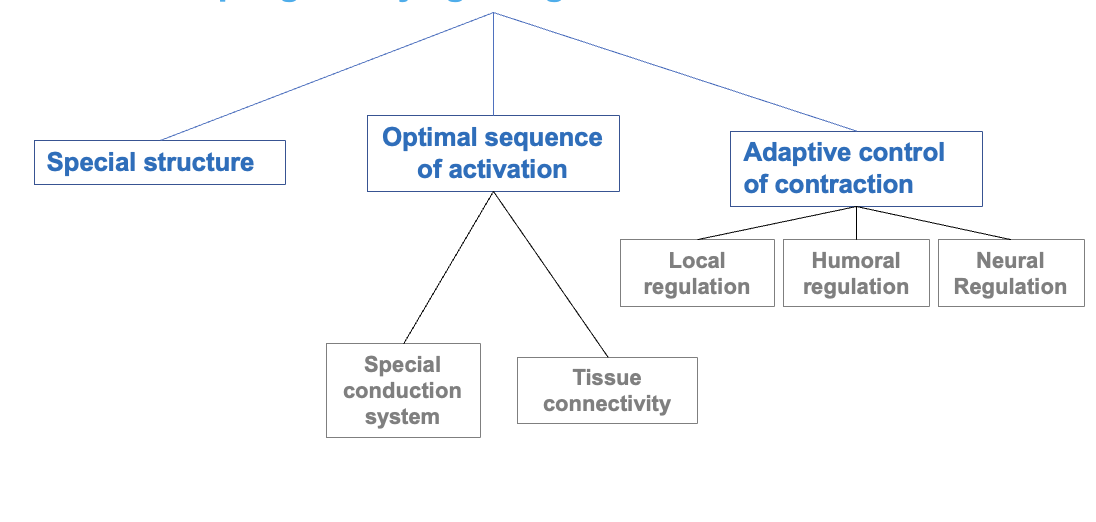
שני עקרונות מרכזיים מאפשרים ללב לבצע פעולה מכנית יעילה:
- מבנה הלב - סידור הסיבים, שכבות השריר והצורה המרחבית.
- רצף האקטיבציה החשמלית - הסדר שבו האות החשמלי מתפשט ומפעיל את חלקי הלב.
בסופו של יום, תפקידה של המערכת החשמלית הוא לתזמן את ההתכווצות המכנית, כך שהדם יוזרק ביעילות.
מבנה סיבי השריר ותנועת הסחיטה של הלב
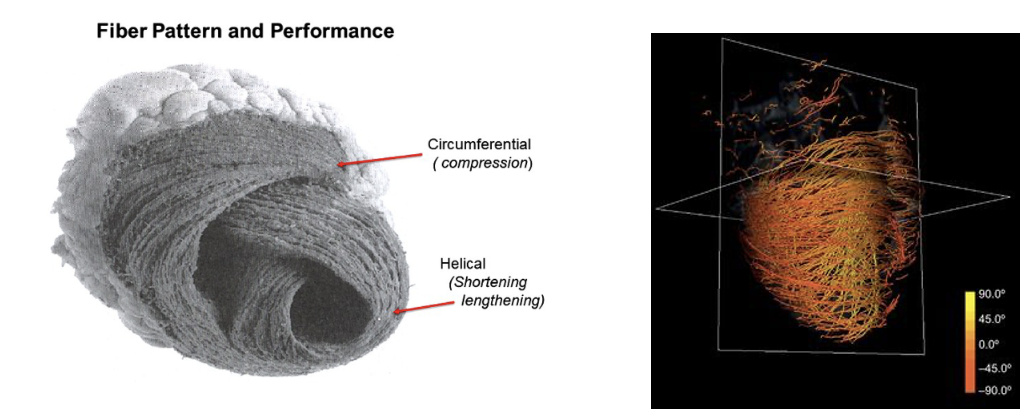
כדי להזריק דם, הלב צריך להתכווץ בצורה שמקטינה את נפח החדרים ודוחפת את הדם לכיוון המוצא. לכן ההתכווצות היעילה של החדרים מתחילה באזור ה־Apex ומתקדמת כלפי בסיס הלב.
מבנה סיבי השריר תורם לכך:
- סיבים היקפיים / Circumferential fibers מקטינים את קוטר החדר.
- סיבים אלכסוניים / Helical fibers יוצרים תנועת סחיטה וטוויסט.
- בדופן הלב יש שכבות של סיבי שריר בכיוונים שונים: מהאנדוקרדיום לכיוון האפיקרדיום זווית הסיבים משתנה בהדרגה.
התוצאה היא לא רק כיווץ פשוט, אלא תנועת סחיטה שמעלה את יעילות ההזרקה.
באקוקרדיוגרפיה אפשר לראות את השינוי בנפח החדרים במהלך ההתכווצות. ב־long axis רואים חתך אורכי של הלב, וב־short axis רואים חתך רוחבי. בדוגמה שהוצגה נראה לב היפרטרופי, כלומר לב עם דופן חדר שמאל עבה מאוד. זה ממצא פתולוגי שיכול להופיע, למשל, בעקבות עומס לחץ גבוה או מוטציות בחלבונים סרקומריים, אבל הוא גם מדגים היטב את תנועת הטוויסט של הלב בזמן ההתכווצות.
תאי הלב והצימוד בין תאים
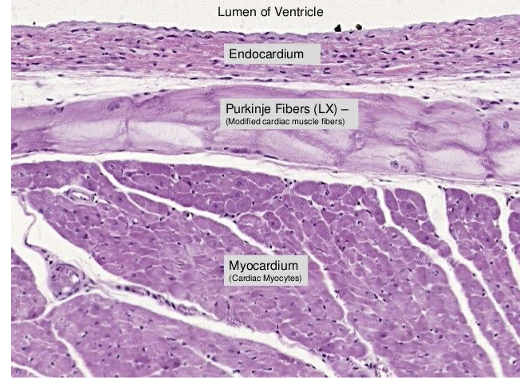 |  |
בלב יש תאי שריר מתכווצים וגם תאים שעברו התמיינות לתפקידי הולכה וקיצוב. גם תאי מערכת ההולכה הם קרדיומיוציטים, אך הם מתמחים בהעברת אות חשמלי ולא בהפקת כוח מכני משמעותי.
סיבי Purkinje, למשל, הם תאי לב גדולים יחסית, עם יכולת התכווצות נמוכה ופחות מבנים סרקומריים פעילים. התפקיד המרכזי שלהם הוא הולכת אות חשמלי במהירות, לשריר החדר.
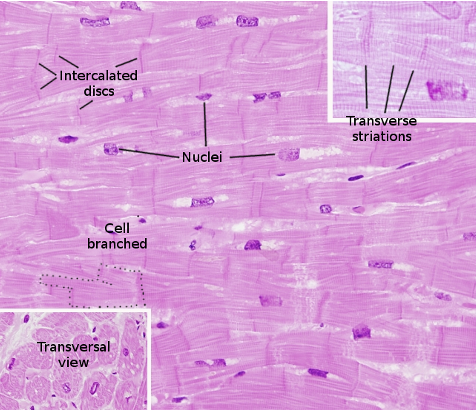
Gap Junctions ו־Intercalated Discs
 | 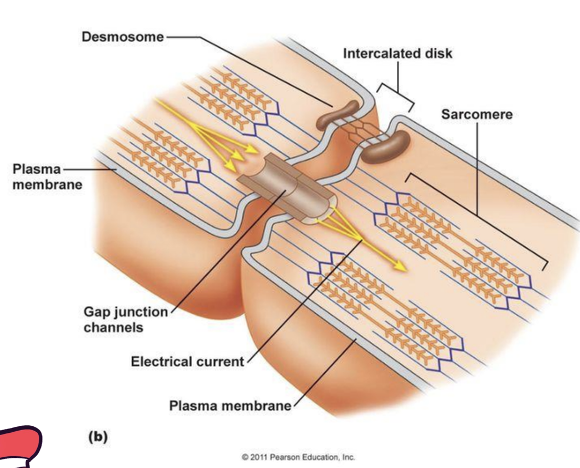 |
תאי שריר הלב מחוברים ביניהם דרך intercalated discs, שבהם יש גם חיבור מכני וגם חיבור חשמלי (לעומת תאי שריר שלד, שמבודדים זה מזה).
החיבור החשמלי נעשה דרך gap junctions:
- תעלות בעלות מוליכות גבוהה
- מאפשרות מעבר זרם בין תאים שכנים
- לא תעלות יונים ספציפיות כמו תעלת $\ce{Na+}$ או $\ce{Ca^2+}$.
- כשמתח הממברנה בתא מסוים עולה, התא השכן “מרגיש” את השינוי דרך החיבור החשמלי
כך תאי שריר הלב מתנהגים כרשת מתואמת: גם אם סיב Purkinje לא מגיע לכל תא ותא, האות החשמלי יכול להתפשט בין הקרדיומיוציטים עצמם.
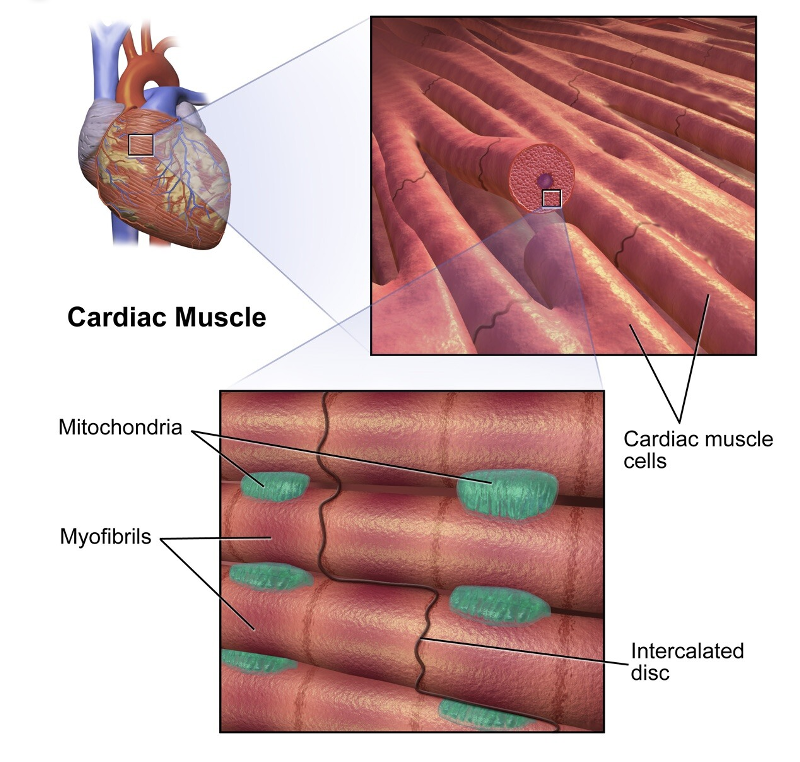
ה־intercalated disc מספק גם צימוד מכני. אם תא מתכווץ, התא הצמוד אליו מחובר מכנית, ולכן הרקמה כולה יכולה לפעול בצורה מסונכרנת.
במצבים פתולוגיים כמו איסכמיה, אזור שלא מקבל דם עלול להפוך חומצי ונקרוטי. בסביבה כזאת gap junctions יכולים להיסגר, וכך האזור הפגוע מבודד חשמלית מהרקמה הבריאה. סביב אזור כזה יכול להיווצר border zone, אזור גבול שעשוי להיות מסוכן מבחינת הפרעות קצב.
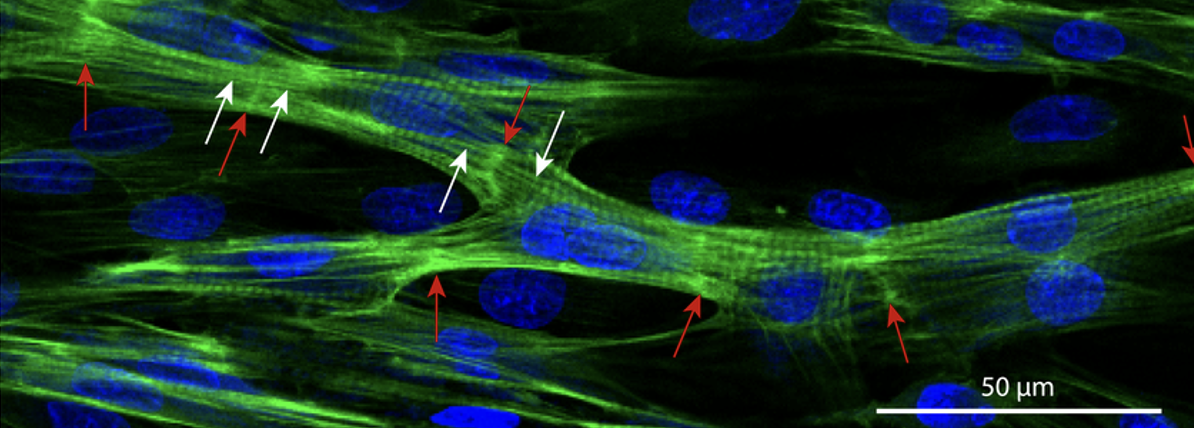
תאי לב בתרבית
גם בלי מערכת הולכה שלמה, קרדיומיוציטים שמחוברים זה לזה יכולים לפעום ולהסתנכרן דרך gap junctions. בתרבית תאי לב שנוצרו מתאי גזע ניתן לראות גל אקטיבציה שמתפשט בין התאים. הדבר מדגים שהסינכרון החשמלי לא תלוי רק במערכת ההולכה, אלא גם בחיבור הישיר בין הקרדיומיוציטים.
מערכת ההולכה של הלב
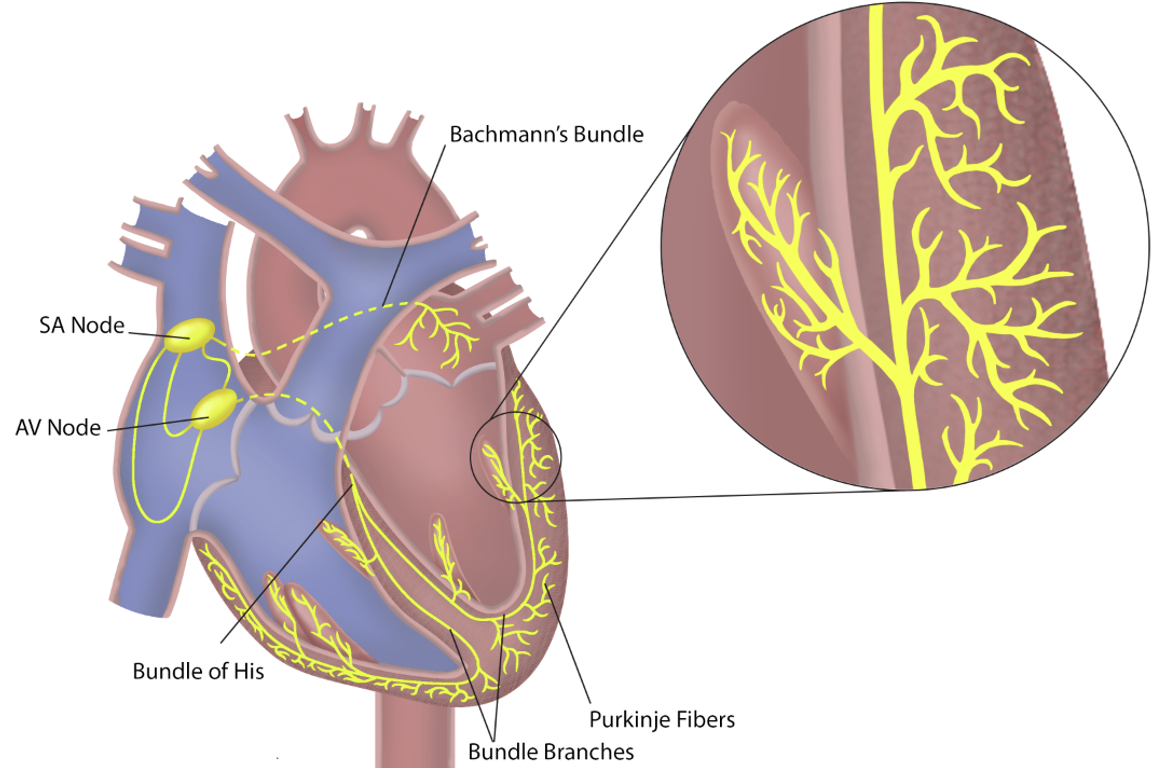
מערכת ההולכה מתזמנת את סדר ההתכווצות:
- SA node יוצר את הקצב הראשוני
- האות מתפשט בעליות וגורם להתכווצות העליות
- האות מגיע ל־AV node, שבו נוצרת השהיה
- לאחר ההשהיה האות עובר ל־Bundle of His
- משם הוא עובר דרך right bundle branch ו־left bundle branch
- האות מגיע ל־Purkinje fibers
- סיבי Purkinje מפעילים את שריר החדרים כך שההתכווצות תתחיל מלמטה ותתקדם כלפי מעלה
האקטיבציה החשמלית בלב קיימת כדי ליצור תזמון מכני נכון: קודם העליות, לאחר מכן החדרים, ובחדרים עצמם - הפעלה שמאפשרת הזרקה מלמטה כלפי המוצא.
SA Node - הקוצב הראשי
ה־SA node הוא קוצב הלב הראשי. תאי SA node הם קרדיומיוציטים מסוג קוצב, ולכן הם שונים מתאי שריר חדריים רגילים.
לתאי קוצב אין פוטנציאל מנוחה יציב באמת. מתח הממברנה שלהם נמצא סביב $-60\,\mathrm{mV}$, ועולה בהדרגה עד שמגיע לסף. העלייה ההדרגתית מאפשרת להם לייצר פוטנציאלי פעולה באופן עצמוני.
אם פוטנציאל המנוחה על פני הממברנה נעשה שלילי יותר (התא עובר היפר-פולריזציה), יידרש זמן רב יותר להגיע לסף ולכן קצב הלב ירד. אם נקודת ההתחלה פחות שלילית או אם השיפוע של הדה־פולריזציה הספונטנית חד יותר, הסף יושג מהר יותר וקצב הלב יעלה.
AV Node - השהיה בין עליות לחדרים
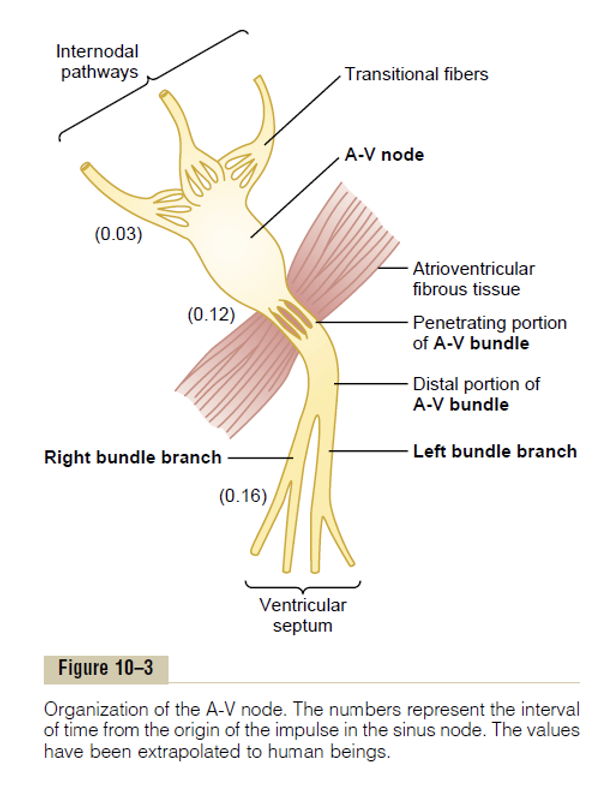
ה־AV node יוצר השהיה בהולכת האות מהעליות לחדרים. ההשהיה הזאת קריטית למילוי החדרים:
- העלייה מתכווצת ומזרימה דם לחדר
- החדר חייב להישאר רפוי בזמן הזה כדי שיוכל להתמלא
- רק לאחר המילוי, האות מתקדם למערכת ההולכה החדרית וגורם להתכווצות החדר.
משך הזמן מתחילת האות ב־SA node, ועד להגעתו והפעלתו של החדר, הוא בערך $0.16\,\mathrm{s}$.
ההולכה האיטית ב־AV node נובעת משני מאפיינים מרכזיים באזור:
- הרבה רקמה פיברוטית ו־extracellular matrix
- פחות gap junctions, ולכן הצימוד החשמלי בין התאים איטי יותר
ה־AV node יכול גם לשמש קוצב חלופי אם ה־SA node לא מתפקד, אך הקצב העצמוני שלו איטי יותר מזה של ה־SA node.
Bundle of His - כבל הולכה מבודד
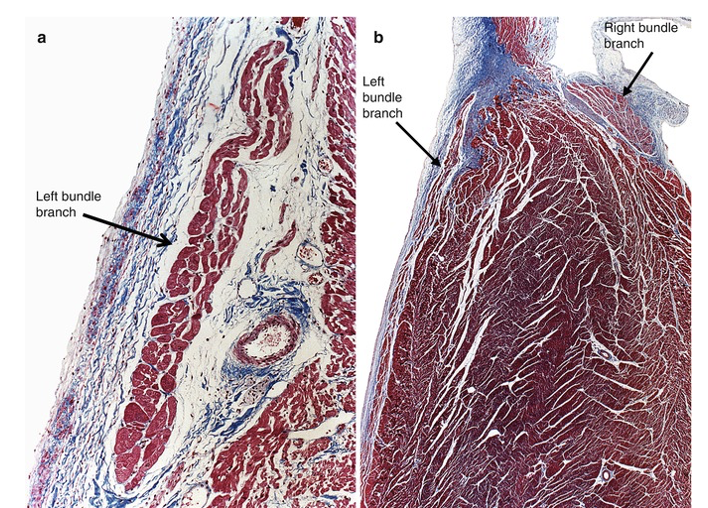
ה־Bundle of His מקבל את האות מה־AV node ומעביר אותו למטה, לכיוון ה־Apex, דרך bundle branches. מהירות ההולכה בו היא בערך $2\,\mathrm{m/s}$.
תפקידו להעביר את האות לנקודה שממנה נכון להתחיל את כיווץ החדרים (ולא לגרום להתכווצות שרירית במישרין). אם ה־Bundle of His היה מפעיל את השריר לאורך הדרך, הבסיס או הספטום היו מתכווצים מוקדם מדי, וההתכווצות לא הייתה מתקדמת באופן יעיל מה־Apex כלפי מעלה.
הבידוד של ה־Bundle of His נובע ממעטפת של רקמה פיברוטית (הוא לא נוירון ואינו מבודד במיאלין). אפשר לחשוב עליו כמו כבל חשמלי בבית: כדי להעביר אות לנקודה רחוקה בלי שהוא “יתפזר” בדרך, הכבל צריך להיות מבודד.
Purkinje Fibers - הולכה מהירה לשריר החדר
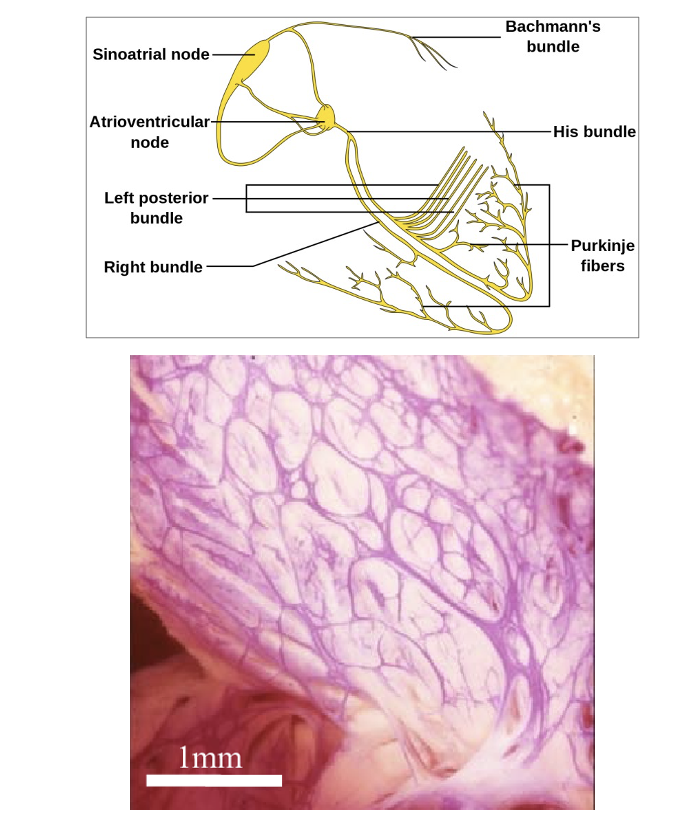
סיבי Purkinje נמצאים בשכבה הסאב־אנדוקרדיאלית של החדרים. הם גדולים יותר מסיבי שריר חדריים רגילים, ומוליכים פוטנציאלי פעולה במהירות גבוהה - בערך $1.5\text{-}4.0\,\mathrm{m/s}$.
ההולכה המהירה מאפשרת פיזור כמעט מיידי של האות החשמלי בשאר שריר החדר. היא מהירה בהרבה מההולכה בשריר החדר הרגיל, ומהירה במיוחד ביחס להולכה האיטית באזור ה־AV node.
מהירות ההולכה הגבוהה קשורה לצימוד חשמלי יעיל דרך gap junctions. סיבי Purkinje מפעילים את ה־Myocardium החדרי ומאפשרים כיווץ מסונכרן של החדרים.
לסיבי Purkinje יש גם יכולת מסוימת לייצר פעילות עצמונית, אך בקצב איטי יותר מזה של ה־SA node וה־AV node. לכן, במצב תקין הם לא קובעים את קצב הלב, אך אם הקוצבים העיקריים לא פועלים או שההולכה מהם נחסמת, הם יכולים לשמש כקוצב חלופי.
רצף ההולכה בלב וקוצבים סמויים
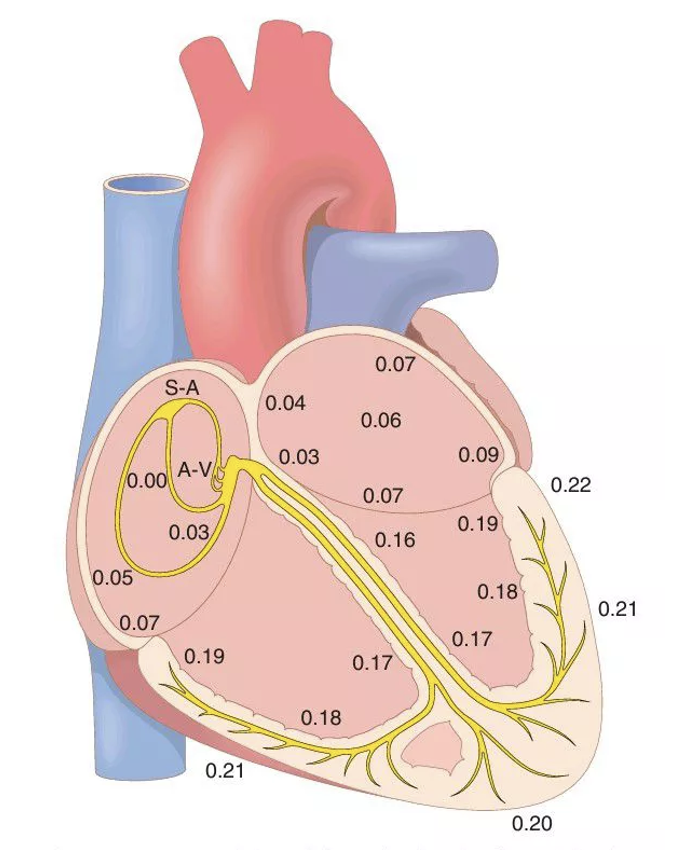 | 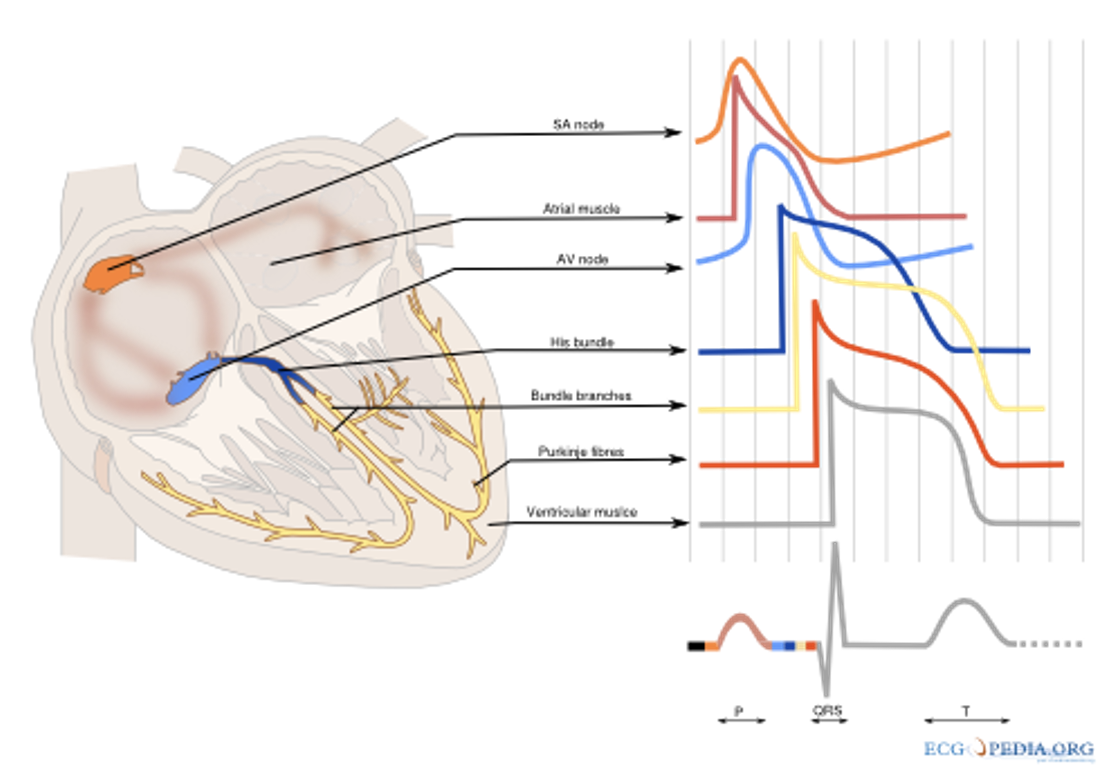 |
במערכת ההולכה קיימת היררכיה של קוצבים פוטנציאליים. ככל ששיפוע הדה־פולריזציה הספונטנית בפאזה 4 חד יותר, הקצב העצמוני מהיר יותר.
| אזור | קצב עצמוני משוער |
|---|---|
| SA node | 70–80 פעימות בדקה |
| AV node | 40–60 פעימות בדקה |
| Bundle of His | כ־40 פעימות בדקה |
| Purkinje fibers | 15–20 פעימות בדקה |
ה־SA node מדכא את הקוצבים שמתחתיו משום שהוא יורה (מייצר פוטנציאלי פעולה) מהר יותר. אם הוא נכשל, ה־AV node יכול לקחת פיקוד בקצב איטי יותר. אם גם הוא אינו מעביר או אינו יורה, אזורים נמוכים יותר במערכת ההולכה עשויים להפוך לקוצב בפועל. קוצב שמתחיל לפעול ממיקום שאינו הקוצב הראשי נקרא ectopic pacemaker.
חשוב להפריד בין שני מושגים שונים:
- קצב firing עצמוני - כמה מהר תא או אזור מסוגל לייצר פוטנציאלי פעולה
- מהירות הולכה - כמה מהר האות מתפשט לאורך הרקמה
לדוגמה, ה־AV node יכול לייצר קצב עצמוני מהיר יותר מסיבי Purkinje, אבל ההולכה בו איטית מאוד. לעומת זאת, סיבי Purkinje מוליכים מהר מאוד, אף שהקצב העצמוני שלהם איטי.
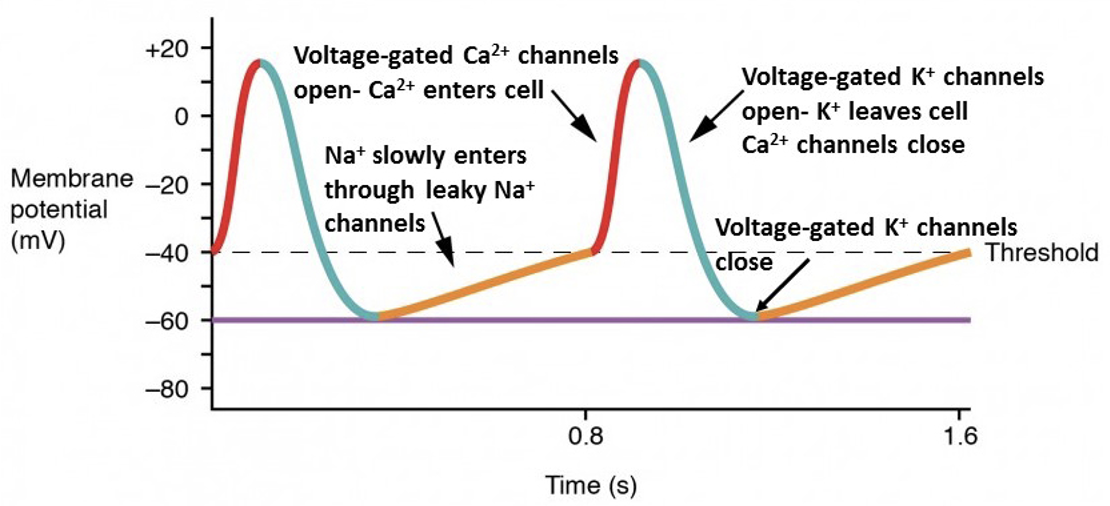
פוטנציאל הפעולה של תאי קוצב - Nodal Action Potential
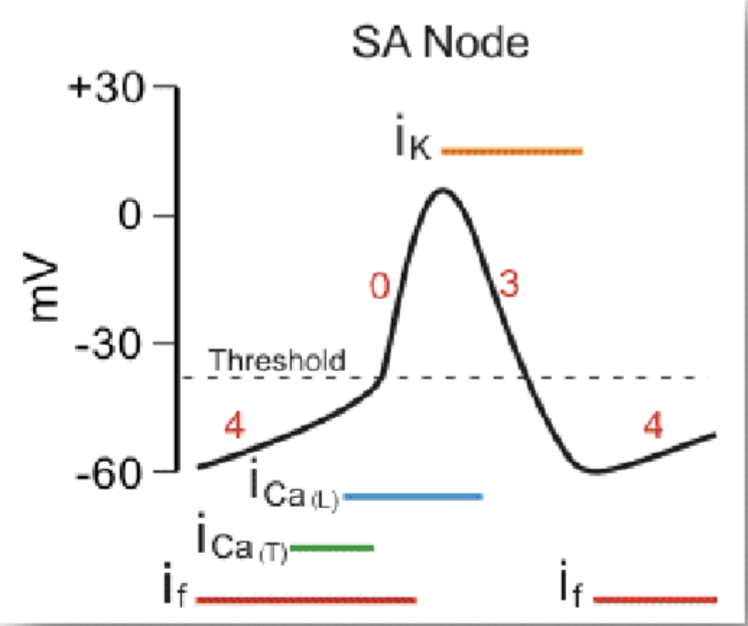
תאי הקוצב הם slow response cells. פוטנציאל הפעולה שלהם כולל בעיקר את פאזה 4, פאזה 0 ופאזה 3. אין להם פאזה 1 ופאזה 2, ולכן אין להם plateau כמו בתאי החדר.
המאפיינים המרכזיים:
- פוטנציאל הממברנה סביב $-60\,\mathrm{mV}$
- אין מנוחה יציבה באמת
- קיימת דה־פולריזציה ספונטנית עד לסף
- העלייה בפאזה 0 איטית יחסית לתאי חדר
- אין plateau
- העלייה בפוטנציאל הפעולה תלויה בעיקר בתעלות $\ce{Ca^2+}$ ולא בתעלות $\ce{Na+}$ מהירות
עקרון היונים
יונים חיוביים שנכנסים לתא מעלים את מתח הממברנה. יונים חיוביים שיוצאים מהתא מורידים את מתח הממברנה.
באופן כללי:
- $\ce{Na+}$ ו־$\ce{Ca^2+}$ נכנסים לתא ותורמים לדה־פולריזציה
- $\ce{K+}$ יוצא מהתא ותורם לרה־פולריזציה
פאזה 4 - דה־פולריזציה ספונטנית
בפאזה 4 יש זרמי דלף איטיים, שנקראים גם funny currents. הם גורמים לעלייה הדרגתית של מתח הממברנה.
- $\ce{Na+}$ נכנס בהדרגה דרך תעלות funny
- בהמשך, סביב $-45\,\mathrm{mV}$, נפתחות תעלות $\ce{Ca^2+}$ מסוג T
- הכניסה של יונים חיוביים מקרבת את התא לסף
פאזה 0 - דה־פולריזציה
כשהתא מגיע לסף, נפתחות תעלות $\ce{Ca^2+}$ תלויות-מתח. כניסת $\ce{Ca^2+}$ גורמת לעלייה בפוטנציאל הממברנה. מכיוון שהעלייה תלויה בתעלות סידן איטיות יחסית, ה־upstroke בתאי קוצב איטי יותר מזה של תאי חדר.
פאזה 3 - רה־פולריזציה
בשלב זה תעלות $\ce{Ca^2+}$ נסגרות, ותעלות $\ce{K+}$ נפתחות. $\ce{K+}$ יוצא מהתא, מתח הממברנה יורד, והתא חוזר לערך שממנו מתחילה שוב הדה־פולריזציה הספונטנית.
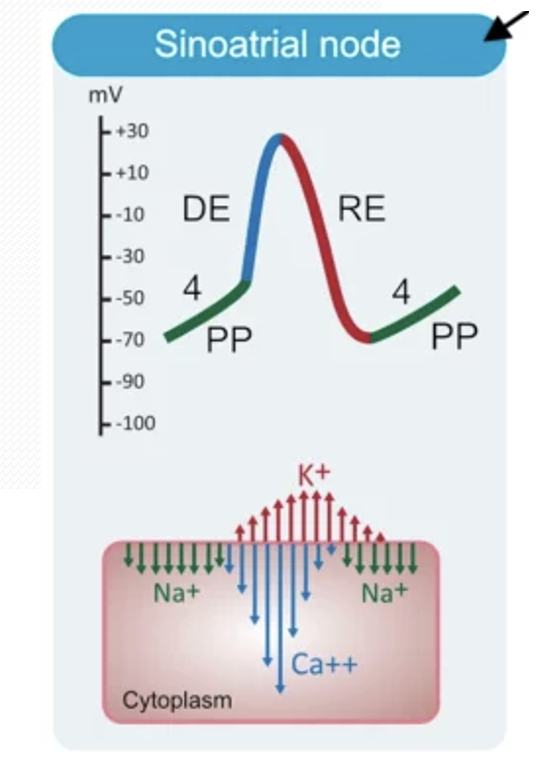
ויסות קצב הלב דרך פוטנציאל הקוצב
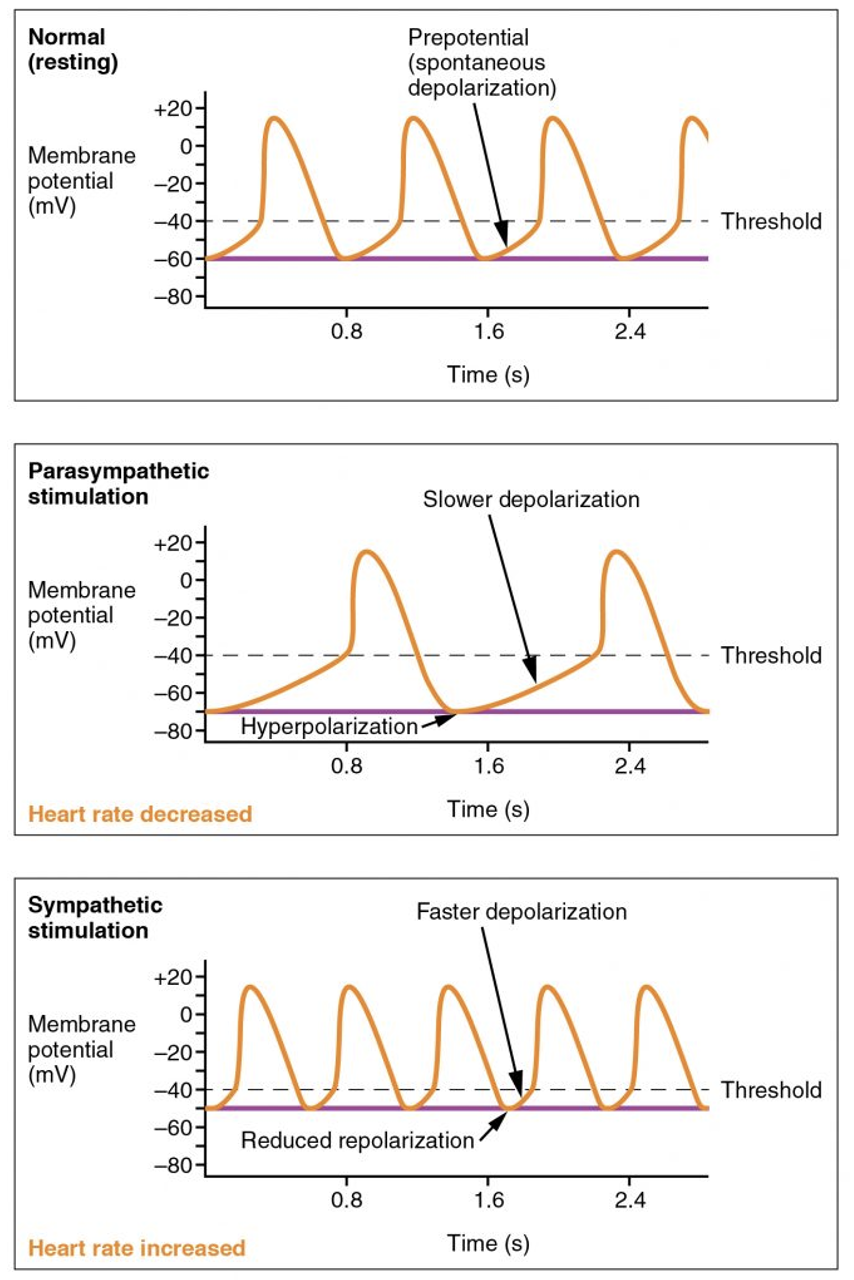
קצב הלב נקבע בעיקר על ידי שני פרמטרים בתאי הקוצב:
- השיפוע של פאזה 4 - כמה מהר מתח הממברנה מגיע לסף
- פוטנציאל ההתחלה - עד כמה נקודת ההתחלה של התא קרובה (או רחוקה) מהסף
השפעה פאראסימפתטית מורידה את קצב הלב; היא יכולה לגרום להיפרפולריזציה של הממברנה או להקטין את השיפוע של פאזה 4, ולכן יידרש יותר זמן להגיע לסף.
השפעה סימפתטית מעלה את קצב הלב; היא גורמת לתא להגיע לסף מהר יותר, בין היתר דרך שינוי הקינטיקה של התעלות.
כך הלב מתאים את עצמו לצורך הפיזיולוגי: בשינה ובמנוחה הדופק יורד, ובמאמץ או בסטרס הדופק עולה.
פוטנציאל הפעולה של תאי החדר
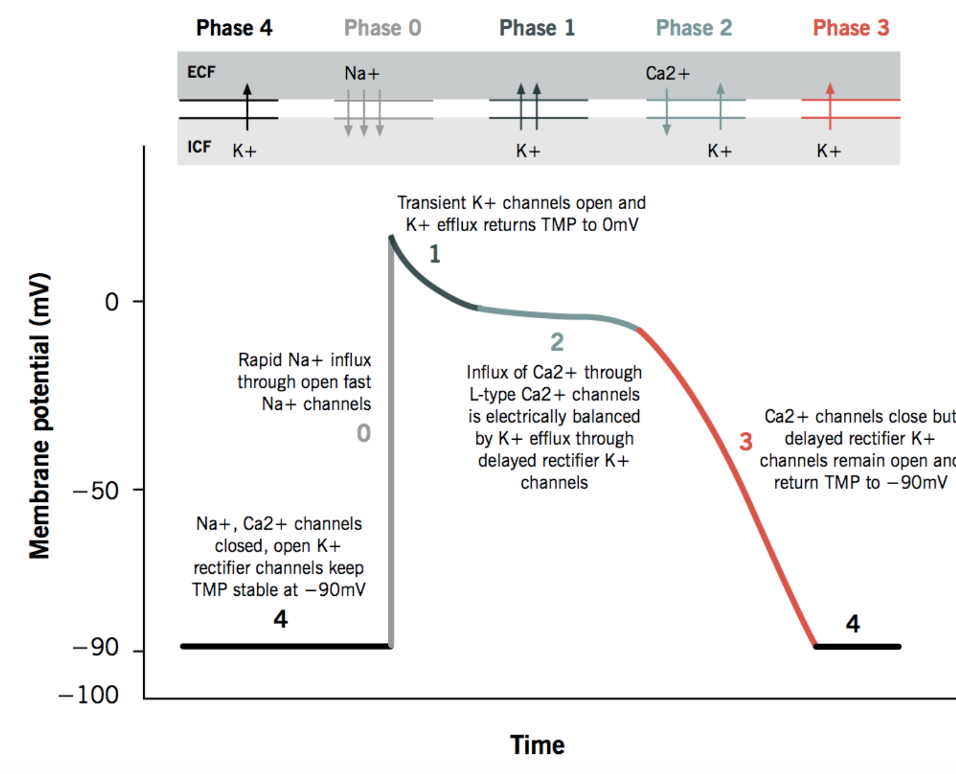
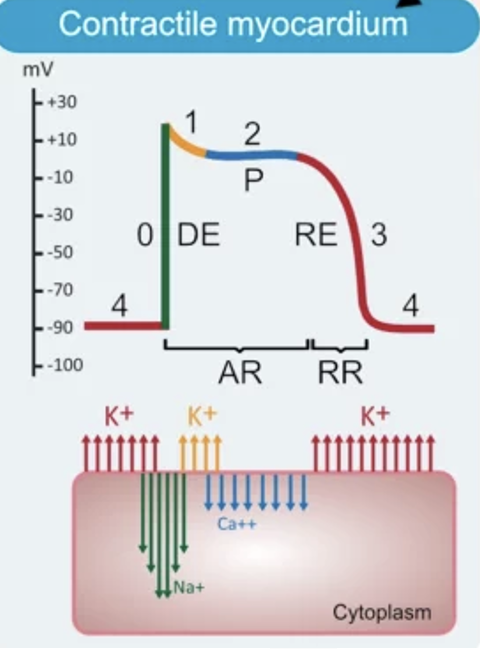
פוטנציאל הפעולה של תאי החדר, תאי העלייה וסיבי Purkinje הוא fast response. בניגוד לתאי קוצב, כאן קיימות כל הפאזות: 0, 1, 2, 3 ו־4.
פאזה 4 - מנוחה יציבה
בתאי חדר פוטנציאל המנוחה יציב יותר, סביב $-90\,\mathrm{mV}$. תעלות $\ce{Na+}$ ותעלות $\ce{Ca^2+}$ סגורות, והמתח נשמר בעיקר דרך זרמי $\ce{K+}$.
בתיאור סכמטי בספרים, פאזה 4 מוצגת כקו ישר. בפועל יכולה להיות נטייה איטית מאוד לפעילות עצמונית, אך במצב פיזיולוגי תקין תאי החדר לא קובעים את הקצב.
פאזה 0 - דה־פולריזציה מהירה
כשהאות מגיע מתא שכן או מסיב Purkinje, נפתחות תעלות $\ce{Na+}$ תלויות-מתח. הכניסה המהירה של $\ce{Na+}$ גורמת לעלייה חדה במתח הממברנה.
זה ההבדל המרכזי בין fast response לבין slow response:
- בתאי חדר, עליית פאזה 0 תלויה בעיקר ב־$\ce{Na+}$ (תעלות מהירות)
- בתאי קוצב, עליית פאזה 0 תלויה בעיקר ב־$\ce{Ca^2+}$ (תעלות איטיות)
פאזה 1 - רה־פולריזציה התחלתית
לאחר העלייה המהירה מתחילה ירידה קצרה במתח. בשלב זה $\ce{K+}$ מתחיל לצאת מהתא, ולכן המתח מתחיל לרדת.
פאזה 2 - Plateau
ה־plateau נוצר מאיזון בין שני זרמים מנוגדים:
- כניסת $\ce{Ca^2+}$ דרך תעלות L-type
- יציאת $\ce{K+}$ מהתא
כניסת הסידן מאריכה את פוטנציאל הפעולה ומאפשרת גם את הקישור בין האות החשמלי לבין ההתכווצות המכנית.
פאזה 3 בתאי חדר - רה־פולריזציה
תעלות הסידן נסגרות, יציאת $\ce{K+}$ נעשית דומיננטית יותר, והמתח חוזר לערך המנוחה סביב $-90\,\mathrm{mV}$.
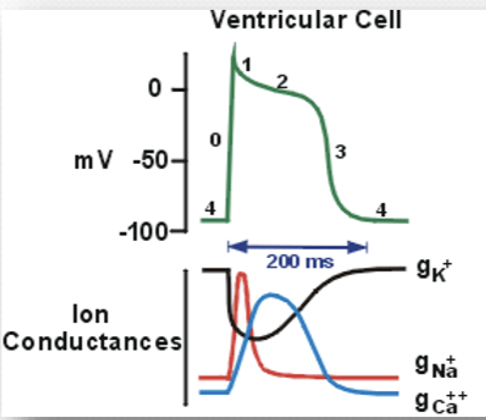
הגרפים של המוליכות מתארים מתי תעלות שונות פתוחות או סגורות. מוליכות גבוהה פירושה שהיון יכול לעבור דרך התעלה, ומוליכות נמוכה פירושה שהתעלה כמעט אינה מעבירה את היון. לכן פאזות שונות של פוטנציאל הפעולה משקפות שינוי בזמן של מוליכות לתעלות $\ce{Na+}$, $\ce{Ca^2+}$ ו־$\ce{K+}$.
סיכום עקרוני של הפאזות בתאי חדר:
| פאזה | האירוע המרכזי | יון דומיננטי |
|---|---|---|
| פאזה 4 | מנוחה יציבה | בעיקר $\ce{K+}$ |
| פאזה 0 | דה־פולריזציה מהירה | כניסת $\ce{Na+}$ |
| פאזה 1 | רה־פולריזציה התחלתית | יציאת $\ce{K+}$ |
| פאזה 2 | Plateau | כניסת $\ce{Ca^2+}$ מול יציאת $\ce{K+}$ |
| פאזה 3 | רה־פולריזציה | יציאת $\ce{K+}$ |
שמירת מפלי הריכוזים של היונים אינה מתבצעת רק דרך התעלות הפסיביות. כדי להחזיר יונים נגד מפל הריכוזים נדרשים מחליפי יונים ותהליכים תלויי-ATP, כמו מנגנוני חילוף לנתרן, אשלגן וסידן. החלק הזה לא היה מוקד השיעור, אבל הוא חשוב להבנת החזרת התא למצבו הבסיסי.
תקופה רפרקטורית
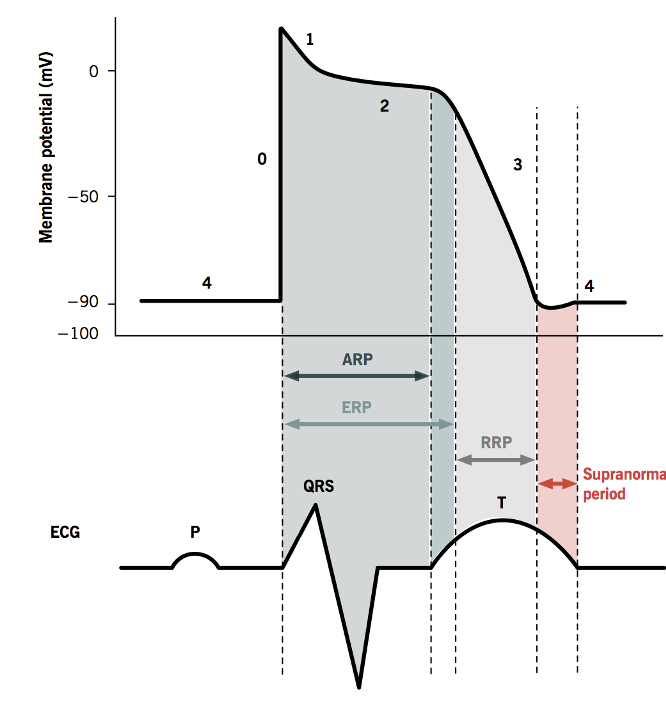
פוטנציאל הפעולה של תא חדר נמשך בערך $100\text{-}300\,\mathrm{ms}$. הפעילות המכנית של התא צמודה אליו ונמשכת מעט אחריו. לכן, בניגוד לשריר שלד, הלב לא יכול לסכום גירויים וליצור tetanus. כל פולס חשמלי אמור להוביל להתכווצות מכנית אחת.
התקופה הרפרקטורית מחולקת לכמה חלקים:
| תקופה | משמעות |
|---|---|
| Absolute refractory period - ARP | התא אינו ניתן לעירור. גם גירוי חזק לא ייצור פוטנציאל פעולה נוסף. |
| Effective refractory period - ERP | ייתכן שינוי קטן במתח הממברנה, אך הוא לא יתפשט ולא יגרום לאקטיבציה מכנית. |
| Relative refractory period - RRP | גירוי חזק מהרגיל יכול ליצור פוטנציאל פעולה נוסף. זו תקופה רגישה מבחינת הפרעות קצב. |
| Supranormal period - SP | תקופה קצרה שבה הממברנה hyperexcitable, וגירוי חלש יחסית יכול לגרום לתגובה. |
התקופה הרפרקטורית מגנה על הלב מפני אקטיבציות חוזרות ומהירות מדי. אם גירוי נוסף מצליח להופיע בתקופה היחסית, הוא יכול ליצור ביט נוסף או להוביל להפרעת קצב, בעיקר ברקמה רגישה או פגועה.
Excitation–Contraction Coupling
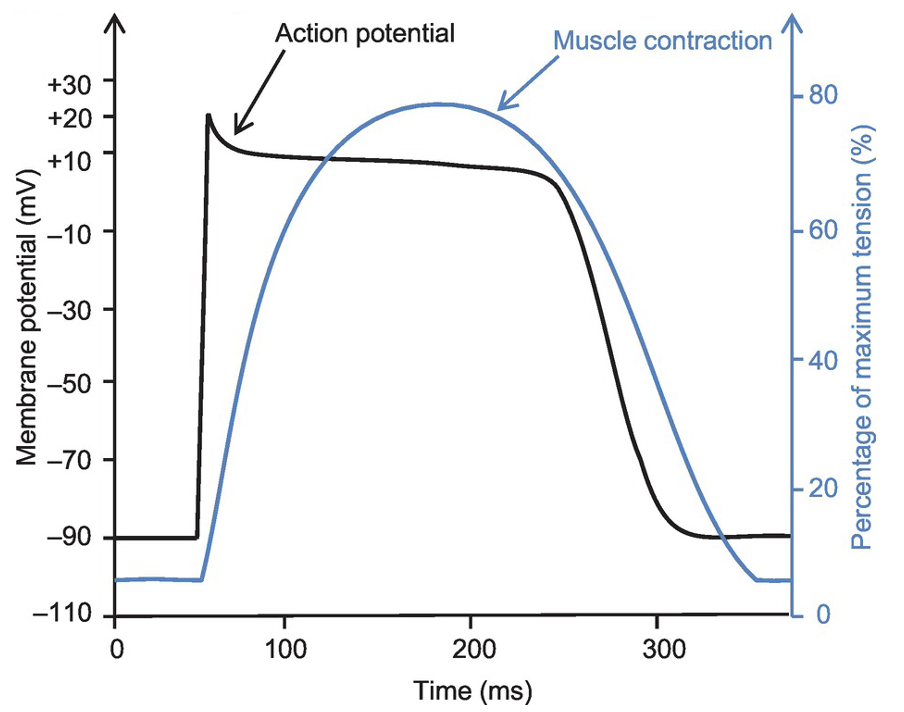
בלב יש צימוד חשמלי-מכני: שינוי במתח הממברנה מוביל להתכווצות מכנית של הקרדיומיוציט.
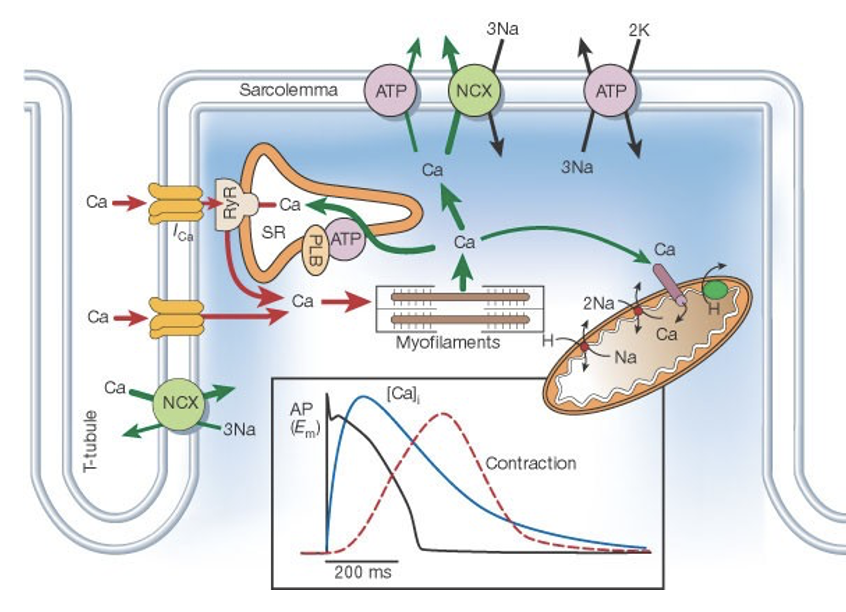
מהאות החשמלי להתכווצות
- פוטנציאל פעולה מתפשט בין קרדיומיוציטים דרך gap junctions
- הדה־פולריזציה מתפשטת לאורך הממברנה ונכנסת פנימה דרך T-tubules
- תעלות $\ce{Ca^2+}$ תלויות-מתח נפתחות בממברנה
- $\ce{Ca^2+}$ חוץ־תאי נכנס לתא
- הסידן שנכנס נקשר ל־ryanodine receptors שעל ה־sarcoplasmic reticulum (SR)
- פתיחת הרצפטורים גורמת לשחרור נוסף של $\ce{Ca^2+}$ מתוך ה־SR
- $\ce{Ca^2+}$ נקשר ל־troponin ומאפשר את פעילות actin ו־myosin
- ראשי myosin מושכים את סיבי actin, והסרקומרים מתקצרים
המנגנון שבו כניסת סידן מבחוץ גורמת לשחרור סידן נוסף מה־SR נקרא calcium-induced calcium release.
כשלושים אחוז מעליית הסידן התוך־תאי מגיעים מהסידן החוץ־תאי, והשאר מגיעים ממאגרי הסידן ב־SR. לכן התכווצות הלב תלויה מאוד בכניסת $\ce{Ca^2+}$ מבחוץ, יותר מאשר שריר שלד.
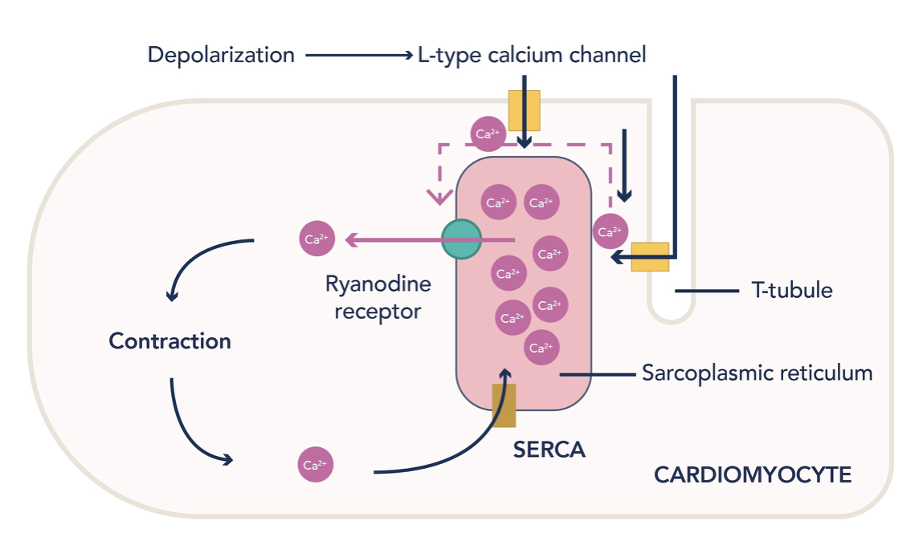
ההבדל משריר שלד
בשריר שלד יש הפעלה עצבית דרך neuromuscular junction ואצטילכולין. בלב אין צורך בנוירוטרנסמיטר בכל פעימה. האות החשמלי מתפשט דרך מערכת ההולכה ודרך gap junctions בין תאי שריר הלב.
בנוסף לכך, בשריר שלד הדה־פולריזציה יכולה להספיק לשחרור סידן מה־SR, ואילו בלב הכניסה של סידן חוץ־תאי היא חלק מרכזי מהפעלת השחרור מתוך ה־SR.
סידן, כוח התכווצות והרפיה
כמות הסידן שמשתחררת מה־SR קשורה לכוח ההתכווצות: יותר כניסת $\ce{Ca^2+}$ מבחוץ ויותר אגירת $\ce{Ca^2+}$ ב־SR יכולים להגביר את ה־contractility.
כדי שהתא יוכל להירגע ולהתכונן לפעימה הבאה, צריך להחזיר את הסידן למאגרים או להוציא אותו מהתא. החזרת הסידן ל־SR נעשית בין היתר דרך SERCA, והוצאת סידן מהתא נעשית דרך מחליפי יונים ומנגנונים תלויי-אנרגיה. כשיש ירידה ביכולת לייצר ATP, למשל בעקה מטבולית או איסכמיה, קשה יותר לשמור על מאזן הסידן, ועלולה להופיע עלייה בסידן התוך־תאי.
דור פסקל