חזקים בהפרשות?
נסו 10 שאלות בנושא, עם עדיפות לשאלות שלא הצלחתם. בסיום תקבלו ציון וסקירה על הטעויות שלכם. הצלחתם? גלו בחנים בדפים נוספים
תוצאות המבחן
היסטוריית מבחנים
טוען את השאלות...
אנא המתן...
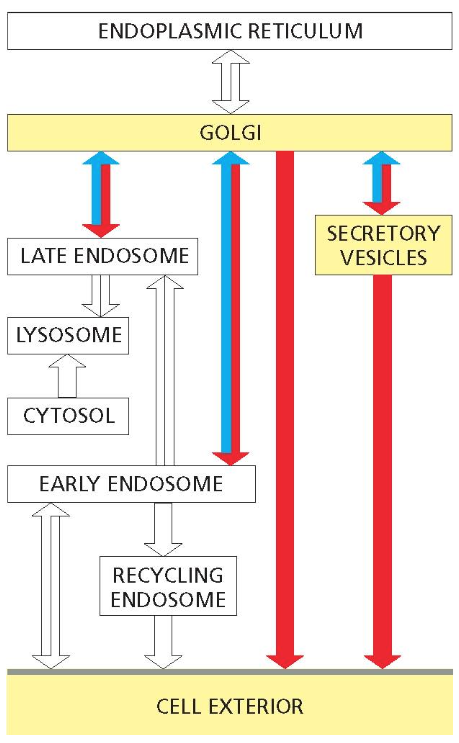
מבוא: מהרשת האנדופלסמטית אל פני התא
אקסוציטוזה מייצגת את התהליך המשלים לאנדוציטוזה - הוצאת חומרים מהתא אל הסביבה החיצונית. תהליך זה חיוני להפרשת הורמונים, נוירוטרנסמיטרים, אנזימים עיכול, וחלבונים רבים אחרים. המסלול המלא, מהרשת האנדופלסמטית (ER) דרך מערכת הגולג׳י ועד להפרשה, מכונה המסלול הסקרטורי (secretory pathway).
בפרק זה נתמקד באירועים המתרחשים ברשת הטרנס־גולג׳י (Trans-Golgi Network - TGN), האזור הדיסטלי של מערכת הגולג׳י הפונה אל הממברנה הפלסמטית. ה־TGN משמש כתחנת מיון מרכזית, שבה מתקבלות החלטות קריטיות לגבי היעד הסופי של כל חלבון.
שלושת המסלולים מהטרנס־גולג׳י
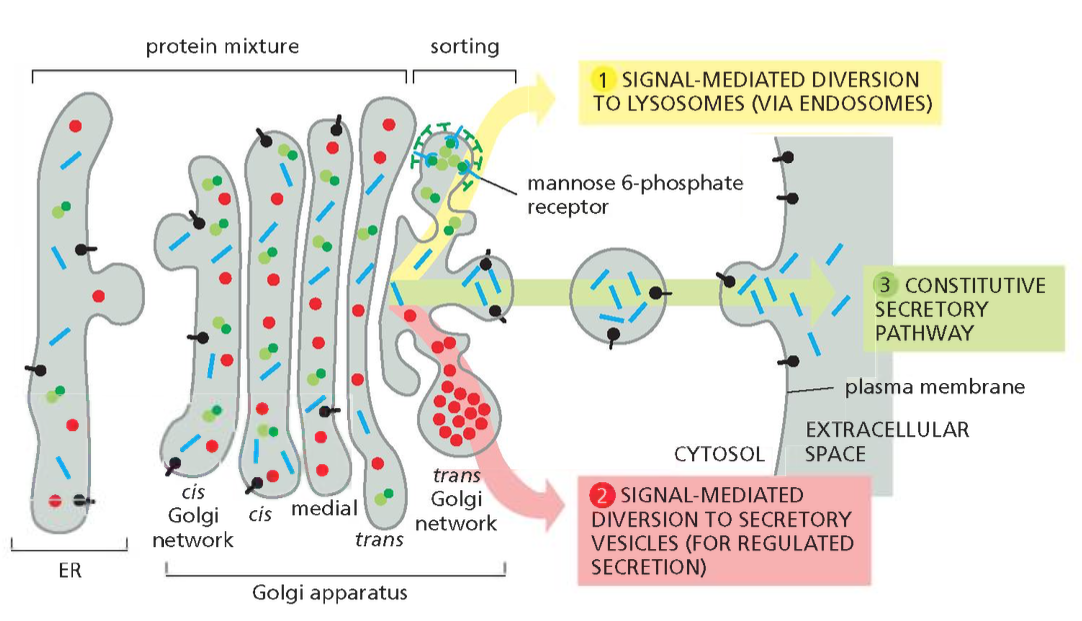
1. המסלול הליזוזומלי
הליזוזום הוא אברון מיוחד המתמחה בפירוק מקרומולקולות. הסביבה החומצית הקיצונית שלו (pH 5-4.5) וריכוז האנזימים ההידרוליטיים הגבוה הופכים אותו ל”מרכז המיחזור” של התא. חלבונים שמיועדים לליזוזום חייבים להיות מסומנים בצורה ספציפית כדי למנוע הפרשה שלהם מהתא או הגעה שלהם ליעדים שגויים.
2. הפרשה מבוקרת (Regulated Secretion)
מסלול ההפרשה המבוקרת מאפשר לתאים לשלוט על העיתוי המדויק של ההפרשה. החומרים נאגרים בגרנולות הפרשה בוגרות הממתינות לאות ספציפי - בדרך כלל עלייה בריכוז הסידן התוך־תאי. דוגמאות קלאסיות להפרשה מבוקרת כוללות:
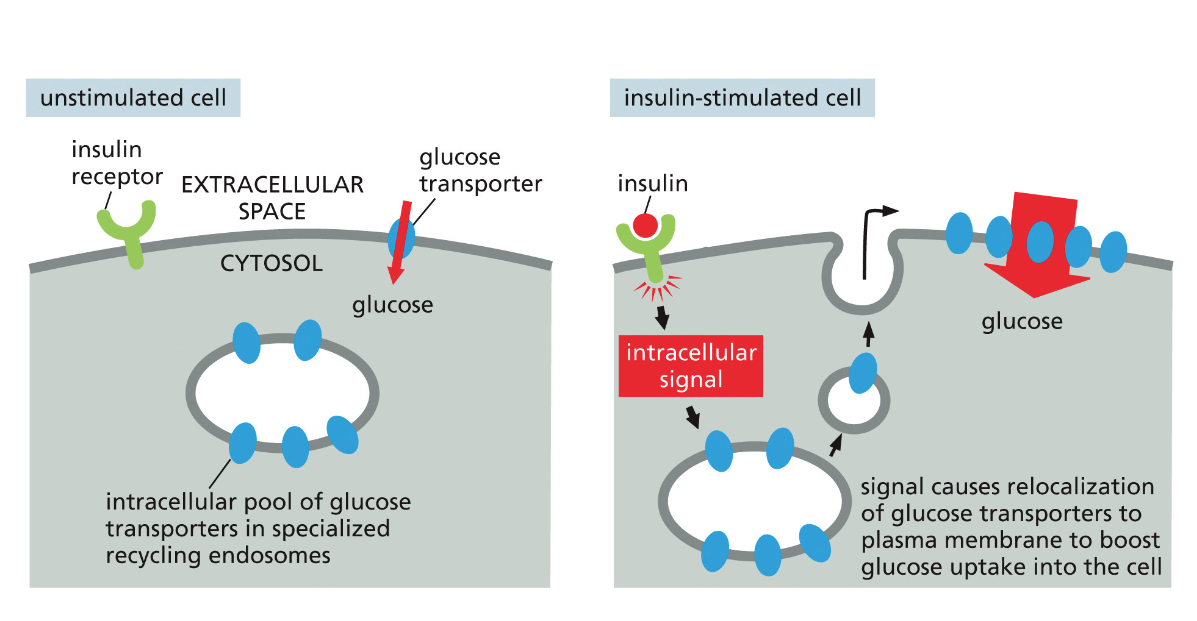
- הפרשת אינסולין מתאי בטא בלבלב בתגובה לעליית גלוקוז בדם
- שחרור נוירוטרנסמיטרים בסינפסות עצביות
- הפרשת אנזימי עיכול מתאי אצינר בלבלב
3. הפרשה קונסטיטוטיבית (Constitutive Secretion)
זהו מסלול ה”ברירת מחדל” - חלבונים שאינם נושאים סימני מיון ספציפיים מופרשים באופן רציף מהתא. מסלול זה חיוני לחידוש מתמיד של הממברנה הפלסמטית ולהפרשת חלבוני מטריקס חוץ־תאי.
סימון חלבונים ליזוזומליים: מנגנון המנוז-6-פוספט (M6P)
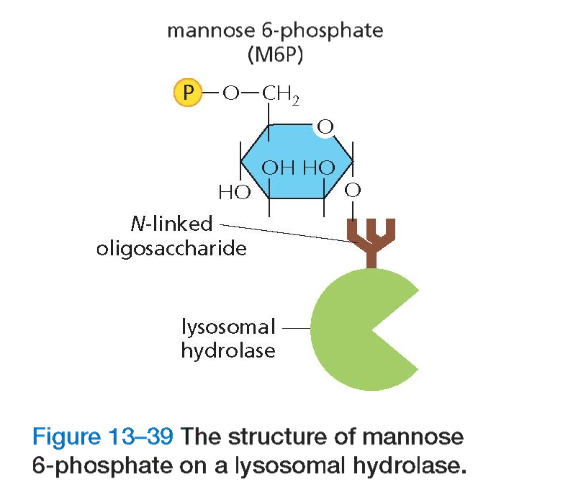
העיקרון הביוכימי
חלבונים המיועדים לליזוזום מסומנים באמצעות קבוצת מנוז-6-פוספט (M6P). תהליך הסימון מורכב ומתרחש בשלבים:
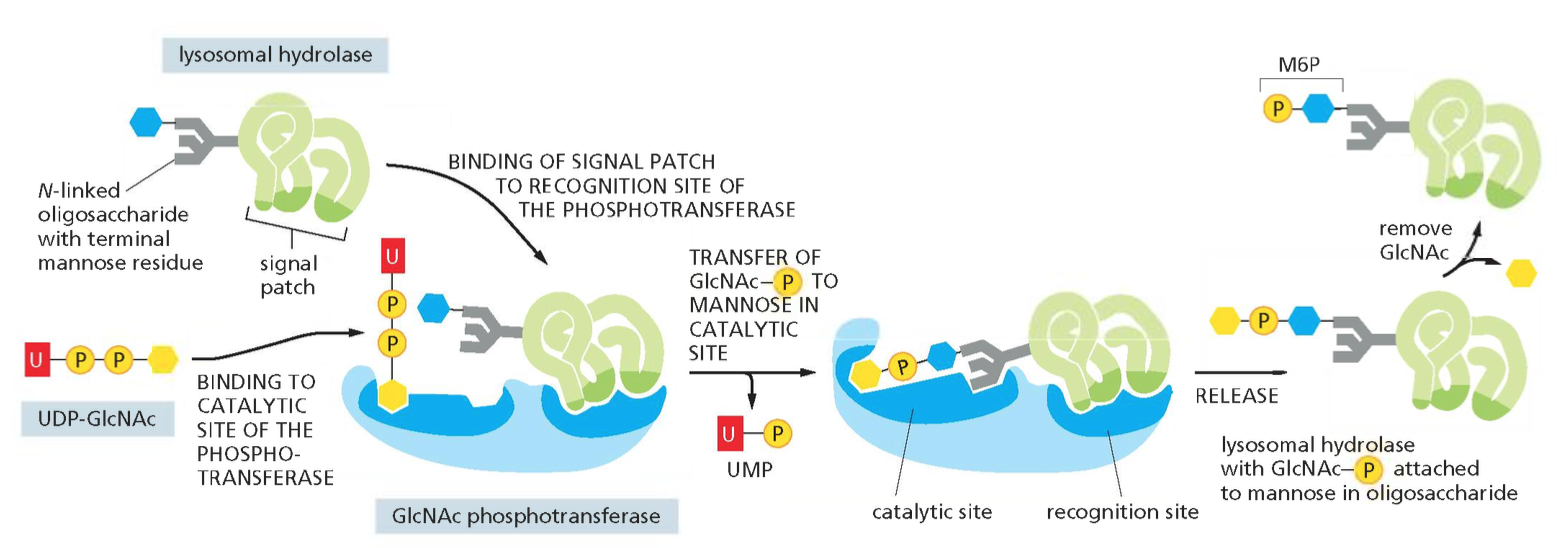
- שלב 1 - זיהוי ראשוני: אנזימים ליזוזומליים מכילים רצף אות מיוחד שנקרא “signal patch” - מבנה תלת־ממדי שמורכב מחומצות אמינו שאינן בהכרח סמוכות ברצף הראשוני.
- שלב 2 - הוספת הסימון: בציסטרנות הגולג׳י, האנזים $\text{GlcNAc-phosphotransferase}$ מזהה את ה־signal patch ומוסיף $\text{N-acetylglucosamine-phosphate}$ לשיירי מנוז על גליקופרוטאינים.
- שלב 3 - חשיפת האות: אנזים נוסף מסיר את ה־N-acetylglucosamine וחושף את קבוצת הפוספט על המנוז.
מנגנון הקישור והשחרור תלוי pH
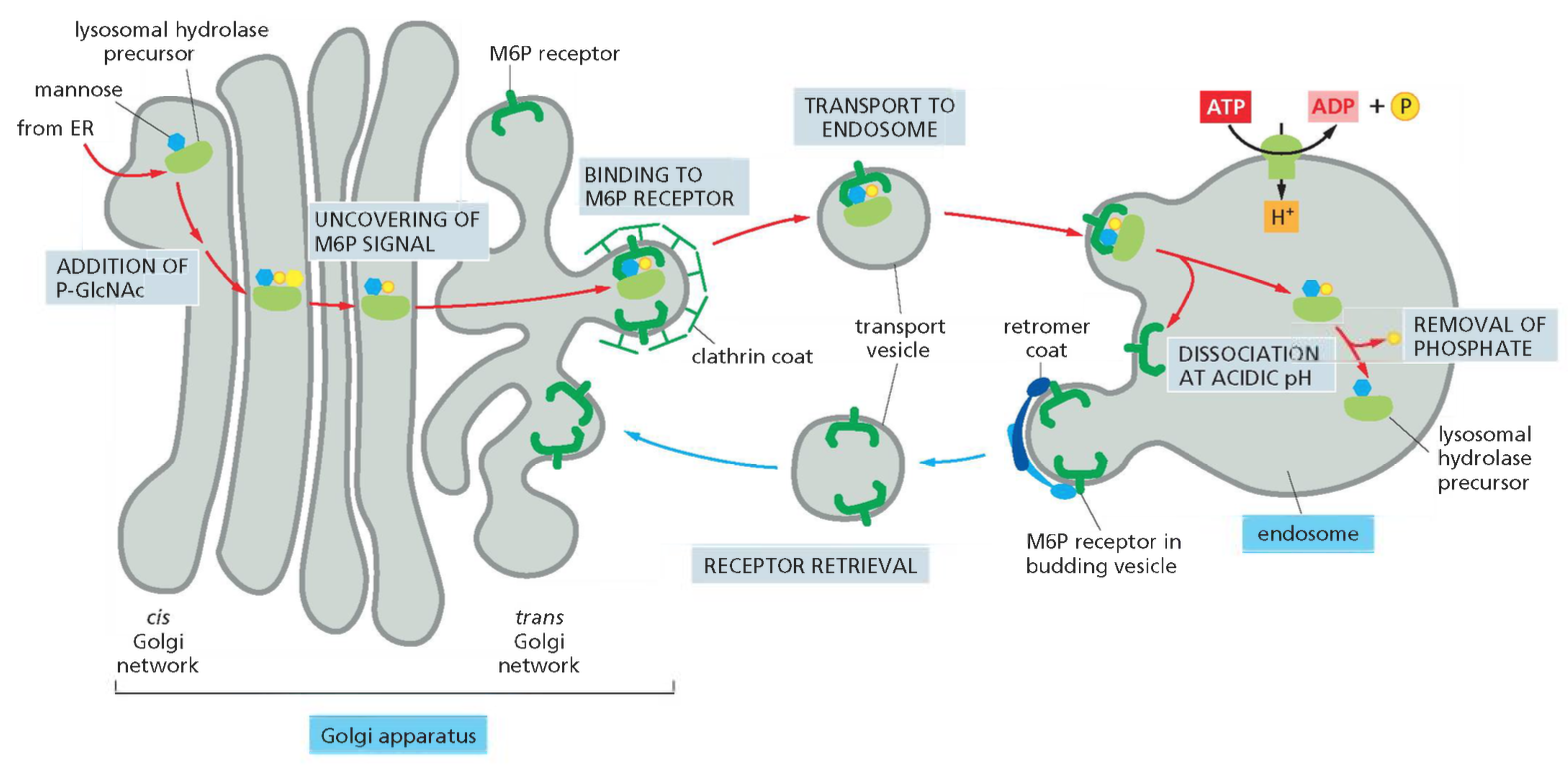
רצפטורי M6P בטרנס־גולג׳י קושרים את החלבונים המסומנים ב־pH ניטרלי (6.5-7.0). השלפוחיות העטופות קלתרין המכילות את קומפלקס הרצפטור-ליגנד נעות לעבר האנדוזומים המאוחרים והליזוזומים. ירידת ה־pH (ל־5.5-5.0) גורמת לדיסוציאציה של הקומפלקס: החלבון הליזוזומלי משתחרר לחלל הליזוזום, בעוד הרצפטור ממוחזר חזרה לגולג׳י באמצעות שלפוחיות עטופות רטרומר.
כמנגנון הגנה נוסף, פוספטאזות ליזוזומליות מסירות את קבוצת הפוספט מה־M6P, מונעות קישור חוזר לרצפטור וחזרה לא רצויה לגולג׳י.
מחלות אגירה ליזוזומליות: כשהמערכת כושלת
פגמים במנגנון ה־M6P או באנזימים ליזוזומליים גורמים למחלות אגירה ליזוזומליות. מחלות אלה מאופיינות בהצטברות חומרים שאינם מפורקים בתאים, במיוחד בנוירונים. הביטוי הקליני הראשוני הוא לרוב נוירולוגי - עיכוב התפתחותי חמור, ניוון נוירונים, ומוות מוקדם.
הרגישות המיוחדת של נוירונים נובעת מאופיים הפוסט-מיטוטי - הם אינם מתחלקים ולכן אינם יכולים “לדלל” את החומרים המצטברים באמצעות חלוקת תא. דוגמאות למחלות כוללות:
- מחלת טיי-זקס (Tay-Sachs) - חסר ב־hexosaminidase A
- מחלת גושה (Gaucher) - חסר ב־glucocerebrosidase
- מחלת פומפה (Pompe) - חסר ב־acid α-glucosidase
השכיחות הגבוהה של מחלות אלה באוכלוסיות מבודדות גנטית (כמו יהודים אשכנזים) נובעת מאפקט המייסד ונישואי קרובים היסטוריים.
תאים מפרישים מתמחים: ארגון מרחבי של ההפרשה
תאי גובלט ותאי פאנת
תאים אפיתליאליים מפרישים במעי מדגימים התמחות קיצונית להפרשה. תאי גובלט (Goblet cells) מפרישים ריר להגנה על האפיתל, בעוד תאי פאנת (Paneth cells) מפרישים פפטידים אנטי-מיקרוביאליים. בתאים אלה:
- גרנולות ההפרשה תופסות את מרבית נפח התא
- האברונים האחרים (גרעין, ER, גולג׳י) דחוסים לאזור בזאלי צר
- קיימת פולריות ברורה - הפרשה מתרחשת אך ורק מהצד האפיקלי
יצירת גרנולות הפרשה בוגרות
התהליך כולל מספר שלבי ריכוז והבשלה:
שלב הגרנולות הלא־בוגרות: שלפוחיות עטופות קלתרין יוצאות מה־TGN ומתמזגות ליצירת גרנולות ראשוניות. בשלב זה הגרנולות מכילות גם את החלבונים המיועדים להפרשה וגם חלבונים וליפידים עודפים.
תהליך ההבשלה והעיבוי: במהלך ההבשלה מתרחש תהליך של “עיבוי סלקטיבי”:
- חלבונים המיועדים להפרשה מתרכזים במרכז הגרנולה
- חומרים עודפים ממוחזרים חזרה לגולג׳י בשלפוחיות עטופות קלתרין
- התהליך חוזר על עצמו, מגדיל בהדרגה את ריכוז המטען
בסוף התהליך, גרנולות בוגרות מכילות ריכוז גבוה פי 300-200 של חלבונים להפרשה בהשוואה לריכוזם ב־ER.
מנגנון ההפרשה המבוקרת: תפקיד הסידן
חלבוני SNARE ותהליך ה־Priming
גרנולות הפרשה בוגרות נעות לאזור ההפרשה (למשל, הממברנה האפיקלית או האזור הפרה־סינפטי) שם הן עוברות:
- Docking: חלבוני v-SNAREs על הגרנולה (וזיקולה) מזהים t-SNAREs על הממברנה המטרה
- Priming: יצירת קומפלקס SNARE יציב המקרב את הממברנות עד למרחק של 2-1 ננומטר, אך עדיין מונע היתוך ספונטני
- היתוך תלוי-סידן: עלייה מקומית בריכוז הסידן (מ־100 ננומולר ל־100-10 מיקרומולר) גורמת לשינוי קונפורמציוני בחלבוני SNARE, המוביל להיתוך הממברנות ושחרור המטען.
חשיבות המנגנון בנוירונים
בסינפסות עצביות, המנגנון מאפשר תגובה תוך מילישניות לפוטנציאל פעולה:
- שלפוחיות סינפטיות ממתינות ב”מצב מוכן” (primed state)
- פתיחת תעלות סידן תלויות-מתח גורמת לזרימת סידן מקומית
- היתוך מסונכרן של מספר שלפוחיות משחרר נוירוטרנסמיטרים לסינפסה
מיחזור שלפוחיות סינפטיות: יעילות מקסימלית
המנגנון המולקולרי
נוירונים פיתחו מנגנון מיחזור מהיר לשלפוחיות סינפטיות, המאפשר תפקוד רציף ללא תלות מוחלטת בסינתזה חדשה:
Kiss-and-Run: בחלק מהמקרים, השלפוחית לא מתמזגת לחלוטין אלא יוצרת נקבובית זמנית, משחררת את תוכנה ומתנתקת
מיחזור מלא: לאחר היתוך מלא, חלבוני השלפוחית (כולל טרנספורטרים לנוירוטרנסמיטרים) נשארים בממברנה. אנדוציטוזה מקומית יוצרת שלפוחיות חדשות המכילות את החלבונים הדרושים.
מנגנון הטעינה מחדש
השלפוחיות הממוחזרות נטענות מחדש בנוירוטרנסמיטרים באמצעות:
V-ATPase: משאבת פרוטונים היוצרת גרדיאנט pH (pH 5.5 בשלפוחית לעומת 7.2 בציטופלסמה)
אנטיפורטרים ספציפיים: מנצלים את גרדיאנט הפרוטונים להכנסת נוירוטרנסמיטרים כנגד מפל הריכוזים שלהם. לדוגמה, VGLUT (vesicular glutamate transporter) מחליף פרוטון יוצא בגלוטמט נכנס.
מנגנון זה מסביר את פעולתם של תרופות נוגדות דיכאון מסוג SSRI - הן חוסמות את הטרנספורטרים המחזירים סרוטונין מהסינפסה לתא הפרה־סינפטי, מגדילות את זמן השהייה של הנוירוטרנסמיטר בסינפסה.
פולריות תאית ומיון חלבונים
מיון ישיר (Direct Sorting)
בתאים פולריים (כגון תאי אפיתל), חלבונים מסוימים חייבים להגיע לדומיין ממברנלי ספציפי. במיון ישיר:
- חלבונים נושאים סיגנלי מיון המכוונים אותם לדומיין האפיקלי או הבזולטרלי
- SNAREs ספציפיים מבטיחים היתוך רק עם הממברנה המתאימה
טרנסציטוזה
במנגנון חלופי זה:
- חלבונים מופרשים תחילה לדומיין ממברנלי אחד (לרוב הבזולטרלי)
- אנדוציטוזה סלקטיבית קולטת חלבונים ספציפיים
- השלפוחיות האנדוציטיות חוצות את התא ומתמזגות עם הדומיין הנגדי
טרנסציטוזה חשובה במיוחד להעברת נוגדנים מהאם לעובר או לתינוק היונק, כפי שראינו בפרק הקודם.
סיכום: רשת משולבת של מסלולי הובלה
מערכת האקסוציטוזה מדגימה את המורכבות והדיוק של התהליכים התאיים. שלושת המסלולים מה־TGN - ליזוזומלי, הפרשה מבוקרת, והפרשה קונסטיטוטיבית - מאפשרים לתא להתאים את תפקודו לצרכים משתנים. המנגנונים המולקולריים, מסימון M6P ועד לוויסות על ידי סידן, מבטיחים דיוק במיון ובהפרשה. הבנת מנגנונים אלה חיונית להבנת פתולוגיות רבות ולפיתוח טיפולים חדשניים.