תוכן העניינים:
- הובלה בציטופלזמה וכניסה לגרעין
- עקרונות יסוד לכל הווירוסים
- ביטוי גנים מדורג - Cascade
- מחזור ליטי ולטנטי
- וירוסי DNA - מנגנונים ספציפיים
- RNA Polymerases תאיים - איזה וירוסים משתמשים במה
- פרומוטורים ואנהנסרים
- פרומוטורים ואנהנסרים
- סיכום: אסטרטגיות מיקום
הובלה בציטופלזמה וכניסה לגרעין
הציטופלזמה צפופה מאוד, ודיפוזיה פסיבית לבדה לא מספיקה לווירוס שצריך להגיע ליעדו. הפתרון: הווירוסים “תופסים טרמפ” על מערכת המיקרוטובולים התאית. חלבונים מוטוריים כמו Dynein ו־Kinesin צועדים לאורך המיקרוטובולים תוך פירוק ATP.
- Herpesvirus עובר fusion עם ממברנת התא והקפסיד עצמו מועבר לאורך המיקרוטובולים.
- Adenovirus לעומתו נכנס בתהליך אנדוציטוזה - הקפסיד ארוז בוסיקולת אנדוזום, ירידת ה־pH גורמת לשינוי קונפורמציה בחלבונים ולשחרור הקפסיד לציטופלזמה.
| וירוס | מנגנון כניסה | מה מועבר על המיקרוטובולים |
|---|---|---|
| Herpesvirus | Fusion עם ממברנת התא | הקפסיד עצמו |
| Adenovirus | אנדוציטוזה ← ירידת pH ← שחרור מהאנדוזום | תחילה הוסיקולה, לאחר מכן הקפסיד |
לאחר מכן, הווירוס צריך לחצות את הממברנה הגרעינית דרך ה־NPC (Nuclear Pore Complex). הכלל הבסיסי: חלבון לא יכול “להחליט” להיכנס לגרעין - הוא חייב לשאת Nuclear Localization Signal (NLS) שמזוהה על ידי חלבוני ייבוא, שמובילים אותו דרך ה־NPC.
וירוסים שונים פיתחו אסטרטגיות שונות כדי לעקוף את המגבלה הזו:
- Influenza - גנום RNA מפולח; כל סגמנט ארוז עם חלבון בעל NLS ונכנס לגרעין בנפרד
- Adenovirus - הקפסיד נפתח מחוץ ל־NPC; חלבון טרמינלי עם NLS מוביל את הגנום פנימה
- Herpesvirus - הקפסיד עוגן ב־NPC אך לא נכנס. ה־DNA ארוז בלחץ פנימי אדיר של כ־20 אטמוספירות (שווה ערך לכ־190 מטר מתחת לפני הים). ה־Portal נפתח וה־DNA מוזרק לגרעין בלחץ - בדיוק כמו בקטריופאג’ים
- וירוסים קטנים - קטנים מספיק לעבור ב־NPC בשלמותם
| וירוס | אסטרטגיית כניסה לגרעין |
|---|---|
| Influenza | גנום RNA מפולח - כל סגמנט ארוז עם חלבון בעל NLS, כל סגמנט נכנס בנפרד |
| Adenovirus | הקפסיד נפתח מחוץ ל־NPC; חלבון טרמינלי עם NLS מוביל את הגנום פנימה |
| Herpesvirus | הקפסיד עוגן ב־NPC אך לא נכנס; ה־DNA ארוז בלחץ ~20 אטמוספירות (≈ 190 מ’ מתחת לים) - ה־Portal נפתח וה־DNA מוזרק לגרעין בלחץ |
| וירוסים קטנים | קטנים מספיק לעבור ב־NPC בשלמותם |
עקרונות יסוד לכל הווירוסים
וירוסים הם טפילים תוך־תאיים אובליגטוריים - הם תלויים לחלוטין בריבוזומים של התא המאכסן לייצור חלבונים. לכן המטרה המרכזית של כל וירוס היא לייצר mRNA שהמערכת התאית מכירה ויכולה לתרגם. סינתזת ה־RNA ושכפול הגנום יכולים להתבצע על ידי אנזימים ויראליים או תאיים, תלוי בוירוס.
מיקום הגנום נגזר מהלוגיקה: וירוסי DNA צריכים את RNA Pol II התאי שנמצא בגרעין, לכן הם בדרך כלל בגרעין. וירוסי RNA רוצים להיות קרוב לריבוזומים בציטופלזמה.
חריגים חשובים:
- Poxvirus (DNA בציטופלזמה - מביא מנגנון משלו)
- Hepadnavirus (גנום בגרעין, שכפול בציטופלזמה)
- Influenza ו־Retrovirus (RNA בגרעין).
| סוג גנום | מיקום רגיל | סיבה | יוצאי דופן |
|---|---|---|---|
| DNA | גרעין | מנגנון שעתוק תאי נמצא שם | Poxvirus (ציטופלזמה); Hepadnavirus (גנום בגרעין, שכפול בציטופלזמה) |
| RNA | ציטופלזמה | ריבוזומים נמצאים שם | Retrovirus; Influenza (RNA בגרעין) |
לגבי RNA Polymerases תאיים: רוב הווירוסים משתמשים ב־RNA Pol II לייצור mRNA. RNA Pol III משמש חלק מהווירוסים לייצור RNA פונקציונלי קצר ומדויק. אין כרגע דוגמאות לווירוס המשתמש ב־RNA Pol I.
ביטוי גנים מדורג - Cascade
אחד העקרונות החשובים ביותר בווירולוגיה: הגנים הנגיפיים לא מתבטאים כולם בבת אחת, אלא בקסקדה מבוקרת.
-
Immediate Early - הגנים הראשונים, מתבטאים תוך דקות מההדבקה. תוצריהם הם בדרך כלל Transcription Factors שמפעילים את השלב הבא. אינם תלויים בחלבונים ויראליים חדשים - המערכת התאית מספיקה, ולעיתים החלבון כבר מגיע עם הוויריון עצמו (כמו VP16 ב־HSV).
-
Early - מקודדים בעיקר לחלבוני שכפול: DNA Polymerase, אנזימים נלווים. תלויים ב־Immediate Early, אך אינם תלויים בשכפול הגנום.
-
Late - חלבוני קפסיד וחלבונים מבניים. מתבטאים רק לאחר שכפול הגנום - ומסיבות טובות: אין טעם לייצר קפסידים ריקים לפני שיש גנומים לארוז, וחלבוני קפסיד נוצרים בכמויות עצומות ורעילים לתא, לכן עדיף לייצרם רק לקראת סוף ההדבקה.
Immediate Early → Early → שכפול הגנום → Late
| שלב | מה מתבטא | תלות | דוגמאות |
|---|---|---|---|
| Immediate Early | Transcription factors | לא תלוי בחלבונים ויראליים חדשים; לעיתים החלבון מגיע עם הוויריון | SV40: Large T-Ag; Adenovirus: E1A; HSV: VP16 |
| Early | חלבוני שכפול (DNA Pol, אנזימים) | תלוי ב־Immediate Early; אינו תלוי בשכפול | |
| שכפול הגנום | — | נקודת מפנה מרכזית | |
| Late | חלבוני קפסיד (מבניים) | רק לאחר שכפול |
למה Late רק אחרי שכפול?
- אין טעם לייצר קפסידים ריקים לפני שיש גנומים לארוז
- חלבוני Late נוצרים בכמויות עצומות ורעילים לתא - עדיף לייצרם רק לקראת סוף ההדבקה
כיצד מזהים בניסוי מה שייך לאיזה שלב:
- מוסיפים מעכב סינתזת חלבון - אם עדיין מתבטא, זה Immediate Early.
- מוסיפים מעכב שכפול הגנום - אם עדיין מתבטא, זה Early; אם לא מתבטא, זה Late.
| שיטה | מה מגלים |
|---|---|
| מעכב סינתזת חלבון (cycloheximide) - עדיין מתבטא? | Immediate Early - לא תלוי בחלבונים ויראליים חדשים |
| מעכב סינתזת חלבון - לא מתבטא? | Early לפחות - תלוי ב־IE |
| מעכב שכפול הגנום - עדיין מתבטא? | Early - לא תלוי בשכפול |
| מעכב שכפול הגנום - לא מתבטא? | Late - תלוי בשכפול |
מחזור ליטי ולטנטי
כשוירוס כמו Herpesvirus מגיע לתא מטרה, הוא יכול לבחור באחת משתי אסטרטגיות:
- Lytic cycle: שכפול מסיבי, ייצור ויריונים, פיצוץ התא.
- Latency: הגנום נשמר בתא (כפלסמיד מעגלי/אפיזום, או לאחר אינטגרציה לגנום המאכסן), ביטוי מינימלי שרק שומר על הגנום ומונע זיהוי חיסוני.
- בעת סטרס - Reactivation ומעבר חזרה לליטי.
ההחלטה תלויה גם בסוג התא: אותו וירוס יכול להיות ליטי בתא אחד ולטנטי בתא אחר.
| Lytic | Latency | |
|---|---|---|
| מה קורה | שכפול מסיבי, ייצור ויריונים, פיצוץ התא | הגנום נשמר בתא, ביטוי מינימלי של חלבונים |
| שמירת הגנום | — | כפלסמיד מעגלי (אפיזום) או אינטגרציה לגנום המאכסן |
| יתרון | הפצה מהירה | הימנעות ממערכת חיסון, שרידות ארוכת-טווח |
| מי עובר | כל הווירוסים | בעיקר Herpesvirus וRetrovirus באיקריוטים |
reactivation מתרחש בעת סטרס (UV, חום, מחלה) - הווירוס עובר מלטנסי חזרה לליטי.
בקטריופאג’ λ - מודל קלאסי
שני חלבוני מפתח קובעים אם הווירוס ייבחר בלטנסי או בליטי: cI ו־Cro.
cI (Lambda Repressor) מדכא גנים ליטיים ומחזק את הביטוי של עצמו בלולאת משוב חיובי - כל עוד הוא קיים, הווירוס נשאר בלטנסי. אך הוא רגיש לסטרס: פרוטאז תאי חותך ומפרק אותו. ברגע שcI נעלם, Cro מצטבר, מעכב את cI ומפעיל את הגנים הליטיים.
מנגנון מעניין נוסף: תקשורת בין תאים (Arbitrium). בפאזה הליטית נוצר חלבון קטן שמופרש לסביבה. כשריכוזו גבוה - כלומר הרבה חיידקים כבר מודבקים - הוא מעודד כניסה ללטנסי בתאים חדשים. כך הווירוס לא “הורג” את כל המאכסנים הפוטנציאליים שלו.
| חלבון | פעולה | מה קורה בסטרס |
|---|---|---|
cI (Lambda Repressor) | מדכא גנים ליטיים; מחזק ביטוי עצמו (positive feedback) | פרוטאז תאי חותך אותו ← נעלם |
| Cro | מעכב cI; מפעיל גנים ליטיים | מצטבר ברגע ש־cI יורד |
כל עוד cI גובר ← לטנסי. ברגע שנעלם ← Cro משתלט ← ליטי.
תקשורת בין תאים (Arbitrium): בפאזה הליטית נוצר חלבון קטן שמופרש לסביבה. כשריכוזו גבוה (= הרבה תאים כבר נדבקו), הוא מעכב מעבר לליטי בתאים חדשים - מנגנון שמונע מהווירוס להרוג את כל המאכסנים הפוטנציאליים.
Superinfection Immunity: וירוס בלטנסי מונע כניסת וירוסים נוספים מאותו סוג (מעכב אנזימים המפרקים פפטידוגליקן, ומונע כניסת DNA ויראלי) - לא צריך לזכור פרטים, רק את הרעיון.
וירוסי DNA - מנגנונים ספציפיים
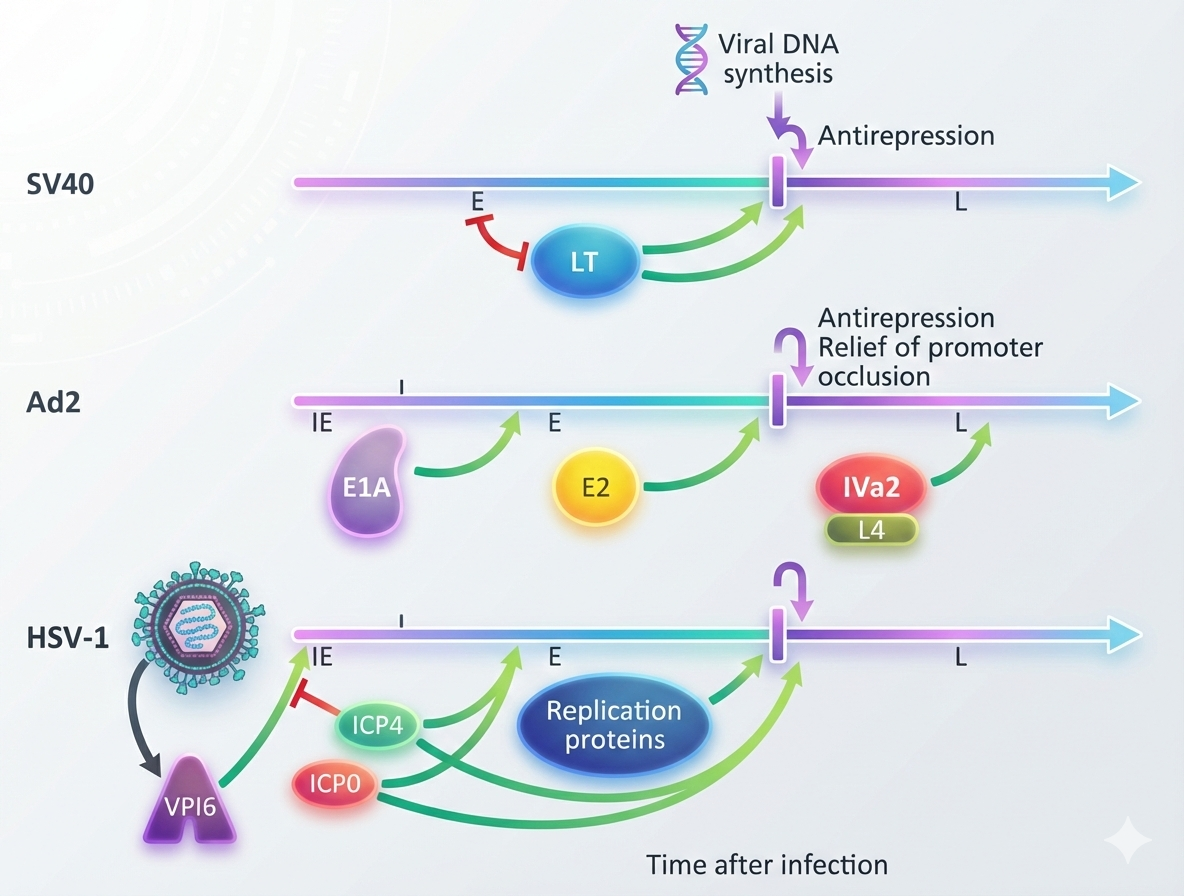
SV40
גנום דו־גדילי מעגלי ($\sim 5,000 \, \mathrm{bp}$), ארוז בנוקלאוזומים גם בתוך הוויריון עצמו. Large T-Antigen (תוצר Early) חוזר לגרעין ומגייס את מערכת הרפליקציה התאית לשכפל את הגנום הנגיפי.
מנגנון הבקרה על Late genes מעניין (“דילול הרפרסור”):
חלבון תאי (IBP) נמצא ברמה קבועה בתא ומדכא את ה־Late Promoter.
- בתחילת ההדבקה: יש מעט גנומים ויראליים - IBP מספיק לדכא הכל.
- לאחר שכפול: מספר הגנומים עולה בגדול אך כמות ה־IBP נשארת קבועה - הוא לא מספיק לדכא את כולם, וה־Late genes מתחילים להתבטא.
Adenovirus
גנום דו־גדילי ליניארי ($\sim 36,000 \, \mathrm{bp}$). חלבון ה־Immediate Early, E1A, הוא הדמות המרכזית כאן. הוא פועל על ידי קישור ל־Rb (Retinoblastoma protein).
במצב תקין, Rb קושר ומעכב את E2F (Transcription factor), ומונע מהתא להיכנס לשלב S-phase (השלב שבו מתרחשת סינתזת DNA).
כשE1A קושר את Rb, E2F משתחרר ופעיל - מה שגורם לביטוי גנים ויראליים וגם דוחף את התא ל־S-phase, שם, יש שפע נוקלאוטידים לשכפול הווירוס.
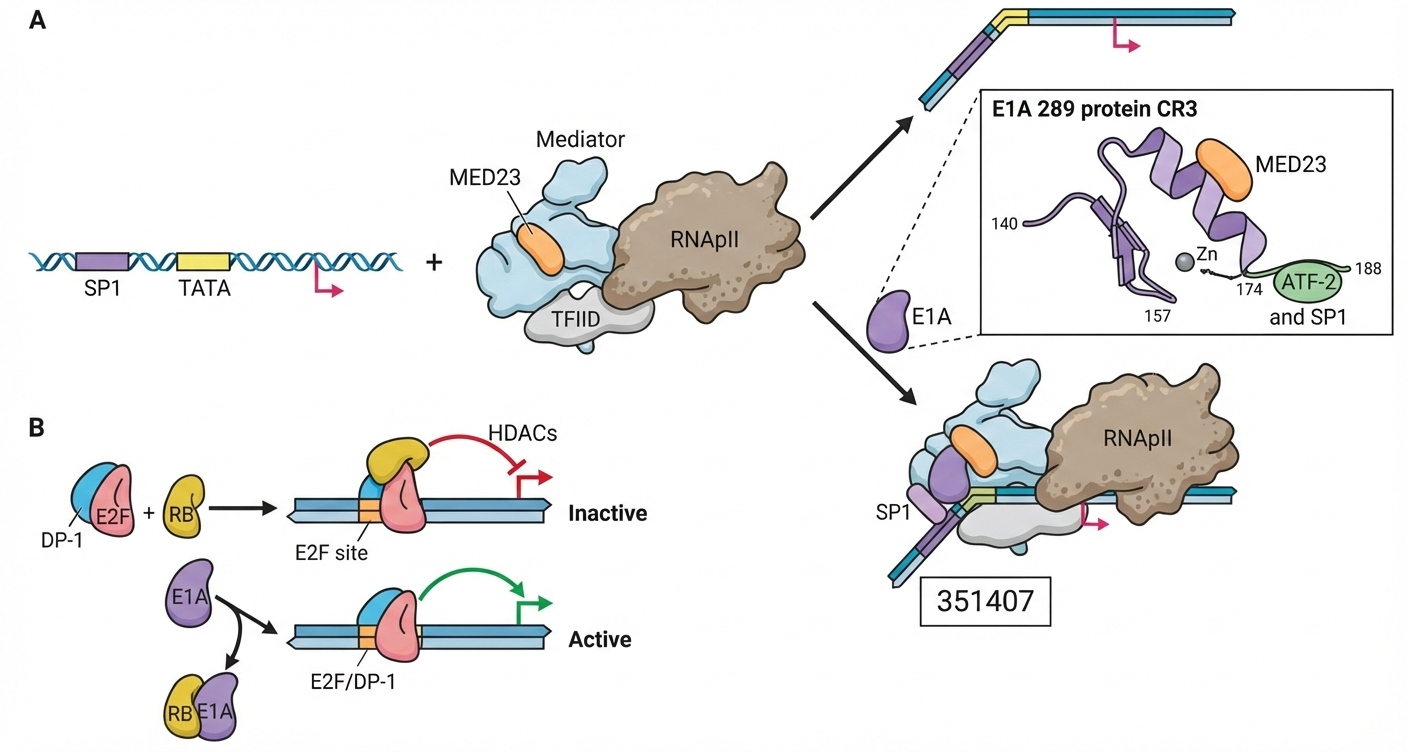
הקשר לסרטן: Papillomavirus (E7) עושה אותו דבר בדיוק לRb. Rb הוא Tumor Suppressor קלאסי, ומוטציות בו גורמות לסרטן. יש אפילו אותו רצף שמור (conserved) שמזהה את Rb בוירוסים שונים - עדות לאבולוציה מתכנסת.
גילוי היסטורי חשוב: ה־splicing התגלה ב־Adenovirus. כשהיברידיזציה בין ה־DNA ל־mRNA גילתה loops גדולים - הוכחה שלא כל רצף ה־DNA מיוצג ב־mRNA הבשל.
HSV-1 (Herpes Simplex Virus)
VP16 מגיע עם הוויריון (חלבון Tegument) ויוצר קומפלקס עם שני חלבונים תאיים - Oct-1 ו־HCF - הופך אותם לאקטיבטורי שעתוק חזקים ומפעיל את Immediate Early genes (ICP4, ICP0). הקפסידים גדולים מדי ל־NPC, ולכן הם יוצאים בתהליך של ממש קריעת ממברנת הגרעין - Nuclear Egress.
מדוע לטנסי בנוירונים? הכל תלוי ב־HCF. בתאי אפיתל, HCF נמצא בגרעין ← קומפלקס VP16+Oct-1+HCF נוצר ← Lytic cycle. בנוירונים, HCF נמצא בציטופלזמה ← הקומפלקס לא נוצר ← Latency. בלטנסי, הגנום ארוז ב־repressive chromatin. בעת סטרס, פוספורילציה של היסטונים פותחת את הכרומטין ← reactivation.
קלינית: זה מסביר את פצעי השפתיים החוזרים. הווירוס נדבק לתאי אפיתל (ליטי) ← עובר לנוירוני הגנגליון (לטנסי) ← UV/חום/סטרס ← reactivation ← נדידה חזרה לשפתיים ← פצעים. חוזר ונשנה לכל החיים.
מחזור ליטי:
- הקפסיד נכנס עם חלבוני Tegument (שכבה בין קפסיד לממברנה)
- VP16 (חלבון Tegument שמגיע עם הוויריון) ← יוצר קומפלקס עם Oct-1 + HCF ← מפעיל Immediate Early genes (ICP4, ICP0)
- קפסידים גדולים מדי ל־NPC ← Nuclear Egress: קריעת הממברנה הגרעינית
מדוע לטנסי בנוירונים?
תאי אפיתל נוירונים מיקום HCF גרעין ציטופלזמה VP16 + Oct-1 + HCF קומפלקס נוצר בגרעין HCF לא בגרעין ← קומפלקס לא נוצר תוצאה Lytic cycle Latency בלטנסי: הגנום ארוז ב־repressive chromatin. בעת סטרס: פוספורילציה של היסטונים ← chromatin נפתח ← reactivation.
קלינית: HSV-1 ← פצעי שפתיים. וירוס נשאר רדום בגנגליון ← UV/חום/סטרס ← reactivation ← נדידה חזרה לשפתיים ← פצעים חוזרים לכל החיים.
Poxvirus (Vaccinia) - חריג קיצוני
למרות שהוא וירוס DNA, משכפל בציטופלזמה בלבד ומביא את כל מנגנון השעתוק שלו:
- Viral RNA polymerase (דומה לפולימראזות אוקריוטיות)
- mRNA capping enzyme
- Poly(A) polymerase
- Methyltransferases
לאחר כניסה לתא, הקפסיד נפתח חלקית, mRNA יוצא ועובר תרגום, והחלבונים שנוצרים ממשיכים את מחזור ההדבקה. נקודה חשובה: הוא עדיין צריך נוקלאוטידים מהתא - אותם הוא לא מביא.
AAV (Adeno-Associated Virus) ssDNA
גנום חד־גדילי (ssDNA) בוויריון. לאחר כניסה, המערכת התאית משלימה ל־dsDNA. אינו יכול לשכפל ביעילות לבד ודורש helper virus (Adenovirus או HSV) - ומכאן שמו, שכן תמיד גילו אותו ביחד עם Adenovirus. כיום כלי מרכזי ב־gene therapy בשל בטיחותו היחסית.
RNA Polymerases תאיים - איזה וירוסים משתמשים במה
| פולימראז | מה הוא מייצר | שימוש ויראלי |
|---|---|---|
RNA Pol I | rRNA (18S, 28S, 5.8S), tRNA | אין דוגמאות לווירוס המשתמש בו |
RNA Pol II | mRNA, microRNA, lncRNA | רוב הווירוסים - מייצרים mRNA לחלבונים שלהם |
RNA Pol III | RNA קצר ומדויק (tRNA, 5S rRNA) | חלק מהווירוסים - לייצור RNA פונקציונלי (לא mRNA) |
פרומוטורים ואנהנסרים
Promoter ממוקם בדיוק לפני הגן - מיקומו וכיוונו קריטיים. מכיל לעיתים TATA box הנקשר על ידי TBP (TATA Binding Protein); כ־50% מהפרומוטורים התאיים מכילים TATA box.
Enhancer שונה מהותית: הוא יכול לפעול ממרחקים עצומים (מאות אלפי $\mathrm{bp}$), מ־upstream או downstream לפרומוטור, ואפילו בכיוון הפוך - לכן הוא מוגדר כ־position and orientation independent.
המנגנון הוא DNA looping - לולאה פיזית ב־DNA מקרבת את האנהנסר לפרומוטור. מסתבר שאנהנסרים גם מייצרים RNA קצר שאינו מקודד לחלבון (eRNA), שמסייע לחיבור הפיזי הזה.
פרומוטורים ואנהנסרים
| Promoter | Enhancer | |
|---|---|---|
| מיקום | בדיוק לפני הגן, מיקום קריטי | יכול להיות upstream, downstream, או רחוק מאוד (עד מאות אלפי bp) |
| כיוון | חד־כיווני | פועל גם בכיוון הפוך |
| מנגנון | מקום תחילת השעתוק | DNA looping - לולאה פיזית מקרבת בין אנהנסר לפרומוטור |
| מייצר RNA? | לא | כן - eRNA (enhancer RNA) שאינו מקודד לחלבון, ומסייע לחיבור הפיזי |
| הגדרה | — | רצף שמגביר שעתוק position and orientation independent |
| מי קושר | TBP קושר TATA box (~50% מהפרומוטורים התאיים) | Transcription factors + coactivators |
KSHV כדוגמה מחקרית עכשווית: נמצאו 6 אנהנסרים בגנום - 2 קונסטיטוטיביים/לטנטיים, 1 ספציפי לתאי אנדותל, ו־4 ליטיים בלבד. הפעלת אנהנסר ליטי יכולה לדחוף את הווירוס לליטי סייקל, ועיכובו - אולי לעכבו.
גילויים היסטוריים דרך וירוסים:
- Splicing - גילוי ב־Adenovirus (loops בהיברידיזציה DNA-mRNA)
- Enhancers - האנהנסר הראשון גולה ב־SV40 (שני רצפים של 72 bp ← פי 100 ביטוי)
- General Transcription Factors (GTFs) - זוהו דרך ניסויי in vitro עם פרומוטורים ויראליים (HIV LTR, Adenovirus Major Late Promoter) - ניסוי G-less cassette
לשיעורים הבאים: Retrovirus, RNA viruses, Hepadnavirus
סיכום: אסטרטגיות מיקום
| סוג וירוס | מיקום | סיבה |
|---|---|---|
| רוב DNA viruses | גרעין | משתמשים ב־RNA Pol II תאי |
| Poxvirus | ציטופלזמה | מביא מנגנון משלו |
| רוב RNA viruses | ציטופלזמה | קרוב לריבוזומים |
| Influenza (RNA) | גרעין | חריג |
| Retrovirus | גרעין | חריג |