תוכן העניינים:
- Sonic Hedgehog (Shh)
- כולסטרול
- Smo
- שני מודלים שמסבירים את תפקיד Patched
- Primary Cilia
- GPCR
- Shh ביונקים
- Shh Production
- Dispatch
- Notch
- Feedback Loops
Sonic Hedgehog (Shh)
משפחת ה־Hedgehog כוללת שלושה ליגנדים: Shh, Ihh ו־Dhh. הרצפטורים הם Ptch1 ו־Ptch2, והמולקולה שמעבירה את הסיגנל בתוך התא היא Smoothened (Smo). בהמשך המסלול פועלים פקטורי השעתוק Gli1, Gli2, Gli3.
Shh Pathway
העיקרון הבסיסי של המסלול שמור אבולוציונית ומתחלק לשני מצבים: מצב שבו אין ליגנד, ומצב שבו יש ליגנד.
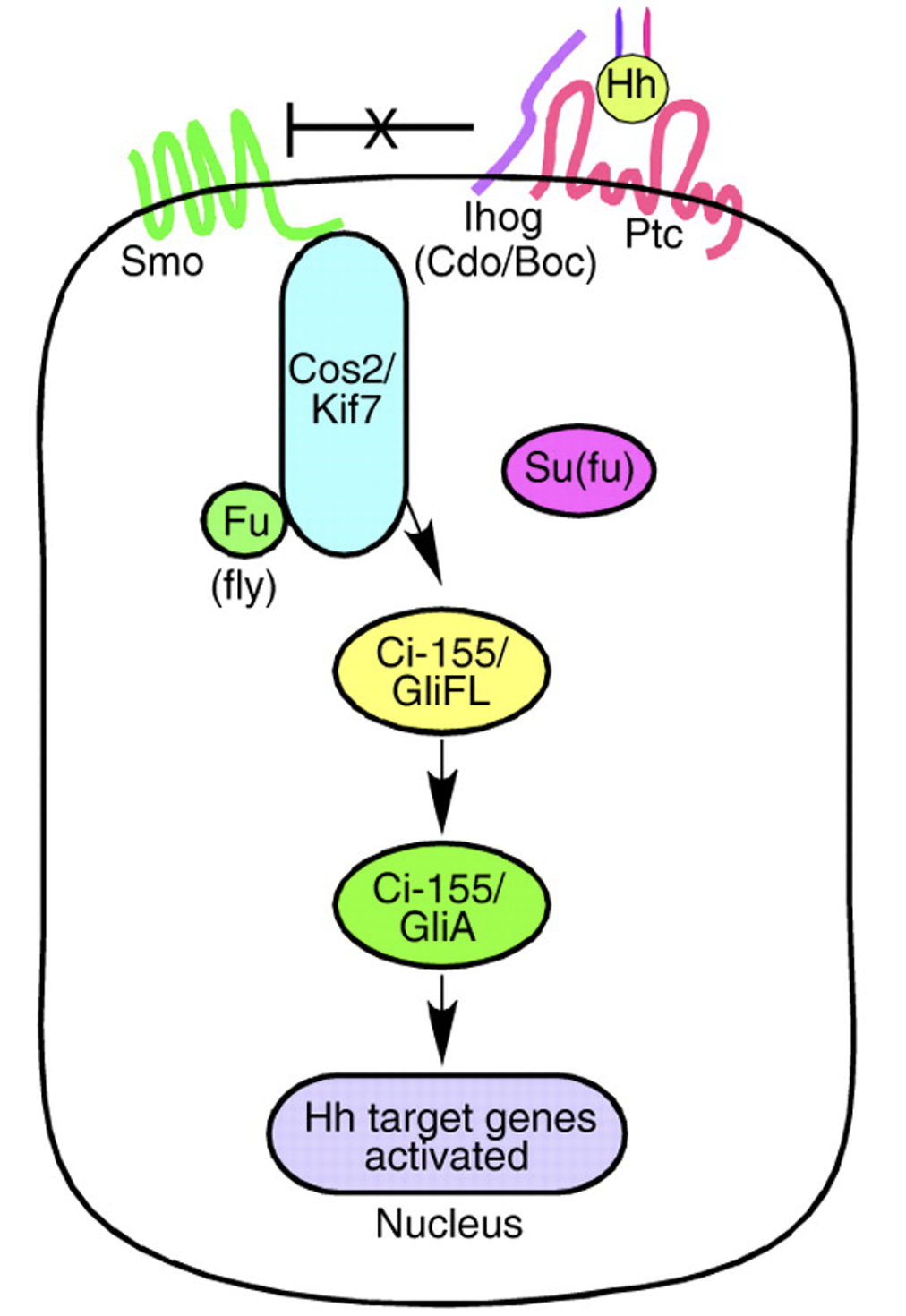 | 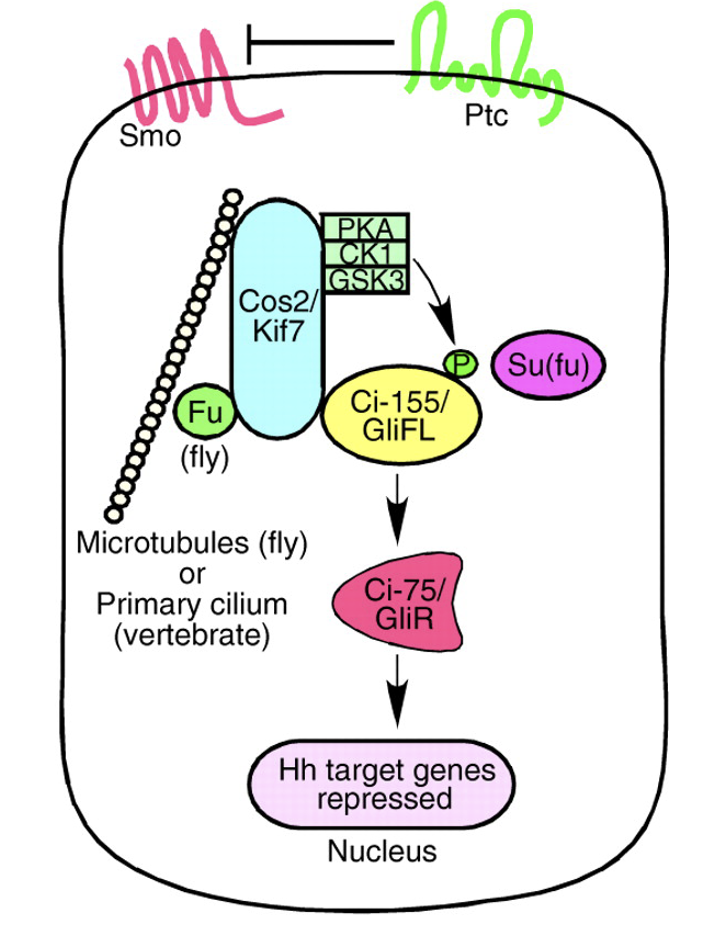 |
מצב ללא ליגנד
כשאין ליגנד בסביבה (התמונה השמאלית), Patched מעכב את Smoothened, ולכן המסלול כבוי. פקטור השעתוק, Gi-155 בזבובים (או GliFL מלשון full-length ביונקים), עובר עיבוד חלקי: הוא מזורחן, מסומן לדגרדציה חלקית בפרוטאוזום, ובמקום החלבון המלא מתקבלת צורה קצרה ורפרסורית. בזבוב מקבלים את Ci-75, וביונקים את GliR. הצורה הרפרסורית (שהיא transcription factor לפי השיעור) נכנסת לגרעין ויושבת על גני המטרה של המסלול (כרפרסור), ולכן אין שעתוק של גני Hedgehog.
מצב עם ליגנד
כשיש ליגנד (התמונה הימנית), Sonic Hedgehog נקשר ל־Patched (הרצפטור) ומעכב אותו. ברגע שהעיכוב של Patched משתחרר Smoothened נהייה פעיל. כתוצאה מכך פקטור השעתוק (Ci-155/GliFL) כבר לא עובר עיבוד חלקי לרפרסור, אלא נשאר באורך מלא ועובר שינוי נוסף, לא פרוטאוליטי, שהופך אותו לצורה אקטיבטורית, GliA. הצורה האקטיבטורית נכנסת לגרעין וגורמת להפעלה של שעתוק.
באיורים למעלה - המעבר מצבע ורוד לצבע ירוק מסמן את ההחלפה מרפרסור לאקטיבטור.
- GliR - Repressor form of Gli
- GliA - Activator form of Gli
Smo ו־Ptch1
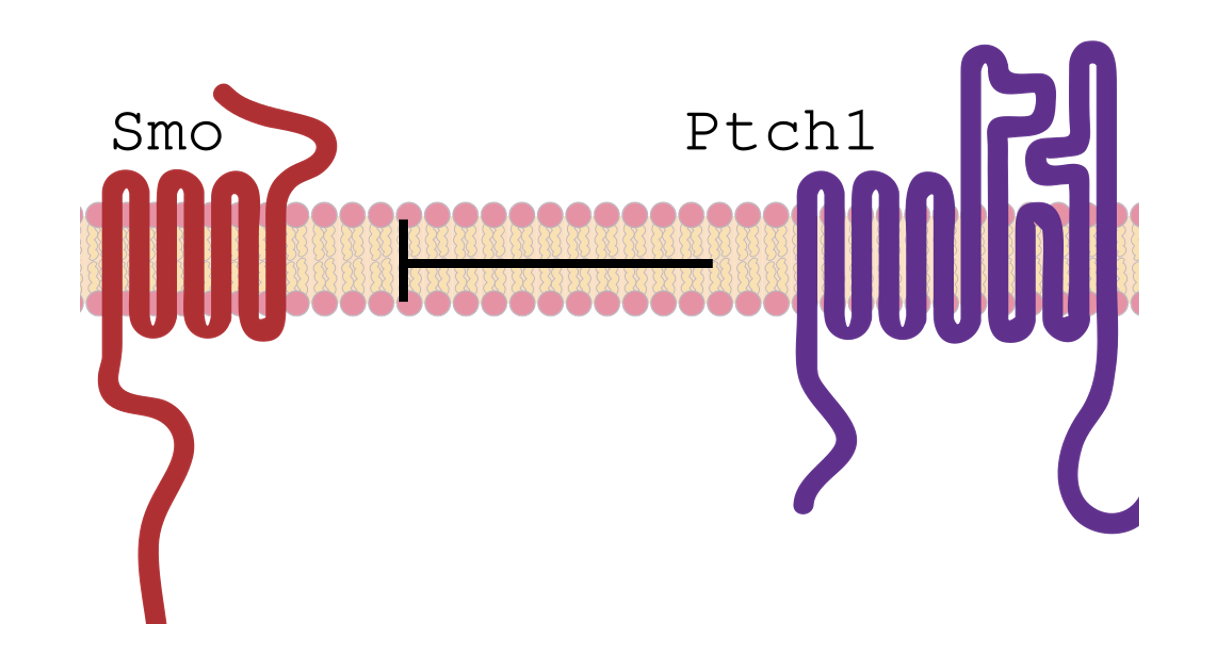
Smoothened (השמאלי באיור) הוא חלבון ממברנלי שחוצה את הממברנה שבע פעמים, ולכן מזכיר מבחינה מבנית חלבוני GPCR. לעומתו, Patched (הימני) חוצה את הממברנה 12 פעמים.
היחס בין Smo ל־Ptch1 הוא Sub-stoichiometric. כלומר, Patched לא נקשר ל־Smoothened ביחס פשוט של אחד לאחד ומעכב אותו (אם זה היה המצב היינו מצפים ליחס סטויכיומטרי פשוט). העובדה שזה לא כך רומזת ש־Patched כנראה לא מעכב את Smoothened במגע ישיר, אלא פועל בדרך אחרת, ככל הנראה כטרנספורטר.
חלבונים סאב־סטויכיומטרים לדוגמה הם אנזימים או טרנספורטרים.
The Transporter Hypothesis
מתוך הנתונים לעיל עלתה השערת הטרנספורטר, לפיה Patched הוא טרנספורטר שמעביר מולקולה קטנה כלשהי, והיא זאת שקובעת אם Smoothened יהיה פעיל או לא.
אפשר היה לחשוב על שני כיוונים:
-
Patched (האדום בתמונה) מוציא מהממברנה או מהסביבתה מולקולת אקטיבטור, ולכן בהיעדר הליגנד shh אין מה שיפעיל את Smoothened (הכחול בתמונה).
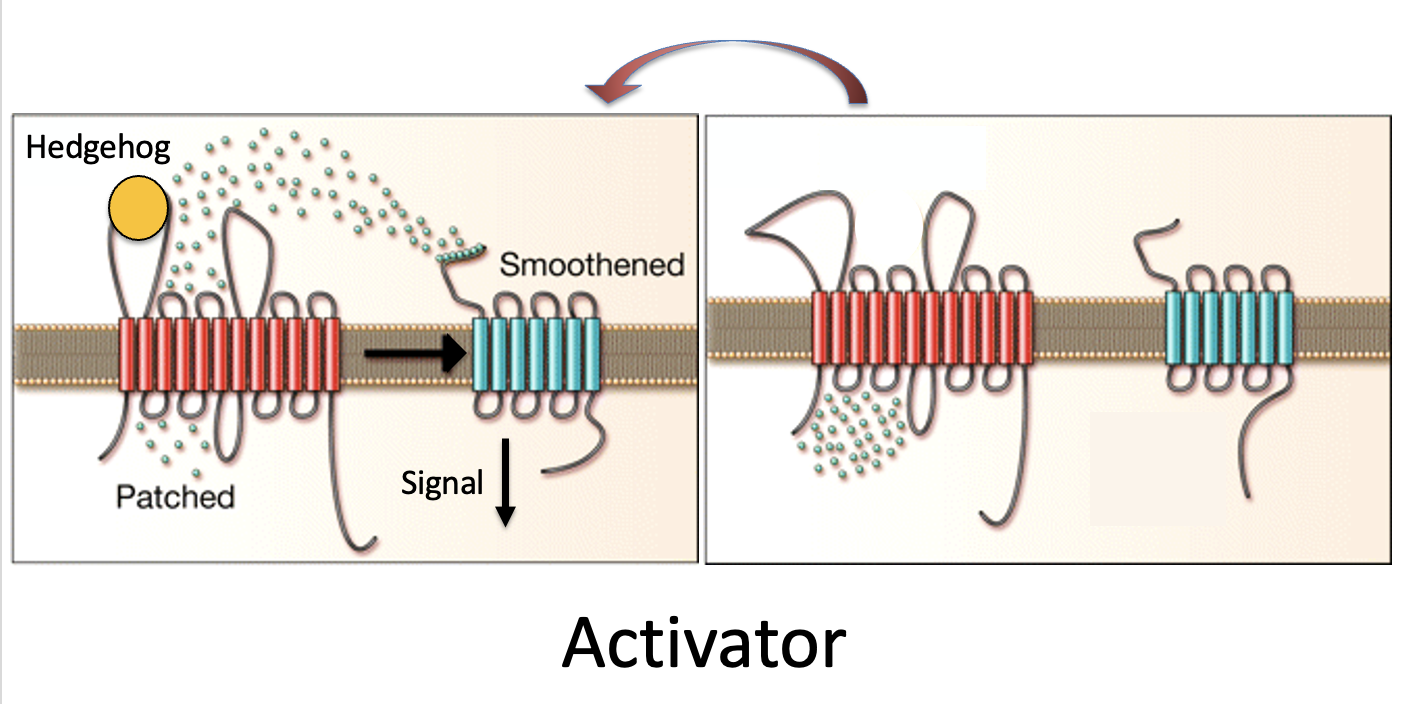
-
Patched מעביר מולקולת מעכב, וכך מונע מ־Smoothened לפעול.
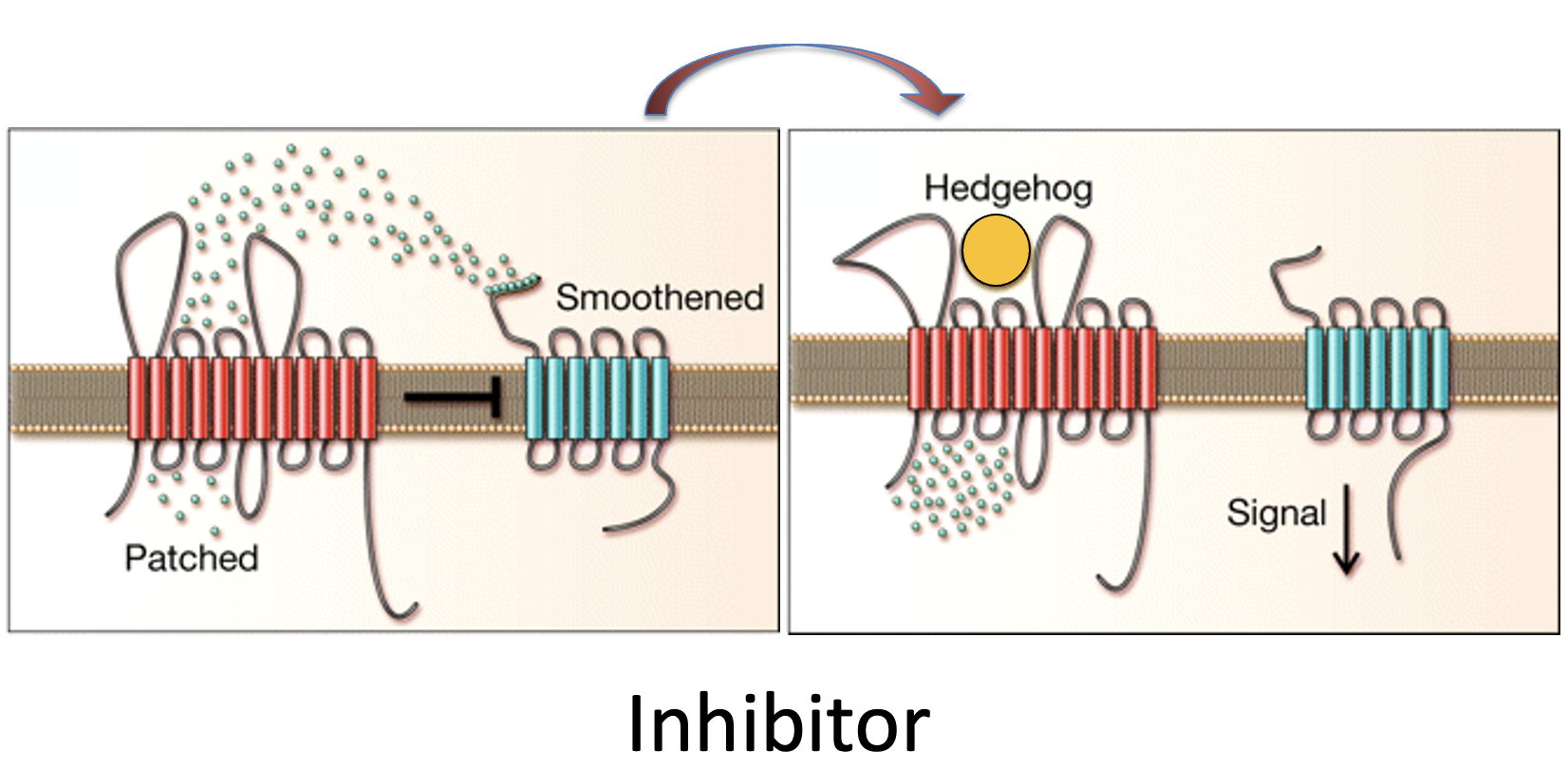
בשני המקרים הליגנד Shh נקשר ל־Patched, משנה את פעילות הטרנספורטר שלו, ובכך משנה בעקיפין את מצב הפעילות של Smoothened.
הנקודות הקטנות באיור אינן Hedgehog עצמו, אלא מולקולה אחרת במסלול, קטנה יותר, ש־Patched יודע להעביר.
כולסטרול
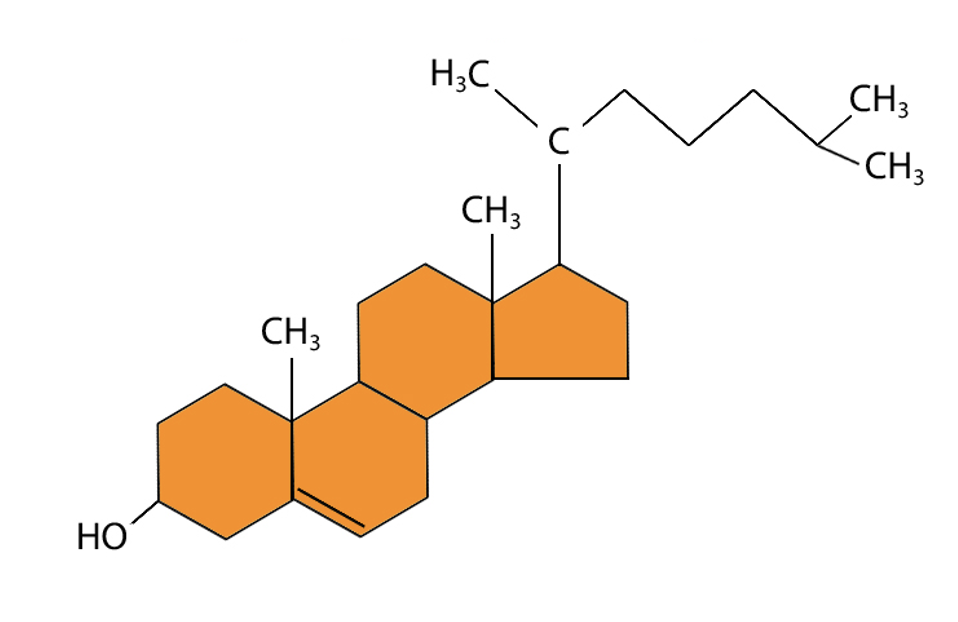
המולקולה שהתבררה כמועמדת הרלוונטית היא כולסטרול. לכולסטרול יש שלד הידרופובי קשיח, ורק קבוצת הידרוקסיל אחת שבולטת מעט לכיוון פני הממברנה. חשוב לזכור שכולסטרול חופשי נמצא במצב תקין רק בממברנה. לא מדובר במולקולה שנעה בחופשיות בציטוזול, אלא ברכיב ממברנלי.
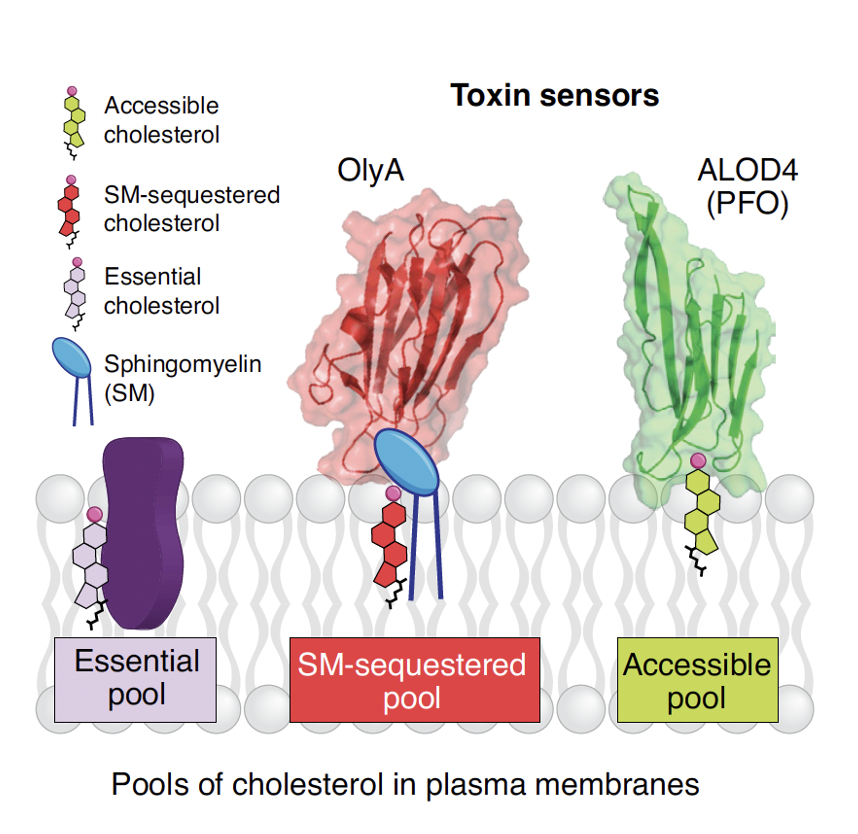
בתוך הממברנה אין “בריכה” אחת אחידה של כולסטרול, אלא יש כמה מאגרים שונים:
-
Essential pool - כולסטרול שקשור לרכיבים חיוניים בממברנה ולכן אינו זמין.
-
SM-sequestered pool - מאגר שבו הכולסטרול קשור ל־Sphingomyelin, וגם הוא אינו זמין.
-
Accessible pool - המאגר של הכולסטרול החופשי והנגיש. זה הכולסטרול שמעניין אותנו בהקשר של Smoothened.
אפשר לזהות את המאגרים השונים באמצעות חלבונים ייעודיים: למשל OlyA מזהה כולסטרול שקשור ל־sphingomyelin, ואילו ALOD4 מזהה את המאגר הנגיש של הכולסטרול החופשי.
Smo
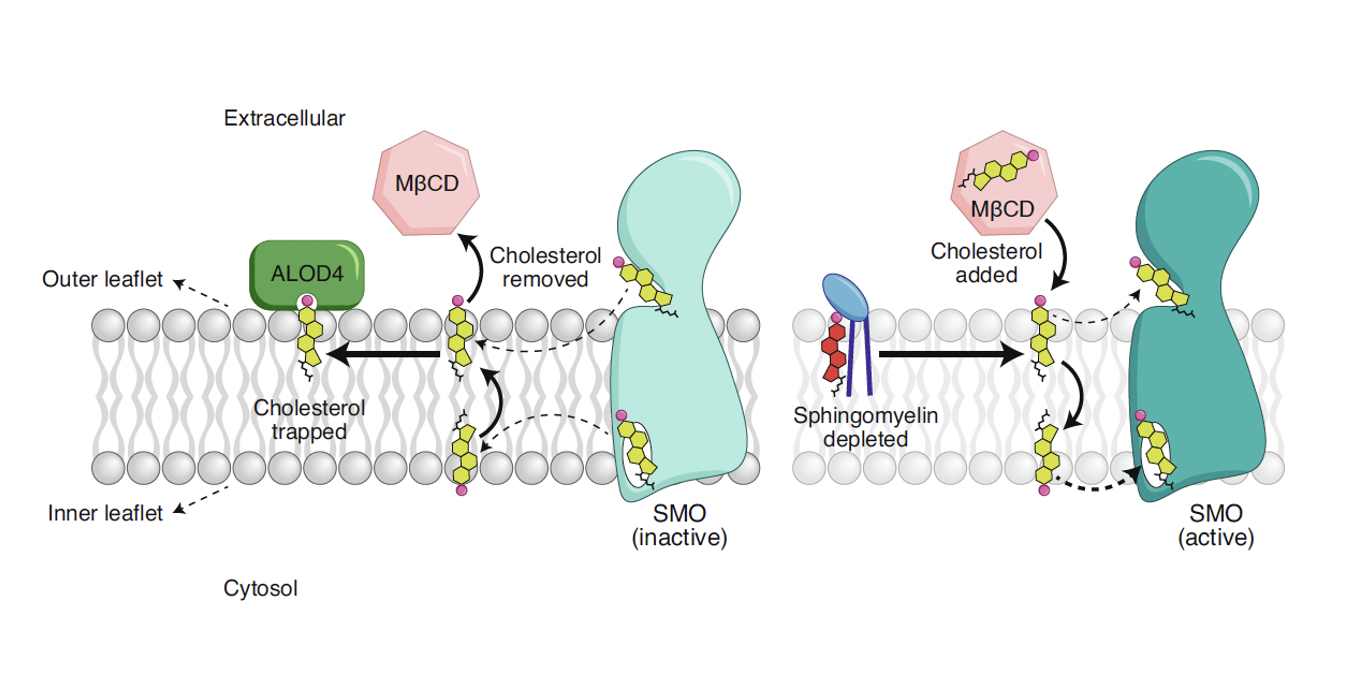
הנקודה המרכזית היא שכולסטרול הוא הליגנד של Smoothened. כשמרוקנים את הממברנה מכולסטרול נגיש, Smoothened מפסיק להיות פעיל, וכשמעלים את ריכוז הכולסטרול החופשי, Smoothened נעשה פעיל.
ממבנים קריסטלוגרפיים גם ידוע של־Smoothened יש אתרים שיכולים לקשור כולסטרול. לכן, הכולסטרול כאן הוא לא רק רכיב מבני של הממברנה, אלא ממש מולקולה שמפעילה את החלבון. מכאן גם ברור כיצד הקשר בין Patched ל־Smoothened אינו ישיר: Patched שולט בזמינות של הכולסטרול, והכולסטרול שולט בפעילות של Smoothened.
שני מודלים שמסבירים את תפקיד Patched
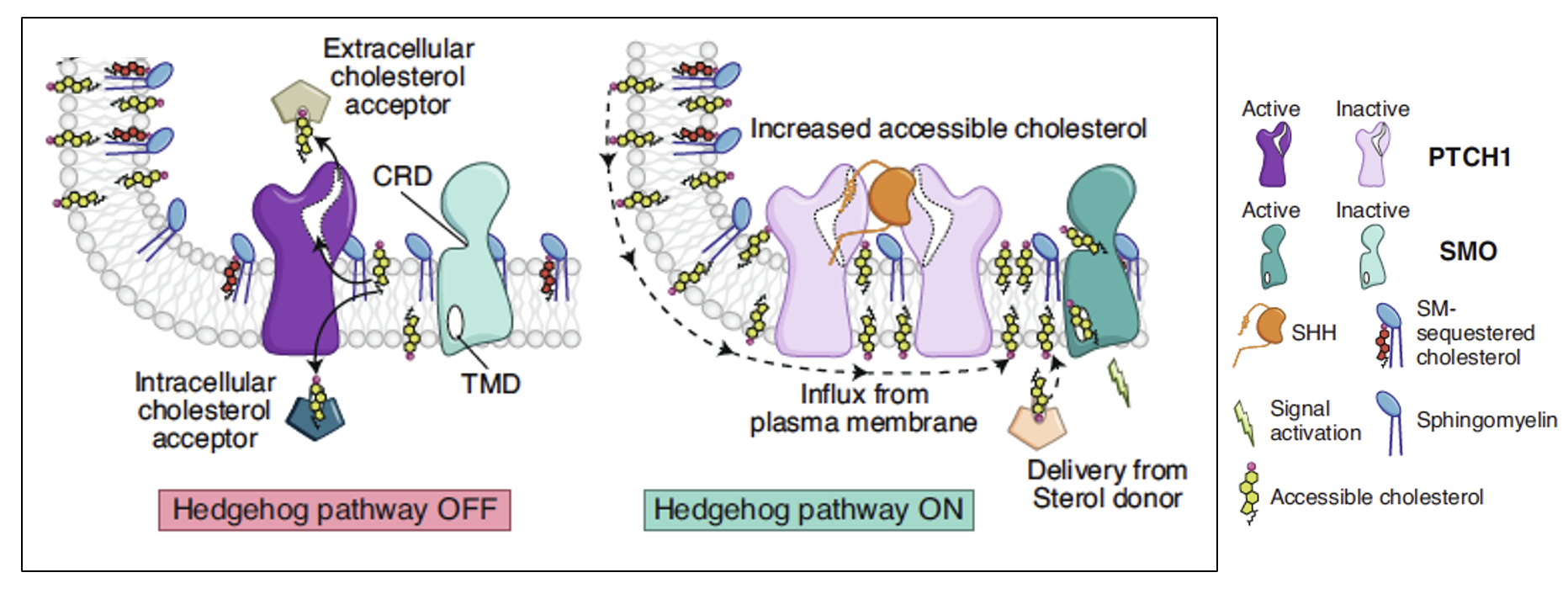
במודל הראשון Patched מסלק כולסטרול מהממברנה אל אקספטור כלשהו, שאיננו יודעים עדיין לזהות. כל עוד Patched פעיל, ריכוז הכולסטרול הנגיש בממברנה נשאר נמוך, ולכן אין ליגנד שייקשר ל־Smoothened והוא נשאר לא פעיל. כאשר Shh נקשר ל־Patched, פעילות הטרנספורט נעצרת; הכולסטרול נשאר בממברנה, נקשר ל־Smoothened, והמסלול מופעל.
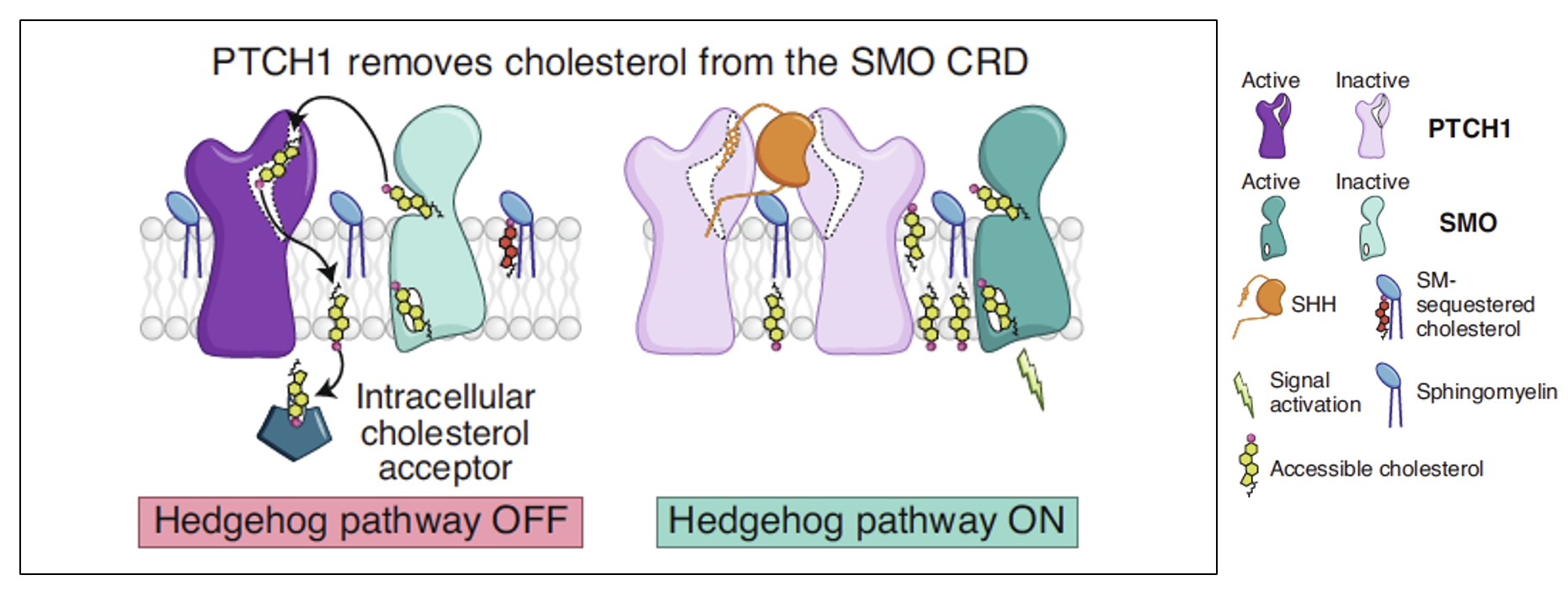
במודל השני Patched עדיין מסלק כולסטרול, אבל לא מהממברנה באופן כללי אלא ישירות מ־Smoothened. כלומר, הוא “שולף” מהחלבון את הכולסטרול הדרוש להפעלתו. גם כאן ברגע ש־Shh נקשר ל־Patched, התהליך הזה נעצר, הכולסטרול נשאר קשור ל־Smoothened, ו־Smoothened הופך פעיל.
ההבדל בין שני המודלים הוא מכני: האם Patched מוריד את רמת הכולסטרול בסביבה של החלבון, או פועל ישירות על החלבון עצמו. העיקרון נשאר זהה.
Ptc as an Antiporter
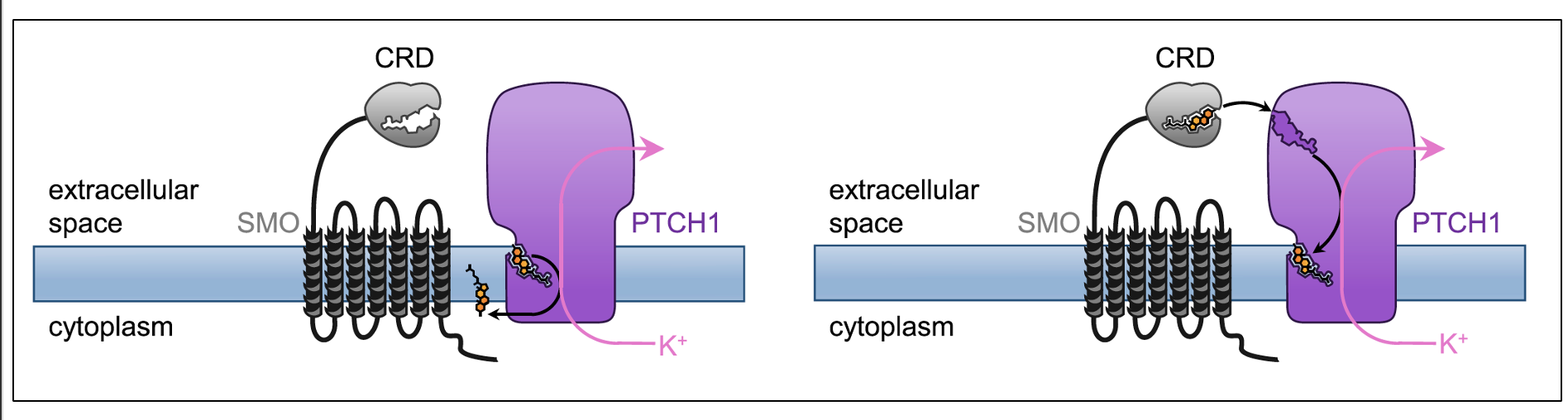
כדי לבצע טרנספורט צריך אנרגיה. Patched הוא antiporter, והוא מנצל את מפל הריכוזים של אשלגן (מבפנים החוצה) כדי לבצע את פעולתו. ריכוז האשלגן גבוה בתוך התא, ומפל הריכוזים מאפשר ל־Patched לבצע את העברת המולקולה בלי להסתמך ישירות על ATP. הרעיון החשוב כאן הוא ש־Patched איננו חלבון פסיבי; הוא טרנספורטר פעיל שמשתמש במפל יונים כדי לשלוט בזמינות הכולסטרול ובכך במצב של המסלול כולו.
Primary Cilia
כדי להבין כיצד מסלול Shh פועל ביונקים צריך לעבור דרך אברון תאי חשוב: Primary Cilia.

לרוב התאים יש Primary Cilia אחד. לפעמים רואים שניים אבל זה חריג. זה מבנה דמוי אנטנה שבולט מפני התא, ויש לו תפקיד חשוב בתפקוד תאי ובקליטת סיגנלים. פגיעות בו קשורות לקבוצת מחלות רחבה בשם ciliopathies.
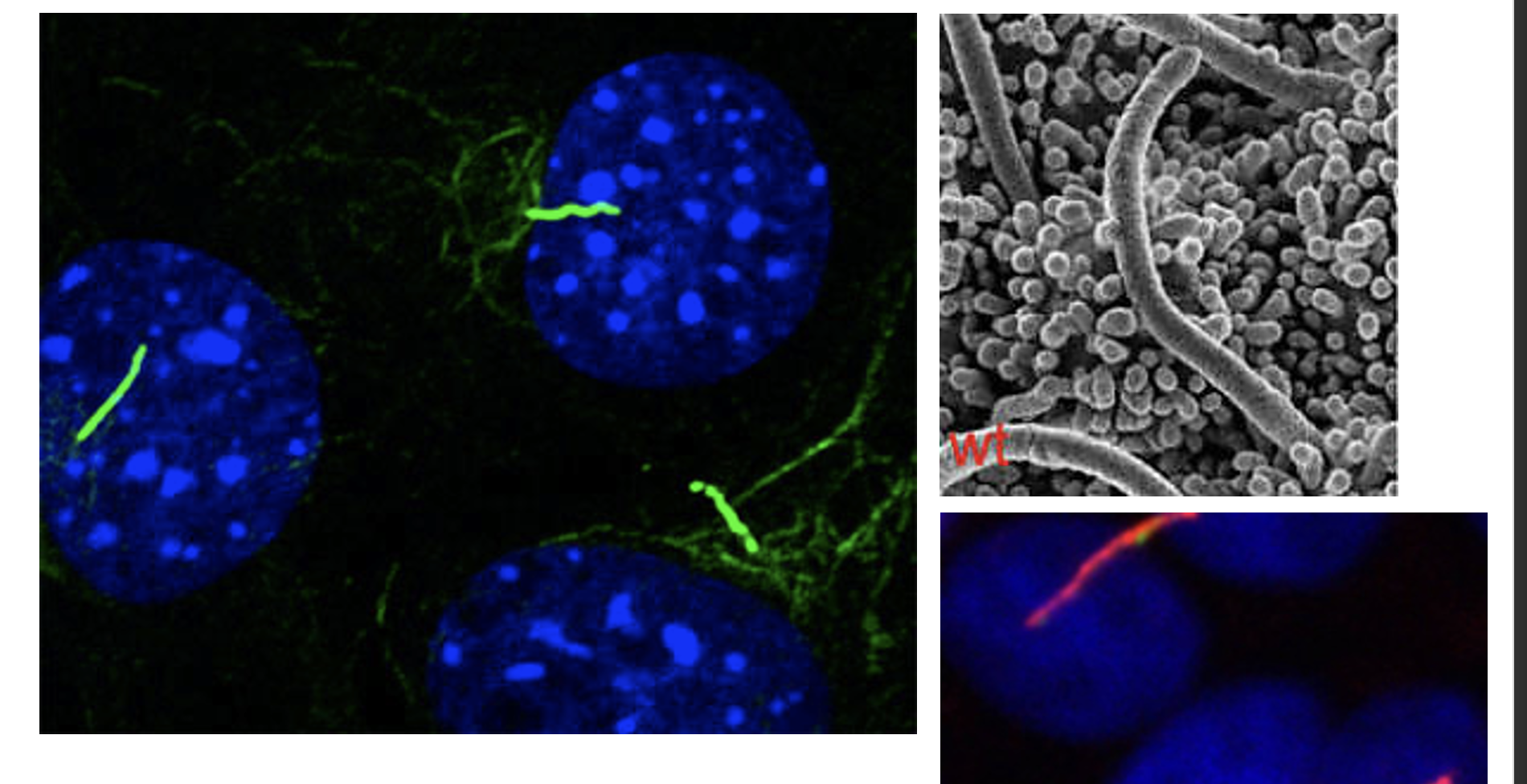
אפשר לזהות Primary Cilia בעזרת צביעה של גרעינים ב־DAPI ובמקביל צביעה אימונוהיסטוכימית של חלבון שנמצא ספציפית ב־Cilia. כך מתקבל מבט ברור על ה־Cilia כשלוחה בודדת שיוצאת מהתא.
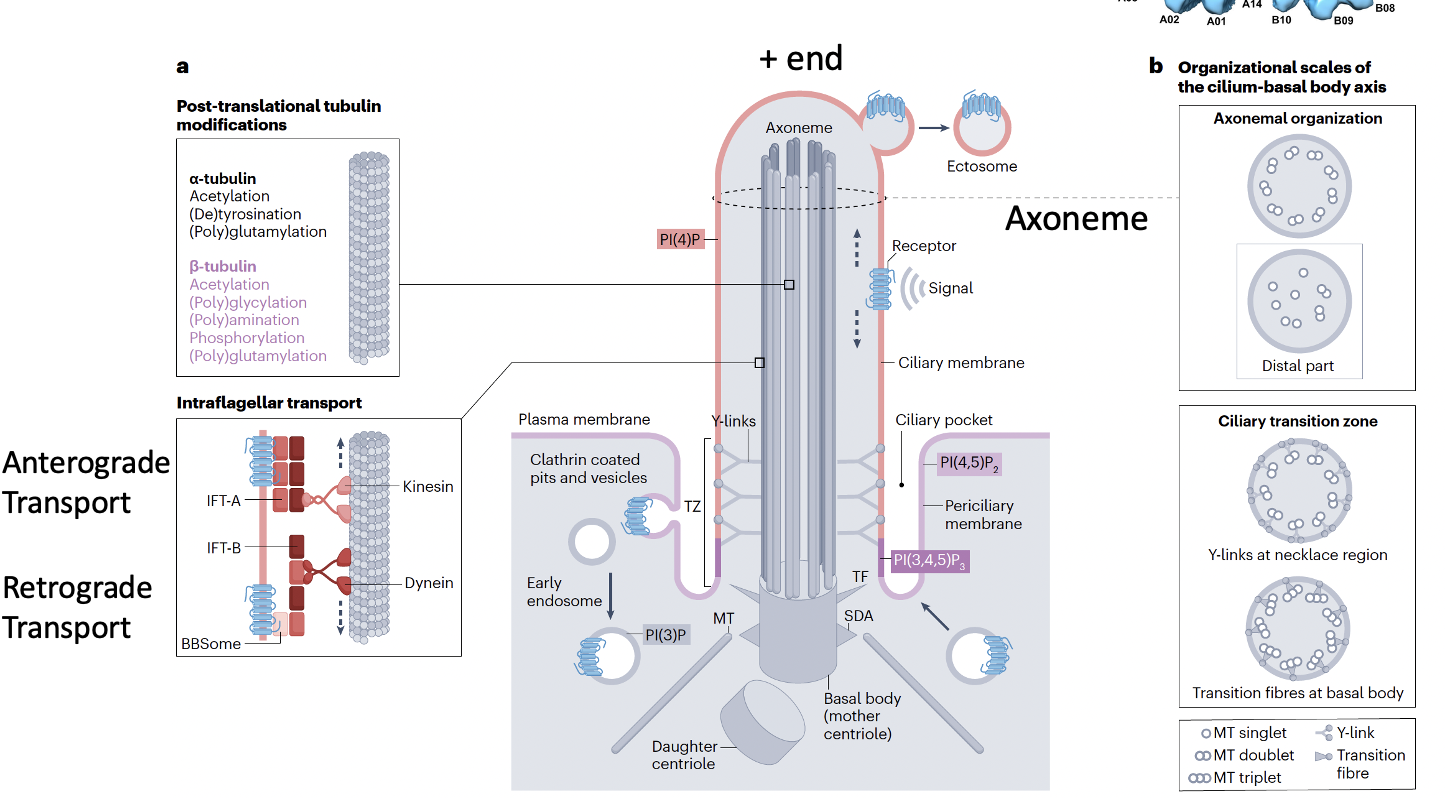
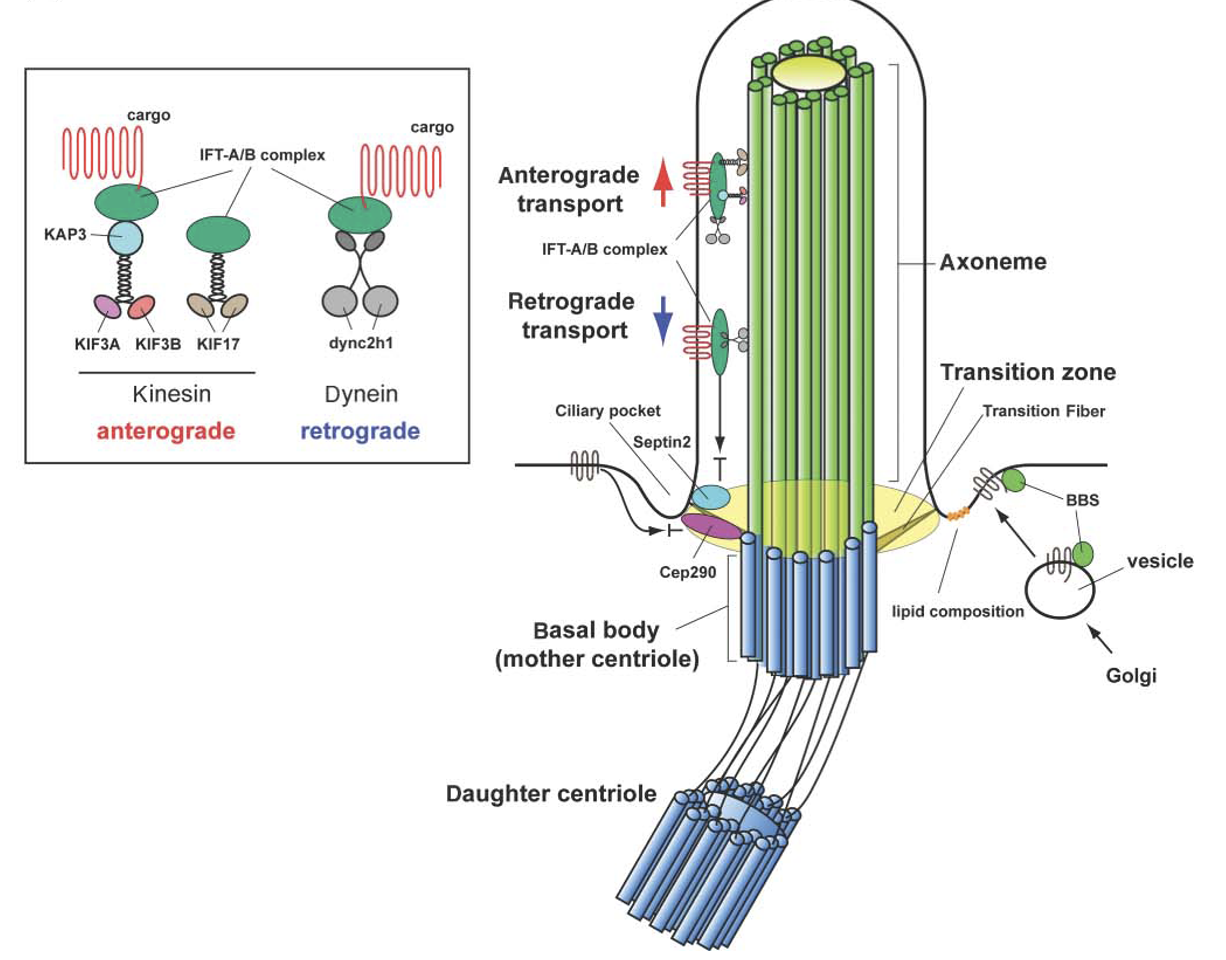
בבסיס ה־Primary Cilia נמצאות שתי צנטריולות, וצנטריולת האם משמשת כ־Basal body שממנו נבנה ה־Cilia. שלד ה־Cilia בנוי ממיקרוטובולים המסודרים באופן מקביל, והמבנה הזה נקרא axoneme.
בחתך רוחבי רואים תשעה זוגות של מיקרוטובולים, doublets, שכל אחד מהם מורכב מ־A-tubule מלא ו־B-tubule חלקי.
בבסיס המבנה נמצא אזור חשוב בשם Transition zone, ובו יש Y-links שמחברים בין האקסונם לממברנה. ה־Transition zone מתפקד כמסננת: הוא קובע אילו חלבונים רשאים להיכנס ל־Cilia ואילו לא.
גם למיקרוטובולים עצמם יש כיווניות: ה־minus end נמצא בבסיס וה־plus end בקצה המרוחק, והם עוברים מודיפיקציות שונות הדרושות לפעילות התקינה של ה־Cilia.
Anterograde and Retrograde Transport
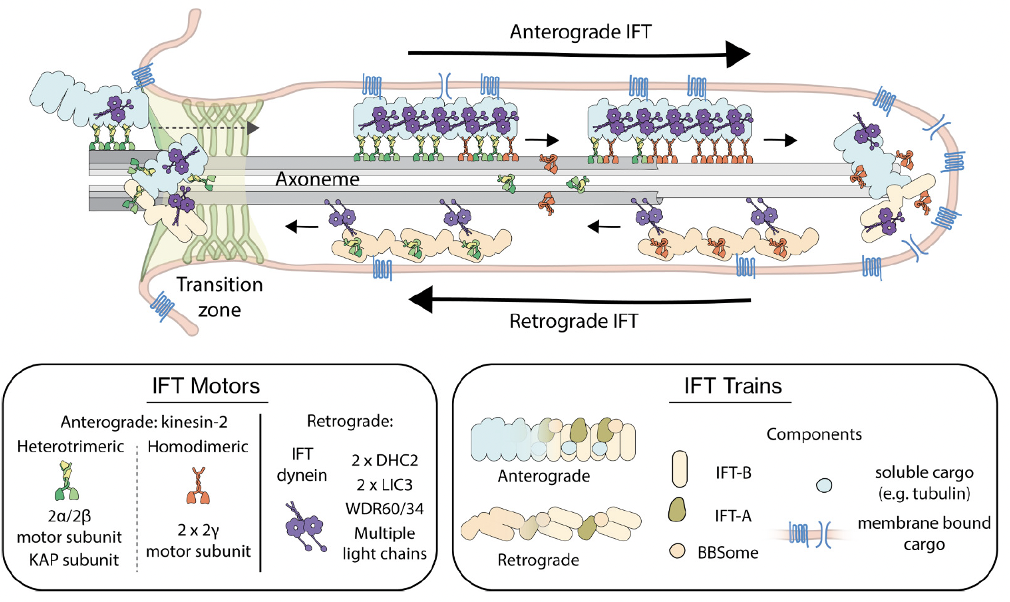
העברת מטענים בתוך ה־Cilia נעשית בעזרת קומפלקסים גדולים בשם IFT-A ו־IFT-B, שפועלים כמו רכבות משא. הם נטענים בחלבונים שונים, כולל חלבונים טרנסממברנליים, ונעים לאורך המיקרוטובולים.
-
Anterograde Transport - תנועה מהבסיס אל הקצה, כלומר לכיוון ה־plus end, מתבצעת בעזרת קִינֵזִין (Kinesin).
-
Retrograde Transport - תנועה מהקצה חזרה לבסיס, מתבצעת בעזרת Dynein אל ה־minus end.
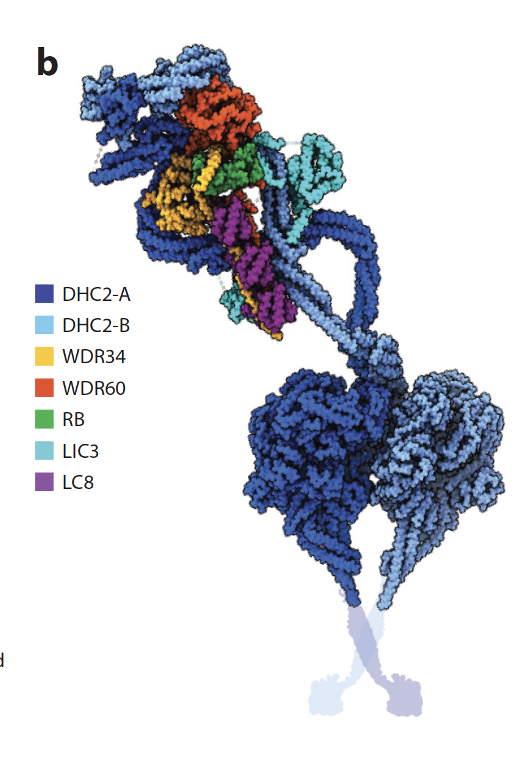
ה־Dynein נישא תחילה במצב לא פעיל על גבי רכבות ה־Anterograde. כשהרכבת מגיעה לקצה הוא עובר שינוי קונפורמציה, נעשה פעיל, ומתחיל את הדרך חזרה. כך נוצר מחזור מתמשך של הבאת מטענים לקצה (החיובי), פריקה שלהם, וארגון מחדש של רכבות החזרה.
אחת הנקודות היפות היא שהמערכת גם מונעת התנגשויות: הקינזין נע על B-tubule, ואילו הדיינין נע על A-tubule.
היפטרות מ־Primary Cilia
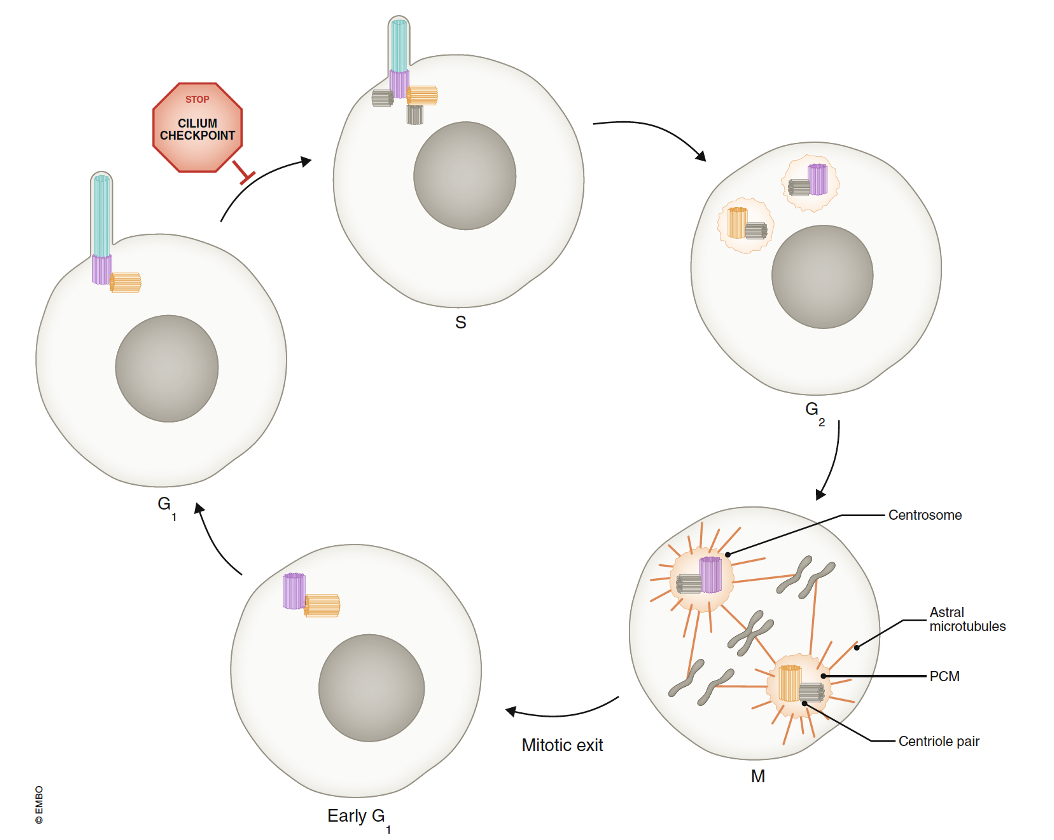
בעיה חשובה: תאים בעובר מתחלקים כל הזמן, אבל כדי להתחלק הם צריכים את הצנטריולות. לכן תא לא יכול גם להחזיק Primary Cilia וגם להיכנס לחלוקה בו זמנית. לפני הכניסה ל־S phase יש למעשה מחסום: התא חייב להיפטר מה־Cilia, ורק אחר כך הוא יכול לשכפל צנטריולות ולהמשיך למיטוזה.
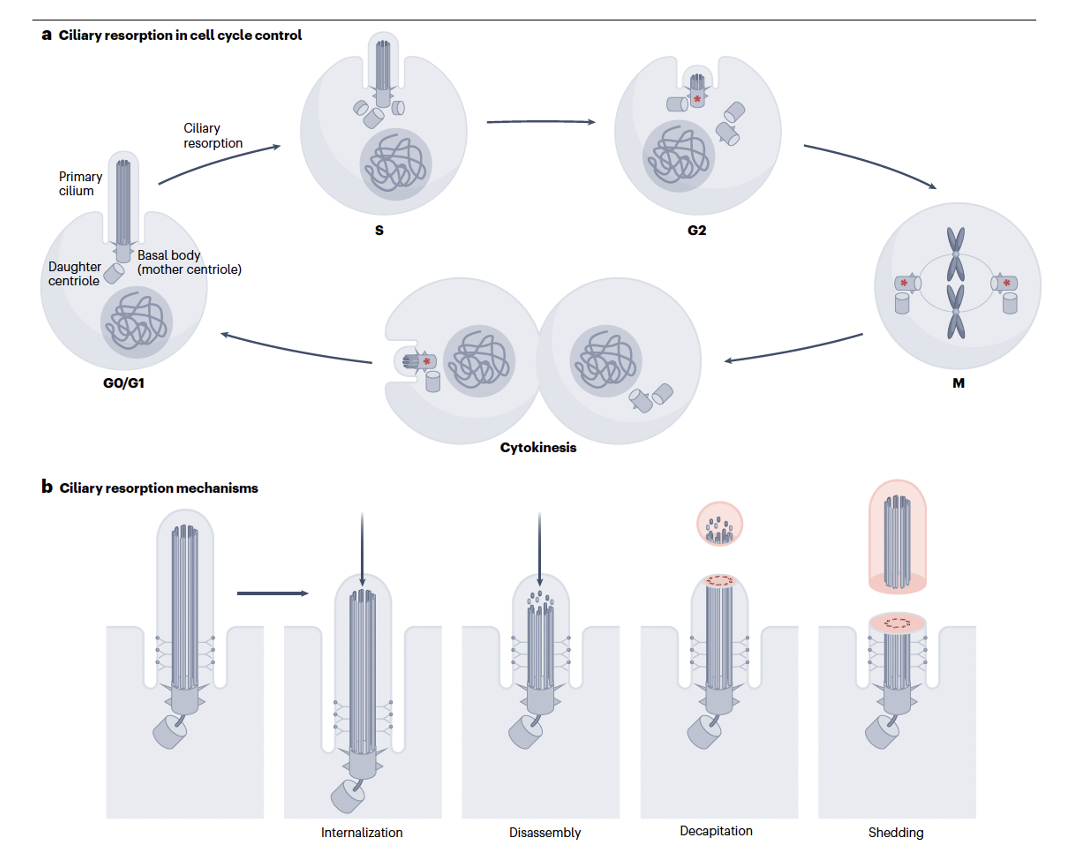
אפשר להיפטר מה־Cilia בכמה דרכים; אפשר להכניס אותו פנימה בהדרגה, אפשר לפרק אותו מן הקצה, ואפשר לבצע Decapitation, כלומר חיתוך של המבנה עד להיעלמותו. לאחר שהתא מסיים להתחלק אפשר לבנות את ה־Cilia מחדש. עצם העובדה שהתא משקיע שוב ושוב כל כך הרבה אנרגיה ביצירה, פירוק ובנייה מחדש שלו מדגישה עד כמה הוא חשוב.
Immotile and Motile Cilia
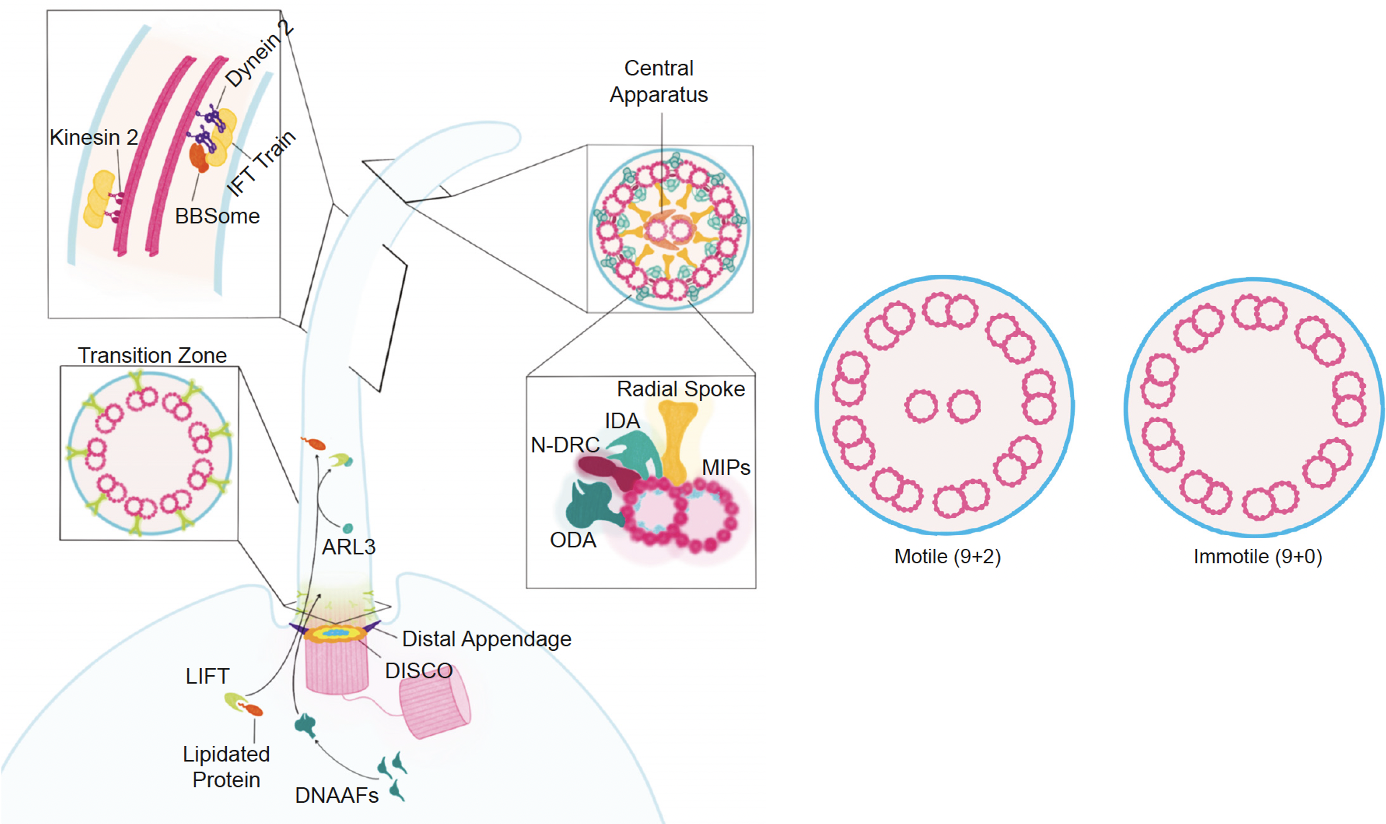
לא כל ה־Cilia זהים.
-
Immobile - ה־Primary Cilia הקלאסי בעל מבנה של 9+0: תשעה doublets בלי זוג מרכזי, ולכן הוא בדרך כלל אינו נייד ומשמש בעיקר לחישה.
-
Mobile - לעומת זאת יש Cilia או flagella מסוג 9+2, בהם יש גם זוג מרכזי של מיקרוטובולים וגם מנועים פנימיים, ולכן הם מסוגלים לנוע. דוגמה מובהקת לכך היא הפלאגלה (שוטון) של תאי זרע.
GPCR
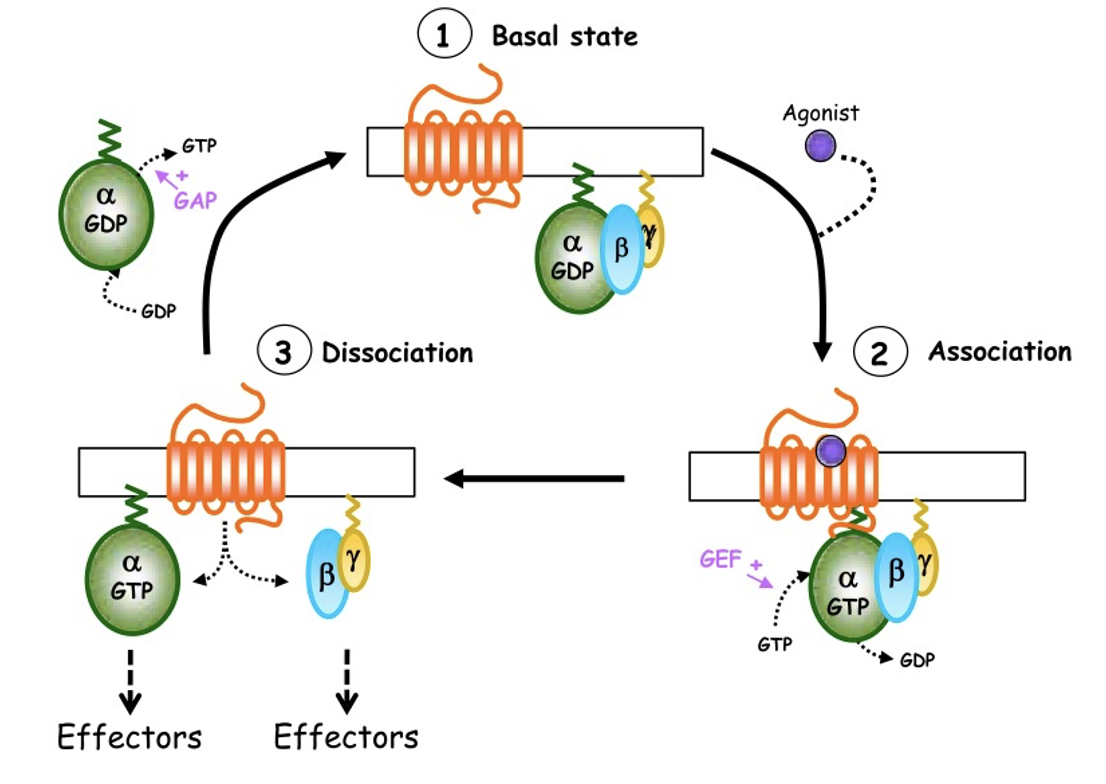
כדי להבין את גרסת היונקים של מסלול Shh צריך לרענן בקצרה את עקרונות GPCR. חלבון G הטרוטרימרי מורכב משלוש תת־יחידות: α, β ו־γ.
במצב הלא פעיל, תת־היחידה α קשורה ל־GDP. כשליגנד נקשר לרצפטור מתרחש שחלוף של GDP ב־GTP (בעזרת GEF), תת־היחידה α נפרדת, והמערכת עוברת למצב פעיל.
כדי לכבות את הסיגנל פועל GAP, שמזרז את פירוק ה־GTP וחזרה למצב הלא פעיל.
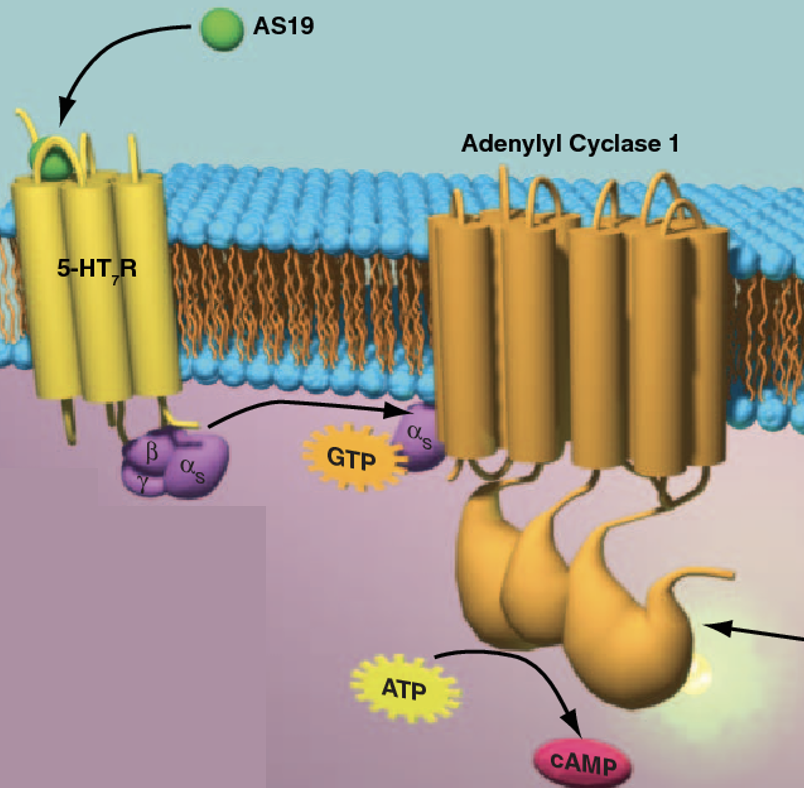
אחד היעדים האפשריים של חלבון G פעיל הוא Adenylyl Cyclase, שמייצר cAMP. המולקולה הזאת מפעילה את PKA.
PKA
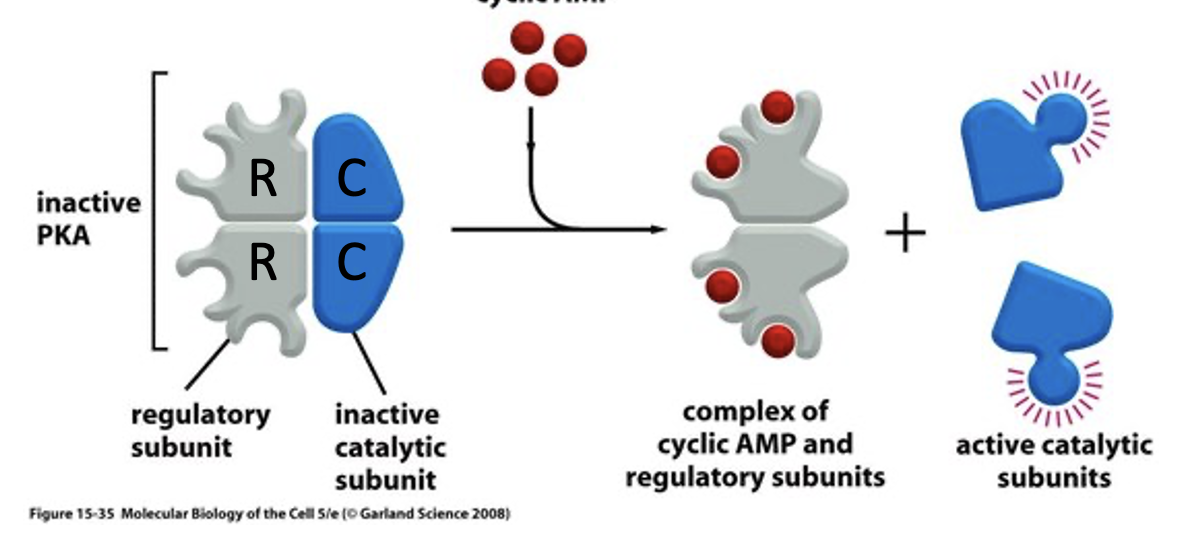
Protein kinase A מורכב משתי תת־יחידות רגולטוריות ושתי תת־יחידות קטליטיות. כאשר cAMP נקשר לתת־היחידות הרגולטוריות, התת־יחידות הקטליטיות משתחררות ונעשות פעילות. זה שלב חשוב, כי בהמשך המסלול של Shh ביונקים יש ל־PKA תפקיד מרכזי בעיבוד של GLI.
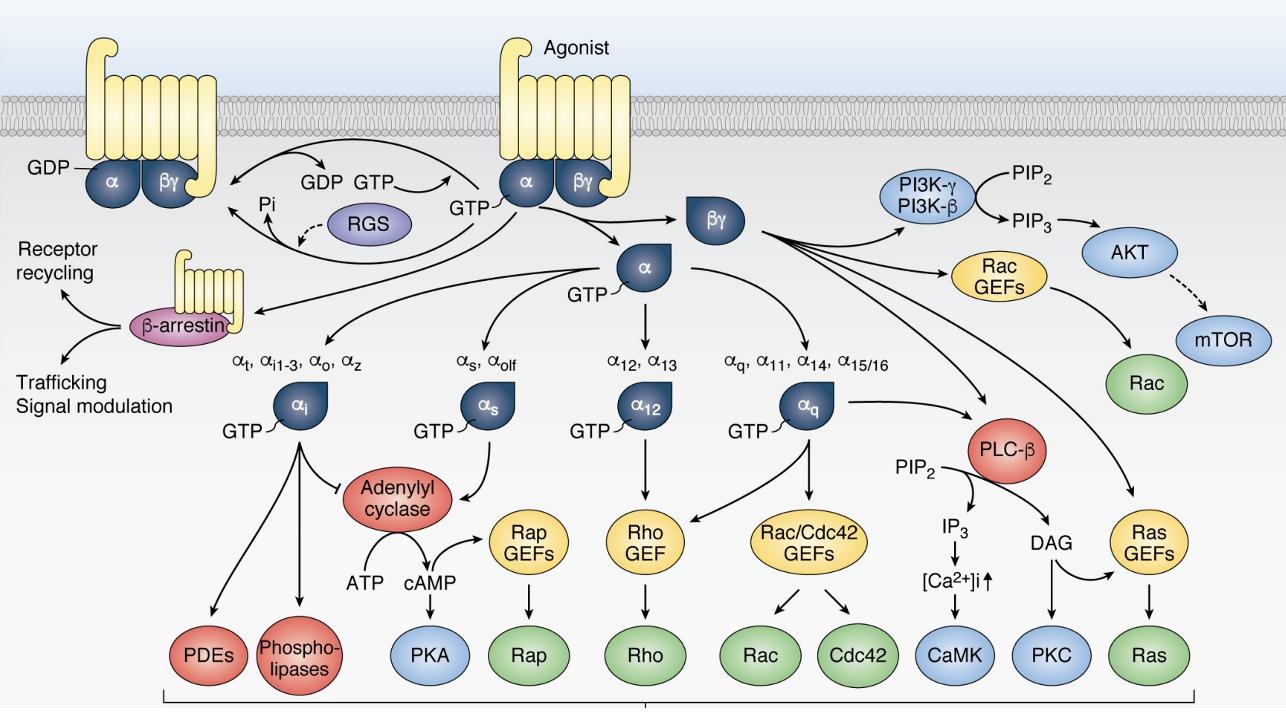
חשוב גם לזכור שאין תת־יחידה α אחת בלבד. יש כמה סוגים, ולכל אחד מהם השפעה אחרת. למשל, αs מפעילה את Adenylyl Cyclase ומעלה את רמות ה־cAMP, בעוד αi מעכבת אותו ומורידה את רמות ה־cAMP.
בנוסף לכך קיימים גם small G proteins, שזקוקים ל־GEF ול־GAP משלהם, ויכולים להפעיל מסלולים אחרים כמו בקרה על ציטוסקלטון. לכן הפעלה של GPCR לא תמיד מובילה לאותה התוצאה; הכול תלוי באיזה סוג של תת־יחידת α מופעלת ובאיזה הקשר תאי המסלול פועל.
Shh ביונקים
ביונקים מסלול Shh תלוי ב־Primary Cilia; אם פוגעים ב־Cilia, המסלול לא יעבוד. זה כבר לא רק העיקרון הכללי של Hedgehog, אלא גרסה ממברנלית-תאית ספציפית ליונקים.
GLI-FL (Full Length)
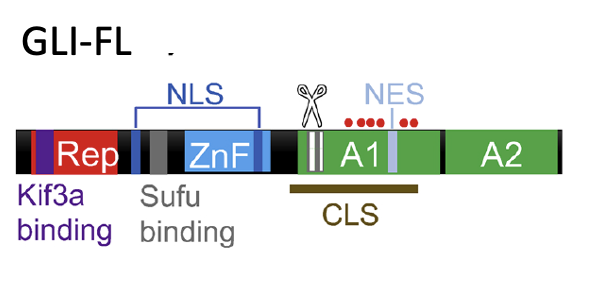
- NES - Nuclear Exit (Export - according to google) Sequence
- NLS - Nuclear Localization Sequence
- Rep - Repressor domain
- A1/2 - Transactivation domains
- CLS - Cilia localization signal
GLI הוא פקטור שעתוק. ל־GLI full length יש גם אותות כניסה ויציאה מהגרעין, גם דומיין רפרסורי וגם דומיינים של אקטיבציה. בנוסף לכך יש לו Cilia localization signal, ולכן הוא מתמקד ב־Primary Cilia.
זאת נקודה מכרעת: ה־Cilia הוא לא רק מקום שבו “עובר משהו”, אלא ממש פלטפורמה שעליה החלבון מעובד ונגזר גורלו.
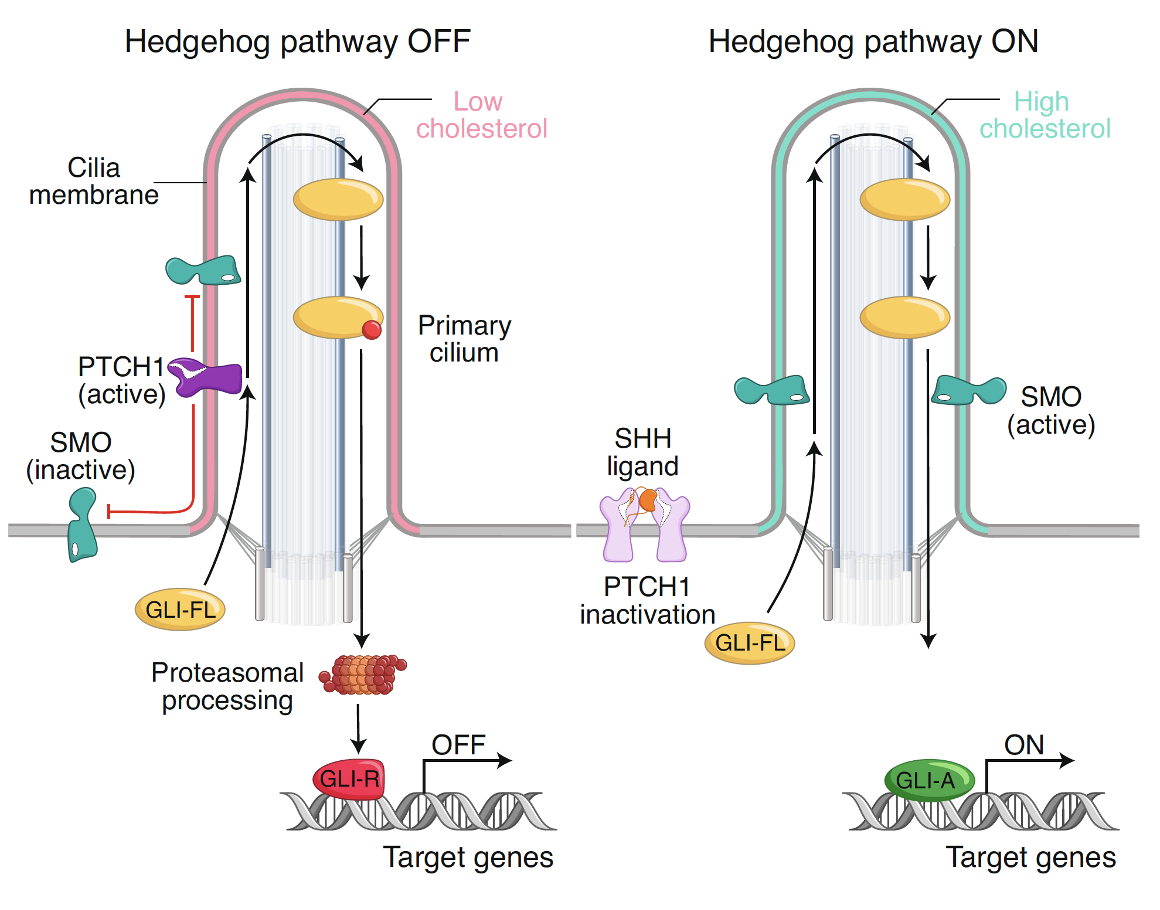
-
כשאין Hedgehog - Patched פעיל, Smoothened אינו פעיל, ו־GLI full length נכנס ל־Cilia אך בסופו של דבר ממשיך למסלול שמוביל ליצירת GliR.
-
כשיש Shh - Patched מעוכב, Smoothened פעיל, ו־GLI full length כבר לא הולך למסלול של רפרסיה אלא נשמר באורך מלא וממשיך לכיוון אקטיבטורי.
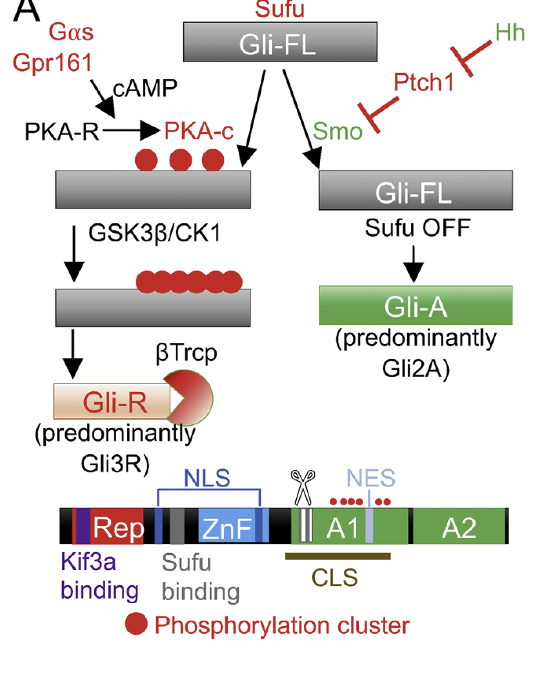
כאן נכנס לתמונה החלבון SUFU. GLI full length קשור ל־SUFU, ובמצב שאין סיגנל הוא עובר פוספורילציה תחילה על ידי PKA, ואחר כך גם על ידי CK1 ו־GSK3β. רצף הפוספורילציות מכוון אותו לעיבוד פרוטאוזומלי חלקי ומוביל ליצירת הצורה הרפרסורית GliR.
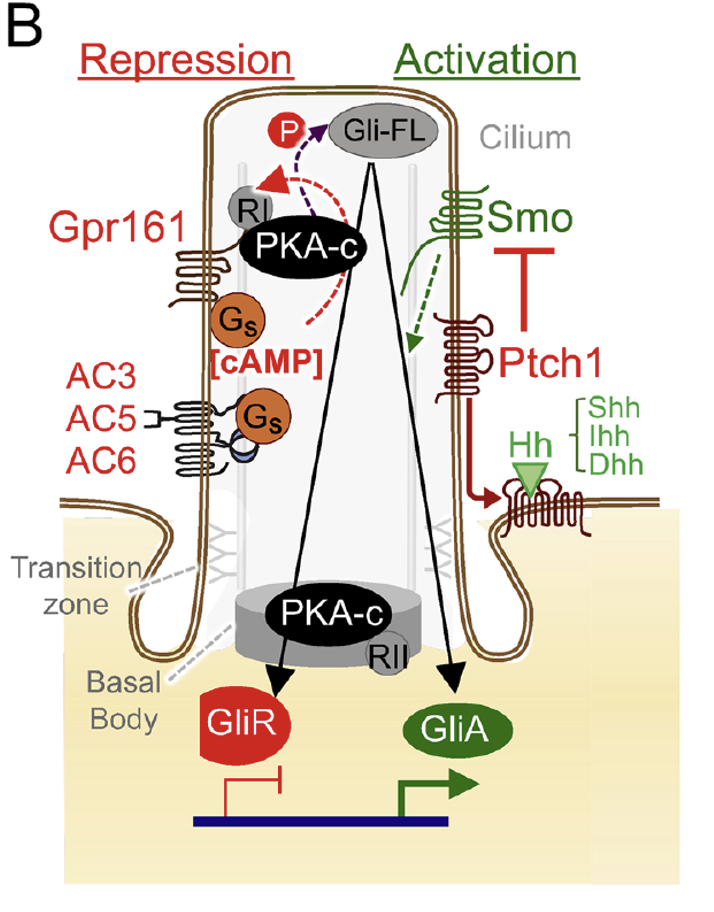
כאשר Shh קיים בסביבה המצב משתנה: Smoothened נעשה פעיל, המסלול שמוביל לפעילות PKA משתנה, ו־GLI לא ממשיך למסלול עיבוד לרפרסור. במקום זאת הוא נשאר בצורתו המלאה, עובר שינוי שמאפשר לו לפעול כאקטיבטור, ויוצא מה־Cilia בתור GliA. המעבר הזה עדיין לא פוענח לחלוטין מבחינה מכנית, אבל ברמת הלוגיקה של המסלול התוצאה ברורה: בלי Shh מתקבל GliR, ועם Shh מתקבל GliA.
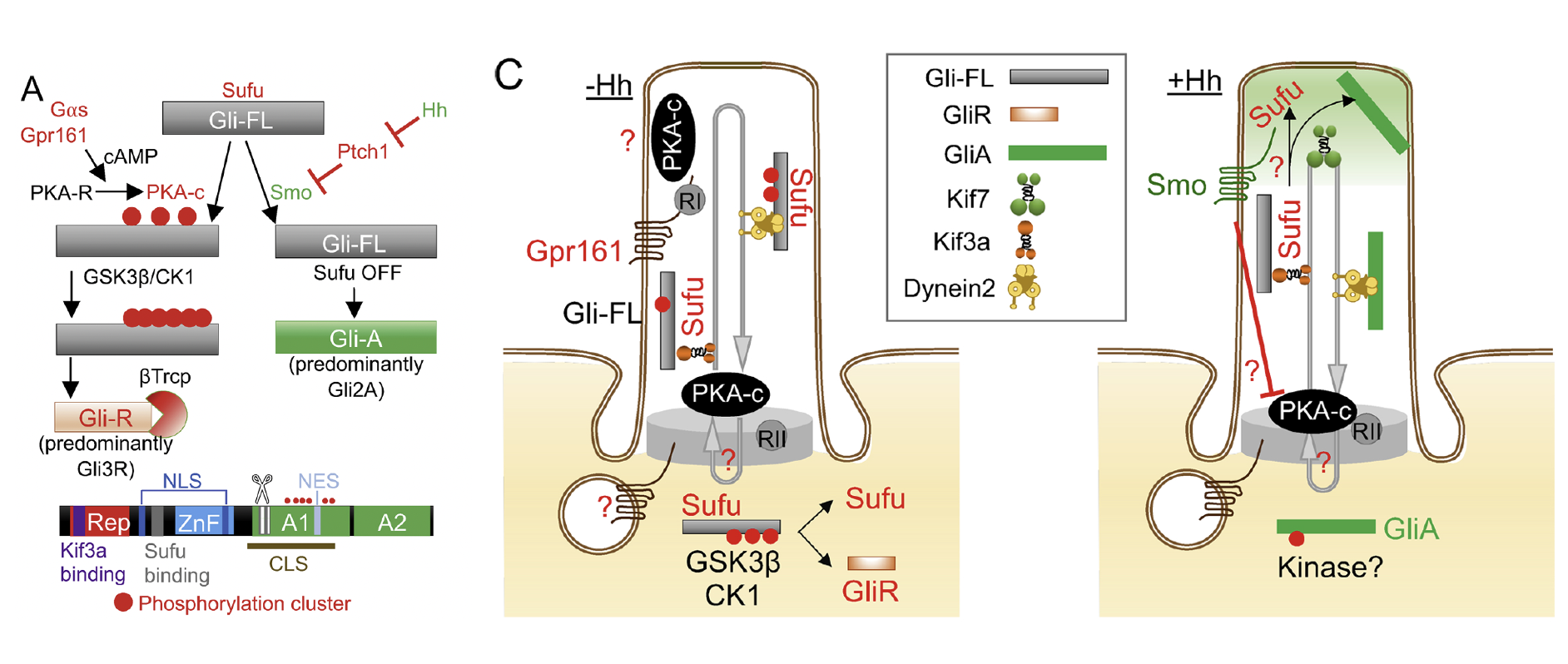
לכן בגרסת היונקים של המסלול אפשר לחשוב על ה־Primary Cilia כמקום שבו מתקבלת ההכרעה: החלבון GLI נכנס לשם בצורה מלאה (full length), והמצב של Smoothened ושל PKA קובע אם הוא ייצא כרפרסור או כאקטיבטור.
Shh Production
כדי להבין את המסלול צריך גם להבין איך הליגנד עצמו נוצר.
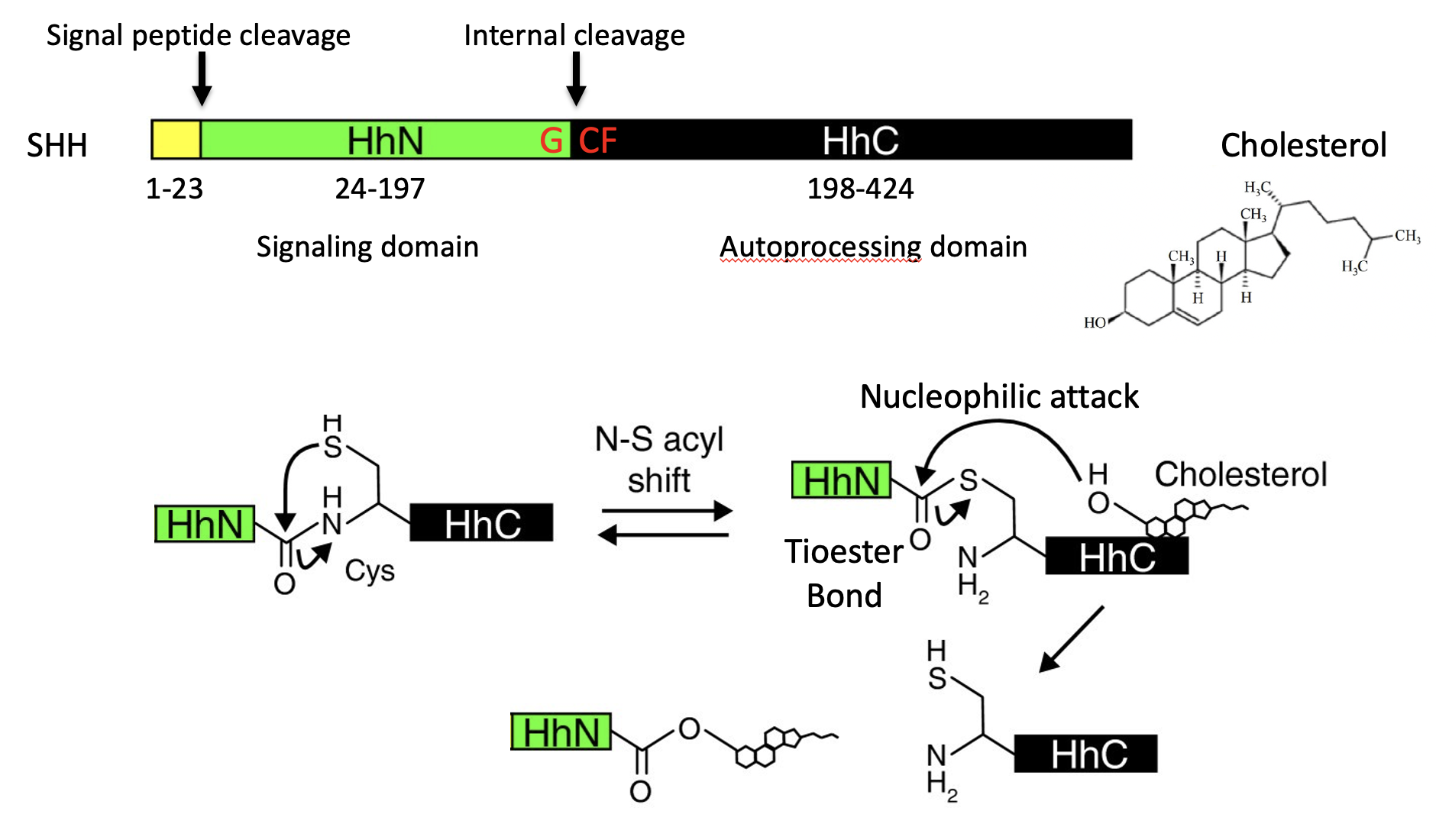
Shh מסונתז ב־ER. בתחילת הדרך יש לו Signal peptide שמכוון אותו להיכנס ל־ER, ולאחר מכן הוא עובר עיבוד פנימי.
לחלבון יש שני חלקים עיקריים:
- החלק האמיני, HhN, שהוא האזור הסיגנלי שעתיד לשמש כליגנד
- החלק הקרבוקסילי, HhC, שהוא Auto-processing domain.
החלק הקרבוקסילי מבצע על החלבון עצמו ביקוע אוטוקטליטי. בתהליך הזה הכולסטרול נקשר קוולנטית אל הקצה הקרבוקסילי של האזור הסיגנלי, והחלק האחורי של החלבון מוסר. התוצאה היא ליגנד פעיל שאליו מחובר כולסטרול.
אוטוקטליזה היא תגובה כימית שבה אחד מתוצרי התגובה משמש גם כזרז לאותה תגובה. במקרה זה התגובה מכונה תגובה אוטוקטליטית. מוכרות צורות רבות של אוטוקטליזה. (ויקיפדיה)
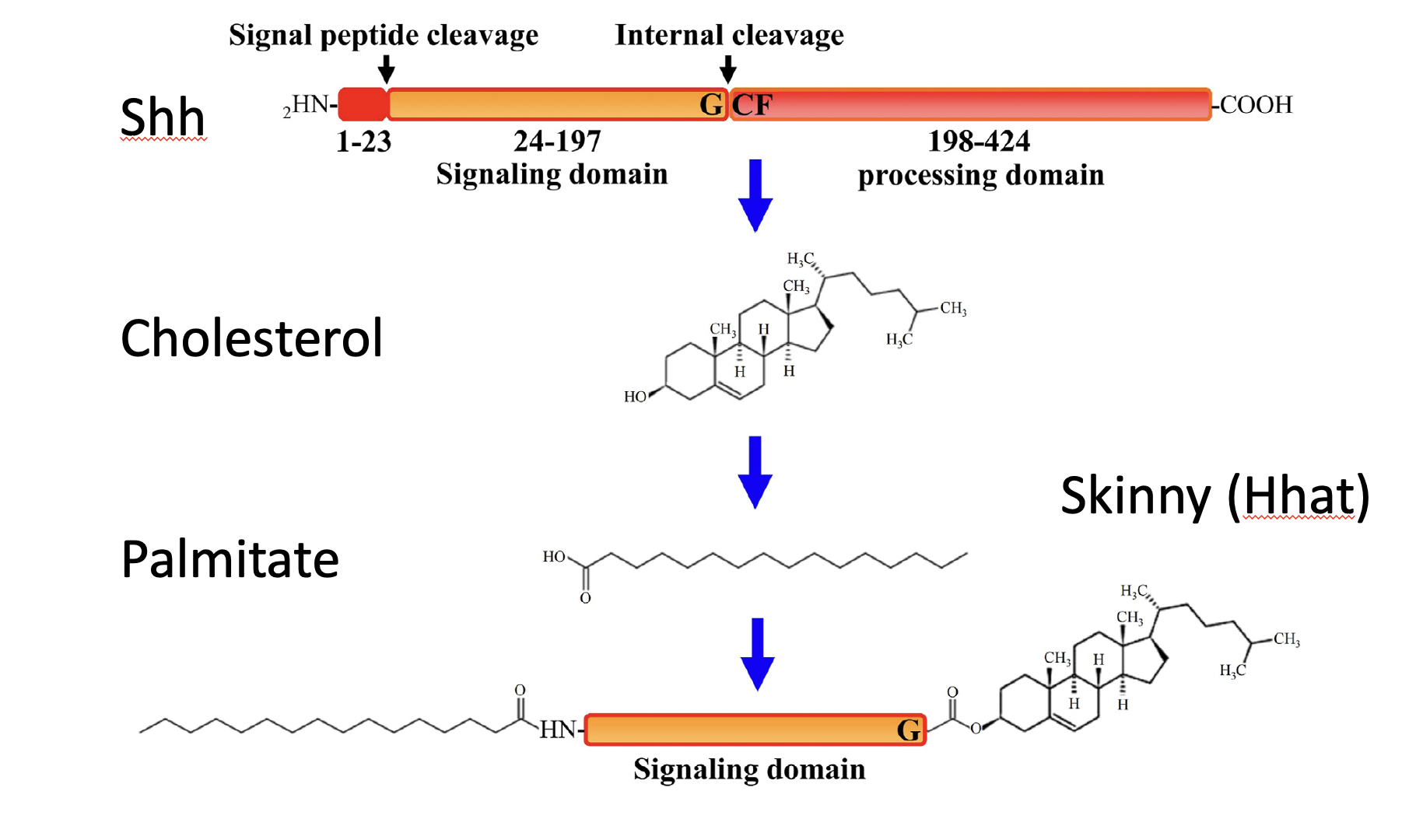
בנוסף לכך מתבצעת גם Palmitoylation של הקצה האמיני. האנזים שמבצע את המודיפיקציה הזאת הוזכר בשם Skinny hedgehog. כך מתקבל ליגנד שיש עליו גם Cholesterol וגם Palmitate. שתי המודיפיקציות הליפידיות האלה מצמידות את Shh לממברנה ומחייבות מנגנון מיוחד כדי לשחרר אותו ולהפיץ אותו.
המבנים הקריסטלוגרפיים של Shh ושל Ptc1
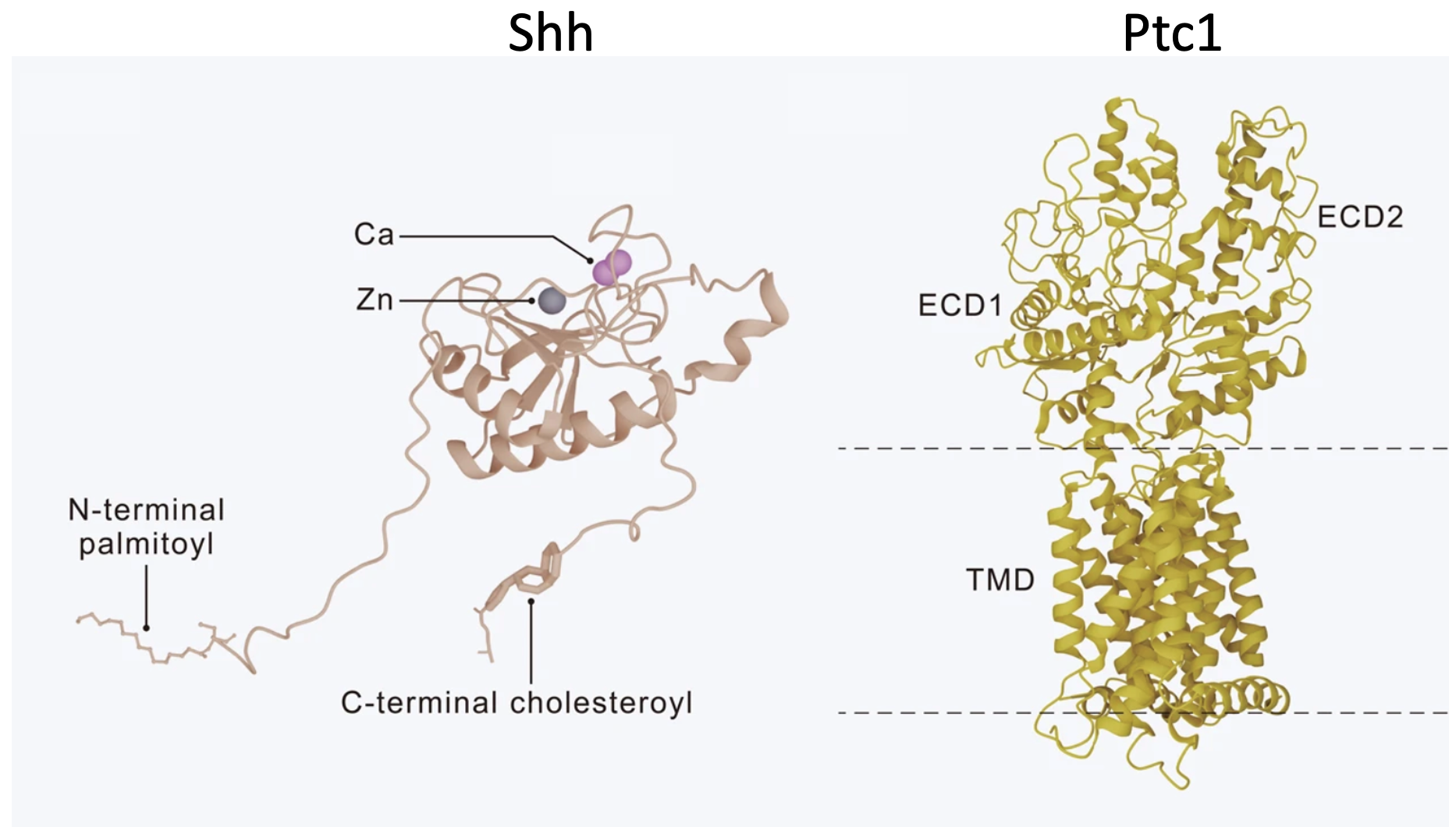
המבנים הקריסטלוגרפיים מאפשרים לראות איך Shh נקשר ל־Patched.
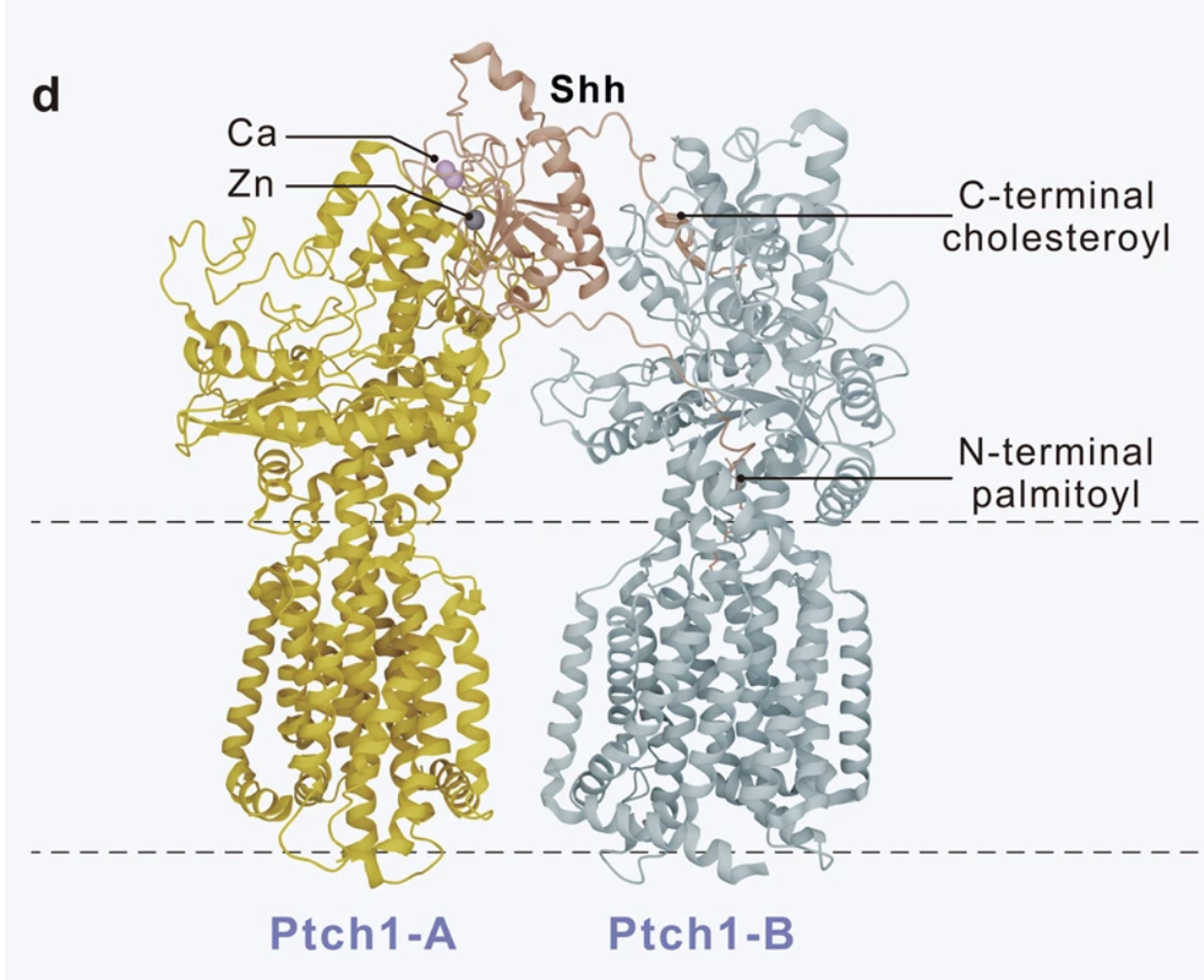
הקומפלקס שנראה כאן הוא 1 Shh : 2 Ptch1: מולקולת Shh אחת נקשרת לשתי מולקולות של Ptch1, אבל לא באותה צורה. אחת מהן יוצרת מגע דרך ממשק חלבוני, ואילו השנייה מקיימת אינטראקציה חזקה עם המודיפיקציות הליפידיות של Shh, כלומר עם ה־Palmitate וה־Cholesterol. בצורה הזאת Shh גם מעכב את פעילות הטרנספורטר של Patched וגם מקדם אינטרנליזציה ודגרדציה שלו.
אינטרנליזציה - הכנסה של משהו פנימה אל תוך התא. המנגנון התאי הוא אנדוציטוזה.
Dispatch
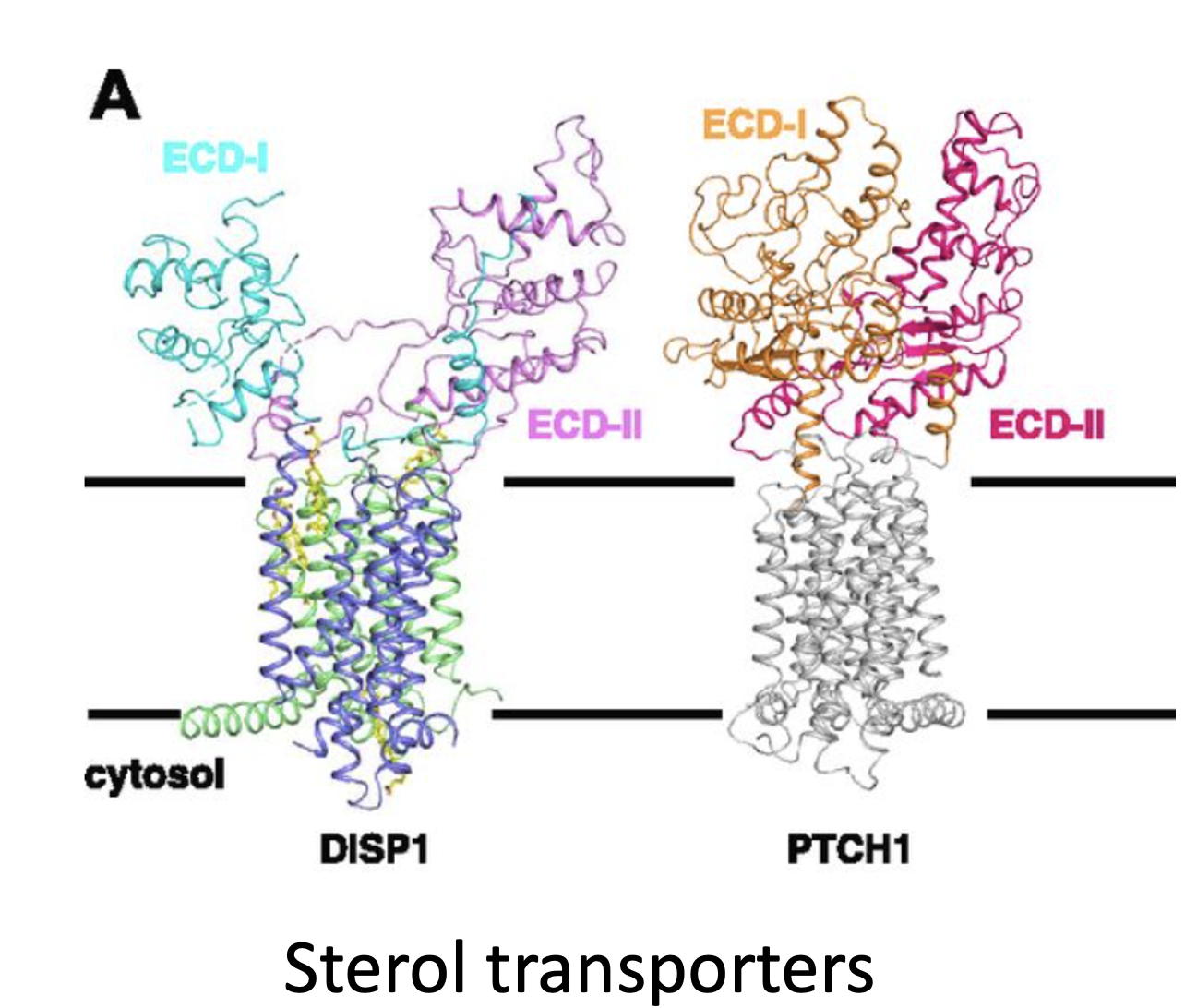
אחרי ש־Shh עובר את המודיפיקציות לעיל עולה השאלה איך הוא בכלל משתחרר מהממברנה. כאן נכנס לתמונה Dispatch (Disp), חלבון ממברנלי נוסף שחוצה את הממברנה 12 פעמים. גם לו יש מאפיינים של טרנספורטר וגם Sterol-sensing domain. הוא זה שמסייע להוציא את Shh מהממברנה.
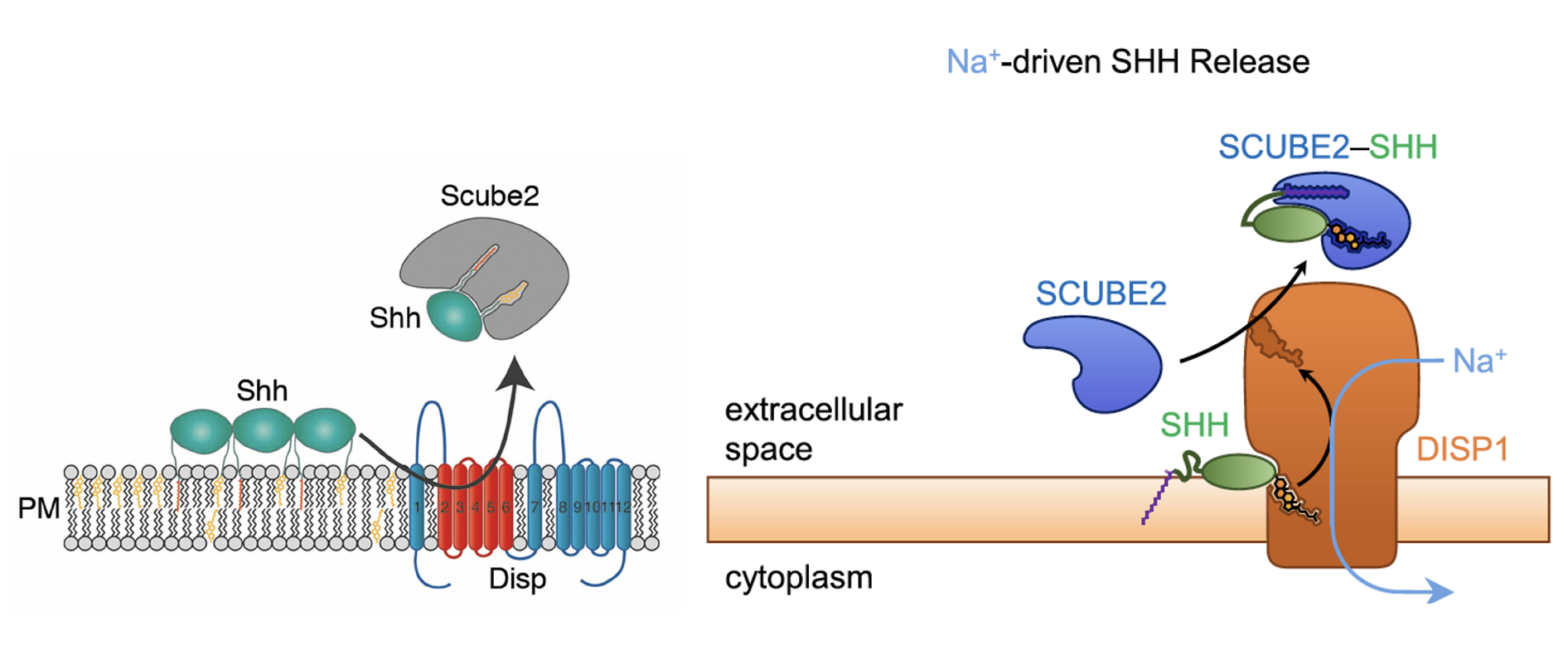
בשלב הבא הליגנד מועבר ל־Scube, חלבון שמסוגל לקשור את המודיפיקציות הליפידיות שלו. כך Shh יכול לעבור למצב מסיס יותר ולהמשיך במרחב החוץ־תאי. בניגוד ל־Patched, שעובד על מפל אשלגן, Dispatch משתמש במפל נתרן.
Cdon/Boc
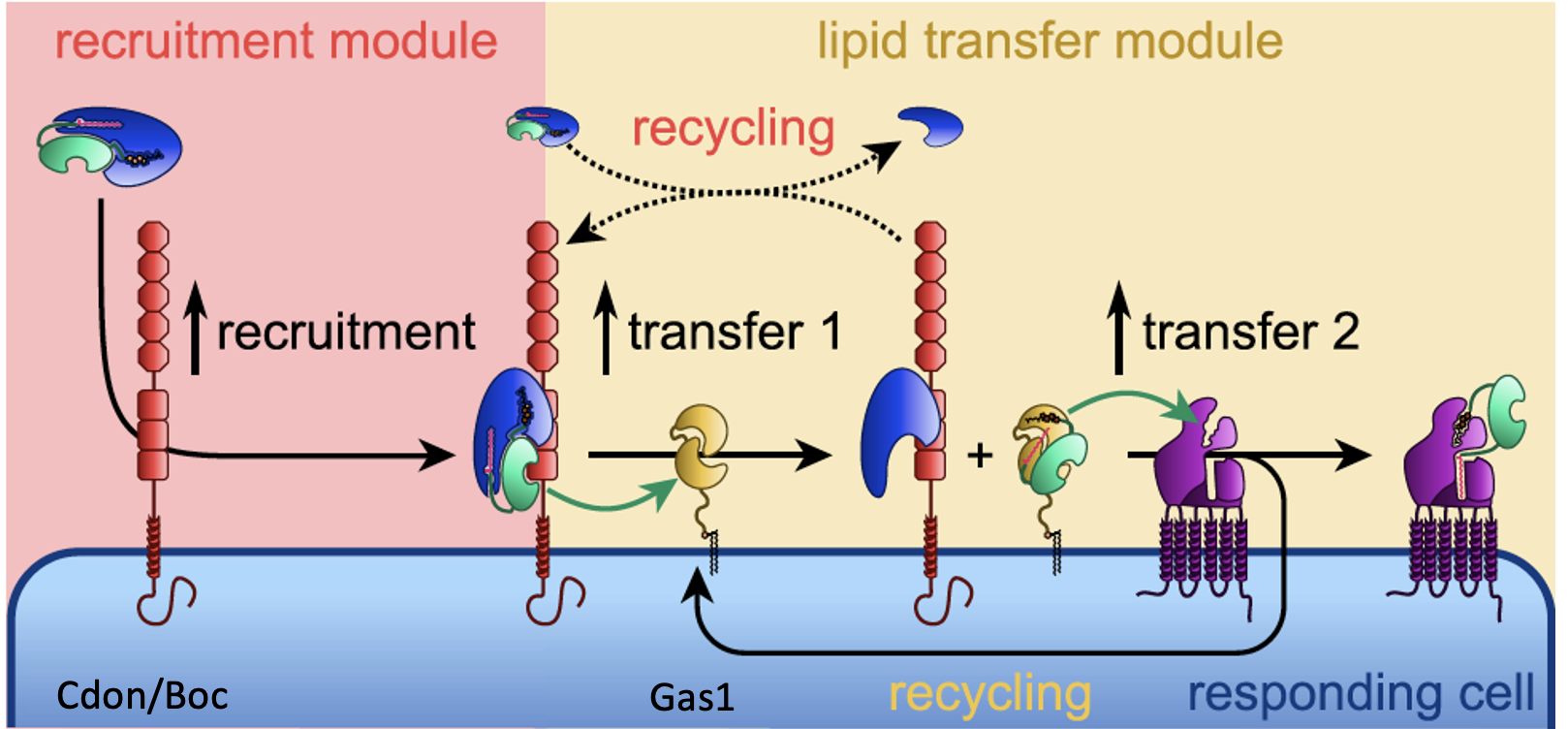
לאחר מכן נכנסים לפעולה גם Cdon ו־Boc, שהם קו־רצפטורים טרנסממברנליים, וגם Gas1, שהוא חלבון הקשור לממברנה בעזרת GPI Anchor. הם מסייעים בהעברה של Shh מן הקומפלקס עם Scube אל Patched שעל תא המטרה. כך מתקבל מסלול מסודר של ייצור, עיבוד, שחרור, נשיאה וקבלה של הליגנד.
ביקוע והפרדה
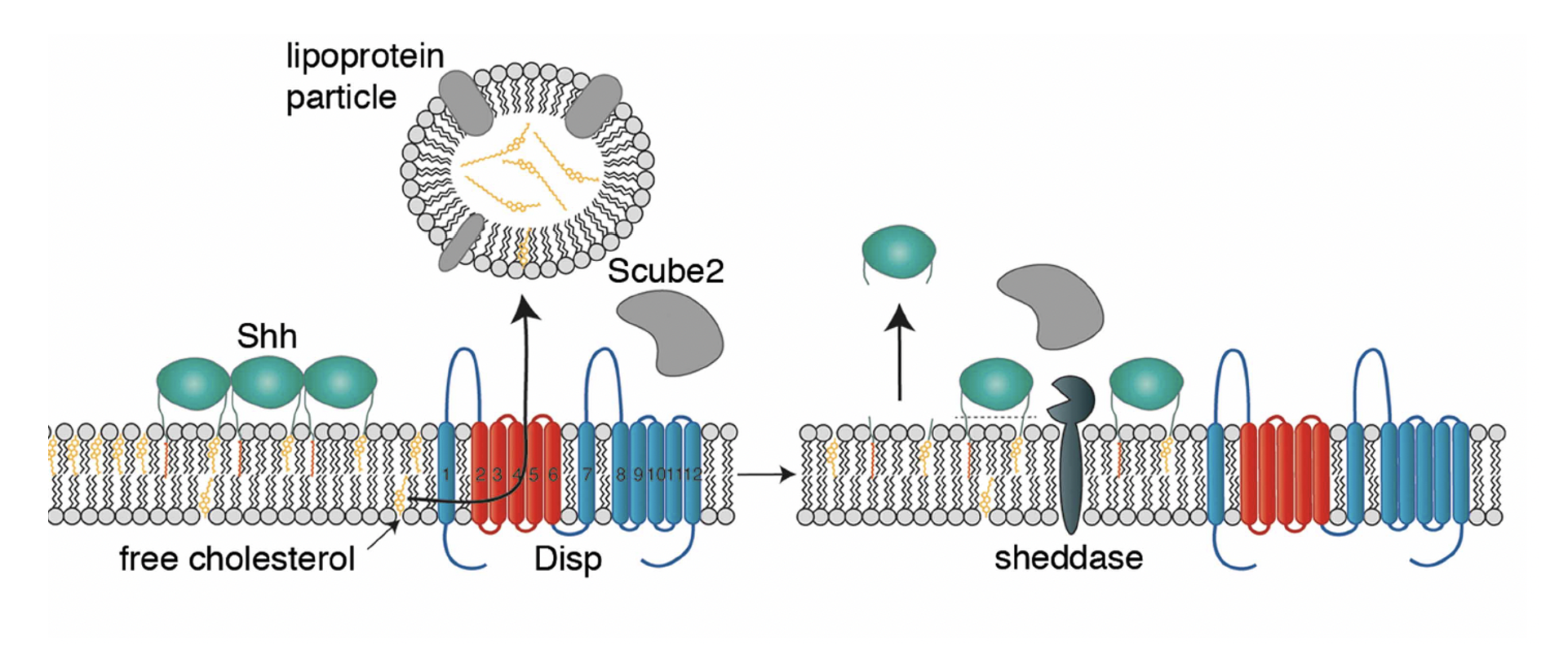
קיים מודל נוסף, לפיו Sheddases מבצעים ביקוע ומשחררים את Shh מהממברנה, כך שהליגנד יכול להשתחרר מבלי לעבור בדיוק את אותו תהליך הובלה, אבל יש לכך מחיר: הצורה המשתחררת חלשה יותר מבחינה תפקודית, ולא יוצרת את הקומפלקס המלא. המודל הזה מוצג כאפשרות שעדיין אינה סגורה לחלוטין.
Notch
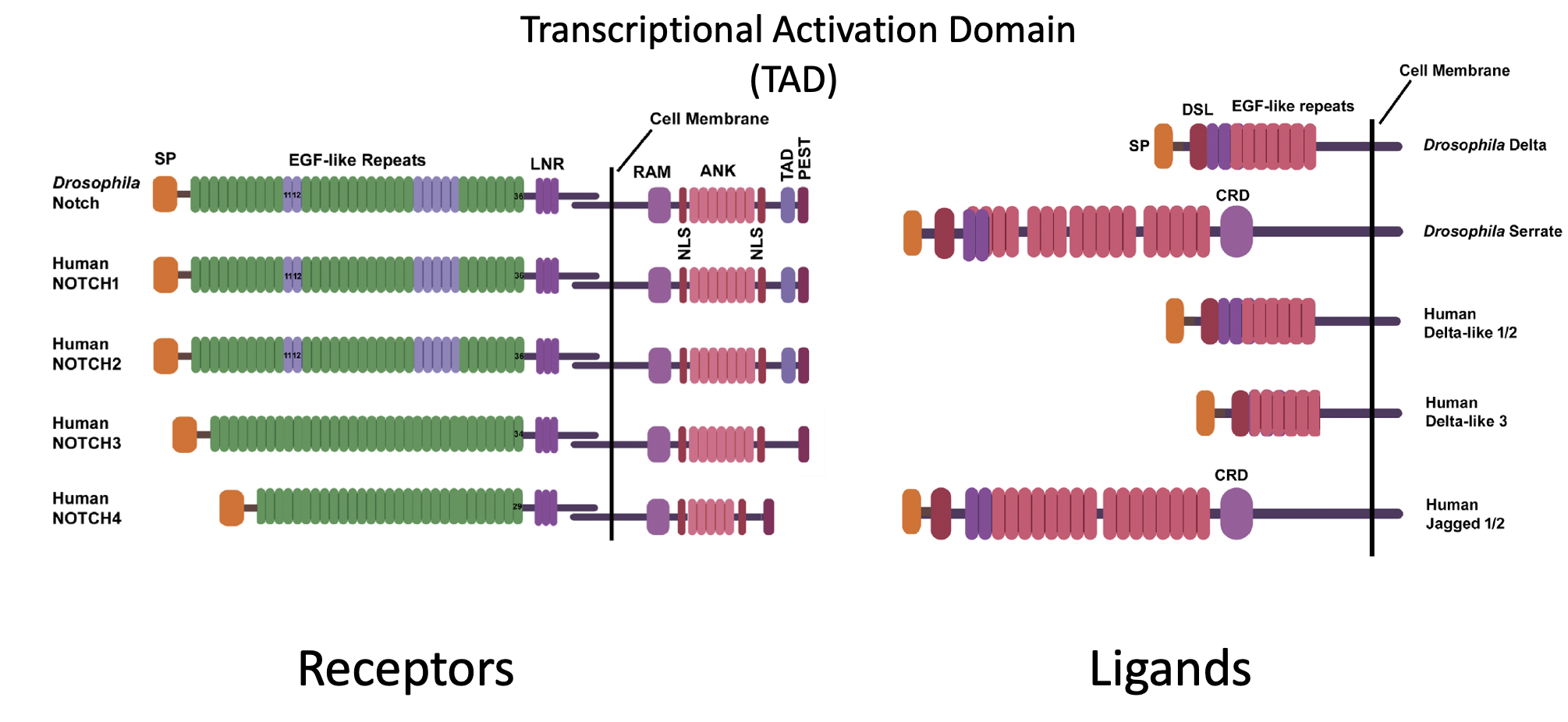
המאפיין הבולט של מסלול Notch הוא שגם הרצפטור וגם הליגנד הם טרנסממברנליים. המשמעות: בניגוד למסלולים שבהם ליגנד מופרש ויכול לעבור לדיפוזיה, כאן התקשורת דורשת מגע ישיר בין תאים סמוכים.
הרצפטורים
הרצפטורים כוללים ביונקים את Notch1-4. בחלק החוץ־תאי שלהם יש מספר רב של EGF-like repeats, והם אחראים על הקישור לליגנד. בנוסף יש דומיינים בשם LNR, שתורמים לכך שהרצפטור לא יופעל בקלות בלי קישור תקין.
Notch מסונתז תחילה כפוליפפטיד אחד, ואז עובר ביקוע לשני פוליפפטידים שנשארים קשורים זה לזה בקשר לא קוולנטי. בחלק התוך־תאי נמצאים בין השאר NLS, שמאפשר כניסה לגרעין, ו־TAD, שמאפשר הפעלת שעתוק.
הליגנדים
גם הליגנדים של Notch הם חלבונים טרנסממברנליים, והם כוללים דומיין חשוב בשם DSL, שמתווך את הקישור לרצפטור.
הפעלה
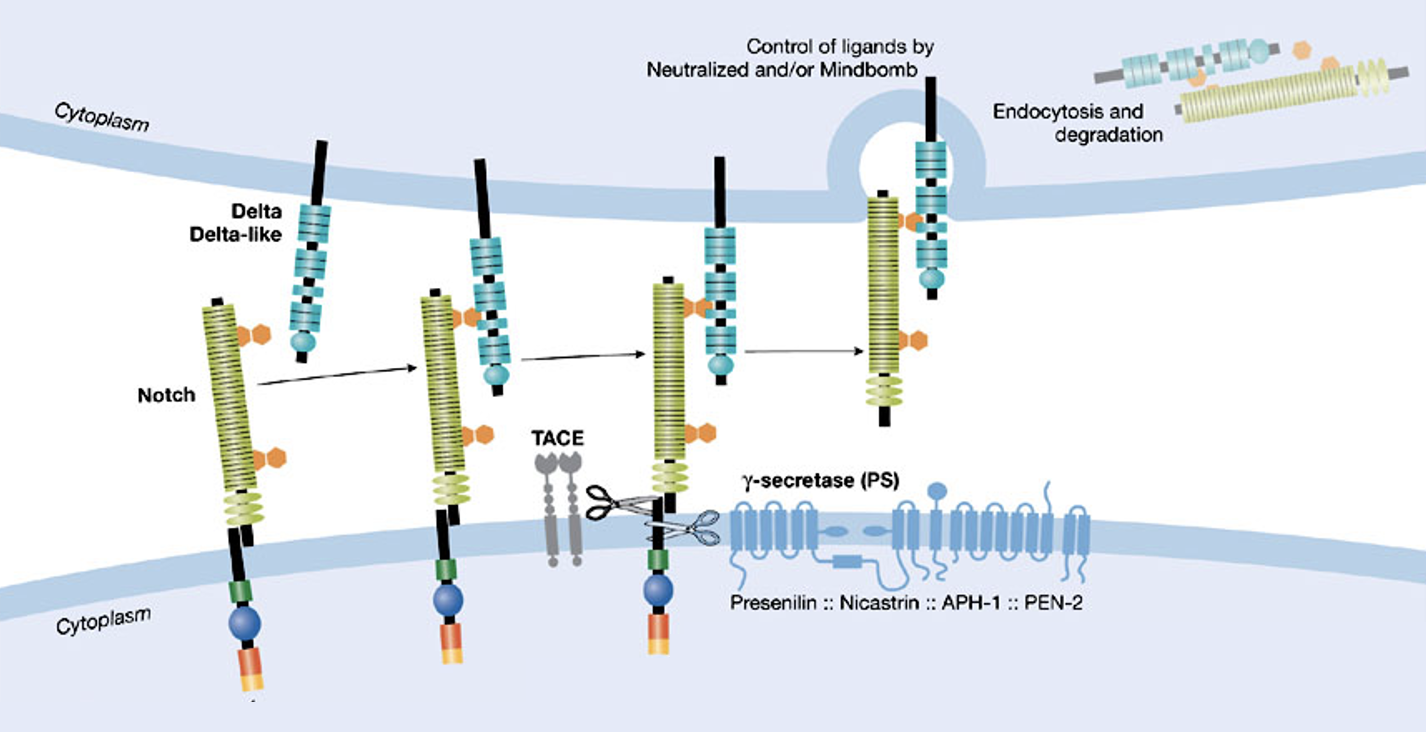
כאשר ליגנד של תא נקשר ל־Notch של תא סמוך, המבנה של הרצפטור משתנה ונחשף אזור קרוב לממברנה, שם פועל פרוטאז בשם TACE, שמבצע את הביקוע הראשון. לאחר מכן פועל γ-secretase, שמבצע ביקוע נוסף בתוך הממברנה עצמה.
כתוצאה מהביקוע השני משתחרר החלק התוך־תאי של Notch, שנקרא NICD — Notch intracellular domain. בגלל שיש לו NLS, הוא נכנס לגרעין.
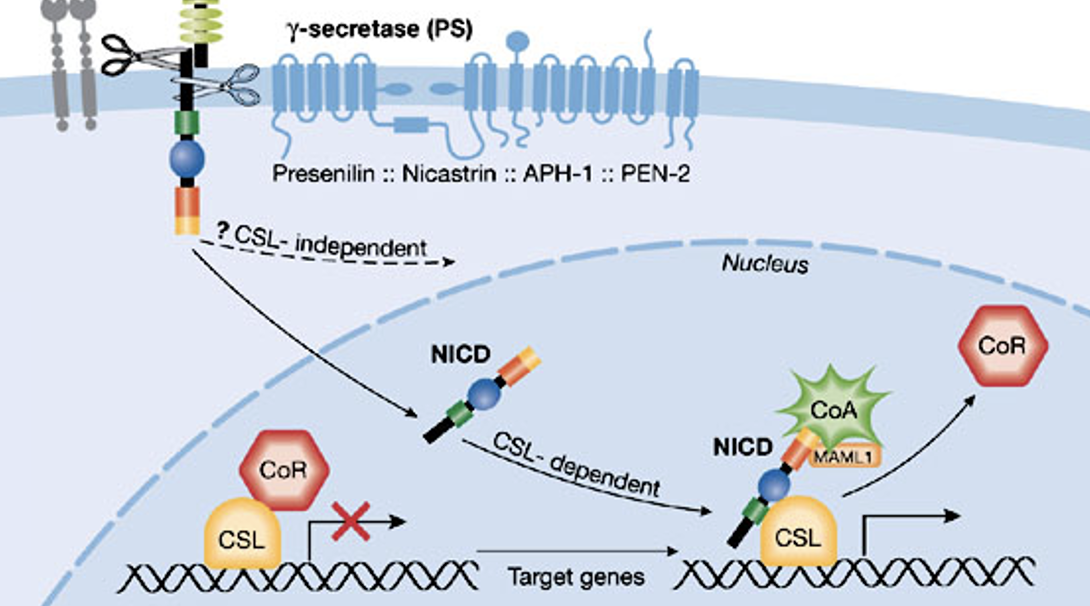
בגרעין, NICD פוגש את פקטור השעתוק CSL. כשאין סיגנל, CSL יושב על הדנ”א יחד עם קו־רפרסורים ומדכא שעתוק. כאשר NICD נכנס, הוא נקשר ל־CSL, מחליף את הקו־רפרסורים במפעילי שעתוק, והמערכת כולה עוברת מרפרסיה לאקטיבציה.
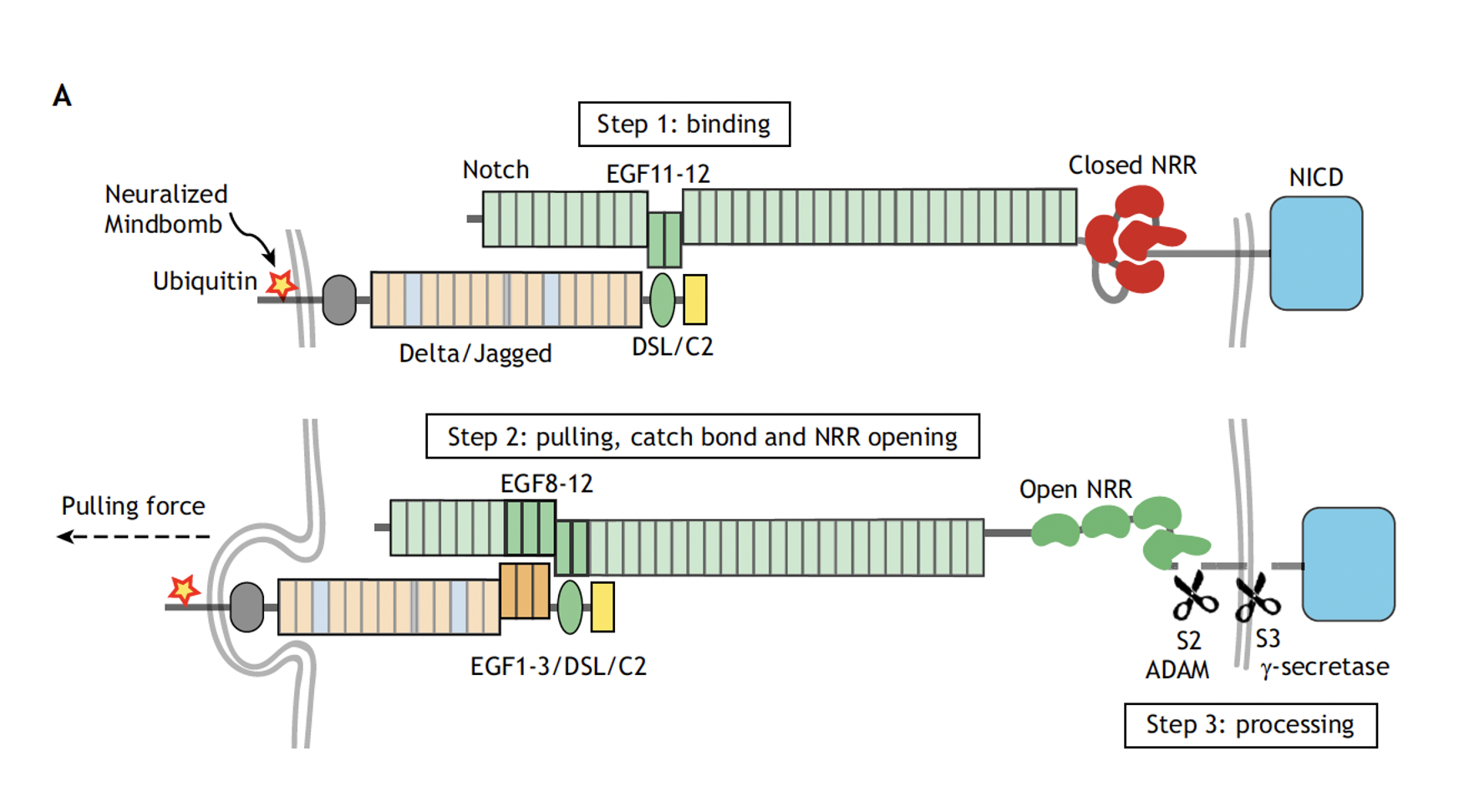
המסלול של Notch נשען על העיקרון הבא: קישור בין שני תאים גורם לסדרה של ביקועים פרוטאוליטיים, משחרר את NICD, וזה נכנס לגרעין ומשנה את מצב השעתוק.
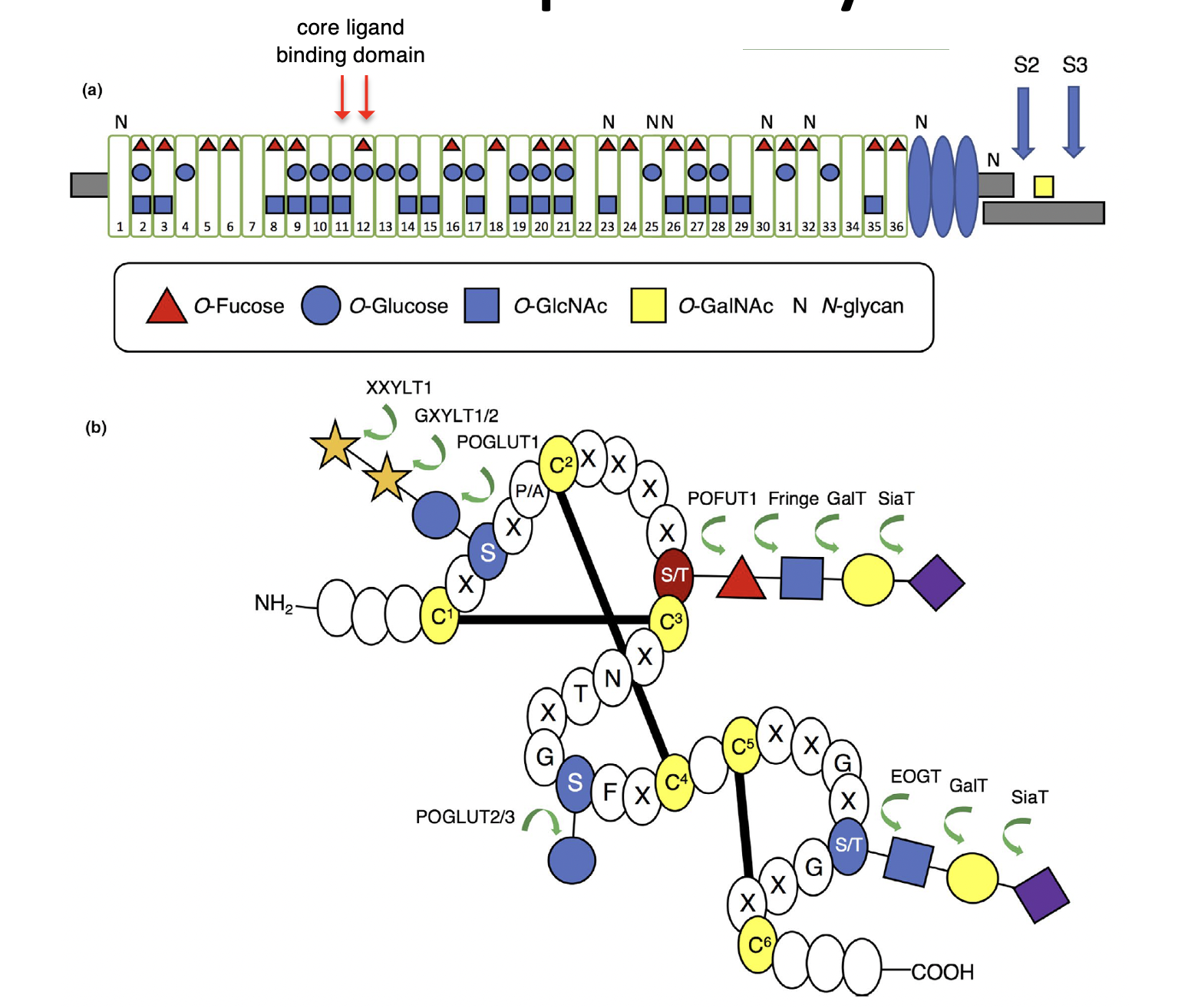
על גבי ה־EGF-like repeats של Notch קיימות גם מודיפיקציות סוכריות. באיור סומן למשל Fucose (המשולש האדום).
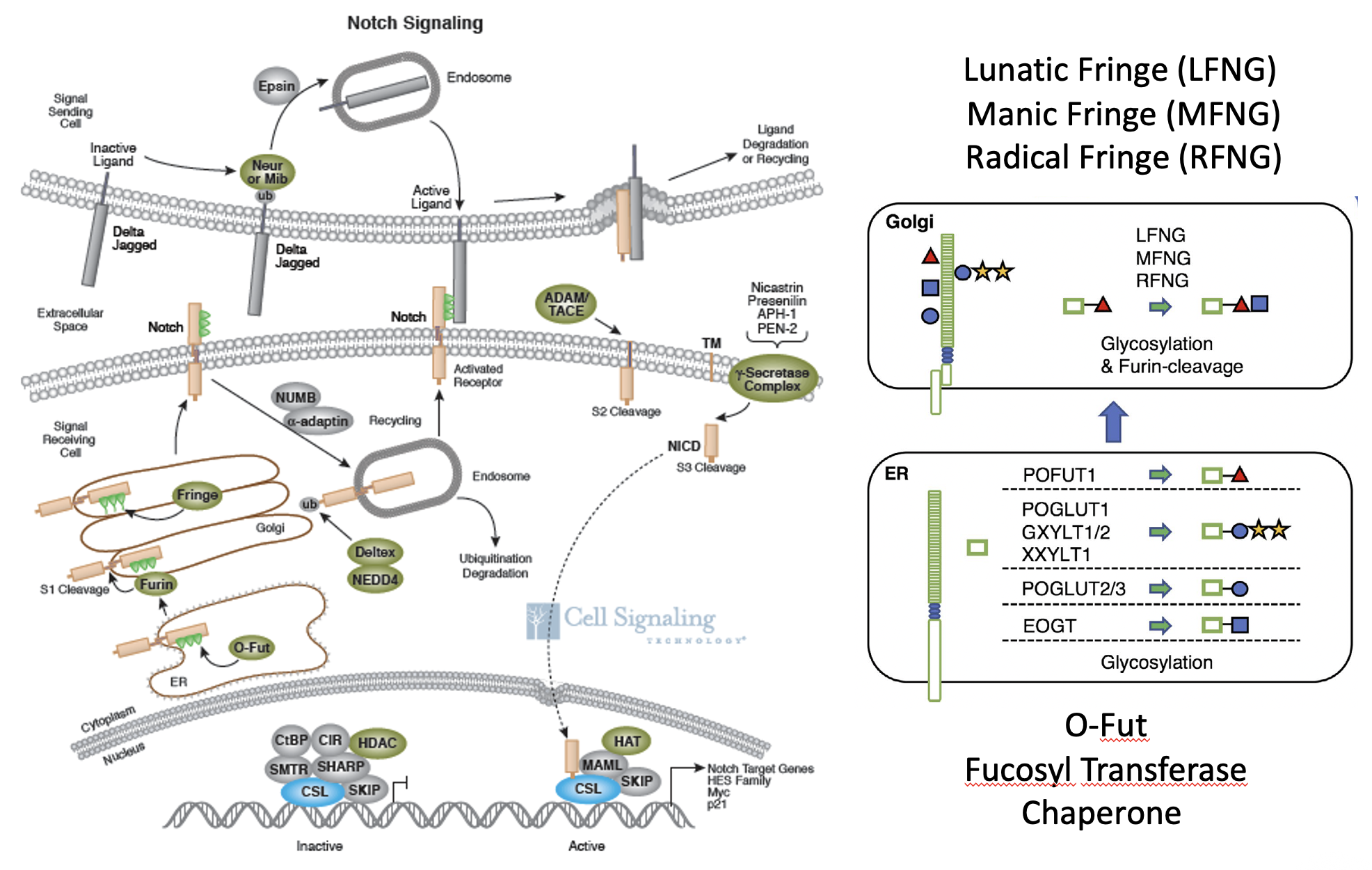
האנזים O-Fut מוסיף את הפוקוז. המודיפיקציות האלה משפיעות על תכונות הקישור של הרצפטור ועל פעילותו.
Feedback Loops
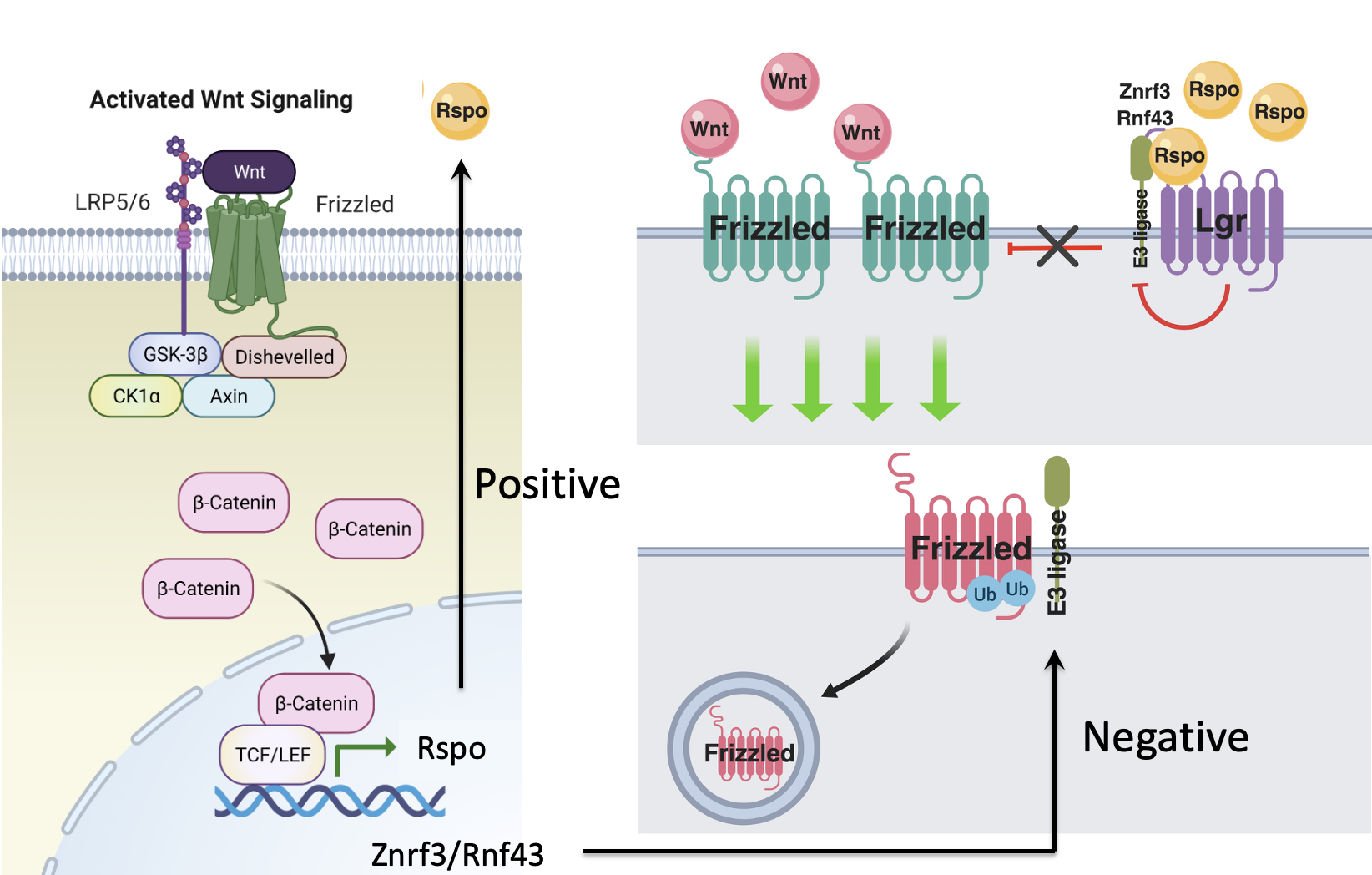
חזרו על רעיון כללי יותר של לולאות משוב במסלולי איתות.
אם גן מטרה של מסלול מסוים מחזק את אותו מסלול, מתקבלת לולאת משוב חיובית. כך למשל, RSPO1 מגביר את הפעילות של Wnt, ובו זמנית Wnt מגביר את הביטוי של RSPO1.
לעומת זאת, אם גן מטרה של המסלול מקודד לחלבון שמחליש אותו, מתקבלת לולאת משוב שלילית.
לכן מסלולי האיתות אינם רק קו ישר של ליגנד, רצפטור ותגובה, אלא מערכות דינמיות שיכולות להגביר את עצמן או לכבות את עצמן בהתאם לגנים שהן מפעילות.
דור פסקל