תוכן העניינים:
- חזרה - תרגיל טופולוגיה
- ארגון הגנום האנושי
- כרומוזומים - אינטרפאזה לעומת מיטוזה
- מבנה הכרומוזום
- בדיקת קריוטיפ - פריסה כרומוזומלית
- כרומוזום חיידקי
- כרומטין
- הנוקלאוזום - יחידת הבסיס של הכרומטין
- וריאנטים של היסטונים
- רגולציה אפיגנטית - ארבע רמות
- פוזיטיב סופרקויל כתוצר לוואי של טרנסקריפציה ורפליקציה
חזרה - תרגיל טופולוגיה
מאיפה מגיעה האנרגיה בחיתוך נוקלאז?
שאלה: האם נוקלאז דורש אנרגיה חיצונית כדי לחתוך את השלד הפוספוסוכרי?
תשובה: לא. הנוקלאז מבצע התקפה נוקלאופילית על קשר פוספוסוכרי, שהוא קשר עתיר אנרגיה. האנרגיה מגיעה מהקשר עצמו, לא ממקור חיצוני.
לעומת זאת, סגירה של ניק על ידי ליגאז כן דורשת אנרגיה מ־ATP - כי אנחנו צריכים להחזיר את האנרגיה לקשר כדי לסגור אותו.
כללים לחישוב - Tw, Wr, Lk
החוק הבסיסי: כל עוד השלד הפוספוסוכרי לא נשבר - Lk לא משתנה. כל שינוי ב־Tw מפוצה מיד ב־Wr ולהפך.
-
מצב רילקס: Wr = 0, לכן Lk = Tw.
-
מולקולה עם ניק (שבר חד־גדילי): Wr = 0 תמיד, לא משנה מה עושים למולקולה - כי השלד לא סגור ולכן לא ניתן להכניס בה מתח פיתולי.
-
מולקולה ליניארית: גם בה Wr = 0 תמיד, כי הקצוות פתוחים.
-
אקסונוקלאז על מולקולה מעגלית: לא קורה שום דבר - אין קצוות פתוחים לחתוך מהם.
-
אנדונוקלאז על מולקולה מעגלית: מאפס את ה־Wr - כל המתח הפיתולי משתחרר, בין אם החיתוך חד־גדילי ובין אם דו־גדילי.
-
חימום מולקולה ליניארית ל־100°: מפריד את הגדילים לשני חד־גדילים - מוריד את ה־Tw, ואין מצב טופולוגי.
-
חימום מולקולה מעגלית: הגדילים לא יכולים להיפרד לגמרי - מקבלים קטננט: שתי לולאות מעגליות משולבות זו בזו עם Lk = 1.
דוגמאות חישוב
שאלה 1
חשב מהו ערך המתח הפיתולי Wr (super coiling) במולקולת DNA מעגלית באורך 800 בסיסים בעלת מספר טופולוגי Lk = 100.
מולקולה של 800 בסיסים, $\text{Lk} = 100$:
\[\begin{aligned} \text{Tw} &= \frac{800}{10} = 80 \\[6pt] \text{Wr} &= \text{Lk} - \text{Tw} = 100 - 80 = \boxed{+20} \end{aligned}\](פוזיטיב סופרקויל).
שאלה 2
מולקולה מעגלית, $1{,}000$ זוגות בסיסים, מצב רילקס:
\[\begin{aligned} \text{Tw} &= 100 \\ \text{Wr} &= 0 \\ \text{Lk} &= 100 \\ \end{aligned}\]שאלה 3
מולקולת DNA מעגלית באורך 1000 בסיסים נמצאת במצב רילקס. כתוצאה ממעבר של RNA polymerase נפתחו 5 סיבובים הליקליים ב DNA (ללא שבירה). מה יהיו ערכי Tw, Wr ו Lk?
הפעלנו RNA פולימראז שפתח חמישה סיבובים הליקליים:
-
השלד לא נשבר, לכן $\text{Lk}$ נשמר:
\[\text{Lk} = 100\] -
$\text{Tw}$ ירד - הפולימראז פתח חמישה סיבובים הליקליים, לכן $\text{Tw}$ החדש הוא:
\[\text{Tw} = 100 - 5 = 95\] -
$\text{Wr}$ עלה - כדי לפצות על הירידה ב־Tw, ה־Wr חייב לעלות ב־5 סיבובים:
\[\text{Wr} = 100 - 95 = \boxed{+5}\]
(פוזיטיב סופרקויל)
שאלה 4
מולקולה של $10{,}000$ זוגות בסיסים, $\text{Wr} = -500$:
\[\begin{aligned} \text{Tw} &= 1{,}000 \\ \text{Wr} &= -500 \\ \text{Lk} &= 500 \\ \end{aligned}\]הפעלנו אנזים שהוסיף $\text{Lk} = +100$, לכן $\text{Lk}$ החדש הוא $600$.
$\text{Tw}$ נשמר: $1{,}000$, ולכן $\text{Wr}$ החדש הוא $600 - 1{,}000 = -400$.
על הסימן בחישוב: $\text{Wr}$ שלילי פירושו נגטיב סופרקויל (סיבוב שמאלי). כשמוסיפים סיבובים חיוביים למולקולה עם $\text{Wr}$ שלילי, עושים אלגברה רגילה: $-500 + 100 = -400$.
שאלות נוספות
אנזים מסוג אנדונוקלאז הוסף למולקולות DNA מעגלית באורך 300 בסיסים המכילה מתח פיתולי חיובי Wr=+30. מהו ערך ה wr לאחר החיתוך?
- Wr = 0 כי החיתוך שחרר את המתח הפיתולי
אנזים מסוג אקסונוקלאז הוסף למולקולת DNA מעגלית באורך 300 בסיסים המכילה מתח פיתולי Wr=-25. מהו ערך ה Wr לאחר החיתוך?
- Wr = -25 כי החיתוך לא שחרר את המתח הפיתולי, הוא רק קיצר את המולקולה.
מולקולת DNA מעגלית באורך 1000 בסיסים הופקה מחיידק ונבדקה באלקטרופזה בג׳ל. כמה מולקולות בעלות מוביליות שונה סביר שנראה בג׳ל?
- סביר שנראה שני בנדים: אחד של מולקולות במצב סופרקויל (המצב הטבעי בתא), ובנד נוסף של מולקולות במצב רילקס (שספגו ניקים בתהליך ההפקה).
הערה: במצב התיאורטי כל המולקולות נמצאות במצב סופרקויל, אבל בפועל במהלך ההפקה הן עלולות לספוג ניקים ולהשתחרר מהמתח הפיתולי, ולכן נראה גם בנד של מולקולות רילקס.
ארגון הגנום האנושי
כרומוזומים
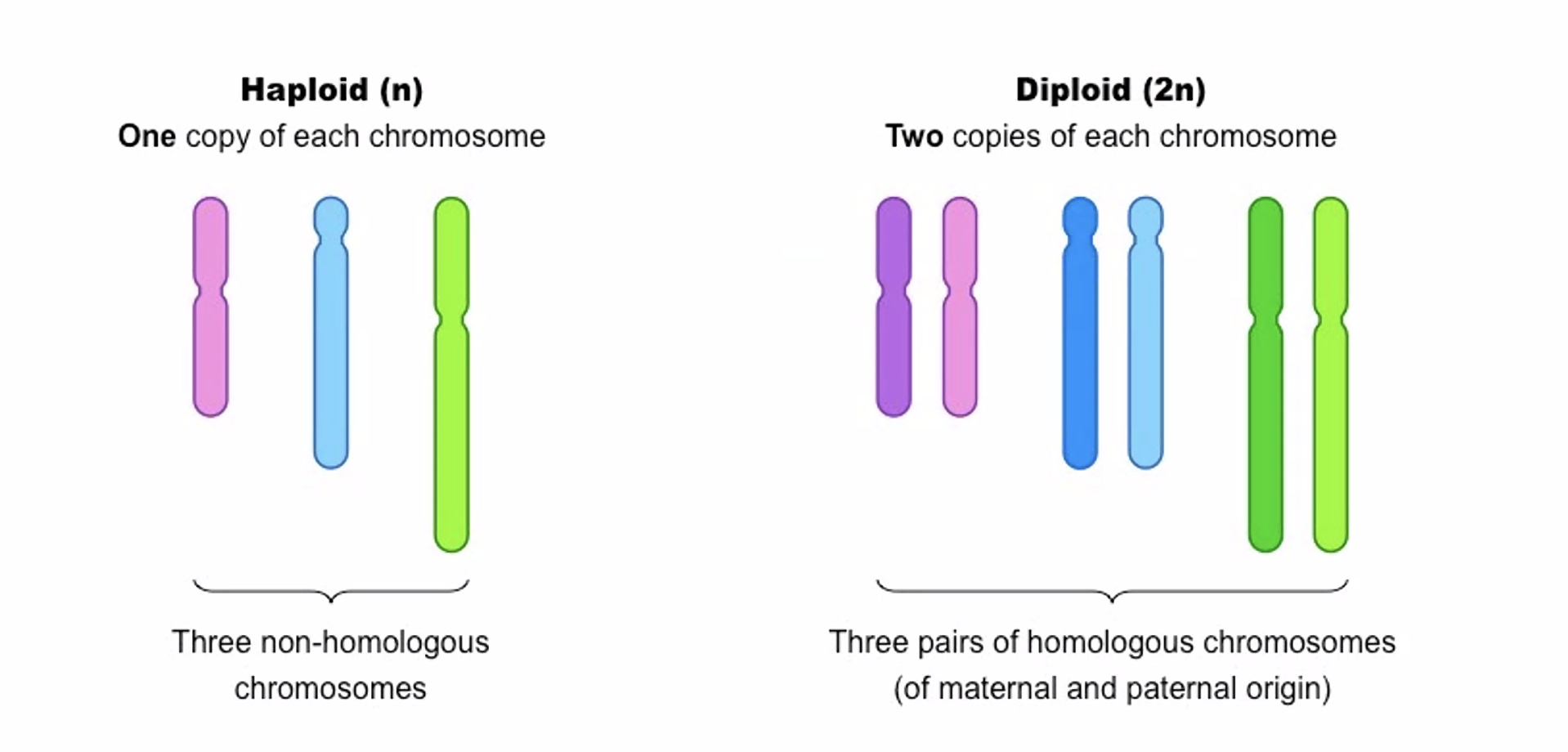
הגנום האנושי מחולק ל־46 יחידות ליניאריות - כרומוזומים. הוא דיפלואידי (2n): יש שני עותקים מכל כרומוזום, אחד מהאב ואחד מהאם. שני כרומוזומים זהים שנושאים רצף זהה נקראים כרומוזומים הומולוגיים. תא הפלואידי (n) הוא תא עם עותק אחד מכל כרומוזום.
22 זוגות נקראים אוטוזומים, וזוג אחד הוא כרומוזומי המין: נשים נושאות XX, גברים נושאים XY. כרומוזום Y קטן בהרבה מ־X, כמעט ולא מקודד לגנים, ונוכחותו היא הסיגנל שקובע התפתחות כזכר.
מספור הכרומוזומים
הכרומוזומים מוספרו לפי שלושה פרמטרים: גודל נראה במיקרוסקופ, מיקום הצנטרומר ופספוס בצביעת גימזה. הסתבר שהמספור לא תמיד מדויק - כרומוזום 21 למשל קצר מולקולרית מכרומוזום 22, אבל האזור הקרוב לצנטרומר אצלו נצבע פחות טוב בגימזה ולכן נראה קצר יותר בהסתכלות מיקרוסקופית. המספור ההיסטורי נשמר כדי למנוע בלבול.
הכרומוזום לפני ואחרי הכפלה
-
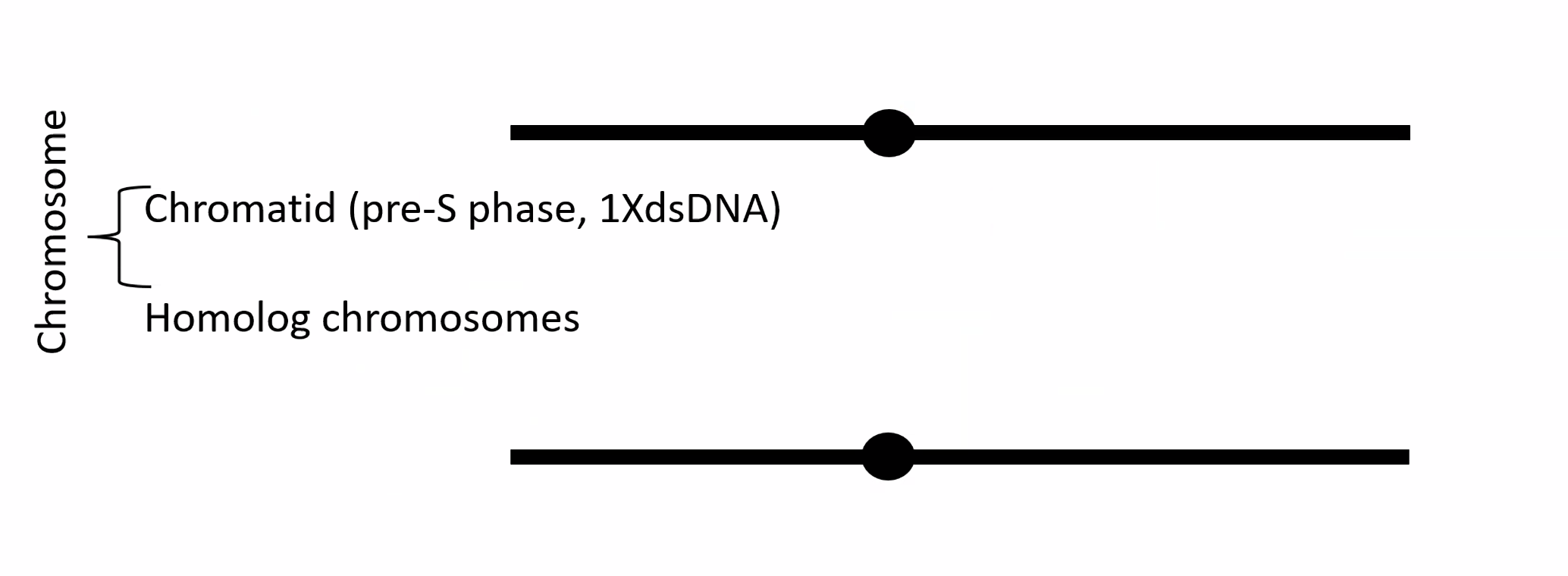
לפני שלב S: לכל כרומוזום יש שני כרומוזומים הומולוגיים, כל אחד מהם מכיל דו־גדיל אחד.
-
אחרי שלב S (הכפלה): כל דו־גדיל עבר הכפלה, לכן כל כרומוזום מכיל שתי כרומטידות אחיות (Sister Chromatids) - שתי מולקולות DNA זהות שנוצרו מהרפליקציה. הן נשארות צמודות אחת לשנייה בתהליך שנקרא Sister Chromatid Cohesion, עד לשלב האנאפאזה.
בסך הכול בתא לפני חלוקה יש ארבע מולקולות DNA כמעט זהות.
 | 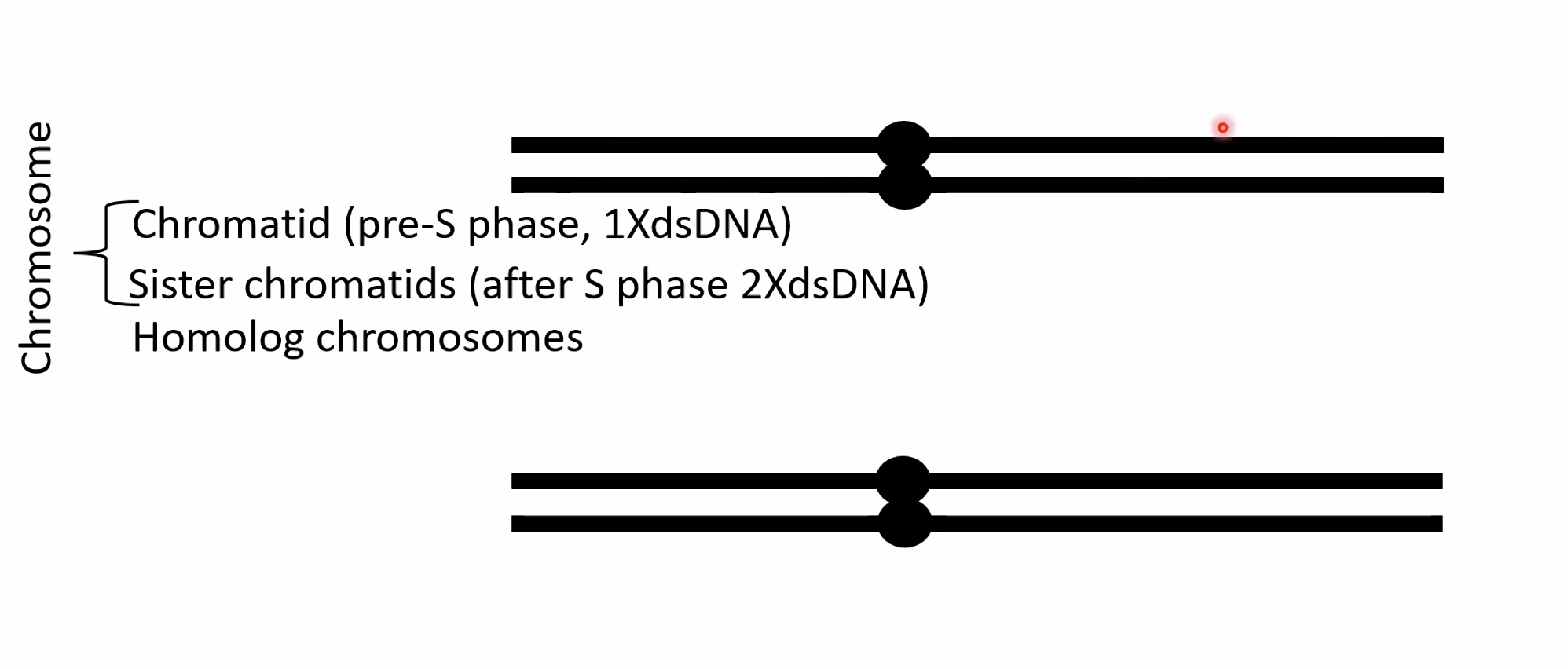 |
- G1 - כרומוזום = כרומטידה אחת
- S - מתבצע שכפול DNA
- אחרי S, ב־G2 - כל כרומוזום בנוי משתי כרומטידות אחיות
- הן נשארות מחוברות עד ההפרדה במיטוזה
כרומוזומים - אינטרפאזה לעומת מיטוזה
-
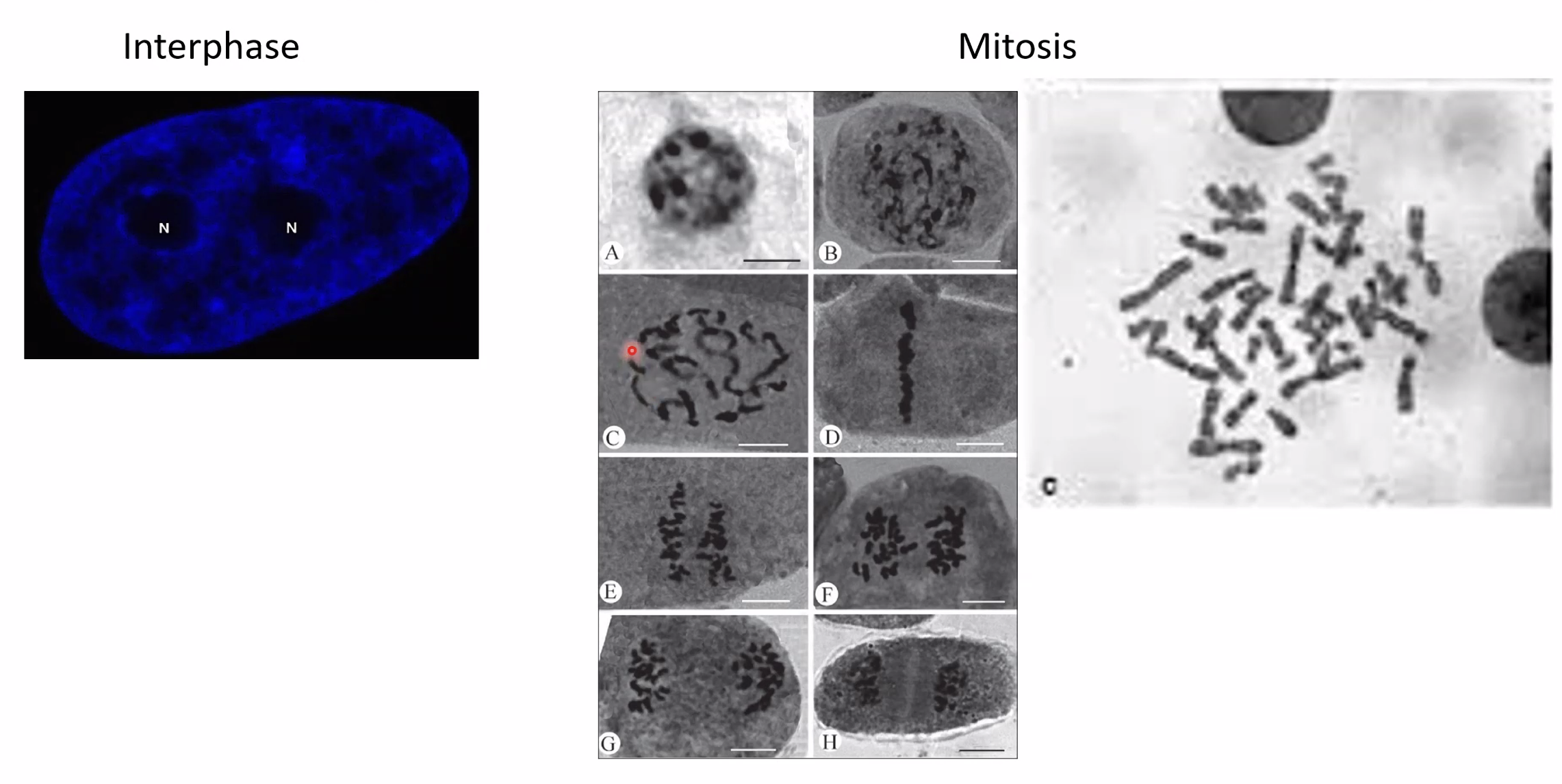
באינטרפאזה: ה־DNA פרוס על פני שטח הגרעין, אין מבנים מוגדרים נראים. צביעת DAPI מראה אזורים כהים ובהירים בלבד.
-
במיטוזה: ה־DNA עובר דחיסה דרמטית לצורת מקלות - הכרומוזומים המיטוטיים. בפרומטאפאזה שתי הכרומטידות האחיות עדיין מוחזקות יחד בצנטרומר ונראות בצורה דמויית X.
מבנה הכרומוזום
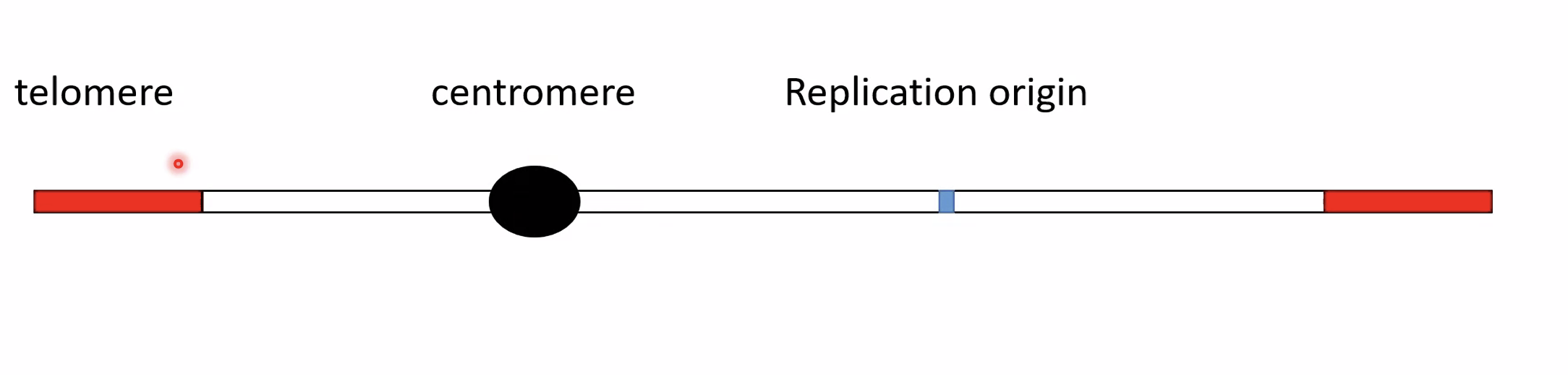
הצנטרומר
היצרות הנראית לאורך הכרומוזום. תפקידו הביולוגי: נקודת החיבור של הכרומוזום לסיבי הכישור (Spindle microtubules) שמבצעים את הפרדת הכרומוזומים לתאי הבת.
הצנטרומר מחלק את הכרומוזום לשתי זרועות:
- זרוע קצרה - p (מהמילה הצרפתית petit)
- זרוע ארוכה - q
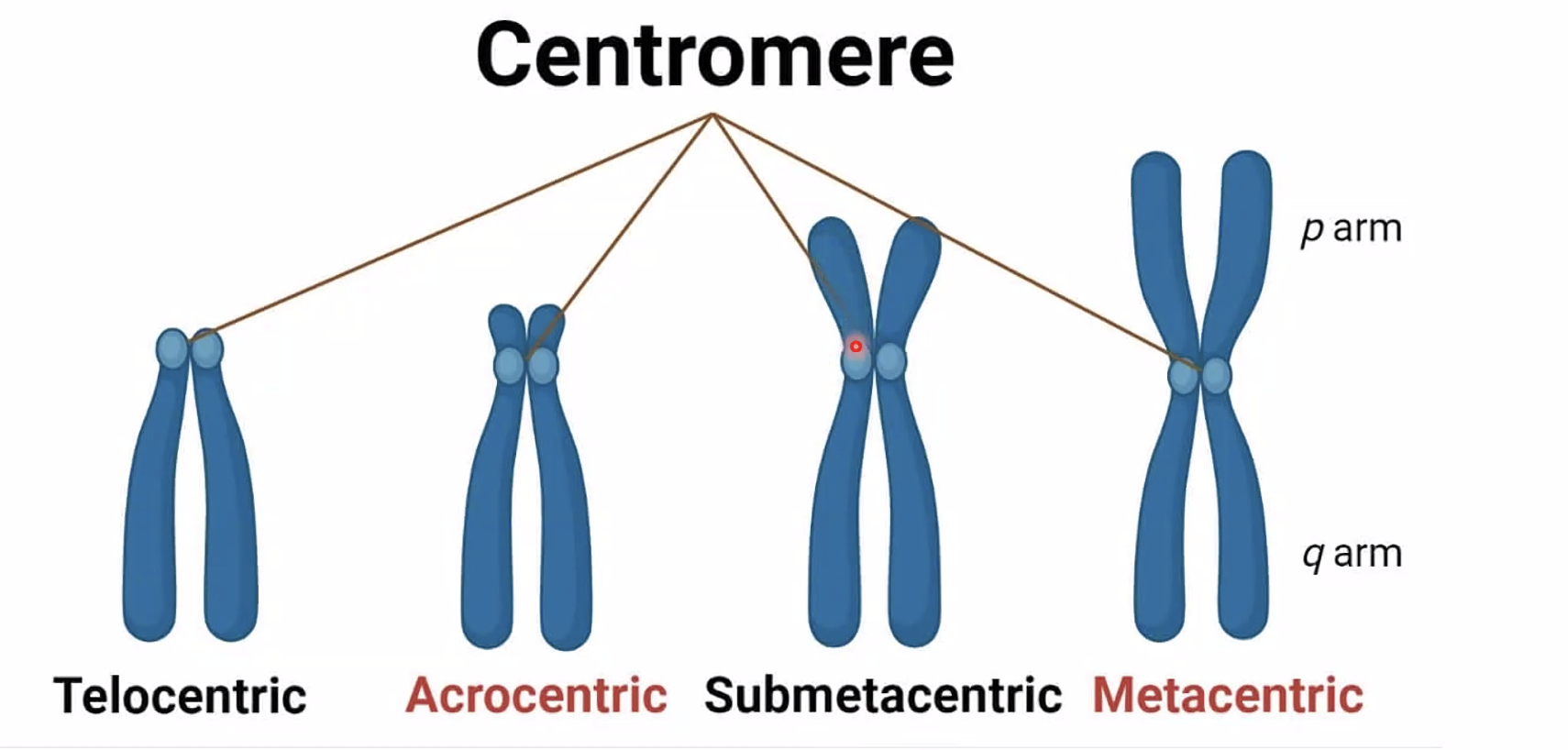
לפי מיקום הצנטרומר:
- מטאצנטרי - בדיוק במרכז, שתי זרועות שוות
- סאבמטאצנטרי - לא ממש במרכז
- אקרוצנטרי - קרוב מאוד לקצה, זרוע קצרה קטנה מאוד
- טלוצנטרי - ממש בקצה (בעכבר למשל, לא באדם)
חשוב: לכל כרומוזום חייב להיות צנטרומר אחד בדיוק. שני צנטרומרים יגרמו לכרומוזום להיקרע - כי יש שתי נקודות קישור לספינדל שיכולות למשוך לכיוונים מנוגדים.
הטלומרים
רצפי DNA מיוחדים בקצות הכרומוזומים הליניאריים. תפקידם:
-
הגנה מאקסונוקלאזות - קצה חופשי של DNA הוא מטרה לאקסונוקלאזות. הטלומרים נועלים את הקצה ומגנים עליו.
-
מניעת הידבקות בין כרומוזומים - ללא טלומרים, מערכת תיקון ה־DNA תתייחס לקצה כאל שבר ותדביק כרומוזומים זה לזה. זה אכן קורה בתאים סרטניים שבהם הטלומרים התקצרו.
-
עיגון קצוות לשמירה על מתח פיתולי - כמו שלמדנו בטופולוגיה, כדי להכניס מתח פיתולי לכרומוזום ליניארי הקצוות חייבים להיות קבועים. הטלומרים ממלאים את התפקיד הזה.
-
התקצרות תלוית גיל - הטלומרים מתקצרים עם כל מחזור חלוקה, ולכן ניתן לעקוב אחרי הגיל הכרונולוגי של הכרומוזום.
אתרי ראשית הכפלה - Origins of Replication
רפליקציה לא יכולה להתחיל בכל נקודה ב־DNA - יש אתרים מיוחדים שמהם מתחיל התהליך. הם מאופיינים ב־Tw נמוך, יחסית פתוחים ובדרך כלל לא מכוסים בנוקלאוזומים, מה שמקל על חלבוני מערכת הרפליקציה להיקשר ולהתחיל. לאוקריוטים יש הרבה אתרי ראשית הכפלה לאורך הגנום.
שלושת האלמנטים החיוניים לכרומוזום: צנטרומר + טלומרים + אתר ראשית הכפלה. שלושה אלמנטים אלה בלבד - לא משנה מה התוכן הגנטי - נדרשים כדי שמקטע DNA יהיה לו קיום עצמאי ויציב בתא.
על בסיס זה ניתן לבנות YAC (Yeast Artificial Chromosome): לוקחים מקטע DNA כלשהו (למשל, מקטע DNA אנושי), מוסיפים לו טלומרים, צנטרומר ואתר ראשית הכפלה, ומגדלים אותו בתוך שמר - הכרומוזום המלאכותי יתנהג בדיוק כמו כרומוזום שמרי רגיל: יוכפל בשלב S, יעבור סגרגציה במיטוזה ויישמר יציב.
בדיקת קריוטיפ - פריסה כרומוזומלית
התהליך
בשביל לראות כרומוזומים בבירור צריך תאים בשלב מיטוטי. שלבי הפרוטוקול:
-
הפקת תאים וגידול: לרוב מתאי מי שפיר (אמניוצנטזיס), מגדלים במעבדה מספר ימים.
-
סינכרוניזציה - שתי שיטות:
-
קולצ’יצין / נוקודאזול: חומרים שמעכבים פולימריזציה של מיקרוטובולים. ללא ספינדל, ה־checkpoint שמוודא קישור ביפולרי של הכרומוזומים אינו מסופק ← כל תא שמגיע לפרומטאפאזה נעצר. עם הזמן רוב התאים מסתנכרנים בפרומטאפאזה.
-
Double Thymidine Block: מדלדלים את הטימידין (T) מהתאים ← תאים שמנסים לבצע רפליקציה נעצרים בתחילת שלב S כי אין להם T. כשמוסיפים T בחזרה, כולם מתחילים מנקודה מסונכרנת. מחכים למשך הזמן שלוקח לתאים לעבור משלב S למיטוזה, ואז עוצרים אותם.
-
-
טיפול היפוטוני: שמים את התאים במלח נמוך ← מים נכנסים ← התא מתנפח. המטרה: הכרומוזומים הצפופים מופרדים זה מזה, כדי שבעת פיצוץ התא (להלן) הם לא ייפלו אחד על השני.
-
פיצוץ מכני: מטפטפים את התאים הנפוחים מגובה על גבי סלייד זכוכית. המכה גורמת לגרעין להיפרס על הסלייד. הכרומוזומים (בעלי מטען שלילי) נצמדים לזכוכית; שאר תוכן התא נשטף עם דטרגנט ועם בופרים.
-
צביעה:
-
DAPI / Hoechst: פלואורסצנטיים, נקשרים ב־Minor Groove באופן לא־ספציפי. מראים את צללית הכרומוזום כולו.
-
גימזה (G-banding): יוצרת דפוס פספוס ייחודי לכל כרומוזום - אזורים שנצבעים חזק ואזורים שנצבעים חלש. כל פס מייצג סדר גודל של מיליוני בסיסים.
-
מה ניתן לזהות?
הרזולוציה גסה מאוד - ניתן לזהות:
- טריזומיות (שלושה עותקים במקום שניים): 13, 18, 21
- טרנסלוקציות גדולות - חתיכה של מיליוני בסיסים שעברה מכרומוזום לכרומוזום
- חסרים וכפולים גדולים ברמת מגה־בייסים
לא ניתן לזהות שינויים ברמת בסיס בודד, indels קטנים, או רוב המחלות הגנטיות הנדירות.
טריזומיות ויאביליות: רק טריזומיות 13, 18 ו־21 מאפשרות לידה. בכל שאר הכרומוזומים - הטריזומיה גורמת להפלה ספונטנית, כי הכרומוזומים האחרים גדולים ו”חשובים” מדי מבחינת הגנים שהם נושאים. טריזומיה היא תהליך אקראי שקורה לכל הכרומוזומים - השאלה היא רק אם העובר יכול לשרוד אחריה.
SKY - Spectral Karyotyping
שיטה המבוססת על היברידיזציה (FISH) - כל כרומוזום מסומן בצבע פלואורסצנטי ייחודי על ידי פרובים ספציפיים. כך ניתן לזהות טרנסלוקציות ביתר קלות: חתיכה “מהכרומוזום האדום” שנדבקה לכרומוזום אחר נראית מיד בצבע שונה.
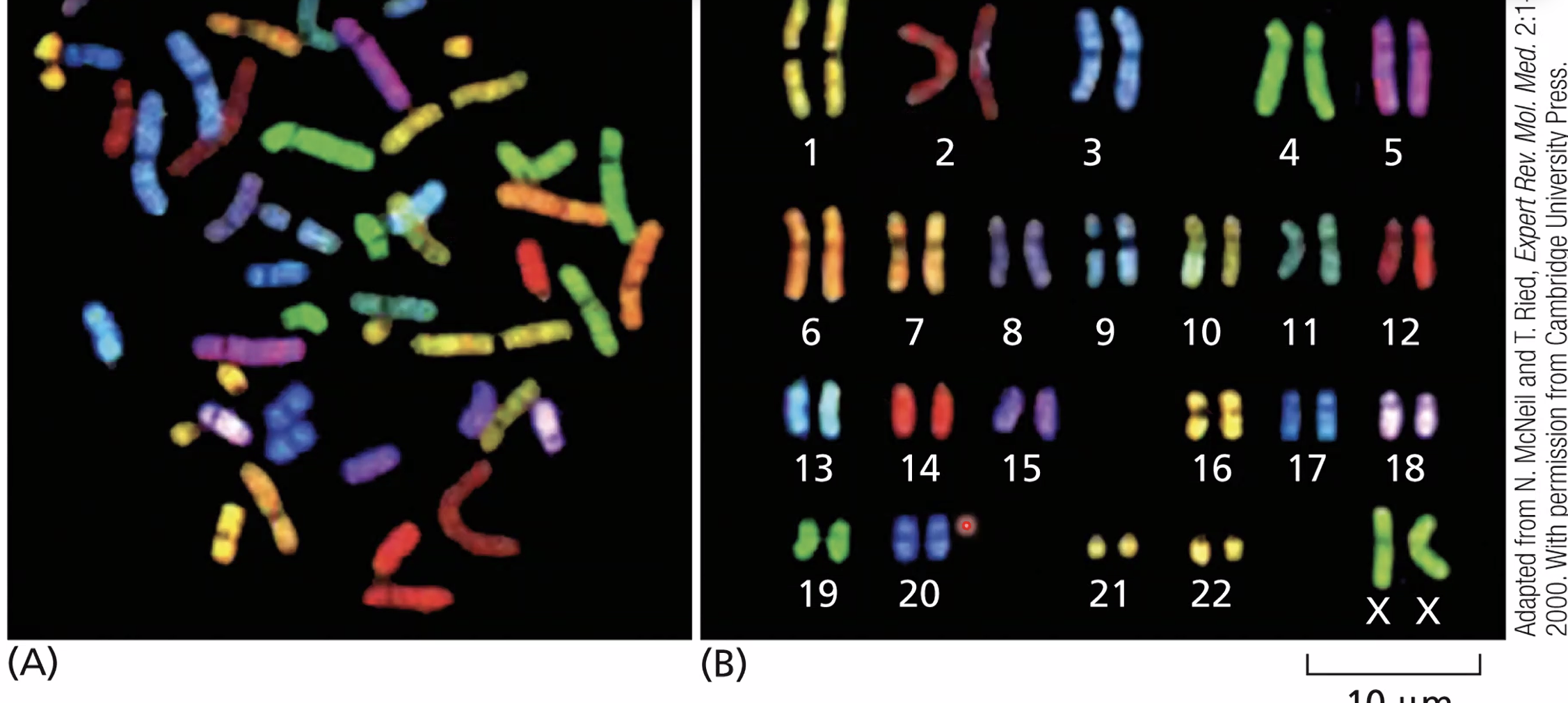
דוגמאות קליניות
-
תסמונת דאון - טריזומיה 21: שלושה כרומוזומים 21 במקום שניים. ניתן לראות בספירת הכרומוזומים בפריסה.
-
טרנסלוקציה 14;21: באופן פונקציונלי גם מייצרת מצב של עודף ביטוי של כרומוזום 21 ← מופע קליני של תסמונת דאון.
-
כרומוזום פילדלפיה - t(9;22): טרנסלוקציה בין כרומוזומים 9 ו־22 יוצרת גן כימרי BCR-ABL. הפרומוטור של הגן מוחלף ← הגן שהיה מושתק מתחיל להתבטא ביתר ← התחלקות מואצת של תאי דם לבנים ← לוקמיה.
מבט לעתיד: קריוטיפ הולך ומוחלף בטכנולוגיות ריצוף מודרניות. כיום, לזיהוי טריזומיה 21 ניתן לבצע ניתוח Cell-free fetal DNA (cfDNA) - DNA עוברי חופשי שמסתובב בדם האם, ללא צורך בדקירת מי שפיר הכרוכה בסיכון לעובר.
כרומוזום חיידקי
שונה מהותית מהכרומוזום האנושי:
- מעגלי - לא ליניארי
- אין צנטרומר - חלוקה לתאי הבת נעשית בדיפוזיה, לא על ידי ספינדל. ברמת אוכלוסייה זה עובד ברוב המקרים
- אין טלומרים - הכרומוזום מעגלי, לא צריך
- אתר ראשית הכפלה אחד - לעומת הרבה אתרים באיקריוטים
- אין היסטונים ונוקלאוזומים - יש חלבון שנקרא נוקלאואיד שהוא דמוי-היסטון ברמה מסוימת, אבל אין אריזה לכרומטין כמו באיקריוטים
DNA מיטוכונדריאלי - שריד אבולוציוני לחיידק שנבלע בסימביוזה לתא האיקריוטי. הוא מעגלי כמו כרומוזום חיידקי, יש לו אתר ראשית הכפלה אחד, והוא לא ארוז בכרומטין.
כרומטין
מהו כרומטין?
כרומטין הוא ה־DNA יחד עם חלבונים נלווים. השם ניתן כבר בסוף המאה ה־19 על ידי ביולוגים כמו וולטר פלמינג - הרבה לפני שידעו שמדובר בחומר הגנטי - כי הוא נצבע בצבעים בסיסיים (χρώμα ביוונית = צבע). רוב ה־DNA בתא נמצא כמעט תמיד ארוז בצורת כרומטין; רק אזורים נקודתיים חשופים.
למה כרומטין?
-
דחיסה: ה־DNA בתא אנושי, אם נפרוס אותו, מגיע לאורך של כ־2 מטרים. כל זה צריך להידחס לתוך גרעין שגודלו כ־10 מיקרון. הכרומטין מאפשר זאת באמצעות ליפוף ה־DNA סביב חלבונים.
-
הגנה: כאשר ה־DNA ארוז היטב, הוא פחות חשוף לנזקים.
-
רגולציה: הכרומטין מאפשר בקרה על ביטוי גנים - אילו גנים יהיו פעילים ואילו מושתקים - באמצעות מעבר בין מצב פתוח למצב סגור.
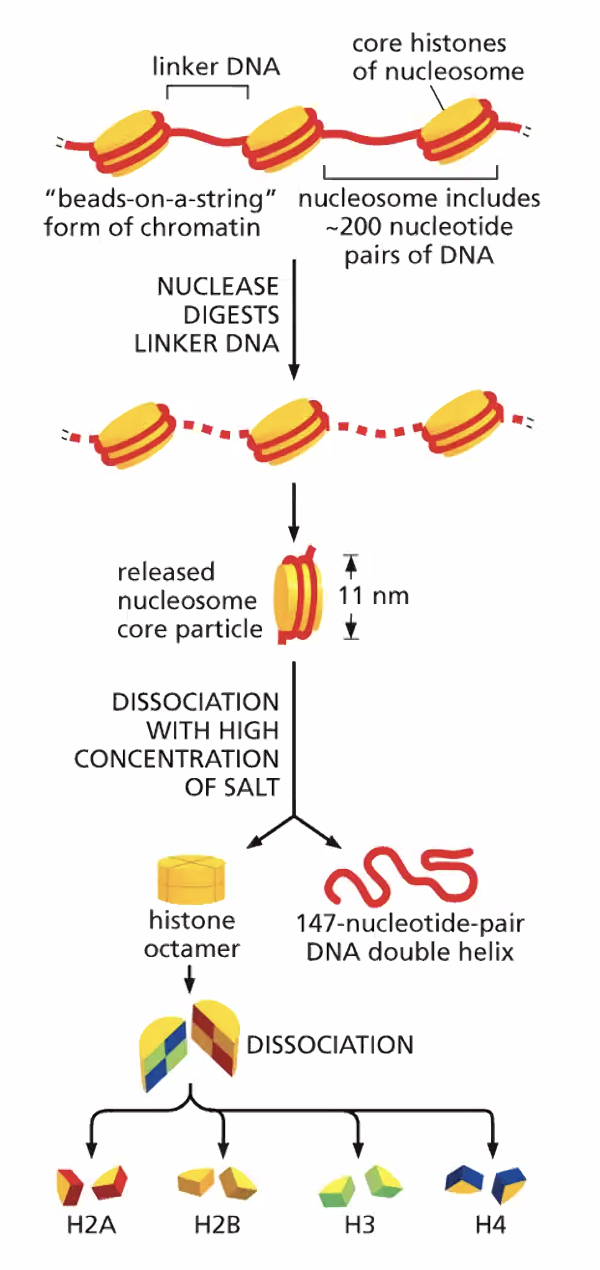
הנוקלאוזום - יחידת הבסיס של הכרומטין
מבנה
שמונה חלבוני היסטון - שני עותקים מכל אחד מארבעת ההיסטונים הליבתיים: H2A, H2B, H3, H4 - מתארגנים לכדור (octamer), סביבו מלופף ה־DNA בסיבוב ימני כ־1.65 פעמים (בערך 146 נוקלאוטידים).
גודל הנוקלאוזום כ־10 ננומטר. לכן הסיב נקרא לפעמים “10nm fiber” או “Beads on a String” - חרוזים על חוט - כי כך הוא נראה במיקרוסקופ אלקטרוני: נוקלאוזום, ספייסר, נוקלאוזום, ספייסר וכן הלאה.
בין כל שני נוקלאוזומים יש Linker DNA של כ־50 נוקלאוטידים - מקטע שלא מלופף על היסטון. יחד עם 146 בסיסי הנוקלאוזום, מתקבלת יחידה חוזרת של כ־200 בסיסים.
לכל ההיסטונים מבנה מרכזי משותף (Histone fold domain), ומה שמבדיל ביניהם הוא הזנב N-terminal שבולט החוצה מהנוקלאוזום ונחשף לסביבה.
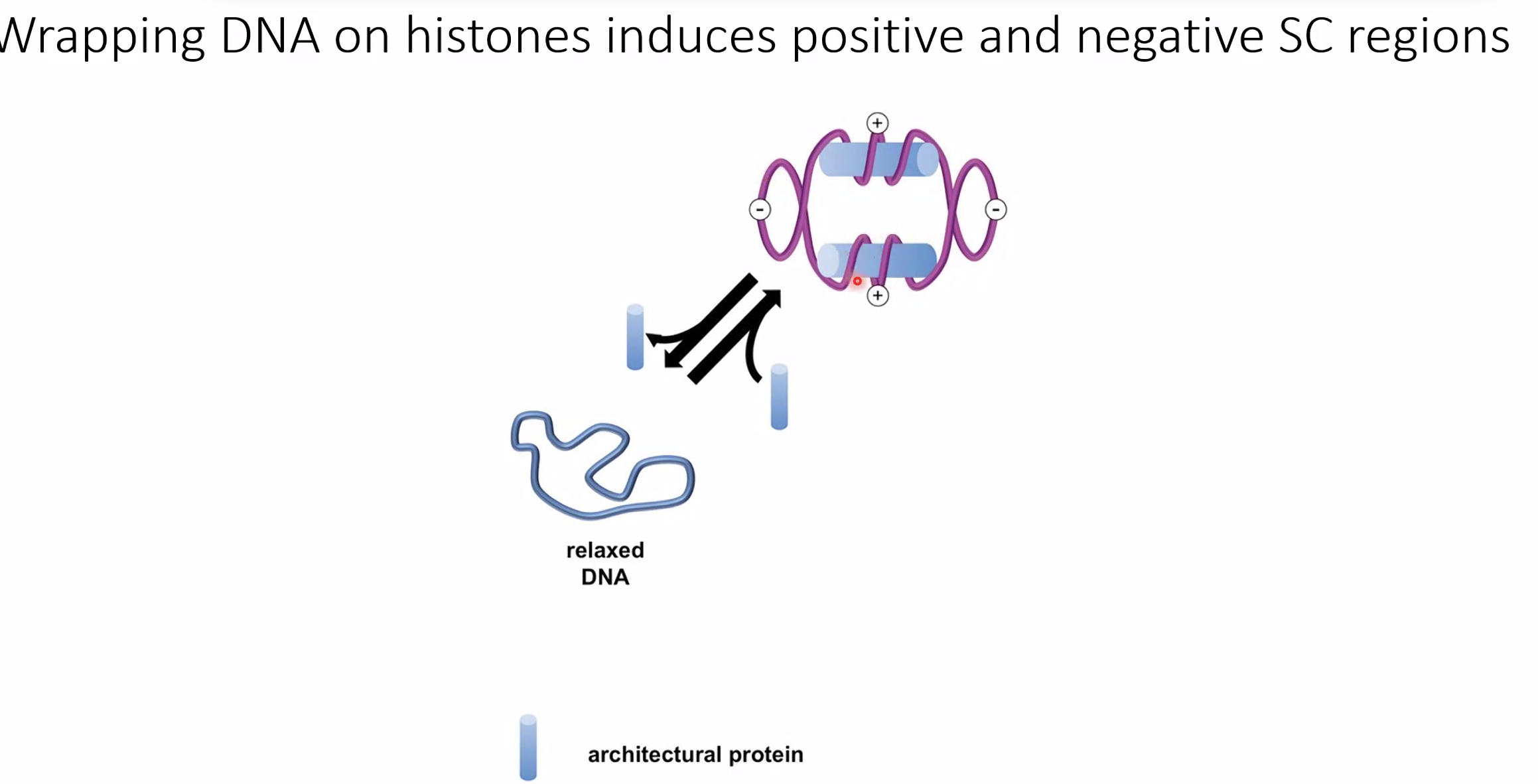
נוקלאוזום, סופרקויל והגנה
הסיבוב הימני של ה־DNA סביב ההיסטונים מכניס פוזיטיב סופרקויל לאזור הנוקלאוזום עצמו. ה־Linker DNA שבין שני נוקלאוזומים מפצה על כך בנגטיב סופרקויל. המשמעות הפונקציונלית: ה־Linker DNA פתוח יחסית, מה שמאפשר לגורמי שעתוק ולחלבוני הרפליקציה גישה. לכן, פרומוטורים ואתרי ראשית הכפלה נמצאים בדרך כלל באזורים שאינם מכוסים בנוקלאוזומים.
נוקלאזות ונוקלאוזומים: נוקלאזות יחתכו בקלות את ה־Linker DNA החשוף, אך ה־$146 \, \mathrm{bp}$ שמלופפים סביב ההיסטון מוגנים - החלבונים מפריעים לנוקלאז לזהות ולחתוך.
Cell-free DNA (cfDNA): כשתאים מתים, הם משחררים DNA לזרם הדם. נוקלאזות בדם מפרקות את ה־Linker DNA החשוף, אבל שומרים שריד של כ־146bp שהיה מוגן בנוקלאוזום. ניתן לבודד את הקטעים האלה מהדם ולנתח אותם - לזיהוי טריזומיות עובריות ולאבחון גנטי של גידולים סרטניים (Liquid biopsy), ללא צורך בביופסיה פולשנית.
Footprinting: טכניקה מעבדתית שמשתמשת בנוקלאזות כדי לגלות היכן נמצאים חלבונים על ה־DNA. אזורים מוגנים = חלבון קשור שם. כך מזהים מיקומי נוקלאוזומים ואתרי קישור של גורמי שעתוק.
היסטון H1 - ה־Linker Histone
H1 אינו חלק מהאוקטמר - הוא חלבון חיצוני שיושב ב־Linker DNA ומחבר בין ה־DNA המלופף על ההיסטון לזנב ה־Linker. הוא מאפשר דחיסה נוספת של הנוקלאוזומים זה לזה ויצירת “30nm fiber” - הרמה הבאה של ארגון הכרומטין.
וריאנטים של היסטונים
לצד ארבעת ההיסטונים הרגילים יש וריאנטים עם תפקידים ספציפיים מאוד. שניים שחשוב לזכור:
-
CENP-A: מחליף את H3 בצנטרומרים בלבד. זהו הסמן המולקולרי שמגדיר את מיקום הצנטרומר ומאפשר לבנות עליו את הקינטוכור (מַחְבַּר הַכִּישׁוֹר) - המבנה שמחבר לספינדל (כישור החלוקה). -
H2A.X: מחליף את H2A באזורים שיש בהם שבר דו־גדילי. ברגע שנוצר שבר ב־DNA,H2A.Xמזורחן ומסמן את אזור השבר למערכת התיקון. כשהתיקון נגמר,H2A.Xמוסר ומוחלף בחזרה ב־H2A הרגיל.
רגולציה אפיגנטית - ארבע רמות
1. מתילציה של DNA
DNA Methyltransferases מוסיפות קבוצת מתיל על ציטוזין בצמד CpG (ציטוזין שאחריו גואנין, על אותו גדיל). המתילציה נעשית בדרך כלל על CpG islands - אזורים עשירים בצמדי CG.
- מתילציה = השתקה - כרומטין נסגר, טרנסקריפציה מתדכאת
- דה־מתילציה = פתיחה - כרומטין נפתח, טרנסקריפציה מתאפשרת
שימו לב: מתילציה על DNA (על C ב־CpG) שונה ממתילציה על היסטונים.
2. מודיפיקציות קוולנטיות על היסטונים
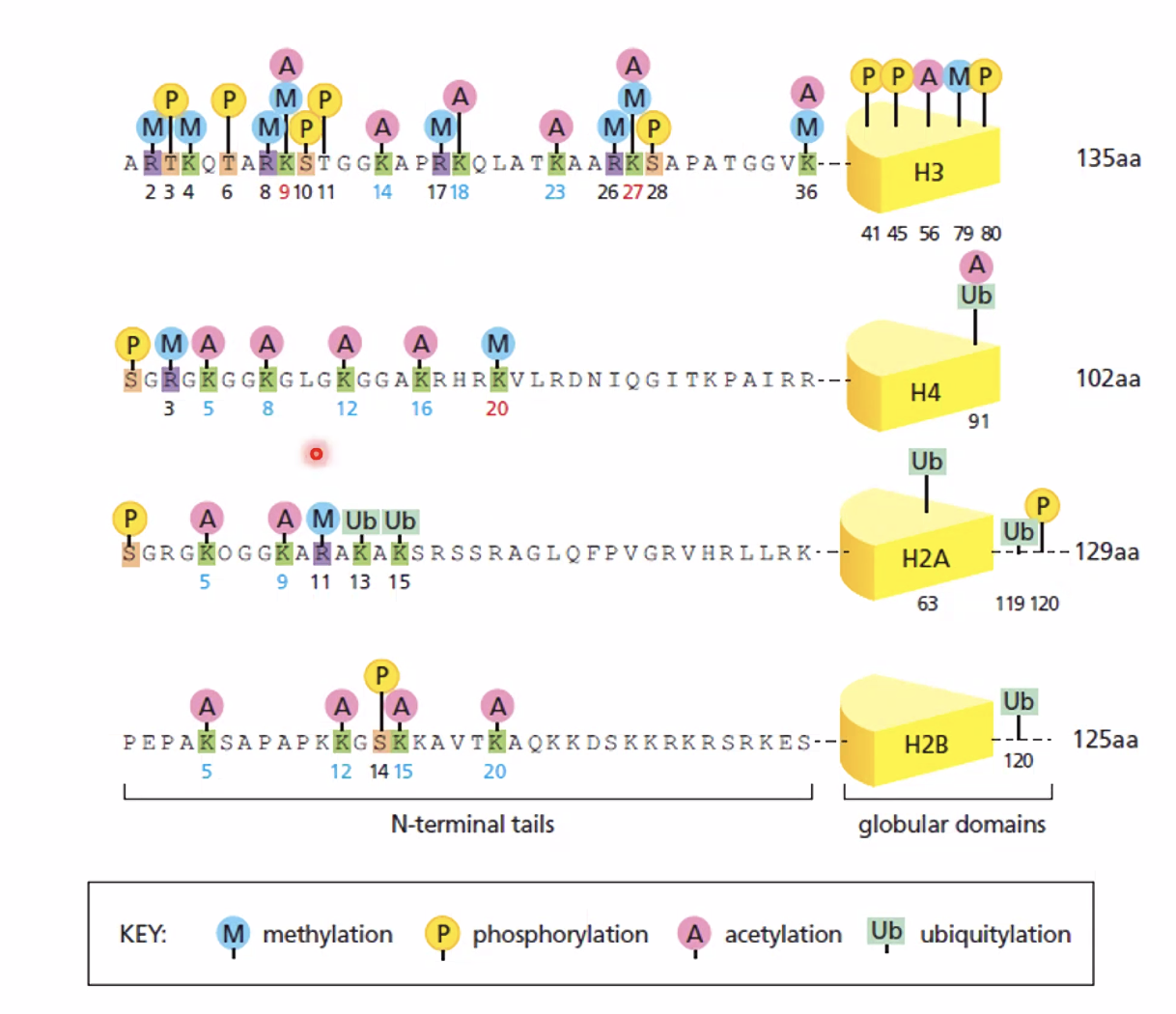
הזנב N-terminal של ההיסטון בולט החוצה מהנוקלאוזום ונחשף. אנזימים מגיעים ועושים עליו מודיפיקציות בדרכים שונות: מתילציה, אצטילציה, פוספורילציה, יוביקוויטינציה ועוד. לכל מודיפיקציה יש משמעות שונה.
כלל אצבע בסיסי (עם חריגים):
- אצטילציה ← כרומטין פתוח (קבוצת אצטיל גדולה ← הפרעה סטרית ← הנוקלאוזומים מתרחקים)
- מתילציה ← כרומטין סגור (קבוצת מתיל קטנה ← לא מפריעה ← מאפשרת דחיסה)
המודיפיקציות נמצאות על זנב ה־N-terminal כי הוא זמין - בולט החוצה ואפשר לגשת אליו, בניגוד ל־Histone fold שנמצא בתוך הנוקלאוזום ומוסתר.
לפי מה שנאמר בשיעור, אין צורך לזכור את הטבלה המלאה. יש מתילציות שקשורות דווקא לביטוי גנים, ויש מודיפיקציות שמעורבות בתיקון DNA. הרעיון הכללי הוא מה שחשוב.
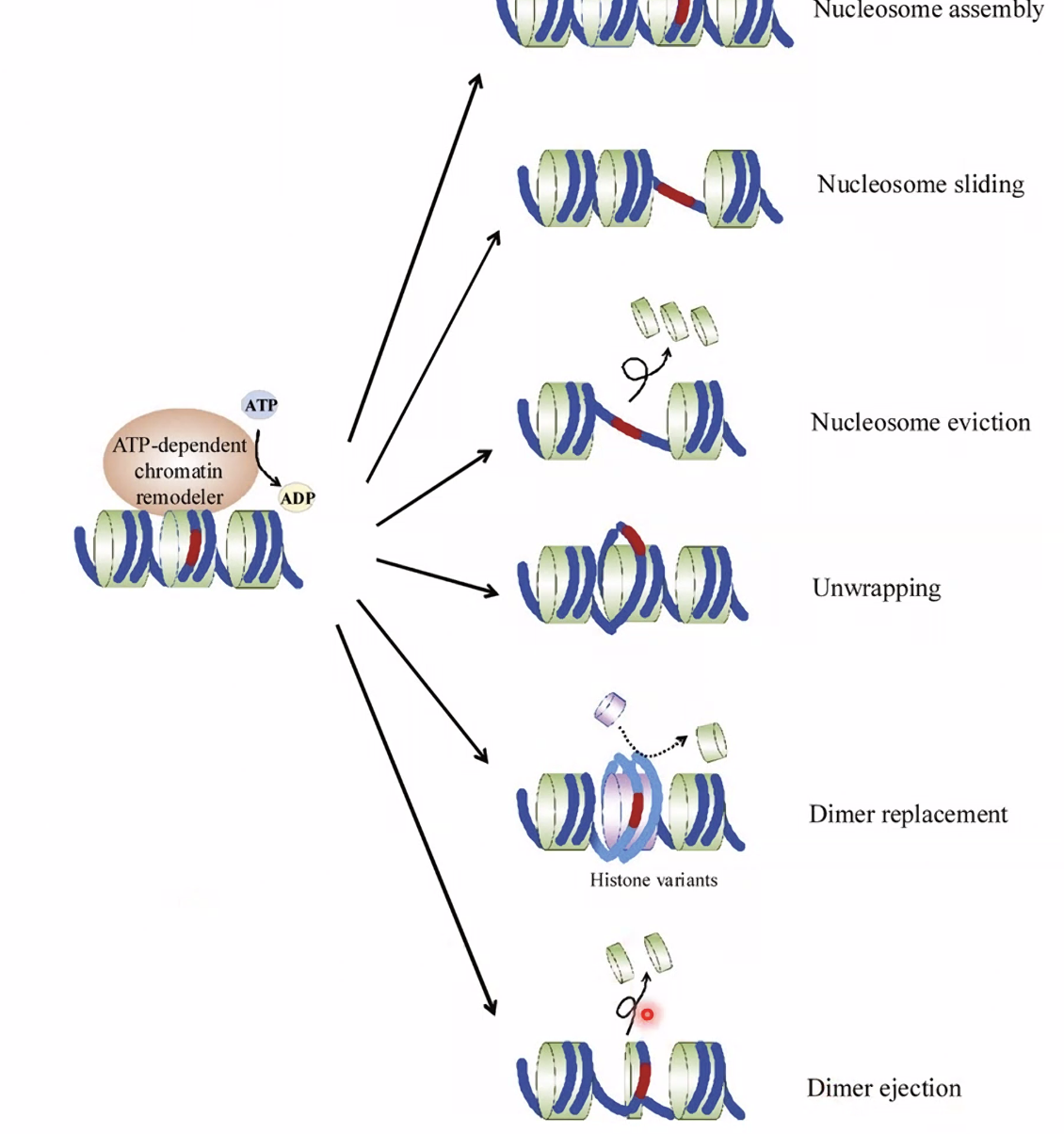
3. Chromatin Remodeling - שיפוץ כרומטין
קומפלקסים של חלבונים Remodelers שמשתמשים בATP כדי לשנות את מצב הנוקלאוזומים. מה שהם יודעים לעשות:
- Sliding - להזיז נוקלאוזום לאורך ה־DNA
- Ejection - לפנות נוקלאוזום לחלוטין ולחשוף DNA
- Unwrapping - להרפות את אחיזת ה־DNA בהיסטון ולהנגיש אותו
- Replacement - להחליף היסטון רגיל בווריאנט (למשל H3 ב־CENP-A בצנטרומר)
SWI/SNF - דוגמה לרימודלר מפורסם שמבצע ejection. מוטציות ב־SWI/SNF נפוצות מאוד בסרטן - שיבוש שלו גורם לאיזון שגוי בין אזורים פתוחים לסגורים, מה שמאפשר ביטוי לא תקין של אונקוגנים או השתקת גנים מעכבי סרטן.
4. Non-coding RNA
RNA שאינו מקודד לחלבון יכול לשלוט על כרומטין. הדוגמה הקלאסית: XIST - lncRNA המיוצר מכרומוזום X אחד בנשים, נקשר לאורכו וגורם לדחיסה שמשתיקה אותו לחלוטין. זהו מנגנון X-inactivation - האחראי ל־Barr Body הנראה כגוש כהה בגרעין של תאי נקבה. המנגנון המדויק עדיין לא מובן לחלוטין.
פוזיטיב סופרקויל כתוצר לוואי של טרנסקריפציה ורפליקציה
כשה־RNA פולימראז (או DNA פולימראז) מתקדם לאורך ה־DNA, הוא מהווה חסם טופולוגי - ה־DNA קשור אליו ולא יכול להסתובב חופשי. כתוצאה מכך:
- לפני הפולימראז - ה־DNA נדחס ← פוזיטיב סופרקויל
- אחרי הפולימראז - ה־DNA נמתח ← נגטיב סופרקויל
ככל שהפולימראז מתקדם, הפוזיטיב סופרקויל שמצטבר לפניו מגדיל את ההתנגדות להתקדמות - עד שהפולימראז לא יכול להמשיך. טופואיזומראזות (שנדון בהן בשיעור הבא) נכנסות שם כדי לשחרר את המתח ולאפשר המשך.
דור פסקללכן הטרנסקריפציה מתרחשת על נגטיב סופרקויל (האזור מאחורי הפולימראז, שם ה־DNA פתוח יחסית) - ולא כי ה־DNA כולו בנגטיב סופרקויל, אלא כי נגטיב הסופרקויל מתפתח דינמית כתוצאה מהתהליך עצמו.